99b729abc6996ce4aa5fa56c54af3c26.ppt
- Количество слайдов: 24

Использование нанотехнологических подходов для разработки нового поколения вакцин и терапевтических препаратов А. Л. Гинцбург ГУ НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи РАМН 1

Оптимистические прогнозы середины прошлого столетия в отношении борьбы с инфекциями не оправдались. По данным воз ежегодно в мире от инфекционных болезней умирает 16 млн человек. За последние десятилетия человечество столкнулось с десятком новых инфекционных заболеваний. В основе многих тяжелых хронических заболеваний, которые ранее считались соматическими, лежит инфицирование определенным патогенным микроорганизмом. 2

В то же время, как показали два прошедших столетия, самым надежным способом защиты человеческой популяции от инфекций это вакцинация. Вакцины созданы против 34 возбудителей инфекционных заболеваний, а человечество поражает более 400 инфекций. Последние достижения иммунологии и микробиологии с конструктивными возможностями био и нанотехнологий дают возможность приступить к созданию вакцин против тех возбудителей инфекционных заболеваний, для которых они еще не созданы и к принципиальному улучшению качества существующих вакцин. 3
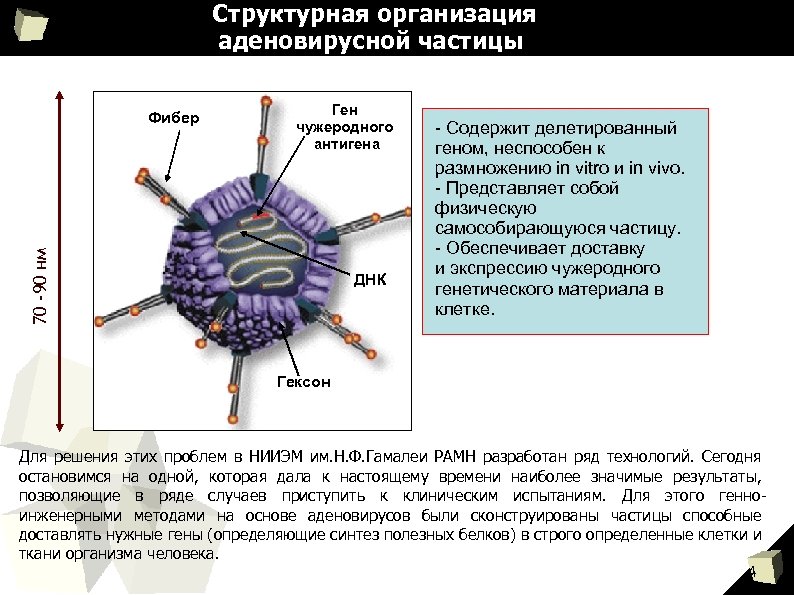
Структурная организация аденовирусной частицы Ген чужеродного антигена 7 0 - 9 0 нм Фибер ДНК - Содержит делетированный геном, неспособен к размножению in vitro и in vivo. - Представляет собой физическую самособирающуюся частицу. - Обеспечивает доставку и экспрессию чужеродного генетического материала в клетке. Гексон Для решения этих проблем в НИИЭМ им. Н. Ф. Гамалеи РАМН разработан ряд технологий. Сегодня остановимся на одной, которая дала к настоящему времени наиболее значимые результаты, позволяющие в ряде случаев приступить к клиническим испытаниям. Для этого генноинженерными методами на основе аденовирусов были сконструированы частицы способные доставлять нужные гены (определяющие синтез полезных белков) в строго определенные клетки и ткани организма человека. 4
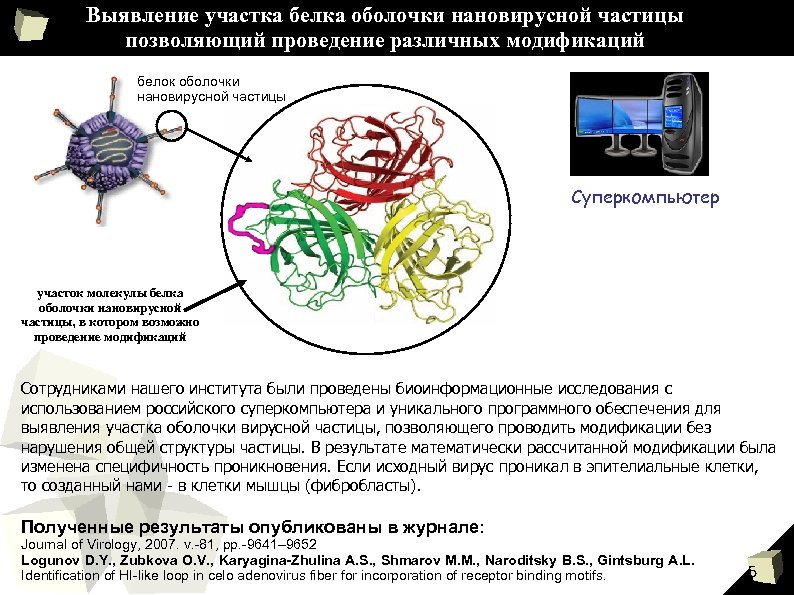
Выявление участка белка оболочки нановирусной частицы позволяющий проведение различных модификаций белок оболочки нановирусной частицы Суперкомпьютер участок молекулы белка оболочки нановирусной частицы, в котором возможно проведение модификаций Сотрудниками нашего института были проведены биоинформационные исследования с использованием российского суперкомпьютера и уникального программного обеспечения для выявления участка оболочки вирусной частицы, позволяющего проводить модификации без нарушения общей структуры частицы. В результате математически рассчитанной модификации была изменена специфичность проникновения. Если исходный вирус проникал в эпителиальные клетки, то созданный нами - в клетки мышцы (фибробласты). Полученные результаты опубликованы в журнале: Journal of Virology, 2007. v. -81, pp. -9641– 9652 Logunov D. Y. , Zubkova O. V. , Karyagina-Zhulina A. S. , Shmarov M. M. , Naroditsky B. S. , Gintsburg A. L. Identification of HI-like loop in celo adenovirus fiber for incorporation of receptor binding motifs. 5
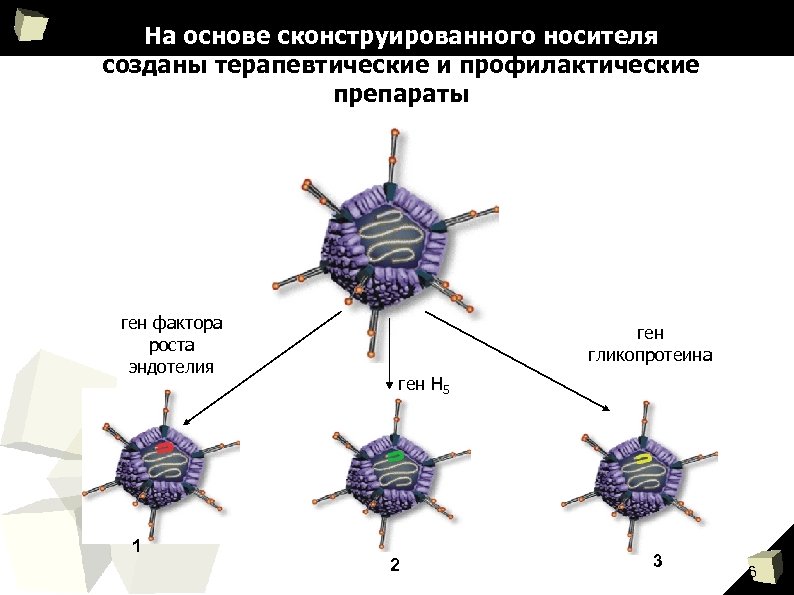
На основе сконструированного носителя созданы терапевтические и профилактические препараты ген фактора роста эндотелия 1 ген гликопротеина ген Н 5 2 3 6

Препараты для генной терапии, разработанные в ГУ НИИЭМ им. Н. Ф. Гамалеи РАМН Аденовирусные частицы содержат гены ангиогенина и фактора роста эндотелия сосудов для лечения хронических облитерирующих заболеваний артерий нижних конечностей человека • Препарат создан совместно с Российским научным центром хирургии РАМН; • Начаты клинические испытания препарата на базе Российского научного центра хирургии РАМН; • Результаты работ опубликованы и запатентованы. Вестник Российской АМН, 2006, № 9 -10, С. 6 -10. Н. П. Бочков, Б. А. Константинов, А. В. Гавриленко, В. З. Тарантул, Е. Д. Свердлов, Б. С. Народицкий, А. Л. Гинцбург. Генно-инженерные технологии в лечении хронической ишемии нижних конечностей. 7

Кандидатные аденовирусные вакцины разработанные в ГУ НИИЭМ им. Н. Ф. Гамалеи РАМН Кандидатная вирусная вакцина против вируса гриппа птиц H 5 N 1 • Разработана и испытывается совместно с ФГУ “Федеральный центр охраны здоровья животных”, г. Владимир; • Эффективность кандидатной нановирусной вакцины против вируса гриппа птиц H 5 N 1 в опытах на животных достигает 95%; • Разработанная технология получения вакцин позволяют, в случае появления нового эндемичного штамма вируса гриппа, создать адекватный вариант вакцины в течении 30 -45 дней; • Разработанная технология получения нановирусных вакцин запатентована. 8

Кандидатные аденовирусные вакцины разработанные в ГУ НИИЭМ им. Н. Ф. Гамалеи РАМН Кандидатная вакцина против вируса бешенства • В лабораторных исследованиях эффективность вакцины для животных против вируса бешенства составила 95 -98%; • Кандидатная нановирусная вакцина подготовлена для полевых испытаний на базе ВНИИ ветеринарной вирусологии и микробиологии РАСХН, г. Покров Журнал микробиологии, эпидемиологии и иммунобиологии, 2006, № 4, С. 69 -71. М. М. Шмаров, И. Л. Тутыхина, С. Ж. Цыбанов, Б. В. Новиков, Б. С. Народицкий, А. Л. Гинцбург Индукция проективного иммунного ответа у мышей, вакцинированных рекомбинантным аденовирусом птиц CELO, экспрессирующим гликопротеин G вируса бешенства. 9
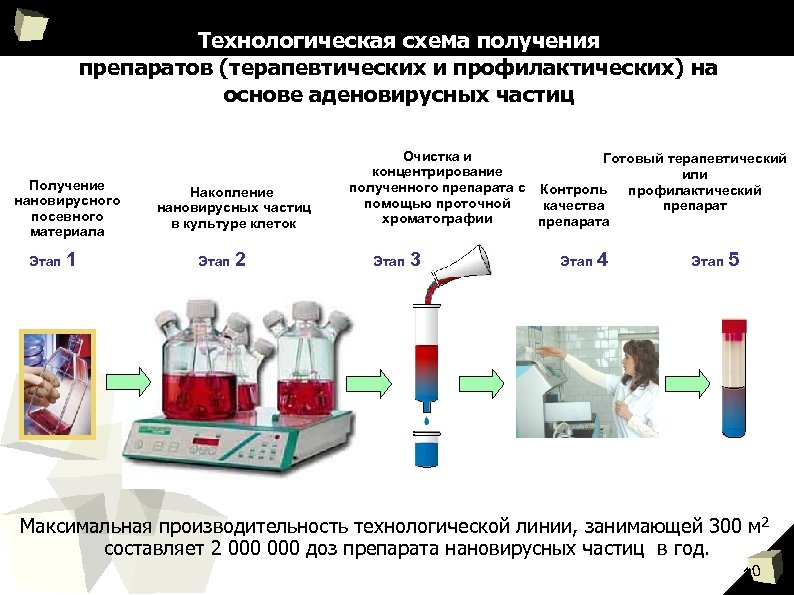
Технологическая схема получения препаратов (терапевтических и профилактических) на основе аденовирусных частиц Получение нановирусного посевного материала Этап 1 Накопление нановирусных частиц в культуре клеток Этап 2 Очистка и Готовый терапевтический концентрирование или полученного препарата с Контроль профилактический помощью проточной качества препарат хроматографии препарата Этап 3 Этап 4 Этап 5 Максимальная производительность технологической линии, занимающей 300 м 2 составляет 2 000 доз препарата нановирусных частиц в год. 10

Требования к “идеальной” субъединичной вакцине Для полноценного иммунного ответа на субъединичный АГ (а только такие вакцины могут полностью гарантировать безопасность на фоне массовых иммунодефицитных состояний (разного генеза) необходимо выполнить ряд условий: 1) Вакцина должна содержать АГ взаимодействующий с Toll-подобными рецепторами (стимулирующими врожденный иммунитет). 2) Вакцина должна содержать АГ специфичный (стимулировать приобретенный иммунитет). для конкретного патогена 3) АГ должен быть определенным образом представлен в составе нанометрового носителя, чтобы гарантировать кластаризацию рецепторов АГ. Второй подход подразумевает создание идеальной субъединичной вакцины. Здесь перечислены требования к такой вакцине, исходя из уровня наших знаний по иммунологии и микробиологии. Препарат должен содержать два типа лигандов взаимодействующих с двумя типами рецепторов, находящихся на клетках иммунной системы. Взаимодействие с первым типом рецепторов активирует врожденный иммунитет (то, что в быту мы называем воспалением). Взаимодействие со вторым типом рецепторов активирует приобретенный иммунитет. 11
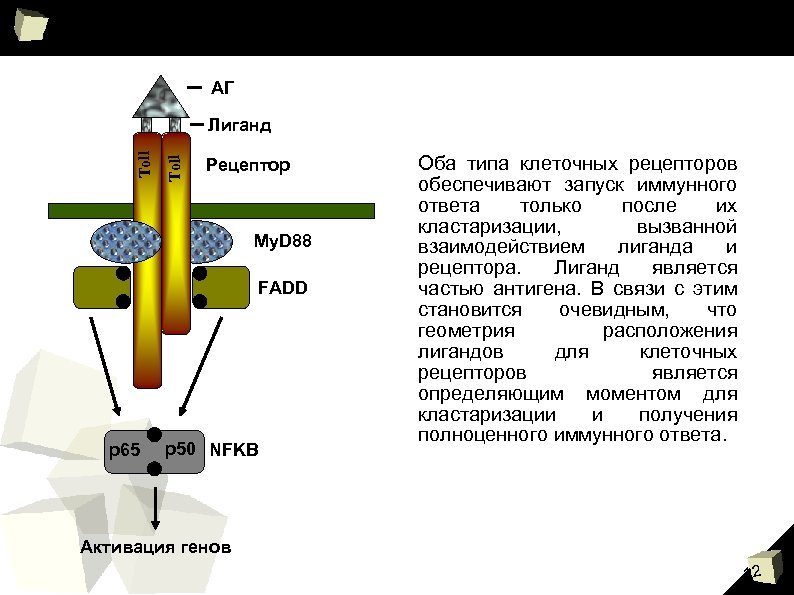
АГ Toll Лиганд Рецептор My. D 88 FADD p 65 p 50 NFKB Оба типа клеточных рецепторов обеспечивают запуск иммунного ответа только после их кластаризации, вызванной взаимодействием лиганда и рецептора. Лиганд является частью антигена. В связи с этим становится очевидным, что геометрия расположения лигандов для клеточных рецепторов является определяющим моментом для кластаризации и получения полноценного иммунного ответа. Активация генов 12
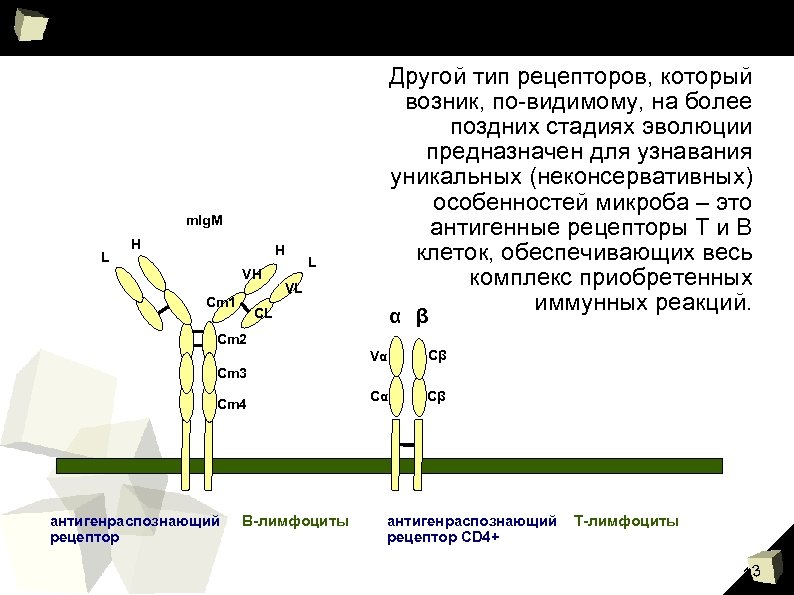
Другой тип рецепторов, который возник, по-видимому, на более поздних стадиях эволюции предназначен для узнавания уникальных (неконсервативных) особенностей микроба – это антигенные рецепторы Т и В клеток, обеспечивающих весь комплекс приобретенных иммунных реакций. mlg. M L H H VH Cm 1 L VL α β CL Cm 2 Vα Cβ Cm 3 Cm 4 антигенраспознающий рецептор В-лимфоциты антигенраспознающий рецептор CD 4+ Т-лимфоциты 13
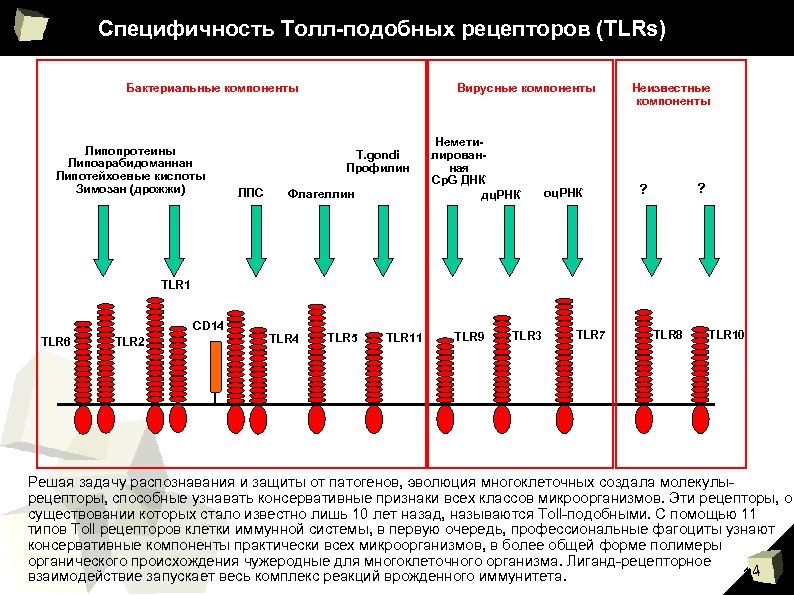
Специфичность Толл-подобных рецепторов (TLRs) Бактериальные компоненты Липопротеины Липоарабидоманнан Липотейхоевые кислоты Зимозан (дрожжи) Вирусные компоненты T. gondi Профилин ЛПС Флагеллин Неметилированная Cp. G ДНК дц. РНК оц. РНК Неизвестные компоненты ? ? TLR 1 CD 14 TLR 6 TLR 2 TLR 4 TLR 5 TLR 11 TLR 9 TLR 3 TLR 7 TLR 8 TLR 10 Решая задачу распознавания и защиты от патогенов, эволюция многоклеточных создала молекулырецепторы, способные узнавать консервативные признаки всех классов микроорганизмов. Эти рецепторы, о существовании которых стало известно лишь 10 лет назад, называются Toll-подобными. С помощью 11 типов Toll рецепторов клетки иммунной системы, в первую очередь, профессиональные фагоциты узнают консервативные компоненты практически всех микроорганизмов, в более общей форме полимеры органического происхождения чужеродные для многоклеточного организма. Лиганд-рецепторное 14 взаимодействие запускает весь комплекс реакций врожденного иммунитета.
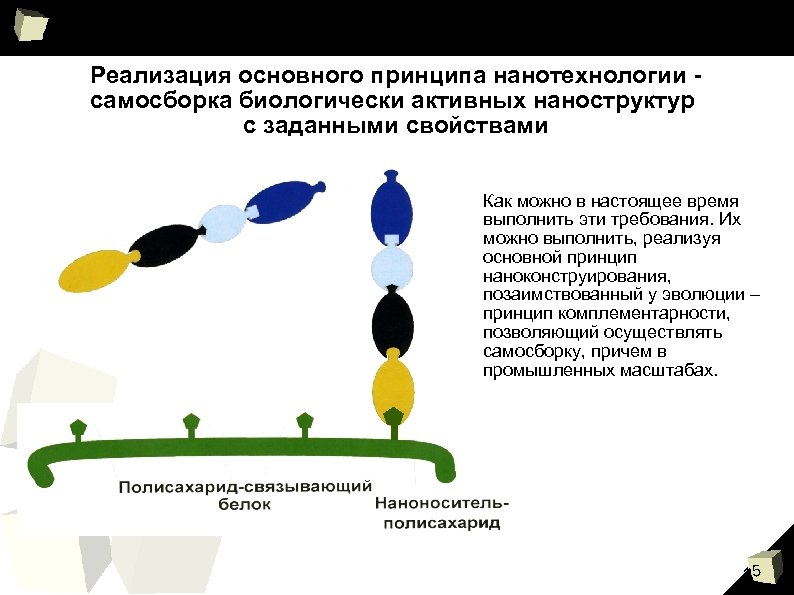
Реализация основного принципа нанотехнологии самосборка биологически активных наноструктур с заданными свойствами Как можно в настоящее время выполнить эти требования. Их можно выполнить, реализуя основной принцип наноконструирования, позаимствованный у эволюции – принцип комплементарности, позволяющий осуществлять самосборку, причем в промышленных масштабах. 15
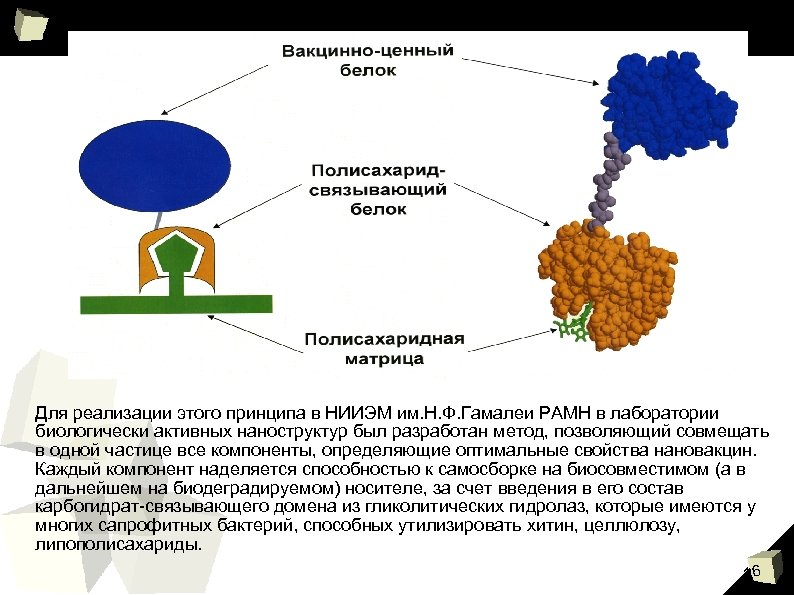
Для реализации этого принципа в НИИЭМ им. Н. Ф. Гамалеи РАМН в лаборатории биологически активных наноструктур был разработан метод, позволяющий совмещать в одной частице все компоненты, определяющие оптимальные свойства нановакцин. Каждый компонент наделяется способностью к самосборке на биосовместимом (а в дальнейшем на биодеградируемом) носителе, за счет введения в его состав карбогидрат-связывающего домена из гликолитических гидролаз, которые имеются у многих сапрофитных бактерий, способных утилизировать хитин, целлюлозу, липополисахариды. 16
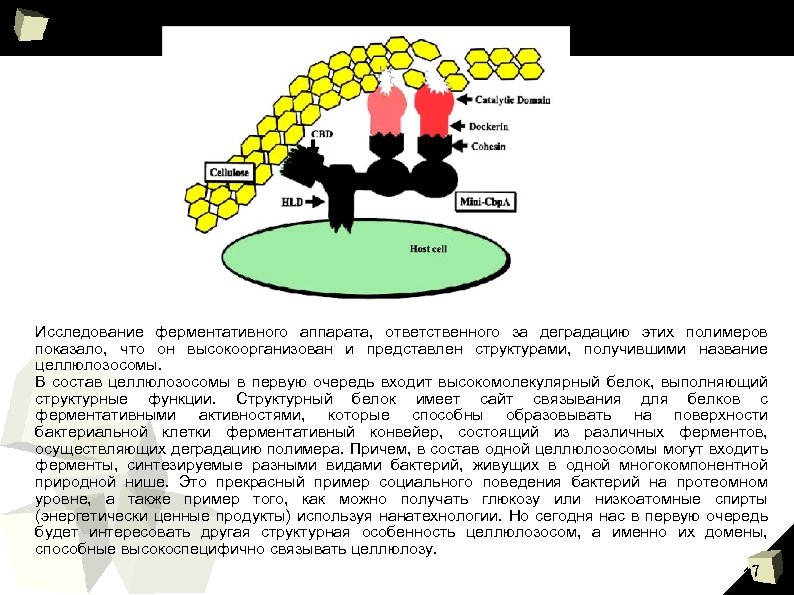
Исследование ферментативного аппарата, ответственного за деградацию этих полимеров показало, что он высокоорганизован и представлен структурами, получившими название целлюлозосомы. В состав целлюлозосомы в первую очередь входит высокомолекулярный белок, выполняющий структурные функции. Структурный белок имеет сайт связывания для белков с ферментативными активностями, которые способны образовывать на поверхности бактериальной клетки ферментативный конвейер, состоящий из различных ферментов, осуществляющих деградацию полимера. Причем, в состав одной целлюлозосомы могут входить ферменты, синтезируемые разными видами бактерий, живущих в одной многокомпонентной природной нише. Это прекрасный пример социального поведения бактерий на протеомном уровне, а также пример того, как можно получать глюкозу или низкоатомные спирты (энергетически ценные продукты) используя нанатехнологии. Но сегодня нас в первую очередь будет интересовать другая структурная особенность целлюлозосом, а именно их домены, способные высокоспецифично связывать целлюлозу. 17

Трехмерная структура ЦСД и ГСД 5’ 3’ N C В настоящее время генетическая организация ряда белков, содержащих целлюло- и гликанозосвязывающие домены известна. Фактически сама природа в процессе эволюции сделала все необходимое для того, чтобы была возможность использовать эти домены в составе гибридных белков. На 5’ и 3’ концах ДНК-фрагмента, кодирующего домен, имеются спейсерные последовательности, соответствующие С- и N-концевой частям белкового фрагмента, присоединение к которым, как было показано нами, не влияет на целлюлозо- и гликаносвязывающую способность. 18
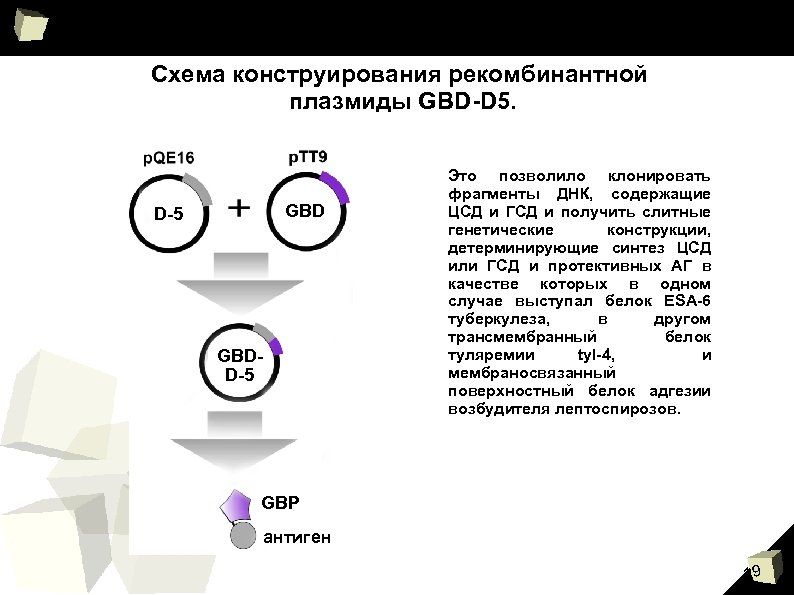
Схема конструирования рекомбинантной плазмиды GBD-D 5. GBD D-5 GBDD-5 Это позволило клонировать фрагменты ДНК, содержащие ЦСД и ГСД и получить слитные генетические конструкции, детерминирующие синтез ЦСД или ГСД и протективных АГ в качестве которых в одном случае выступал белок ESA-6 туберкулеза, в другом трансмембранный белок туляремии tyl-4, и мембраносвязанный поверхностный белок адгезии возбудителя лептоспирозов. GBP антиген 19
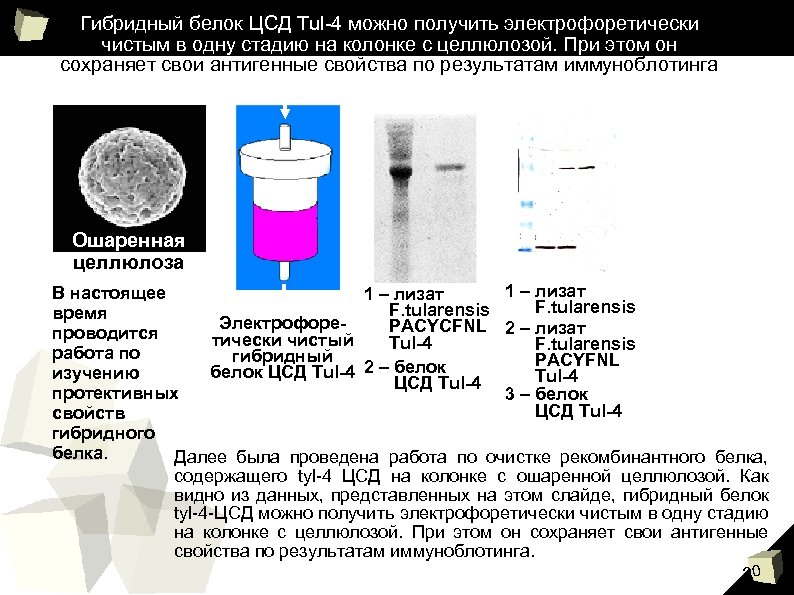
Гибридный белок ЦСД Tul-4 можно получить электрофоретически чистым в одну стадию на колонке с целлюлозой. При этом он сохраняет свои антигенные свойства по результатам иммуноблотинга лизат 1 2 3 Ошаренная целлюлоза 1 – лизат В настоящее 1 – лизат F. tularensis время Электрофоре. PACYCFNL 2 – лизат проводится тически чистый Tul-4 F. tularensis работа по гибридный PACYFNL белок ЦСД Tul-4 2 – белок изучению Tul-4 ЦСД Tul-4 протективных 3 – белок ЦСД Tul-4 свойств гибридного белка. Далее была проведена работа по очистке рекомбинантного белка, содержащего tyl-4 ЦСД на колонке с ошаренной целлюлозой. Как видно из данных, представленных на этом слайде, гибридный белок tyl-4 -ЦСД можно получить электрофоретически чистым в одну стадию на колонке с целлюлозой. При этом он сохраняет свои антигенные свойства по результатам иммуноблотинга. 20
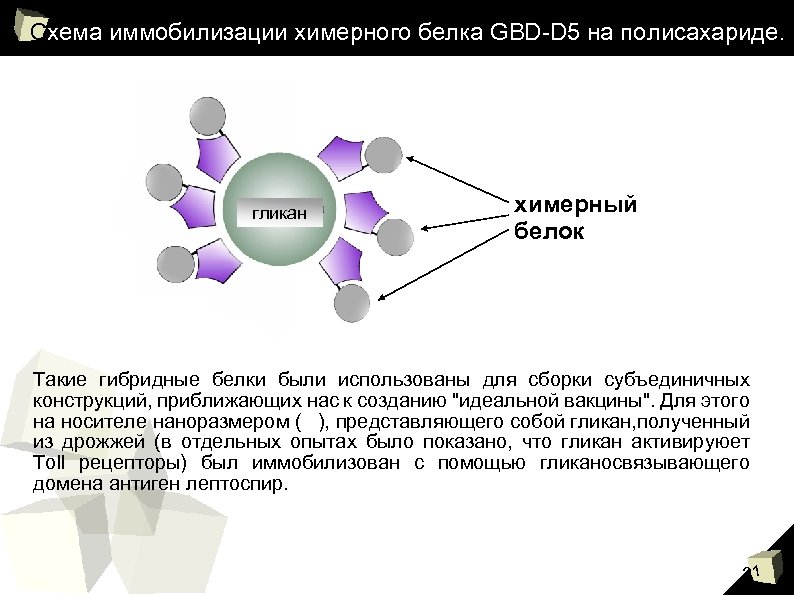
Схема иммобилизации химерного белка GBD-D 5 на полисахариде. гликан химерный белок Такие гибридные белки были использованы для сборки субъединичных конструкций, приближающих нас к созданию "идеальной вакцины". Для этого на носителе наноразмером ( ), представляющего собой гликан, полученный из дрожжей (в отдельных опытах было показано, что гликан активируюет Toll рецепторы) был иммобилизован с помощью гликаносвязывающего домена антиген лептоспир. 21
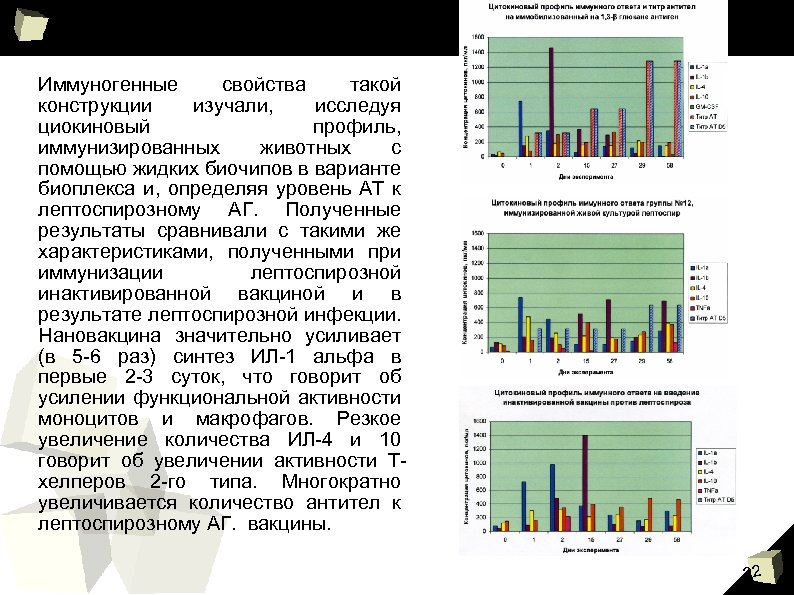
Иммуногенные свойства такой конструкции изучали, исследуя циокиновый профиль, иммунизированных животных с помощью жидких биочипов в варианте биоплекса и, определяя уровень АТ к лептоспирозному АГ. Полученные результаты сравнивали с такими же характеристиками, полученными при иммунизации лептоспирозной инактивированной вакциной и в результате лептоспирозной инфекции. Нановакцина значительно усиливает (в 5 -6 раз) синтез ИЛ-1 альфа в первые 2 -3 суток, что говорит об усилении функциональной активности моноцитов и макрофагов. Резкое увеличение количества ИЛ-4 и 10 говорит об увеличении активности Тхелперов 2 -го типа. Многократно увеличивается количество антител к лептоспирозному АГ. вакцины. 22

Таким образом, в настоящее время мы располагаем рядом технологий, аналогичных тем, что заложены в конструкторе "Лего", позволяющим создавать различные комбинации наноконструкций, пригодных для поиска наиболее эффективной на пути создания субъединичной вакцины. 23
Сдерживающим моментом здесь, как и в большинстве наноразработок, имеющих отношение к медицине является отсутствие биосовестимых и биодеградируемых наноматериалов, как для создания иммунобиологических препаратов, так и мишень-ориентированной доставки лекарства, всех видов протезирования и т. п. Эту проблему нанобиологического материаловедения с нашей точки зрения необходимо выделить в отдельную подпрограмму в рамках нанотехнологического проекта в стране. 24
99b729abc6996ce4aa5fa56c54af3c26.ppt