Использование метода проточной цитофлюориметрии в диагностике

























2 Лейкозы + проточная цитофлюориметрия Ижевск 2010.ppt
- Количество слайдов: 74
 Использование метода проточной цитофлюориметрии в диагностике гемобластозов Толстолуцкая Татьяна Олеговна Ижевская государственная медицинская академия Кафедра клинической биохимии и лабораторной диагностики Ижевск, 2008 г.
Использование метода проточной цитофлюориметрии в диагностике гемобластозов Толстолуцкая Татьяна Олеговна Ижевская государственная медицинская академия Кафедра клинической биохимии и лабораторной диагностики Ижевск, 2008 г.
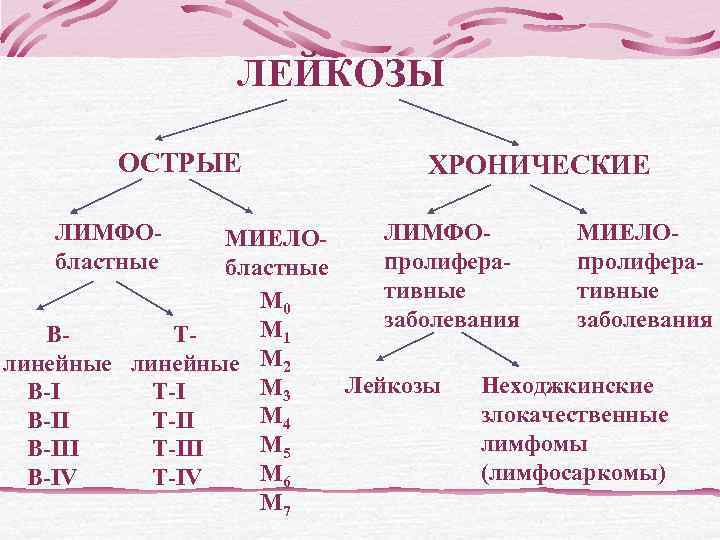
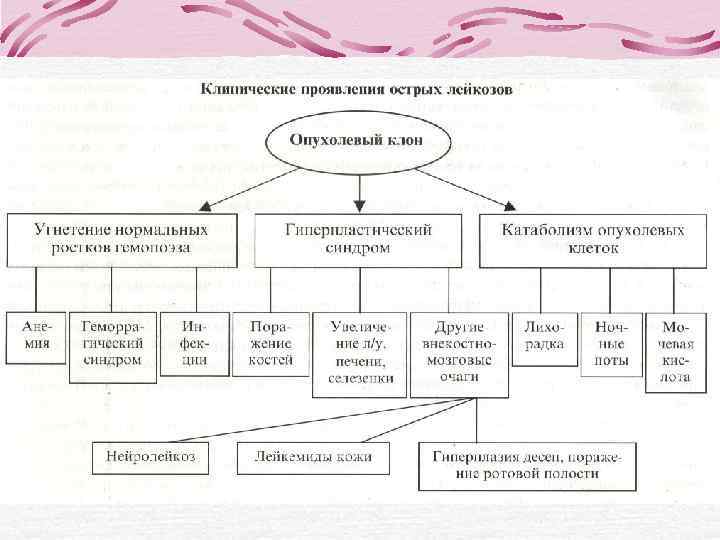
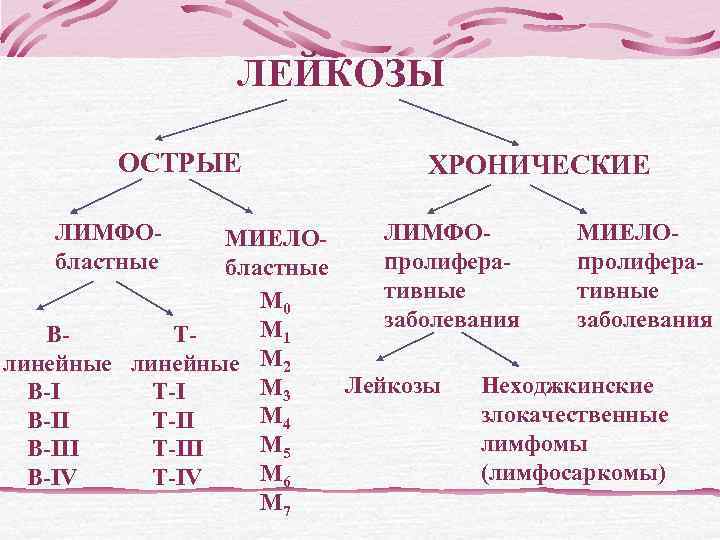
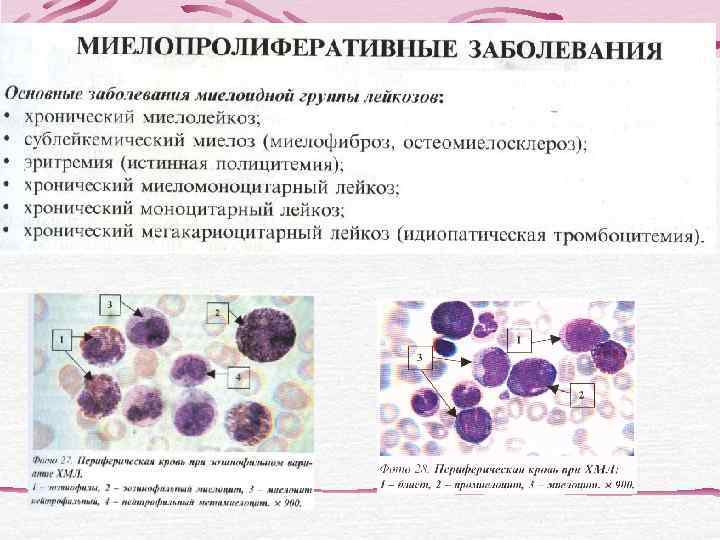
 ЛЕЙКОЗЫ ОСТРЫЕ ХРОНИЧЕСКИЕ ЛИМФО- МИЕЛО- ЛИМФО- МИЕЛО- бластные пролифера- М 0 тивные М 1 заболевания В- Т- линейные М 2 В-I Т-I М 3 Лейкозы Неходжкинские В-II Т-II М 4 злокачественные В-III Т-III М 5 лимфомы В-IV Т-IV М 6 (лимфосаркомы) М 7
ЛЕЙКОЗЫ ОСТРЫЕ ХРОНИЧЕСКИЕ ЛИМФО- МИЕЛО- ЛИМФО- МИЕЛО- бластные пролифера- М 0 тивные М 1 заболевания В- Т- линейные М 2 В-I Т-I М 3 Лейкозы Неходжкинские В-II Т-II М 4 злокачественные В-III Т-III М 5 лимфомы В-IV Т-IV М 6 (лимфосаркомы) М 7
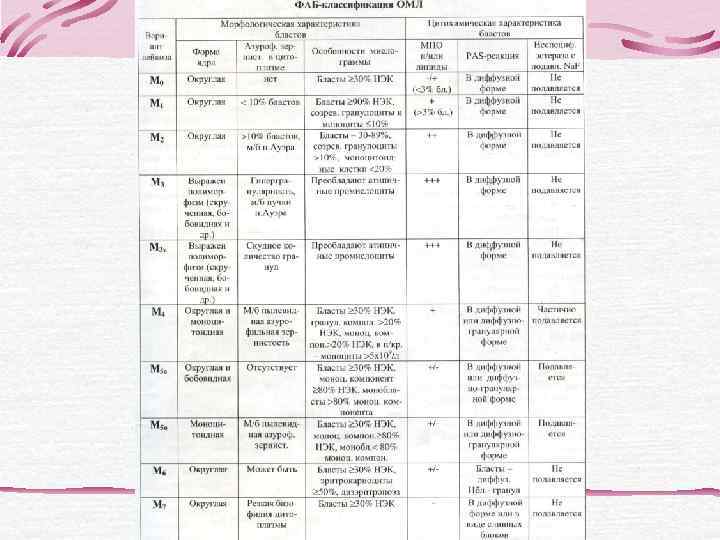
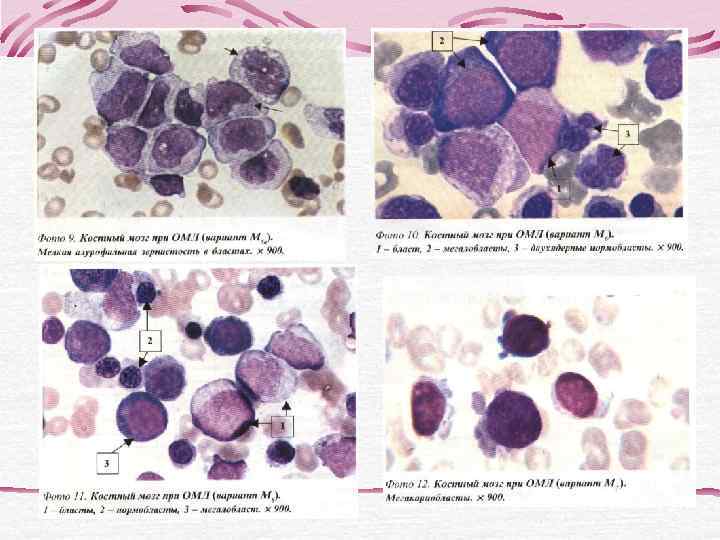
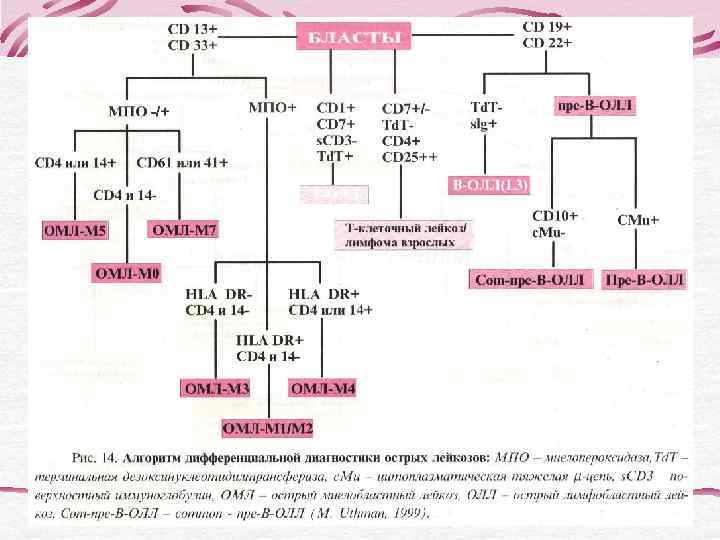
 ОСТРЫЕ ЛЕЙКОЗЫ ЛИМФОБЛАСТНЫЕ МИЕЛОБЛАСТНЫЕ (МБЛ) М 0 - острый МБЛ с минимальной миелоидной дифференцировкой бластов М 1 - острый МБЛ без созревания В- Т- М 2 - острый МБЛ с созреванием линейные М 3 - острый промиелоцитарный лейкоз М 3 v – атипичный или гипогранулярный В-I Т-I вариант острого промиелоцитарного лейкоза В-II Т-II М 4 – острый миеломонобластный лейкоз В-III Т-III М 4 эоз – острый миеломонобластный лейкоз с В-IV Т-IV эозинофилией М 5 а – острый монобластный лейкоз без созревания М 5 в – острый монобластный лейкоз с созреванием М 6 – острый эритромиелоз М 7 – острый мегакариобластный лейкоз
ОСТРЫЕ ЛЕЙКОЗЫ ЛИМФОБЛАСТНЫЕ МИЕЛОБЛАСТНЫЕ (МБЛ) М 0 - острый МБЛ с минимальной миелоидной дифференцировкой бластов М 1 - острый МБЛ без созревания В- Т- М 2 - острый МБЛ с созреванием линейные М 3 - острый промиелоцитарный лейкоз М 3 v – атипичный или гипогранулярный В-I Т-I вариант острого промиелоцитарного лейкоза В-II Т-II М 4 – острый миеломонобластный лейкоз В-III Т-III М 4 эоз – острый миеломонобластный лейкоз с В-IV Т-IV эозинофилией М 5 а – острый монобластный лейкоз без созревания М 5 в – острый монобластный лейкоз с созреванием М 6 – острый эритромиелоз М 7 – острый мегакариобластный лейкоз
 FAB Klassifikation der AML
FAB Klassifikation der AML
 Классификация острых миелолейкозов ВОЗ 2001
Классификация острых миелолейкозов ВОЗ 2001
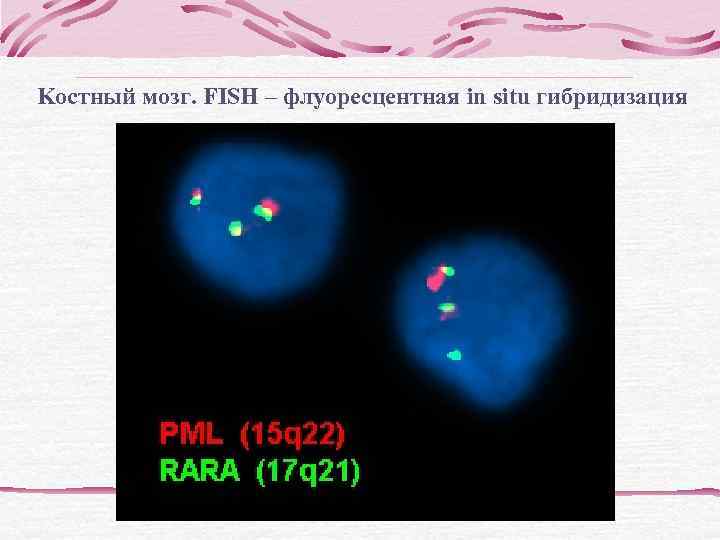
 Kостный мозг. FISH – флуоресцентная in situ гибридизация
Kостный мозг. FISH – флуоресцентная in situ гибридизация
 Использование метода проточной цитофлюориметрии в диагностике гемобластозов Толстолуцкая Татьяна Олеговна Ижевская государственная медицинская академия Кафедра клинической биохимии и лабораторной диагностики Ижевск, 2008 г.
Использование метода проточной цитофлюориметрии в диагностике гемобластозов Толстолуцкая Татьяна Олеговна Ижевская государственная медицинская академия Кафедра клинической биохимии и лабораторной диагностики Ижевск, 2008 г.
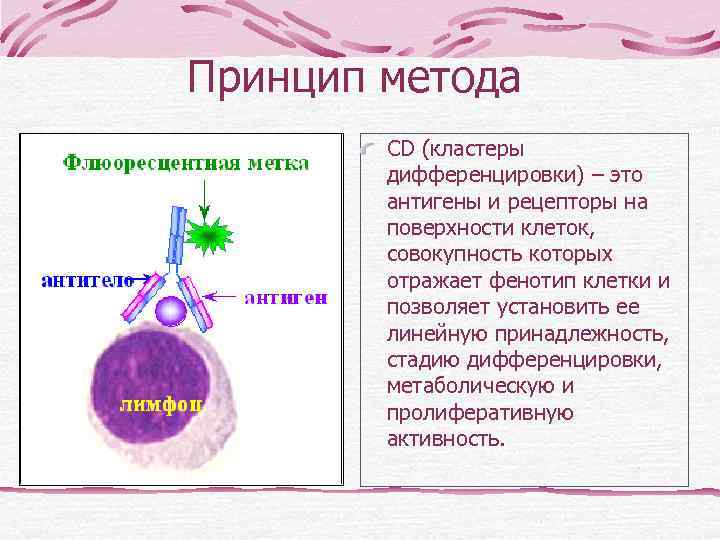
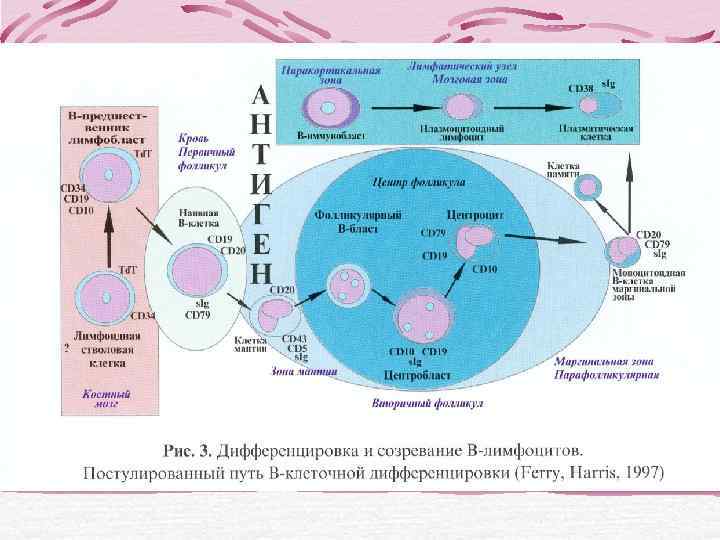
 Принцип метода СD (кластеры дифференцировки) – это антигены и рецепторы на поверхности клеток, совокупность которых отражает фенотип клетки и позволяет установить ее линейную принадлежность, стадию дифференцировки, метаболическую и пролиферативную активность.
Принцип метода СD (кластеры дифференцировки) – это антигены и рецепторы на поверхности клеток, совокупность которых отражает фенотип клетки и позволяет установить ее линейную принадлежность, стадию дифференцировки, метаболическую и пролиферативную активность.
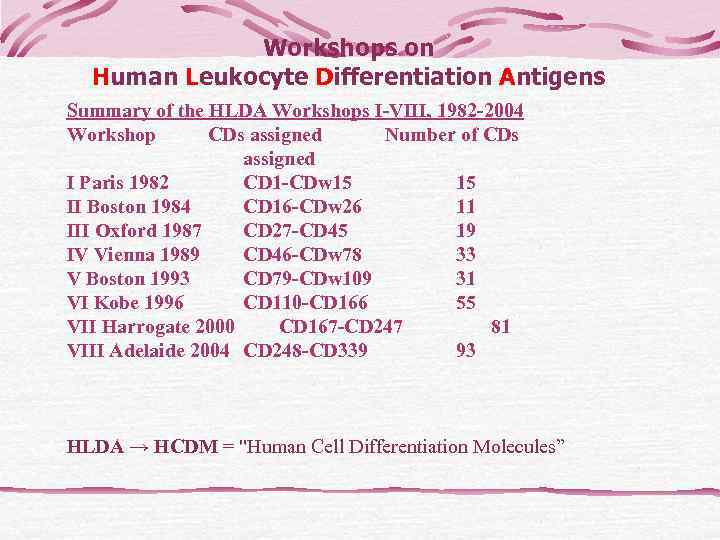
 Workshops on Human Leukocyte Differentiation Antigens Summary of the HLDA Workshops I-VIII, 1982 -2004 Workshop CDs assigned Number of CDs assigned I Paris 1982 CD 1 -CDw 15 II Boston 1984 CD 16 -CDw 26 11 III Oxford 1987 CD 27 -CD 45 19 IV Vienna 1989 CD 46 -CDw 78 33 V Boston 1993 CD 79 -CDw 109 31 VI Kobe 1996 CD 110 -CD 166 55 VII Harrogate 2000 CD 167 -CD 247 81 VIII Adelaide 2004 CD 248 -CD 339 93 HLDA → HCDM = "Human Cell Differentiation Molecules”
Workshops on Human Leukocyte Differentiation Antigens Summary of the HLDA Workshops I-VIII, 1982 -2004 Workshop CDs assigned Number of CDs assigned I Paris 1982 CD 1 -CDw 15 II Boston 1984 CD 16 -CDw 26 11 III Oxford 1987 CD 27 -CD 45 19 IV Vienna 1989 CD 46 -CDw 78 33 V Boston 1993 CD 79 -CDw 109 31 VI Kobe 1996 CD 110 -CD 166 55 VII Harrogate 2000 CD 167 -CD 247 81 VIII Adelaide 2004 CD 248 -CD 339 93 HLDA → HCDM = "Human Cell Differentiation Molecules”
 Оценка иммунологического фенотипа нормальных и опухолевых клеток может проводится различными методами: - реакцией иммунофлюоресценции - иммуногистохимией - иммуноцитохимией - лазерной проточной цитофлюориметрией
Оценка иммунологического фенотипа нормальных и опухолевых клеток может проводится различными методами: - реакцией иммунофлюоресценции - иммуногистохимией - иммуноцитохимией - лазерной проточной цитофлюориметрией
 Преимущества метода лазерной проточной цитофлюориметрии - исследование большого количества клеток (более 10 000 клеток в 1 секунду) - мониторинг минимальной резидуальной болезни в стадии ремиссии - одновременное изучение нескольких антигенных структур на одной клетке - количественная оценка экспрессии антигена - исследование клеточного цикла и изучение анеуплоидных клеток
Преимущества метода лазерной проточной цитофлюориметрии - исследование большого количества клеток (более 10 000 клеток в 1 секунду) - мониторинг минимальной резидуальной болезни в стадии ремиссии - одновременное изучение нескольких антигенных структур на одной клетке - количественная оценка экспрессии антигена - исследование клеточного цикла и изучение анеуплоидных клеток
 Материалом для исследования может быть любая взвесь клеток: - кровь - костный мозг - ликвор - плевральная, асцитическая жидкость - ткань лимфоузла, селезенки - клетки солидных опухолей после предварительной обработки
Материалом для исследования может быть любая взвесь клеток: - кровь - костный мозг - ликвор - плевральная, асцитическая жидкость - ткань лимфоузла, селезенки - клетки солидных опухолей после предварительной обработки
 В основе проточной цитофлюориметрии лежит проведение фотометрических и флюоресцентных измерений отдельных клеток, пересекающих одна за другой вместе с потоком жидкости лазерный луч монохроматического света.
В основе проточной цитофлюориметрии лежит проведение фотометрических и флюоресцентных измерений отдельных клеток, пересекающих одна за другой вместе с потоком жидкости лазерный луч монохроматического света.
 ПРОТОЧНЫЙ ЦИТОФЛУОРИМЕТР FACSCanto II
ПРОТОЧНЫЙ ЦИТОФЛУОРИМЕТР FACSCanto II
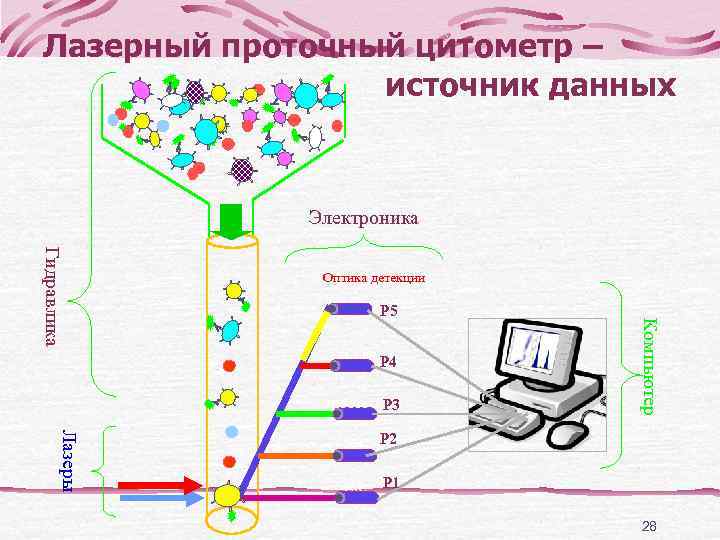
 Лазерный проточный цитометр – источник данных Электроника Гидравлика Оптика детекции P 5 Компьютер FL 2 PE P 4 FL 1 FITC P 3 Лазеры SSC P 2 FSC P 1 28
Лазерный проточный цитометр – источник данных Электроника Гидравлика Оптика детекции P 5 Компьютер FL 2 PE P 4 FL 1 FITC P 3 Лазеры SSC P 2 FSC P 1 28
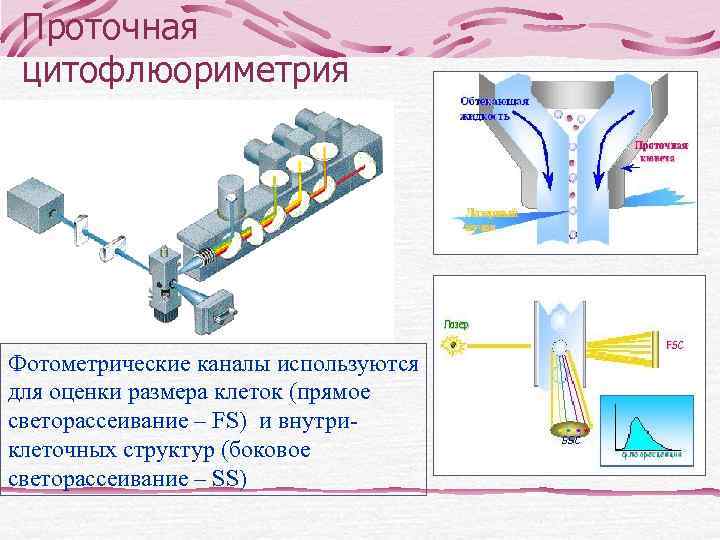
 Проточная цитофлюориметрия Фотометрические каналы используются для оценки размера клеток (прямое светорассеивание – FS) и внутри- клеточных структур (боковое светорассеивание – SS)
Проточная цитофлюориметрия Фотометрические каналы используются для оценки размера клеток (прямое светорассеивание – FS) и внутри- клеточных структур (боковое светорассеивание – SS)
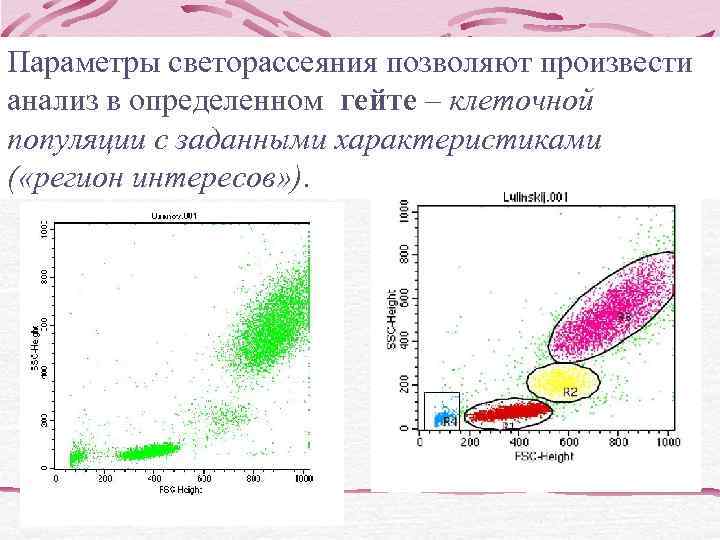
 Параметры светорассеяния позволяют произвести анализ в определенном гейте – клеточной популяции с заданными характеристиками ( «регион интересов» ).
Параметры светорассеяния позволяют произвести анализ в определенном гейте – клеточной популяции с заданными характеристиками ( «регион интересов» ).
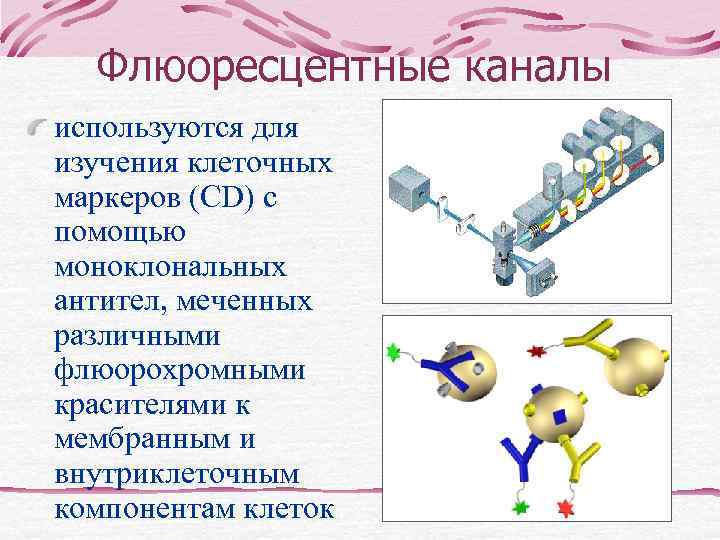
 Флюоресцентные каналы используются для изучения клеточных маркеров (CD) с помощью моноклональных антител, меченных различными флюорохромными красителями к мембранным и внутриклеточным компонентам клеток
Флюоресцентные каналы используются для изучения клеточных маркеров (CD) с помощью моноклональных антител, меченных различными флюорохромными красителями к мембранным и внутриклеточным компонентам клеток
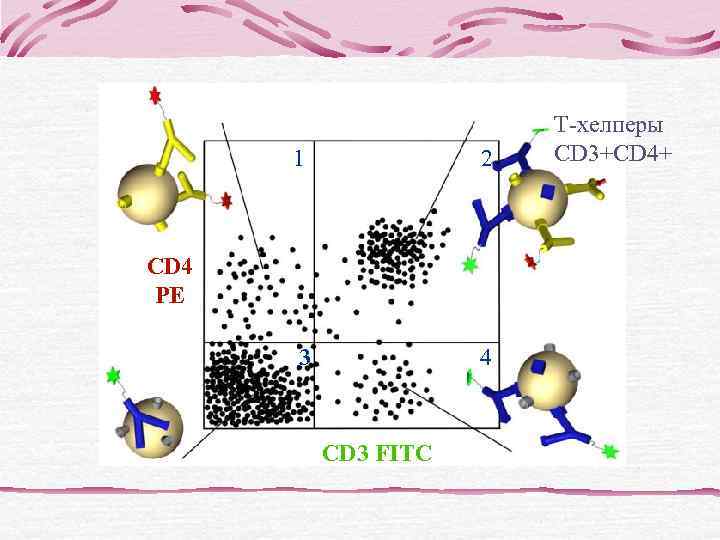
 T-хелперы 1 2 CD 3+CD 4+ СD 4 PE 3 4 CD 3 FITC
T-хелперы 1 2 CD 3+CD 4+ СD 4 PE 3 4 CD 3 FITC
 ЛЕЙКОЗЫ ОСТРЫЕ ХРОНИЧЕСКИЕ ЛИМФО- МИЕЛО- ЛИМФО- МИЕЛО- бластные пролифера- М 0 тивные М 1 заболевания В- Т- линейные М 2 В-I Т-I М 3 Лейкозы Неходжкинские В-II Т-II М 4 злокачественные В-III Т-III М 5 лимфомы В-IV Т-IV М 6 (лимфосаркомы) М 7
ЛЕЙКОЗЫ ОСТРЫЕ ХРОНИЧЕСКИЕ ЛИМФО- МИЕЛО- ЛИМФО- МИЕЛО- бластные пролифера- М 0 тивные М 1 заболевания В- Т- линейные М 2 В-I Т-I М 3 Лейкозы Неходжкинские В-II Т-II М 4 злокачественные В-III Т-III М 5 лимфомы В-IV Т-IV М 6 (лимфосаркомы) М 7
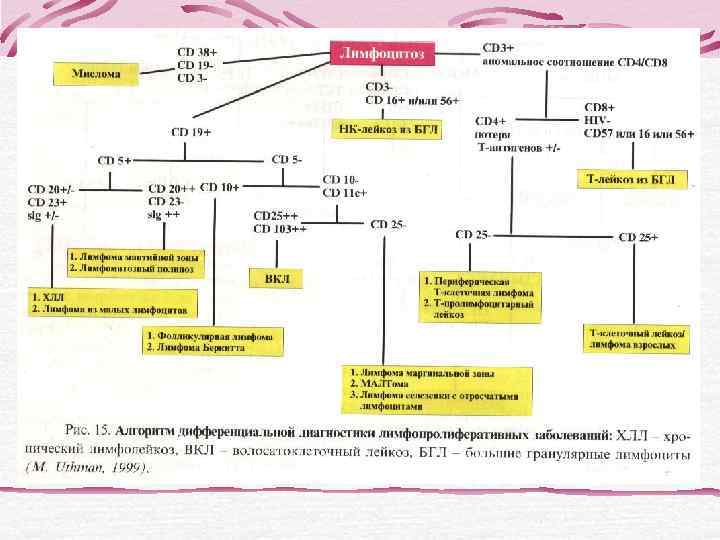
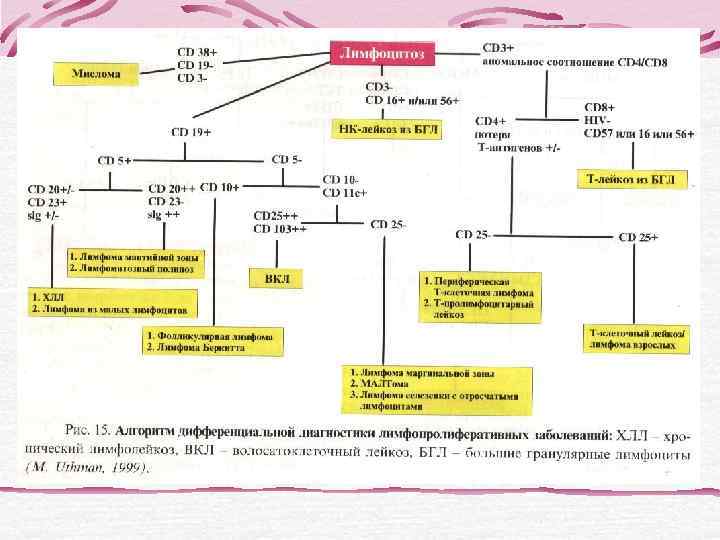
 Проточная цитофлуориметрия ? Хронический Наблюдай и лимфолейкоз? жди? Лимфома зоны Хлорамбуцил? мантии? Флударабин? Фолликулярная Мабтера? лимфома? Кэмпас? Лимфома Удаление маргинальной селезенки? зоны селезенки? Полихимиоте Лейкоцитоз рапия CHOP? Абсолютный Т – клеточная лимфома? лимфоцитоз
Проточная цитофлуориметрия ? Хронический Наблюдай и лимфолейкоз? жди? Лимфома зоны Хлорамбуцил? мантии? Флударабин? Фолликулярная Мабтера? лимфома? Кэмпас? Лимфома Удаление маргинальной селезенки? зоны селезенки? Полихимиоте Лейкоцитоз рапия CHOP? Абсолютный Т – клеточная лимфома? лимфоцитоз
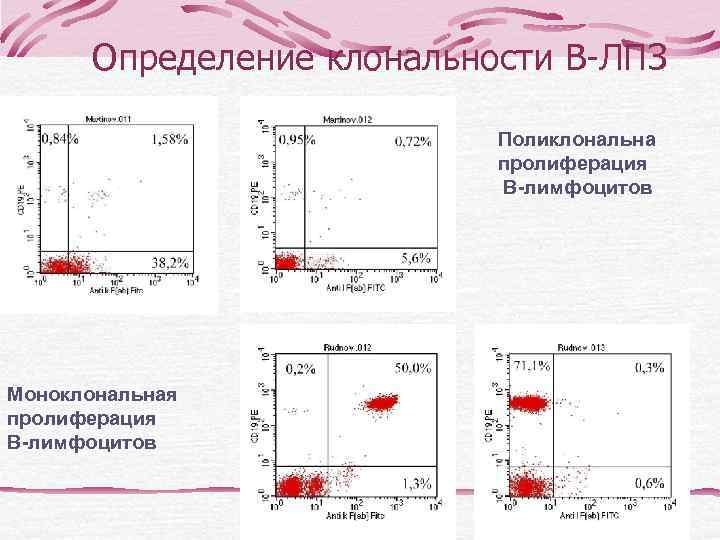
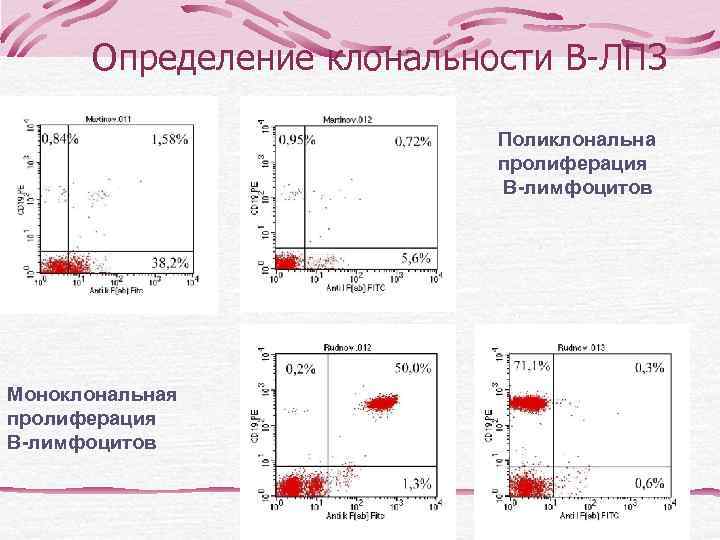
 Определение клональности В-ЛПЗ Поликлональна пролиферация В-лимфоцитов Моноклональная пролиферация В-лимфоцитов
Определение клональности В-ЛПЗ Поликлональна пролиферация В-лимфоцитов Моноклональная пролиферация В-лимфоцитов
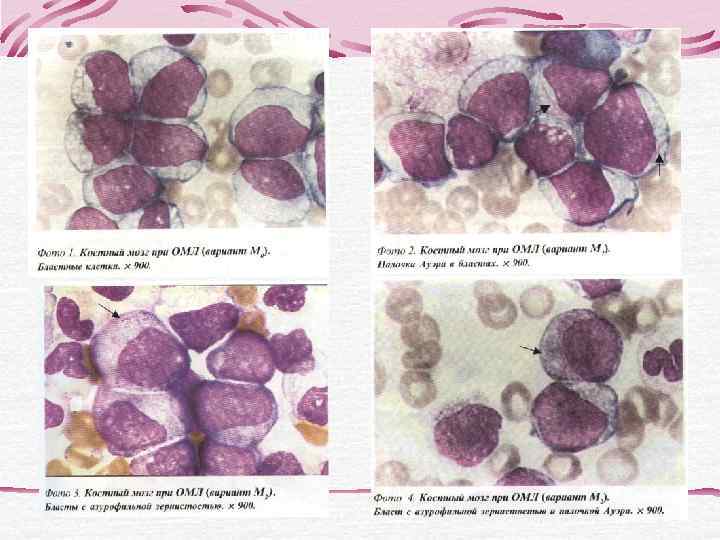
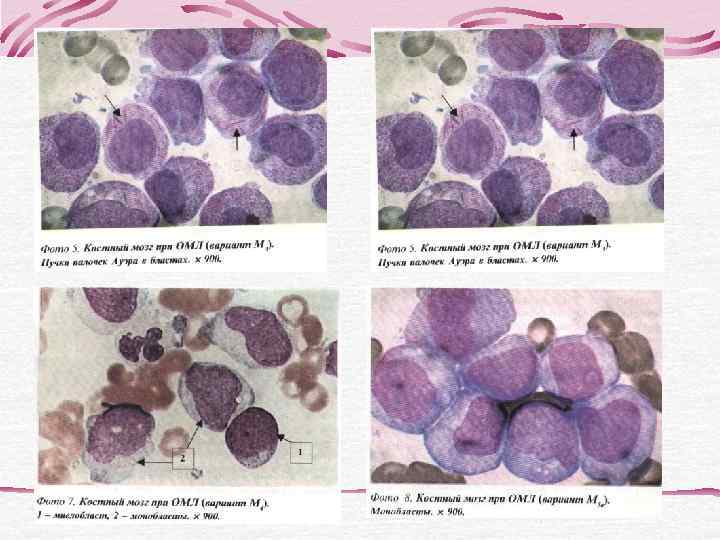
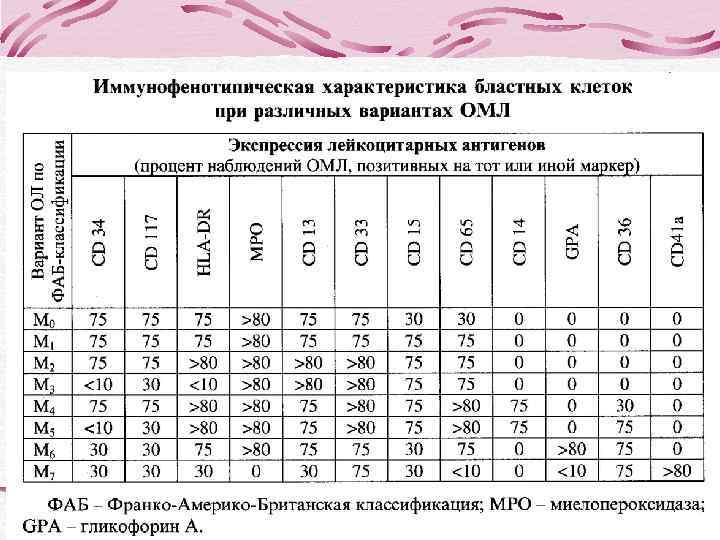
 В пунктате КМ бластные клетки составляют 88, 2%, представлены преимущественно мезоформами с умеренным ядерно-цитоплазматическим соотношением и слабой базофилией цитоплазмы. Форма ядер в основном округлая, структура хроматина нежная. Зернистость не определяется. МПО и липиды отрицательные, PAS-положительное вещество в гранулярной форме в единичных бластных клетках. Установление морфоцитохимического варианта острого лейкоза затруднено. При иммунофенотипировании КМ выявлен фенотип бластных клеток: CD 34+, HLA-DR+, CD 13+, CD 33+, CD 7+ Заключение: иммунофенотип бластных клеток соответствует М 0 варианту ОМЛ с коэкспрессией Т- клеточного антигена CD 7, что отражает неблагоприятный прогноз заболевания.
В пунктате КМ бластные клетки составляют 88, 2%, представлены преимущественно мезоформами с умеренным ядерно-цитоплазматическим соотношением и слабой базофилией цитоплазмы. Форма ядер в основном округлая, структура хроматина нежная. Зернистость не определяется. МПО и липиды отрицательные, PAS-положительное вещество в гранулярной форме в единичных бластных клетках. Установление морфоцитохимического варианта острого лейкоза затруднено. При иммунофенотипировании КМ выявлен фенотип бластных клеток: CD 34+, HLA-DR+, CD 13+, CD 33+, CD 7+ Заключение: иммунофенотип бластных клеток соответствует М 0 варианту ОМЛ с коэкспрессией Т- клеточного антигена CD 7, что отражает неблагоприятный прогноз заболевания.
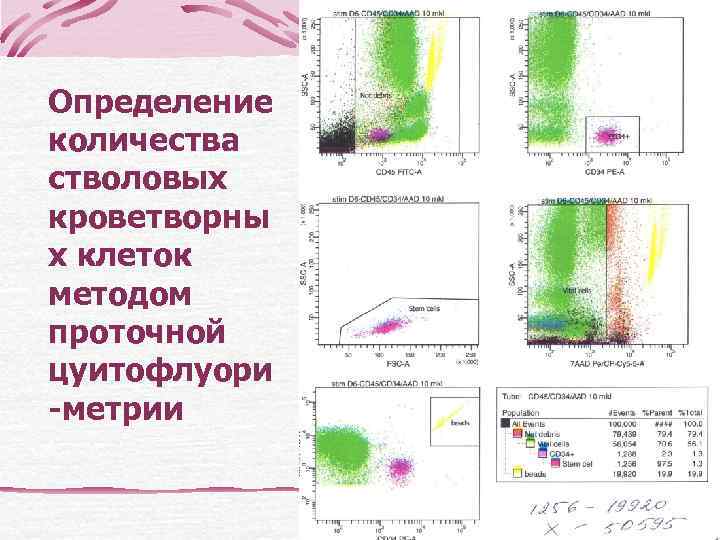
 Определение количества стволовых кроветворны х клеток методом проточной цуитофлуори -метрии
Определение количества стволовых кроветворны х клеток методом проточной цуитофлуори -метрии
 Клиническое значение иммунофенотипизирования на примере ОЛЛ Multizentrische Therapieoptimierungsstudie der akuten lymphatischen Leukämie bei Erwachsenen und Adoleszenten ab 15 Jahren GMALL 07/2003 (Hoelzer-Protokoll) Иммунофенотипические критерии:
Клиническое значение иммунофенотипизирования на примере ОЛЛ Multizentrische Therapieoptimierungsstudie der akuten lymphatischen Leukämie bei Erwachsenen und Adoleszenten ab 15 Jahren GMALL 07/2003 (Hoelzer-Protokoll) Иммунофенотипические критерии:
 Бифенотипические острые лейкозы Points B lymphoid T lymphoid myeloid * * May be expressed in some cases of precursor T lymphoblastic leukaemia/lymphoma European Group for the Immunological Characterization of Leukemias (EGIL) Leukemia (1995) 9, 1783 -1786 Brunning et al. Acute leukaemias of ambigous lineage. WHO Classification of Tumours: Tumours of Hematopietic and lymphoid tissues. 2001
Бифенотипические острые лейкозы Points B lymphoid T lymphoid myeloid * * May be expressed in some cases of precursor T lymphoblastic leukaemia/lymphoma European Group for the Immunological Characterization of Leukemias (EGIL) Leukemia (1995) 9, 1783 -1786 Brunning et al. Acute leukaemias of ambigous lineage. WHO Classification of Tumours: Tumours of Hematopietic and lymphoid tissues. 2001
 ЭРИТРЕМИЯ
ЭРИТРЕМИЯ
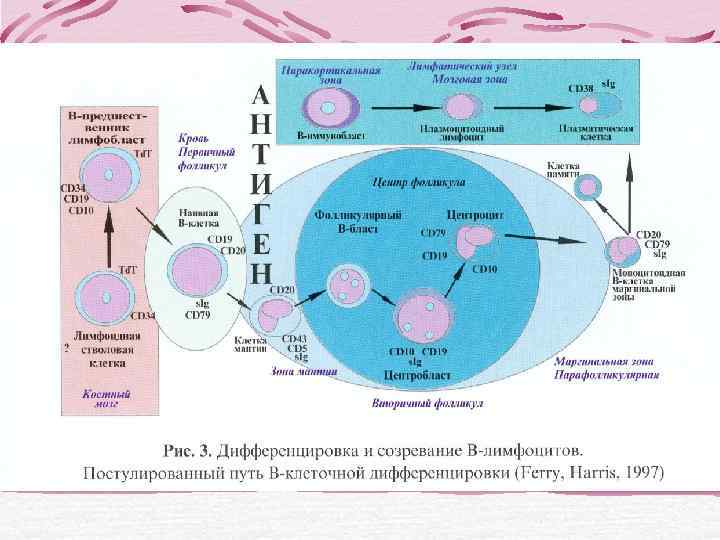
 Лимфопролиферативные заболевания В-клеточные опухоли Т- и НК-клеточные опухоли Из предшест- Из зрелых венников (периферических) В-клеток Т-клеток
Лимфопролиферативные заболевания В-клеточные опухоли Т- и НК-клеточные опухоли Из предшест- Из зрелых венников (периферических) В-клеток Т-клеток
 В-клеточные опухоли лимфоидной ткани Из предшественников В-клеток В-лимфобластная лимфома/лейкоз из клеток-предшественников В-клеточные опухоли из зрелых (периферических) клеток: В-клеточный ХЛЛ/лимфома из малых лимфоцитов В-клеточный пролимфоцитарный лейкоз Лимфоплазмоцитарная лимфома Лимфома маргинальной зоны селезенки Волосатоклеточный лейкоз Плазмоклеточная миелома/плазмоцитома Нодальная В-клеточная лимфома маргинальной зоны MALT-лимфома Фолликулярная лимфома Лимфома из клеток мантийной зоны Диффузная крупноклеточная лимфома Лимфома/лейкоз Беркитта
В-клеточные опухоли лимфоидной ткани Из предшественников В-клеток В-лимфобластная лимфома/лейкоз из клеток-предшественников В-клеточные опухоли из зрелых (периферических) клеток: В-клеточный ХЛЛ/лимфома из малых лимфоцитов В-клеточный пролимфоцитарный лейкоз Лимфоплазмоцитарная лимфома Лимфома маргинальной зоны селезенки Волосатоклеточный лейкоз Плазмоклеточная миелома/плазмоцитома Нодальная В-клеточная лимфома маргинальной зоны MALT-лимфома Фолликулярная лимфома Лимфома из клеток мантийной зоны Диффузная крупноклеточная лимфома Лимфома/лейкоз Беркитта
 Определение клональности В-ЛПЗ Поликлональна пролиферация В-лимфоцитов Моноклональная пролиферация В-лимфоцитов
Определение клональности В-ЛПЗ Поликлональна пролиферация В-лимфоцитов Моноклональная пролиферация В-лимфоцитов
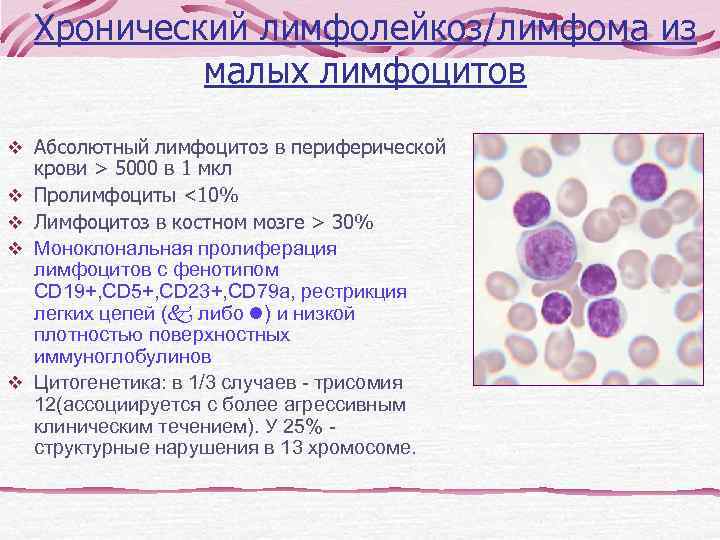
 Хронический лимфолейкоз/лимфома из малых лимфоцитов Абсолютный лимфоцитоз в периферической крови > 5000 в 1 мкл Пролимфоциты <10% Лимфоцитоз в костном мозге > 30% Моноклональная пролиферация лимфоцитов с фенотипом СD 19+, CD 5+, CD 23+, CD 79 a, рестрикция легких цепей ( либо ) и низкой плотностью поверхностных иммуноглобулинов Цитогенетика: в 1/3 случаев - трисомия 12(ассоциируется с более агрессивным клиническим течением). У 25% - структурные нарушения в 13 хромосоме.
Хронический лимфолейкоз/лимфома из малых лимфоцитов Абсолютный лимфоцитоз в периферической крови > 5000 в 1 мкл Пролимфоциты <10% Лимфоцитоз в костном мозге > 30% Моноклональная пролиферация лимфоцитов с фенотипом СD 19+, CD 5+, CD 23+, CD 79 a, рестрикция легких цепей ( либо ) и низкой плотностью поверхностных иммуноглобулинов Цитогенетика: в 1/3 случаев - трисомия 12(ассоциируется с более агрессивным клиническим течением). У 25% - структурные нарушения в 13 хромосоме.
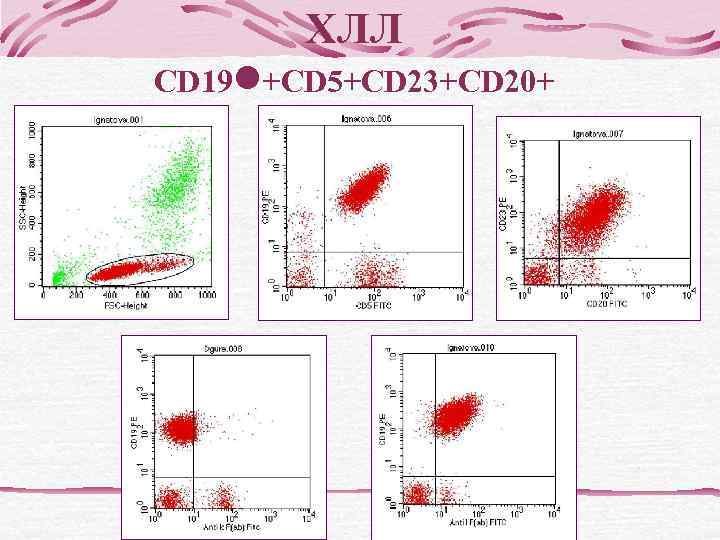
 ХЛЛ CD 19 +CD 5+CD 23+CD 20+
ХЛЛ CD 19 +CD 5+CD 23+CD 20+
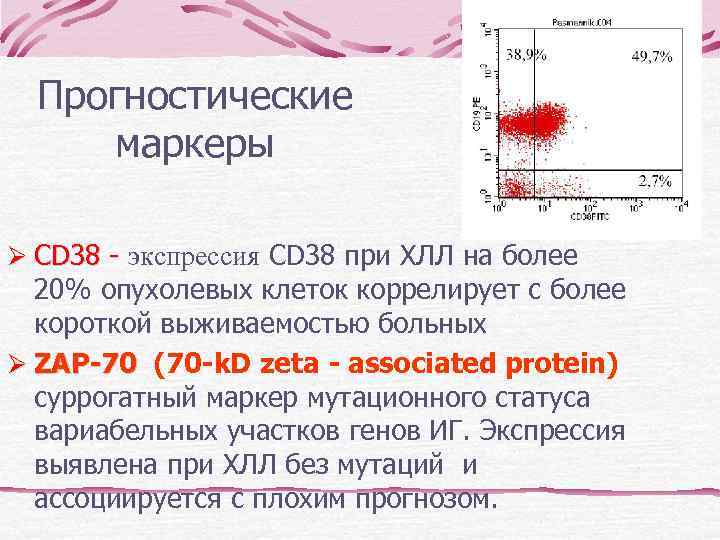
 Прогностические маркеры CD 38 - экспрессия CD 38 при ХЛЛ на более 20% опухолевых клеток коррелирует с более короткой выживаемостью больных ZAP-70 (70 -k. D zeta - associated protein) суррогатный маркер мутационного статуса вариабельных участков генов ИГ. Экспрессия выявлена при ХЛЛ без мутаций и ассоциируется с плохим прогнозом.
Прогностические маркеры CD 38 - экспрессия CD 38 при ХЛЛ на более 20% опухолевых клеток коррелирует с более короткой выживаемостью больных ZAP-70 (70 -k. D zeta - associated protein) суррогатный маркер мутационного статуса вариабельных участков генов ИГ. Экспрессия выявлена при ХЛЛ без мутаций и ассоциируется с плохим прогнозом.
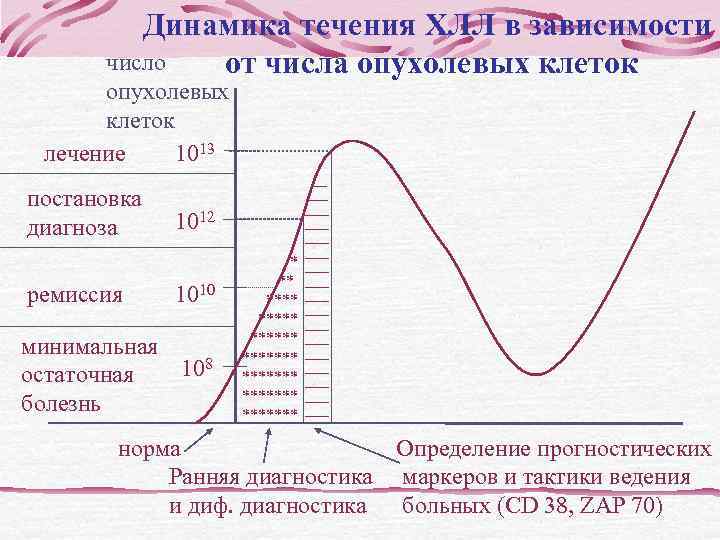
 Динамика течения ХЛЛ в зависимости число от числа опухолевых клеток опухолевых клеток лечение 1013 ---- постановка ------ диагноза 1012 ------ * ------ ** ------ ремиссия 1010 **** ------ ***** ------ ****** минимальная ******* ------ остаточная 108 ******* ------ ******* болезнь ******* ------ норма Определение прогностических Ранняя диагностика маркеров и тактики ведения и диф. диагностика больных (CD 38, ZAP 70)
Динамика течения ХЛЛ в зависимости число от числа опухолевых клеток опухолевых клеток лечение 1013 ---- постановка ------ диагноза 1012 ------ * ------ ** ------ ремиссия 1010 **** ------ ***** ------ ****** минимальная ******* ------ остаточная 108 ******* ------ ******* болезнь ******* ------ норма Определение прогностических Ранняя диагностика маркеров и тактики ведения и диф. диагностика больных (CD 38, ZAP 70)
 Фолликулярная лимфома Группа лимфоидных опухолей, происходящих из светлых центров размножения фолликулов (центроцитов/центробластов) Составляет от 30 -40% всех лимфоидных опухолей, средний возраст больных– 59 лет. Опухолевый аналог-В-лимфоцит из фолликулярного центра Соматические Ig. VH мутации Критическим молекулярным событием в патогенезе фолликулярной лимфомы является транслокация t(14; 18) (в 80 -90% случаях) с высокой конститутивной экспрессией BCL-2, что обеспечивает преимущество в выживании опухолевых клеток и ингибицию апоптоза
Фолликулярная лимфома Группа лимфоидных опухолей, происходящих из светлых центров размножения фолликулов (центроцитов/центробластов) Составляет от 30 -40% всех лимфоидных опухолей, средний возраст больных– 59 лет. Опухолевый аналог-В-лимфоцит из фолликулярного центра Соматические Ig. VH мутации Критическим молекулярным событием в патогенезе фолликулярной лимфомы является транслокация t(14; 18) (в 80 -90% случаях) с высокой конститутивной экспрессией BCL-2, что обеспечивает преимущество в выживании опухолевых клеток и ингибицию апоптоза
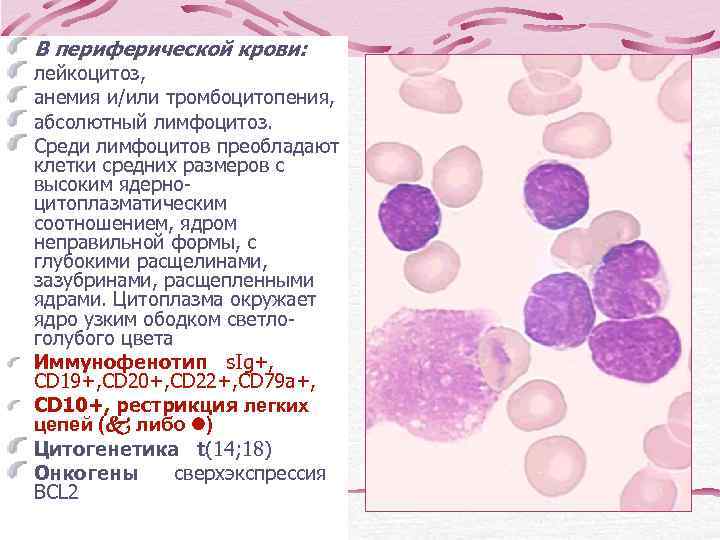
 В периферической крови: лейкоцитоз, анемия и/или тромбоцитопения, абсолютный лимфоцитоз. Среди лимфоцитов преобладают клетки средних размеров с высоким ядерно- цитоплазматическим соотношением, ядром неправильной формы, с глубокими расщелинами, зазубринами, расщепленными ядрами. Цитоплазма окружает ядро узким ободком светло- голубого цвета Иммунофенотип s. Ig+, CD 19+, CD 20+, CD 22+, CD 79 a+, CD 10+, рестрикция легких цепей ( либо ) Цитогенетика t(14; 18) Онкогены сверхэкспрессия BCL 2
В периферической крови: лейкоцитоз, анемия и/или тромбоцитопения, абсолютный лимфоцитоз. Среди лимфоцитов преобладают клетки средних размеров с высоким ядерно- цитоплазматическим соотношением, ядром неправильной формы, с глубокими расщелинами, зазубринами, расщепленными ядрами. Цитоплазма окружает ядро узким ободком светло- голубого цвета Иммунофенотип s. Ig+, CD 19+, CD 20+, CD 22+, CD 79 a+, CD 10+, рестрикция легких цепей ( либо ) Цитогенетика t(14; 18) Онкогены сверхэкспрессия BCL 2
 Лимфома из клеток мантийной зоны Составляет 6% всех злокачественных неходжкинских лимфом Опухолевый субстрат –наивный В-лимфоцит зоны мантии (CD 19+CD 5+CD 23 -) Наиболее характерные клинические признаки: генерализованная лимфаденопатия, поражение печени, селезенки, костного мозга (в 50 -82% наблюдений). Три цитологических варианта (мелкоклеточный, полиморфноклеточный, бластоидный)
Лимфома из клеток мантийной зоны Составляет 6% всех злокачественных неходжкинских лимфом Опухолевый субстрат –наивный В-лимфоцит зоны мантии (CD 19+CD 5+CD 23 -) Наиболее характерные клинические признаки: генерализованная лимфаденопатия, поражение печени, селезенки, костного мозга (в 50 -82% наблюдений). Три цитологических варианта (мелкоклеточный, полиморфноклеточный, бластоидный)
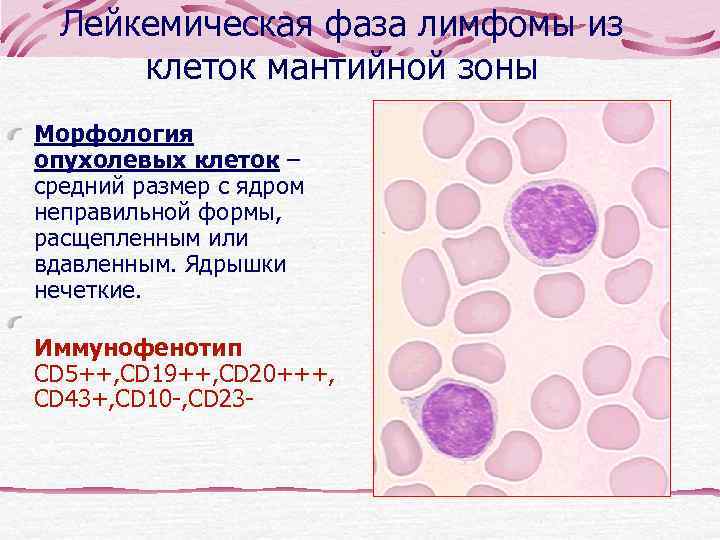
 Лейкемическая фаза лимфомы из клеток мантийной зоны Морфология опухолевых клеток – средний размер с ядром неправильной формы, расщепленным или вдавленным. Ядрышки нечеткие. Иммунофенотип CD 5++, CD 19++, CD 20+++, CD 43+, CD 10 -, CD 23 -
Лейкемическая фаза лимфомы из клеток мантийной зоны Морфология опухолевых клеток – средний размер с ядром неправильной формы, расщепленным или вдавленным. Ядрышки нечеткие. Иммунофенотип CD 5++, CD 19++, CD 20+++, CD 43+, CD 10 -, CD 23 -
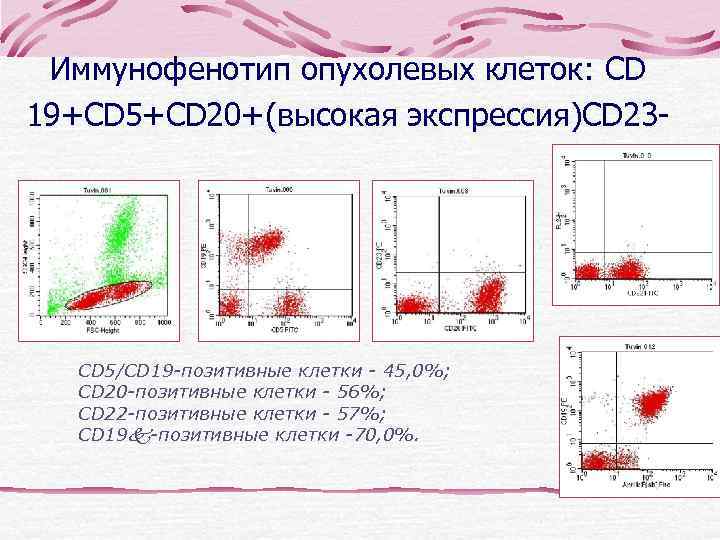
 Иммунофенотип опухолевых клеток: CD 19+CD 5+CD 20+(высокая экспрессия)CD 23 - CD 5/CD 19 -позитивные клетки - 45, 0%; CD 20 -позитивные клетки - 56%; CD 22 -позитивные клетки - 57%; CD 19 -позитивные клетки -70, 0%.
Иммунофенотип опухолевых клеток: CD 19+CD 5+CD 20+(высокая экспрессия)CD 23 - CD 5/CD 19 -позитивные клетки - 45, 0%; CD 20 -позитивные клетки - 56%; CD 22 -позитивные клетки - 57%; CD 19 -позитивные клетки -70, 0%.
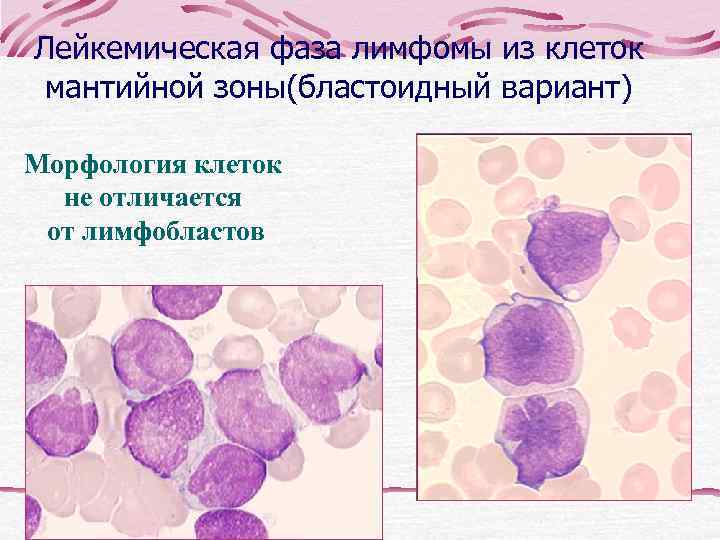
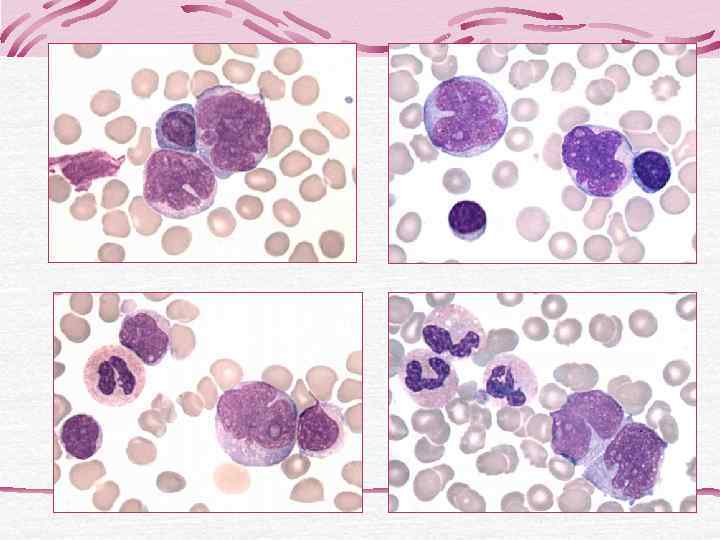
 Лейкемическая фаза лимфомы из клеток мантийной зоны(бластоидный вариант) Морфология клеток не отличается от лимфобластов
Лейкемическая фаза лимфомы из клеток мантийной зоны(бластоидный вариант) Морфология клеток не отличается от лимфобластов
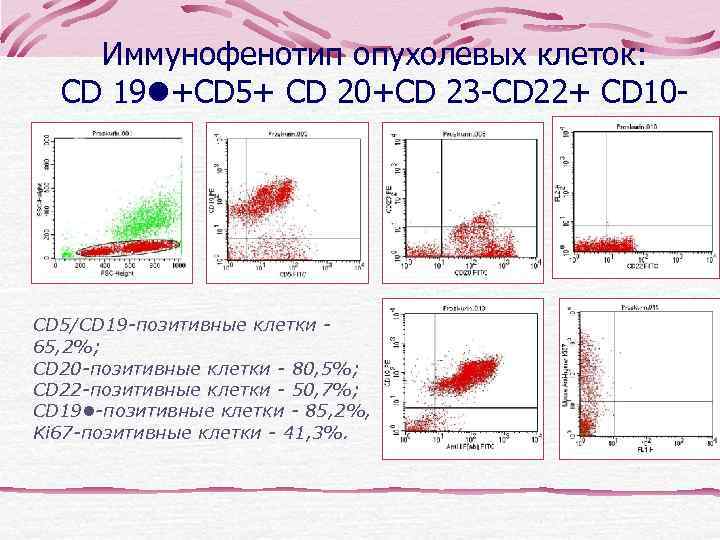
 Иммунофенотип опухолевых клеток: CD 19 +CD 5+ CD 20+CD 23 -CD 22+ CD 10 - CD 5/CD 19 -позитивные клетки - 65, 2%; CD 20 -позитивные клетки - 80, 5%; CD 22 -позитивные клетки - 50, 7%; CD 19 -позитивные клетки - 85, 2%, Ki 67 -позитивные клетки - 41, 3%.
Иммунофенотип опухолевых клеток: CD 19 +CD 5+ CD 20+CD 23 -CD 22+ CD 10 - CD 5/CD 19 -позитивные клетки - 65, 2%; CD 20 -позитивные клетки - 80, 5%; CD 22 -позитивные клетки - 50, 7%; CD 19 -позитивные клетки - 85, 2%, Ki 67 -позитивные клетки - 41, 3%.
 Лимфомы маргинальной зоны Экстранодальная Нодальная лимфома MALT-типа Лимфома селезенки Опухолевый субстрат – моноцитоидные В-клетки
Лимфомы маргинальной зоны Экстранодальная Нодальная лимфома MALT-типа Лимфома селезенки Опухолевый субстрат – моноцитоидные В-клетки
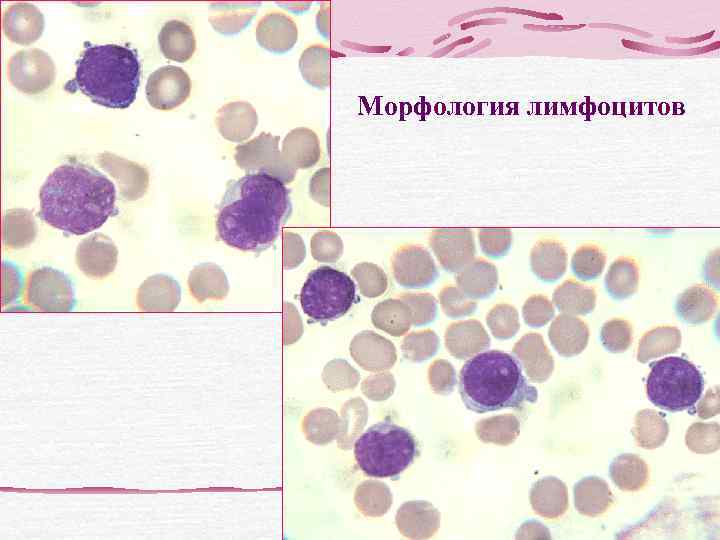
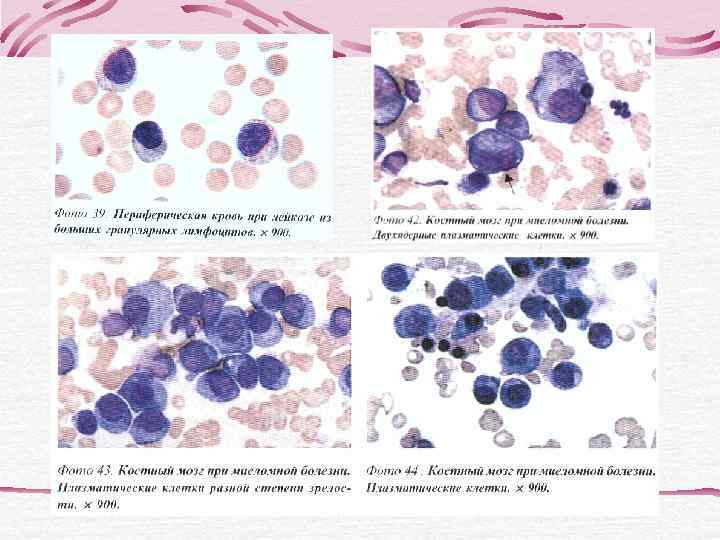
 Морфология лимфоцитов
Морфология лимфоцитов
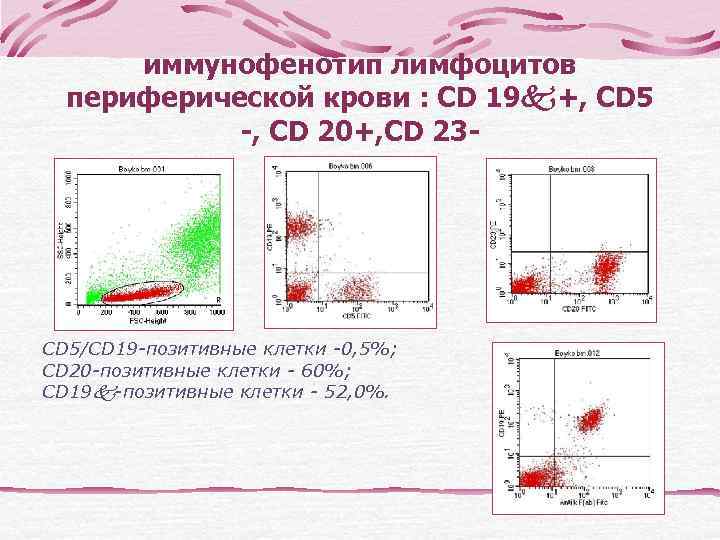
 иммунофенотип лимфоцитов периферической крови : CD 19 +, CD 5 -, CD 20+, CD 23 - CD 5/CD 19 -позитивные клетки -0, 5%; CD 20 -позитивные клетки - 60%; CD 19 -позитивные клетки - 52, 0%.
иммунофенотип лимфоцитов периферической крови : CD 19 +, CD 5 -, CD 20+, CD 23 - CD 5/CD 19 -позитивные клетки -0, 5%; CD 20 -позитивные клетки - 60%; CD 19 -позитивные клетки - 52, 0%.
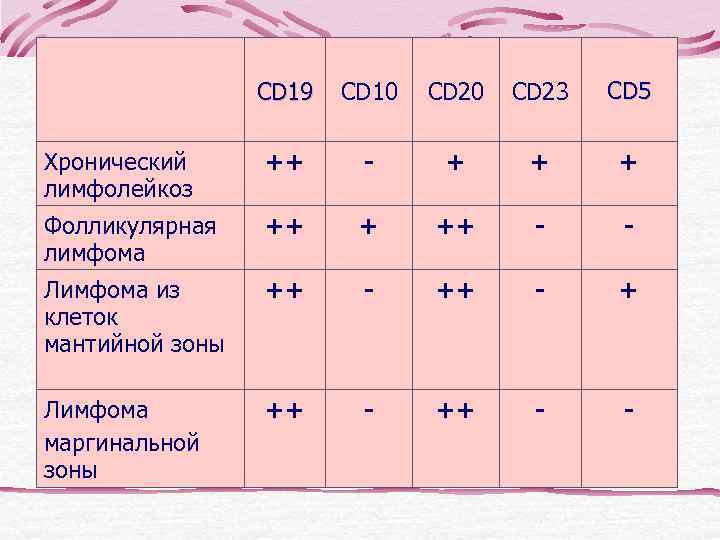
 CD 19 CD 10 CD 23 CD 5 Хронический ++ - + + + лимфолейкоз Фолликулярная ++ + ++ - - лимфома Лимфома из ++ - + клеток мантийной зоны Лимфома ++ - - маргинальной зоны
CD 19 CD 10 CD 23 CD 5 Хронический ++ - + + + лимфолейкоз Фолликулярная ++ + ++ - - лимфома Лимфома из ++ - + клеток мантийной зоны Лимфома ++ - - маргинальной зоны
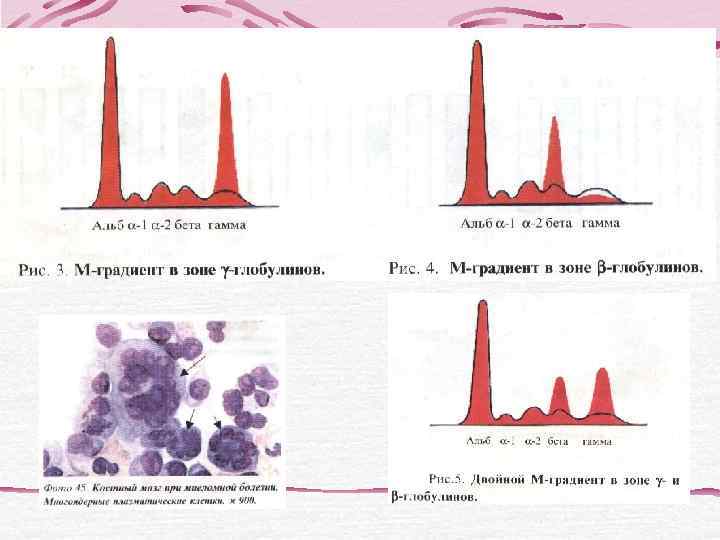
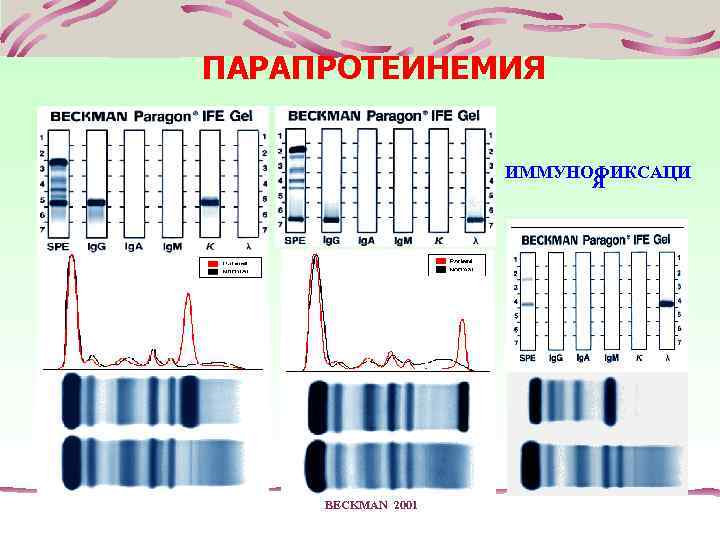
 ПАРАПРОТЕИНЕМИЯ ИММУНОФИКСАЦИ Я BECKMAN 2001
ПАРАПРОТЕИНЕМИЯ ИММУНОФИКСАЦИ Я BECKMAN 2001
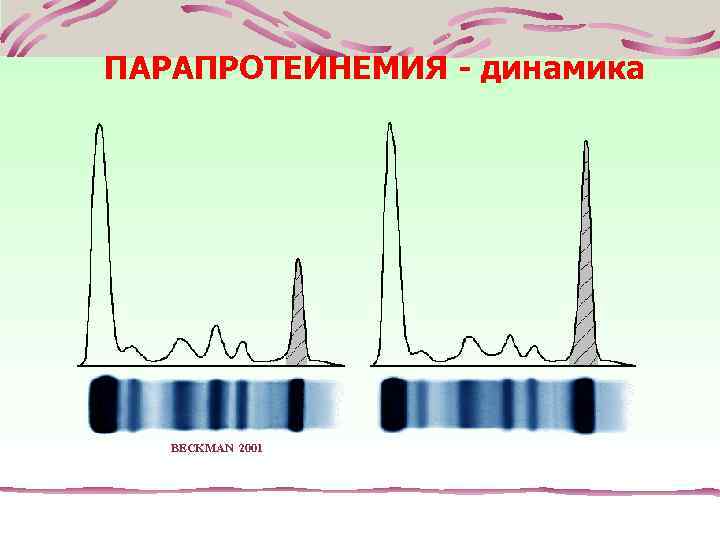
 ПАРАПРОТЕИНЕМИЯ - динамика BECKMAN 2001
ПАРАПРОТЕИНЕМИЯ - динамика BECKMAN 2001
 БЛАГОДАРЮ ЗА ВНИМАНИЕ!Благодарю за внимание!
БЛАГОДАРЮ ЗА ВНИМАНИЕ!Благодарю за внимание!



























