3b949ee78c72172e750c073fd6047aa2.ppt
- Количество слайдов: 55

Isomerie • Identiek ! ©BEN
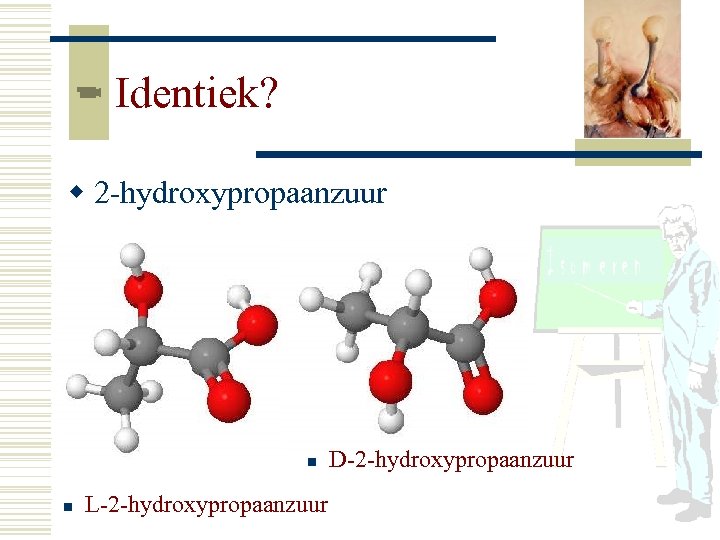
Identiek? w 2 -hydroxypropaanzuur n n L-2 -hydroxypropaanzuur D-2 -hydroxypropaanzuur
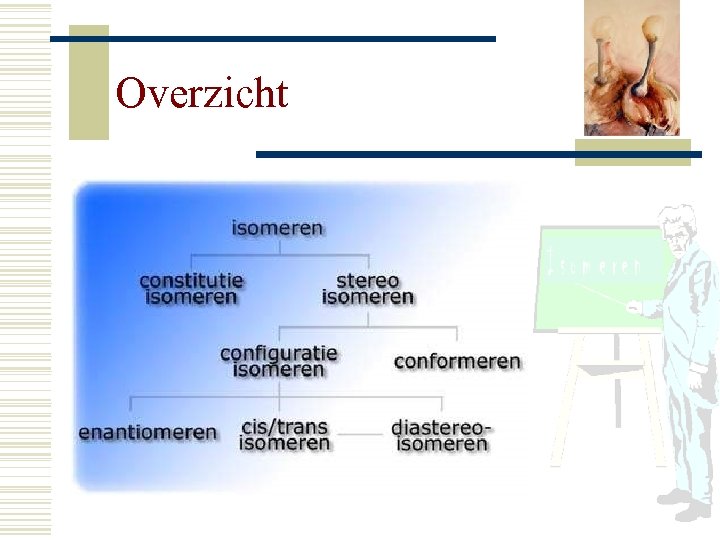
Overzicht
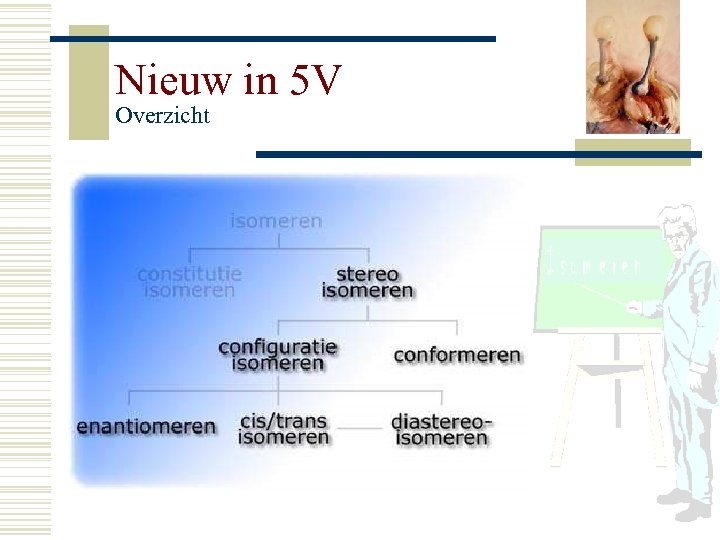
Nieuw in 5 V Overzicht

Isomeren Algemeen w Definitie n Isomeren zijn moleculen met dezelfde molecuulformule (brutoformule) maar een andere bouw. n C 2 H 6 O
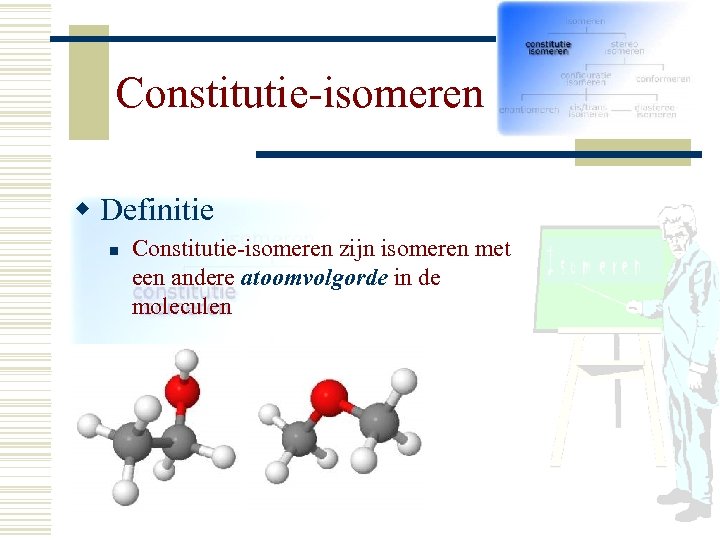
Constitutie-isomeren w Definitie n Constitutie-isomeren zijn isomeren met een andere atoomvolgorde in de moleculen
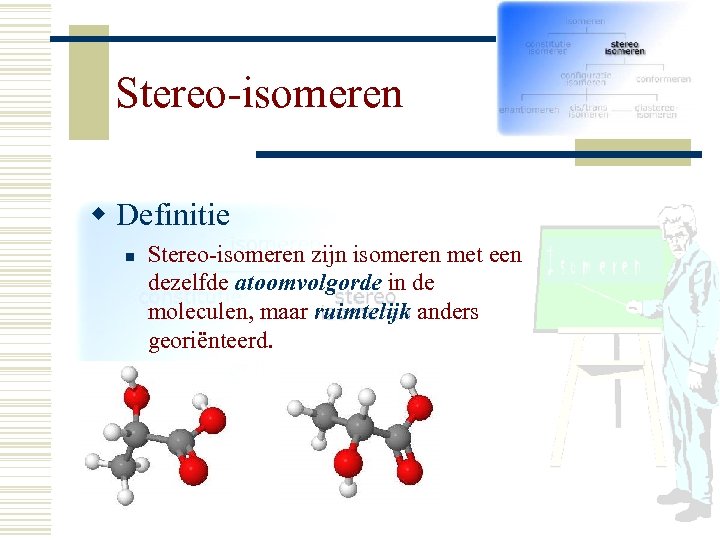
Stereo-isomeren ww Definitie Constitutie-isomeren zijn isomeren met Stereo-isomeren zijn isomeren met een andereatoomvolgorde in de dezelfde atoomvolgorde in de moleculen maar ruimtelijk anders moleculen, georiënteerd. n n
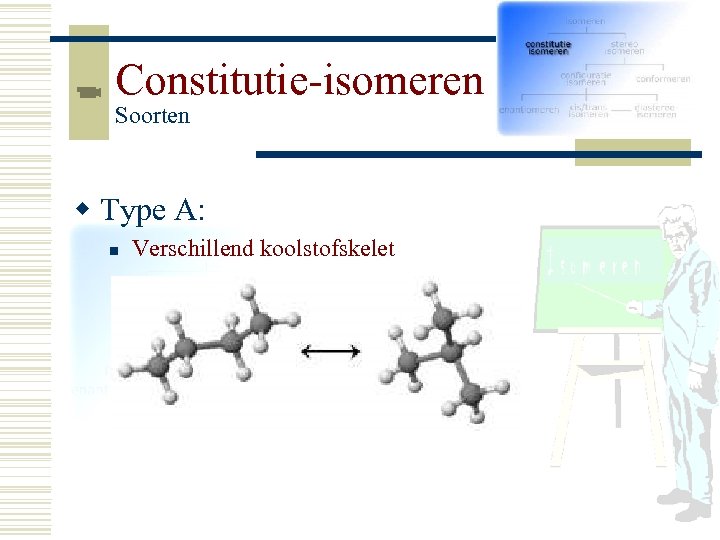
Constitutie-isomeren Soorten w Type A: n Verschillend koolstofskelet
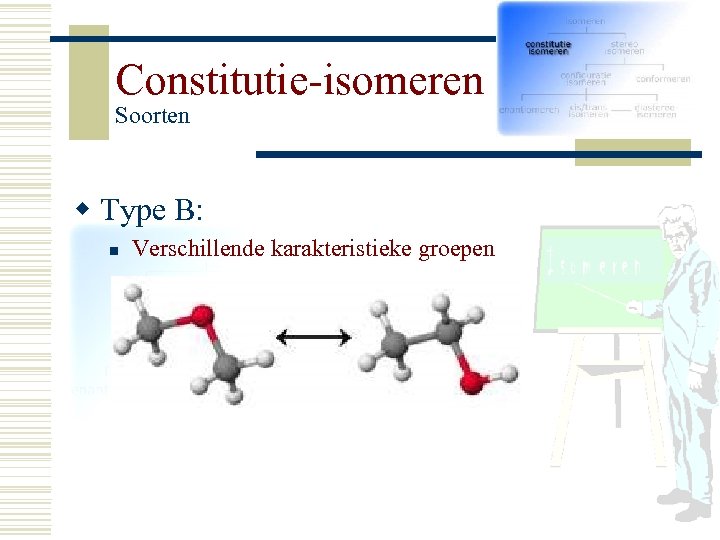
Constitutie-isomeren Soorten w Type B: n Verschillende karakteristieke groepen
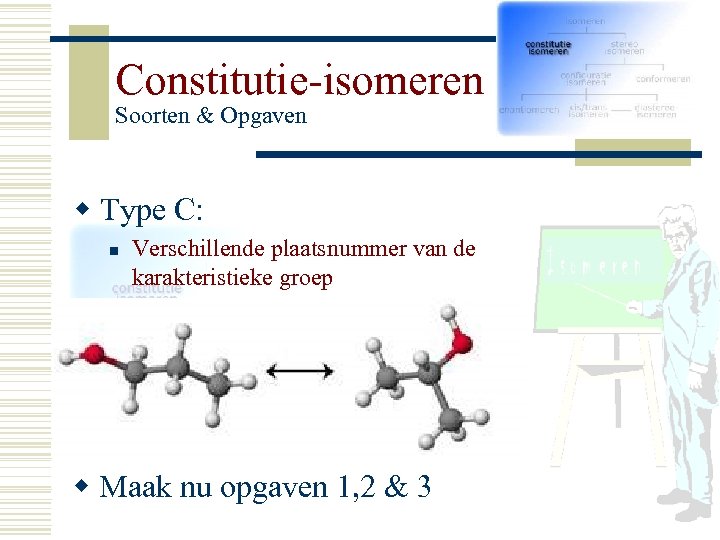
Constitutie-isomeren Soorten & Opgaven w Type C: n Verschillende plaatsnummer van de karakteristieke groep w Maak nu opgaven 1, 2 & 3
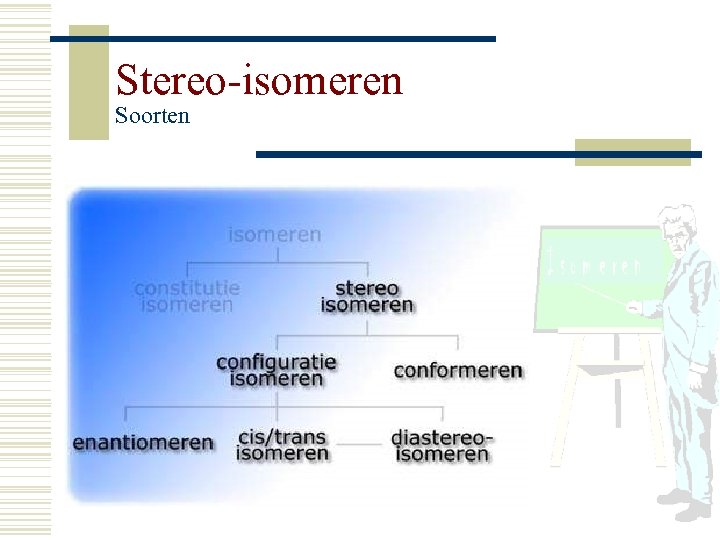
Stereo-isomeren Soorten

Conformeren w Definitie n n Conformeren zijn dezelfde moleculen in een andere lichaamshouding Conformeren zijn eigenlijk geen isomeren. l Conformeren gaan in elkaar over door draaiing over een enkele binding
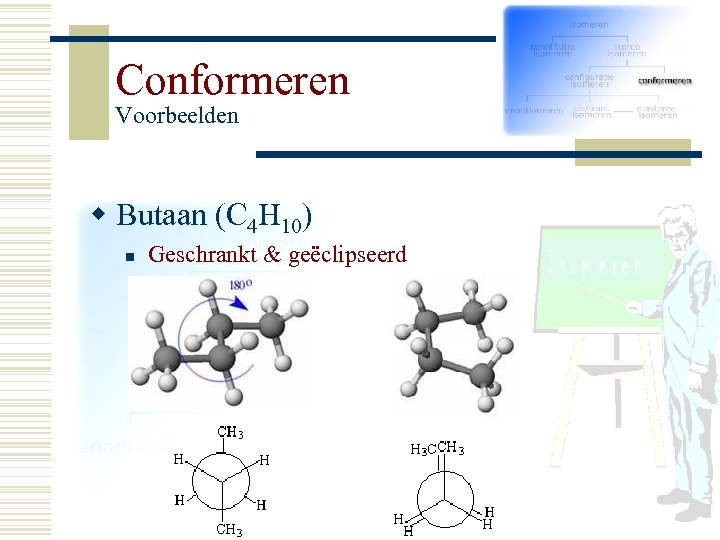
Conformeren Voorbeelden w Butaan (C 4 H 10) n Geschrankt & geëclipseerd
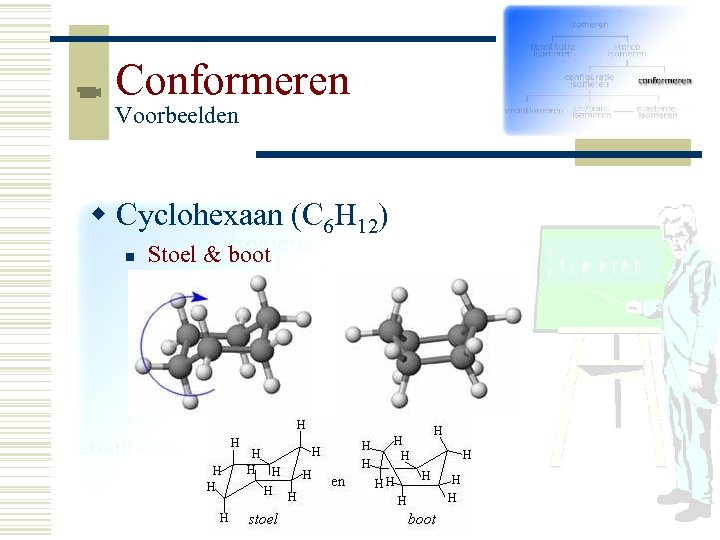
Conformeren Voorbeelden w Cyclohexaan (C 6 H 12) n Stoel & boot

Configuratie-isomeren w Definitie: n Bij configuratie-isomeren zijn verschillen niet op te heffen door draaiing rond enkelvoudige bindingen w Drie soorten: n n n Cis-trans isomeren Enantiomeren Diastereo-isomeren

Cis-trans-isomeren w Kenmerken: n Cis-trans isomeren hebben een starre binding l l n C=C Ring Aan elk atoom van de starre binding zitten twee verschillende atoomgroepen.

Cis-trans-isomeren Opgaven w Maak opgave 5 & 6 w Ga van onderstaande stoffen na of er sprake is van cis/trans-isomerie n n n 3 -hexeen 3 -ethyl-3 -hepteen 1 -chloor-3 -methylcyclobutaan.
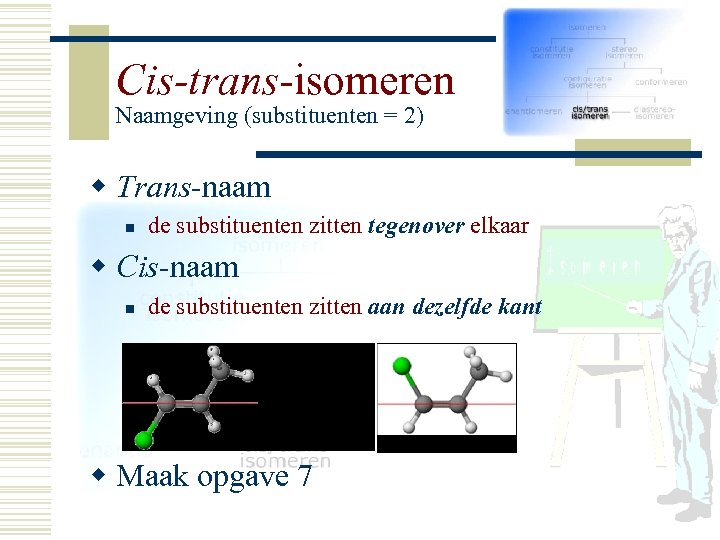
Cis-trans-isomeren Naamgeving (substituenten = 2) w Trans-naam n de substituenten zitten tegenover elkaar w Cis-naam n de substituenten zitten aan dezelfde kant w Maak opgave 7

Cis-trans-isomeren Naamgeving (substituenten > 2) w Regel 1: l l l Neem de twee koolstofatomen van de dubbele binding centraal. Kijk naar de groepen of atomen die gebonden zijn aan het linker koolstofatoom van de dubbele binding. Stel de prioriteit van ieder atoom vast, waarbij het atoom met hoogste atoomnummer de hoogste prioriteit krijgt. Kijk naar de groepen of atomen die gebonden zijn aan het rechter koolstofatoom van de dubbele binding. Stel de prioriteit van ieder atoom vast, waarbij het atoom met hoogste atoomnummer de hoogste prioriteit krijgt.
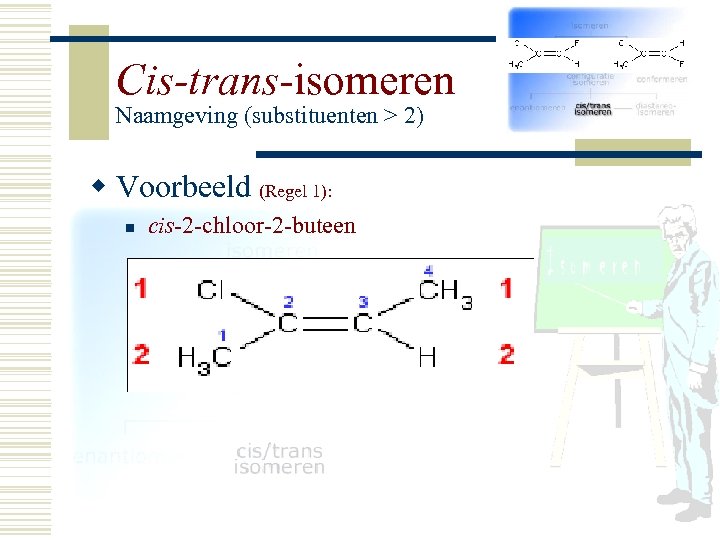
Cis-trans-isomeren Naamgeving (substituenten > 2) w Voorbeeld (Regel 1): n cis-2 -chloor-2 -buteen

Cis-trans-isomeren Naamgeving (substituenten > 2) w Regel 2: l l l Als regel 1 geen uitsluitsel biedt. Er wordt nu gekeken naar de prioriteit van de daaraan gebonden atomen. Ook daarvoor geldt dat het hoogste atoomnummer een hogere prioriteit geeft. w Voorbeeld: n trans-3 -methyl-2 -penteen
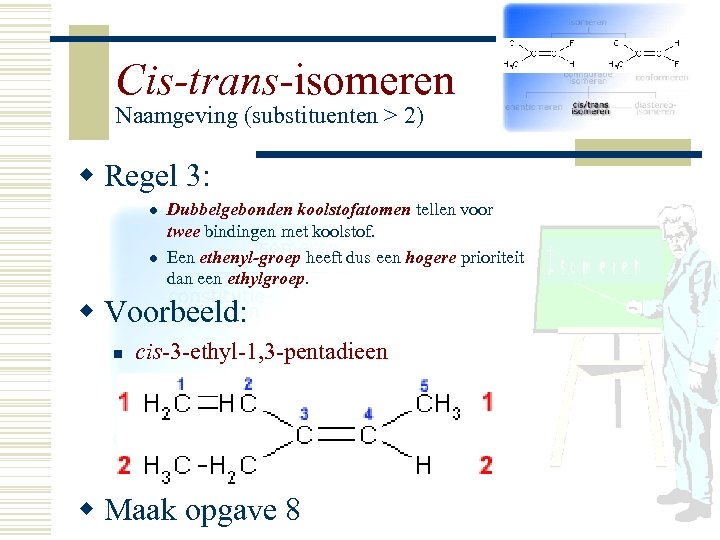
Cis-trans-isomeren Naamgeving (substituenten > 2) w Regel 3: l l Dubbelgebonden koolstofatomen tellen voor twee bindingen met koolstof. Een ethenyl-groep heeft dus een hogere prioriteit dan een ethylgroep. w Voorbeeld: n cis-3 -ethyl-1, 3 -pentadieen w Maak opgave 8
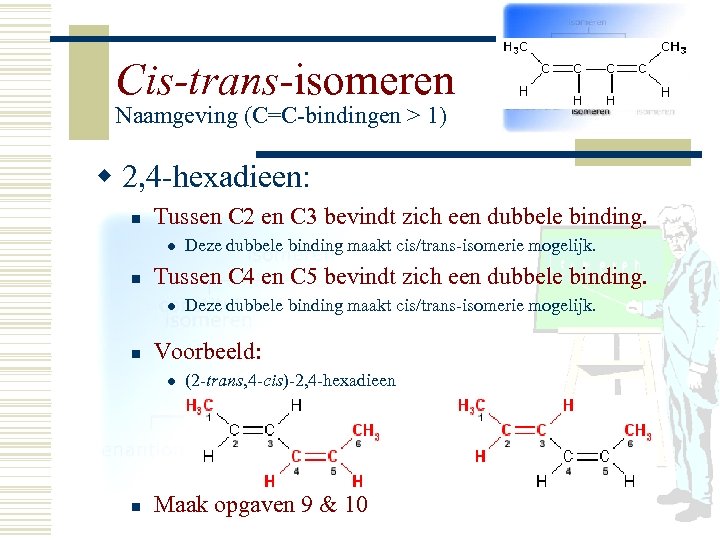
Cis-trans-isomeren Naamgeving (C=C-bindingen > 1) w 2, 4 -hexadieen: n Tussen C 2 en C 3 bevindt zich een dubbele binding. l n Tussen C 4 en C 5 bevindt zich een dubbele binding. l n Deze dubbele binding maakt cis/trans-isomerie mogelijk. Voorbeeld: l n Deze dubbele binding maakt cis/trans-isomerie mogelijk. (2 -trans, 4 -cis)-2, 4 -hexadieen Maak opgaven 9 & 10

Enantiomeren w Definitie n n Enantiomeren zijn moleculen die elkaars spiegelbeeld zijn maar die niet met elkaar tot dekking gebracht kunnen worden. Enantiomeren worden daarom ook wel spiegelbeeld-isomeren genoemd.
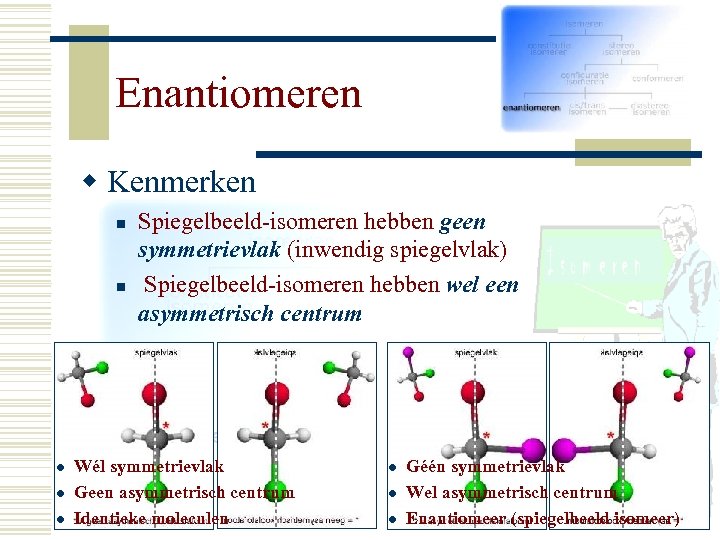
Enantiomeren w Kenmerken n n l l l Spiegelbeeld-isomeren hebben geen symmetrievlak (inwendig spiegelvlak) Spiegelbeeld-isomeren hebben wel een asymmetrisch centrum Wél symmetrievlak Geen asymmetrisch centrum Identieke moleculen l l l Géén symmetrievlak Wel asymmetrisch centrum Enantiomeer (spiegelbeeld isomeer)

Enantiomeren Het asymmetrisch C-atoom w Kenmerken n n Het asymmetrische centrum is tetraëdisch (AX 4 of AX 3 E). Het asymmetrische centrum heeft vier verschillende atoomgroepen gebonden.

Enantiomeren Het asymmetrisch C-atoom zoeken w Werkwijze l Bekijk alleen atomen met een tetraëdische omringing. l Teken of draai een molecuul zo dat je alle groepen, die aan het te onderzoeken koolstofatoom verbonden zijn, duidelijk kunt zien. Bepaal in gedachte, of door cirkels te zetten, welke groepen er aan het te onderzoeken koolstofatoom gebonden zijn: l w groep 1: w groep 2: w groep 3: w groep 4: l n -COOH (carbonzuur) -H (waterstofatoom) -Cl (chlooratoom) -H (waterstofatoom) Zijn de vier gebonden groepen vier verschillende groepen dan is het onderzochte koolstofatoom een asymmetrisch koolstofatoom. In dit voorbeeld is het betreffende koolstofatoom dus geen asymmetrisch atoom.

Enantiomeren Opgaven & modellenpracticum w Doen ! n n n Maak opgaven 11 t/m 14 Voer experiment 9. 1 (deel 1 t/m 5) uit § 9. 3 uit en maak het bijbehorende meetrapport in je Werkboek. Internetopdracht ‘Molecuulbouwer’: Het asymmetrisch koolstofatoom Internetopdracht ‘Molecuulbouwer’: Enantiomeren Internetopdracht ‘Molecuulbouwer’: Constitutie-isomeren & Enantiomeren
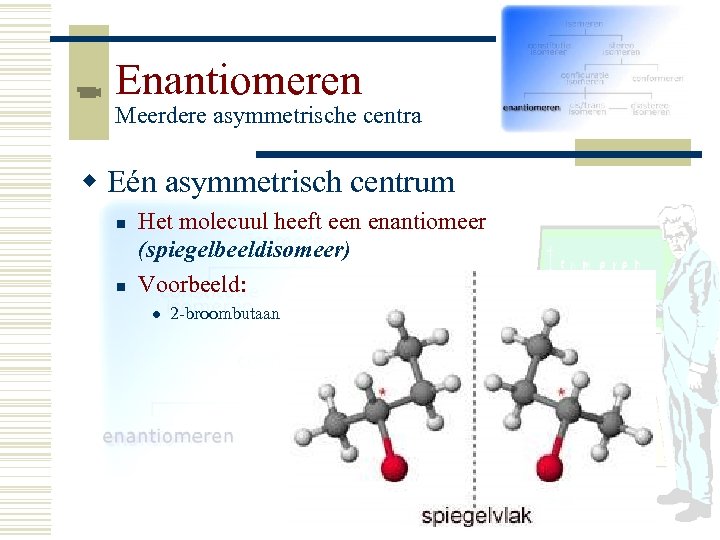
Enantiomeren Meerdere asymmetrische centra w Eén asymmetrisch centrum n n Het molecuul heeft een enantiomeer (spiegelbeeldisomeer) Voorbeeld: l 2 -broombutaan
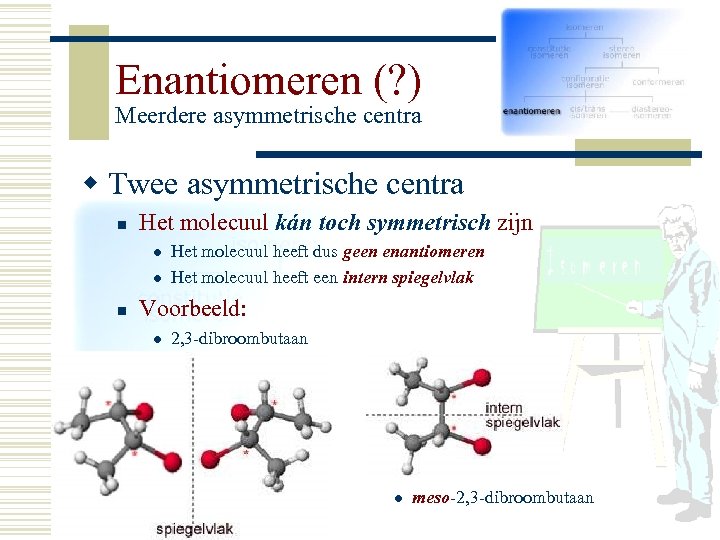
Enantiomeren (? ) Meerdere asymmetrische centra w Twee asymmetrische centra n Het molecuul kán toch symmetrisch zijn l l n Het molecuul heeft dus geen enantiomeren Het molecuul heeft een intern spiegelvlak Voorbeeld: l 2, 3 -dibroombutaan l meso-2, 3 -dibroombutaan
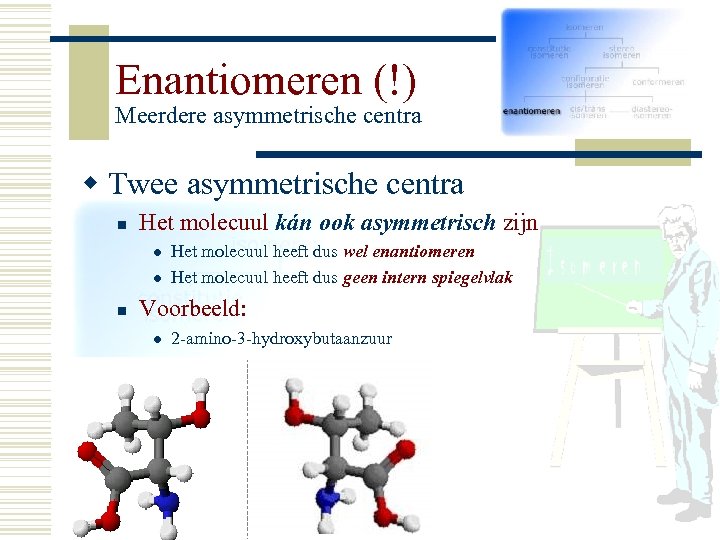
Enantiomeren (!) Meerdere asymmetrische centra w Twee asymmetrische centra n Het molecuul kán ook asymmetrisch zijn l l n Het molecuul heeft dus wel enantiomeren Het molecuul heeft dus geen intern spiegelvlak Voorbeeld: l 2 -amino-3 -hydroxybutaanzuur
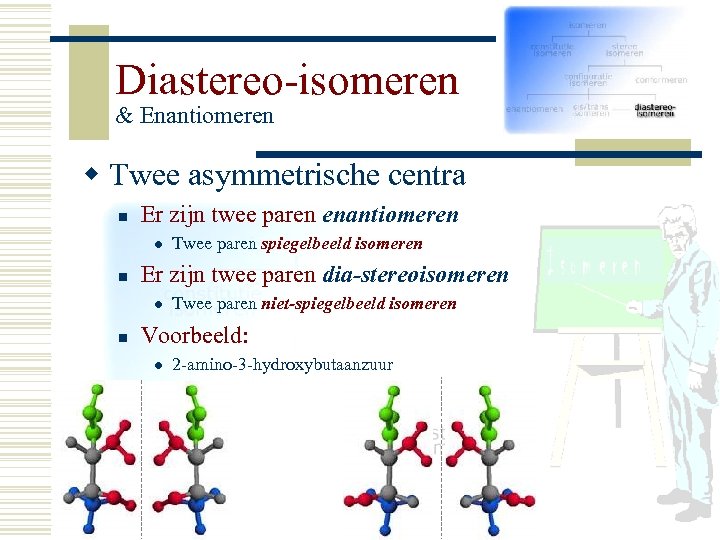
Diastereo-isomeren & Enantiomeren w Twee asymmetrische centra n Er zijn twee paren enantiomeren l n Er zijn twee paren dia-stereoisomeren l n Twee paren spiegelbeeld isomeren Twee paren niet-spiegelbeeld isomeren Voorbeeld: l 2 -amino-3 -hydroxybutaanzuur
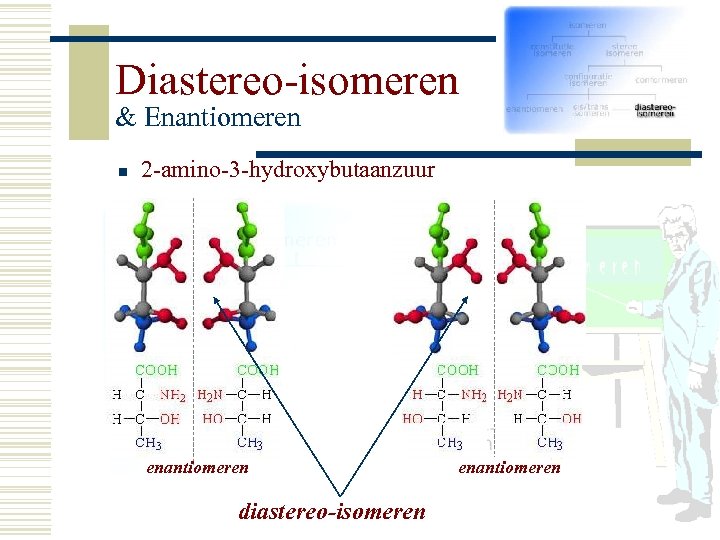
Diastereo-isomeren & Enantiomeren n 2 -amino-3 -hydroxybutaanzuur enantiomeren diastereo-isomeren enantiomeren

Enantiomeren & Diastereo-isomeren Opgaven & modellenpracticum w Doen ! n n n Maak opgaven 15 & 16 Voer experiment 9. 1 (deel 6 t/m 8) uit § 9. 3 uit en maak het bijbehorende meetrapport in je Werkboek. Internetopdracht ‘Molecuulbouwer’: Constitutie-isomeren, Enantiomeren & Diastereoisomeren
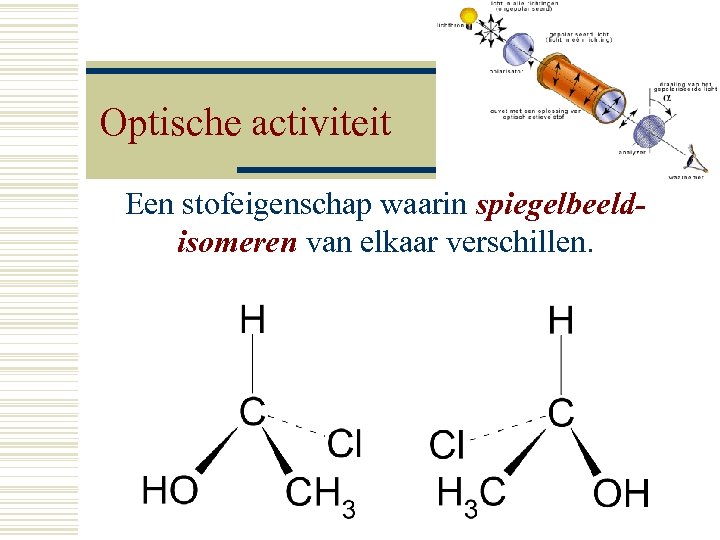
Optische activiteit Een stofeigenschap waarin spiegelbeeldisomeren van elkaar verschillen.
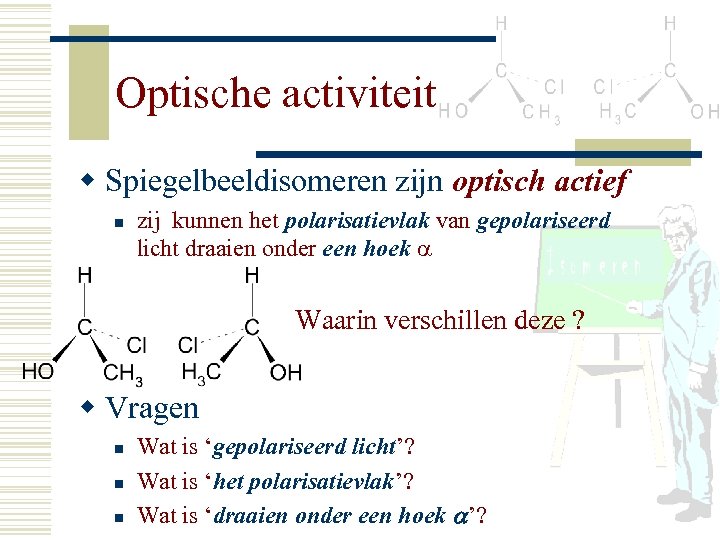
Optische activiteit w Spiegelbeeldisomeren zijn optisch actief n zij kunnen het polarisatievlak van gepolariseerd licht draaien onder een hoek Waarin verschillen deze ? w Vragen n Wat is ‘gepolariseerd licht’? Wat is ‘het polarisatievlak’? Wat is ‘draaien onder een hoek ’?
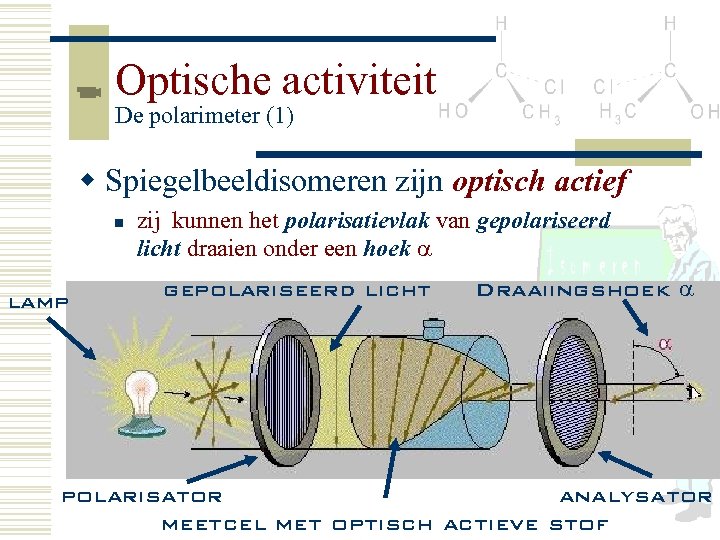
Optische activiteit De polarimeter (1) w Spiegelbeeldisomeren zijn optisch actief n lamp zij kunnen het polarisatievlak van gepolariseerd licht draaien onder een hoek gepolariseerd licht Draaiingshoek polarisator analysator meetcel met optisch actieve stof
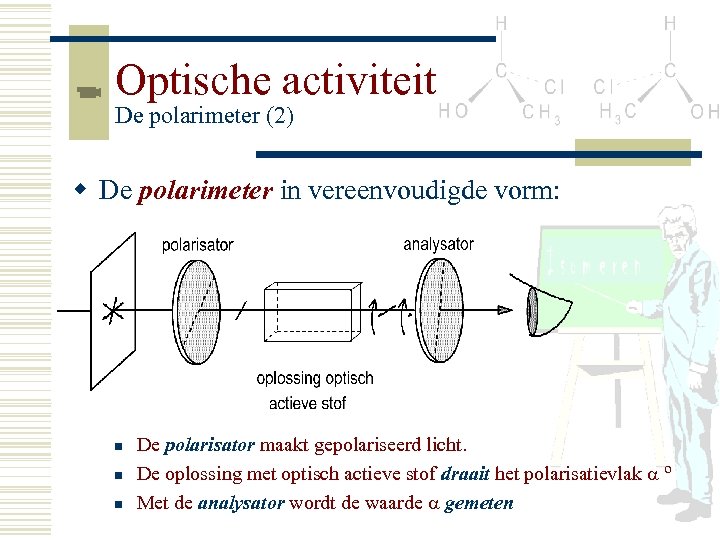
Optische activiteit De polarimeter (2) w De polarimeter in vereenvoudigde vorm: n n n De polarisator maakt gepolariseerd licht. De oplossing met optisch actieve stof draait het polarisatievlak º Met de analysator wordt de waarde gemeten

Optische activiteit Factoren die de waarde bepalen w De mate waarin het polarisatievlak gedraaid wordt, wordt de draaiingshoek genoemd. w De draaiingshoek wordt bepaald door: n n n de soort optisch actieve stof ( 0); voor suiker bedraagt deze 66, 5 º de concentratie (c) in g/m. L waarin de optisch actieve stof aanwezig is de afstand (l) in dm die het licht aflegt in de oplossing van de optisch actieve stof w In formule: = 0. c. l

Naamgeving Linksdraaiend & rechtsdraaiend w Naamgeving op basis van gedrag in de polarimeter: n Indien het gepolariseerde licht naar rechts (met de klok mee) wordt gedraaid: l l l n rechtsdraaiend teken: (-) voorbeeld: (-)-1 -chloor-1 -ethanol Indien het gepolariseerde licht naar links (tegen de klok in) wordt gedraaid: l linksdraaiend teken: (+) voorbeeld: (+)-1 -chloor-1 -ethanol
Naamgeving D & L-methode (1) w Naamgeving op basis van de structuur van de moleculen: n n gebaseerd op afspraken de oriëntatie van de atoomgroepen rond het asymmetrisch centrum is bepalend w Voorbeeld: n 2 -hydroxypropaanzuur (melkzuur)

Naamgeving D & L-methode (2) w 2 -hydroxypropaanzuur (melkzuur) n Melkzuur bevat aan het asymmetrische centrum de volgende substituenten: l l n n n H-atoom massa: 1, 0 u CH 3 -atoomgroep massa: 15, 0 u OH- atoomgroep massa: 17, 0 u COOH-atoomgroep massa: 45, 0 u Houd de lichtste substituent ‘in de hand’ Kijk langs de as van het asymmetrisch centrum en deze lichtste substituent Rangschik de andere substituenten naar toenemende massa: l l Linksom geöriënteerd: L-configuratie Rechtsom geöriënteerd: D-configuratie w Maak opgave 17 L-2 -hydroxypropaanzuur D-2 -hydroxypropaanzuur
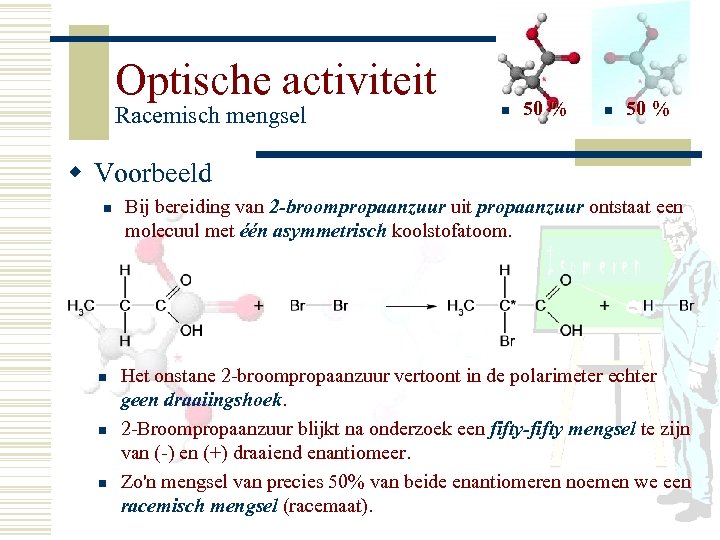
Optische activiteit Racemisch mengsel n 50 % w Voorbeeld n n Bij bereiding van 2 -broompropaanzuur uit propaanzuur ontstaat een molecuul met één asymmetrisch koolstofatoom. Het onstane 2 -broompropaanzuur vertoont in de polarimeter echter geen draaiingshoek. 2 -Broompropaanzuur blijkt na onderzoek een fifty-fifty mengsel te zijn van (-) en (+) draaiend enantiomeer. Zo'n mengsel van precies 50% van beide enantiomeren noemen we een racemisch mengsel (racemaat).

Optische activiteit Opgaven & modellenpracticum w Doen ! n n n Maak opgaven 18 & 19 Voer experiment ‘leermoment 8’ uit Internetopdracht ‘Zoetstoffen’ : l Bekijk de site over aspartaam als herhalingsopdracht
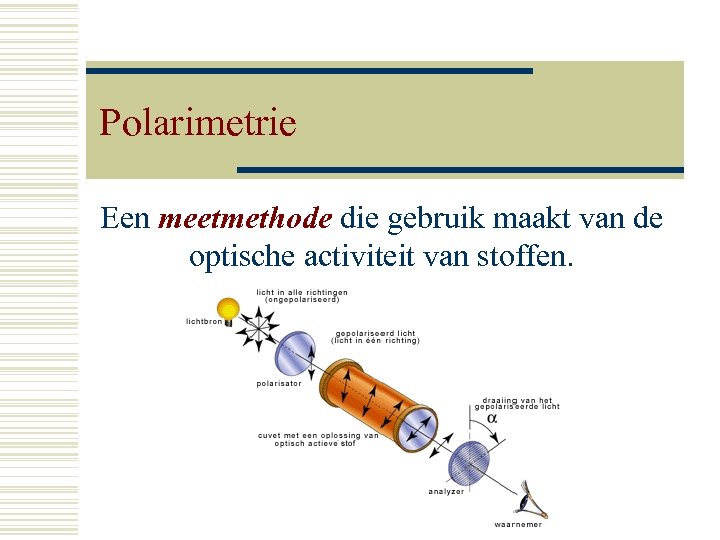
Polarimetrie Een meetmethode die gebruik maakt van de optische activiteit van stoffen.

Gehaltebepalingen van optisch actieve stoffen. w De meetmethode die gebruik maakt van de optische activiteit van stoffen wordt ‘polarimetrie’ genoemd. n n Meet de draaiiingshoek van een oplossing met een optisch actieve stof. Vergelijk deze met de draaiingshoeken van een ijkserie. w Voorbeeld: n Het suikergehalte van 7 -Up
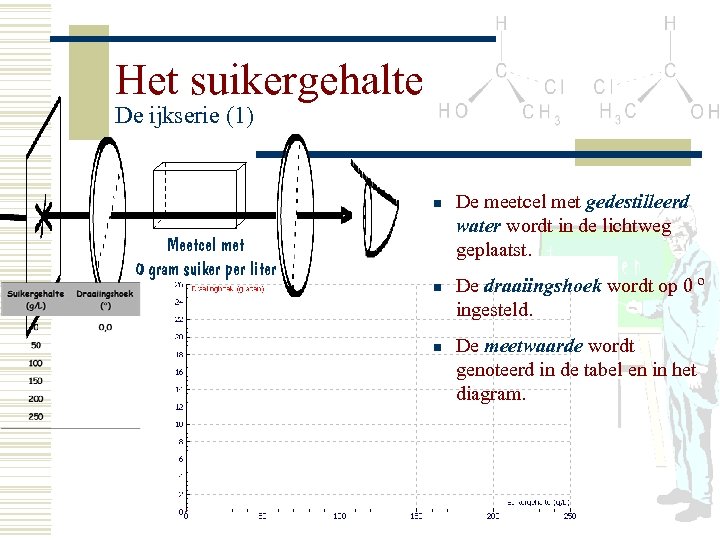
Het suikergehalte De ijkserie (1) n Meetcel met 0 gram suiker per liter n n De meetcel met gedestilleerd water wordt in de lichtweg geplaatst. De draaiingshoek wordt op 0 º ingesteld. De meetwaarde wordt genoteerd in de tabel en in het diagram.
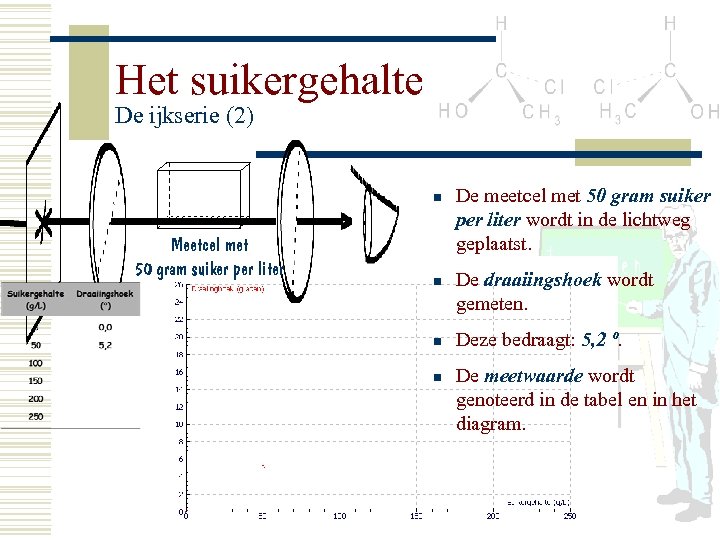
Het suikergehalte De ijkserie (2) n Meetcel met 50 gram suiker per liter n n n De meetcel met 50 gram suiker per liter wordt in de lichtweg geplaatst. De draaiingshoek wordt gemeten. Deze bedraagt: 5, 2 º. De meetwaarde wordt genoteerd in de tabel en in het diagram.
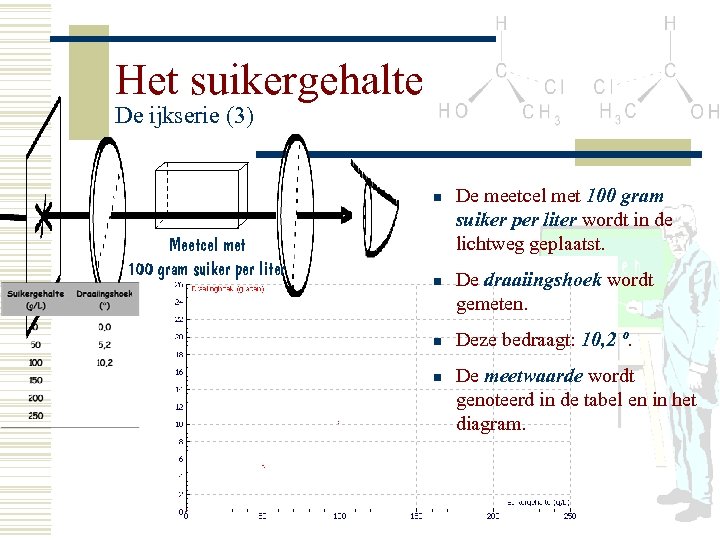
Het suikergehalte De ijkserie (3) n Meetcel met 100 gram suiker per liter n n n De meetcel met 100 gram suiker per liter wordt in de lichtweg geplaatst. De draaiingshoek wordt gemeten. Deze bedraagt: 10, 2 º. De meetwaarde wordt genoteerd in de tabel en in het diagram.
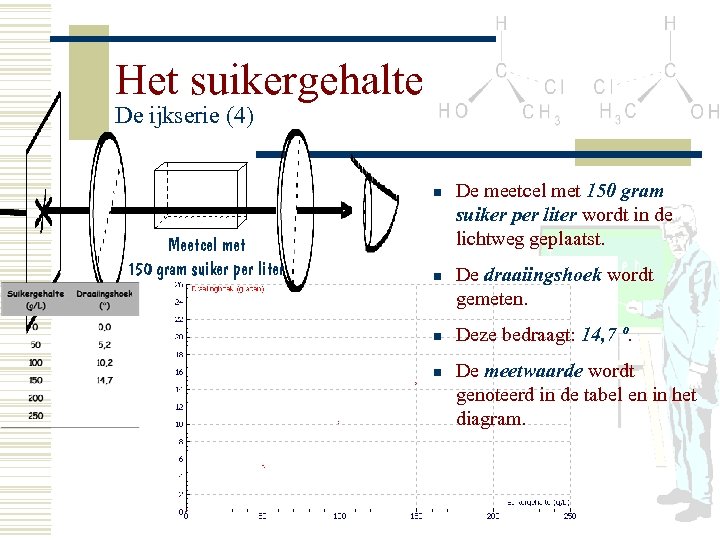
Het suikergehalte De ijkserie (4) n Meetcel met 150 gram suiker per liter n n n De meetcel met 150 gram suiker per liter wordt in de lichtweg geplaatst. De draaiingshoek wordt gemeten. Deze bedraagt: 14, 7 º. De meetwaarde wordt genoteerd in de tabel en in het diagram.
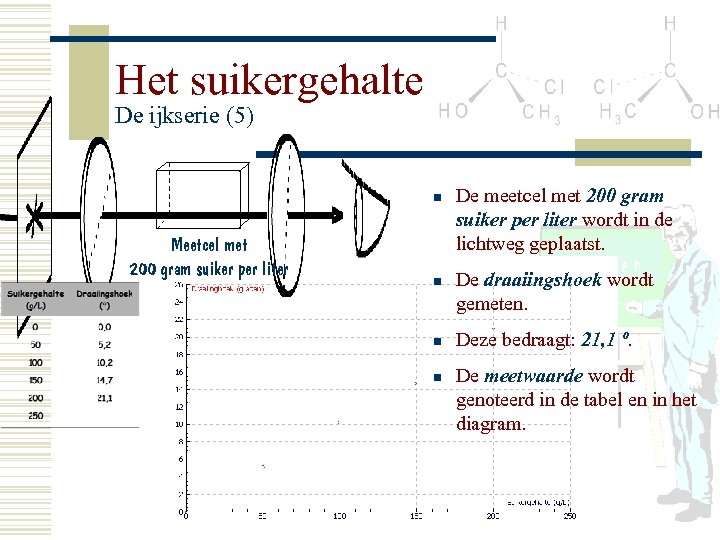
Het suikergehalte De ijkserie (5) n Meetcel met 200 gram suiker per liter n n n De meetcel met 200 gram suiker per liter wordt in de lichtweg geplaatst. De draaiingshoek wordt gemeten. Deze bedraagt: 21, 1 º. De meetwaarde wordt genoteerd in de tabel en in het diagram.
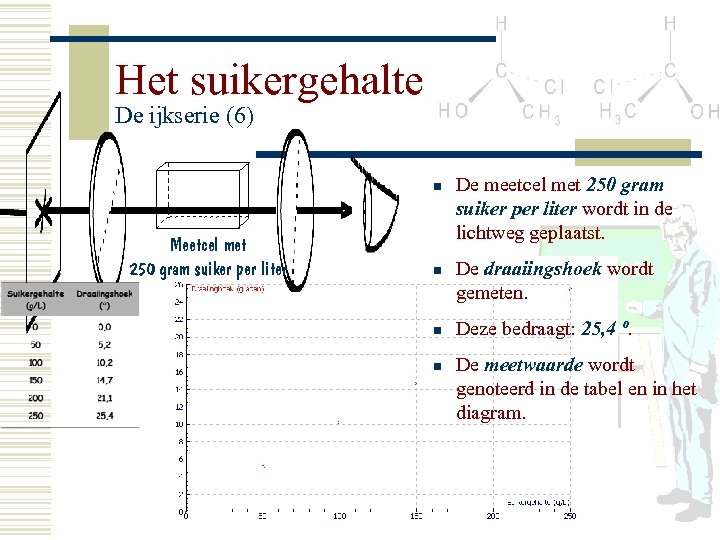
Het suikergehalte De ijkserie (6) n Meetcel met 250 gram suiker per liter n n n De meetcel met 250 gram suiker per liter wordt in de lichtweg geplaatst. De draaiingshoek wordt gemeten. Deze bedraagt: 25, 4 º. De meetwaarde wordt genoteerd in de tabel en in het diagram.
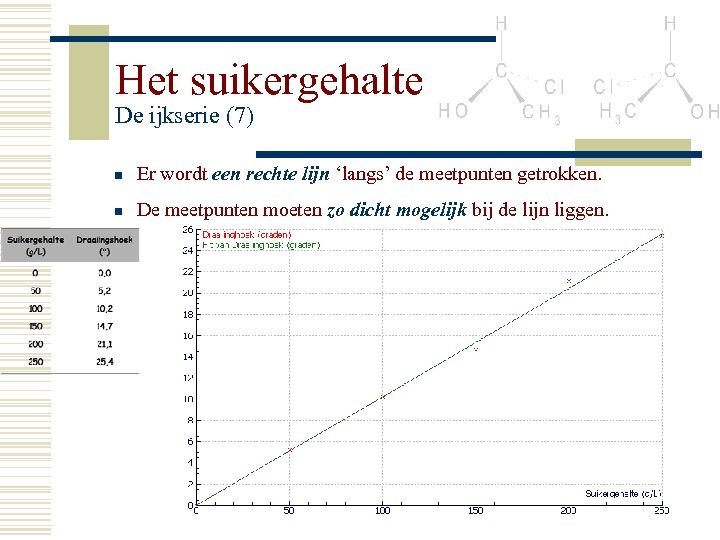
Het suikergehalte De ijkserie (7) n Er wordt een rechte lijn ‘langs’ de meetpunten getrokken. n De meetpunten moeten zo dicht mogelijk bij de lijn liggen.
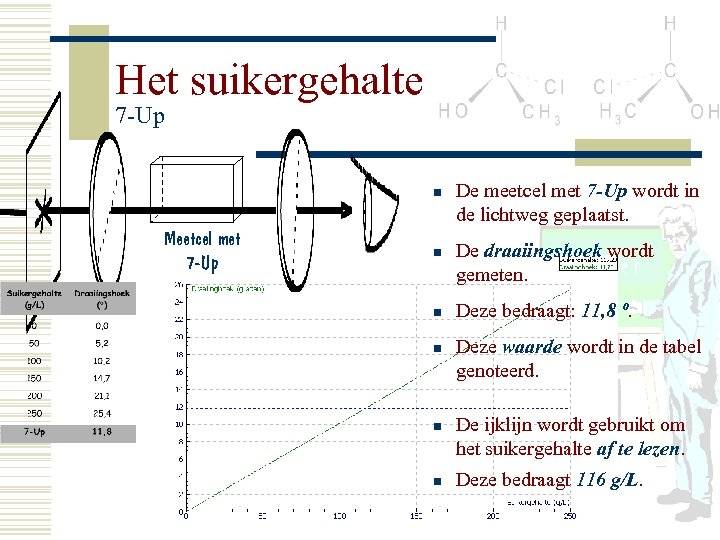
Het suikergehalte 7 -Up n Meetcel met 7 -Up n n n De meetcel met 7 -Up wordt in de lichtweg geplaatst. De draaiingshoek wordt gemeten. Deze bedraagt: 11, 8 º. Deze waarde wordt in de tabel genoteerd. De ijklijn wordt gebruikt om het suikergehalte af te lezen. Deze bedraagt 116 g/L.
Einde
3b949ee78c72172e750c073fd6047aa2.ppt