Антигены_МАПО_фин.ppt
- Количество слайдов: 58

ИСКУССТВЕННЫЕ И ЕСТЕСТВЕННЫЕ АНТИГЕНЫ. АНТИГЕННАЯ СПЕЦИФИЧНОСТЬ, ЕЁ БИОЛОГИЧЕСКИЙ СМЫСЛ. проф. Виктор Константинович КОЗЛОВ Профессор кафедр: клинической лабораторной диагностики СЗГМУ им. И. И. Мечникова; микробиологии, иммунологии и инфекционных болезней Новгородского государственного университета им. Ярослава Мудрого; челюстно-лицевой хирургии и хирургической стоматологии Санкт-Петербургского государственного университета.

Антигены – молекулы и надмолекулярные образования (макромолекулярные комплексы, микроорганизмы), индуцирующие комплекс реакций иммунной системы.

Качества антигенов • Чужеродность; • Иммуногенность; • Специфичность.

Чужеродность Определяющее ( «Антигены – это биологические тела и молекулы, в составе и структуре которых зафиксирована чужеродная генетическая информация» ), но не абсолютное качество антигенов (высокая частота встречаемости антител с аутоспецифичностью без явных признаков аутоагрессии).

Наиболее частые варианты имеющей регуляторное значение аутоспецифичности • обычно манифестируется наличием небольших количеств полиспецифичных сывороточных антител или CD 5+ В-лимфоцитов; • специфичность направлена к широко распространенным белкам: альбумину, Ig. G, коллагену, тиреоглобулину, миелину; • возможна специфичность к ДНК и компонентам цитоскелета соматических клеток; • Антитела к идиотипам иммуноглобулинов – другая широко распространенная разновидность аутоспецифичности.

Иммуногенность Способность антигена индуцировать всю совокупность реакций иммунного реагирования (способность задействовать в реализацию иммунореактивности максимально широкий по составу клеточный ансамбль). Иммуногенность определяется: • Молекулярно-химическими особенностями структуры; • Дозой и путем введения антигенов; • Генетическими особенностями отвечающего на антиген биообъекта.

Структурно-химические условия проявления иммуногенности • Достаточная молекулярная масса (появление α-спирали вторичной структуры полипептидов или «складчатости» полисахаридов, увеличение валентности макромолекулы); • Структурное разнообразие детерминант иммунохимической специфичности; • Ограниченная конформационная подвижность и жесткость конформационной структуры; • «Встроенная адъювантность» ; • Построение молекулярных блоков структуры из химических соединений, свойственных живым объектам (L-аминокислоты).

Генетические аспекты иммуногенности • Наличие генетически обусловленной способности к «сильному или слабому иммунному ответу» ; • Взаимосвязь генов иммунного ответа (Ir-гены) с генами, кодирующими продукты главного комплекса гистосовместимости; • Иммуногенность антигена в большей степени может определяться особенностями биологической организации иммунизируемой особи.

Антигенная специфичность • Носителями антигенной специфичности являются части структуры антигена – детерминанты иммунохимической специфичности (эпитопы); • Прослеживается конформационное соответствие между структурой детерминанты и специфичными к ней элементами иммунореактивности (антитела, антиген-распознающие рецепторы клеток); • При этом обеспечивается как возможность иммунного распознавания, так и последующая наработка специфичных иммунных продуктов и клеток.
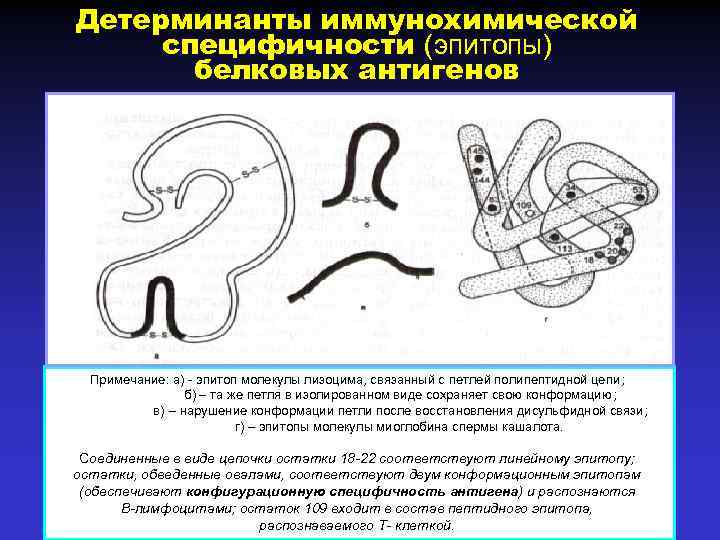
Детерминанты иммунохимической специфичности (эпитопы) белковых антигенов Примечание: а) - эпитоп молекулы лизоцима, связанный с петлей полипептидной цепи; б) – та же петля в изолированном виде сохраняет свою конформацию; в) – нарушение конформации петли после восстановления дисульфидной связи; г) – эпитопы молекулы миоглобина спермы кашалота. Соединенные в виде цепочки остатки 18 -22 соответствуют линейному эпитопу; остатки, обведенные овалами, соответствуют двум конформационным эпитопам (обеспечивают конфигурационную специфичность антигена) и распознаются В-лимфоцитами; остаток 109 входит в состав пептидного эпитопа, распознаваемого Т- клеткой.


ВАРИАНТЫ АНТИГЕНОВ
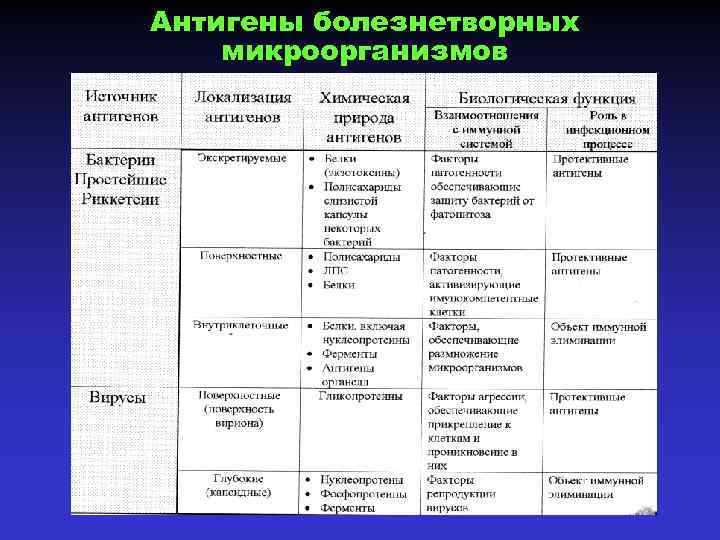
Антигены болезнетворных микроорганизмов

Характеристика анатоксинов - инактивированных бактериальных экзотоксинов
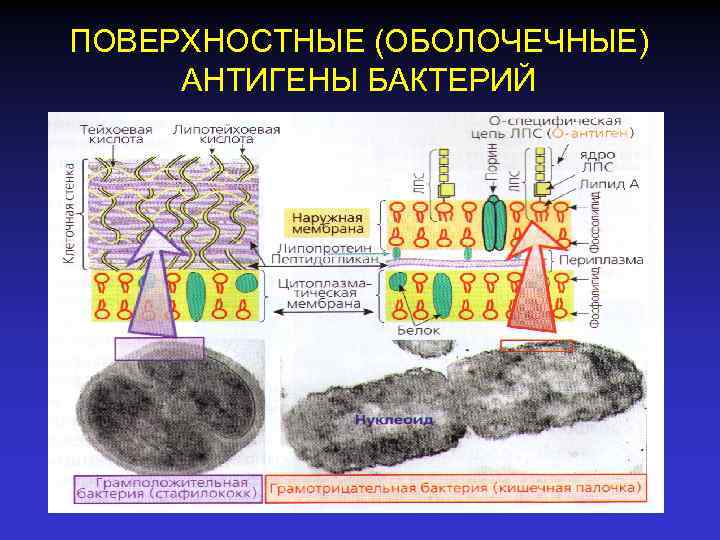
ПОВЕРХНОСТНЫЕ (ОБОЛОЧЕЧНЫЕ) АНТИГЕНЫ БАКТЕРИЙ

Антигенная структура бактерий Примечание: строение клеточной стенки бактерий. Пептидогликановый слой присутствует в клеточной стенки всех бактерий, липидный бислой характерен для грамотрицательных бактерий.
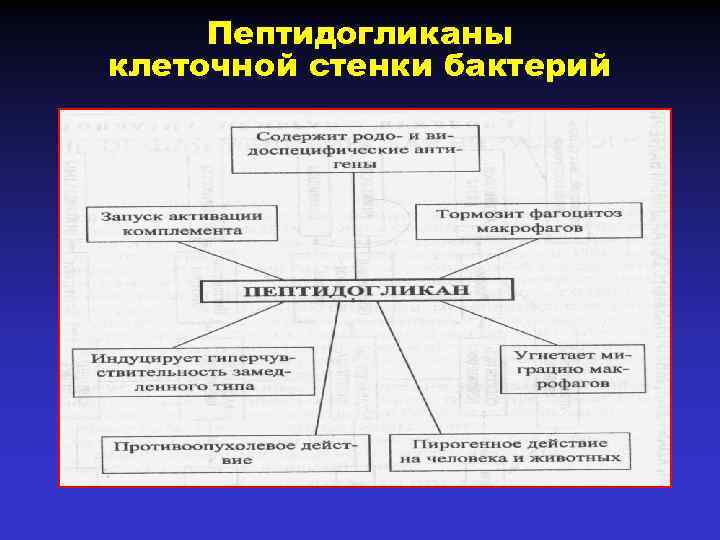
Пептидогликаны клеточной стенки бактерий

Антигенная структура вирусов Структура вируса гриппа

АНТИГЕНЫ РАЗЛИЧНЫХ ВИРУСОВ

Схема строения зрелого вириона вируса иммунодефицита человека 1. Наружный отросток оболочки ВИЧ, состоящий из 2 -х белков gp 120 и gp 41 2. Мембрана вириона клеточного происхождения 3. Белки мембраны клеточного происхождения (HLА и др. ) 4. Матриксный слой - р 17 5. Оболочка нуклеокапсида – р 24 6. Геномная РНК (две одноцепочечные молекулы) 7. Ферменты комплекса интеграции (обратная транскриптаза, интеграза, РНК-аза Н) 8. Нуклеопротеины (p 7, Vpr и ? )
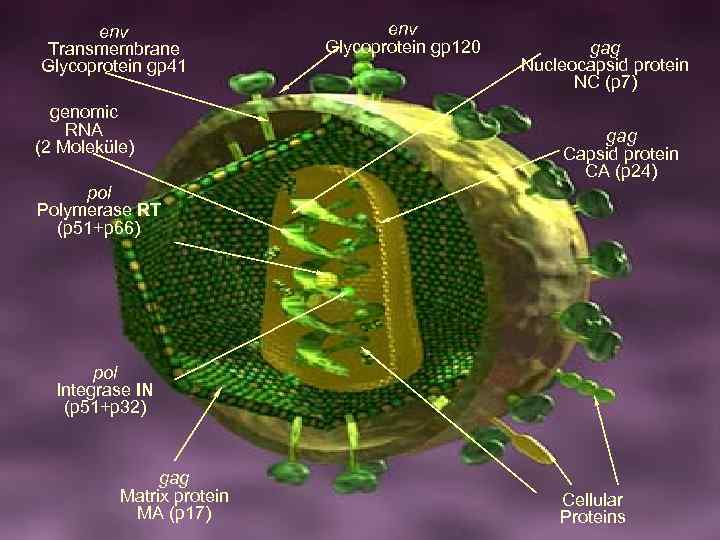
env Transmembrane Glycoprotein gp 41 genomic RNA (2 Moleküle) env Glycoprotein gp 120 gag Nucleocapsid protein NC (p 7) gag Capsid protein CA (p 24) pol Polymerase RT (p 51+p 66) pol Integrase IN (p 51+p 32) gag Matrix protein MA (p 17) Cellular Proteins

СВОЙСТВА HCV • • • высокая генетическая вариабельность, существование у одного хозяина набора вирионов, имеющих измененные, но близкородственные геномы - квазивидов вируса, постоянное изменение состава оболочечных антигенов, тропность к гепатоцитам, способность к внепеченочной репликации, персистенция в клетках иммунной системы – лимфоцитах и моноцитах крови, мононуклеарных фагоцитах печени, что инициирует региональную и общую дисфункцию иммунной системы.

Традиционные вакцины
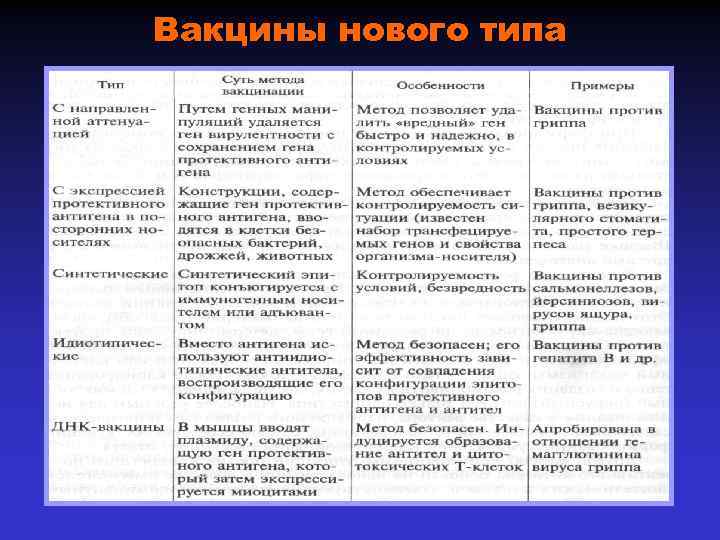
Вакцины нового типа
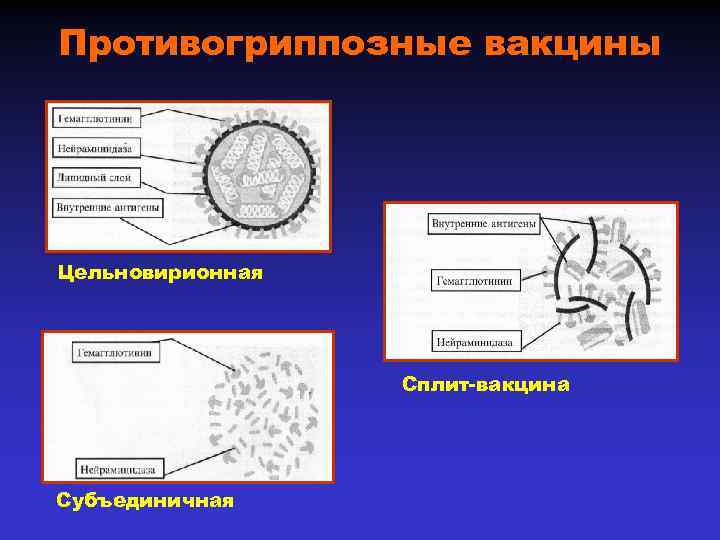
Противогриппозные вакцины Цельновирионная Сплит-вакцина Субъединичная
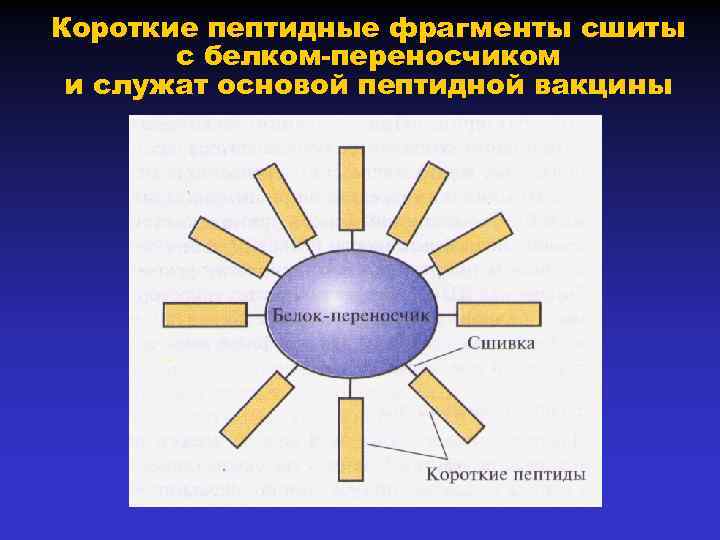
Короткие пептидные фрагменты сшиты с белком-переносчиком и служат основой пептидной вакцины

Иммунокорригирующие препараты бактериального происхождения

Спектр иммунокорригирующей активности вакциноподобных препаратов

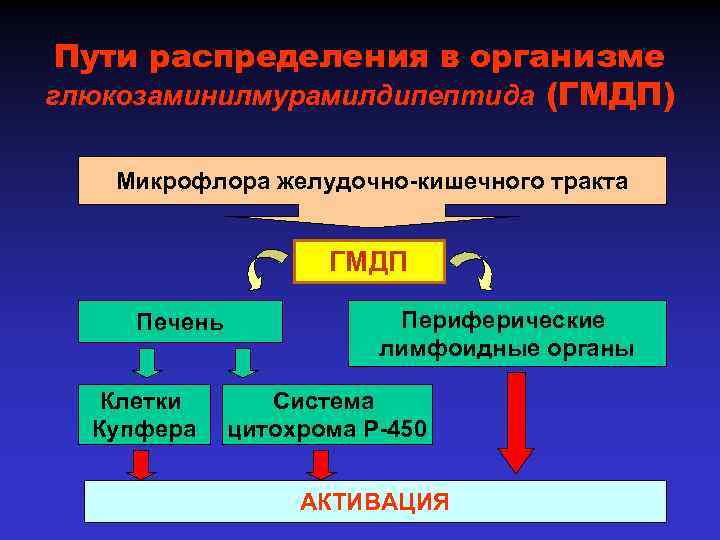
Пути распределения в организме глюкозаминилмурамилдипептида (ГМДП) Микрофлора желудочно-кишечного тракта ГМДП Печень Клетки Купфера Периферические лимфоидные органы Система цитохрома Р-450 АКТИВАЦИЯ

Механизм биологической активности ГМДП Модификация спектра поверхностных антигенов клеток-мишеней: клетки миело-моноцитарного ряда • увеличение экспрессии HLA-DR антигенов • увеличение экспрессии рецепторов IL-2 опухолевые клетки • увеличение экспрессии опухоль-ассоциированных антигенов • стимуляция экспрессии молекул клеточной адгезии
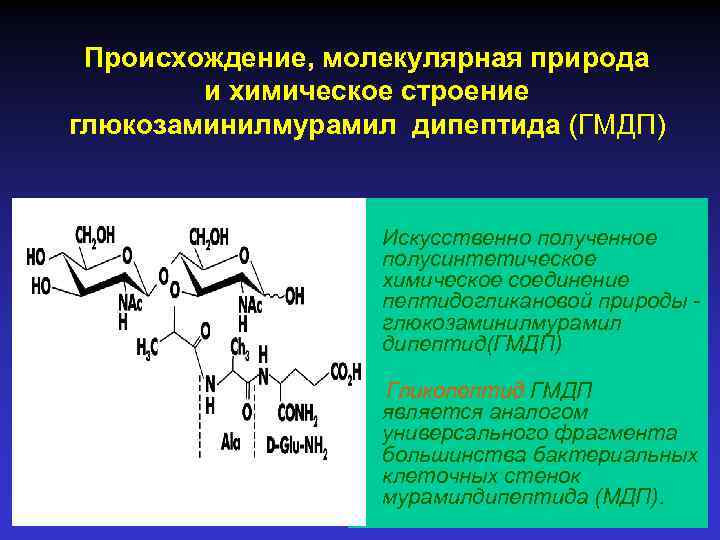
Происхождение, молекулярная природа и химическое строение глюкозаминилмурамил дипептида (ГМДП) • Искусственно полученное полусинтетическое химическое соединение пептидогликановой природы глюкозаминилмурамил дипептид(ГМДП) Гликопептид ГМДП является аналогом универсального фрагмента большинства бактериальных клеточных стенок мурамилдипептида (МДП).

Условно-патогенная микрофлора и развитии иммунопатологических реакций при заболеваниях ЖКТ Обеспечивает развитие хронических заболеваний, индуцируя и поддерживая воспалительную реакцию. В результате постоянного контакта с липополисахаридами грамотрицательных бактерий происходит поликлональная стимуляция В -лимфоцитов, выработка антител к ЛПС, которые могут вступать в перекрестные реакции с ДНК клеток, результатом чего является выработка антител к собственной ДНК и инициализация аутоиммунных реакций. В результате усиления функциональной активности нейтрофилов и макрофагов под воздействием ЛПС происходит интенсивная продукция провоспалительных цитокинов. Липополисахариды грамотрицательных бактерий способствуют альтернативному пути активации комплемента, усугубляя развитие воспалительных реакций. ЛПС непосредственно воздействуют на эндотелий сосудов, активируя эндотелиальные клетки (ЭК). При повторном контакте ЛПС с сенсибилизированными ЭК развиваются участки геморрагическо-некротического воспаления по типу локального или генерализованного феномена Шварцмана.
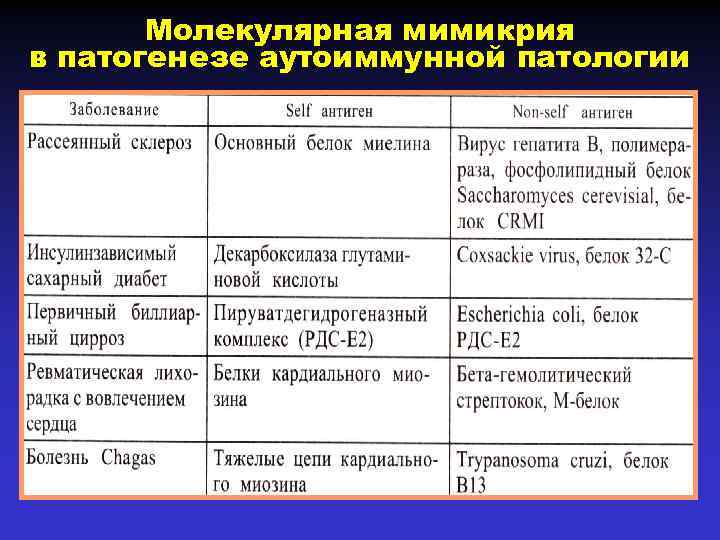
Молекулярная мимикрия в патогенезе аутоиммунной патологии

Аллергены – этиологические факторы Ig. E-зависимого анафилактического шока Полные белковые антигены • Пищевые — яйца, коровье молоко, орехи, ракообразные, моллюски, бобовые; • Яды — пчелы, осы и другие; • Вакцины — коревая, гриппозная, столбнячная; • Гормоны — инсулин, кортикотропин, тиротропин; • Антисыворотки — лошадиная, антитимоноцитарная, антилимфоцитарный глобулин против ядов; • Ферменты — стрептокиназа, хемопапаины; • Латекс — хирургические перчатки, эндотрахеальные трубки; • Аллергенные экстракты — домашняя пыль, перхоть животных, пыльца трав.

Специфические опухолевые антигены

Опухоль-эмбриональные антигены антиген

ОНКОМАРКЕРЫ • Эмбриональные антигены • Онкофетальные трансплантационные антигены • Дифференцировочные антигены • Продукты онкогенов • Ростовые и трансформирующие факторы • Ферменты и изоферменты


УЗНАВАНИЕ АНТИГЕНОВ И ИНИЦИАЦИЯ ИММУНОРЕАКТИВНОСТИ проф. Виктор Константинович КОЗЛОВ Профессор кафедр: клинической лабораторной диагностики СЗГМУ им. И. И. Мечникова; микробиологии, иммунологии и инфекционных болезней Новгородского государственного университета им. Ярослава Мудрого; челюстно-лицевой хирургии и хирургической стоматологии Санкт-Петербургского государственного университета. Директор Института высоких медицинских технологий Санкт-Петербургского государственного университета

СТРУКТУРЫ, УЗНАЮЩИЕ АНТИГЕНЫ
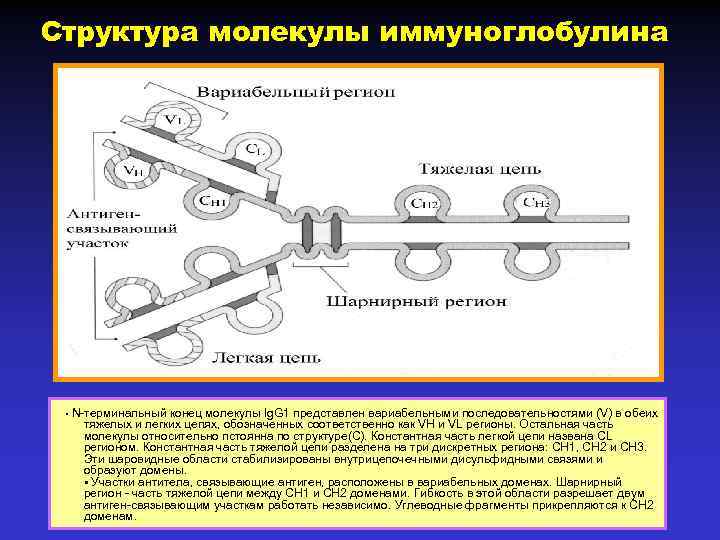
Структура молекулы иммуноглобулина • N-терминальный конец молекулы Ig. G 1 представлен вариабельными последовательностями (V) в обеих тяжелых и легких цепях, обозначенных соответственно как VH и VL регионы. Остальная часть молекулы относительно пстоянна по структуре(С). Константная часть легкой цепи названа CL регионом. Константная часть тяжелой цепи разделена на три дискретных региона: CH 1, CH 2 и CH 3. Эти шаровидные области стабилизированы внутрицепочечными дисульфидными связями и образуют домены. • Участки антитела, связывающие антиген, расположены в вариабельных доменах. Шарнирный регион - часть тяжелой цепи между CH 1 и CH 2 доменами. Гибкость в этой области разрешает двум антиген-связывающим участкам работать независимо. Углеводные фрагменты прикрепляются к CH 2 доменам.
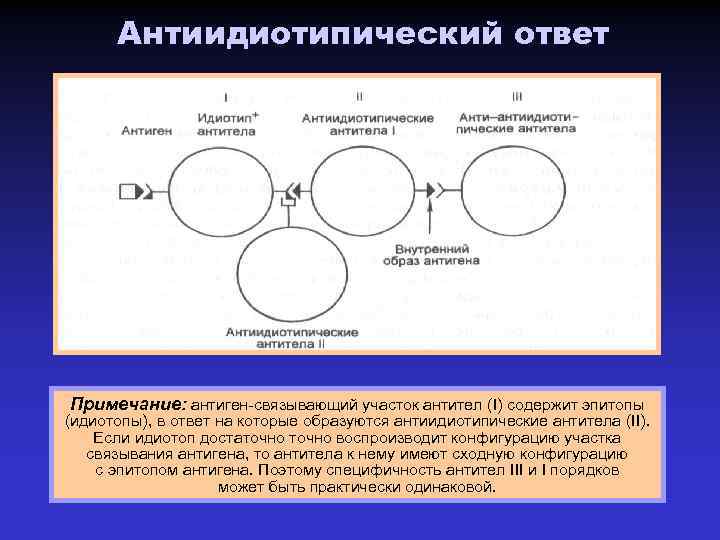
Антиидиотипический ответ Примечание: антиген-связывающий участок антител (I) содержит эпитопы (идиотопы), в ответ на которые образуются антиидиотипические антитела (II). Если идиотоп достаточно воспроизводит конфигурацию участка связывания антигена, то антитела к нему имеют сходную конфигурацию с эпитопом антигена. Поэтому специфичность антител III и I порядков может быть практически одинаковой.
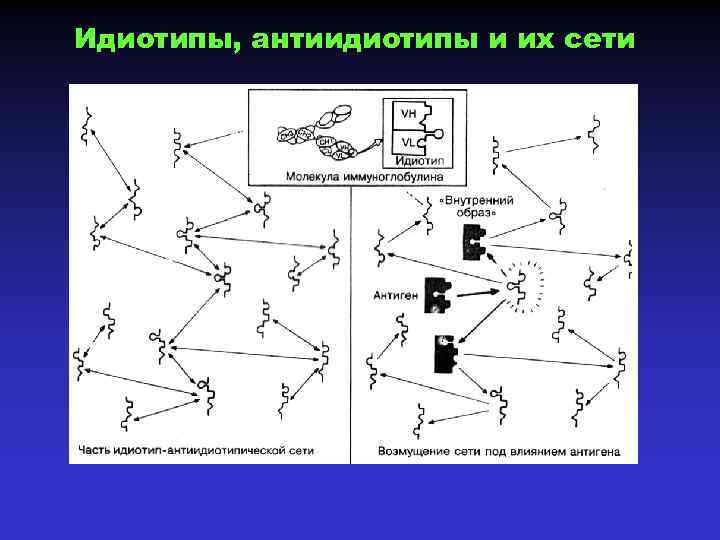
Идиотипы, антиидиотипы и их сети

Мембранная форма иммуноглобулина – рецептор узнавания антигена В-лимфоцита (в синей рамке) • • Комплекс BCR состоит из m. Ig. M, ассоциированного с гетеродимером Igα-Igβ. Остатки тирозина в ITAM-мотивах молекул Igα-Igβ фосфорилируются тирозинкиназой Lyn (р - участки фосфорилирования). Остатки тирозина после этого могут связаться с доменами тирозинкиназы Syk. Совместное фосфорилирование тирозина, выполненное фосфотирозинкиназами Lyn, Syk и Btk является пусковым механизмом активации фосфолипазы Сγ (PLCγ) для гидролиза фосфатидилинозитол-дифосфата (PIP 2). При гидролизе PIP 2 образуются инозитолтрифосфат (IP 3) и диацилглицерол (DAG). IP 3 индуцирует мобилизацию кальция из внутриклеточного пула , а DAG активирует протеинкиназу С (PKC). После опустошения внутриклеточного кальциевого пула происходит раскрытие кальциевых каналов на клеточной мембране, и начинается проникновение ионов кальция внутрь клетки. Результатом описанных реакций становится перемещение в ядро активированных MAP-киназ (ERK, JNK и p 38), а также ядерных факторов NF-k. B и NF-AT (после дефосфорилирования) где они регулируют ядерную транскрипцию.
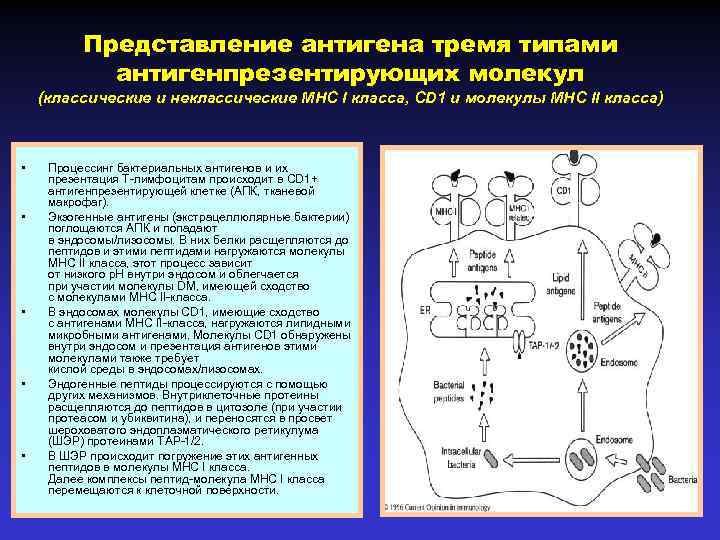
Представление антигена тремя типами антигенпрезентирующих молекул (классические и неклассические MHC I класса, CD 1 и молекулы MHC II класса) • • • Процессинг бактериальных антигенов и их презентация Т-лимфоцитам происходит в CD 1+ антигенпрезентирующей клетке (АПК, тканевой макрофаг). Экзогенные антигены (экстрацеллюлярные бактерии) поглощаются АПК и попадают в эндосомы/лизосомы. В них белки расщепляются до пептидов и этими пептидами нагружаются молекулы MHC II класса, этот процесс зависит от низкого p. H внутри эндосом и облегчается при участии молекулы DM, имеющей сходство с молекулами МНС II-класса. В эндосомах молекулы CD 1, имеющие сходство с антигенами МНС II-класса, нагружаются липидными микробными антигенами. Молекулы CD 1 обнаружены внутри эндосом и презентация антигенов этими молекулами также требует кислой среды в эндосомах/лизосомах. Эндогенные пептиды процессируются с помощью других механизмов. Внутриклеточные протеины расщепляются до пептидов в цитозоле (при участии протеасом и убиквитина), и переносятся в просвет шероховатого эндоплазматического ретикулума (ШЭР) протеинами TAP-1/2. В ШЭР происходит погружение этих антигенных пептидов в молекулы МНС I класса. Далее комплексы пептид-молекула MHC I класса перемещаются к клеточной поверхности.
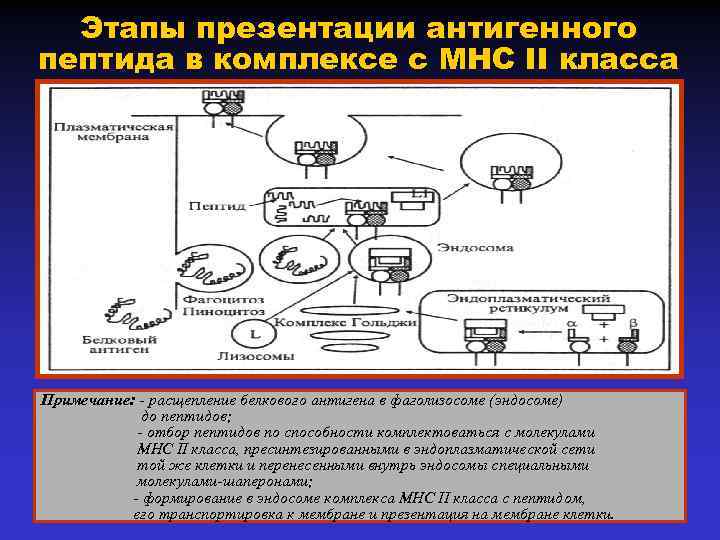
Этапы презентации антигенного пептида в комплексе с MHC II класса Примечание: - расщепление белкового антигена в фаголизосоме (эндосоме) до пептидов; - отбор пептидов по способности комплектоваться с молекулами МНС II класса, пресинтезированными в эндоплазматической сети той же клетки и перенесенными внутрь эндосомы специальными молекулами-шаперонами; - формирование в эндосоме комплекса МНС II класса с пептидом, его транспортировка к мембране и презентация на мембране клетки.
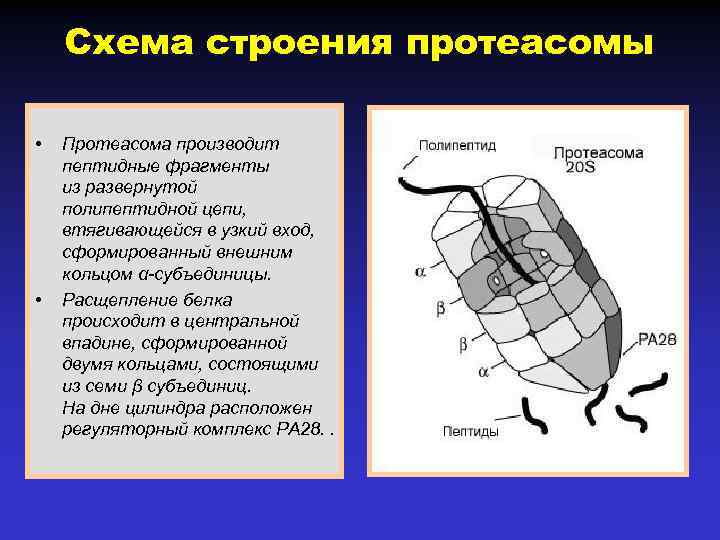
Схема строения протеасомы • • Протеасома производит пептидные фрагменты из развернутой полипептидной цепи, втягивающейся в узкий вход, сформированный внешним кольцом α-субъединицы. Расщепление белка происходит в центральной впадине, сформированной двумя кольцами, состоящими из семи β субъединиц. На дне цилиндра расположен регуляторный комплекс PA 28. .
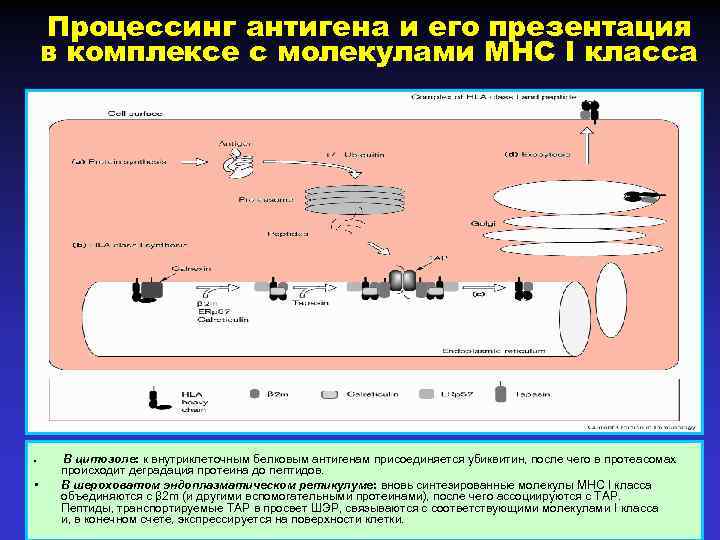
Процессинг антигена и его презентация в комплексе с молекулами MHC I класса • • В цитозоле: к внутриклеточным белковым антигенам присоединяется убиквитин, после чего в протеасомах происходит деградация протеина до пептидов. В шероховатом эндоплазматическом ретикулуме: вновь синтезированные молекулы МНС I класса объединяются с β 2 m (и другими вспомогательными протеинами), после чего ассоциируются с ТАР. Пептиды, транспортируемые ТАР в просвет ШЭР, связываются с соответствующими молекулами I класса и, в конечном счете, экспрессируется на поверхности клетки.

Характеристика профессиональных антигенпрезентирующих клеток
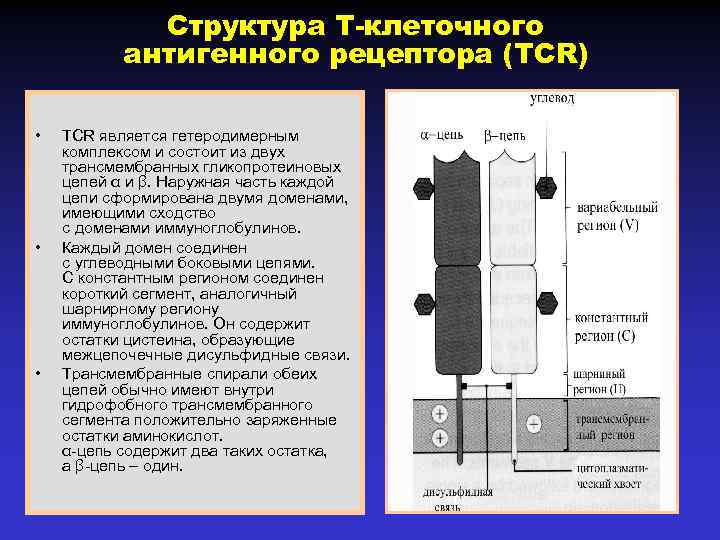
Структура Т-клеточного антигенного рецептора (TCR) • • • TCR является гетеродимерным комплексом и состоит из двух трансмембранных гликопротеиновых цепей α и β. Наружная часть каждой цепи сформирована двумя доменами, имеющими сходство с доменами иммуноглобулинов. Каждый домен соединен с углеводными боковыми цепями. С константным регионом соединен короткий сегмент, аналогичный шарнирному региону иммуноглобулинов. Он содержит остатки цистеина, образующие межцепочечные дисульфидные связи. Трансмембранные спирали обеих цепей обычно имеют внутри гидрофобного трансмембранного сегмента положительно заряженные остатки аминокислот. α-цепь содержит два таких остатка, а β-цепь – один.
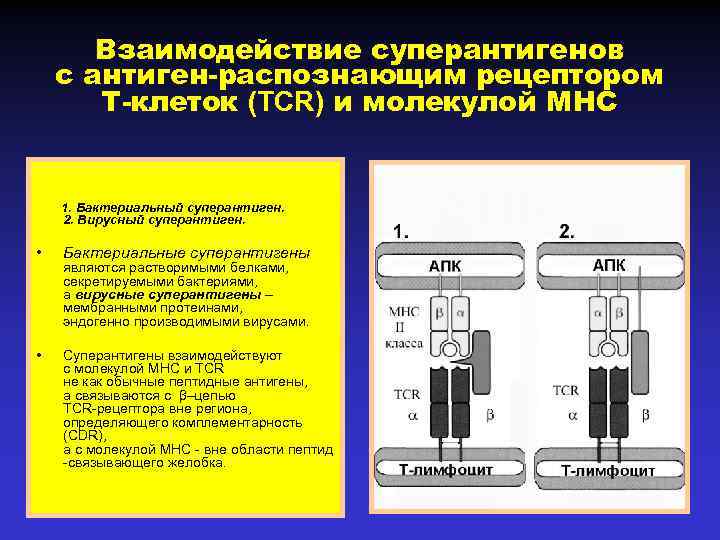
Взаимодействие суперантигенов с антиген-распознающим рецептором Т-клеток (TCR) и молекулой МНС 1. Бактериальный суперантиген. 2. Вирусный суперантиген. • Бактериальные суперантигены • Суперантигены взаимодействуют с молекулой МНС и TCR не как обычные пептидные антигены, а связываются с β–цепью TCR-рецептора вне региона, определяющего комплементарность (CDR), а с молекулой МНС - вне области пептид -связывающего желобка. являются растворимыми белками, секретируемыми бактериями, а вирусные суперантигены – мембранными протеинами, эндогенно производимыми вирусами.
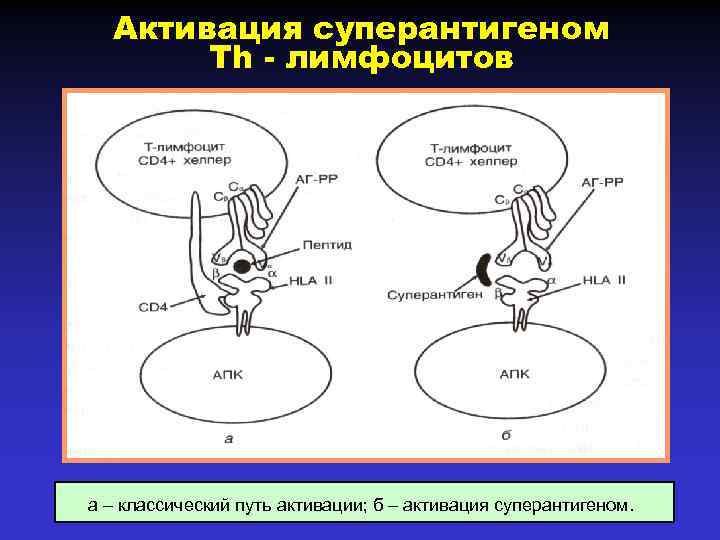
Активация суперантигеном Тh - лимфоцитов а – классический путь активации; б – активация суперантигеном.
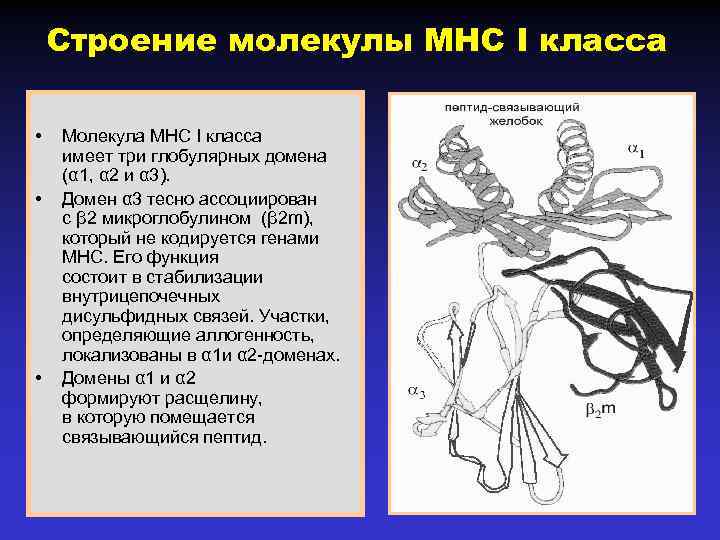
Строение молекулы MHC I класса • • • Молекула МНС I класса имеет три глобулярных домена (α 1, α 2 и α 3). Домен α 3 тесно ассоциирован с β 2 микроглобулином (β 2 m), который не кодируется генами MHC. Его функция состоит в стабилизации внутрицепочечных дисульфидных связей. Участки, определяющие аллогенность, локализованы в α 1 и α 2 -доменах. Домены α 1 и α 2 формируют расщелину, в которую помещается связывающийся пептид.
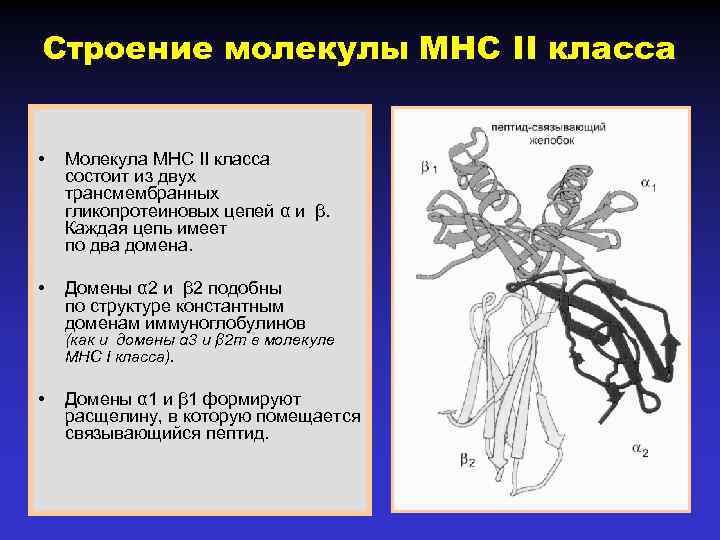
Строение молекулы MHC II класса • Молекула МНС II класса состоит из двух трансмембранных гликопротеиновых цепей α и β. Каждая цепь имеет по два домена. • Домены α 2 и β 2 подобны по структуре константным доменам иммуноглобулинов (как и домены α 3 и β 2 m в молекуле МНС I класса). • Домены α 1 и β 1 формируют расщелину, в которую помещается связывающийся пептид.
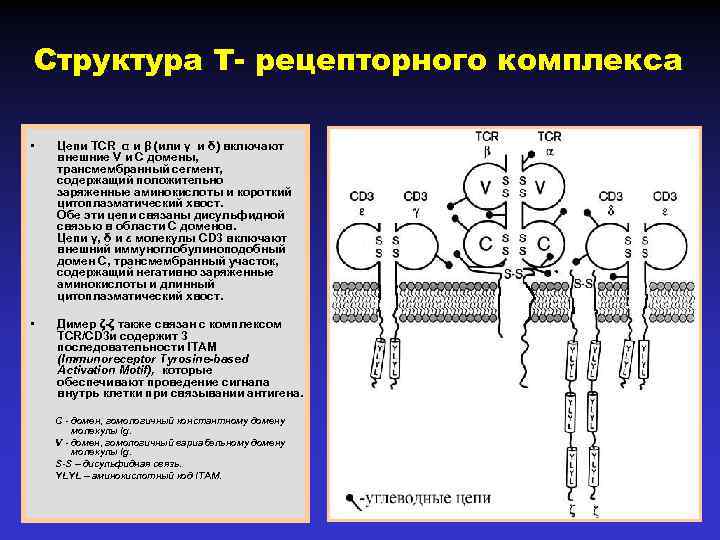
Структура Т- рецепторного комплекса • Цепи TCR α и β (или γ и δ) включают внешние V и C домены, трансмембранный сегмент, содержащий положительно заряженные аминокислоты и короткий цитоплазматический хвост. Обе эти цепи связаны дисульфидной связью в области C доменов. Цепи γ, δ и ε молекулы CD 3 включают внешний иммуноглобулиноподобный домен C, трансмембранный участок, содержащий негативно заряженные aминокислоты и длинный цитоплазматический хвост. • Димер ζ-ζ также связан с комплексом TCR/CD 3 и содержит 3 последовательности ITAM (Immunoreceptor Tyrosine-based Activation Motif), которые обеспечивают проведение сигнала внутрь клетки при связывании антигена. С - домен, гомологичный константному домену молекулы Ig. V - домен, гомологичный вариабельному домену молекулы Ig. S-S – дисульфидная связь. YLYL – аминокислотный код ITAM.
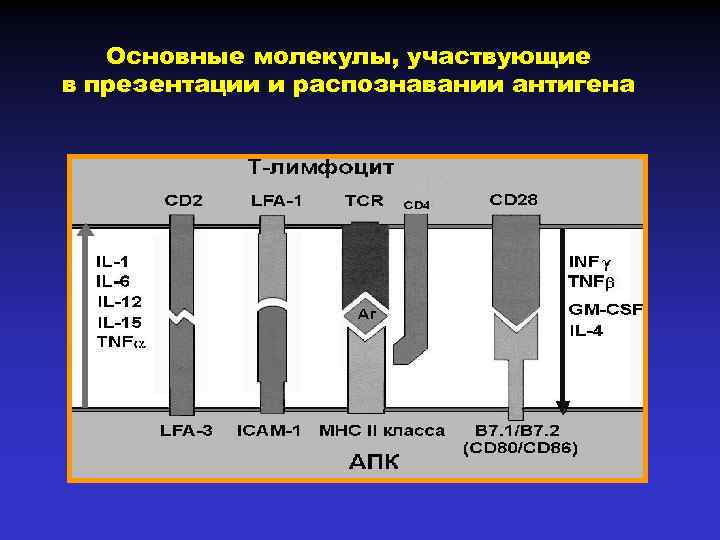
Основные молекулы, участвующие в презентации и распознавании антигена

Антигены_МАПО_фин.ppt