17_Ионные равновесия в растворах.ppt
- Количество слайдов: 21
 Ионные равновесия в растворах Лекция 17 по курсу «Общая химия»
Ионные равновесия в растворах Лекция 17 по курсу «Общая химия»
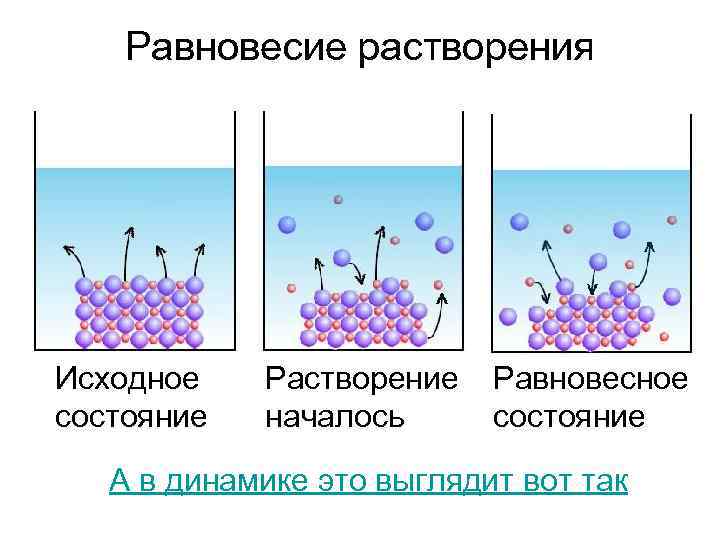 Равновесие растворения Исходное состояние Растворение началось Равновесное состояние А в динамике это выглядит вот так
Равновесие растворения Исходное состояние Растворение началось Равновесное состояние А в динамике это выглядит вот так
 Константа (произведение) растворимости Ktx. Any(к) ⇄ y+ x. Kt (р) + x– y. An (р) В старых книгах обозначают как ПР Применима только к малорастворимым и нерастворимым электролитам!
Константа (произведение) растворимости Ktx. Any(к) ⇄ y+ x. Kt (р) + x– y. An (р) В старых книгах обозначают как ПР Применима только к малорастворимым и нерастворимым электролитам!
 Расчет растворимости по Ks a) В чистой воде Ag. Cl(к) ⇄ Ag+(р) + Cl–(р) (размерность моль2/дм 2 подразумевается, но не пишется) По уравнению реакции: (т. к. никаких других источников ионов в растворе нет) моль/дм 3 Нашли концентрацию. А растворимость?
Расчет растворимости по Ks a) В чистой воде Ag. Cl(к) ⇄ Ag+(р) + Cl–(р) (размерность моль2/дм 2 подразумевается, но не пишется) По уравнению реакции: (т. к. никаких других источников ионов в растворе нет) моль/дм 3 Нашли концентрацию. А растворимость?
 Расчет растворимости по Ks (продолжение) Растворимость – масса вещества в 100 г растворителя = 1 г/см 3 (для разб. растворов верно!) Допущения: m. Ag. Cl << mраствора В 1000 г воды В 100 г воды 1. 25 10 -5 моль Ag. Cl 1. 25 10 -6 моль Ag. Cl SAg. Cl = 1. 25 10 -6 143. 5 = 1. 79 10– 3 Количество Ag. Cl (моль) в 100 г воды МAg. Cl, г/моль
Расчет растворимости по Ks (продолжение) Растворимость – масса вещества в 100 г растворителя = 1 г/см 3 (для разб. растворов верно!) Допущения: m. Ag. Cl << mраствора В 1000 г воды В 100 г воды 1. 25 10 -5 моль Ag. Cl 1. 25 10 -6 моль Ag. Cl SAg. Cl = 1. 25 10 -6 143. 5 = 1. 79 10– 3 Количество Ag. Cl (моль) в 100 г воды МAg. Cl, г/моль
 Расчет растворимости солей с многозарядными ионами Ca 3(PO 4)2 ⇄ 3 Ca 2+ + 2 PO 43– SCa 3(PO 4)2 = 1. 13∙ 10 -7∙ 310 = 3. 53∙ 10– 5 г/дм 3 или 3. 53∙ 10– 6 г на 100 г растворителя
Расчет растворимости солей с многозарядными ионами Ca 3(PO 4)2 ⇄ 3 Ca 2+ + 2 PO 43– SCa 3(PO 4)2 = 1. 13∙ 10 -7∙ 310 = 3. 53∙ 10– 5 г/дм 3 или 3. 53∙ 10– 6 г на 100 г растворителя
 Способы смещения равновесия растворимости 1. Повышение температуры – S↑ 2. Добавление одноименного иона – S↓ 3. Добавление реагента, участвующего в конкурирующем равновесии с катионом или анионом – S↑ 4. Добавление электролита, не имеющего общих ионов – обычно S немного ↑ (солевой эффект). Причина: количество ионов ↑ взаимодействие между ними ↑ активность ионов↓
Способы смещения равновесия растворимости 1. Повышение температуры – S↑ 2. Добавление одноименного иона – S↓ 3. Добавление реагента, участвующего в конкурирующем равновесии с катионом или анионом – S↑ 4. Добавление электролита, не имеющего общих ионов – обычно S немного ↑ (солевой эффект). Причина: количество ионов ↑ взаимодействие между ними ↑ активность ионов↓
 Влияние одноименных ионов Ktx. Any(к) ⇄ y+ x. Kt (р) + x– y. An (р) Повышение концентрации Kty+ = const Автоматически снижается концентрация Anx–! (произведение должно остаться постоянным)
Влияние одноименных ионов Ktx. Any(к) ⇄ y+ x. Kt (р) + x– y. An (р) Повышение концентрации Kty+ = const Автоматически снижается концентрация Anx–! (произведение должно остаться постоянным)
 Расчет растворимости по Ks б) В растворе с одноименным ионом: Рассчитаем SAg. Cl в 0, 01 М растворе Na. Cl Ag. Cl(к) ⇄ Ag+(р) + Cl–(р) Поскольку x << 0. 01, то: моль/дм 3 А в чистой воде? Растворимость уменьшилась в 800 раз!
Расчет растворимости по Ks б) В растворе с одноименным ионом: Рассчитаем SAg. Cl в 0, 01 М растворе Na. Cl Ag. Cl(к) ⇄ Ag+(р) + Cl–(р) Поскольку x << 0. 01, то: моль/дм 3 А в чистой воде? Растворимость уменьшилась в 800 раз!
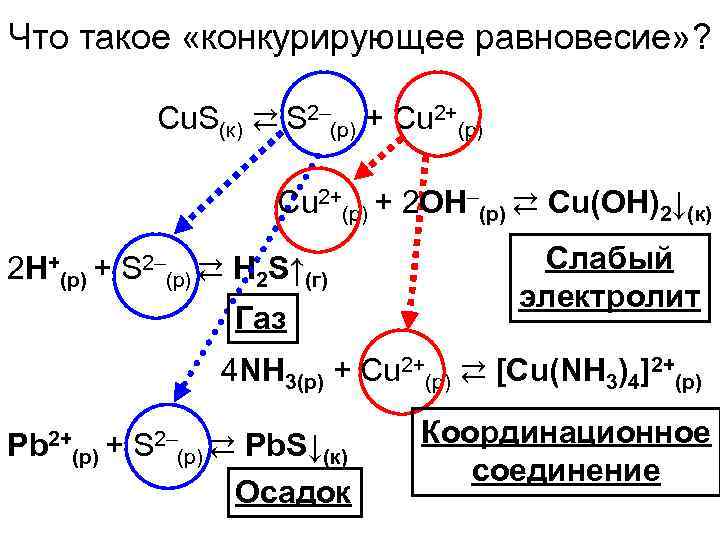 Что такое «конкурирующее равновесие» ? Cu. S(к) ⇄ S 2–(р) + Cu 2+(р) + 2 OH–(р) ⇄ Cu(OH)2↓(к) 2 H+(р) + S 2–(р) ⇄ H 2 S↑(г) Газ Слабый электролит 4 NH 3(р) + Cu 2+(р) ⇄ [Cu(NH 3)4]2+(р) Pb 2+(р) + S 2–(р) ⇄ Pb. S↓(к) Осадок Координационное соединение
Что такое «конкурирующее равновесие» ? Cu. S(к) ⇄ S 2–(р) + Cu 2+(р) + 2 OH–(р) ⇄ Cu(OH)2↓(к) 2 H+(р) + S 2–(р) ⇄ H 2 S↑(г) Газ Слабый электролит 4 NH 3(р) + Cu 2+(р) ⇄ [Cu(NH 3)4]2+(р) Pb 2+(р) + S 2–(р) ⇄ Pb. S↓(к) Осадок Координационное соединение
 Гидролиз От греч. hydro – вода, lysis – разложение Взаимодействие сложного вещества с водой (не менее 2 продуктов!) Обычно – реакция обмена без изменения степени окисления +5 – 1 PCl 5 + H 2 O = H 3 PO 4 + HCl Реже – окислительно-восстановительная: – 1 +1 0 Ca. H 2 + H 2 O = Ca(OH)2 + H 2↑ SO 3 + H 2 O = H 2 SO 4 Реакция соединения – не гидролиз!
Гидролиз От греч. hydro – вода, lysis – разложение Взаимодействие сложного вещества с водой (не менее 2 продуктов!) Обычно – реакция обмена без изменения степени окисления +5 – 1 PCl 5 + H 2 O = H 3 PO 4 + HCl Реже – окислительно-восстановительная: – 1 +1 0 Ca. H 2 + H 2 O = Ca(OH)2 + H 2↑ SO 3 + H 2 O = H 2 SO 4 Реакция соединения – не гидролиз!
 Гидролиз солей Реакция, обратная реакции нейтрализации Соль Результат Пример Сильной кислоты Гидролиза нет Na. Cl + H 2 O – реакция не идет и сильного основания Гидролиз по и слабого основания катиону, кислая среда в растворе Zn. Cl 2 + H 2 O Zn 2+ + H 2 O Zn(OH)Cl + HCl Zn(OH)+ + H+ Гидролиз по аниону, щелочная среда в растворе K 2 CO 3 + H 2 O CO 32– + H 2 O KHCO 3 + KOH HCO 3– + OH– Гидролиз по катиону и аниону, иногда необратимо. Среда зависит от силы кислоты и основания Cu(CH 3 COO)2 + H 2 O Cu(OH)CH 3 COO + CH 3 COOH Cu 2+ + H 2 O Cu(OH)+ + H+ CH 3 COO – + H 2 O CH 3 COOH + + OH– Сильной кислоты Слабой кислоты и сильного основания Слабой кислоты и слабого основания
Гидролиз солей Реакция, обратная реакции нейтрализации Соль Результат Пример Сильной кислоты Гидролиза нет Na. Cl + H 2 O – реакция не идет и сильного основания Гидролиз по и слабого основания катиону, кислая среда в растворе Zn. Cl 2 + H 2 O Zn 2+ + H 2 O Zn(OH)Cl + HCl Zn(OH)+ + H+ Гидролиз по аниону, щелочная среда в растворе K 2 CO 3 + H 2 O CO 32– + H 2 O KHCO 3 + KOH HCO 3– + OH– Гидролиз по катиону и аниону, иногда необратимо. Среда зависит от силы кислоты и основания Cu(CH 3 COO)2 + H 2 O Cu(OH)CH 3 COO + CH 3 COOH Cu 2+ + H 2 O Cu(OH)+ + H+ CH 3 COO – + H 2 O CH 3 COOH + + OH– Сильной кислоты Слабой кислоты и сильного основания Слабой кислоты и слабого основания
 Степень и константа гидролиза h = nгидролиз. /nобщ. – степень гидролиза Na. CN + H 2 O ⇄ Na. OH + HCN CN– + H 2 O ⇄ OH– + HCN – константа гидролиза Значений Kh в справочниках нет! Почему?
Степень и константа гидролиза h = nгидролиз. /nобщ. – степень гидролиза Na. CN + H 2 O ⇄ Na. OH + HCN CN– + H 2 O ⇄ OH– + HCN – константа гидролиза Значений Kh в справочниках нет! Почему?
 Kh и константа диссоциации Гидролиз CN– + H 2 O ⇄ OH– + HCN Диссоциация HCN + H 2 O ⇄ H 3 O+ + CN–
Kh и константа диссоциации Гидролиз CN– + H 2 O ⇄ OH– + HCN Диссоциация HCN + H 2 O ⇄ H 3 O+ + CN–
 Ступенчатый гидролиз PO 43– + H 2 O ⇄ HPO 42– + OH– HPO 42– + H 2 O ⇄ H 2 PO 4– + OH– H 2 PO 4– + H 2 O ⇄ H 3 PO 4 + OH– У кислоты три константы диссоциации У соли три константы гидролиза Какую на какую константу нужно умножать, чтобы получить Kw? ? ? ?
Ступенчатый гидролиз PO 43– + H 2 O ⇄ HPO 42– + OH– HPO 42– + H 2 O ⇄ H 2 PO 4– + OH– H 2 PO 4– + H 2 O ⇄ H 3 PO 4 + OH– У кислоты три константы диссоциации У соли три константы гидролиза Какую на какую константу нужно умножать, чтобы получить Kw? ? ? ?
 Факторы, влияющие на равновесие гидролиза • Природа гидролизующейся соли (см. выше) • Концентрация раствора • Добавление веществ со свойствами кислот или оснований • Добавление веществ, способных образовывать комплексы с гидролизующимися ионами • Температура
Факторы, влияющие на равновесие гидролиза • Природа гидролизующейся соли (см. выше) • Концентрация раствора • Добавление веществ со свойствами кислот или оснований • Добавление веществ, способных образовывать комплексы с гидролизующимися ионами • Температура
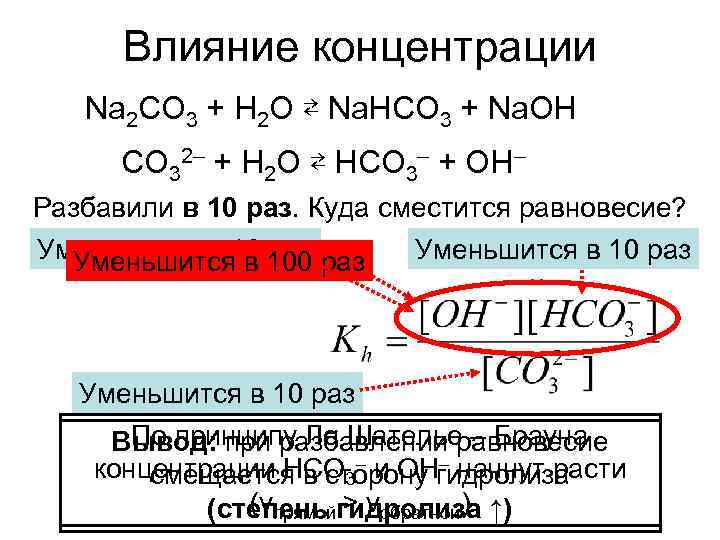 Влияние концентрации Na 2 CO 3 + H 2 O ⇄ Na. HCO 3 + Na. OH CO 32– + H 2 O ⇄ HCO 3– + OH– Разбавили в 10 раз. Куда сместится равновесие? Уменьшится в 10 100 раз Уменьшится в 10 раз По принципу Ле Шателье – Брауна Вывод: при разбавлении равновесие – начнут расти концентрации HCO 3– и OHгидролиза смещается в сторону (vпрямой > vобратной) (степень гидролиза ↑)
Влияние концентрации Na 2 CO 3 + H 2 O ⇄ Na. HCO 3 + Na. OH CO 32– + H 2 O ⇄ HCO 3– + OH– Разбавили в 10 раз. Куда сместится равновесие? Уменьшится в 10 100 раз Уменьшится в 10 раз По принципу Ле Шателье – Брауна Вывод: при разбавлении равновесие – начнут расти концентрации HCO 3– и OHгидролиза смещается в сторону (vпрямой > vобратной) (степень гидролиза ↑)
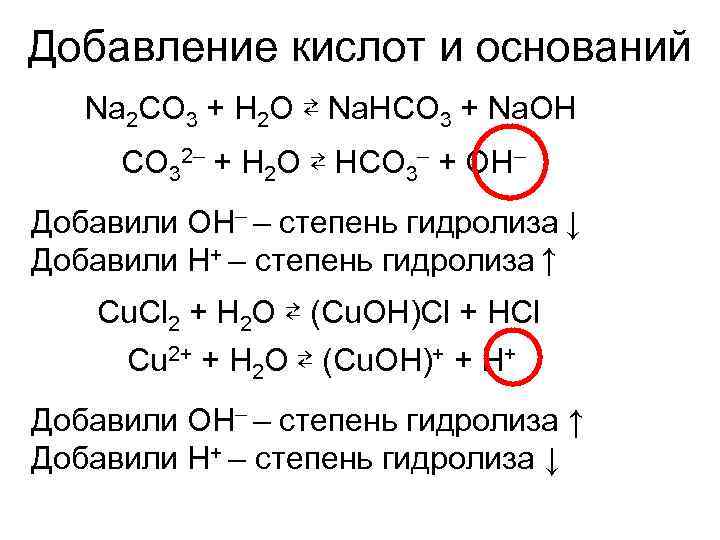 Добавление кислот и оснований Na 2 CO 3 + H 2 O ⇄ Na. HCO 3 + Na. OH CO 32– + H 2 O ⇄ HCO 3– + OH– Добавили OH– – степень гидролиза ↓ Добавили H+ – степень гидролиза ↑ Cu. Cl 2 + H 2 O ⇄ (Cu. OH)Cl + HCl Cu 2+ + H 2 O ⇄ (Cu. OH)+ + H+ Добавили OH– – степень гидролиза ↑ Добавили H+ – степень гидролиза ↓
Добавление кислот и оснований Na 2 CO 3 + H 2 O ⇄ Na. HCO 3 + Na. OH CO 32– + H 2 O ⇄ HCO 3– + OH– Добавили OH– – степень гидролиза ↓ Добавили H+ – степень гидролиза ↑ Cu. Cl 2 + H 2 O ⇄ (Cu. OH)Cl + HCl Cu 2+ + H 2 O ⇄ (Cu. OH)+ + H+ Добавили OH– – степень гидролиза ↑ Добавили H+ – степень гидролиза ↓
 Влияние температуры Что такое гидролиз? Реакция, обратная нейтрализации! Реакция нейтрализации в ионной форме: H+ + OH– = H 2 O Для сильных кислот/оснований – ровно столько, для слабых не так экзотермично Значит, для гидролиза Вывод: T↑ – степень гидролиза ↑
Влияние температуры Что такое гидролиз? Реакция, обратная нейтрализации! Реакция нейтрализации в ионной форме: H+ + OH– = H 2 O Для сильных кислот/оснований – ровно столько, для слабых не так экзотермично Значит, для гидролиза Вывод: T↑ – степень гидролиза ↑
 Виды равновесий в растворах (Уже изученные нами) Равновесие Пример Применимость Константа + – Диссо- H 2 SO 3(р) ⇄ H (р) + HSO 3 (р) HSO 3–(р) ⇄ H+(р) + SO 32–(р) циации Диссоциации К слабым электролитам 2+ – Осаж- Ca(OH)2(к) ⇄ Ca (р) + 2 OH (р) дения К мало- и не- Растворимости растворимым электролитам CN–(р) + H 2 O ⇄ HCN(р) + OH–(р) К солям сла. Гидробых кислот лиза (оснований) Гидролиза
Виды равновесий в растворах (Уже изученные нами) Равновесие Пример Применимость Константа + – Диссо- H 2 SO 3(р) ⇄ H (р) + HSO 3 (р) HSO 3–(р) ⇄ H+(р) + SO 32–(р) циации Диссоциации К слабым электролитам 2+ – Осаж- Ca(OH)2(к) ⇄ Ca (р) + 2 OH (р) дения К мало- и не- Растворимости растворимым электролитам CN–(р) + H 2 O ⇄ HCN(р) + OH–(р) К солям сла. Гидробых кислот лиза (оснований) Гидролиза
 Виды равновесий в растворах (Пока не изучались в этом курсе) Равновесие Пример Применимость Константа 3+ – 2+ Восстанов- 2 Fe (р) + 2 I (р) ⇄ 2 Fe (р) + I 2(р) ления/окисления К окислительно-восстановительным процессам Комплексо- Fe(CN)63–(р) ⇄ Fe 3+(р) + 6 CN–(р) образования К координаци- Нестойкости онным соединениям Не используется (вместо нее – окислительно-восстановительный потенциал Е)
Виды равновесий в растворах (Пока не изучались в этом курсе) Равновесие Пример Применимость Константа 3+ – 2+ Восстанов- 2 Fe (р) + 2 I (р) ⇄ 2 Fe (р) + I 2(р) ления/окисления К окислительно-восстановительным процессам Комплексо- Fe(CN)63–(р) ⇄ Fe 3+(р) + 6 CN–(р) образования К координаци- Нестойкости онным соединениям Не используется (вместо нее – окислительно-восстановительный потенциал Е)


