Л.6 Ионная проводимость в твердых телах.pptx
- Количество слайдов: 48
 Ионная проводимость в твердых телах
Ионная проводимость в твердых телах
 Ионная проводимость Понятие проводимости чаще всего ассоциируется с направленным переносом электронов, осуществляющемся в металлах и полупроводниках под действием разности потенциалов. Однако очень важное значение имеет и ионная проводимость.
Ионная проводимость Понятие проводимости чаще всего ассоциируется с направленным переносом электронов, осуществляющемся в металлах и полупроводниках под действием разности потенциалов. Однако очень важное значение имеет и ионная проводимость.
 Ионная проводимость • 30 -е годы XIX века – первые упоминания об ионной проводимости – М. Фарадей обнаружил аномально высокую проводимость сульфида серебра. Несколько позже им было отмечено резкое увеличение проводимости фторида свинца при фазовом переходе ок. 720 К. Но о принципиально новом типе носителей заряда речь еще не идет. • Высокая ионная проводимость ионных кристаллов была описана только через 80 лет Турбандтом и Лоренцом для α-Ag. I. Она появлялась только при фазовом переходе ок. 420 К. • Поток работ по исследованию твердых ионных электролитов возрос лишь в 60 -е годы XX в. после обнаружения высокой ионной проводимости (0, 35 См/см) у кристаллов Rb. Ag 4 I 5 и описания Бредли и Грином проводящих свойств β-глинозема, которые было предложено использовать для конструирования аккумуляторов. • В 80 -е годы XX в. появился журнал “Solid state ionics”.
Ионная проводимость • 30 -е годы XIX века – первые упоминания об ионной проводимости – М. Фарадей обнаружил аномально высокую проводимость сульфида серебра. Несколько позже им было отмечено резкое увеличение проводимости фторида свинца при фазовом переходе ок. 720 К. Но о принципиально новом типе носителей заряда речь еще не идет. • Высокая ионная проводимость ионных кристаллов была описана только через 80 лет Турбандтом и Лоренцом для α-Ag. I. Она появлялась только при фазовом переходе ок. 420 К. • Поток работ по исследованию твердых ионных электролитов возрос лишь в 60 -е годы XX в. после обнаружения высокой ионной проводимости (0, 35 См/см) у кристаллов Rb. Ag 4 I 5 и описания Бредли и Грином проводящих свойств β-глинозема, которые было предложено использовать для конструирования аккумуляторов. • В 80 -е годы XX в. появился журнал “Solid state ionics”.
 Ионный кристалл Кристаллические вещества, в которых сцепление между частицами обусловлено преимущественно ионными связями. Поскольку между ионными и полярными ковалентными связями существует непрерывный переход, то нет резкой границы и между ионными и ковалентными кристаллами. К ионным относят кристаллы, в которых связи между атомами наиболее полярны. В основном это соли щелочных и щелочно-земельных металлов. Они отличаются высокими температурами плавления, обычно значительной ШЗЗ, обладают ионной проводимостью при высоких температурах и рядом специфических оптических свойств (например, ионные кристаллы могут быть прозрачны в ближней области ИК спектра).
Ионный кристалл Кристаллические вещества, в которых сцепление между частицами обусловлено преимущественно ионными связями. Поскольку между ионными и полярными ковалентными связями существует непрерывный переход, то нет резкой границы и между ионными и ковалентными кристаллами. К ионным относят кристаллы, в которых связи между атомами наиболее полярны. В основном это соли щелочных и щелочно-земельных металлов. Они отличаются высокими температурами плавления, обычно значительной ШЗЗ, обладают ионной проводимостью при высоких температурах и рядом специфических оптических свойств (например, ионные кристаллы могут быть прозрачны в ближней области ИК спектра).
 Ионный кристалл Ионные кристаллы могут быть построены как из одноатомных, так и из многоатомных ионов. Ионные кристаллы I типа - кристаллы галогенидов щелочных и щелочно-земельных металлов; анионы располагаются по закону плотнейшей шаровой упаковки, катионы занимают соответствующие пустоты. Наиболее характерные структуры такого типа - Na. Cl, Cs. Cl, Ca. F 2. Ионные кристаллы II типа построены из одноатомных катионов тех же металлов и конечных или бесконечных анионных фрагментов. Конечные анионы (кислотные остатки) - NO 3 -, SO 42 -, СО 32 - и др. кислотные остатки могут соединяться в бесконечные цепи, слои или образовывать трехмерный каркас, в полостях которого располагаются катионы.
Ионный кристалл Ионные кристаллы могут быть построены как из одноатомных, так и из многоатомных ионов. Ионные кристаллы I типа - кристаллы галогенидов щелочных и щелочно-земельных металлов; анионы располагаются по закону плотнейшей шаровой упаковки, катионы занимают соответствующие пустоты. Наиболее характерные структуры такого типа - Na. Cl, Cs. Cl, Ca. F 2. Ионные кристаллы II типа построены из одноатомных катионов тех же металлов и конечных или бесконечных анионных фрагментов. Конечные анионы (кислотные остатки) - NO 3 -, SO 42 -, СО 32 - и др. кислотные остатки могут соединяться в бесконечные цепи, слои или образовывать трехмерный каркас, в полостях которого располагаются катионы.
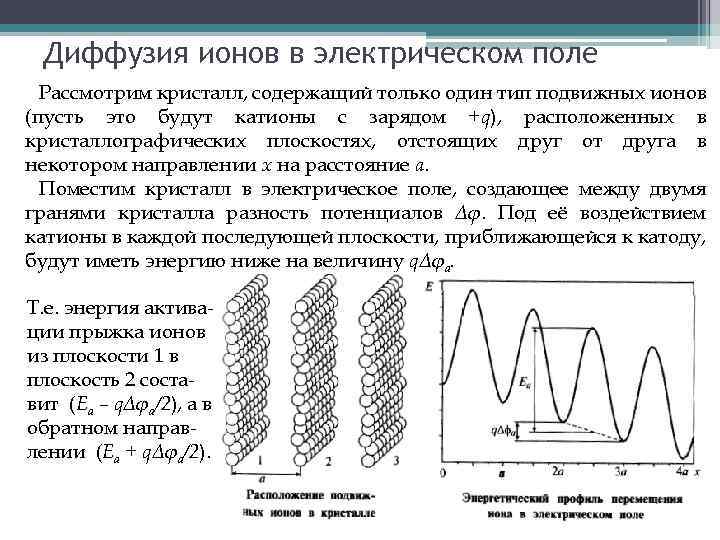 Диффузия ионов в электрическом поле Рассмотрим кристалл, содержащий только один тип подвижных ионов (пусть это будут катионы с зарядом +q), расположенных в кристаллографических плоскостях, отстоящих друг от друга в некотором направлении х на расстояние а. Поместим кристалл в электрическое поле, создающее между двумя гранями кристалла разность потенциалов Δφ. Под её воздействием катионы в каждой последующей плоскости, приближающейся к катоду, будут иметь энергию ниже на величину qΔφа. Т. е. энергия активации прыжка ионов из плоскости 1 в плоскость 2 составит (Ea – qΔφа/2), а в обратном направлении (Ea + qΔφа/2).
Диффузия ионов в электрическом поле Рассмотрим кристалл, содержащий только один тип подвижных ионов (пусть это будут катионы с зарядом +q), расположенных в кристаллографических плоскостях, отстоящих друг от друга в некотором направлении х на расстояние а. Поместим кристалл в электрическое поле, создающее между двумя гранями кристалла разность потенциалов Δφ. Под её воздействием катионы в каждой последующей плоскости, приближающейся к катоду, будут иметь энергию ниже на величину qΔφа. Т. е. энергия активации прыжка ионов из плоскости 1 в плоскость 2 составит (Ea – qΔφа/2), а в обратном направлении (Ea + qΔφа/2).
 Диффузия ионов в электрическом поле Тогда поток ионов через сечение S составит (C – объемная концентрация носителей заряда, а v 0 – предэкспоненциальный множитель соотношения, определяющего частоту их прыжков): Т. к. кристалл является однородным, то падение напряжения по его длине будет происходить линейно и Δφа = aΔφа/l (l – длина кристалла в направлении x). Т. к. число плоскостей в кристалле велико, то выигрыш в энергии при переносе между ними чаще всего очень мал по сравнению с Ea и k. T. Поэтому можно допустить, что: Т. о. получаем:
Диффузия ионов в электрическом поле Тогда поток ионов через сечение S составит (C – объемная концентрация носителей заряда, а v 0 – предэкспоненциальный множитель соотношения, определяющего частоту их прыжков): Т. к. кристалл является однородным, то падение напряжения по его длине будет происходить линейно и Δφа = aΔφа/l (l – длина кристалла в направлении x). Т. к. число плоскостей в кристалле велико, то выигрыш в энергии при переносе между ними чаще всего очень мал по сравнению с Ea и k. T. Поэтому можно допустить, что: Т. о. получаем:
 Диффузия ионов в электрическом поле Из этого можно заключить, что удельная электропроводность кристалла в направлении x составит: Первый сомножитель (Cq) представляет собой удельный заряд носителей электричества на единицу объема, а второй их подвижность u = (a 2 v 0/k. T)exp(-Ea/k. T). При отсутствии взаимодействия между частицами ионная подвижность связана с величиной коэффициента диффузии соотношением Нернста-Эйнштейна: u = q. D/k. T. Т. е. Уравнение для удельной электропроводности чаще всего используют в упрощенном виде (Eσ – энергия активации подвижности). Это соотношение называют уравнением Френкеля.
Диффузия ионов в электрическом поле Из этого можно заключить, что удельная электропроводность кристалла в направлении x составит: Первый сомножитель (Cq) представляет собой удельный заряд носителей электричества на единицу объема, а второй их подвижность u = (a 2 v 0/k. T)exp(-Ea/k. T). При отсутствии взаимодействия между частицами ионная подвижность связана с величиной коэффициента диффузии соотношением Нернста-Эйнштейна: u = q. D/k. T. Т. е. Уравнение для удельной электропроводности чаще всего используют в упрощенном виде (Eσ – энергия активации подвижности). Это соотношение называют уравнением Френкеля.
 Диффузия ионов в электрическом поле В большинстве ионных кристаллов можно выделить одни тип ионов, обладающих значительно большей подвижностью по сравнению с другими. Поэтому твердые электролиты часто считают униполярными. Тем не менее, к твердым электролитам также применяют понятие числа переноса (t+ и t-). Как правило, t+ обычно сильно превышает t-. Также, как и для жидких электролитов числа переноса сильно зависят от температуры. Таким образом можно заключить, что в большинстве твердых электролитов преобладает катионная проводимость. Анионная же доминирует лишь в немногих структурах (например, флюоритоподобные кристаллы Ca. F 2, Pb. F 2, Zr. O 2 и т. д. ), а которых имеется компактный анион и сравнительно большой катион с большим зарядом.
Диффузия ионов в электрическом поле В большинстве ионных кристаллов можно выделить одни тип ионов, обладающих значительно большей подвижностью по сравнению с другими. Поэтому твердые электролиты часто считают униполярными. Тем не менее, к твердым электролитам также применяют понятие числа переноса (t+ и t-). Как правило, t+ обычно сильно превышает t-. Также, как и для жидких электролитов числа переноса сильно зависят от температуры. Таким образом можно заключить, что в большинстве твердых электролитов преобладает катионная проводимость. Анионная же доминирует лишь в немногих структурах (например, флюоритоподобные кристаллы Ca. F 2, Pb. F 2, Zr. O 2 и т. д. ), а которых имеется компактный анион и сравнительно большой катион с большим зарядом.
 Основные закономерности переноса ионов в кристаллах Подавляющее большинство твердых ионных соединений при комнатной температуре обладает ионной проводимостью порядка 10 -10 – 10 -14 См/см. И даже вблизи температуры плавления она остается невысокой. Однако за последние 40 лет открыт не один десяток соединений ионная проводимость которых уже при сравнительно невысоких температурах достигает 10 -3 – 1 См/см. Характерным признаком таких соединений является очень высокая концентрация носителей заряда – до 1018 см-3. Материалы, обладающие высокой ионной проводимостью, назвали суперионными проводниками (superionic conductors). Суперионная проводимость — очень высокая ионная электропроводность в ионных кристаллах, сравнимая с электропроводностью жидких электролитов, основанная на легкой миграции ионов по всей кристаллической решетке.
Основные закономерности переноса ионов в кристаллах Подавляющее большинство твердых ионных соединений при комнатной температуре обладает ионной проводимостью порядка 10 -10 – 10 -14 См/см. И даже вблизи температуры плавления она остается невысокой. Однако за последние 40 лет открыт не один десяток соединений ионная проводимость которых уже при сравнительно невысоких температурах достигает 10 -3 – 1 См/см. Характерным признаком таких соединений является очень высокая концентрация носителей заряда – до 1018 см-3. Материалы, обладающие высокой ионной проводимостью, назвали суперионными проводниками (superionic conductors). Суперионная проводимость — очень высокая ионная электропроводность в ионных кристаллах, сравнимая с электропроводностью жидких электролитов, основанная на легкой миграции ионов по всей кристаллической решетке.
 Основные закономерности переноса ионов в кристаллах Поиск новых твердых электролитов привел к открытию некоторых соединений с каркасной структурой, имеющих высокую подвижность катионов. Одним из наиболее интересных и потенциально полезных соединений является Na 3 Zr 2 PSi 2 O 12, названный его создателями (Хопг, Кафалас и Гуденаф) NASICON (от англ. Na Super. Ionic CONductor). Структурный каркас NASICON образован сочленением вершин октаэдров Zr. O 6 и тетраэдров (Р, Si)О 4, при этом образуется трехмерная сеть каналов, в которых располагаются ионы Na+. Натриевая проводимость NASICON сравнима по уровню с проводимостью βглинозема.
Основные закономерности переноса ионов в кристаллах Поиск новых твердых электролитов привел к открытию некоторых соединений с каркасной структурой, имеющих высокую подвижность катионов. Одним из наиболее интересных и потенциально полезных соединений является Na 3 Zr 2 PSi 2 O 12, названный его создателями (Хопг, Кафалас и Гуденаф) NASICON (от англ. Na Super. Ionic CONductor). Структурный каркас NASICON образован сочленением вершин октаэдров Zr. O 6 и тетраэдров (Р, Si)О 4, при этом образуется трехмерная сеть каналов, в которых располагаются ионы Na+. Натриевая проводимость NASICON сравнима по уровню с проводимостью βглинозема.
 Основные закономерности переноса ионов в кристаллах
Основные закономерности переноса ионов в кристаллах
 Основные закономерности переноса ионов в кристаллах Так для соединения Li. Zr 2(PO 4)3 со структурой НАСИКОН могут быть получены две структурные модификации. В низкотемпературной триклинной модификации ионы лития распределены и однозначно локализованы. Как следствие, высокой ионной проводимости для нее не наблюдается. В высокотемпературной ромбоэдрической модификации с использованием метода дифракции нейтронов удалось локализовать только 70% ионов лития, в то время как оставшиеся 30% оказались делокализованы в каналах проводимости. Т. е. можно заключить, что в суперионных проводниках одна из подрешеток – анионная или катионная - остается твердой, а другая переходит в «квазижидкое» , высокоподвижное, неупорядоченное состояние. Как правило, величина электропроводности этих соединений вполне сопоставима с таковой для расплавов.
Основные закономерности переноса ионов в кристаллах Так для соединения Li. Zr 2(PO 4)3 со структурой НАСИКОН могут быть получены две структурные модификации. В низкотемпературной триклинной модификации ионы лития распределены и однозначно локализованы. Как следствие, высокой ионной проводимости для нее не наблюдается. В высокотемпературной ромбоэдрической модификации с использованием метода дифракции нейтронов удалось локализовать только 70% ионов лития, в то время как оставшиеся 30% оказались делокализованы в каналах проводимости. Т. е. можно заключить, что в суперионных проводниках одна из подрешеток – анионная или катионная - остается твердой, а другая переходит в «квазижидкое» , высокоподвижное, неупорядоченное состояние. Как правило, величина электропроводности этих соединений вполне сопоставима с таковой для расплавов.
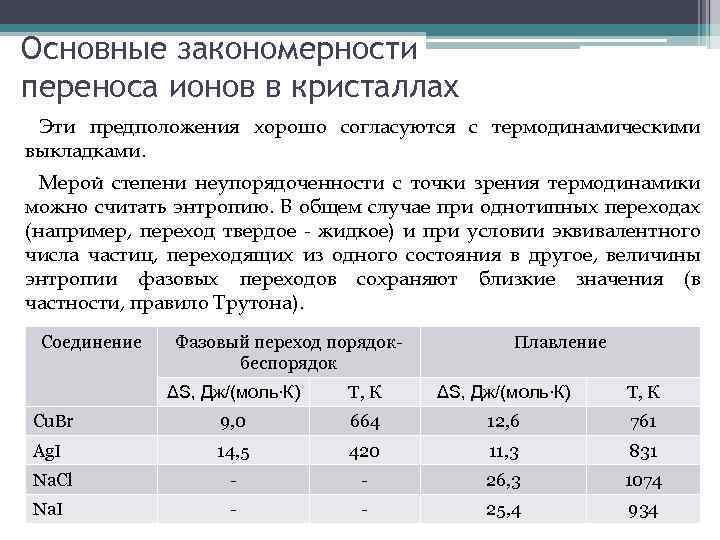 Основные закономерности переноса ионов в кристаллах Эти предположения хорошо согласуются с термодинамическими выкладками. Мерой степени неупорядоченности с точки зрения термодинамики можно считать энтропию. В общем случае при однотипных переходах (например, переход твердое - жидкое) и при условии эквивалентного числа частиц, переходящих из одного состояния в другое, величины энтропии фазовых переходов сохраняют близкие значения (в частности, правило Трутона). Соединение Фазовый переход порядокбеспорядок Плавление ΔS, Дж/(моль∙К) Т, К Cu. Br 9, 0 664 12, 6 761 Ag. I 14, 5 420 11, 3 831 Na. Cl - - 26, 3 1074 Na. I - - 25, 4 934
Основные закономерности переноса ионов в кристаллах Эти предположения хорошо согласуются с термодинамическими выкладками. Мерой степени неупорядоченности с точки зрения термодинамики можно считать энтропию. В общем случае при однотипных переходах (например, переход твердое - жидкое) и при условии эквивалентного числа частиц, переходящих из одного состояния в другое, величины энтропии фазовых переходов сохраняют близкие значения (в частности, правило Трутона). Соединение Фазовый переход порядокбеспорядок Плавление ΔS, Дж/(моль∙К) Т, К Cu. Br 9, 0 664 12, 6 761 Ag. I 14, 5 420 11, 3 831 Na. Cl - - 26, 3 1074 Na. I - - 25, 4 934
 Основные закономерности переноса ионов в кристаллах Каким требованиям должно удовлетворять соединение, чтобы входящие в его состав ионы могли проявлять высокую подвижность? Ионы – носители заряда: • слабая связь в решетке; • способность проникать через грани координационных полиэдров с небольшим сечением. А значит ионы должны иметь: • малый заряд; • относительно малый радиус. На ранних этапах исследования ионной проводимости считали, что она может быть присуща только двум «магическим» ионам – одновалентным меди и серебру (радиус ок. 0, 1 нм)
Основные закономерности переноса ионов в кристаллах Каким требованиям должно удовлетворять соединение, чтобы входящие в его состав ионы могли проявлять высокую подвижность? Ионы – носители заряда: • слабая связь в решетке; • способность проникать через грани координационных полиэдров с небольшим сечением. А значит ионы должны иметь: • малый заряд; • относительно малый радиус. На ранних этапах исследования ионной проводимости считали, что она может быть присуща только двум «магическим» ионам – одновалентным меди и серебру (радиус ок. 0, 1 нм)
 Основные закономерности переноса ионов в кристаллах Более крупные катионы также могут переходить в суперионное состояние, но только при наличии в структуре крупных каналов и, как правило, при высоких температурах. Так, например, для некоторых систем на основе феррита рубидия при 1000 К проводимость превышает 0, 1 См/см. В суперионное состояние могут переходить и двухвалентные катионы, но, как правило, проводимость таких систем не превышает 10 -3 См/см даже при высоких температурах. Высокая ионная проводимость по анионам проявляется лишь для самых малых из них и то только при высоких температурах (F- - R = 0, 136 нм, O 2 - - R = 0, 14 нм).
Основные закономерности переноса ионов в кристаллах Более крупные катионы также могут переходить в суперионное состояние, но только при наличии в структуре крупных каналов и, как правило, при высоких температурах. Так, например, для некоторых систем на основе феррита рубидия при 1000 К проводимость превышает 0, 1 См/см. В суперионное состояние могут переходить и двухвалентные катионы, но, как правило, проводимость таких систем не превышает 10 -3 См/см даже при высоких температурах. Высокая ионная проводимость по анионам проявляется лишь для самых малых из них и то только при высоких температурах (F- - R = 0, 136 нм, O 2 - - R = 0, 14 нм).
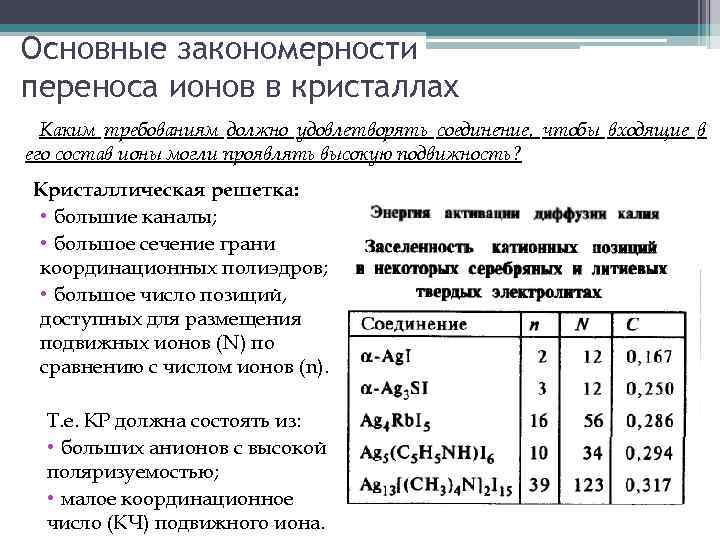 Основные закономерности переноса ионов в кристаллах Каким требованиям должно удовлетворять соединение, чтобы входящие в его состав ионы могли проявлять высокую подвижность? Кристаллическая решетка: • большие каналы; • большое сечение грани координационных полиэдров; • большое число позиций, доступных для размещения подвижных ионов (N) по сравнению с числом ионов (n). Т. е. КР должна состоять из: • больших анионов с высокой поляризуемостью; • малое координационное число (КЧ) подвижного иона.
Основные закономерности переноса ионов в кристаллах Каким требованиям должно удовлетворять соединение, чтобы входящие в его состав ионы могли проявлять высокую подвижность? Кристаллическая решетка: • большие каналы; • большое сечение грани координационных полиэдров; • большое число позиций, доступных для размещения подвижных ионов (N) по сравнению с числом ионов (n). Т. е. КР должна состоять из: • больших анионов с высокой поляризуемостью; • малое координационное число (КЧ) подвижного иона.
 Ионная проводимость твердых растворов Высокая проводимость Высокая подвижность носителей заряда Высокая концентрация носителей электричества Т. е. изменяя концентрацию носителей заряда (заряженных дефектов) можно значительно увеличить ионную проводимость ряда материалов. В качестве примера рассмотрим кристалл хлорида натрия, легированный малым количеством хлорида магния. Если пренебречь ассоциацией дефектов, то можно считать, что концентрация натриевых вакансий будет точно равна концентрации примеси.
Ионная проводимость твердых растворов Высокая проводимость Высокая подвижность носителей заряда Высокая концентрация носителей электричества Т. е. изменяя концентрацию носителей заряда (заряженных дефектов) можно значительно увеличить ионную проводимость ряда материалов. В качестве примера рассмотрим кристалл хлорида натрия, легированный малым количеством хлорида магния. Если пренебречь ассоциацией дефектов, то можно считать, что концентрация натриевых вакансий будет точно равна концентрации примеси.
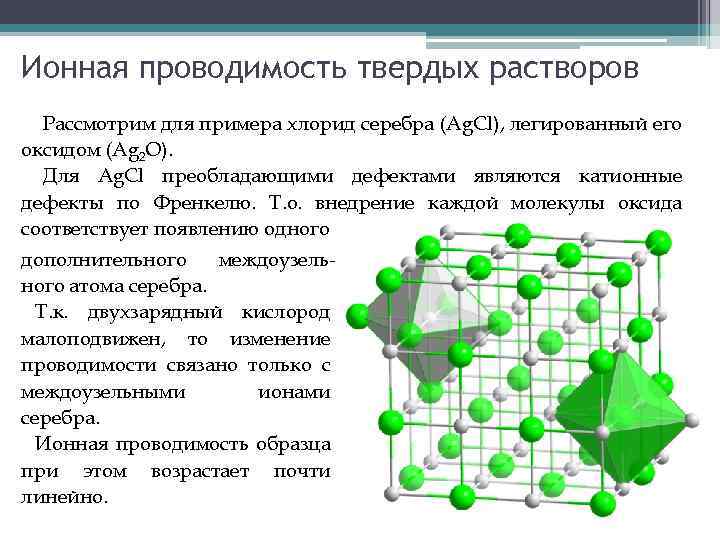 Ионная проводимость твердых растворов Рассмотрим для примера хлорид серебра (Ag. Cl), легированный его оксидом (Ag 2 O). Для Ag. Cl преобладающими дефектами являются катионные дефекты по Френкелю. Т. о. внедрение каждой молекулы оксида соответствует появлению одного дополнительного междоузельного атома серебра. Т. к. двухзарядный кислород малоподвижен, то изменение проводимости связано только с междоузельными ионами серебра. Ионная проводимость образца при этом возрастает почти линейно.
Ионная проводимость твердых растворов Рассмотрим для примера хлорид серебра (Ag. Cl), легированный его оксидом (Ag 2 O). Для Ag. Cl преобладающими дефектами являются катионные дефекты по Френкелю. Т. о. внедрение каждой молекулы оксида соответствует появлению одного дополнительного междоузельного атома серебра. Т. к. двухзарядный кислород малоподвижен, то изменение проводимости связано только с междоузельными ионами серебра. Ионная проводимость образца при этом возрастает почти линейно.
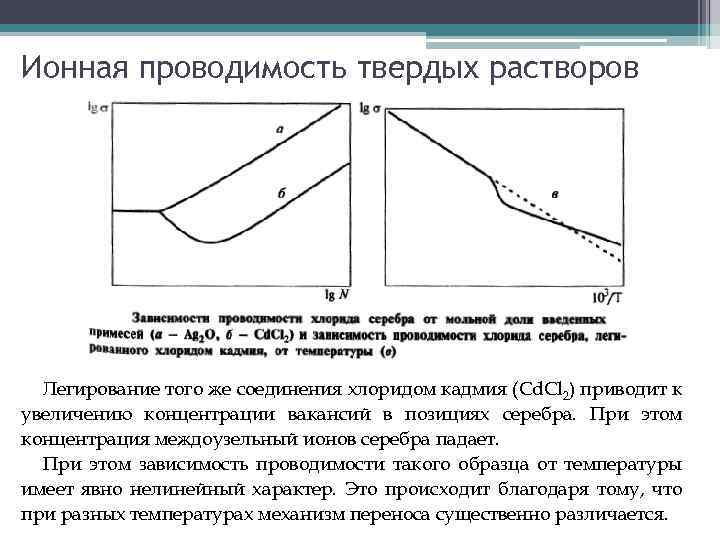 Ионная проводимость твердых растворов Легирование того же соединения хлоридом кадмия (Cd. Cl 2) приводит к увеличению концентрации вакансий в позициях серебра. При этом концентрация междоузельный ионов серебра падает. При этом зависимость проводимости такого образца от температуры имеет явно нелинейный характер. Это происходит благодаря тому, что при разных температурах механизм переноса существенно различается.
Ионная проводимость твердых растворов Легирование того же соединения хлоридом кадмия (Cd. Cl 2) приводит к увеличению концентрации вакансий в позициях серебра. При этом концентрация междоузельный ионов серебра падает. При этом зависимость проводимости такого образца от температуры имеет явно нелинейный характер. Это происходит благодаря тому, что при разных температурах механизм переноса существенно различается.
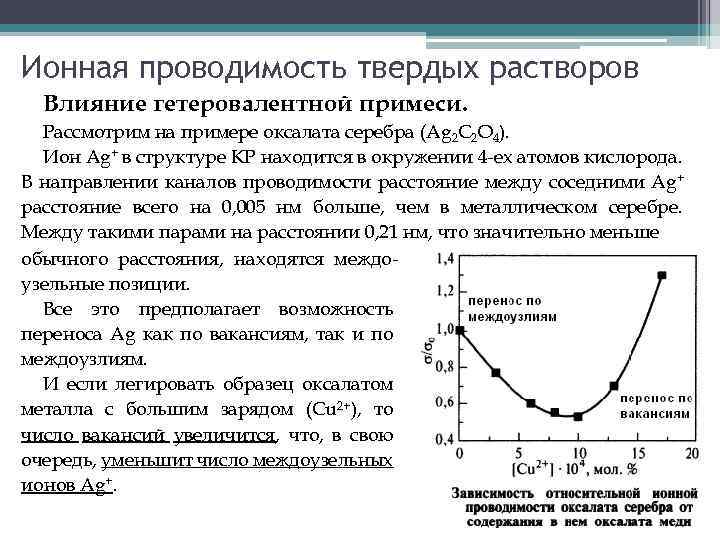 Ионная проводимость твердых растворов Влияние гетеровалентной примеси. Рассмотрим на примере оксалата серебра (Ag 2 C 2 O 4). Ион Ag+ в структуре КР находится в окружении 4 -ех атомов кислорода. В направлении каналов проводимости расстояние между соседними Ag+ расстояние всего на 0, 005 нм больше, чем в металлическом серебре. Между такими парами на расстоянии 0, 21 нм, что значительно меньше обычного расстояния, находятся междоузельные позиции. Все это предполагает возможность переноса Ag как по вакансиям, так и по междоузлиям. И если легировать образец оксалатом металла с большим зарядом (Cu 2+), то число вакансий увеличится, что, в свою очередь, уменьшит число междоузельных ионов Ag+.
Ионная проводимость твердых растворов Влияние гетеровалентной примеси. Рассмотрим на примере оксалата серебра (Ag 2 C 2 O 4). Ион Ag+ в структуре КР находится в окружении 4 -ех атомов кислорода. В направлении каналов проводимости расстояние между соседними Ag+ расстояние всего на 0, 005 нм больше, чем в металлическом серебре. Между такими парами на расстоянии 0, 21 нм, что значительно меньше обычного расстояния, находятся междоузельные позиции. Все это предполагает возможность переноса Ag как по вакансиям, так и по междоузлиям. И если легировать образец оксалатом металла с большим зарядом (Cu 2+), то число вакансий увеличится, что, в свою очередь, уменьшит число междоузельных ионов Ag+.
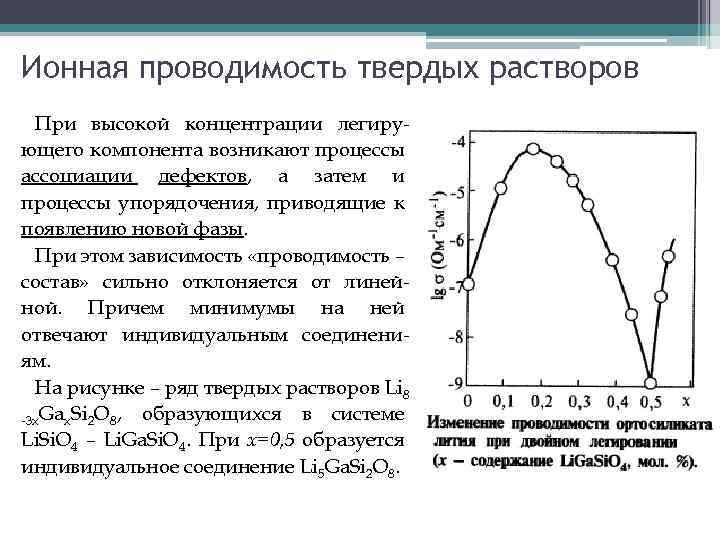 Ионная проводимость твердых растворов При высокой концентрации легирующего компонента возникают процессы ассоциации дефектов, а затем и процессы упорядочения, приводящие к появлению новой фазы. При этом зависимость «проводимость – состав» сильно отклоняется от линейной. Причем минимумы на ней отвечают индивидуальным соединениям. На рисунке – ряд твердых растворов Li 8 образующихся в системе -3 x. Gax. Si 2 O 8, Li. Si. O 4 – Li. Ga. Si. O 4. При х=0, 5 образуется индивидуальное соединение Li 5 Ga. Si 2 O 8.
Ионная проводимость твердых растворов При высокой концентрации легирующего компонента возникают процессы ассоциации дефектов, а затем и процессы упорядочения, приводящие к появлению новой фазы. При этом зависимость «проводимость – состав» сильно отклоняется от линейной. Причем минимумы на ней отвечают индивидуальным соединениям. На рисунке – ряд твердых растворов Li 8 образующихся в системе -3 x. Gax. Si 2 O 8, Li. Si. O 4 – Li. Ga. Si. O 4. При х=0, 5 образуется индивидуальное соединение Li 5 Ga. Si 2 O 8.
 Ионная проводимость твердых растворов Самый простой случай – легирование кристалла соединением той же валентности, причем, образующим с ним твердый раствор. Пусть AY и BY формируют непрерывный ряд твердых растворов состава Ax. B 1 -x. Y (где А+ и В+ способны перемещаться по кристаллу, а Y образует трехмерно связанный остов). В таком случае замена А+ на В+ должна приводить к слабой деформации остова и малым изменениям подвижности катионов. Суммарная проводимость будет складываться из проводимостей по катионам. Т. е. σ будет линейно зависеть от х. Но если катионная подвижность одномерна, т. е. совершается вдоль упорядоченно ориентированных каналов, то введение даже небольшого количества примеси с малой подвижностью значительно снизит проводимость.
Ионная проводимость твердых растворов Самый простой случай – легирование кристалла соединением той же валентности, причем, образующим с ним твердый раствор. Пусть AY и BY формируют непрерывный ряд твердых растворов состава Ax. B 1 -x. Y (где А+ и В+ способны перемещаться по кристаллу, а Y образует трехмерно связанный остов). В таком случае замена А+ на В+ должна приводить к слабой деформации остова и малым изменениям подвижности катионов. Суммарная проводимость будет складываться из проводимостей по катионам. Т. е. σ будет линейно зависеть от х. Но если катионная подвижность одномерна, т. е. совершается вдоль упорядоченно ориентированных каналов, то введение даже небольшого количества примеси с малой подвижностью значительно снизит проводимость.
 Ионная проводимость твердых растворов Стоит отметить также, что в реальных системах при введении легирующей добавки подвижность носителей заряда изменяется в зависимости от состава твердого раствора, что приводит к нелинейности изменения проводимости. Такие изменения происходят, например, при последовательном замещении одного подвижного катиона на другой в разного рода стеклах. Для большинства случаев эта зависимость проходит через минимум. Проводимость по каждому из катионов существенно понижается с уменьшением его содержания. Причем степень понижения тем больше, чем выше разница радиусов.
Ионная проводимость твердых растворов Стоит отметить также, что в реальных системах при введении легирующей добавки подвижность носителей заряда изменяется в зависимости от состава твердого раствора, что приводит к нелинейности изменения проводимости. Такие изменения происходят, например, при последовательном замещении одного подвижного катиона на другой в разного рода стеклах. Для большинства случаев эта зависимость проходит через минимум. Проводимость по каждому из катионов существенно понижается с уменьшением его содержания. Причем степень понижения тем больше, чем выше разница радиусов.
 Ионная проводимость твердых растворов Это происходит потому, что при смешанном катионном составе координационные полиэдры имеют разный размер. Т. е. при перемещении катиона одного типа образовавшаяся вакансия (координационный полиэдр) должна несколько перестроиться для катиона другого типа, что требует времени и, в конечном итоге, снижает суммарную проводимость. К тому же вероятность образования вакансии нужного размера в непосредственной близости довольно мала. Подобная нелинейная, проходящая через минимум зависимость проводимости от состава в случае соединений щелочных металлов получила название полищелочного эффекта. С ростом температуры влияние этого эффекта снижается.
Ионная проводимость твердых растворов Это происходит потому, что при смешанном катионном составе координационные полиэдры имеют разный размер. Т. е. при перемещении катиона одного типа образовавшаяся вакансия (координационный полиэдр) должна несколько перестроиться для катиона другого типа, что требует времени и, в конечном итоге, снижает суммарную проводимость. К тому же вероятность образования вакансии нужного размера в непосредственной близости довольно мала. Подобная нелинейная, проходящая через минимум зависимость проводимости от состава в случае соединений щелочных металлов получила название полищелочного эффекта. С ростом температуры влияние этого эффекта снижается.
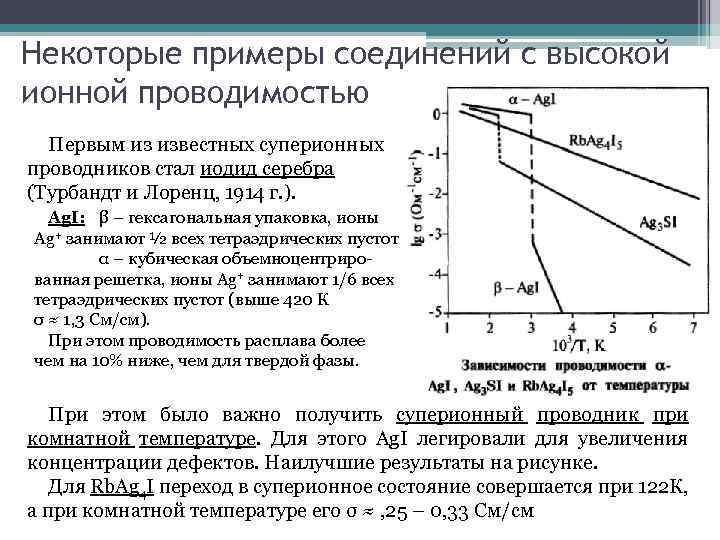 Некоторые примеры соединений с высокой ионной проводимостью Первым из известных суперионных проводников стал иодид серебра (Турбандт и Лоренц, 1914 г. ). Ag. I: β – гексагональная упаковка, ионы Ag+ занимают ½ всех тетраэдрических пустот α – кубическая объемноцентрированная решетка, ионы Ag+ занимают 1/6 всех тетраэдрических пустот (выше 420 К σ ≈ 1, 3 См/см). При этом проводимость расплава более чем на 10% ниже, чем для твердой фазы. При этом было важно получить суперионный проводник при комнатной температуре. Для этого Ag. I легировали для увеличения концентрации дефектов. Наилучшие результаты на рисунке. Для Rb. Ag 4 I переход в суперионное состояние совершается при 122 К, а при комнатной температуре его σ ≈ , 25 – 0, 33 См/см
Некоторые примеры соединений с высокой ионной проводимостью Первым из известных суперионных проводников стал иодид серебра (Турбандт и Лоренц, 1914 г. ). Ag. I: β – гексагональная упаковка, ионы Ag+ занимают ½ всех тетраэдрических пустот α – кубическая объемноцентрированная решетка, ионы Ag+ занимают 1/6 всех тетраэдрических пустот (выше 420 К σ ≈ 1, 3 См/см). При этом проводимость расплава более чем на 10% ниже, чем для твердой фазы. При этом было важно получить суперионный проводник при комнатной температуре. Для этого Ag. I легировали для увеличения концентрации дефектов. Наилучшие результаты на рисунке. Для Rb. Ag 4 I переход в суперионное состояние совершается при 122 К, а при комнатной температуре его σ ≈ , 25 – 0, 33 См/см
 Некоторые примеры соединений с высокой ионной проводимостью Для одновалентной меди (имеющей сходное с серебром строение электронных оболочек) описан сходный с соединениями серебра набор твердых электролитов. Но для меди характерны более низкие значения проводимости в связи с существенно более меньшим радиусом катиона.
Некоторые примеры соединений с высокой ионной проводимостью Для одновалентной меди (имеющей сходное с серебром строение электронных оболочек) описан сходный с соединениями серебра набор твердых электролитов. Но для меди характерны более низкие значения проводимости в связи с существенно более меньшим радиусом катиона.
 Некоторые примеры соединений с высокой ионной проводимостью Для конструирования источников тока принципиальное значение имеет величина окислительно-восстановительного потенциала, характеризующего переход ионов из металла в ионный кристалл. Использование серебро- и медьпроводящих электролитов позволяет получать источники тока с весьма низким напряжением. В этом плане от них выгодно отличаются системы, обладающие проводимостью по ионам натрия и лития.
Некоторые примеры соединений с высокой ионной проводимостью Для конструирования источников тока принципиальное значение имеет величина окислительно-восстановительного потенциала, характеризующего переход ионов из металла в ионный кристалл. Использование серебро- и медьпроводящих электролитов позволяет получать источники тока с весьма низким напряжением. В этом плане от них выгодно отличаются системы, обладающие проводимостью по ионам натрия и лития.
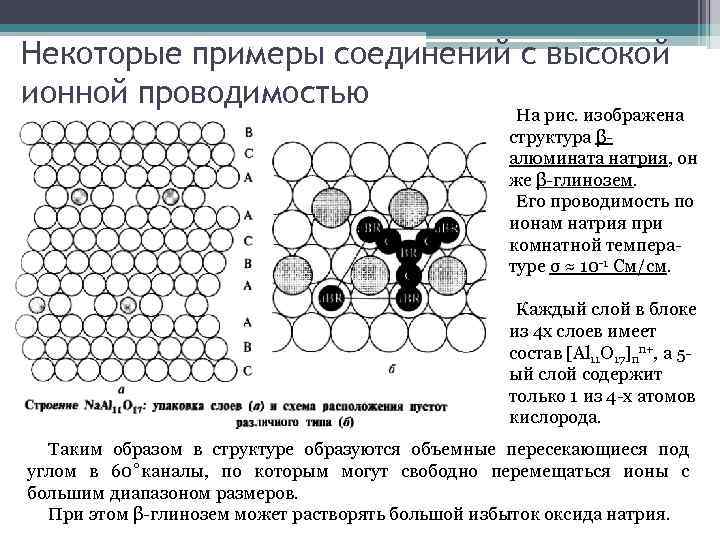 Некоторые примеры соединений с высокой ионной проводимостью На рис. изображена структура βалюмината натрия, он же β-глинозем. Его проводимость по ионам натрия при комнатной температуре σ ≈ 10 -1 См/см. Каждый слой в блоке из 4 х слоев имеет состав [Al 11 O 17]nn+, а 5 ый слой содержит только 1 из 4 -х атомов кислорода. Таким образом в структуре образуются объемные пересекающиеся под углом в 60˚каналы, по которым могут свободно перемещаться ионы с большим диапазоном размеров. При этом β-глинозем может растворять большой избыток оксида натрия.
Некоторые примеры соединений с высокой ионной проводимостью На рис. изображена структура βалюмината натрия, он же β-глинозем. Его проводимость по ионам натрия при комнатной температуре σ ≈ 10 -1 См/см. Каждый слой в блоке из 4 х слоев имеет состав [Al 11 O 17]nn+, а 5 ый слой содержит только 1 из 4 -х атомов кислорода. Таким образом в структуре образуются объемные пересекающиеся под углом в 60˚каналы, по которым могут свободно перемещаться ионы с большим диапазоном размеров. При этом β-глинозем может растворять большой избыток оксида натрия.
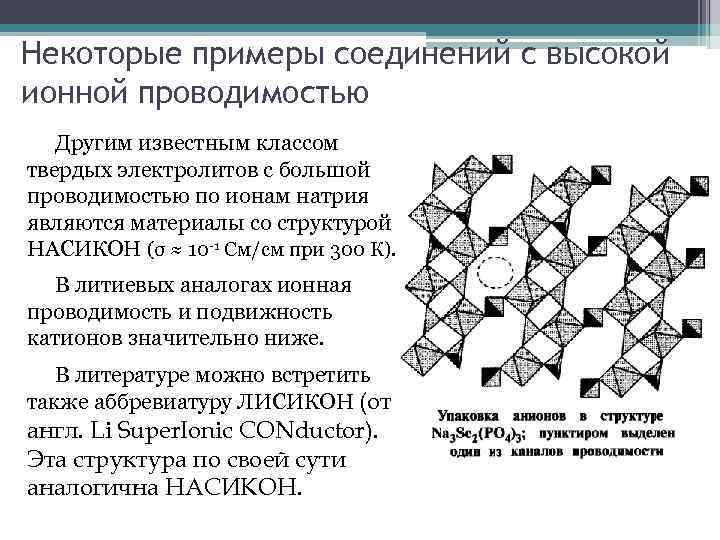 Некоторые примеры соединений с высокой ионной проводимостью Другим известным классом твердых электролитов с большой проводимостью по ионам натрия являются материалы со структурой НАСИКОН (σ ≈ 10 -1 См/см при 300 К). В литиевых аналогах ионная проводимость и подвижность катионов значительно ниже. В литературе можно встретить также аббревиатуру ЛИСИКОН (от англ. Li Super. Ionic CONductor). Эта структура по своей сути аналогична НАСИКОН.
Некоторые примеры соединений с высокой ионной проводимостью Другим известным классом твердых электролитов с большой проводимостью по ионам натрия являются материалы со структурой НАСИКОН (σ ≈ 10 -1 См/см при 300 К). В литиевых аналогах ионная проводимость и подвижность катионов значительно ниже. В литературе можно встретить также аббревиатуру ЛИСИКОН (от англ. Li Super. Ionic CONductor). Эта структура по своей сути аналогична НАСИКОН.
 Механизм перехода вещества в суперионное состояние Переход ионного кристалла в суперионное состояние при нагревании обусловлен структурной трансформацией кристаллической решетки. При нагревании амплитуда колебательных и вращательных движений атомов растет, но при достижении некоторой пороговой температуры дальнейшее её увеличение становится невозможным в рамках старой КР. Переход в суперионное состояние можно рассмотреть на простой модели – цепочке водородных связей.
Механизм перехода вещества в суперионное состояние Переход ионного кристалла в суперионное состояние при нагревании обусловлен структурной трансформацией кристаллической решетки. При нагревании амплитуда колебательных и вращательных движений атомов растет, но при достижении некоторой пороговой температуры дальнейшее её увеличение становится невозможным в рамках старой КР. Переход в суперионное состояние можно рассмотреть на простой модели – цепочке водородных связей.
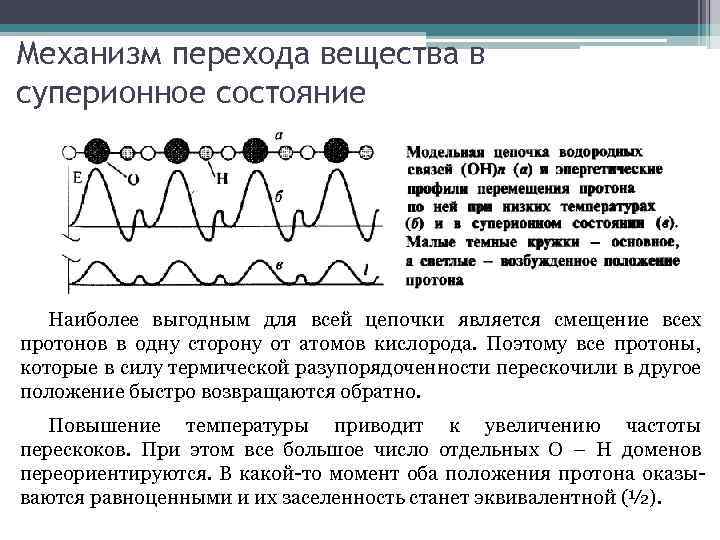 Механизм перехода вещества в суперионное состояние Наиболее выгодным для всей цепочки является смещение всех протонов в одну сторону от атомов кислорода. Поэтому все протоны, которые в силу термической разупорядоченности перескочили в другое положение быстро возвращаются обратно. Повышение температуры приводит к увеличению частоты перескоков. При этом все большое число отдельных О – Н доменов переориентируются. В какой-то момент оба положения протона оказываются равноценными и их заселенность станет эквивалентной (½).
Механизм перехода вещества в суперионное состояние Наиболее выгодным для всей цепочки является смещение всех протонов в одну сторону от атомов кислорода. Поэтому все протоны, которые в силу термической разупорядоченности перескочили в другое положение быстро возвращаются обратно. Повышение температуры приводит к увеличению частоты перескоков. При этом все большое число отдельных О – Н доменов переориентируются. В какой-то момент оба положения протона оказываются равноценными и их заселенность станет эквивалентной (½).
 Механизм перехода вещества в суперионное состояние Такая ситуация характерна и для многих других структур. Наличие в объеме вещества хотя бы одного переориентированного атома понижает энергию переориентации соседей, двух – еще больше и т. д. Но качественные изменения происходят, когда доля таких переориентаций достигает нескольких процентов. При этом материал переходит в суперионное состояние постепенно и границы раздела между разными фазами являются лабильными и мигрируют по структуре, пока весь материал не перестроится.
Механизм перехода вещества в суперионное состояние Такая ситуация характерна и для многих других структур. Наличие в объеме вещества хотя бы одного переориентированного атома понижает энергию переориентации соседей, двух – еще больше и т. д. Но качественные изменения происходят, когда доля таких переориентаций достигает нескольких процентов. При этом материал переходит в суперионное состояние постепенно и границы раздела между разными фазами являются лабильными и мигрируют по структуре, пока весь материал не перестроится.
 Механизм перехода вещества в суперионное состояние Увеличить число дефектов можно не только термически, но и путем принудительного их введения в структуру КР (легирование гетеровалентными примесями). При таком легировании изменение происходит аналогичным образом. структуры Дефекты склонны к образованию ассоциатов, которые затем переходят в отдельную фазу (чаще всего фаза, богатая дефектами - ромбоэдрическая). Критическим порогом для перехода вещества в суперионное состояние является дефектность на уровне нескольких процентов.
Механизм перехода вещества в суперионное состояние Увеличить число дефектов можно не только термически, но и путем принудительного их введения в структуру КР (легирование гетеровалентными примесями). При таком легировании изменение происходит аналогичным образом. структуры Дефекты склонны к образованию ассоциатов, которые затем переходят в отдельную фазу (чаще всего фаза, богатая дефектами - ромбоэдрическая). Критическим порогом для перехода вещества в суперионное состояние является дефектность на уровне нескольких процентов.
 Ионная проводимость стёкол и полимеров Стекла и полимеры находятся в метастабильном состоянии – в них нарушен дальний порядок, что приводит к изменениям условий переноса ионов и образования дефектов. Энергии ионов, находящихся в «узлах» и «междоузлиях» решетки существенно сближаются, поэтому концентрация дефектов в некристаллических телах значительно выше. В общем случае энергия активации каждого отдельного акта переноса может как повыситься, так и понизиться. Поэтому общая энергия активации переноса может и увеличиться. Но чаще всего она ниже, чем для кристаллов.
Ионная проводимость стёкол и полимеров Стекла и полимеры находятся в метастабильном состоянии – в них нарушен дальний порядок, что приводит к изменениям условий переноса ионов и образования дефектов. Энергии ионов, находящихся в «узлах» и «междоузлиях» решетки существенно сближаются, поэтому концентрация дефектов в некристаллических телах значительно выше. В общем случае энергия активации каждого отдельного акта переноса может как повыситься, так и понизиться. Поэтому общая энергия активации переноса может и увеличиться. Но чаще всего она ниже, чем для кристаллов.
 Ионная проводимость стёкол и полимеров Стекла и полимеры находятся в метастабильном состоянии – в них нарушен дальний порядок, что приводит к изменениям условий переноса ионов и образования дефектов. Энергии ионов, находящихся в «узлах» и «междоузлиях» решетки существенно сближаются, поэтому концентрация дефектов в некристаллических телах значительно выше. В общем случае энергия активации каждого отдельного акта переноса может как повыситься, так и понизиться. Поэтому общая энергия активации переноса может и увеличиться. Но чаще всего она ниже, чем для кристаллов.
Ионная проводимость стёкол и полимеров Стекла и полимеры находятся в метастабильном состоянии – в них нарушен дальний порядок, что приводит к изменениям условий переноса ионов и образования дефектов. Энергии ионов, находящихся в «узлах» и «междоузлиях» решетки существенно сближаются, поэтому концентрация дефектов в некристаллических телах значительно выше. В общем случае энергия активации каждого отдельного акта переноса может как повыситься, так и понизиться. Поэтому общая энергия активации переноса может и увеличиться. Но чаще всего она ниже, чем для кристаллов.
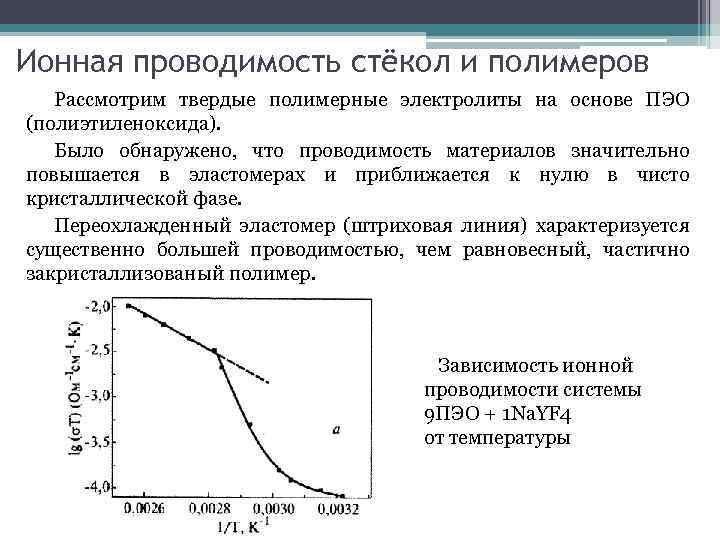 Ионная проводимость стёкол и полимеров Рассмотрим твердые полимерные электролиты на основе ПЭО (полиэтиленоксида). Было обнаружено, что проводимость материалов значительно повышается в эластомерах и приближается к нулю в чисто кристаллической фазе. Переохлажденный эластомер (штриховая линия) характеризуется существенно большей проводимостью, чем равновесный, частично закристаллизованый полимер. Зависимость ионной проводимости системы 9 ПЭО + 1 Na. YF 4 от температуры
Ионная проводимость стёкол и полимеров Рассмотрим твердые полимерные электролиты на основе ПЭО (полиэтиленоксида). Было обнаружено, что проводимость материалов значительно повышается в эластомерах и приближается к нулю в чисто кристаллической фазе. Переохлажденный эластомер (штриховая линия) характеризуется существенно большей проводимостью, чем равновесный, частично закристаллизованый полимер. Зависимость ионной проводимости системы 9 ПЭО + 1 Na. YF 4 от температуры
 Ионная проводимость стёкол и полимеров Перколяционная модель. Перескок иона из исходной позиции в следующую происходит после того, как в результате колебаний цепи в ней будет достигнуто подходящее расположение функциональных групп, участвующих в координации иона. В рамках данной теории легко объясняется кинетическая затрудненность процессов кристаллизации. Именно поэтому на политерме проводимости появляется петля гистерезиса – проводимость при нагревании в одинаковых условиях меньше, чем при охлаждении. Подобным же механизмом переноса объясняется и полищелочной эффект в стеклообразных электролитах.
Ионная проводимость стёкол и полимеров Перколяционная модель. Перескок иона из исходной позиции в следующую происходит после того, как в результате колебаний цепи в ней будет достигнуто подходящее расположение функциональных групп, участвующих в координации иона. В рамках данной теории легко объясняется кинетическая затрудненность процессов кристаллизации. Именно поэтому на политерме проводимости появляется петля гистерезиса – проводимость при нагревании в одинаковых условиях меньше, чем при охлаждении. Подобным же механизмом переноса объясняется и полищелочной эффект в стеклообразных электролитах.
 Особенности протонной проводимости Протон Элементарная частица с экстремально малым радиусом и без электронных оболочек В отличие от электрона не отталкивается от электронных оболочек атомов КР, а притягивается, причем максимально эффективно. Механизм перемещения протона в конденсированных средах кардинально отличается от механизма, присущего другим ионам и электронам
Особенности протонной проводимости Протон Элементарная частица с экстремально малым радиусом и без электронных оболочек В отличие от электрона не отталкивается от электронных оболочек атомов КР, а притягивается, причем максимально эффективно. Механизм перемещения протона в конденсированных средах кардинально отличается от механизма, присущего другим ионам и электронам
 Особенности протонной проводимости Стоит отметить, что для протонной проводимости ключевыми являются не только колебательные, но и вращательные движения водородной связи. Некоторые особенности водородной связи: В отличие от других ионов протон не может существовать в отрыве от электроотрицательных атомов • в любой момент времени протон образует ковалентную и направленную связь, причем для возможности его переноса эта связь должна иметь «+» на водороде; • Для протона наиболее типично координационное число 2 (редко 3) О–Н–О; • При ненулевых температурах возможна осцилляция протона между электроотрицательными атомами О–Н- - -О О- - -Н–О причем для коротких водородных связей она может осуществляться по туннельному механизму.
Особенности протонной проводимости Стоит отметить, что для протонной проводимости ключевыми являются не только колебательные, но и вращательные движения водородной связи. Некоторые особенности водородной связи: В отличие от других ионов протон не может существовать в отрыве от электроотрицательных атомов • в любой момент времени протон образует ковалентную и направленную связь, причем для возможности его переноса эта связь должна иметь «+» на водороде; • Для протона наиболее типично координационное число 2 (редко 3) О–Н–О; • При ненулевых температурах возможна осцилляция протона между электроотрицательными атомами О–Н- - -О О- - -Н–О причем для коротких водородных связей она может осуществляться по туннельному механизму.
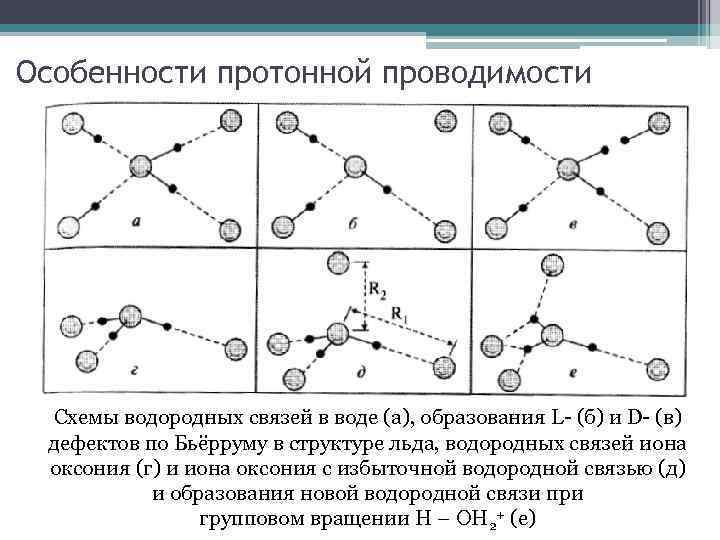 Особенности протонной проводимости Схемы водородных связей в воде (а), образования L- (б) и D- (в) дефектов по Бьёрруму в структуре льда, водородных связей иона оксония (г) и иона оксония с избыточной водородной связью (д) и образования новой водородной связи при групповом вращении Н – ОН 2+ (е)
Особенности протонной проводимости Схемы водородных связей в воде (а), образования L- (б) и D- (в) дефектов по Бьёрруму в структуре льда, водородных связей иона оксония (г) и иона оксония с избыточной водородной связью (д) и образования новой водородной связи при групповом вращении Н – ОН 2+ (е)
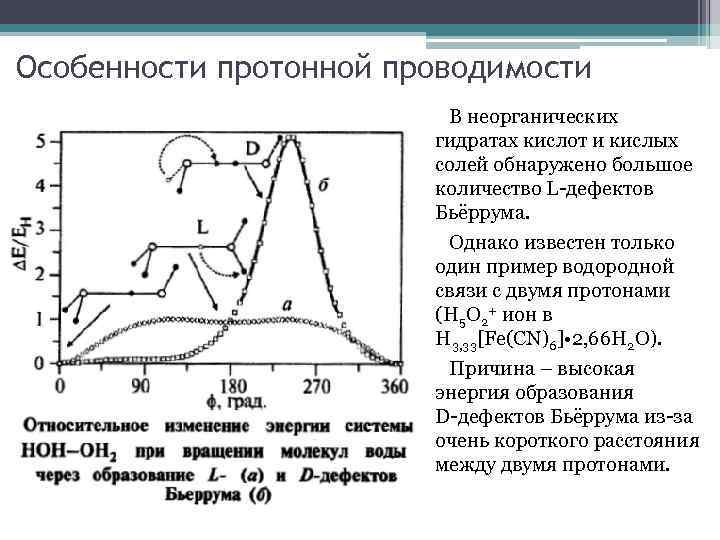 Особенности протонной проводимости В неорганических гидратах кислот и кислых солей обнаружено большое количество L-дефектов Бьёррума. Однако известен только один пример водородной связи с двумя протонами (H 5 O 2+ ион в H 3, 33[Fe(CN)6] • 2, 66 H 2 O). Причина – высокая энергия образования D-дефектов Бьёррума из-за очень короткого расстояния между двумя протонами.
Особенности протонной проводимости В неорганических гидратах кислот и кислых солей обнаружено большое количество L-дефектов Бьёррума. Однако известен только один пример водородной связи с двумя протонами (H 5 O 2+ ион в H 3, 33[Fe(CN)6] • 2, 66 H 2 O). Причина – высокая энергия образования D-дефектов Бьёррума из-за очень короткого расстояния между двумя протонами.
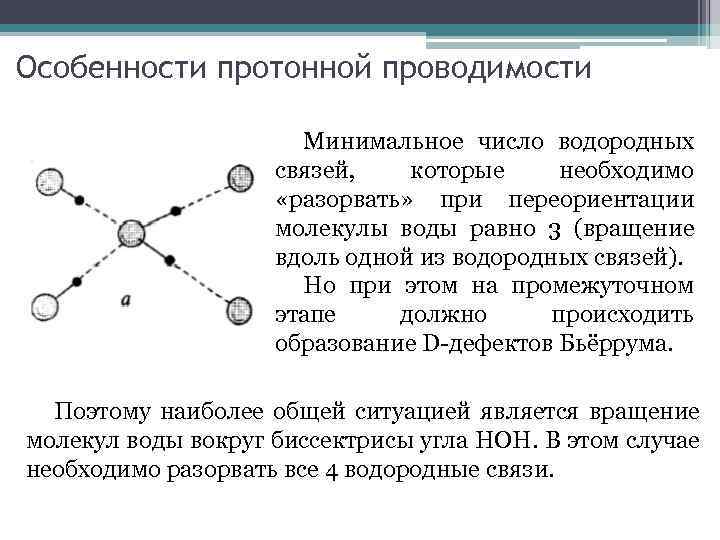 Особенности протонной проводимости Минимальное число водородных связей, которые необходимо «разорвать» при переориентации молекулы воды равно 3 (вращение вдоль одной из водородных связей). Но при этом на промежуточном этапе должно происходить образование D-дефектов Бьёррума. Поэтому наиболее общей ситуацией является вращение молекул воды вокруг биссектрисы угла НОН. В этом случае необходимо разорвать все 4 водородные связи.
Особенности протонной проводимости Минимальное число водородных связей, которые необходимо «разорвать» при переориентации молекулы воды равно 3 (вращение вдоль одной из водородных связей). Но при этом на промежуточном этапе должно происходить образование D-дефектов Бьёррума. Поэтому наиболее общей ситуацией является вращение молекул воды вокруг биссектрисы угла НОН. В этом случае необходимо разорвать все 4 водородные связи.
 Особенности протонной проводимости Чем меньше водородных связей образует молекула воды, тем выше ее вращательная подвижность, тем проще она «отдаст» протон. Увеличение концентрации ионов оксония уменьшает подвижность молекул воды вследствие увеличения энергии водородных связей. Т. о. для наибольшей подвижности протонов необходимо: высокая концентрация протонов; слабые водородные связи; низкая протонакцепторная способность анионов; высокая концентрация L-дефектов Бьёррума; кооперативность явлений. • • •
Особенности протонной проводимости Чем меньше водородных связей образует молекула воды, тем выше ее вращательная подвижность, тем проще она «отдаст» протон. Увеличение концентрации ионов оксония уменьшает подвижность молекул воды вследствие увеличения энергии водородных связей. Т. о. для наибольшей подвижности протонов необходимо: высокая концентрация протонов; слабые водородные связи; низкая протонакцепторная способность анионов; высокая концентрация L-дефектов Бьёррума; кооперативность явлений. • • •
 Особенности протонной проводимости Большинство низкотемпературных протонных проводников – это гидраты кислот и кислых солей. Увеличение числа молекул воды в них ведет к росту протонной проводимости вплоть до ее значений в водных растворах. Поэтому логично предполагать, что протонная подвижность в твердых гидратах кислот и в их водных растворах имеет сходную природу – так называемый «эстафетный механизм» . Отличие только в концентрации кислотных протонов и меньшей интенсивности колебаний в твердых телах.
Особенности протонной проводимости Большинство низкотемпературных протонных проводников – это гидраты кислот и кислых солей. Увеличение числа молекул воды в них ведет к росту протонной проводимости вплоть до ее значений в водных растворах. Поэтому логично предполагать, что протонная подвижность в твердых гидратах кислот и в их водных растворах имеет сходную природу – так называемый «эстафетный механизм» . Отличие только в концентрации кислотных протонов и меньшей интенсивности колебаний в твердых телах.
 Применение ионных проводников Иони стор (суперконденсатор, ультраконденсатор, двухслойный электрохимический конденсатор, англ. EDLC, Electric double-layer capacitor) — электрохимическое устройство, конденсатор с органическим или неорганическим электролитом, «обкладками» в котором служитдвойной электрический слой на границе раздела электрода и электролита.
Применение ионных проводников Иони стор (суперконденсатор, ультраконденсатор, двухслойный электрохимический конденсатор, англ. EDLC, Electric double-layer capacitor) — электрохимическое устройство, конденсатор с органическим или неорганическим электролитом, «обкладками» в котором служитдвойной электрический слой на границе раздела электрода и электролита.
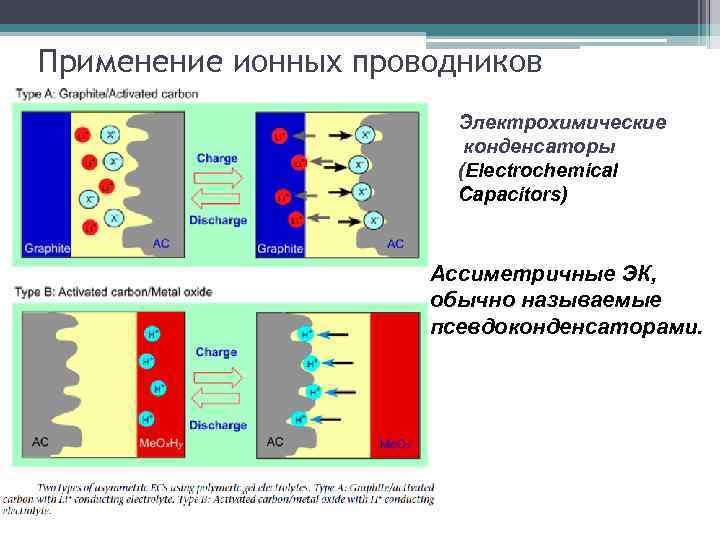 Применение ионных проводников Электрохимические конденсаторы (Electrochemical Capacitors) Ассиметричные ЭК, обычно называемые псевдоконденсаторами.
Применение ионных проводников Электрохимические конденсаторы (Electrochemical Capacitors) Ассиметричные ЭК, обычно называемые псевдоконденсаторами.
 Литература • Бокштейн Б. С. , Ярославцев А. Б. Диффузия атомов и ионов в твердых телах: – М. : МИСИС, 2005. – 362 с. • Терминологический спектр физики: Словарь/ Ин-т физики молекул и кристаллов УНЦ РАН и др. ; Под общ. ред. В. А. Мазунова; Авт. -сост. : В. А. Мазунов и др. -2 -е изд. , испр. и доп. - Уфа, 2000. - 203 с. • Вест А. Химия твердого тела. Теория и приложения: В 2 -х ч. Ч. 2 - Пер. с англ. Под редакцией академика Ю. Д. Третьякова. М. : Мир, 1988. – 336 с. • P. Padma Kumar, S. Yashonath. Structure, Conductivity and Ionic Motion in Na 1+x. Zr 2 Six. P 3 -x. O 12: A Simulation Study // J. Phys. Chem. B, 2002, V. 106, pp. 7081 -7089. • P. Padma Kumar, S. Yashonath. A Full Interionic Potential for Na 1+x. Zr 2 Six. P 3 -x. O 12 Superionic Conductors // J. Am. Chem. Soc. (Communication), 2002 , V. 124, pp. 3828 -3829. • A. Moreira dos Santos, F. M. B. Marques, L. D. Carlos, J. Rocha. Photoluminescence of lanthanide NASICONs: Na 5 Ln. Si 4 O 12, Ln = Eu, Tb. // J. Mater. Chem. , 2006, V. 16, pp. 3139 -3144.
Литература • Бокштейн Б. С. , Ярославцев А. Б. Диффузия атомов и ионов в твердых телах: – М. : МИСИС, 2005. – 362 с. • Терминологический спектр физики: Словарь/ Ин-т физики молекул и кристаллов УНЦ РАН и др. ; Под общ. ред. В. А. Мазунова; Авт. -сост. : В. А. Мазунов и др. -2 -е изд. , испр. и доп. - Уфа, 2000. - 203 с. • Вест А. Химия твердого тела. Теория и приложения: В 2 -х ч. Ч. 2 - Пер. с англ. Под редакцией академика Ю. Д. Третьякова. М. : Мир, 1988. – 336 с. • P. Padma Kumar, S. Yashonath. Structure, Conductivity and Ionic Motion in Na 1+x. Zr 2 Six. P 3 -x. O 12: A Simulation Study // J. Phys. Chem. B, 2002, V. 106, pp. 7081 -7089. • P. Padma Kumar, S. Yashonath. A Full Interionic Potential for Na 1+x. Zr 2 Six. P 3 -x. O 12 Superionic Conductors // J. Am. Chem. Soc. (Communication), 2002 , V. 124, pp. 3828 -3829. • A. Moreira dos Santos, F. M. B. Marques, L. D. Carlos, J. Rocha. Photoluminescence of lanthanide NASICONs: Na 5 Ln. Si 4 O 12, Ln = Eu, Tb. // J. Mater. Chem. , 2006, V. 16, pp. 3139 -3144.


