Ион — ионное взаимодействие в растворах электролитов Лекция































28460-ion.ppt
- Количество слайдов: 38
 Ион - ионное взаимодействие в растворах электролитов Лекция 3
Ион - ионное взаимодействие в растворах электролитов Лекция 3
 Условие равновесия в растворе электролитов Ионы находятся на больших расстояниях и взаимодействие электростатическое При увеличении концентрации электростатическое взаимодействие осложняется ион-дипольным Наличие ассоциации ионов Все виды взаимодействия описывает активность ионов в условиях наличия равновесия ассоциат-диссоциат
Условие равновесия в растворе электролитов Ионы находятся на больших расстояниях и взаимодействие электростатическое При увеличении концентрации электростатическое взаимодействие осложняется ион-дипольным Наличие ассоциации ионов Все виды взаимодействия описывает активность ионов в условиях наличия равновесия ассоциат-диссоциат
 Термодинамическое описание ион - ионного взаимодействия Всю совокупность взаимодействий, возникающих в растворах электролитов, можно формально описать, используя вместо концентраций ионов С i – активности ионов ai. Предполагается, что все термодинамические соотношения, записанные в форме уравнений для идеальных растворов, но содержащие активности, строго согласуются с результатами экспериментальных измерений. Все виды взаимодействий (за исключением изменения состава раствора) без учета их физической природы сводятся к отклонению активностей от соответствующих концентраций.
Термодинамическое описание ион - ионного взаимодействия Всю совокупность взаимодействий, возникающих в растворах электролитов, можно формально описать, используя вместо концентраций ионов С i – активности ионов ai. Предполагается, что все термодинамические соотношения, записанные в форме уравнений для идеальных растворов, но содержащие активности, строго согласуются с результатами экспериментальных измерений. Все виды взаимодействий (за исключением изменения состава раствора) без учета их физической природы сводятся к отклонению активностей от соответствующих концентраций.
 Химические потенциалы и активности
Химические потенциалы и активности
 Химический потенциал
Химический потенциал
 Химический потенциал соли
Химический потенциал соли
 Средняя активность
Средняя активность
 Средний коэффициент активности
Средний коэффициент активности
 Коэффициент симметрии электролита LiCl: L = 1 CaS: L = 1 AlPO4: L = 1 K2SO4: L =1,587 Fe(NO3)2: L =1,587 Fe(NO3)3: L =2,280 AlCl3: L =2,280 K4[Fe(CN)6]: L =3,031 Fe2(SO4)3: L =2,551
Коэффициент симметрии электролита LiCl: L = 1 CaS: L = 1 AlPO4: L = 1 K2SO4: L =1,587 Fe(NO3)2: L =1,587 Fe(NO3)3: L =2,280 AlCl3: L =2,280 K4[Fe(CN)6]: L =3,031 Fe2(SO4)3: L =2,551
 Теория сильных электролитов ( Петер Дебай и Эрих Хюккель, 1923 г.) Основные положения: 1) Электролит всегда полностью диссоциирован (α = 1). 2) Растворитель – это континуум с диэлектрической проницаемостью ε. 3) Ионы участвуют ТОЛЬКО в 2 процессах: хаотическом тепловом движении и электростатическом (кулоновском) взаимодействии друг с другом. Никакие другие процессы и взаимодействия не учитываются. Это возможно в достаточно разбавленных растворах, близких по свойствам к идеальным. 4) Ионы энергетически распределены в растворе согласно закону Больцмана.
Теория сильных электролитов ( Петер Дебай и Эрих Хюккель, 1923 г.) Основные положения: 1) Электролит всегда полностью диссоциирован (α = 1). 2) Растворитель – это континуум с диэлектрической проницаемостью ε. 3) Ионы участвуют ТОЛЬКО в 2 процессах: хаотическом тепловом движении и электростатическом (кулоновском) взаимодействии друг с другом. Никакие другие процессы и взаимодействия не учитываются. Это возможно в достаточно разбавленных растворах, близких по свойствам к идеальным. 4) Ионы энергетически распределены в растворе согласно закону Больцмана.
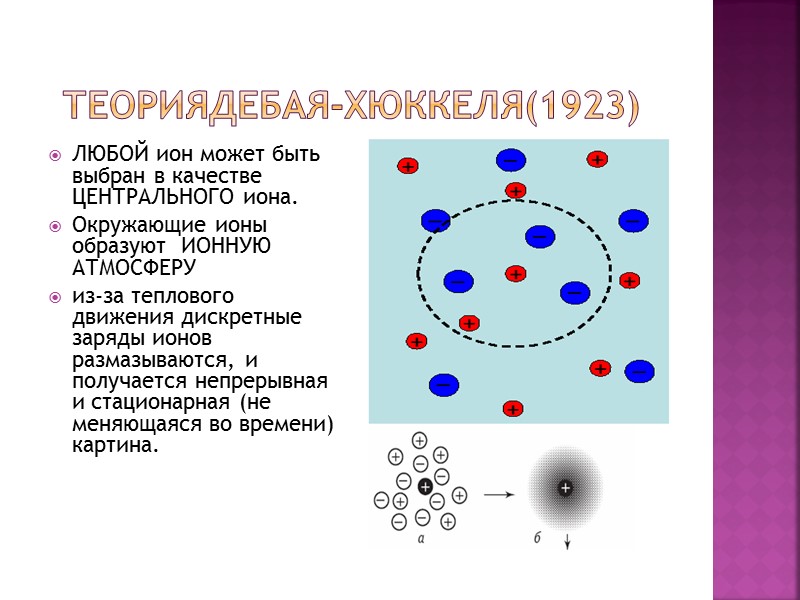
 ТеорияДебая-Хюккеля(1923) ЛЮБОЙ ион может быть выбран в качестве ЦЕНТРАЛЬНОГО иона. Окружающие ионы образуют ИОННУЮ АТМОСФЕРУ из-за теплового движения дискретные заряды ионов размазываются, и получается непрерывная и стационарная (не меняющаяся во времени) картина.
ТеорияДебая-Хюккеля(1923) ЛЮБОЙ ион может быть выбран в качестве ЦЕНТРАЛЬНОГО иона. Окружающие ионы образуют ИОННУЮ АТМОСФЕРУ из-за теплового движения дискретные заряды ионов размазываются, и получается непрерывная и стационарная (не меняющаяся во времени) картина.
 Уравнение Пуассона непрерывная и стационарная (не меняющаяся во времени) картина позволяет использовать континуальное (непрерывное) уравнение Пуассона – фундаментальное уравнение электростатики, связывающее электрический потенциал и плотность заряда
Уравнение Пуассона непрерывная и стационарная (не меняющаяся во времени) картина позволяет использовать континуальное (непрерывное) уравнение Пуассона – фундаментальное уравнение электростатики, связывающее электрический потенциал и плотность заряда
 Математическое описание ионной атмосферы
Математическое описание ионной атмосферы
 первое приближение теории (Дебая-Хюккеля) Ионы имеют точечные размеры и могут сближаться неограниченно В каждой точке пространства в пределах ионной атмосферы локальная концентрация каждого сорта ионов ni отличаются от его равновесной объемной концентрации ni0. Это и определяет величину объемного заряда в этой точке
первое приближение теории (Дебая-Хюккеля) Ионы имеют точечные размеры и могут сближаться неограниченно В каждой точке пространства в пределах ионной атмосферы локальная концентрация каждого сорта ионов ni отличаются от его равновесной объемной концентрации ni0. Это и определяет величину объемного заряда в этой точке
 Величина объемного заряда в точке
Величина объемного заряда в точке
 Дебаевский радиус ионной атмосферы
Дебаевский радиус ионной атмосферы
 Обратная дебаевская длина
Обратная дебаевская длина
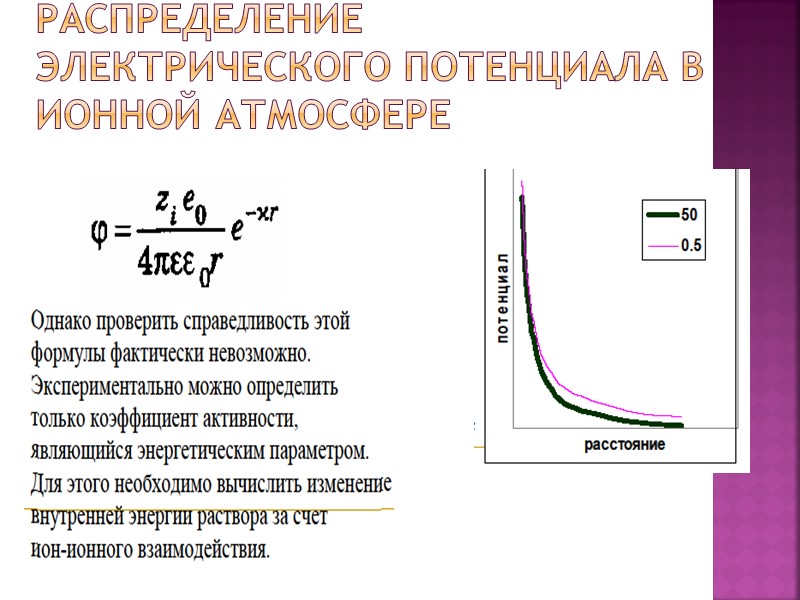
 Распределение электрического потенциала в ионной атмосфере
Распределение электрического потенциала в ионной атмосфере
 Энергия центрального иона и дебаевская длина
Энергия центрального иона и дебаевская длина
 Потенциал ионной атмосферы
Потенциал ионной атмосферы
 Работа и энергия Гиббса
Работа и энергия Гиббса
 Коэффициент активности
Коэффициент активности
 Изменение свободной энергии
Изменение свободной энергии
 Первое приближение теории ДХ для коэффициентов активности
Первое приближение теории ДХ для коэффициентов активности
 Вычисление ионной силы раствора
Вычисление ионной силы раствора
 Предельный закон Дебая-Хюккеля
Предельный закон Дебая-Хюккеля
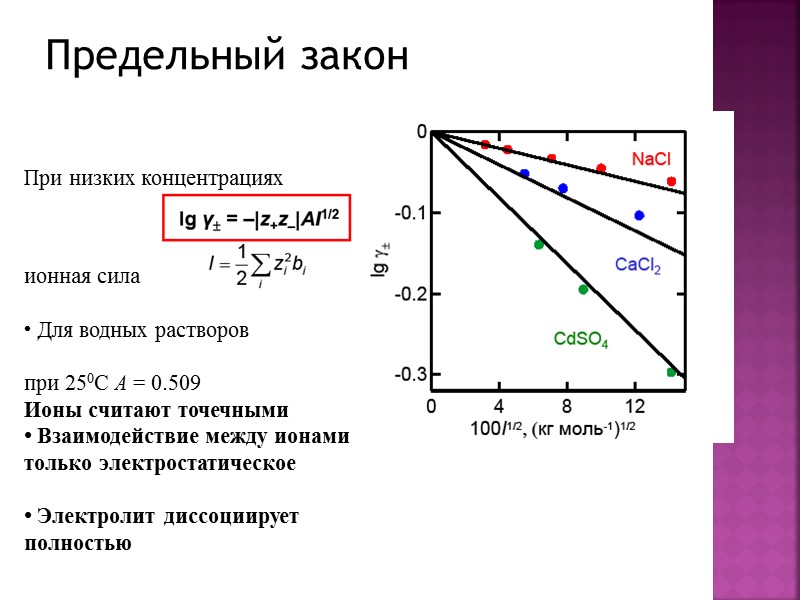
 Предельный закон При низких концентрациях ионная сила • Для водных растворов при 250C A = 0.509 Ионы считают точечными • Взаимодействие между ионами только электростатическое • Электролит диссоциирует полностью
Предельный закон При низких концентрациях ионная сила • Для водных растворов при 250C A = 0.509 Ионы считают точечными • Взаимодействие между ионами только электростатическое • Электролит диссоциирует полностью
 согласие с экспериментом в разбавленных растворах
согласие с экспериментом в разбавленных растворах
 Сильное расхождение с экспериментом в концентрированных растворах
Сильное расхождение с экспериментом в концентрированных растворах
 Причины концентрационной ограниченности первого приближения теории ДХ 1) Использование континуального уравнения Пуассона означает, что никак не учитывается молекулярная структура растворителя. 2) Ионы считаются математическими точками (могут сближаться неограниченно), что неверно. 3) Игнорирование изменения ε раствора по сравнению с растворителем. 4) Игнорирование всех других возможных взаимодействий (ион-дипольное, сольватация, образование водородных связей, ассоциатов, комплексов и т.д.).
Причины концентрационной ограниченности первого приближения теории ДХ 1) Использование континуального уравнения Пуассона означает, что никак не учитывается молекулярная структура растворителя. 2) Ионы считаются математическими точками (могут сближаться неограниченно), что неверно. 3) Игнорирование изменения ε раствора по сравнению с растворителем. 4) Игнорирование всех других возможных взаимодействий (ион-дипольное, сольватация, образование водородных связей, ассоциатов, комплексов и т.д.).

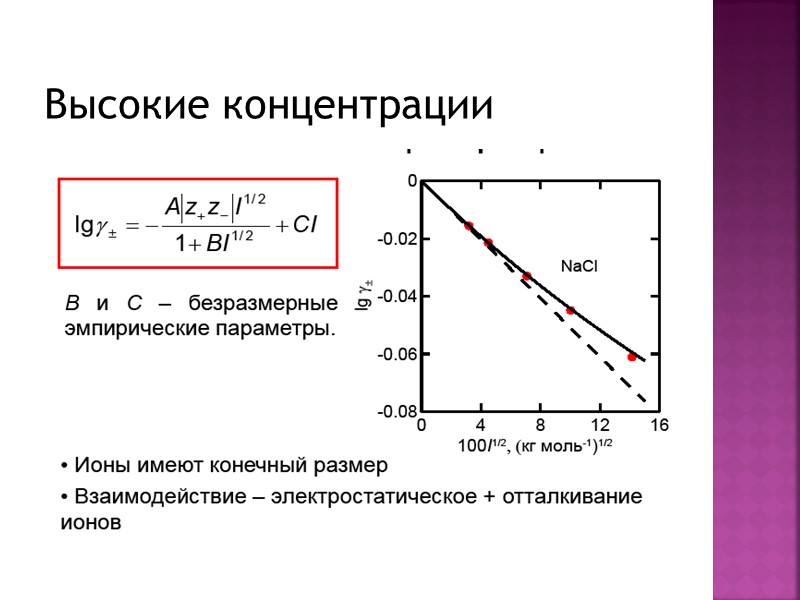
 Высокие концентрации
Высокие концентрации
 Второе приближение теории Дебая-Хюккеля
Второе приближение теории Дебая-Хюккеля
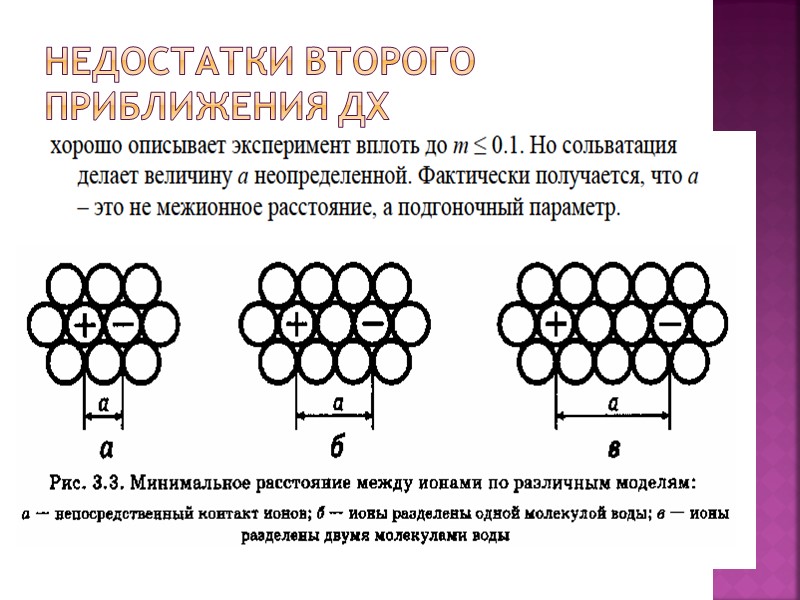
 Недостатки второго приближения ДХ
Недостатки второго приближения ДХ
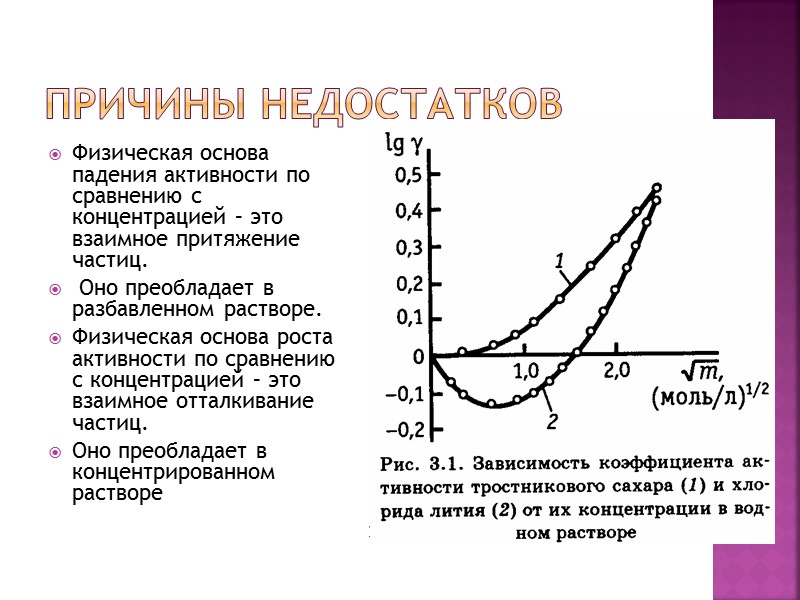
 Причины недостатков Физическая основа падения активности по сравнению с концентрацией – это взаимное притяжение частиц. Оно преобладает в разбавленном растворе. Физическая основа роста активности по сравнению с концентрацией – это взаимное отталкивание частиц. Оно преобладает в концентрированном растворе
Причины недостатков Физическая основа падения активности по сравнению с концентрацией – это взаимное притяжение частиц. Оно преобладает в разбавленном растворе. Физическая основа роста активности по сравнению с концентрацией – это взаимное отталкивание частиц. Оно преобладает в концентрированном растворе
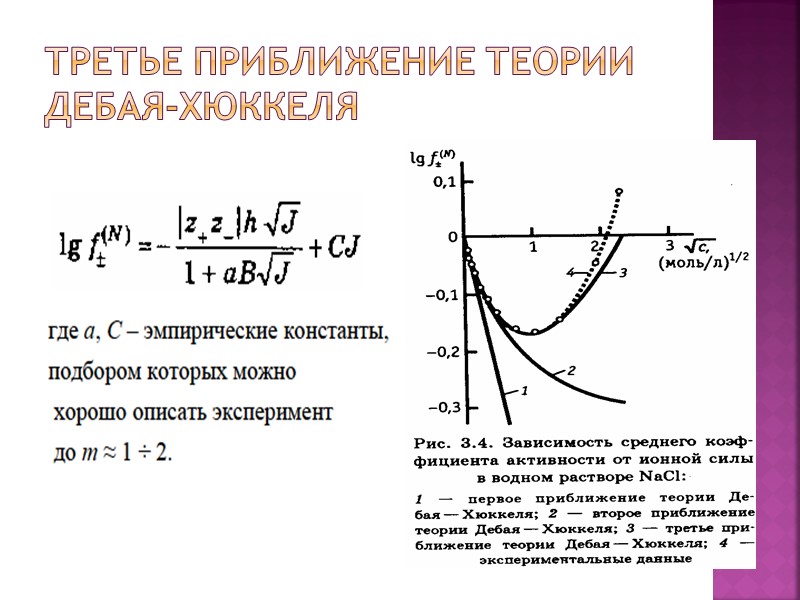
 Третье приближение теории Дебая-Хюккеля
Третье приближение теории Дебая-Хюккеля
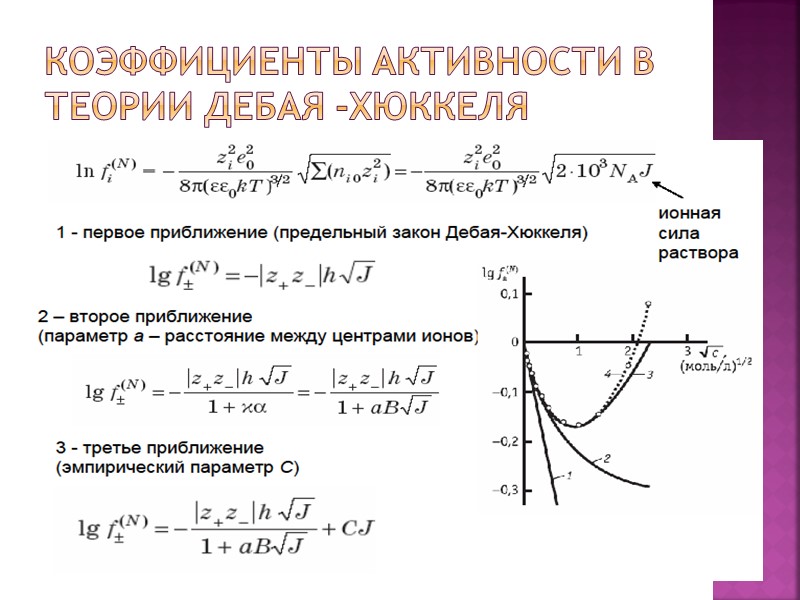
 Коэффициенты активности в теории Дебая -Хюккеля
Коэффициенты активности в теории Дебая -Хюккеля
 Контрольные вопросы Что такое ионофоры и ионогены? Из каких энергий складывается энергия кристаллической решетки? Чему равна энергия сольватации 1 моля иона Что такое реальная энергия сольватации?
Контрольные вопросы Что такое ионофоры и ионогены? Из каких энергий складывается энергия кристаллической решетки? Чему равна энергия сольватации 1 моля иона Что такое реальная энергия сольватации?

