лекция 6.ppt
- Количество слайдов: 42

Инженерная энзимология

Иммобилизация ферментов – это любое ограничение свободы движения белковых молекул (или их фрагментов) в пространстве. • • Преимущества иммобилизованных ферментов перед нативными предшественниками: 1. Гетерогенный катализатор легко отделим от реакционной среды, что дает возможность остановить реакцию в любой момент, использовать фермент повторно, а также получать чистый от фермента продукт. 2. Ферментативный процесс с использованием иммобилизованных ферментов можно проводить непрерывно, регулируя скорость катализируемой реакции и выход продукта. 3. Модификация фермента целенаправленно изменяет его свойства, такие как специфичность, зависимость каталитической активности от р. Н, ионного состава и других параметров среды, стабильность к денатурирующим воздействиям. 4. Можно регулировать каталитическую активность иммобилизованных ферментов путем изменения свойств носителя.
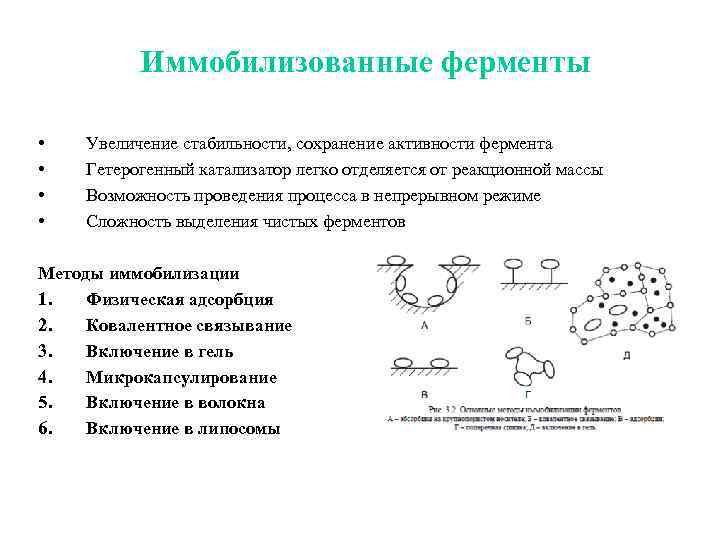
Иммобилизованные ферменты • • Увеличение стабильности, сохранение активности фермента Гетерогенный катализатор легко отделяется от реакционной массы Возможность проведения процесса в непрерывном режиме Сложность выделения чистых ферментов Методы иммобилизации 1. Физическая адсорбция 2. Ковалентное связывание 3. Включение в гель 4. Микрокапсулирование 5. Включение в волокна 6. Включение в липосомы

Типы иммобилизации Физическая иммобилизация Иммобилизация, при которой фермент не соединен с носителем ковалентными связями Физическая иммобилизация может быть проведена путем - адсорбции на нерастворимых носителях - включения в поры геля - использования полупроницаемых оболочек (мембран) - включения в двухфазную реакционную среду, где фермент растворим и может находиться только в одной из фаз. Химическая иммобилизация Путем химического воздействия на структуру фермента в его молекуле создаются новые ковалентные связи, в частности между белком и носителем. Адсорбция на носителе Включение в гель Отделение с помощью полупроницаемой мембраны Использование двухфазной реакционной среды
Носители для иммобилизованных ферментов • • • Для получения иммобилизованных ферментов используется ограниченное число как органических, так и неорганических носителей. К носителям предъявляются следующие требования - высокая химическая и биологическая стойкость; - высокая химическая прочность; - достаточная проницаемость для фермента и субстратов, пористость, большая удельная поверхность; - возможность получения в виде удобных в технологическом отношении форм (гранул, мембран); - легкая активация; - высокая гидрофильность; - невысокая стоимость.
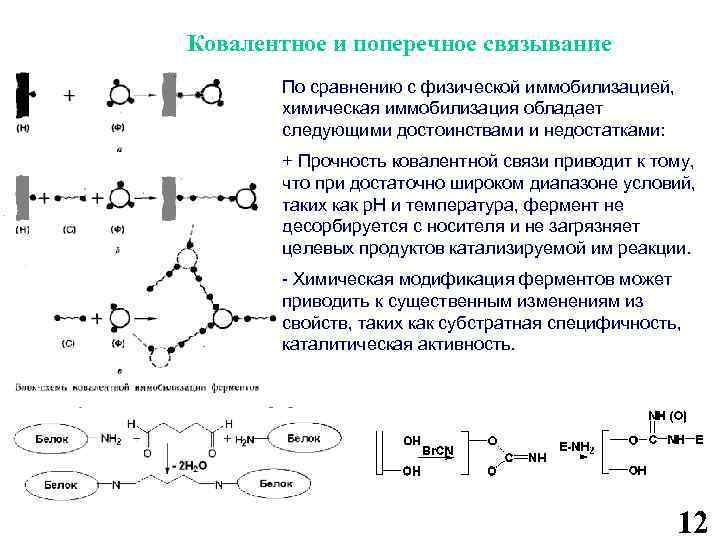
Ковалентное и поперечное связывание По сравнению с физической иммобилизацией, химическая иммобилизация обладает следующими достоинствами и недостатками: + Прочность ковалентной связи приводит к тому, что при достаточно широком диапазоне условий, таких как p. H и температура, фермент не десорбируется с носителя и не загрязняет целевых продуктов катализируемой им реакции. - Химическая модификация ферментов может приводить к существенным изменениям из свойств, таких как субстратная специфичность, каталитическая активность. 12
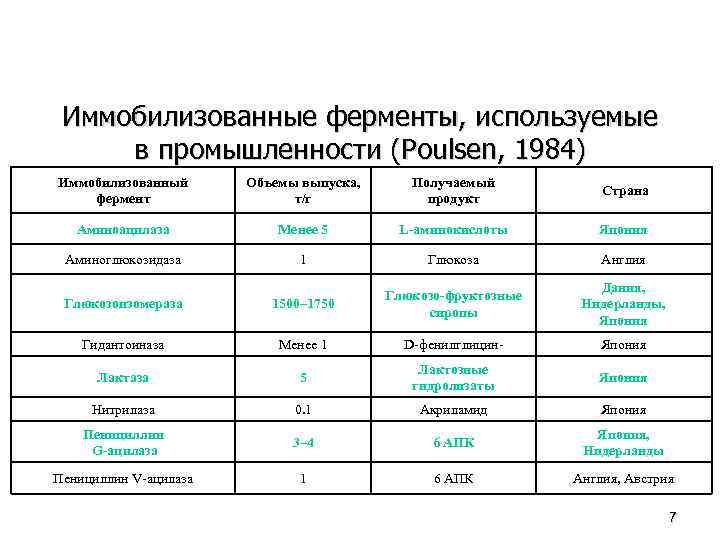
Иммобилизованные ферменты, используемые в промышленности (Poulsen, 1984) Иммобилизованный фермент Объемы выпуска, т/г Получаемый продукт Страна Аминоацилаза Менее 5 L аминокислоты Япония Аминоглюкозидаза 1 Глюкоза Англия Глюкозоизомераза 1500– 1750 Глюкозо фруктозные сиропы Дания, Нидерланды, Япония Гидантоиназа Менее 1 D-фенилглицин- Япония Лактаза 5 Лактозные гидролизаты Япония Нитрилаза 0. 1 Акриламид Япония Пенициллин G ацилаза 3– 4 6 АПК Япония, Нидерланды Пенициллин V-ацилаза 1 6 АПК Англия, Австрия 7
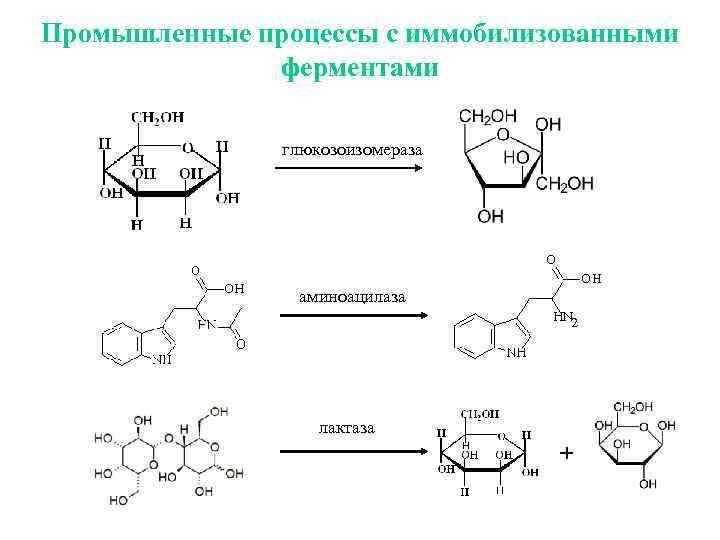
Промышленные процессы с иммобилизованными ферментами глюкозоизомераза аминоацилаза 2 лактаза +

Иммобилизованные клетки • • Иммобилизованные клетки имеют ряд преимуществ как перед иммобилизованными ферментами, так и перед свободными клетками: - отсутствие затрат на выделение и очистку ферментов; - снижение затрат на выделение и очистку продуктов реакции; - более высокая активность и стабильность; - возможность создания непрерывных и полунепрерывных автоматизированных процессов; - способность к длительному функционированию полиферментных систем без экзогенных кофакторов.

• • КОНВЕРТОР ДЛЯ БИОДЕСТРУКЦИИ НЕФТЯНЫХ УГЛЕВОДОРОДОВ ИЗ ВОДНЫХ СРЕД Область применения и назначение: для биоремедиации воды, загрязненной сырой нефтью, нефтяными углеводородами, эмульгированными в воде или растворенными в ней, или плавающие на ее поверхности. • Краткое описание и основные технические характеристики: конвертор на основе нетканого материала с иммобилизованными клетками микроорганизмов. Конвертор пригоден для многоразового использования в 5 -7 циклах без потери активности в качестве твердофазного биодеструктора нефти и нефтяных углеводородов. Время очищения воды до уровня ПДК составляет 4 -34 часа в зависимости от концентрации нефтепродуктов в водной среде. Активность клеток в твердой фазе, иммобилизованных на нетканом материале, при температуре хранения +4÷ 6 0 С не изменяется в течение года.

Иммунобиотехнология

Основы иммунологии Иммунитет • Иммунитет - врожденная или приобретенная способность макроорганизма к защите, специфически направленная против любых генетически чужеродных для него агентов (от лат. immunitas – освобождение от чего-либо). • Иммунитет функционально направлен на уничтожение клеток и веществ, генетически отличающихся от собственных, и на сохранение постоянства внутренней среды макроорганизма (гомеостаза) в течение всей его жизни. • Иммунная система (ИС) – система органов и специализированных клеток макроорганизма, реагирующая на генетически чужеродную информацию/субстанцию и участвующая в защите макроорганизма от такой информации/субстанции. • Иммунный ответ (ИО) – совокупность иммунных реакций организма на воздействие чужеродного агента. • Чужеродный агент, способный вызвать иммунный ответ, называется антигеном.
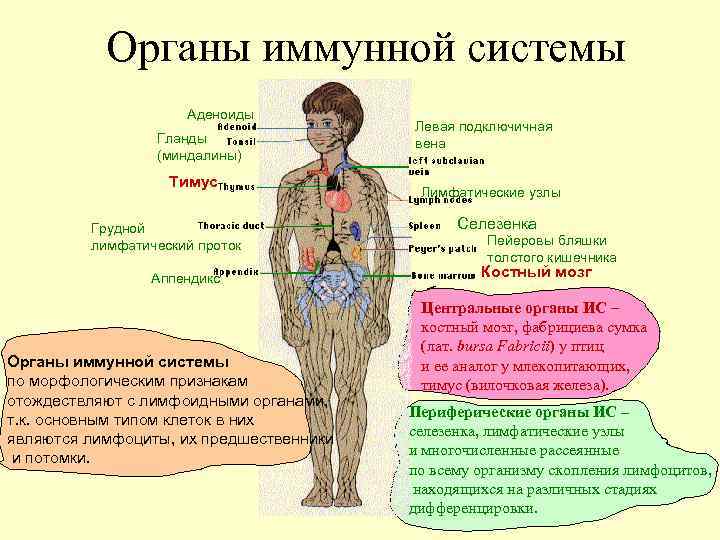
Органы иммунной системы Аденоиды Гланды (миндалины) Тимус Грудной лимфатический проток Аппендикс Органы иммунной системы по морфологическим признакам отождествляют с лимфоидными органами, т. к. основным типом клеток в них являются лимфоциты, их предшественники и потомки. Левая подключичная вена Лимфатические узлы Селезенка Пейеровы бляшки толстого кишечника Костный мозг Центральные органы ИС – костный мозг, фабрициева сумка (лат. bursa Fabricii) у птиц и ее аналог у млекопитающих, тимус (вилочковая железа). Периферические органы ИС – селезенка, лимфатические узлы и многочисленные рассеянные по всему организму скопления лимфоцитов, находящихся на различных стадиях дифференцировки.
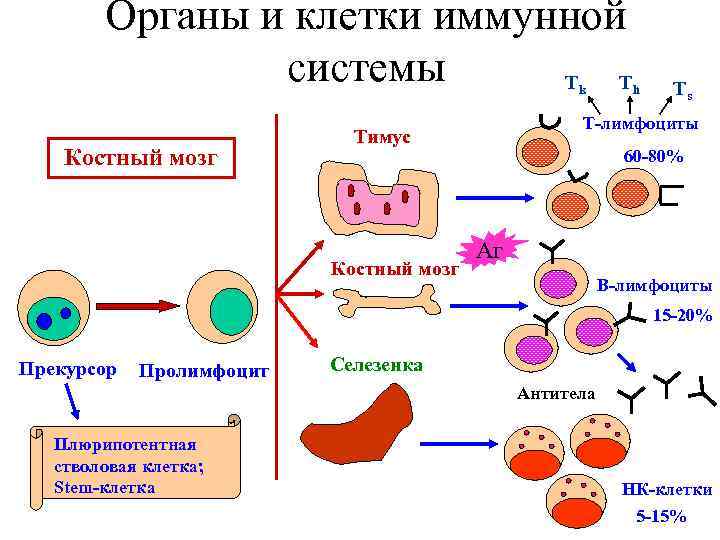
Органы и клетки иммунной системы T T k Костный мозг Ts Т лимфоциты Тимус Костный мозг h 60 80% Аг В лимфоциты 15 20% Прекурсор Пролимфоцит Селезенка Антитела Плюрипотентная стволовая клетка; Stem клетка НК клетки 5 15%

Клетки иммунной системы • В лимфоциты (B клетки) – (от лат. bursa). Лимфоциты, возникающие в процессе АГ-независимой дифференцировки стволовых клеток в фабрициевой сумке у птиц (или ее аналоге у млекопитающих) и в костном мозге. После миграции в селезенку превращаются в антитело-образующие клетки, т. е. участвуют в выработке антител. • Т лимфоциты (Т клетки) – (от лат. tymus). Тимус-зависимые лимфоциты. Появляются в процессе АГ-независимой дифференцировки стволовых клеток в тимусе. Делятся на несколько популяций, которые взаимодействуют с В-лимфоцитами, убивают зараженные вирусом клетки, активируют макрофаги и выполняют многие другие функции. НК - большие гранулярные лимфоциты, обладающие цитотоксичностью против опухолевых клеток и клеток, зараженных вирусами Фагоциты (Нейтрофилы. Макрофаги. Дендритные клетки) • •
НК - большие гранулярные лимфоциты, обладающие цитотоксичностью против опухолевых клеток и клеток, зараженных вирусами
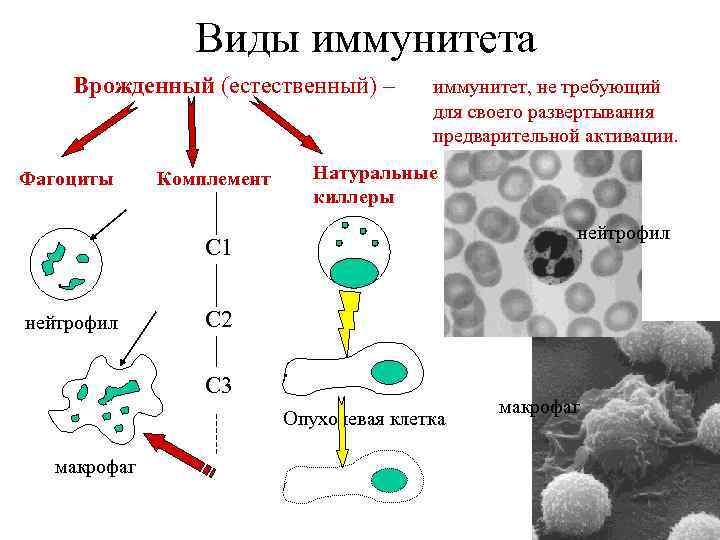
Виды иммунитета Врожденный (естественный) – Фагоциты Комплемент иммунитет, не требующий для своего развертывания предварительной активации. Натуральные киллеры нейтрофил С 1 нейтрофил С 2 С 3 Опухолевая клетка макрофаг

Система комплемента
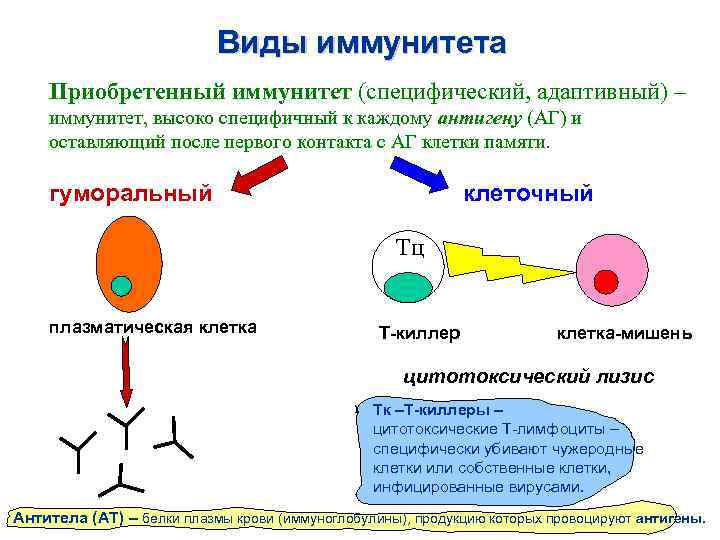
Виды иммунитета Приобретенный иммунитет (специфический, адаптивный) – иммунитет, высоко специфичный к каждому антигену (АГ) и оставляющий после первого контакта с АГ клетки памяти. клеточный гуморальный Тц плазматическая клетка Т-киллер клетка-мишень цитотоксический лизис Tк –Т-киллеры – цитотоксические Т-лимфоциты – специфически убивают чужеродные клетки или собственные клетки, инфицированные вирусами. Антитела (АТ) – белки плазмы крови (иммуноглобулины), продукцию которых провоцируют антигены.

Виды иммунитета • Гуморальный иммунитет – развертывается по линии выработки антител, и основной процесс между АТ и АГ происходит в сыворотке крови (humor); к основному процессу подключаются другие сывороточные факторы (комплемент, цитокины). По этому пути осуществляется противоинфекционная защита. • Клеточный иммунитет – осуществляется сенсибилизированными Т-лимфоцитами, при непосредственном контакте с клеткой- «мишенью» . На Т-лимфоцитах- «киллерах» имеются специальные рецепторы, которые соединяются с «мишенью» и «убивают» ее посредством цитотоксического лизиса. К этим процессам подключается комплемент.

Антигены • Антиген (АГ) – любая чужеродная субстанция (вирусная, бактериальная, химическая, природная, тканевая), способная вызвать иммунный ответ. • Полноценные антигены – антигены, индуцирующие иммунный ответ организма и специфически реагирующие с иммунокомпетентными клетками и антителами. • Гаптены (неполные антигены) – вещества (как правило, низкомолекулярные, Мв < 1000 Да), взаимодействующие со специфическими антителами, но неспособные вызывать иммунный ответ. Приобретают способность вызывать иммунный ответ при конъюгации с крупными молекулами – носителями гаптенов. • Антигенная детерминанта (эпитоп) – участок поверхности молекулы антигена, специфически связывающийся с АГсвязывающим участком (паратопом) антитела. • Валентность антигена – число молекул антител, с которым может взаимодействовать данный антиген.

Антигены • Антигенность (антигенная специфичность) – способность антигена взаимодействовать с АГспецифическими рецепторами Т- и В-лимфоцитов и антителами. • Чужеродность – способность выступать антигеном в отношении данного организма. • Иммуногенность – способность антигена вызывать иммунный ответ.
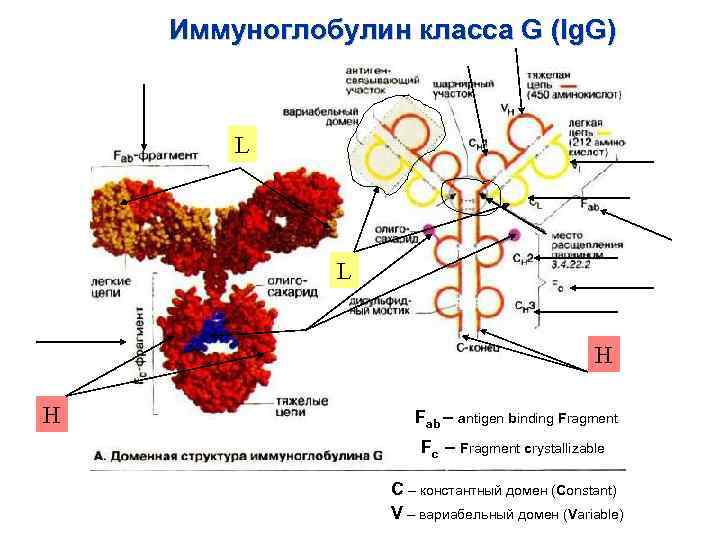
Иммуноглобулин класса G (Ig. G) L L H H Fab – antigen binding Fragment Fc – Fragment crystallizable C – константный домен (Сonstant) V – вариабельный домен (Variable)

Какие бывают антитела? Нескольких классов: Ig. M, Ig. G, Ig. A, Ig. E, Ig. D : Ig. M (иммунноглобулины класса M) — это самые первые антитела, которые образуются при появлении незнакомых антигенов. Поэтому это основные антитела, которые синтезируются у новорожденных и младенцев. Ig. M: Максимум у младенцев. Полезный вывод: если к антигенам конкретного микроба обнаружены Ig. M, то в организме идет острый инфекционный процесс. Ig. G — основной класс антител (до 75%). При первом контакте с антигеном образование Ig. M вскоре сменяется образованием большого количества Ig. G. Обнаружение большого количества этих антител указывает на выздоровление или на то, что конкретное заболевание перенесено недавно. И еще. Из всех классов только Ig. G способны проникать через плаценту к плоду. Ig. A (до 15 20%) — секретируются на поверхность эпителия, находятся в слюне, слезах, молоке. Они защищают слизистые оболочки дыхательных, половых, мочевыводящих и других путей. Ig. E (их мало, 1 2%) — участвуют в аллергических реакциях. Ig. D – очень мало.
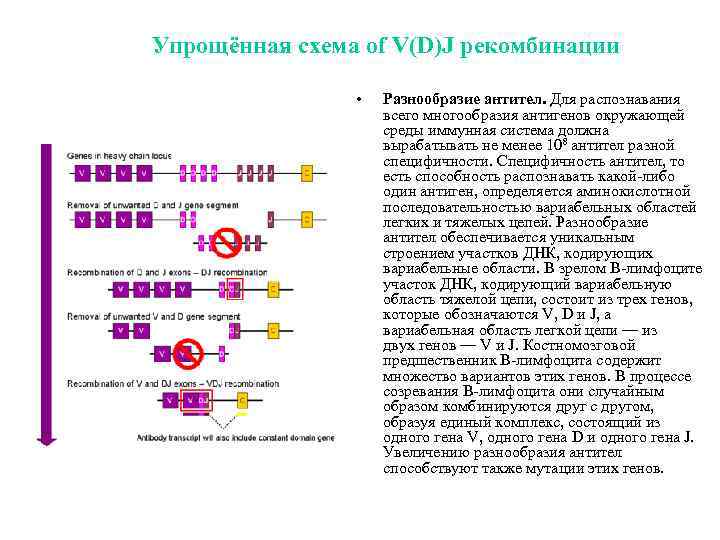
Упрощённая схема of V(D)J рекомбинации • Разнообразие антител. Для распознавания всего многообразия антигенов окружающей среды иммунная система должна вырабатывать не менее 108 антител разной специфичности. Специфичность антител, то есть способность распознавать какой-либо один антиген, определяется аминокислотной последовательностью вариабельных областей легких и тяжелых цепей. Разнообразие антител обеспечивается уникальным строением участков ДНК, кодирующих вариабельные области. В зрелом B-лимфоците участок ДНК, кодирующий вариабельную область тяжелой цепи, состоит из трех генов, которые обозначаются V, D и J, а вариабельная область легкой цепи — из двух генов — V и J. Костномозговой предшественник B-лимфоцита содержит множество вариантов этих генов. В процессе созревания B-лимфоцита они случайным образом комбинируются друг с другом, образуя единый комплекс, состоящий из одного гена V, одного гена D и одного гена J. Увеличению разнообразия антител способствуют также мутации этих генов.
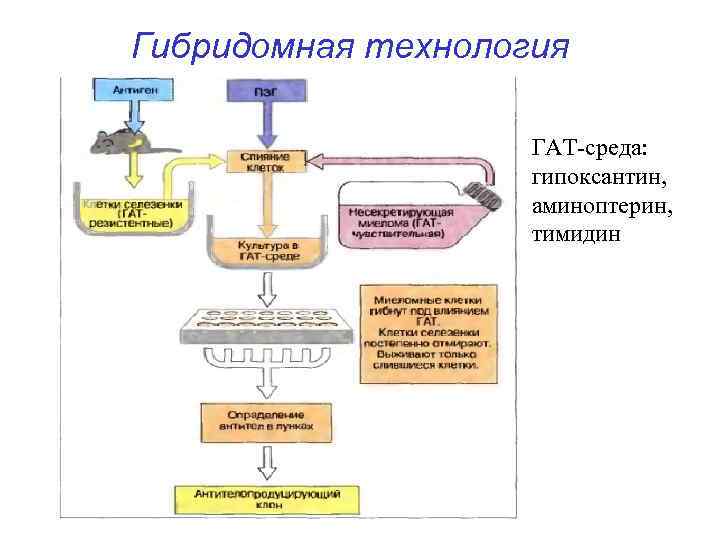
Гибридомная технология ГАТ-среда: гипоксантин, аминоптерин, тимидин

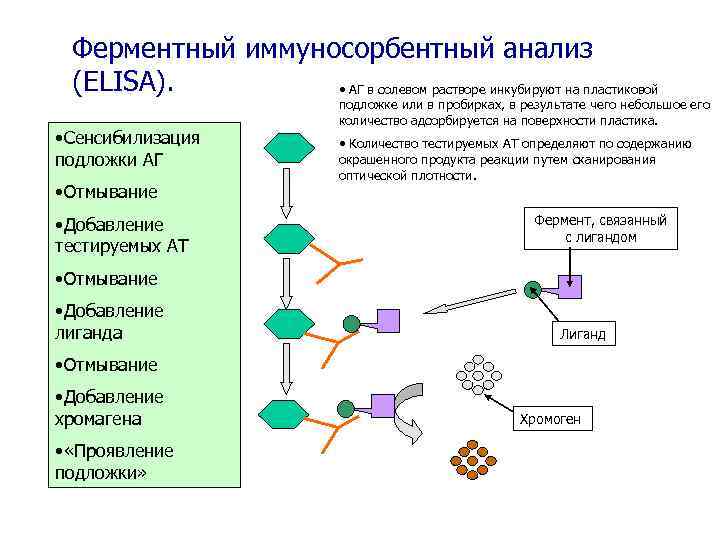
Ферментный иммуносорбентный анализ (ELISA). • АГ в солевом растворе инкубируют на пластиковой • Сенсибилизация подложки АГ • Отмывание • Добавление тестируемых АТ подложке или в пробирках, в результате чего небольшое его количество адсорбируется на поверхности пластика. • Количество тестируемых АТ определяют по содержанию окрашенного продукта реакции путем сканирования оптической плотности. Фермент, связанный с лигандом • Отмывание • Добавление лиганда Лиганд • Отмывание • Добавление хромагена • «Проявление подложки» Хромоген

Использование ИФА-диагностики • ГЕПАТИТ • ЭНТЕРОБАКТЕРИИ • ВИЧ-ИНФЕКЦИИ • СТАФИЛОКОККИ • СИФИЛИС • КОРИНЕБАКТРИИ • ХЛАМИДИОЗ • ВИРУСА ЭПШТЕЙНА-БАРР, ЦИТОМЕГАЛОВИРУСА • ГЕРПЕСНЫЕ ИНФЕКЦИИ • В КЛИНИЧЕСКОЙ БИОХИМИИ (ГЛЮКОЗА, • АТИПИЧНАЯ ПНЕВМОНИЯ БЕЛОК, МОЧЕВИНА, АЛЬБУМИН) • ИНФАРКТ МИОКАРДА • ТОКСОПЛАЗМОЗ

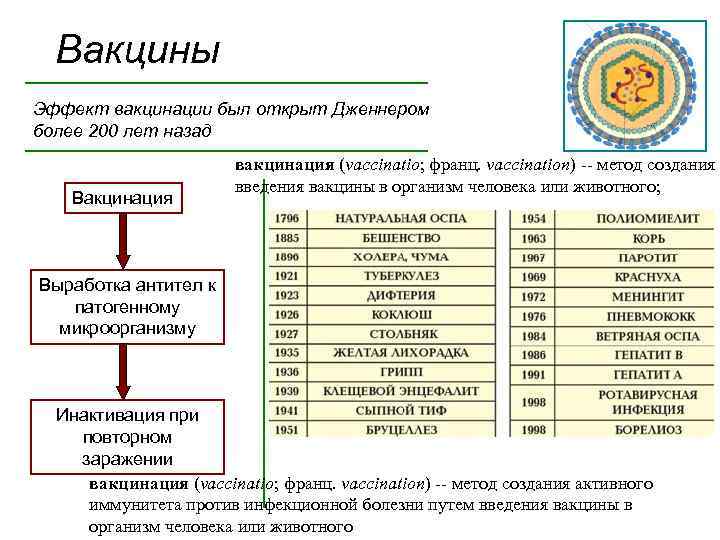
Вакцины Эффект вакцинации был открыт Дженнером более 200 лет назад Вакцинация вакцинация (vaccinatio; франц. vaccination) -- метод создания введения вакцины в организм человека или животного; Выработка антител к патогенному микроорганизму Инактивация при повторном заражении вакцинация (vaccinatio; франц. vaccination) -- метод создания активного иммунитета против инфекционной болезни путем введения вакцины в организм человека или животного

Требования, предъявляемые к современным вакцинам: • Иммуногенность; • Низкая реактогенность (аллергенность); • Не должны обладать тератогенностью (способностью нарушать нормальное развитие эмбриона и вызывать появление различных аномалий развития); • Не должны обладать онкогенностью; • Штаммы, из которых приготовлена вакцина, должны быть генетически стабильны; • Длительный срок хранения; • Технологичность производства; • Простота и доступность в применении.

Ограничения: • не все патогенные микроорганизмы удается культивировать; • для получения вирусов животных и человека требуются дорогостоящие культуры животных клеток; • возможность инфицирования персонала; • риск попадания живых и неослабленных микроорганизмов в партию вакцин; • вирулентность; • изменение активности с течением времени
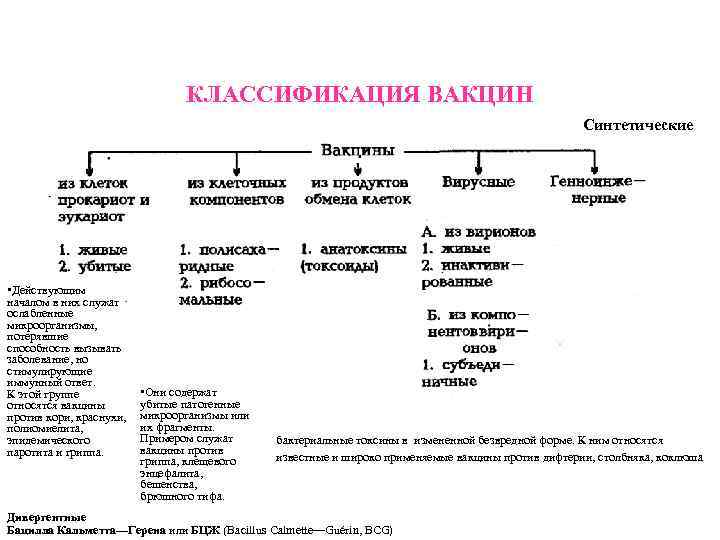
КЛАССИФИКАЦИЯ ВАКЦИН Синтетические • Действующим началом в них служат ослабленные микроорганизмы, потерявшие способность вызывать заболевание, но стимулирующие иммунный ответ. К этой группе относятся вакцины против кори, краснухи, полиомиелита, эпидемического паротита и гриппа. • Они содержат убитые патогенные микроорганизмы или их фрагменты. Примером служат вакцины против гриппа, клещевого энцефалита, бешенства, брюшного тифа. бактериальные токсины в измененной безвредной форме. К ним относятся известные и широко применяемые вакцины против дифтерии, столбняка, коклюша Дивергентные Бацилла Кальметта—Герена или БЦЖ (Bacillus Calmette—Guérin, BCG)
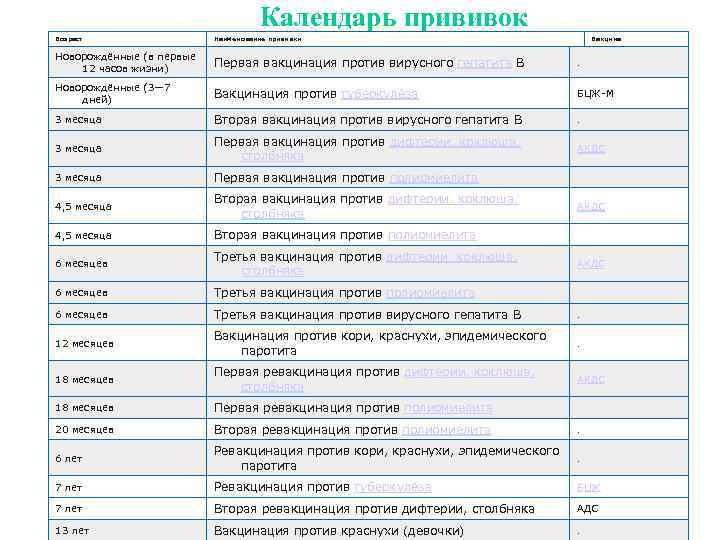
Календарь прививок Возраст Наименование прививки Вакцина Новорождённые (в первые 12 часов жизни) Первая вакцинация против вирусного гепатита B . Новорождённые (3— 7 дней) Вакцинация против туберкулёза БЦЖ-М 3 месяца Вторая вакцинация против вирусного гепатита B . 3 месяца Первая вакцинация против дифтерии, коклюша, столбняка АКДС 3 месяца Первая вакцинация против полиомиелита 4, 5 месяца Вторая вакцинация против дифтерии, коклюша, столбняка АКДС 4, 5 месяца Вторая вакцинация против полиомиелита 6 месяцев Третья вакцинация против дифтерии, коклюша, столбняка АКДС 6 месяцев Третья вакцинация против полиомиелита 6 месяцев Третья вакцинация против вирусного гепатита В . 12 месяцев Вакцинация против кори, краснухи, эпидемического паротита . 18 месяцев Первая ревакцинация против дифтерии, коклюша, столбняка АКДС 18 месяцев Первая ревакцинация против полиомиелита 20 месяцев Вторая ревакцинация против полиомиелита . 6 лет Ревакцинация против кори, краснухи, эпидемического паротита . 7 лет Ревакцинация против туберкулёза БЦЖ 7 лет Вторая ревакцинация против дифтерии, столбняка АДС 13 лет Вакцинация против краснухи (девочки) .

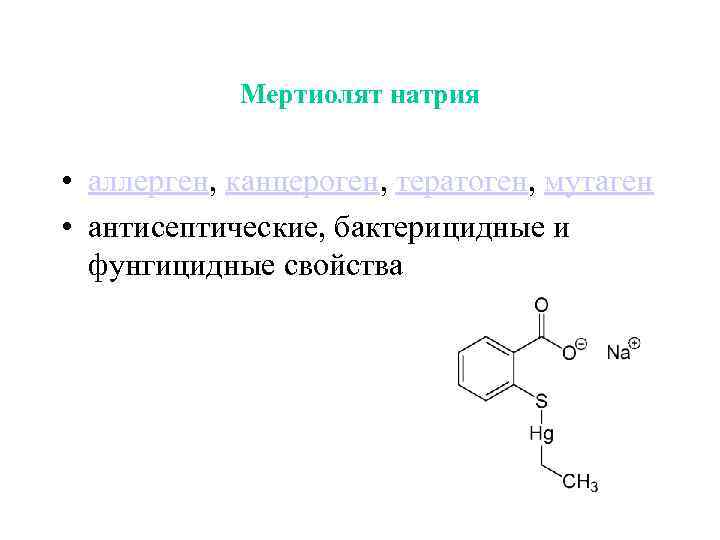
Мертиолят натрия • аллерген, канцероген, тератоген, мутаген • антисептические, бактерицидные и фунгицидные свойства

Должна ли вакцина содержать целые клетки ? Субъединичные вакцины Очищенные поверхностные белки, отдельные компоненты микроорганизма Идентификация компонентов, индуцирующих выработку антител Выделение соответствующего гена Клонирование гена с помощью экспрессирующей системы, далее - получение белка Достоинства: + + + очищенный иммуногенный белок стабилен и безопасен химические свойства известны отсутствуют другие белки и нуклеиновые кислоты => отсутствие нежелательных побочный эффектов Недостатки: - очистка специфического белка стоит дорого - конформация выделенного белка может отличаться от нативной =>изменение его антигенных свойств Используются в случае, если вирус онкогенный, и невозможно использование аттенуированных вакцин
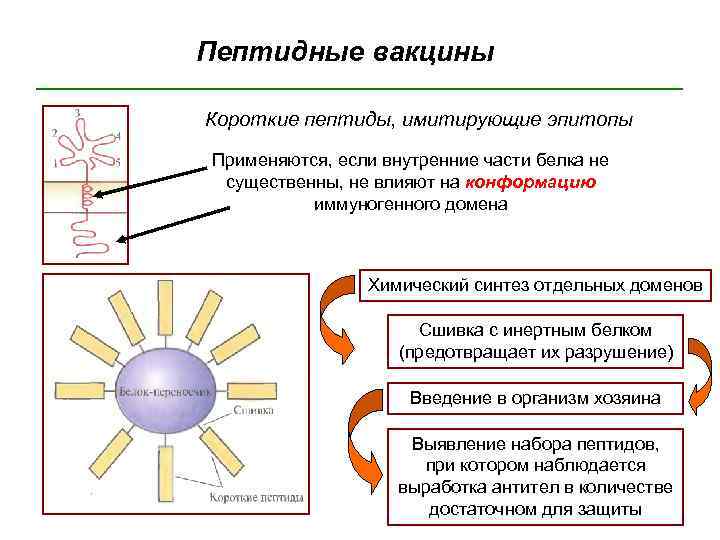
Пептидные вакцины Короткие пептиды, имитирующие эпитопы Применяются, если внутренние части белка не существенны, не влияют на конформацию иммуногенного домена Химический синтез отдельных доменов Сшивка с инертным белком (предотвращает их разрушение) Введение в организм хозяина Выявление набора пептидов, при котором наблюдается выработка антител в количестве достаточном для защиты
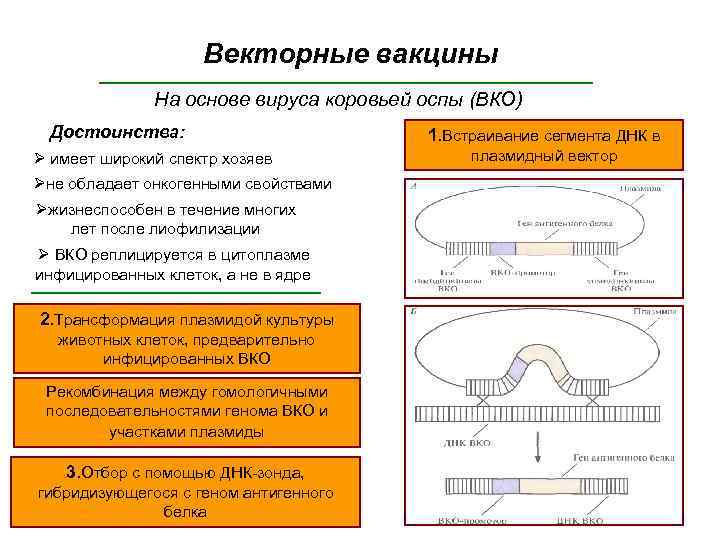
Векторные вакцины На основе вируса коровьей оспы (ВКО) Достоинства: Ø имеет широкий спектр хозяев Øне обладает онкогенными свойствами Øжизнеспособен в течение многих лет после лиофилизации Ø ВКО реплицируется в цитоплазме инфицированных клеток, а не в ядре 2. Трансформация плазмидой культуры животных клеток, предварительно инфицированных ВКО Рекомбинация между гомологичными последовательностями генома ВКО и участками плазмиды 3. Отбор с помощью ДНК-зонда, гибридизующегося с геном антигенного белка 1. Встраивание сегмента ДНК в плазмидный вектор

Модель вируса иммунодефицита человека, ВИЧ 1 – рецептор, при помощи которого вирус присоединяется к клетке; 2 – оболочка; 3 – генетический материал вируса (две молекулы РНК); 4 – белок-фермент, который помогает ВИЧ синтезировать новые вирусные частицы.
лекция 6.ppt