ИНЖЕНЕРНАЯ ЭНЗИМОЛОГИЯ.ppt
- Количество слайдов: 182
 ИНЖЕНЕРНАЯ ЭНЗИМОЛОГИЯ 1
ИНЖЕНЕРНАЯ ЭНЗИМОЛОГИЯ 1
 «ЧИСТАЯ ХИМИЯ» • Химическая промышленность является одним из наиболее важных источников загрязнения окружающей среды • Концепция устойчивого развития предполагает переход к технологиям нового поколения, минимизирующим вред окружающей среде 2
«ЧИСТАЯ ХИМИЯ» • Химическая промышленность является одним из наиболее важных источников загрязнения окружающей среды • Концепция устойчивого развития предполагает переход к технологиям нового поколения, минимизирующим вред окружающей среде 2
 БИОТЕХНОЛОГИЯ • Одним из путей постепенного перехода к «чистой химии» является расширение применения в промышленной химии ферментативного катализа. • Ферменты являются одним из видов продуктов биотехнологии, и изучение возможности их применения в качестве каталитических агентов также является разделом биотехнологии, получившим название «инженерная энзимология» . • Предмет инженерной энзимологии – поиск путей применения ферментов в качестве каталитических агентов для осуществления технологических процессов. 3
БИОТЕХНОЛОГИЯ • Одним из путей постепенного перехода к «чистой химии» является расширение применения в промышленной химии ферментативного катализа. • Ферменты являются одним из видов продуктов биотехнологии, и изучение возможности их применения в качестве каталитических агентов также является разделом биотехнологии, получившим название «инженерная энзимология» . • Предмет инженерной энзимологии – поиск путей применения ферментов в качестве каталитических агентов для осуществления технологических процессов. 3
 БИОТЕХНОЛОГИЯ • Научные задачи – исследование кинетических и структурных основ ферментативного катализа • Инженерные задачи – конструирование технологических процессов, обеспечивающих оптимальные условия и оптимальные технологические параметры производства продуктов 4
БИОТЕХНОЛОГИЯ • Научные задачи – исследование кинетических и структурных основ ферментативного катализа • Инженерные задачи – конструирование технологических процессов, обеспечивающих оптимальные условия и оптимальные технологические параметры производства продуктов 4
 ПРЕИМУЩЕСТВА ФЕРМЕНТОВ КАК КАТАЛИЗАТОРОВ • Пониженная энергоемкость процессов – за счет высокой каталитической эффективности ферментов, что позволяет осуществлять процессы при низких температурах • Пониженная материалоемкость – за счет высокой специфичности ферментов, что сводит к минимуму образование побочных продуктов 5
ПРЕИМУЩЕСТВА ФЕРМЕНТОВ КАК КАТАЛИЗАТОРОВ • Пониженная энергоемкость процессов – за счет высокой каталитической эффективности ферментов, что позволяет осуществлять процессы при низких температурах • Пониженная материалоемкость – за счет высокой специфичности ферментов, что сводит к минимуму образование побочных продуктов 5
 НЕКОТОРЫЕ НЕУДОБСТВА ФЕРМЕНТОВ • Недостаточная стабильность, снижающая срок их использования; • Трудности многократного использования фермента (после одного цикла превращения фермент, как правило, необратимо инактивируется при выделении продукта реакции) • Пути преодоления: поиск более удобных форм применения ферментов, обеспечивающих более высокую стабильность и возможность многократного применения 6
НЕКОТОРЫЕ НЕУДОБСТВА ФЕРМЕНТОВ • Недостаточная стабильность, снижающая срок их использования; • Трудности многократного использования фермента (после одного цикла превращения фермент, как правило, необратимо инактивируется при выделении продукта реакции) • Пути преодоления: поиск более удобных форм применения ферментов, обеспечивающих более высокую стабильность и возможность многократного применения 6
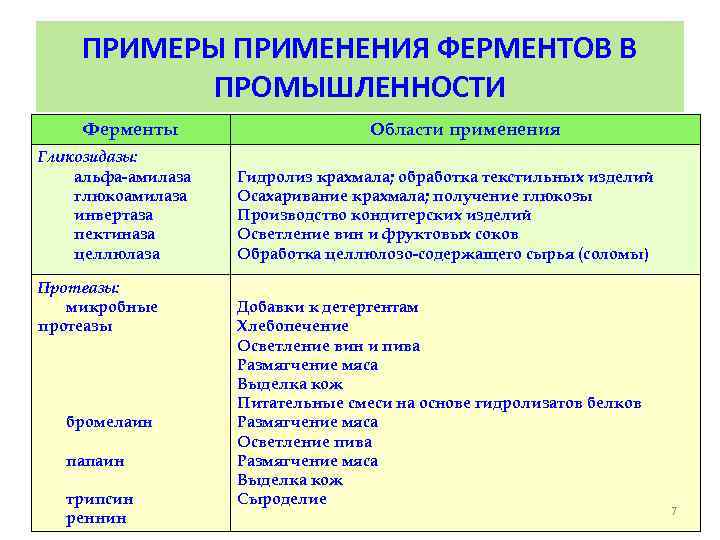 ПРИМЕРЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ В ПРОМЫШЛЕННОСТИ Ферменты Гликозидазы: альфа-амилаза глюкоамилаза инвертаза пектиназа целлюлаза Протеазы: микробные протеазы бромелаин папаин трипсин реннин Области применения Гидролиз крахмала; обработка текстильных изделий Осахаривание крахмала; получение глюкозы Производство кондитерских изделий Осветление вин и фруктовых соков Обработка целлюлозо-содержащего сырья (соломы) Добавки к детергентам Хлебопечение Осветление вин и пива Размягчение мяса Выделка кож Питательные смеси на основе гидролизатов белков Размягчение мяса Осветление пива Размягчение мяса Выделка кож Сыроделие 7
ПРИМЕРЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ В ПРОМЫШЛЕННОСТИ Ферменты Гликозидазы: альфа-амилаза глюкоамилаза инвертаза пектиназа целлюлаза Протеазы: микробные протеазы бромелаин папаин трипсин реннин Области применения Гидролиз крахмала; обработка текстильных изделий Осахаривание крахмала; получение глюкозы Производство кондитерских изделий Осветление вин и фруктовых соков Обработка целлюлозо-содержащего сырья (соломы) Добавки к детергентам Хлебопечение Осветление вин и пива Размягчение мяса Выделка кож Питательные смеси на основе гидролизатов белков Размягчение мяса Осветление пива Размягчение мяса Выделка кож Сыроделие 7
 ПРИМЕРЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ В ПРОМЫШЛЕННОСТИ Ферменты Липазы Оксидоредуктазы глюкозооксидаза каталаза Области применения Модификация вкуса молочных продуктов Добавки к детергентам Удаление кислорода из пищевых продуктов Определение глюкозы в биологических жидкостях (аналитический реагент) Удаление перекиси водорода после стерилизации молочных продуктов Изомеразы глюкозоизомераза Получение глюкозо-фруктозных сиропов Прочие ферменты нитрилгидратаза Получение акриламида 8
ПРИМЕРЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ В ПРОМЫШЛЕННОСТИ Ферменты Липазы Оксидоредуктазы глюкозооксидаза каталаза Области применения Модификация вкуса молочных продуктов Добавки к детергентам Удаление кислорода из пищевых продуктов Определение глюкозы в биологических жидкостях (аналитический реагент) Удаление перекиси водорода после стерилизации молочных продуктов Изомеразы глюкозоизомераза Получение глюкозо-фруктозных сиропов Прочие ферменты нитрилгидратаза Получение акриламида 8
 ИСТОЧНИКИ ПОЛУЧЕНИЯ ФЕРМЕНТОВ • Прокариотические микроорганизмы: бактерии, археи • Низшие эукариоты: дрожжи, микроскопические грибы • Высшие эукариоты (биомасса растений, ткани животных) • Бактерии, археи и низшие эукариоты отбирают из образцов окружающей среды (почвы, водоемы, атмосфера) с помощью селекции на средах, содержащих в качестве источника углерода соединение, для превращения которого необходим катализатор 9
ИСТОЧНИКИ ПОЛУЧЕНИЯ ФЕРМЕНТОВ • Прокариотические микроорганизмы: бактерии, археи • Низшие эукариоты: дрожжи, микроскопические грибы • Высшие эукариоты (биомасса растений, ткани животных) • Бактерии, археи и низшие эукариоты отбирают из образцов окружающей среды (почвы, водоемы, атмосфера) с помощью селекции на средах, содержащих в качестве источника углерода соединение, для превращения которого необходим катализатор 9
 ИСТОЧНИКИ ПОЛУЧЕНИЯ ФЕРМЕНТОВ • Ферменты высших эукариотов получают из биомассы, являющейся отходом пищевых производств. При выявлении фермента, имеющего перспективы промышленного применения, локализуют ген, кодирующий фермент, клонируют и создают штамм-продуцент для последующей организации систематического производства фермента. • Наличие клонированного гена фермента позволяет также осуществлять его модификацию в направлении приспособления технологических характеристик к условиям промышленного использования (повышение термостабильности, модификация специфичности и т. п. ) 10
ИСТОЧНИКИ ПОЛУЧЕНИЯ ФЕРМЕНТОВ • Ферменты высших эукариотов получают из биомассы, являющейся отходом пищевых производств. При выявлении фермента, имеющего перспективы промышленного применения, локализуют ген, кодирующий фермент, клонируют и создают штамм-продуцент для последующей организации систематического производства фермента. • Наличие клонированного гена фермента позволяет также осуществлять его модификацию в направлении приспособления технологических характеристик к условиям промышленного использования (повышение термостабильности, модификация специфичности и т. п. ) 10
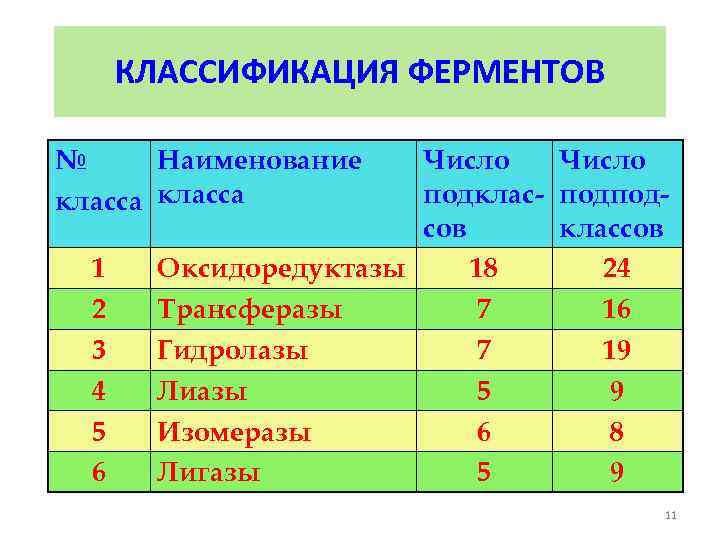 КЛАССИФИКАЦИЯ ФЕРМЕНТОВ № Наименование класса 1 2 3 4 5 6 Число подклас- подподсов классов Оксидоредуктазы 18 24 Трансферазы 7 16 Гидролазы 7 19 Лиазы 5 9 Изомеразы 6 8 Лигазы 5 9 11
КЛАССИФИКАЦИЯ ФЕРМЕНТОВ № Наименование класса 1 2 3 4 5 6 Число подклас- подподсов классов Оксидоредуктазы 18 24 Трансферазы 7 16 Гидролазы 7 19 Лиазы 5 9 Изомеразы 6 8 Лигазы 5 9 11
 СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ • Специфичность ферментов – способность различать близкие по химическому строению субстраты. • В начале ХХ века Фишер сформулировал гипотезу «ключ – замок» - однозначная дискриминация субстратов по их структуре за счет жесткой пространственной организации активного центра фермента • Впоследствии стали обнаруживаться факты, когда строгая специфичность наблюдается не всегда. • Пример - фосфорилирование глюкозы гексокиназой: глюкоза + АТФ → Глюкозо-6 -фосфат + АДФ • Фермент способен фосфорилировать как глюкозу, так и фруктозу, маннозу и ряд других сахаров ( с различными скоростями). • Кошланд – гипотеза индуцированного соответствия – за счет конформационной лабильности фермент может «приспосабливаться» к субстрату 12
СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ • Специфичность ферментов – способность различать близкие по химическому строению субстраты. • В начале ХХ века Фишер сформулировал гипотезу «ключ – замок» - однозначная дискриминация субстратов по их структуре за счет жесткой пространственной организации активного центра фермента • Впоследствии стали обнаруживаться факты, когда строгая специфичность наблюдается не всегда. • Пример - фосфорилирование глюкозы гексокиназой: глюкоза + АТФ → Глюкозо-6 -фосфат + АДФ • Фермент способен фосфорилировать как глюкозу, так и фруктозу, маннозу и ряд других сахаров ( с различными скоростями). • Кошланд – гипотеза индуцированного соответствия – за счет конформационной лабильности фермент может «приспосабливаться» к субстрату 12
 СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ Природа специфичности ферментов: • Кинетическая – фермент способен связывать субстраты различного строения, но скорость каталитических превращений для разных субстратов сильно различается, причем один из них превращается со скоростью, во много раз превосходящей скорости превращения остальных; • Термодинамическая – фермент способен с высоким сродством связывать лишь одно из близких соединений и далее катализировать его превращение. В реальной ситуации имеет место, как правило, комбинация обоих вариантов. 13
СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ Природа специфичности ферментов: • Кинетическая – фермент способен связывать субстраты различного строения, но скорость каталитических превращений для разных субстратов сильно различается, причем один из них превращается со скоростью, во много раз превосходящей скорости превращения остальных; • Термодинамическая – фермент способен с высоким сродством связывать лишь одно из близких соединений и далее катализировать его превращение. В реальной ситуации имеет место, как правило, комбинация обоих вариантов. 13
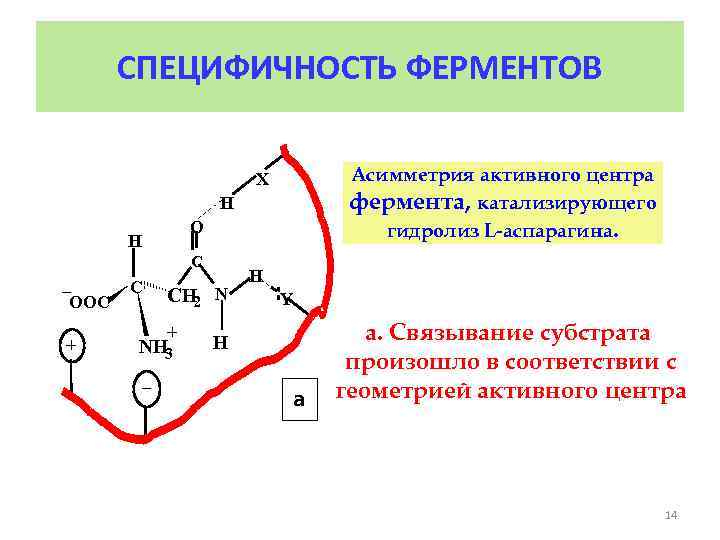 СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ Асимметрия активного центра фермента, катализирующего гидролиз L-аспарагина. X H O H C _ OOC + C CH 2 N + NH 3 _ H Y H а а. Связывание субстрата произошло в соответствии с геометрией активного центра 14
СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ Асимметрия активного центра фермента, катализирующего гидролиз L-аспарагина. X H O H C _ OOC + C CH 2 N + NH 3 _ H Y H а а. Связывание субстрата произошло в соответствии с геометрией активного центра 14
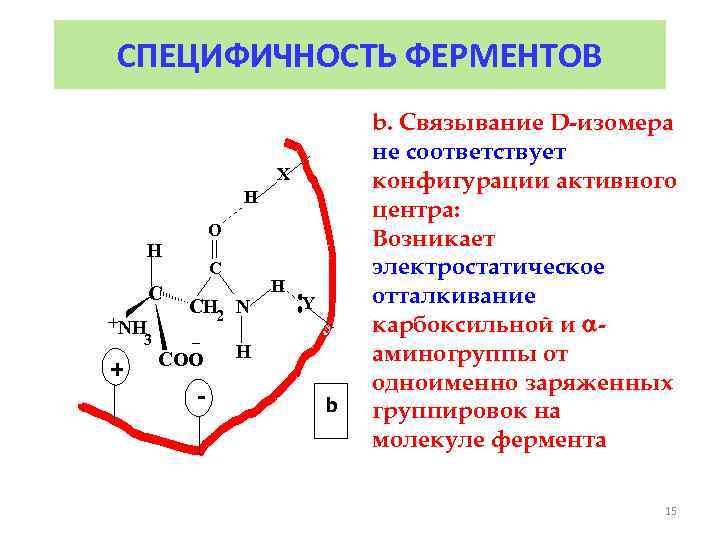 СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ X H O H C +NH 3 + C CH 2 N _ COO - H Y H b b. Связывание D-изомера не соответствует конфигурации активного центра: Возникает электростатическое отталкивание карбоксильной и аминогруппы от одноименно заряженных группировок на молекуле фермента 15
СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ X H O H C +NH 3 + C CH 2 N _ COO - H Y H b b. Связывание D-изомера не соответствует конфигурации активного центра: Возникает электростатическое отталкивание карбоксильной и аминогруппы от одноименно заряженных группировок на молекуле фермента 15
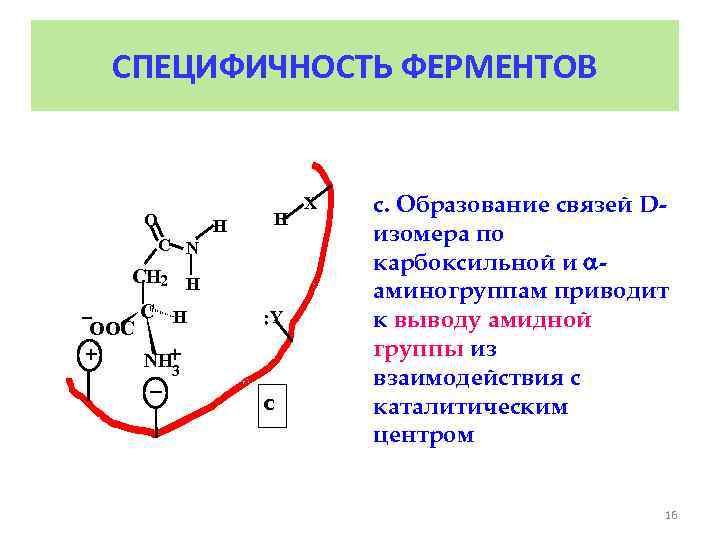 СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ O C N CH 2 H _ C H OOC + H H Y + NH 3 _ c X с. Образование связей Dизомера по карбоксильной и аминогруппам приводит к выводу амидной группы из взаимодействия с каталитическим центром 16
СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ O C N CH 2 H _ C H OOC + H H Y + NH 3 _ c X с. Образование связей Dизомера по карбоксильной и аминогруппам приводит к выводу амидной группы из взаимодействия с каталитическим центром 16
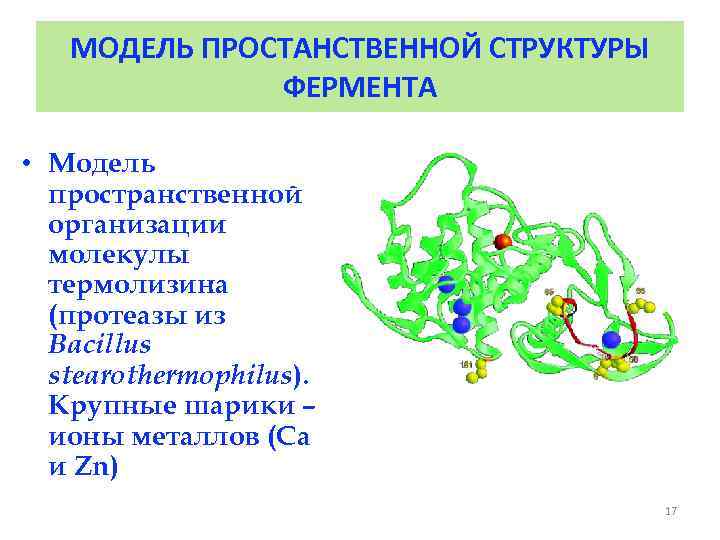 МОДЕЛЬ ПРОСТАНСТВЕННОЙ СТРУКТУРЫ ФЕРМЕНТА • Модель пространственной организации молекулы термолизина (протеазы из Васillus stearothermophilus). Крупные шарики – ионы металлов (Са и Zn) 17
МОДЕЛЬ ПРОСТАНСТВЕННОЙ СТРУКТУРЫ ФЕРМЕНТА • Модель пространственной организации молекулы термолизина (протеазы из Васillus stearothermophilus). Крупные шарики – ионы металлов (Са и Zn) 17
 ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • Принципиальная схема ферментативной реакции • S – субстрат, Е – фермент, ES – ферментсубстратный комплекс, Р – продукт, k – константы скоростей стадий 18
ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • Принципиальная схема ферментативной реакции • S – субстрат, Е – фермент, ES – ферментсубстратный комплекс, Р – продукт, k – константы скоростей стадий 18
 ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • Уравнение скорости (v) реакции может быть получено в виде, приведенном справа – уравнение Михаэлиса Ментен. • Vmax - максимальная скорость, • Кm - константа Михаэлиса 20
ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • Уравнение скорости (v) реакции может быть получено в виде, приведенном справа – уравнение Михаэлиса Ментен. • Vmax - максимальная скорость, • Кm - константа Михаэлиса 20
 ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • Скорость реакции равна максимальной при S>>Km. При этом Vmax =k 2 e, k 2 называют каталитической константой скорости • Соотношение k 2/Km часто называют каталитической эффективностью фермента 21
ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • Скорость реакции равна максимальной при S>>Km. При этом Vmax =k 2 e, k 2 называют каталитической константой скорости • Соотношение k 2/Km часто называют каталитической эффективностью фермента 21
 ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • Уравнение Михаэлиса может быть преобразовано в зависимость обратной скорости реакции (1/v) от обратной концентрации субстрата (1/[S]) 22
ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • Уравнение Михаэлиса может быть преобразовано в зависимость обратной скорости реакции (1/v) от обратной концентрации субстрата (1/[S]) 22
![ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • График зависимости 1/v от 1/[S] выглядит как прямая, отсекающая ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • График зависимости 1/v от 1/[S] выглядит как прямая, отсекающая](https://present5.com/presentation/3/151709482_347782440.pdf-img/151709482_347782440.pdf-22.jpg) ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • График зависимости 1/v от 1/[S] выглядит как прямая, отсекающая на оси ординат отрезок 1/Vmax, а на оси абсцисс – (– 1/Km) 1/v 1/Vmax 1/[S] -1/Km 23
ОСНОВЫ КИНЕТИКИ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ • График зависимости 1/v от 1/[S] выглядит как прямая, отсекающая на оси ординат отрезок 1/Vmax, а на оси абсцисс – (– 1/Km) 1/v 1/Vmax 1/[S] -1/Km 23
 ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • А) р. Н среды • Ферменты представляют собой белки. Свойства их определяются третичной структурой белковой молекулы, формируемой взаимодействием боковых цепей аминокислот. Среди аминокислотных остатков есть способные к ионизации (кислые аминокислоты – аспарагиновая и глутаминовая, основные аминокислоты – лизин, аргинин, гистидин), р. Н должен влиять на их взаимодействие, следовательно, и на структуру белковой глобулы. 24
ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • А) р. Н среды • Ферменты представляют собой белки. Свойства их определяются третичной структурой белковой молекулы, формируемой взаимодействием боковых цепей аминокислот. Среди аминокислотных остатков есть способные к ионизации (кислые аминокислоты – аспарагиновая и глутаминовая, основные аминокислоты – лизин, аргинин, гистидин), р. Н должен влиять на их взаимодействие, следовательно, и на структуру белковой глобулы. 24
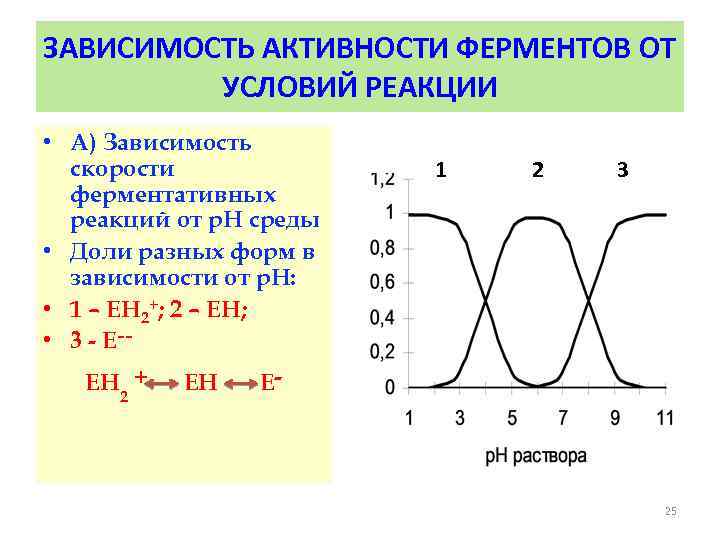 ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • А) Зависимость скорости ферментативных реакций от р. Н среды • Доли разных форм в зависимости от р. Н: • 1 – ЕН 2+; 2 – ЕН; • 3 - Е–– ЕН + ЕН Е- 1 2 3 2 25
ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • А) Зависимость скорости ферментативных реакций от р. Н среды • Доли разных форм в зависимости от р. Н: • 1 – ЕН 2+; 2 – ЕН; • 3 - Е–– ЕН + ЕН Е- 1 2 3 2 25
 ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • А) р. Н среды • Для каждого фермента существует р. Н -оптимум, который может заметно различаться у ферментов, катализирующих сходные реакции. Это необходимо учитывать при планировании технологического использования фермента 26
ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • А) р. Н среды • Для каждого фермента существует р. Н -оптимум, который может заметно различаться у ферментов, катализирующих сходные реакции. Это необходимо учитывать при планировании технологического использования фермента 26
 ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Б) Зависимость скорости ферментативных реакций от температуры • Зависимость скорости химической реакции от температуры выражается известным уравнением АРРЕНИУСА: 27
ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Б) Зависимость скорости ферментативных реакций от температуры • Зависимость скорости химической реакции от температуры выражается известным уравнением АРРЕНИУСА: 27
 ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Для ферментативных реакций зависимость осложняется тем, что параллельно с химической реакцией протекает еще один процесс – термическая денатурация фермента: 28
ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Для ферментативных реакций зависимость осложняется тем, что параллельно с химической реакцией протекает еще один процесс – термическая денатурация фермента: 28
 ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Константа равновесия процесса денатурации К зависит от температуры в соответствии с уравнением Вант-Гоффа: Экспоненциальный вариант этого выражения: 29
ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Константа равновесия процесса денатурации К зависит от температуры в соответствии с уравнением Вант-Гоффа: Экспоненциальный вариант этого выражения: 29
 ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Можно ввести величину «наблюдаемой» константы скорости ферментативной реакции: 30
ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Можно ввести величину «наблюдаемой» константы скорости ферментативной реакции: 30
 ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • С учетом ранее приведенного выражения для К: 31
ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • С учетом ранее приведенного выражения для К: 31
 ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Легко видеть, что при низких температурах, когда ΔS 0/R << ΔH 0/RT , экспоненциальный член в знаменателе мал по сравнению с 1, зависимость близка к Аррениусовской. При повышении температуры ΔH 0/RT быстро падает, экспонента в знаменателе растет, а скорость реакции падает. Появляется температурный оптимум. 32
ЗАВИСИМОСТЬ АКТИВНОСТИ ФЕРМЕНТОВ ОТ УСЛОВИЙ РЕАКЦИИ • Легко видеть, что при низких температурах, когда ΔS 0/R << ΔH 0/RT , экспоненциальный член в знаменателе мал по сравнению с 1, зависимость близка к Аррениусовской. При повышении температуры ΔH 0/RT быстро падает, экспонента в знаменателе растет, а скорость реакции падает. Появляется температурный оптимум. 32
 УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ • Белковая макромолекула при повышении температуры становится более гибкой. Это приводит к изменению специфичности ферментов при повышении температуры – ослабляются ограничения на природу и структуру субстрата. • Термодинамические расчеты здесь затруднены, однако следует иметь в виду, что повышение гибкости макромолекулы фермента должно приводить к увеличению энтропийного вклада в константу равновесия. 33
УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ • Белковая макромолекула при повышении температуры становится более гибкой. Это приводит к изменению специфичности ферментов при повышении температуры – ослабляются ограничения на природу и структуру субстрата. • Термодинамические расчеты здесь затруднены, однако следует иметь в виду, что повышение гибкости макромолекулы фермента должно приводить к увеличению энтропийного вклада в константу равновесия. 33
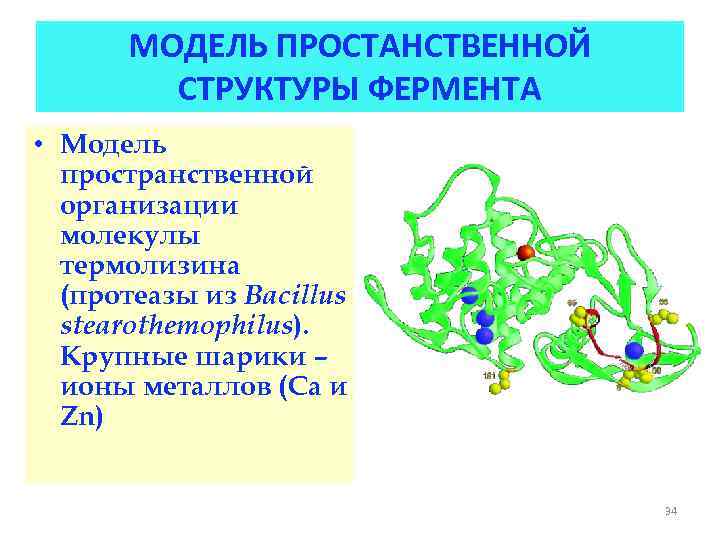 МОДЕЛЬ ПРОСТАНСТВЕННОЙ СТРУКТУРЫ ФЕРМЕНТА • Модель пространственной организации молекулы термолизина (протеазы из Васillus stearothemophilus). Крупные шарики – ионы металлов (Са и Zn) 34
МОДЕЛЬ ПРОСТАНСТВЕННОЙ СТРУКТУРЫ ФЕРМЕНТА • Модель пространственной организации молекулы термолизина (протеазы из Васillus stearothemophilus). Крупные шарики – ионы металлов (Са и Zn) 34
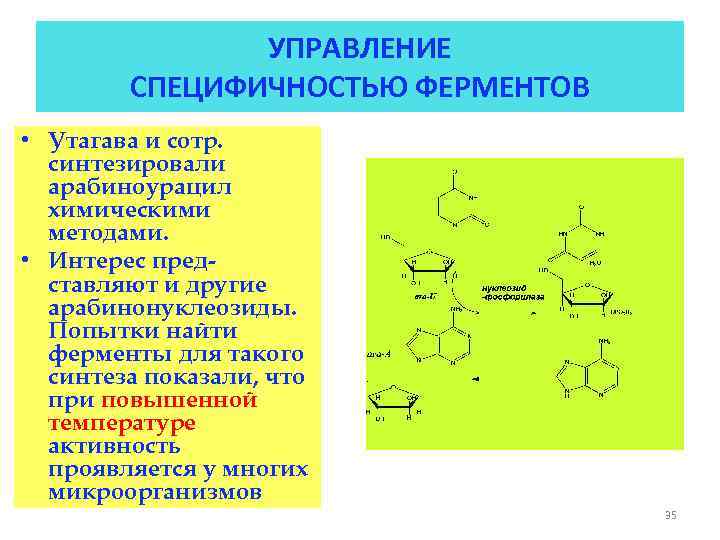 УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ • Утагава и сотр. синтезировали арабиноурацил химическими методами. • Интерес представляют и другие арабинонуклеозиды. Попытки найти ферменты для такого синтеза показали, что при повышенной температуре активность проявляется у многих микроорганизмов 35
УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ • Утагава и сотр. синтезировали арабиноурацил химическими методами. • Интерес представляют и другие арабинонуклеозиды. Попытки найти ферменты для такого синтеза показали, что при повышенной температуре активность проявляется у многих микроорганизмов 35
 УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ Род Escherichia Enterobacter Proteus Kluyvera Salmonella Citrobacter Ervinia Flavobacterium Количество изученных штаммов 33 Количество штаммов, образующих Ара-А 13 11 5 3 2 7 31 10 10 5 3 2 6 4 31 36
УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ Род Escherichia Enterobacter Proteus Kluyvera Salmonella Citrobacter Ervinia Flavobacterium Количество изученных штаммов 33 Количество штаммов, образующих Ара-А 13 11 5 3 2 7 31 10 10 5 3 2 6 4 31 36
 УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ • МОЛЕКУЛЯРНЫЙ ИМПРИНТИНГ – предварительная настройка фермента на субстрат. Фермент, способный катализировать реакции с различными субстратами, переводят в комплекс с тем из них, который нужен для решения данной задачи. Комплекс фиксируют тем или иным способом, а затем диссоциируют. Иными словами, в молекулу фермента «впечатывают» субстрат, формируя структуру белка таким образом, что она настроена на преимущественное взаимодействие именно с этим субстратом. 37
УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ • МОЛЕКУЛЯРНЫЙ ИМПРИНТИНГ – предварительная настройка фермента на субстрат. Фермент, способный катализировать реакции с различными субстратами, переводят в комплекс с тем из них, который нужен для решения данной задачи. Комплекс фиксируют тем или иным способом, а затем диссоциируют. Иными словами, в молекулу фермента «впечатывают» субстрат, формируя структуру белка таким образом, что она настроена на преимущественное взаимодействие именно с этим субстратом. 37
 УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ • Протеолитический фермент субтилизин Carlsberg катализирует переэтерификацию сахарозы и тимидина с винилбутиратом. Раствор, содержащий комплекс фермента с каждым из лигандов, замораживали и затем высушивали лиофильно. Конформационная подвижность молекулы фермента в твердом состоянии чрезвычайно низка, и белок сохраняет конформацию, сформировавшуюся при образовании комплекса. Результаты экспериментов показывают, что скорость переацилирования существенно выше тогда, когда катализатор предварительно настроен на соответствующий субстрат. 38
УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ • Протеолитический фермент субтилизин Carlsberg катализирует переэтерификацию сахарозы и тимидина с винилбутиратом. Раствор, содержащий комплекс фермента с каждым из лигандов, замораживали и затем высушивали лиофильно. Конформационная подвижность молекулы фермента в твердом состоянии чрезвычайно низка, и белок сохраняет конформацию, сформировавшуюся при образовании комплекса. Результаты экспериментов показывают, что скорость переацилирования существенно выше тогда, когда катализатор предварительно настроен на соответствующий субстрат. 38
 УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ 1, 2 – ацилирование сахарозы в пиридине; 3, 4 – ацилирование тимидина в тетрагидрофуране. Импринтинг: 1, 3 – сахарозой, 2, 4 – тимидином. По оси ординат – увеличение скорости реакции с импринтированным ферментом по отношению к неимпринтированному 39
УПРАВЛЕНИЕ СПЕЦИФИЧНОСТЬЮ ФЕРМЕНТОВ 1, 2 – ацилирование сахарозы в пиридине; 3, 4 – ацилирование тимидина в тетрагидрофуране. Импринтинг: 1, 3 – сахарозой, 2, 4 – тимидином. По оси ординат – увеличение скорости реакции с импринтированным ферментом по отношению к неимпринтированному 39
 ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ • Как компонент гомогенной реакционной смеси (добавление раствора фермента к раствору субстратов и других компонентов смеси) • Иммобилизованные ферменты • В виде целых микробных клеток (whole cell catalysts) 40
ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ • Как компонент гомогенной реакционной смеси (добавление раствора фермента к раствору субстратов и других компонентов смеси) • Иммобилизованные ферменты • В виде целых микробных клеток (whole cell catalysts) 40
 ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ • Применение ферментов как компонентов гомогенной реакционной смеси наименее выгодно, поскольку не допускает повторного использования фермента: выделять его из реакционной смеси нецелесообразно из-за больших затрат и неминуемых потерь 41
ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ • Применение ферментов как компонентов гомогенной реакционной смеси наименее выгодно, поскольку не допускает повторного использования фермента: выделять его из реакционной смеси нецелесообразно из-за больших затрат и неминуемых потерь 41
 ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ • Наиболее часто ферменты используются в иммобилизованном состоянии • Иммобилизация – ограничение подвижности фермента – достигается различными способами 42
ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ • Наиболее часто ферменты используются в иммобилизованном состоянии • Иммобилизация – ограничение подвижности фермента – достигается различными способами 42
 ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ Основные преимущества иммобилизованных ферментов: • Повышенная стабильность иммобилизованных ферментов по сравнению с «растворимыми» ; • Простота отделения фермента в активном состоянии от остальной реакционной смеси и возможность многократного использования; • Возможность организации непрерывного процесса. 43
ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ Основные преимущества иммобилизованных ферментов: • Повышенная стабильность иммобилизованных ферментов по сравнению с «растворимыми» ; • Простота отделения фермента в активном состоянии от остальной реакционной смеси и возможность многократного использования; • Возможность организации непрерывного процесса. 43
 ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ • Наиболее распространена иммобилизация ферментов путем присоединения к нерастворимому носителю – МАТРИЦЕ • Присоединение может осуществляться либо с образованием ковалентных связей молекул фермента с поверхностью матрицы, либо без образования таких связей 44
ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ • Наиболее распространена иммобилизация ферментов путем присоединения к нерастворимому носителю – МАТРИЦЕ • Присоединение может осуществляться либо с образованием ковалентных связей молекул фермента с поверхностью матрицы, либо без образования таких связей 44
 ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ Требования к МАТРИЦЕ (Дж. Порат, 1974) • Высокая химическая и биологическая стойкость • Высокая механическая прочность • Достаточная проницаемость для ферментов и субстратов, высокая удельная поверхность, высокая емкость, пористость 45
ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ Требования к МАТРИЦЕ (Дж. Порат, 1974) • Высокая химическая и биологическая стойкость • Высокая механическая прочность • Достаточная проницаемость для ферментов и субстратов, высокая удельная поверхность, высокая емкость, пористость 45
 ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ Требования к МАТРИЦЕ (продолжение): • Возможность получения в удобном для технологического применения виде (гранулы, мембраны, трубы, волокна и пр. ); • Простота перевода в реакционно-способное состояние; • Высокая гидрофильность – для проведения взаимодействия с ферментом в водной среде; • Относительно невысокая стоимость. Матриц, полностью отвечающих всем требованиям, нет 46
ФОРМЫ ПРИМЕНЕНИЯ ФЕРМЕНТОВ Требования к МАТРИЦЕ (продолжение): • Возможность получения в удобном для технологического применения виде (гранулы, мембраны, трубы, волокна и пр. ); • Простота перевода в реакционно-способное состояние; • Высокая гидрофильность – для проведения взаимодействия с ферментом в водной среде; • Относительно невысокая стоимость. Матриц, полностью отвечающих всем требованиям, нет 46
 КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ • В качестве матриц для присоединения ферментов в настоящее время используются природные полимеры и полимеры синтетического происхождения. • Природные полимеры могут быть разделены на группы в соответствии с их биохимической природой: • полисахаридные носители; • белки; • липидные носители. • Синтетические полимеры также могут быть разделены на группы в соответствии со строением основной цепи полимерных молекул: • полиметиленовые; • полиамидные; • полиэфиры. 47
КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ • В качестве матриц для присоединения ферментов в настоящее время используются природные полимеры и полимеры синтетического происхождения. • Природные полимеры могут быть разделены на группы в соответствии с их биохимической природой: • полисахаридные носители; • белки; • липидные носители. • Синтетические полимеры также могут быть разделены на группы в соответствии со строением основной цепи полимерных молекул: • полиметиленовые; • полиамидные; • полиэфиры. 47
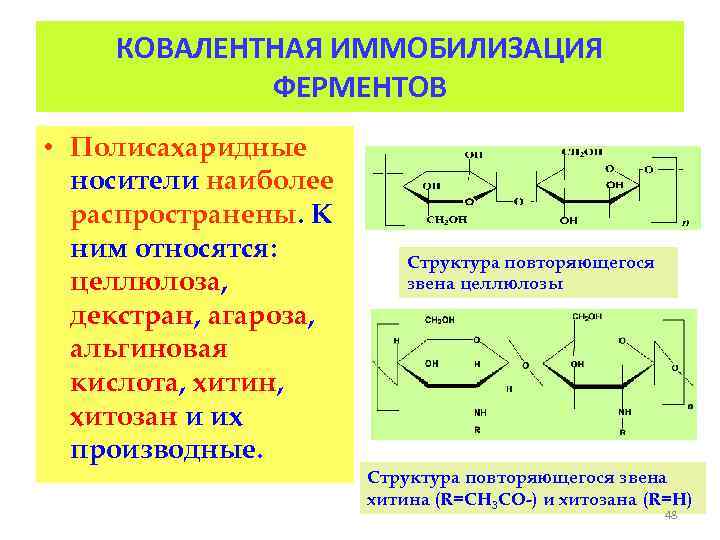 КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ • Полисахаридные носители наиболее распространены. К ним относятся: целлюлоза, декстран, агароза, альгиновая кислота, хитин, хитозан и их производные. Структура повторяющегося звена целлюлозы Структура повторяющегося звена хитина (R=CH 3 CO-) и хитозана (R=H) 48
КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ • Полисахаридные носители наиболее распространены. К ним относятся: целлюлоза, декстран, агароза, альгиновая кислота, хитин, хитозан и их производные. Структура повторяющегося звена целлюлозы Структура повторяющегося звена хитина (R=CH 3 CO-) и хитозана (R=H) 48
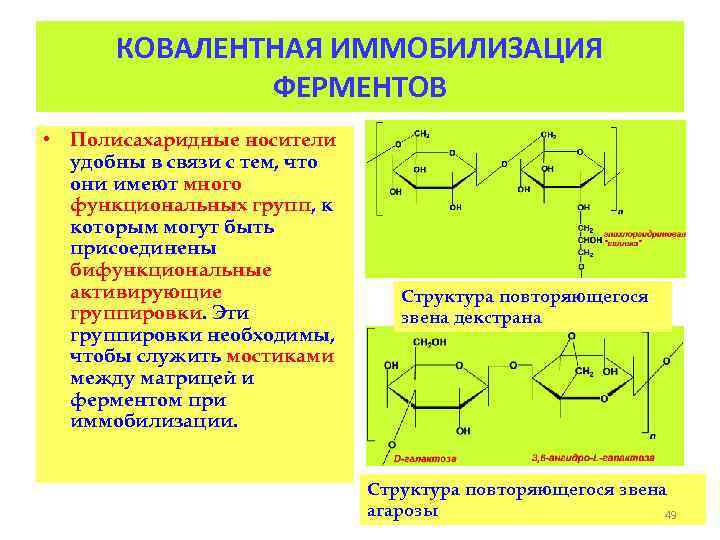 КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ • Полисахаридные носители удобны в связи с тем, что они имеют много функциональных групп, к которым могут быть присоединены бифункциональные активирующие группировки. Эти группировки необходимы, чтобы служить мостиками между матрицей и ферментом при иммобилизации. Структура повторяющегося звена декстрана Структура повторяющегося звена агарозы 49
КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ • Полисахаридные носители удобны в связи с тем, что они имеют много функциональных групп, к которым могут быть присоединены бифункциональные активирующие группировки. Эти группировки необходимы, чтобы служить мостиками между матрицей и ферментом при иммобилизации. Структура повторяющегося звена декстрана Структура повторяющегося звена агарозы 49
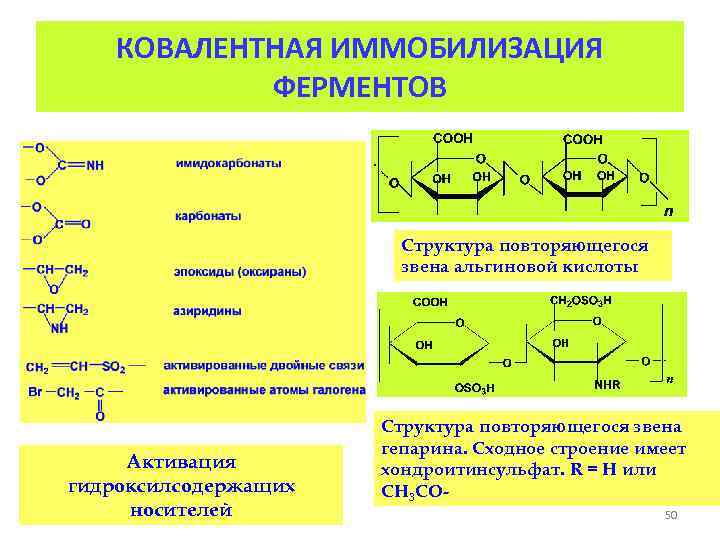 КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ Структура повторяющегося звена альгиновой кислоты Активация гидроксилсодержащих носителей Структура повторяющегося звена гепарина. Сходное строение имеет хондроитинсульфат. R = H или CH 3 CO 50
КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ Структура повторяющегося звена альгиновой кислоты Активация гидроксилсодержащих носителей Структура повторяющегося звена гепарина. Сходное строение имеет хондроитинсульфат. R = H или CH 3 CO 50
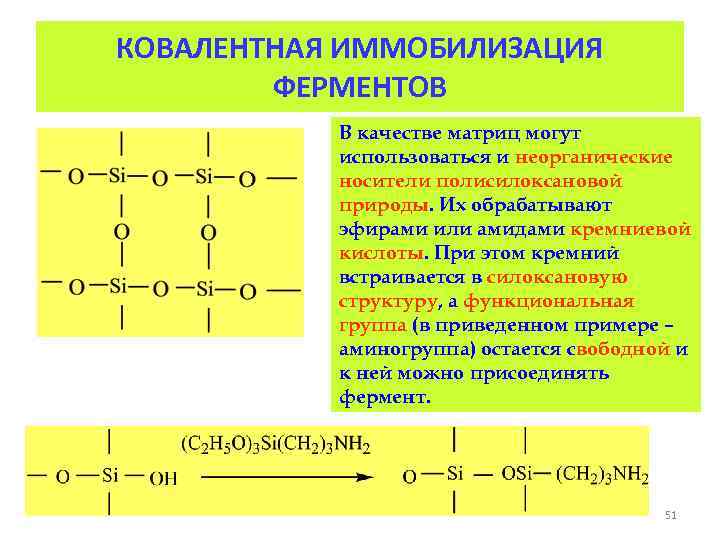 КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ В качестве матриц могут использоваться и неорганические носители полисилоксановой природы. Их обрабатывают эфирами или амидами кремниевой кислоты. При этом кремний встраивается в силоксановую структуру, а функциональная группа (в приведенном примере – аминогруппа) остается свободной и к ней можно присоединять фермент. 51
КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ В качестве матриц могут использоваться и неорганические носители полисилоксановой природы. Их обрабатывают эфирами или амидами кремниевой кислоты. При этом кремний встраивается в силоксановую структуру, а функциональная группа (в приведенном примере – аминогруппа) остается свободной и к ней можно присоединять фермент. 51
 КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ Модификация поверхности силикатного носителя может осуществляться различными производными силанов: -цианопропилтриметоксисилан (I), глицидоксипропилтриметоксисилан (II) и меркаптопропилтриметоксисилан (III). При этом на поверхности носителя появляются функциональные группы для присоединения фермента 52
КОВАЛЕНТНАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ Модификация поверхности силикатного носителя может осуществляться различными производными силанов: -цианопропилтриметоксисилан (I), глицидоксипропилтриметоксисилан (II) и меркаптопропилтриметоксисилан (III). При этом на поверхности носителя появляются функциональные группы для присоединения фермента 52
 ФИЗИЧЕСКАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ • Методы иммобилизации ферментов без образования ковалентной связи с матрицей часто называют физическими. • Условно такие методы можно разделить на следующие группы: • 1) адсорбция ферментов на нерастворимых носителях; • 2) включение в поры геля; • 3) пространственное отделение фермента от остальной части реакционного пространства с помощью полупроницаемой перегородки (мембраны); • 4) включение в двухфазную реакционную среду, когда фермент может находиться и проявлять каталитическую активность лишь в одной из имеющихся в системе фаз (этот случай может рассматриваться как один из вариантов предыдущего, роль мембраны при этом играет межфазовая граница). 53
ФИЗИЧЕСКАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ • Методы иммобилизации ферментов без образования ковалентной связи с матрицей часто называют физическими. • Условно такие методы можно разделить на следующие группы: • 1) адсорбция ферментов на нерастворимых носителях; • 2) включение в поры геля; • 3) пространственное отделение фермента от остальной части реакционного пространства с помощью полупроницаемой перегородки (мембраны); • 4) включение в двухфазную реакционную среду, когда фермент может находиться и проявлять каталитическую активность лишь в одной из имеющихся в системе фаз (этот случай может рассматриваться как один из вариантов предыдущего, роль мембраны при этом играет межфазовая граница). 53
 ФИЗИЧЕСКАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ Е Е носитель Е водная фаза Е Е Е фермент Полупроницаемая мембрана Варианты физической иммобилизации ферментов: Сорбция на поверхности Помещение фермента в контур , отделенный от основного раствора полупроницаемой мембраной; в качестве полупроницаемой мембраны может выступать межфазовая граница (между водной и органической фазами) 54
ФИЗИЧЕСКАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ Е Е носитель Е водная фаза Е Е Е фермент Полупроницаемая мембрана Варианты физической иммобилизации ферментов: Сорбция на поверхности Помещение фермента в контур , отделенный от основного раствора полупроницаемой мембраной; в качестве полупроницаемой мембраны может выступать межфазовая граница (между водной и органической фазами) 54
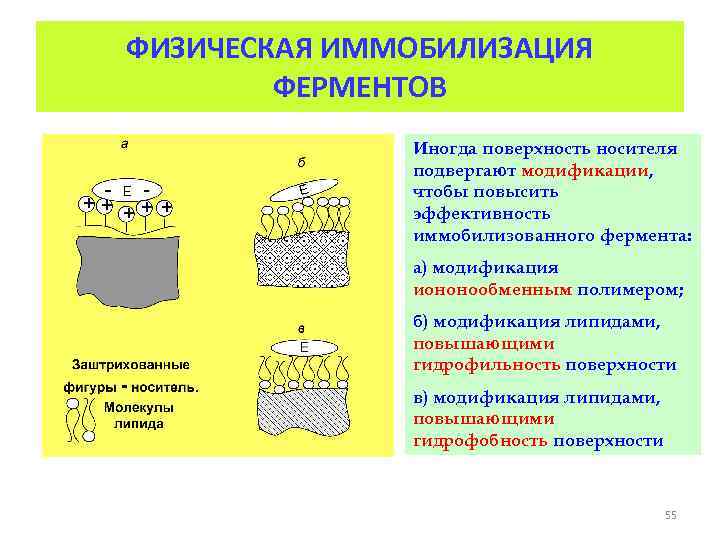 ФИЗИЧЕСКАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ Иногда поверхность носителя подвергают модификации, чтобы повысить эффективность иммобилизованного фермента: а) модификация иононообменным полимером; б) модификация липидами, повышающими гидрофильность поверхности в) модификация липидами, повышающими гидрофобность поверхности 55
ФИЗИЧЕСКАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ Иногда поверхность носителя подвергают модификации, чтобы повысить эффективность иммобилизованного фермента: а) модификация иононообменным полимером; б) модификация липидами, повышающими гидрофильность поверхности в) модификация липидами, повышающими гидрофобность поверхности 55
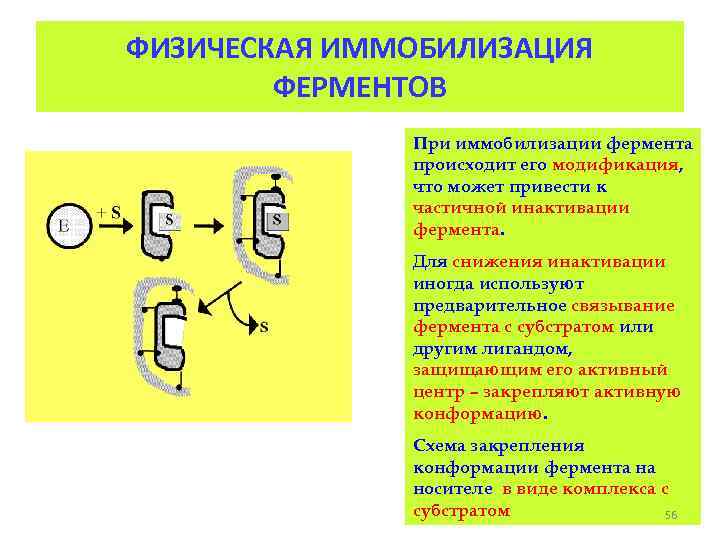 ФИЗИЧЕСКАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ При иммобилизации фермента происходит его модификация, что может привести к частичной инактивации фермента. Для снижения инактивации иногда используют предварительное связывание фермента с субстратом или другим лигандом, защищающим его активный центр – закрепляют активную конформацию. Схема закрепления конформации фермента на носителе в виде комплекса с субстратом 56
ФИЗИЧЕСКАЯ ИММОБИЛИЗАЦИЯ ФЕРМЕНТОВ При иммобилизации фермента происходит его модификация, что может привести к частичной инактивации фермента. Для снижения инактивации иногда используют предварительное связывание фермента с субстратом или другим лигандом, защищающим его активный центр – закрепляют активную конформацию. Схема закрепления конформации фермента на носителе в виде комплекса с субстратом 56
 ПРИМЕНЕНИЕ ФЕРМЕНТОВ В ПРОМЫШЛЕННЫХ ТЕХНОЛОГИЯХ 1 – гидролазы (63%) 2 – оксидоредуктазы (25%) 3 – трансферазы (5%) 4 – лиазы (5%) 5 – изомеразы (1%) 6 – лигазы (1%) Относительная частота использования ферментов различных классов в промышленности Faber, K. Biotransformations. In: Organic Chemistry: A Textbook, 3 rd Ed. ; Springer. Verlag: Berlin, Germany, 1997. 57
ПРИМЕНЕНИЕ ФЕРМЕНТОВ В ПРОМЫШЛЕННЫХ ТЕХНОЛОГИЯХ 1 – гидролазы (63%) 2 – оксидоредуктазы (25%) 3 – трансферазы (5%) 4 – лиазы (5%) 5 – изомеразы (1%) 6 – лигазы (1%) Относительная частота использования ферментов различных классов в промышленности Faber, K. Biotransformations. In: Organic Chemistry: A Textbook, 3 rd Ed. ; Springer. Verlag: Berlin, Germany, 1997. 57
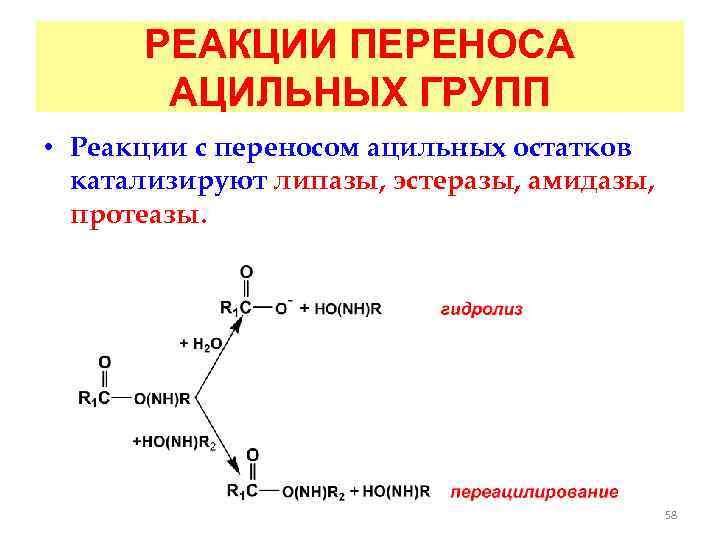 РЕАКЦИИ ПЕРЕНОСА АЦИЛЬНЫХ ГРУПП • Реакции с переносом ацильных остатков катализируют липазы, эстеразы, амидазы, протеазы. 58
РЕАКЦИИ ПЕРЕНОСА АЦИЛЬНЫХ ГРУПП • Реакции с переносом ацильных остатков катализируют липазы, эстеразы, амидазы, протеазы. 58
 РАВНОВЕСИЕ В РЕАКЦИЯХ ГИДРОЛИЗА • Выражение для константы равновесия записано справа. • ci – концентрации исходных веществ и продуктов, • cw – концентрация воды 59
РАВНОВЕСИЕ В РЕАКЦИЯХ ГИДРОЛИЗА • Выражение для константы равновесия записано справа. • ci – концентрации исходных веществ и продуктов, • cw – концентрация воды 59
 РЕАКЦИИ ПЕРЕНОСА АЦИЛЬНЫХ ГРУПП • При использовании в задачах по синтезу различных соединений речь идет обычно о реакциях переацилирования: • 60
РЕАКЦИИ ПЕРЕНОСА АЦИЛЬНЫХ ГРУПП • При использовании в задачах по синтезу различных соединений речь идет обычно о реакциях переацилирования: • 60
 РЕАКЦИИ ПЕРЕНОСА АЦИЛЬНЫХ ГРУПП • В таких реакциях G 0 обычно близко к 0, а константа равновесия, соответственно, близка к 1. • Однако, если реакция проводится в водной среде, то параллельно протекающая реакция гидролиза преобладает из-за высокой концентрации воды. 61
РЕАКЦИИ ПЕРЕНОСА АЦИЛЬНЫХ ГРУПП • В таких реакциях G 0 обычно близко к 0, а константа равновесия, соответственно, близка к 1. • Однако, если реакция проводится в водной среде, то параллельно протекающая реакция гидролиза преобладает из-за высокой концентрации воды. 61
 ПЕРЕНОС АЦИЛЬНЫХ ГРУПП • Для достижения эффективного переацилирования реакции проводят в системах с пониженным содержанием воды или в двухфазных системах. При этом концентрация воды в системе понижается, и равновесие может сдвинуться в желаемую сторону. 62
ПЕРЕНОС АЦИЛЬНЫХ ГРУПП • Для достижения эффективного переацилирования реакции проводят в системах с пониженным содержанием воды или в двухфазных системах. При этом концентрация воды в системе понижается, и равновесие может сдвинуться в желаемую сторону. 62
 ПЕРЕНОС АЦИЛЬНЫХ ГРУПП • Компоненты реакционной смеси в двухфазной системе распределяются между жидкими фазами в соответствии с коэффициентами распределения 63
ПЕРЕНОС АЦИЛЬНЫХ ГРУПП • Компоненты реакционной смеси в двухфазной системе распределяются между жидкими фазами в соответствии с коэффициентами распределения 63
 ПЕРЕНОС АЦИЛЬНЫХ ГРУПП • С учетом распределения компонентов реакционной смеси между двумя жидкими фазами можно показать, что константа равновесия будет выглядеть так: 64
ПЕРЕНОС АЦИЛЬНЫХ ГРУПП • С учетом распределения компонентов реакционной смеси между двумя жидкими фазами можно показать, что константа равновесия будет выглядеть так: 64
 ПЕРЕНОС АЦИЛЬНЫХ ГРУПП • Пусть коэффициенты распределения исходных веществ и продукта реакции подчиняются условию: • В этом случае Кbp>>Kw, равновесие смещается в сторону синтеза 65
ПЕРЕНОС АЦИЛЬНЫХ ГРУПП • Пусть коэффициенты распределения исходных веществ и продукта реакции подчиняются условию: • В этом случае Кbp>>Kw, равновесие смещается в сторону синтеза 65
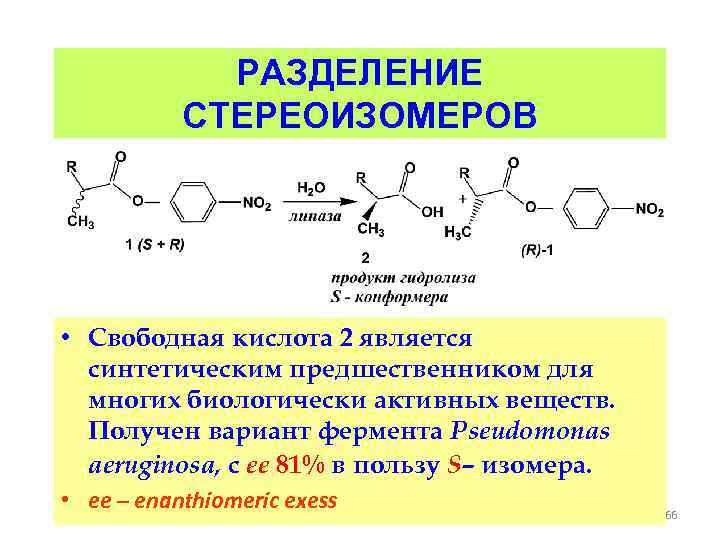 РАЗДЕЛЕНИЕ СТЕРЕОИЗОМЕРОВ • Свободная кислота 2 является синтетическим предшественником для многих биологически активных веществ. Получен вариант фермента Pseudomonas aeruginosa, с ее 81% в пользу S– изомера. • ee – enanthiomeric exess 66
РАЗДЕЛЕНИЕ СТЕРЕОИЗОМЕРОВ • Свободная кислота 2 является синтетическим предшественником для многих биологически активных веществ. Получен вариант фермента Pseudomonas aeruginosa, с ее 81% в пользу S– изомера. • ee – enanthiomeric exess 66
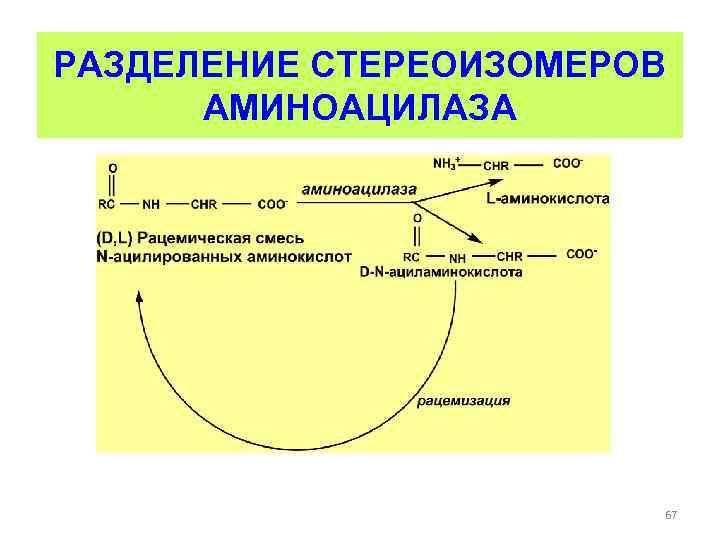 РАЗДЕЛЕНИЕ СТЕРЕОИЗОМЕРОВ АМИНОАЦИЛАЗА 67
РАЗДЕЛЕНИЕ СТЕРЕОИЗОМЕРОВ АМИНОАЦИЛАЗА 67
 РАЗДЕЛЕНИЕ СТЕРЕОИЗОМЕРОВ • В природе встречаются и D-аминокислоты, которые являются компонентами клеточных стенок бактерий, входят в состав некоторых пептидных антибиотиков. • В фармацевтической промышленности их производные часто используются как полупродукты в синтезе фармпрепаратов. 68
РАЗДЕЛЕНИЕ СТЕРЕОИЗОМЕРОВ • В природе встречаются и D-аминокислоты, которые являются компонентами клеточных стенок бактерий, входят в состав некоторых пептидных антибиотиков. • В фармацевтической промышленности их производные часто используются как полупродукты в синтезе фармпрепаратов. 68
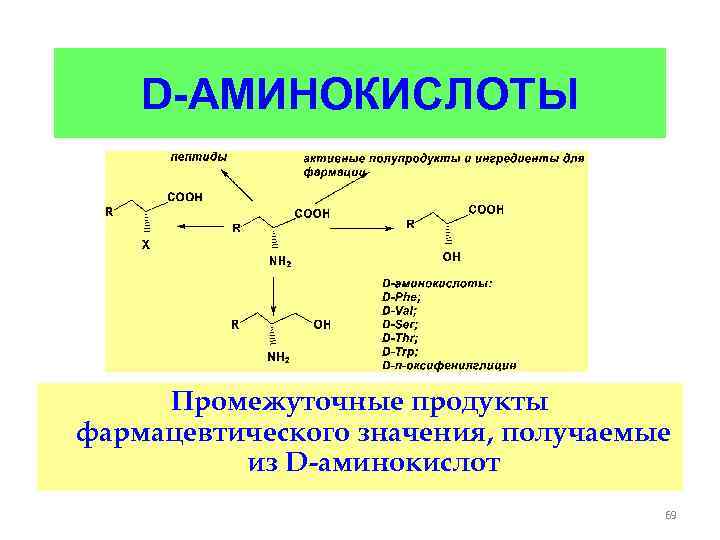 D-АМИНОКИСЛОТЫ Промежуточные продукты фармацевтического значения, получаемые из D-аминокислот 69
D-АМИНОКИСЛОТЫ Промежуточные продукты фармацевтического значения, получаемые из D-аминокислот 69
 РАЗДЕЛЕНИЕ СТЕРЕОИЗОМЕРОВ • Найдены микроорганизмы, у которых имеются ферменты – ацилазы N-ацил-Dаминокислот. Эти ферменты обладают строгой специфичностью к оптической конфигурации субстрата и специфичны к природе аминокислот. • Для D-аспарагиновой, D-глутаминовой кислот и для аминокислот с углеводородной боковой цепью существуют различные ферменты с неперекрывающейся специфичностью. 70
РАЗДЕЛЕНИЕ СТЕРЕОИЗОМЕРОВ • Найдены микроорганизмы, у которых имеются ферменты – ацилазы N-ацил-Dаминокислот. Эти ферменты обладают строгой специфичностью к оптической конфигурации субстрата и специфичны к природе аминокислот. • Для D-аспарагиновой, D-глутаминовой кислот и для аминокислот с углеводородной боковой цепью существуют различные ферменты с неперекрывающейся специфичностью. 70
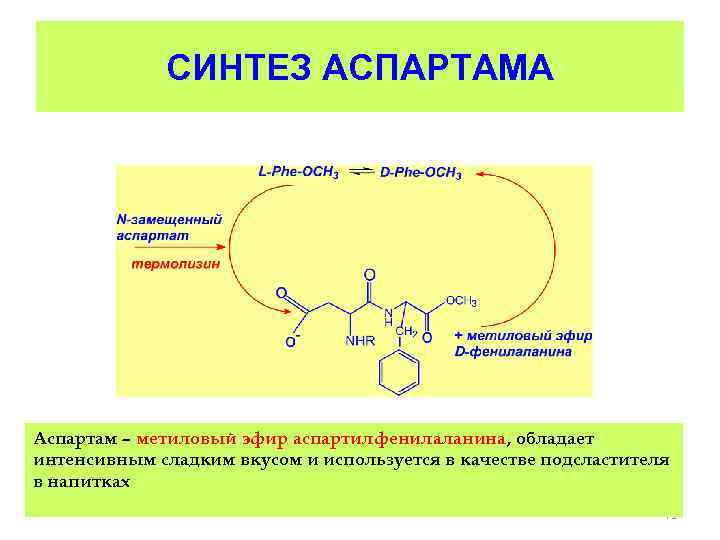 СИНТЕЗ АСПАРТАМА Аспартам – метиловый эфир аспартилфенилаланина, обладает интенсивным сладким вкусом и используется в качестве подсластителя в напитках 71
СИНТЕЗ АСПАРТАМА Аспартам – метиловый эфир аспартилфенилаланина, обладает интенсивным сладким вкусом и используется в качестве подсластителя в напитках 71
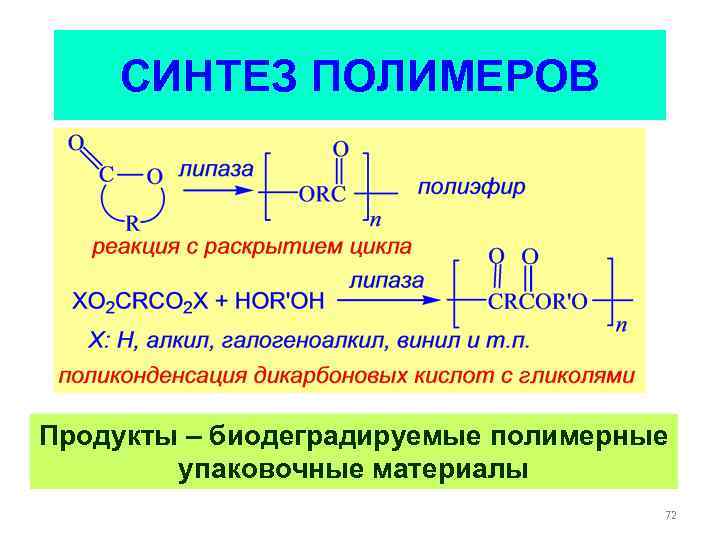 СИНТЕЗ ПОЛИМЕРОВ Продукты – биодеградируемые полимерные упаковочные материалы 72
СИНТЕЗ ПОЛИМЕРОВ Продукты – биодеградируемые полимерные упаковочные материалы 72
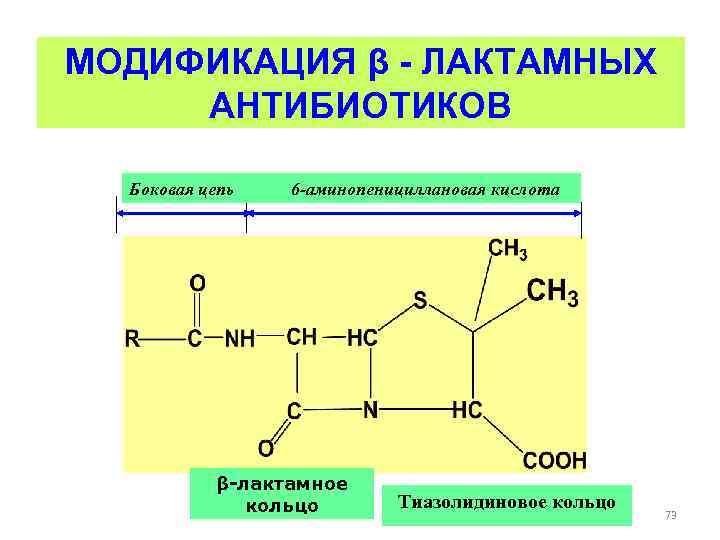 МОДИФИКАЦИЯ β - ЛАКТАМНЫХ АНТИБИОТИКОВ Боковая цепь 6 -аминопенициллановая кислота β-лактамное кольцо Тиазолидиновое кольцо 73
МОДИФИКАЦИЯ β - ЛАКТАМНЫХ АНТИБИОТИКОВ Боковая цепь 6 -аминопенициллановая кислота β-лактамное кольцо Тиазолидиновое кольцо 73
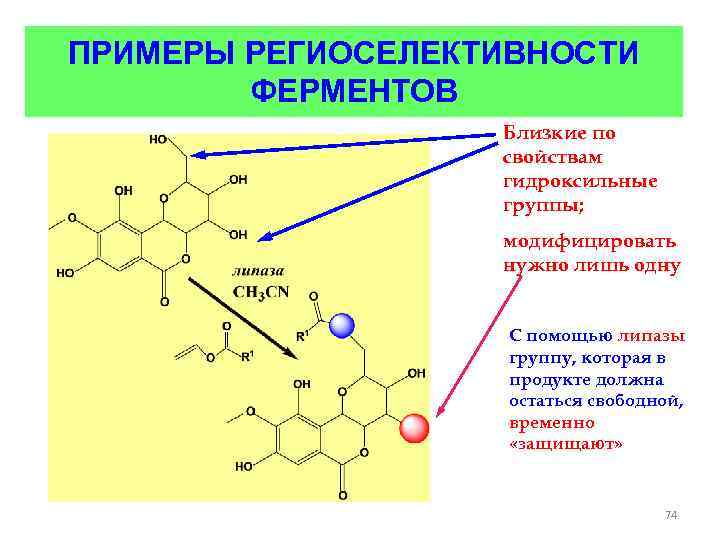 ПРИМЕРЫ РЕГИОСЕЛЕКТИВНОСТИ ФЕРМЕНТОВ Близкие по свойствам гидроксильные группы; модифицировать нужно лишь одну С помощью липазы группу, которая в продукте должна остаться свободной, временно «защищают» 74
ПРИМЕРЫ РЕГИОСЕЛЕКТИВНОСТИ ФЕРМЕНТОВ Близкие по свойствам гидроксильные группы; модифицировать нужно лишь одну С помощью липазы группу, которая в продукте должна остаться свободной, временно «защищают» 74
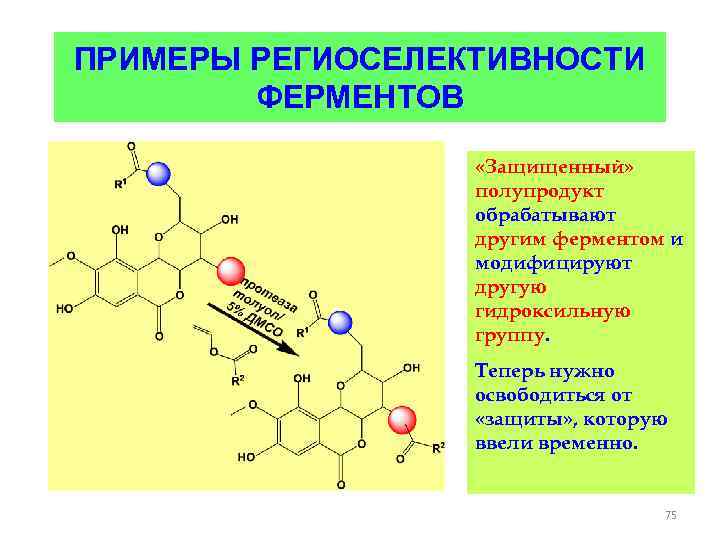 ПРИМЕРЫ РЕГИОСЕЛЕКТИВНОСТИ ФЕРМЕНТОВ «Защищенный» полупродукт обрабатывают другим ферментом и модифицируют другую гидроксильную группу. Теперь нужно освободиться от «защиты» , которую ввели временно. 75
ПРИМЕРЫ РЕГИОСЕЛЕКТИВНОСТИ ФЕРМЕНТОВ «Защищенный» полупродукт обрабатывают другим ферментом и модифицируют другую гидроксильную группу. Теперь нужно освободиться от «защиты» , которую ввели временно. 75
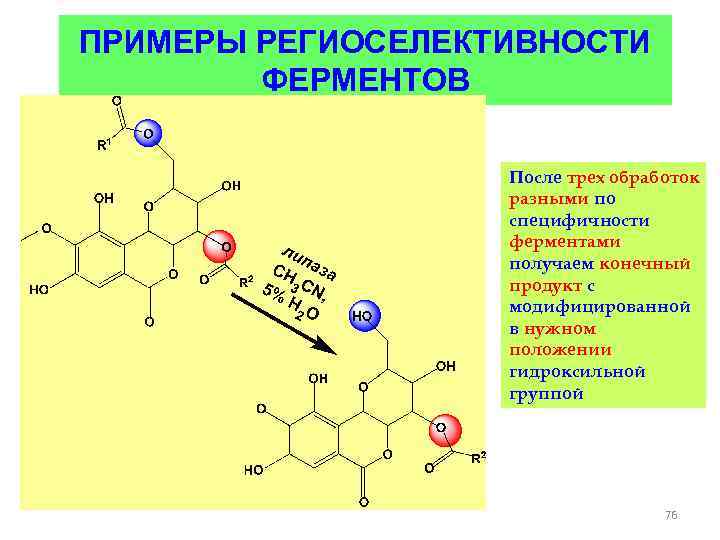 ПРИМЕРЫ РЕГИОСЕЛЕКТИВНОСТИ ФЕРМЕНТОВ После трех обработок разными по специфичности ферментами получаем конечный продукт с модифицированной в нужном положении гидроксильной группой 76
ПРИМЕРЫ РЕГИОСЕЛЕКТИВНОСТИ ФЕРМЕНТОВ После трех обработок разными по специфичности ферментами получаем конечный продукт с модифицированной в нужном положении гидроксильной группой 76
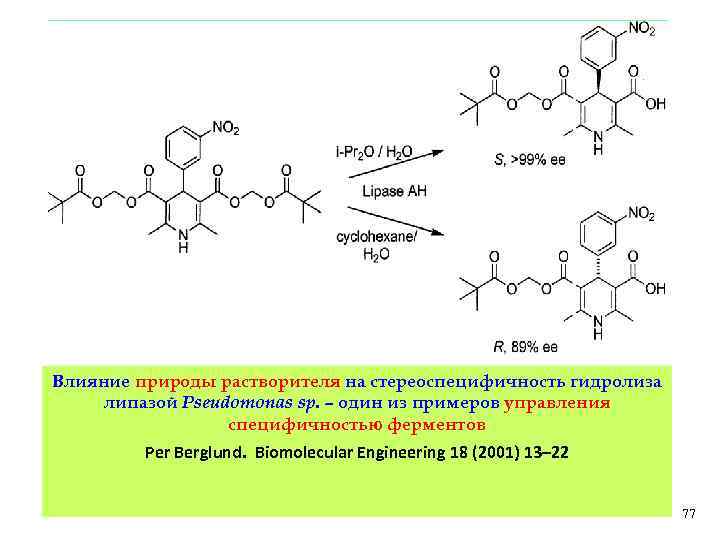 Влияние природы растворителя на стереоспецифичность гидролиза липазой Pseudomonas sp. – один из примеров управления специфичностью ферментов Per Berglund. Biomolecular Engineering 18 (2001) 13– 22 77
Влияние природы растворителя на стереоспецифичность гидролиза липазой Pseudomonas sp. – один из примеров управления специфичностью ферментов Per Berglund. Biomolecular Engineering 18 (2001) 13– 22 77
 РАЗДЕЛЕНИЕ СТРЕРЕОИЗОМЕРОВ ЛИНАЛООЛА 78
РАЗДЕЛЕНИЕ СТРЕРЕОИЗОМЕРОВ ЛИНАЛООЛА 78
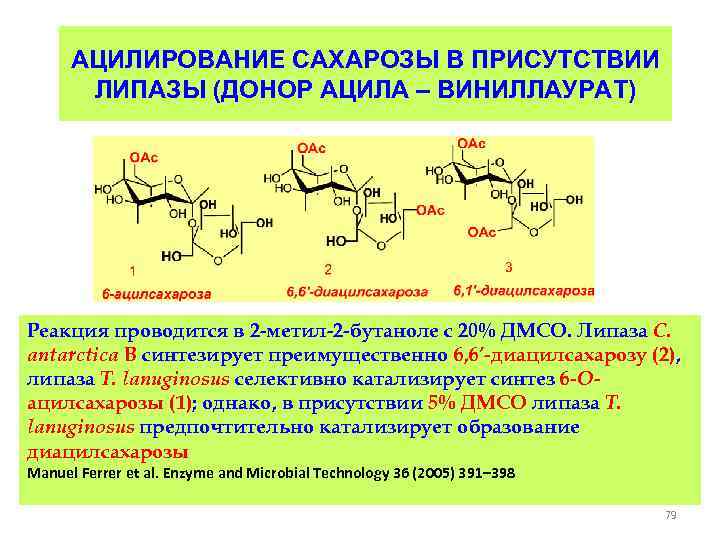 АЦИЛИРОВАНИЕ САХАРОЗЫ В ПРИСУТСТВИИ ЛИПАЗЫ (ДОНОР АЦИЛА – ВИНИЛЛАУРАТ) Реакция проводится в 2 -метил-2 -бутаноле с 20% ДМСО. Липаза C. antarctica B синтезирует преимущественно 6, 6’-диацилсахарозу (2), липаза T. lanuginosus селективно катализирует синтез 6 -Oацилсахарозы (1); однако, в присутствии 5% ДМСО липаза T. lanuginosus предпочтительно катализирует образование диацилсахарозы Manuel Ferrer et al. Enzyme and Microbial Technology 36 (2005) 391– 398 79
АЦИЛИРОВАНИЕ САХАРОЗЫ В ПРИСУТСТВИИ ЛИПАЗЫ (ДОНОР АЦИЛА – ВИНИЛЛАУРАТ) Реакция проводится в 2 -метил-2 -бутаноле с 20% ДМСО. Липаза C. antarctica B синтезирует преимущественно 6, 6’-диацилсахарозу (2), липаза T. lanuginosus селективно катализирует синтез 6 -Oацилсахарозы (1); однако, в присутствии 5% ДМСО липаза T. lanuginosus предпочтительно катализирует образование диацилсахарозы Manuel Ferrer et al. Enzyme and Microbial Technology 36 (2005) 391– 398 79
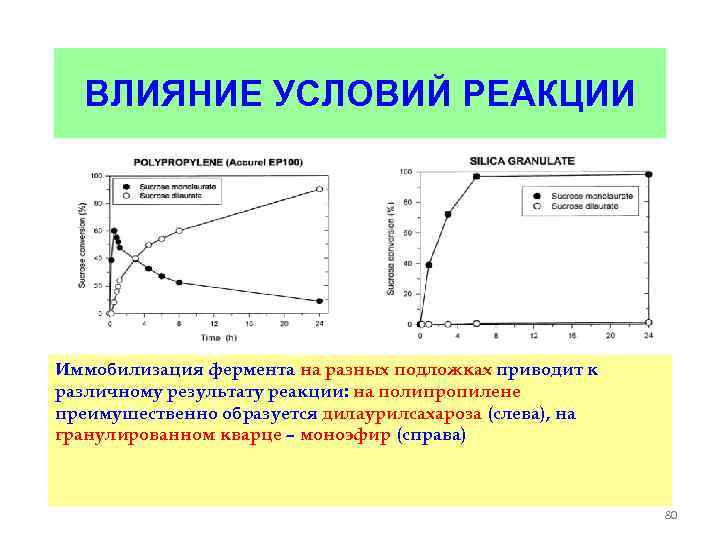 ВЛИЯНИЕ УСЛОВИЙ РЕАКЦИИ Иммобилизация фермента на разных подложках приводит к различному результату реакции: на полипропилене преимушественно образуется дилаурилсахароза (слева), на гранулированном кварце – моноэфир (справа) 80
ВЛИЯНИЕ УСЛОВИЙ РЕАКЦИИ Иммобилизация фермента на разных подложках приводит к различному результату реакции: на полипропилене преимушественно образуется дилаурилсахароза (слева), на гранулированном кварце – моноэфир (справа) 80
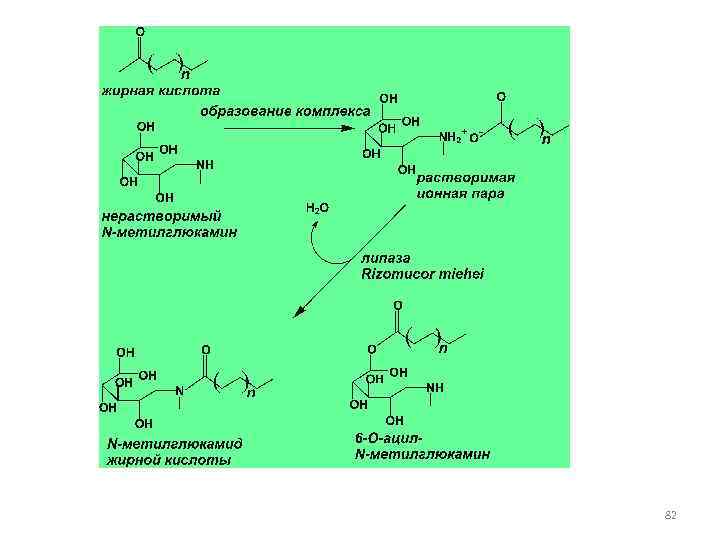
 СИНТЕЗ АМИДОВ • В неводных средах гидрофильные амины растворяются плохо • Для получения амидов с гидрофобными жирными кислотами используют технику с образованием ионных пар, которые растворяются в органических средах • Липазы способны работать в органических средах 81
СИНТЕЗ АМИДОВ • В неводных средах гидрофильные амины растворяются плохо • Для получения амидов с гидрофобными жирными кислотами используют технику с образованием ионных пар, которые растворяются в органических средах • Липазы способны работать в органических средах 81
 82
82
 ИОННЫЕ РАСТВОРИТЕЛИ КАК СРЕДЫ ДЛЯ ПРОВЕДЕНИЯ РЕАКЦИЙ • Помимо воды, водно-органических и органических растворителей в качестве сред для реакций трансацилирования используют «ионные жидкости» : • 1 -октил-3 -нонилимидазолийгексафторфосфат ([onim]PF 6) • 1 -бутил-3 -метилимидазолийгексафторфосфат ([bmim]PF 6) 83
ИОННЫЕ РАСТВОРИТЕЛИ КАК СРЕДЫ ДЛЯ ПРОВЕДЕНИЯ РЕАКЦИЙ • Помимо воды, водно-органических и органических растворителей в качестве сред для реакций трансацилирования используют «ионные жидкости» : • 1 -октил-3 -нонилимидазолийгексафторфосфат ([onim]PF 6) • 1 -бутил-3 -метилимидазолийгексафторфосфат ([bmim]PF 6) 83
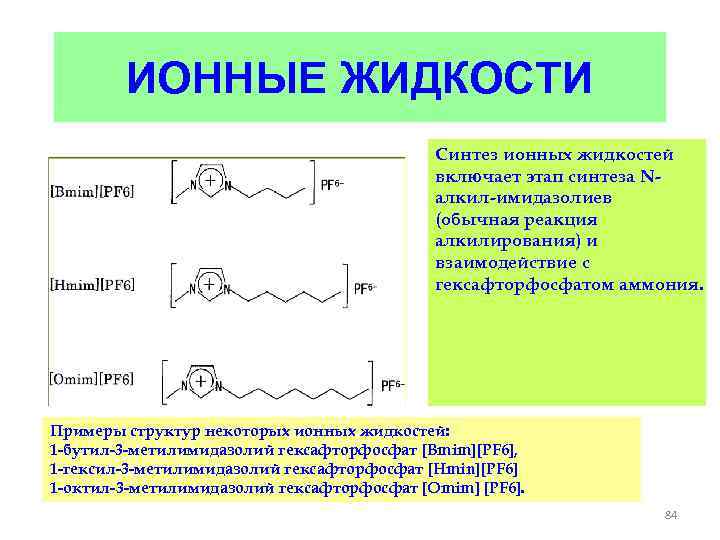 ИОННЫЕ ЖИДКОСТИ Синтез ионных жидкостей включает этап синтеза Nалкил-имидазолиев (обычная реакция алкилирования) и взаимодействие с гексафторфосфатом аммония. Примеры структур некоторых ионных жидкостей: 1 -бутил-3 -метилимидазолий гексафторфосфат [Bmim][PF 6], 1 -гексил-3 -метилимидазолий гексафторфосфат [Hmin][PF 6] 1 -октил-3 -метилимидазолий гексафторфосфат [Omim] [PF 6]. 84
ИОННЫЕ ЖИДКОСТИ Синтез ионных жидкостей включает этап синтеза Nалкил-имидазолиев (обычная реакция алкилирования) и взаимодействие с гексафторфосфатом аммония. Примеры структур некоторых ионных жидкостей: 1 -бутил-3 -метилимидазолий гексафторфосфат [Bmim][PF 6], 1 -гексил-3 -метилимидазолий гексафторфосфат [Hmin][PF 6] 1 -октил-3 -метилимидазолий гексафторфосфат [Omim] [PF 6]. 84
 ОКСИДОРЕДУКТАЗЫ • Оксидоредуктазы – один из наиболее широко представленных и разнообразных классов ферментов • Поскольку окислительновосстановительные реакции сопряжены с переносом электронов, ферменты требуют кофакторов 85
ОКСИДОРЕДУКТАЗЫ • Оксидоредуктазы – один из наиболее широко представленных и разнообразных классов ферментов • Поскольку окислительновосстановительные реакции сопряжены с переносом электронов, ферменты требуют кофакторов 85
 ОКСИДОРЕДУКТАЗЫ • Кофакторы оксидоредуктаз: Никотинамидные коферменты (ферменты группы дегидрогеназ); Флавиновые коферменты и простетические группы (оксидазы); Гемы (пероксидазы, цитохромы и т. п. ); Хиноны; Комплексы железа. 86
ОКСИДОРЕДУКТАЗЫ • Кофакторы оксидоредуктаз: Никотинамидные коферменты (ферменты группы дегидрогеназ); Флавиновые коферменты и простетические группы (оксидазы); Гемы (пероксидазы, цитохромы и т. п. ); Хиноны; Комплексы железа. 86
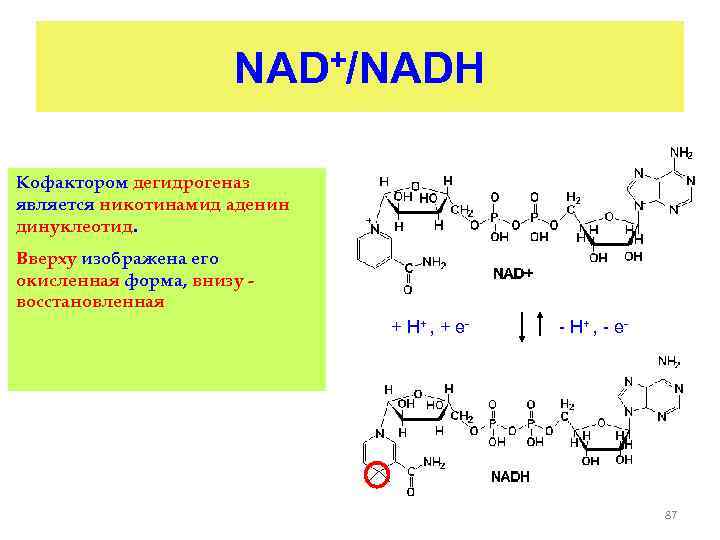 NAD+/NADH Кофактором дегидрогеназ является никотинамид аденин динуклеотид. Вверху изображена его окисленная форма, внизу восстановленная + H+ , + e - - H+ , - e - 87
NAD+/NADH Кофактором дегидрогеназ является никотинамид аденин динуклеотид. Вверху изображена его окисленная форма, внизу восстановленная + H+ , + e - - H+ , - e - 87
 FAD/FADH 2 + 2 H+ , + 2 e- - 2 H+ , - 2 e- Кофактором многих оксидоредуктаз являются производные рибофлавина, например флавинадениндинуклеотид. Слева изображена его окисленная форма, справа – восстановленная. 88
FAD/FADH 2 + 2 H+ , + 2 e- - 2 H+ , - 2 e- Кофактором многих оксидоредуктаз являются производные рибофлавина, например флавинадениндинуклеотид. Слева изображена его окисленная форма, справа – восстановленная. 88
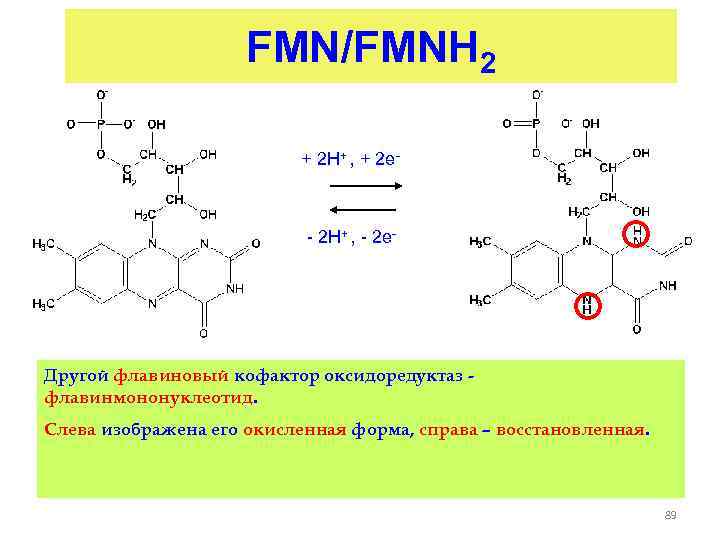 FMN/FMNH 2 + 2 H+ , + 2 e- - 2 H+ , - 2 e- Другой флавиновый кофактор оксидоредуктаз флавинмононуклеотид. Слева изображена его окисленная форма, справа – восстановленная. 89
FMN/FMNH 2 + 2 H+ , + 2 e- - 2 H+ , - 2 e- Другой флавиновый кофактор оксидоредуктаз флавинмононуклеотид. Слева изображена его окисленная форма, справа – восстановленная. 89
 ХИНОИДНЫЕ КОФАКТОРЫ Примеры структур некоторых хиноидных кофакторов оксидоредуктаз Видно, что некоторые из них встроены в полипептидные цепи белков в процессе посттрансляционной модификации белков 90
ХИНОИДНЫЕ КОФАКТОРЫ Примеры структур некоторых хиноидных кофакторов оксидоредуктаз Видно, что некоторые из них встроены в полипептидные цепи белков в процессе посттрансляционной модификации белков 90
 ХИНОИДНЫЕ КОФАКТОРЫ Восстановленные формы кофактора PQQ 91
ХИНОИДНЫЕ КОФАКТОРЫ Восстановленные формы кофактора PQQ 91
 РЕАКЦИИ С УЧАСТИЕМ ОКСИДОРЕДУКТАЗ • В биохимических циклах оксидоредуктазы катализируют процессы, связанные с окислительно-восстановительными процессами в обмене веществ • Способность ферментов этого класса к реакциям с переносом электронов обусловливает образование различных форм активного кислорода, которые способны окислять разные субстраты 92
РЕАКЦИИ С УЧАСТИЕМ ОКСИДОРЕДУКТАЗ • В биохимических циклах оксидоредуктазы катализируют процессы, связанные с окислительно-восстановительными процессами в обмене веществ • Способность ферментов этого класса к реакциям с переносом электронов обусловливает образование различных форм активного кислорода, которые способны окислять разные субстраты 92
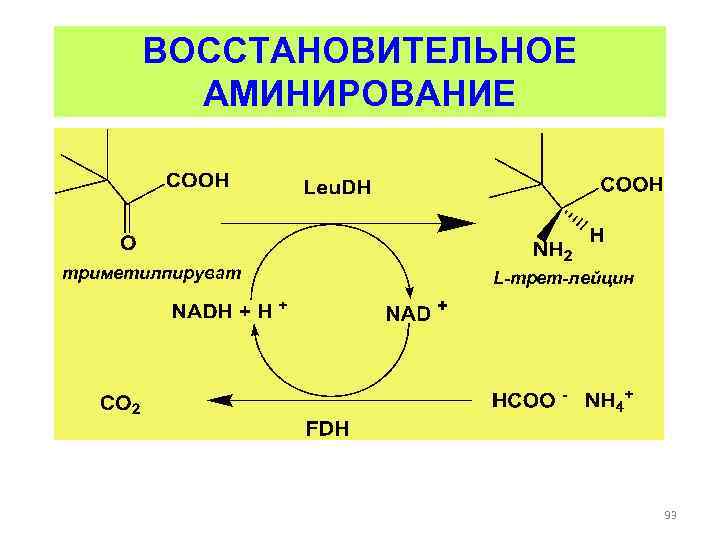 ВОССТАНОВИТЕЛЬНОЕ АМИНИРОВАНИЕ триметилпируват L-трет-лейцин 93
ВОССТАНОВИТЕЛЬНОЕ АМИНИРОВАНИЕ триметилпируват L-трет-лейцин 93
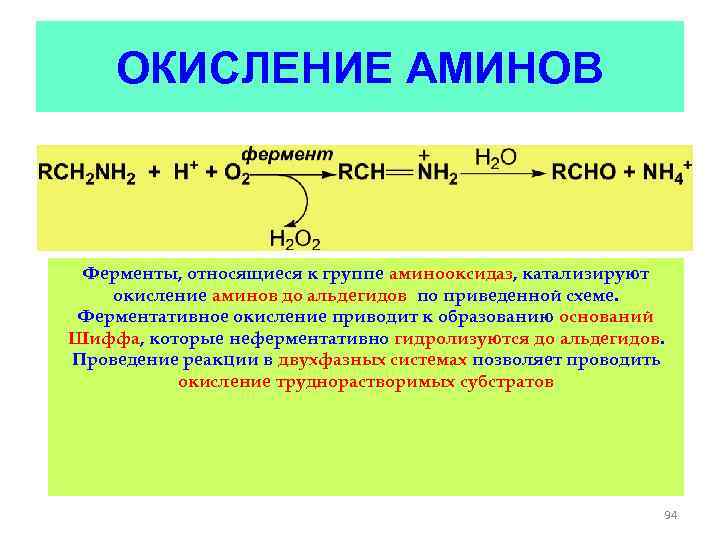 ОКИСЛЕНИЕ АМИНОВ Ферменты, относящиеся к группе аминооксидаз, катализируют окисление аминов до альдегидов по приведенной схеме. Ферментативное окисление приводит к образованию оснований Шиффа, которые неферментативно гидролизуются до альдегидов. Проведение реакции в двухфазных системах позволяет проводить окисление труднорастворимых субстратов 94
ОКИСЛЕНИЕ АМИНОВ Ферменты, относящиеся к группе аминооксидаз, катализируют окисление аминов до альдегидов по приведенной схеме. Ферментативное окисление приводит к образованию оснований Шиффа, которые неферментативно гидролизуются до альдегидов. Проведение реакции в двухфазных системах позволяет проводить окисление труднорастворимых субстратов 94
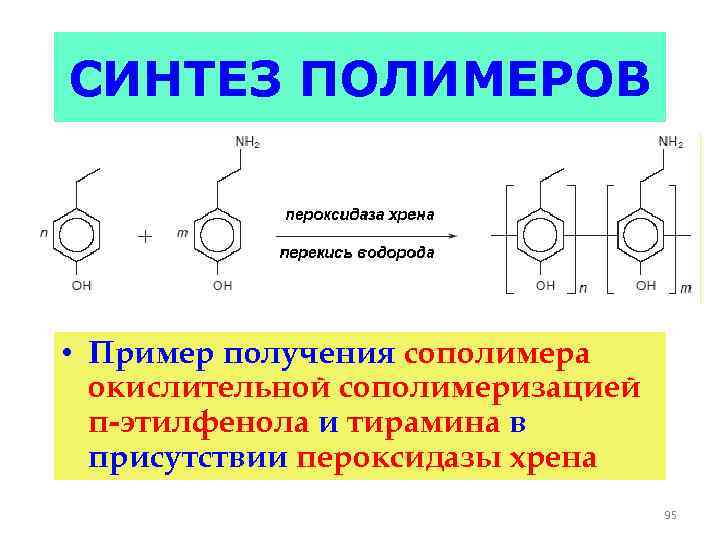 СИНТЕЗ ПОЛИМЕРОВ • Пример получения сополимера окислительной сополимеризацией п-этилфенола и тирамина в присутствии пероксидазы хрена 95
СИНТЕЗ ПОЛИМЕРОВ • Пример получения сополимера окислительной сополимеризацией п-этилфенола и тирамина в присутствии пероксидазы хрена 95
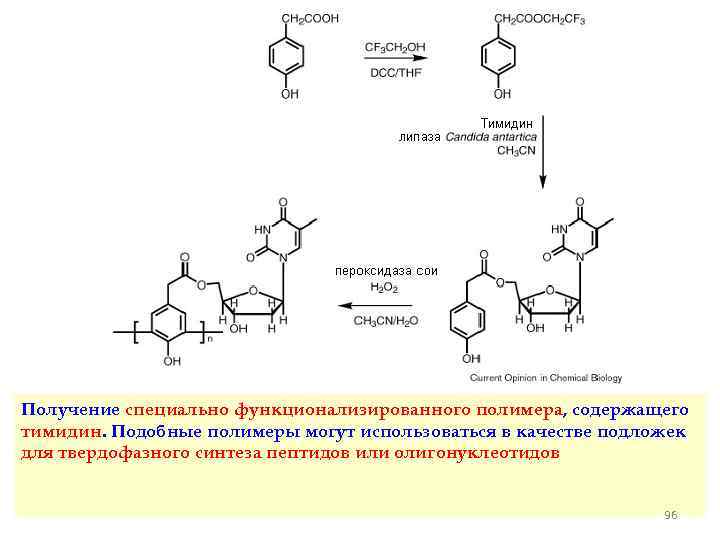 Получение специально функционализированного полимера, содержащего тимидин. Подобные полимеры могут использоваться в качестве подложек для твердофазного синтеза пептидов или олигонуклеотидов 96
Получение специально функционализированного полимера, содержащего тимидин. Подобные полимеры могут использоваться в качестве подложек для твердофазного синтеза пептидов или олигонуклеотидов 96
 РЕАКЦИЯ БАЙЕРА-ВИЛЛИГЕРА Окисление фенхона (5) до фенхолидов (6) и (7). В случае стереоизомерных субстратов реакция идет стереоселективно. 97
РЕАКЦИЯ БАЙЕРА-ВИЛЛИГЕРА Окисление фенхона (5) до фенхолидов (6) и (7). В случае стереоизомерных субстратов реакция идет стереоселективно. 97
 РЕГЕНЕРАЦИЯ КОФАКТОРОВ • Кофакторы – сложные, дорогие соединения, расходующиеся в ходе реакции в стехиометрических количествах • Для обеспечения экономики процесса необходимо осуществлять регенерацию кофакторов – восстановление их потребления в ходе реакции 98
РЕГЕНЕРАЦИЯ КОФАКТОРОВ • Кофакторы – сложные, дорогие соединения, расходующиеся в ходе реакции в стехиометрических количествах • Для обеспечения экономики процесса необходимо осуществлять регенерацию кофакторов – восстановление их потребления в ходе реакции 98
 РЕГЕНЕРАЦИЯ КОФАКТОРОВ • Задача решается путем проведения другой реакции, в которой кофактор используется в противоположном направлении • Пример такой организации процесса – использование формиатдегидрогеназы в случае синтеза трет-лейцина. Система удобна тем, что в продуктом “регенерирующей” реакции является газ, уходящий из системы 99
РЕГЕНЕРАЦИЯ КОФАКТОРОВ • Задача решается путем проведения другой реакции, в которой кофактор используется в противоположном направлении • Пример такой организации процесса – использование формиатдегидрогеназы в случае синтеза трет-лейцина. Система удобна тем, что в продуктом “регенерирующей” реакции является газ, уходящий из системы 99
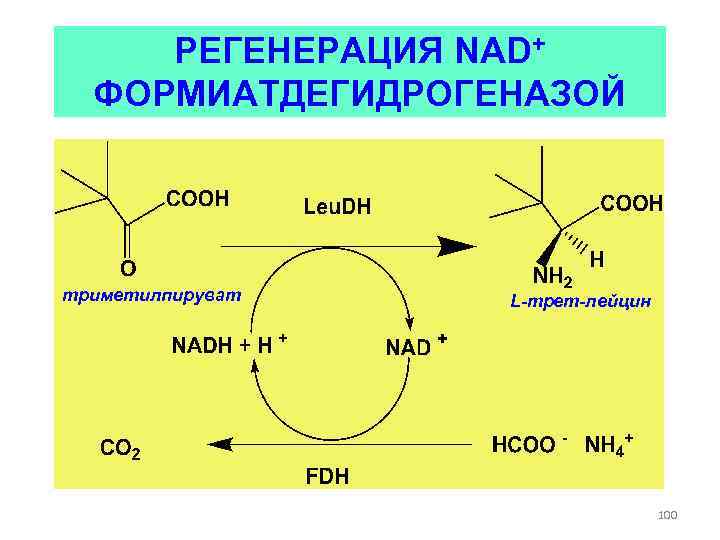 РЕГЕНЕРАЦИЯ NAD+ ФОРМИАТДЕГИДРОГЕНАЗОЙ триметилпируват L-трет-лейцин 100
РЕГЕНЕРАЦИЯ NAD+ ФОРМИАТДЕГИДРОГЕНАЗОЙ триметилпируват L-трет-лейцин 100
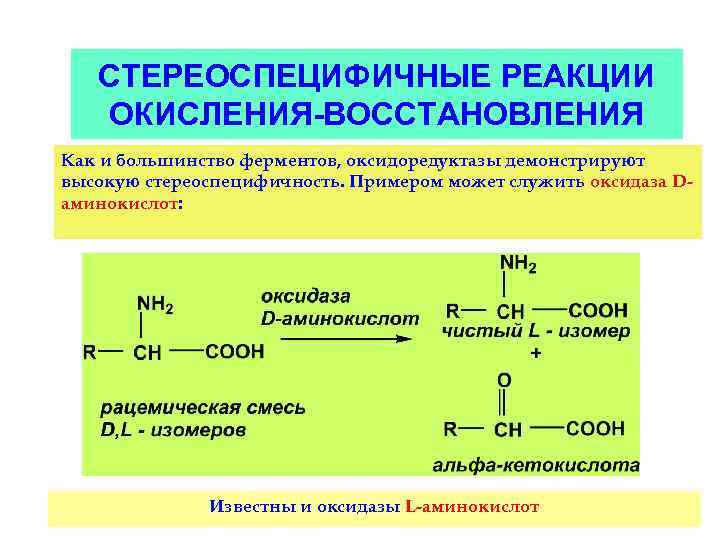 СТЕРЕОСПЕЦИФИЧНЫЕ РЕАКЦИИ ОКИСЛЕНИЯ-ВОССТАНОВЛЕНИЯ Как и большинство ферментов, оксидоредуктазы демонстрируют высокую стереоспецифичность. Примером может служить оксидаза Dаминокислот: Известны и оксидазы L-аминокислот 101
СТЕРЕОСПЕЦИФИЧНЫЕ РЕАКЦИИ ОКИСЛЕНИЯ-ВОССТАНОВЛЕНИЯ Как и большинство ферментов, оксидоредуктазы демонстрируют высокую стереоспецифичность. Примером может служить оксидаза Dаминокислот: Известны и оксидазы L-аминокислот 101
 РЕАКЦИИ С ИСПОЛЬЗОВАНИЕМ ТРАНСФЕРАЗ • Трансферазы – класс ферментов, катализирующих перенос различных групп атомов • Как и в случае оксидо-редуктаз, ферменты этого класса катализируют большое разнообразие реакций и группируются по многим подклассам и подподклассам 104
РЕАКЦИИ С ИСПОЛЬЗОВАНИЕМ ТРАНСФЕРАЗ • Трансферазы – класс ферментов, катализирующих перенос различных групп атомов • Как и в случае оксидо-редуктаз, ферменты этого класса катализируют большое разнообразие реакций и группируются по многим подклассам и подподклассам 104
 КОФАКТОРЫ ТРАНСФЕРАЗ • АТФ и другие нуклеозидтрифосфаты – для фосфотрансфераз • Фосфаты пиридоксаля и пиридоксамина – для аминотрансфераз • S-аденозилметионин (перенос метильных групп) • Биотин – для карбоксилаз (перенос карбоксильных групп) 105
КОФАКТОРЫ ТРАНСФЕРАЗ • АТФ и другие нуклеозидтрифосфаты – для фосфотрансфераз • Фосфаты пиридоксаля и пиридоксамина – для аминотрансфераз • S-аденозилметионин (перенос метильных групп) • Биотин – для карбоксилаз (перенос карбоксильных групп) 105
 РЕАКЦИИ ОБМЕНА • Фермент катализирует замещение группы атомов в соединении на другую, близкую по структуре и функциям • Продукт – другое соединение того же ряда • Показательны примеры в ряду нуклеотидов 106
РЕАКЦИИ ОБМЕНА • Фермент катализирует замещение группы атомов в соединении на другую, близкую по структуре и функциям • Продукт – другое соединение того же ряда • Показательны примеры в ряду нуклеотидов 106
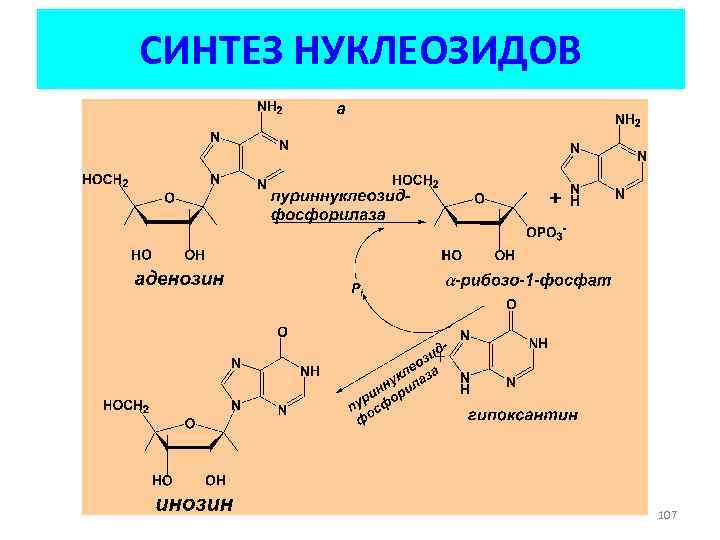 СИНТЕЗ НУКЛЕОЗИДОВ 107
СИНТЕЗ НУКЛЕОЗИДОВ 107
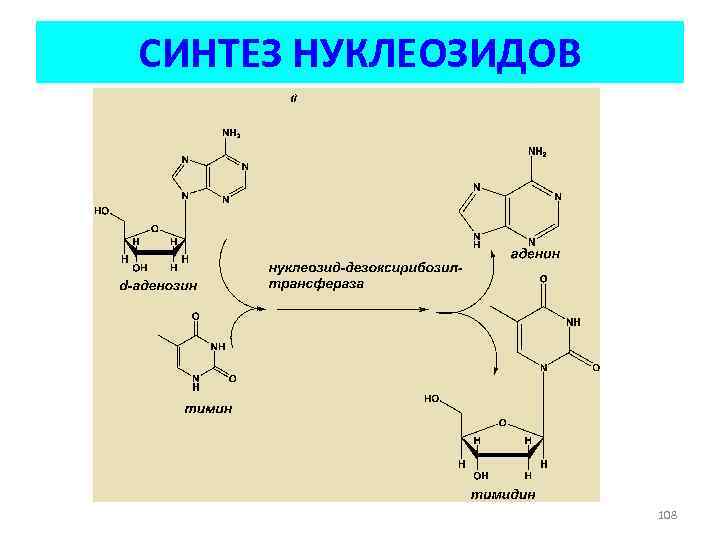 СИНТЕЗ НУКЛЕОЗИДОВ 108
СИНТЕЗ НУКЛЕОЗИДОВ 108
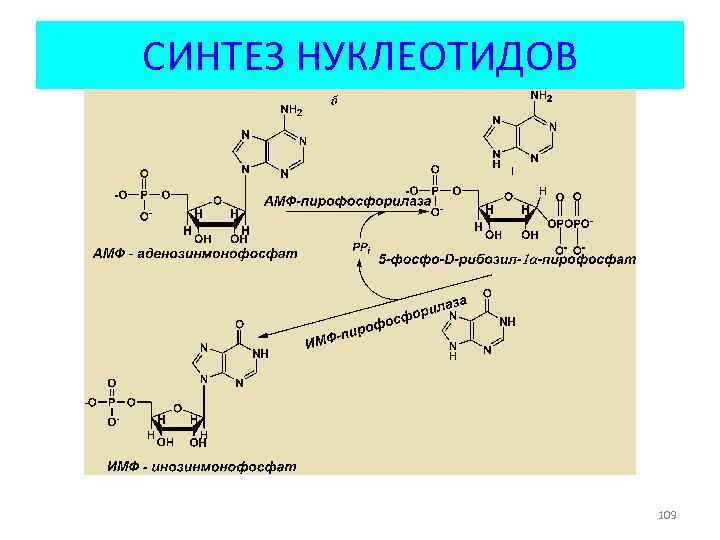 СИНТЕЗ НУКЛЕОТИДОВ 109
СИНТЕЗ НУКЛЕОТИДОВ 109
 НАПРАВЛЕНИЯ ИСПОЛЬЗОВАНИЯ РЕАКЦИЙ ОБМЕНА В РЯДУ НУКЛЕИНОВЫХ ПРОИЗВОДНЫХ • Синтез изотопно меченных нуклеотидов и нуклеозидов из меченых оснований и сахаров • Синтез нуклеотидов с неприродными основаниями и углеводными компонентами 110
НАПРАВЛЕНИЯ ИСПОЛЬЗОВАНИЯ РЕАКЦИЙ ОБМЕНА В РЯДУ НУКЛЕИНОВЫХ ПРОИЗВОДНЫХ • Синтез изотопно меченных нуклеотидов и нуклеозидов из меченых оснований и сахаров • Синтез нуклеотидов с неприродными основаниями и углеводными компонентами 110
 СИНТЕЗ НУКЛЕОЗИДПОЛИФОСФАТОВ • Нуклеозидполифосфаты являются важными метаболитами живых организмов • АТФ используется в медицине в качестве лекарственного средства в кардиологии • Нуклеозидтрифосфаты – важные компоненты систем синтеза генетического материала 111
СИНТЕЗ НУКЛЕОЗИДПОЛИФОСФАТОВ • Нуклеозидполифосфаты являются важными метаболитами живых организмов • АТФ используется в медицине в качестве лекарственного средства в кардиологии • Нуклеозидтрифосфаты – важные компоненты систем синтеза генетического материала 111
 СИНТЕЗ НУКЛЕОЗИДПОЛИФОСФАТОВ • Нуклеозидполифосфаты – макроэргические соединения, которые образуются в организме в ходе катаболических процессов • Получение нулеозидполифосфатов вне организма можно осуществлять ферментативно с помощью фосфотрансфераз 112
СИНТЕЗ НУКЛЕОЗИДПОЛИФОСФАТОВ • Нуклеозидполифосфаты – макроэргические соединения, которые образуются в организме в ходе катаболических процессов • Получение нулеозидполифосфатов вне организма можно осуществлять ферментативно с помощью фосфотрансфераз 112
 СИНТЕЗ НУКЛЕОЗИДПОЛИФОСФАТОВ Исходными продуктами для этих реакций являются нуклеозидмонофосфаты: Схема превращений: NMP + ATP → NDP + ADP нуклеозидмонофосфаткиназы NDP + ATP → NTP + ADP нуклеозиддифосфаткиназа 113
СИНТЕЗ НУКЛЕОЗИДПОЛИФОСФАТОВ Исходными продуктами для этих реакций являются нуклеозидмонофосфаты: Схема превращений: NMP + ATP → NDP + ADP нуклеозидмонофосфаткиназы NDP + ATP → NTP + ADP нуклеозиддифосфаткиназа 113
 СИНТЕЗ НУКЛЕОЗИДПОЛИФОСФАТОВ Здесь снова возникает проблема использования дорогих исходных продуктов – нуклеозидтрифосфатов – в стехиометрических количествах. АТФ в таких реакциях выступает в качестве кофактора. 114
СИНТЕЗ НУКЛЕОЗИДПОЛИФОСФАТОВ Здесь снова возникает проблема использования дорогих исходных продуктов – нуклеозидтрифосфатов – в стехиометрических количествах. АТФ в таких реакциях выступает в качестве кофактора. 114
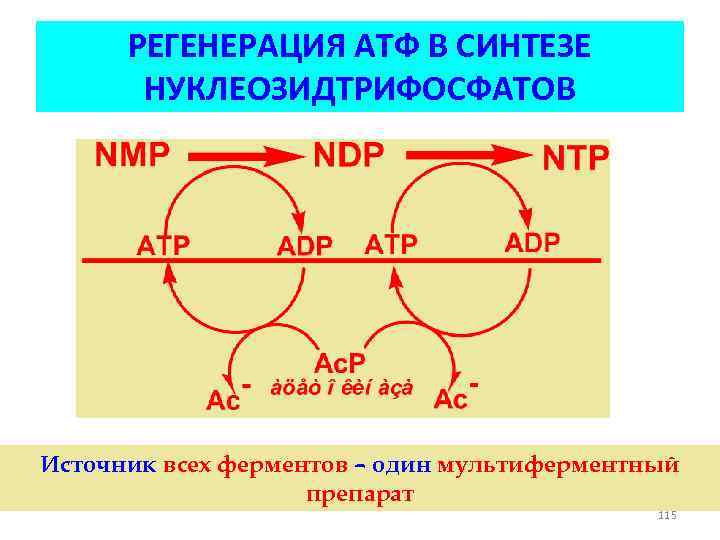 РЕГЕНЕРАЦИЯ АТФ В СИНТЕЗЕ НУКЛЕОЗИДТРИФОСФАТОВ Источник всех ферментов – один мультиферментный препарат 115
РЕГЕНЕРАЦИЯ АТФ В СИНТЕЗЕ НУКЛЕОЗИДТРИФОСФАТОВ Источник всех ферментов – один мультиферментный препарат 115
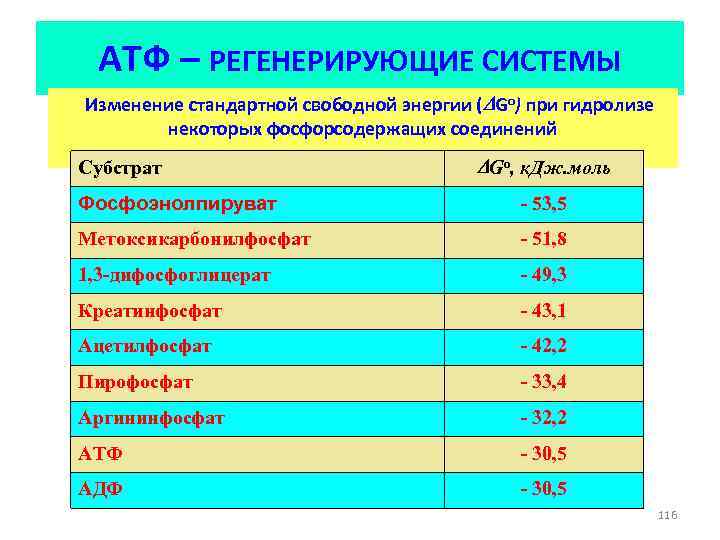 АТФ – РЕГЕНЕРИРУЮЩИЕ СИСТЕМЫ Изменение стандартной свободной энергии ( Go) при гидролизе некоторых фосфорсодержащих соединений Субстрат Go, к. Дж. моль Фосфоэнолпируват - 53, 5 Метоксикарбонилфосфат - 51, 8 1, 3 -дифосфоглицерат - 49, 3 Креатинфосфат - 43, 1 Ацетилфосфат - 42, 2 Пирофосфат - 33, 4 Аргининфосфат - 32, 2 АТФ - 30, 5 АДФ - 30, 5 116
АТФ – РЕГЕНЕРИРУЮЩИЕ СИСТЕМЫ Изменение стандартной свободной энергии ( Go) при гидролизе некоторых фосфорсодержащих соединений Субстрат Go, к. Дж. моль Фосфоэнолпируват - 53, 5 Метоксикарбонилфосфат - 51, 8 1, 3 -дифосфоглицерат - 49, 3 Креатинфосфат - 43, 1 Ацетилфосфат - 42, 2 Пирофосфат - 33, 4 Аргининфосфат - 32, 2 АТФ - 30, 5 АДФ - 30, 5 116
 СИСТЕМЫ РЕГЕНЕРАЦИИ АТФ • Наиболее простым донором макроэргического фосфата для регенерации АТФ является ацетилфосфат, синтез которого легко провести с помощью известных методов органической химии 117
СИСТЕМЫ РЕГЕНЕРАЦИИ АТФ • Наиболее простым донором макроэргического фосфата для регенерации АТФ является ацетилфосфат, синтез которого легко провести с помощью известных методов органической химии 117
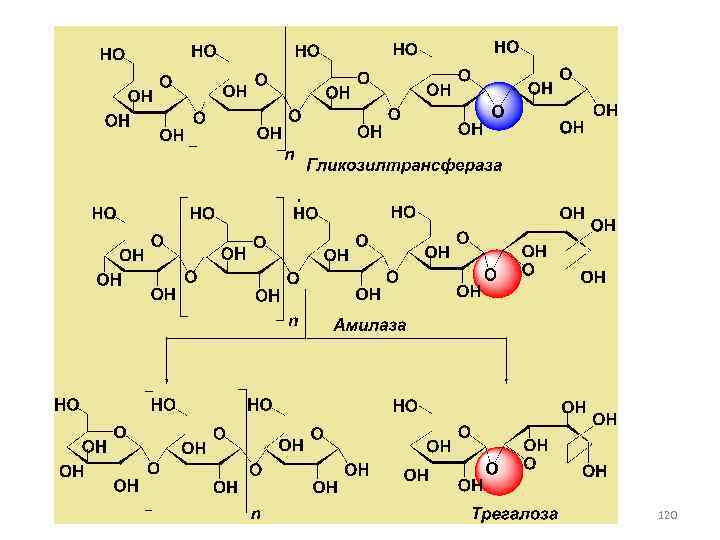
 ТРАНСГЛИКОЗИДАЗНЫЕ РЕАКЦИИ • Синтез трегалозы • Трегалоза – α, α-1, 1 - глюкозилглюкоза – используется как стабилизатор лекарственных средств (особенно белковой природы) и пищевых композиций, а также как компонент косметических средств 119
ТРАНСГЛИКОЗИДАЗНЫЕ РЕАКЦИИ • Синтез трегалозы • Трегалоза – α, α-1, 1 - глюкозилглюкоза – используется как стабилизатор лекарственных средств (особенно белковой природы) и пищевых композиций, а также как компонент косметических средств 119
 120
120
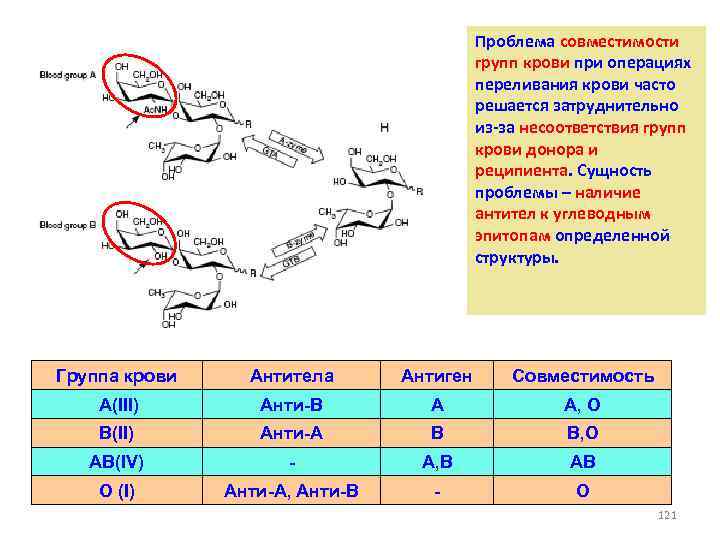 Проблема совместимости групп крови при операциях переливания крови часто решается затруднительно из-за несоответствия групп крови донора и реципиента. Сущность проблемы – наличие антител к углеводным эпитопам определенной структуры. Группа крови Антитела Антиген Совместимость А(III) Анти-В А А, О В(II) Анти-А B В, О АВ(IV) - А, В AB О (I) Анти-А, Анти-В - О 121
Проблема совместимости групп крови при операциях переливания крови часто решается затруднительно из-за несоответствия групп крови донора и реципиента. Сущность проблемы – наличие антител к углеводным эпитопам определенной структуры. Группа крови Антитела Антиген Совместимость А(III) Анти-В А А, О В(II) Анти-А B В, О АВ(IV) - А, В AB О (I) Анти-А, Анти-В - О 121
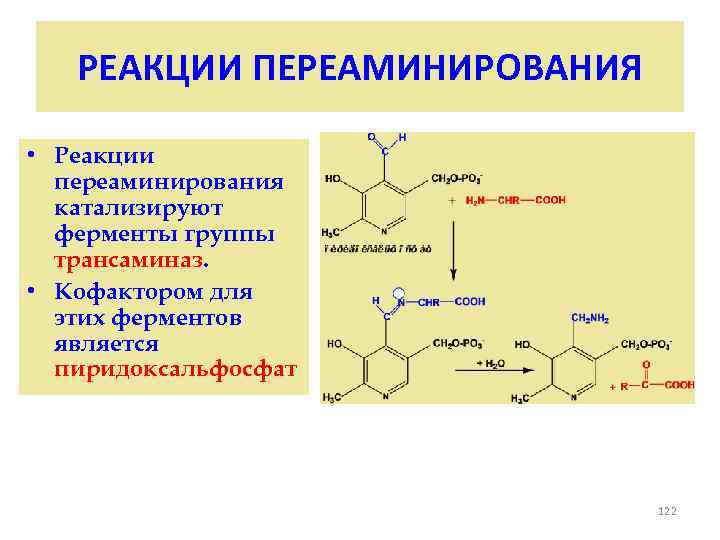 РЕАКЦИИ ПЕРЕАМИНИРОВАНИЯ • Реакции переаминирования катализируют ферменты группы трансаминаз. • Кофактором для этих ферментов является пиридоксальфосфат 122
РЕАКЦИИ ПЕРЕАМИНИРОВАНИЯ • Реакции переаминирования катализируют ферменты группы трансаминаз. • Кофактором для этих ферментов является пиридоксальфосфат 122
 ЛИАЗЫ • В последние годы появились сообщения об использовании лиаз для получения 2 оксикетонов, в частности, бензоинов или 2 -окси-1 фенилпропанонов с хорошими выходами и высокой энантиоселективностью. Исследования в различных лабораториях сконцентрированы на изучении субстратной специфичности бензальдегидлиаз в реакции карболигирования. Подробно изучено влияние условий реакции на стабильность фермента и выход продуктов. Фермент мало устойчив к органическим растворителям, однако ДМСО стабилизирует фермент вплоть до концентрации 30%. При этом концентрация бензальдегида могла быть достигнута до 120 -130 м. М 126
ЛИАЗЫ • В последние годы появились сообщения об использовании лиаз для получения 2 оксикетонов, в частности, бензоинов или 2 -окси-1 фенилпропанонов с хорошими выходами и высокой энантиоселективностью. Исследования в различных лабораториях сконцентрированы на изучении субстратной специфичности бензальдегидлиаз в реакции карболигирования. Подробно изучено влияние условий реакции на стабильность фермента и выход продуктов. Фермент мало устойчив к органическим растворителям, однако ДМСО стабилизирует фермент вплоть до концентрации 30%. При этом концентрация бензальдегида могла быть достигнута до 120 -130 м. М 126
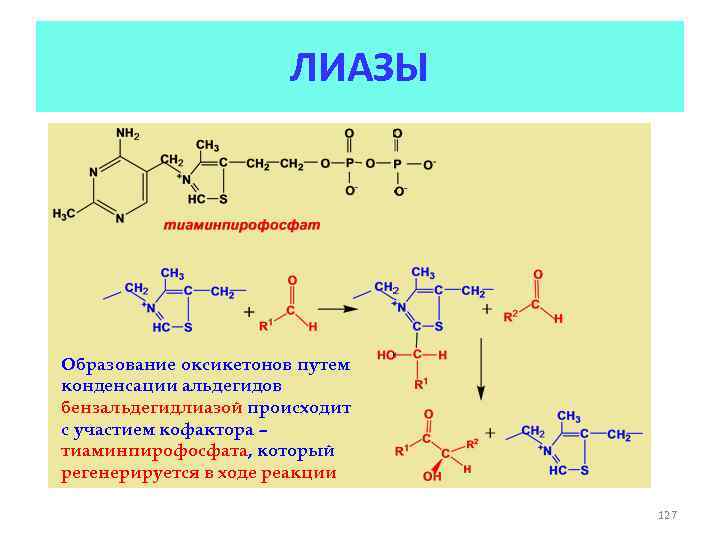 ЛИАЗЫ Образование оксикетонов путем конденсации альдегидов бензальдегидлиазой происходит с участием кофактора – тиаминпирофосфата, который регенерируется в ходе реакции 127
ЛИАЗЫ Образование оксикетонов путем конденсации альдегидов бензальдегидлиазой происходит с участием кофактора – тиаминпирофосфата, который регенерируется в ходе реакции 127
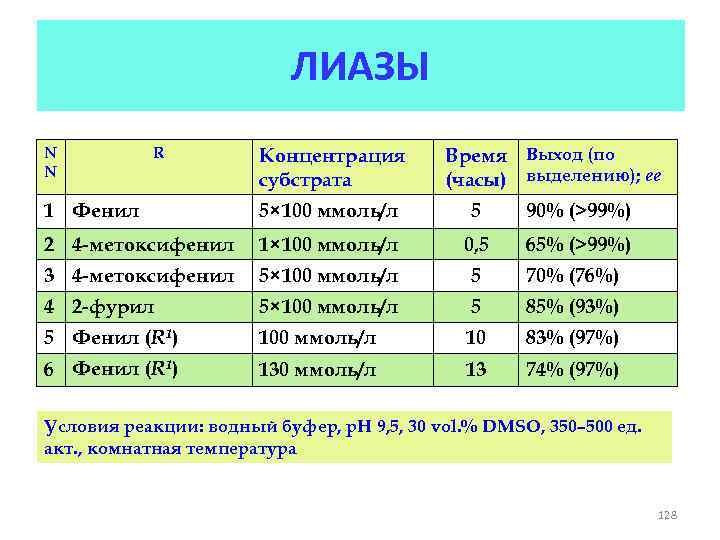 ЛИАЗЫ N N R Концентрация субстрата Время Выход (по (часы) выделению); ее 1 Фенил 5× 100 ммоль/л 5 90% (>99%) 2 4 -метоксифенил 1× 100 ммоль/л 0, 5 65% (>99%) 3 4 -метоксифенил 5× 100 ммоль/л 5 70% (76%) 4 2 -фурил 5× 100 ммоль/л 5 85% (93%) 5 Фенил (R 1) 100 ммоль/л 10 83% (97%) 6 Фенил (R 1) 130 ммоль/л 13 74% (97%) Условия реакции: водный буфер, р. Н 9, 5, 30 vol. % DMSO, 350– 500 ед. акт. , комнатная температура 128
ЛИАЗЫ N N R Концентрация субстрата Время Выход (по (часы) выделению); ее 1 Фенил 5× 100 ммоль/л 5 90% (>99%) 2 4 -метоксифенил 1× 100 ммоль/л 0, 5 65% (>99%) 3 4 -метоксифенил 5× 100 ммоль/л 5 70% (76%) 4 2 -фурил 5× 100 ммоль/л 5 85% (93%) 5 Фенил (R 1) 100 ммоль/л 10 83% (97%) 6 Фенил (R 1) 130 ммоль/л 13 74% (97%) Условия реакции: водный буфер, р. Н 9, 5, 30 vol. % DMSO, 350– 500 ед. акт. , комнатная температура 128
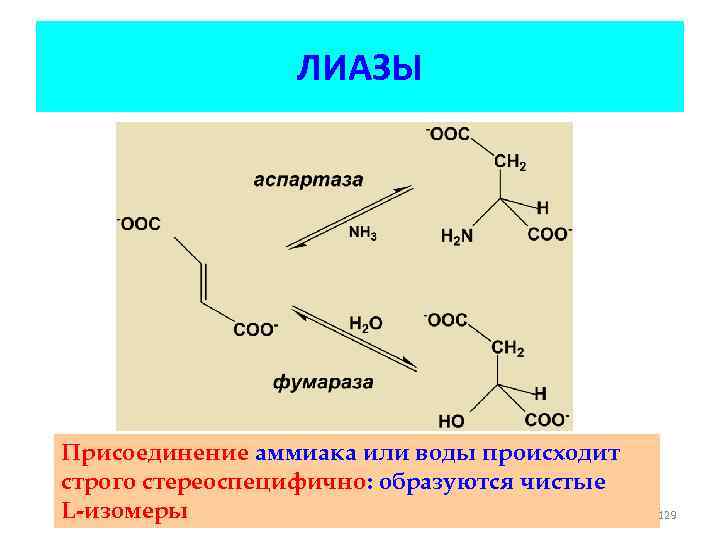 ЛИАЗЫ Присоединение аммиака или воды происходит строго стереоспецифично: образуются чистые L-изомеры 129
ЛИАЗЫ Присоединение аммиака или воды происходит строго стереоспецифично: образуются чистые L-изомеры 129
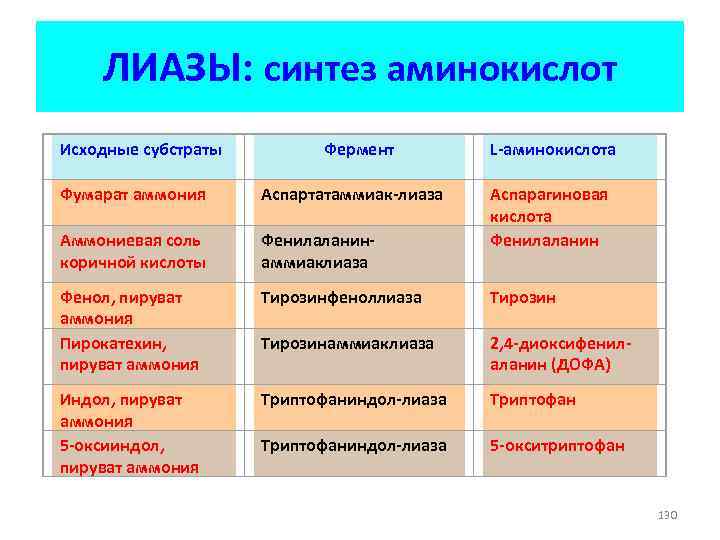 ЛИАЗЫ: синтез аминокислот Исходные субстраты Фермент L-аминокислота Фумарат аммония Аспартатаммиак-лиаза Аспарагиновая кислота Фенилаланин Аммониевая соль коричной кислоты Фенилаланинаммиаклиаза Фенол, пируват аммония Пирокатехин, пируват аммония Тирозинфеноллиаза Тирозинаммиаклиаза 2, 4 -диоксифенилаланин (ДОФА) Индол, пируват аммония 5 -оксииндол, пируват аммония Триптофаниндол-лиаза 5 -окситриптофан 130
ЛИАЗЫ: синтез аминокислот Исходные субстраты Фермент L-аминокислота Фумарат аммония Аспартатаммиак-лиаза Аспарагиновая кислота Фенилаланин Аммониевая соль коричной кислоты Фенилаланинаммиаклиаза Фенол, пируват аммония Пирокатехин, пируват аммония Тирозинфеноллиаза Тирозинаммиаклиаза 2, 4 -диоксифенилаланин (ДОФА) Индол, пируват аммония 5 -оксииндол, пируват аммония Триптофаниндол-лиаза 5 -окситриптофан 130
 НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ БИОТЕХНОЛОГИЯ Биотрансформация с использованием целых клеток Промышленные процессы с применением ферментов 131
НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ БИОТЕХНОЛОГИЯ Биотрансформация с использованием целых клеток Промышленные процессы с применением ферментов 131
 КЛЕТКИ КАК КАТАЛИЗАТОРЫ • Ранее мы рассматривали в качестве каталитических агентов отдельные ферменты • Часто оказывается удобным использовать присутствующие в клетках мультиферментные системы для осуществления in situ многостадийных превращений 132
КЛЕТКИ КАК КАТАЛИЗАТОРЫ • Ранее мы рассматривали в качестве каталитических агентов отдельные ферменты • Часто оказывается удобным использовать присутствующие в клетках мультиферментные системы для осуществления in situ многостадийных превращений 132
 КЛЕТКИ КАК КАТАЛИЗАТОРЫ • Процессы, осуществляемые с использованием микробных клеток в качестве каталитических агентов часто называют биотрансформацией 133
КЛЕТКИ КАК КАТАЛИЗАТОРЫ • Процессы, осуществляемые с использованием микробных клеток в качестве каталитических агентов часто называют биотрансформацией 133
 БИОТРАНСФОРМАЦИЯ Основные процессы биотрансформации: • окислительно-восстановительные реакции; • реакции декарбоксилирования; • реакции дезаминирования; • реакции с углеводными субстратами (гликозилирование, трансгликозилирование); 134
БИОТРАНСФОРМАЦИЯ Основные процессы биотрансформации: • окислительно-восстановительные реакции; • реакции декарбоксилирования; • реакции дезаминирования; • реакции с углеводными субстратами (гликозилирование, трансгликозилирование); 134
 БИОТРАНСФОРМАЦИЯ • алкилирование (метилирование); • реакции переноса ацильных групп (включая гидролиз, при котором ацильные остатки переносятся на воду); • реакции галогенирования; • реакции переноса нуклеотидных остатков; • реакции изомеризации; 135
БИОТРАНСФОРМАЦИЯ • алкилирование (метилирование); • реакции переноса ацильных групп (включая гидролиз, при котором ацильные остатки переносятся на воду); • реакции галогенирования; • реакции переноса нуклеотидных остатков; • реакции изомеризации; 135
 БИОТРАНСФОРМАЦИЯ СТЕРОИДОВ Скелет молекулы стероидов 136
БИОТРАНСФОРМАЦИЯ СТЕРОИДОВ Скелет молекулы стероидов 136
 БИОТРАНСФОРМАЦИЯ СТЕРОИДОВ Трансформация 17 -оксипрогестерона (1) клетками Botrytis cinerea позволила получить 6 -оксипроиз-водное 17 -оксипрогестерона (2) с высокой энантиоселективностью 137
БИОТРАНСФОРМАЦИЯ СТЕРОИДОВ Трансформация 17 -оксипрогестерона (1) клетками Botrytis cinerea позволила получить 6 -оксипроиз-водное 17 -оксипрогестерона (2) с высокой энантиоселективностью 137
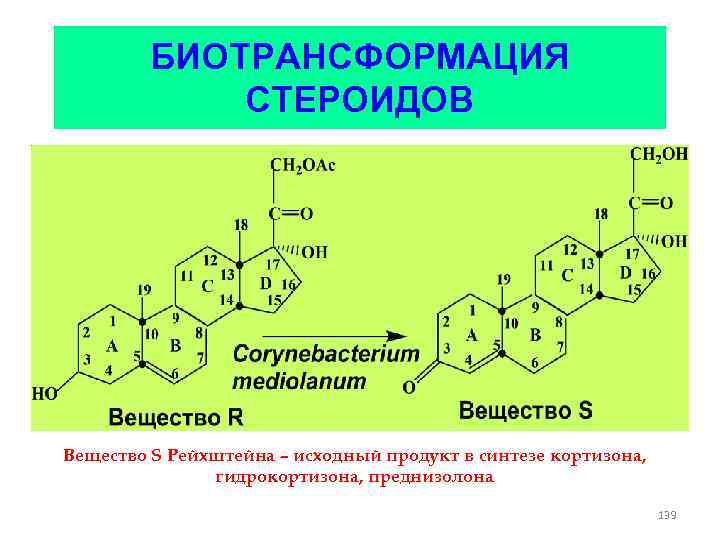 БИОТРАНСФОРМАЦИЯ СТЕРОИДОВ Вещество S Рейхштейна – исходный продукт в синтезе кортизона, гидрокортизона, преднизолона 139
БИОТРАНСФОРМАЦИЯ СТЕРОИДОВ Вещество S Рейхштейна – исходный продукт в синтезе кортизона, гидрокортизона, преднизолона 139
 ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ • Помимо катаболических процессов, связанных с продукцией энергии в организме, углеводы подвергаются метаболическим превращениям с образованием продуктов, используемых в различных целях. Ферментные системы микроорганизмов позволяют проводить биотрансформацию углеводов с целью получения продуктов, используемых в фармации и в качестве диетических пищевых продуктов 140
ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ • Помимо катаболических процессов, связанных с продукцией энергии в организме, углеводы подвергаются метаболическим превращениям с образованием продуктов, используемых в различных целях. Ферментные системы микроорганизмов позволяют проводить биотрансформацию углеводов с целью получения продуктов, используемых в фармации и в качестве диетических пищевых продуктов 140
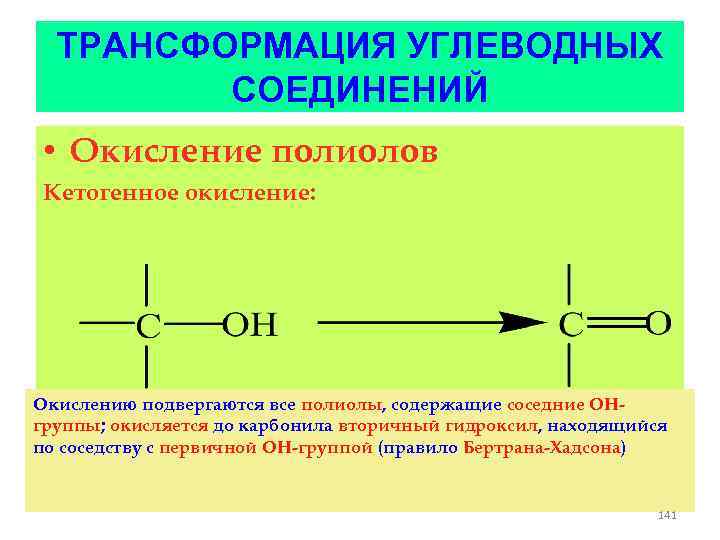 ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ • Окисление полиолов Кетогенное окисление: Окислению подвергаются все полиолы, содержащие соседние ОНгруппы; окисляется до карбонила вторичный гидроксил, находящийся по соседству с первичной ОН-группой (правило Бертрана-Хадсона) 141
ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ • Окисление полиолов Кетогенное окисление: Окислению подвергаются все полиолы, содержащие соседние ОНгруппы; окисляется до карбонила вторичный гидроксил, находящийся по соседству с первичной ОН-группой (правило Бертрана-Хадсона) 141
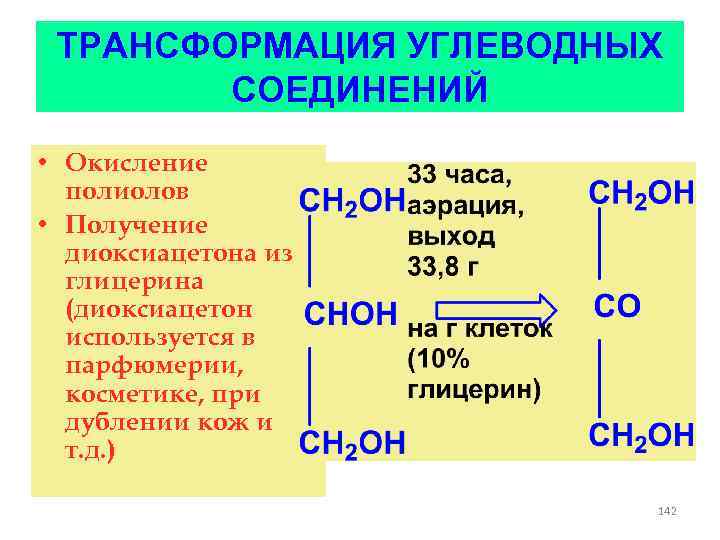 ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ • Окисление полиолов • Получение диоксиацетона из глицерина (диоксиацетон используется в парфюмерии, косметике, при дублении кож и т. д. ) 142
ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ • Окисление полиолов • Получение диоксиацетона из глицерина (диоксиацетон используется в парфюмерии, косметике, при дублении кож и т. д. ) 142
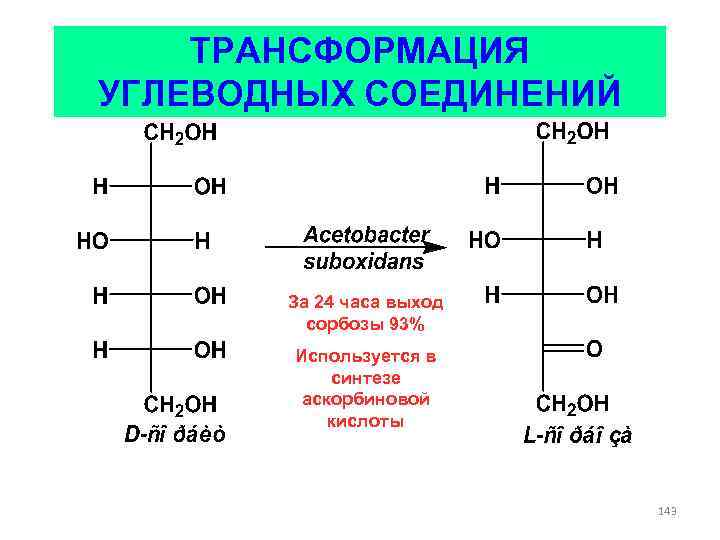 ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ За 24 часа выход сорбозы 93% Используется в синтезе аскорбиновой кислоты 143
ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ За 24 часа выход сорбозы 93% Используется в синтезе аскорбиновой кислоты 143
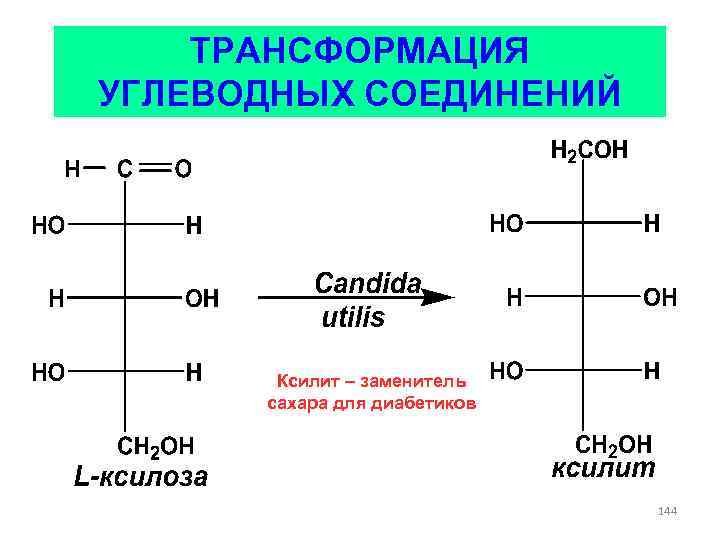 ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ Ксилит – заменитель сахара для диабетиков 144
ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ Ксилит – заменитель сахара для диабетиков 144
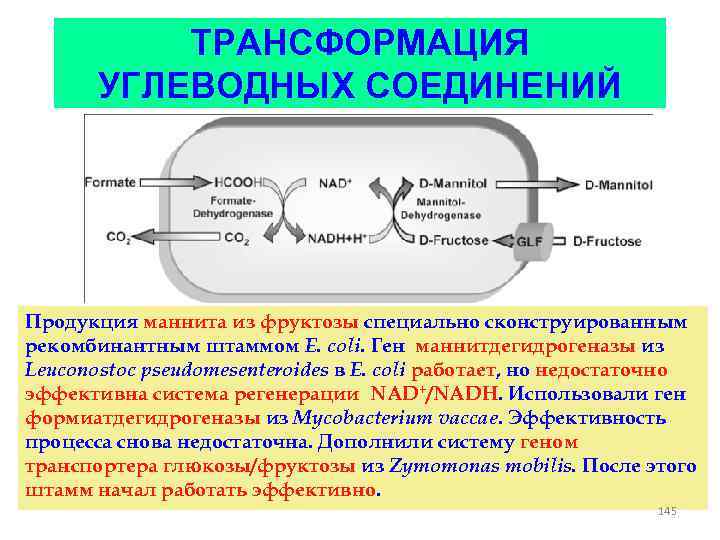 ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ Продукция маннита из фруктозы специально сконструированным рекомбинантным штаммом E. coli. Ген маннитдегидрогеназы из Leuconostoc pseudomesenteroides в E. coli работает, но недостаточно эффективна система регенерации NAD+/NADH. Использовали ген формиатдегидрогеназы из Mycobacterium vaccae. Эффективность процесса снова недостаточна. Дополнили систему геном транспортера глюкозы/фруктозы из Zymomonas mobilis. После этого штамм начал работать эффективно. 145
ТРАНСФОРМАЦИЯ УГЛЕВОДНЫХ СОЕДИНЕНИЙ Продукция маннита из фруктозы специально сконструированным рекомбинантным штаммом E. coli. Ген маннитдегидрогеназы из Leuconostoc pseudomesenteroides в E. coli работает, но недостаточно эффективна система регенерации NAD+/NADH. Использовали ген формиатдегидрогеназы из Mycobacterium vaccae. Эффективность процесса снова недостаточна. Дополнили систему геном транспортера глюкозы/фруктозы из Zymomonas mobilis. После этого штамм начал работать эффективно. 145
 НЕКОТОРЫЕ ПРОМЫШЛЕННЫЕ ПРОЦЕССЫ • Ферменты используются не только в тонком органическом синтезе, но и в крупномасштабных промышленных процессах • Примером может служить осахаривание крахмала и получение глюкозофруктозных сиропов. Объем производства в мире достигает 15 млн. т в год. 148
НЕКОТОРЫЕ ПРОМЫШЛЕННЫЕ ПРОЦЕССЫ • Ферменты используются не только в тонком органическом синтезе, но и в крупномасштабных промышленных процессах • Примером может служить осахаривание крахмала и получение глюкозофруктозных сиропов. Объем производства в мире достигает 15 млн. т в год. 148
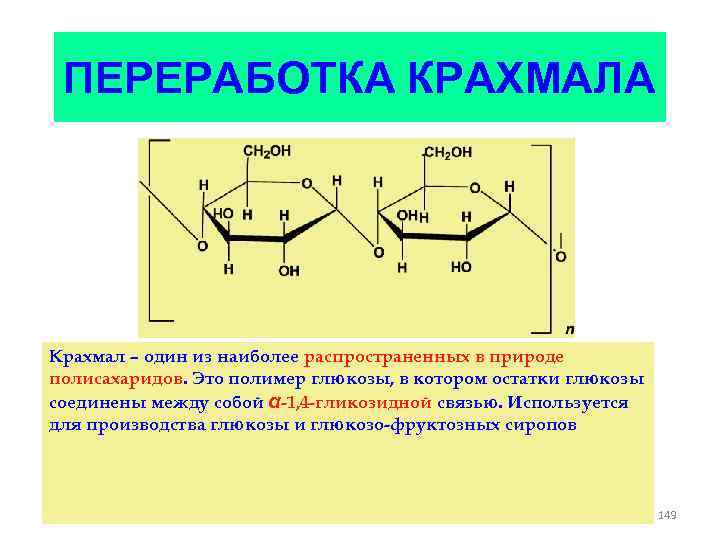 ПЕРЕРАБОТКА КРАХМАЛА Крахмал – один из наиболее распространенных в природе полисахаридов. Это полимер глюкозы, в котором остатки глюкозы соединены между собой α-1, 4 -гликозидной связью. Используется для производства глюкозы и глюкозо-фруктозных сиропов 149
ПЕРЕРАБОТКА КРАХМАЛА Крахмал – один из наиболее распространенных в природе полисахаридов. Это полимер глюкозы, в котором остатки глюкозы соединены между собой α-1, 4 -гликозидной связью. Используется для производства глюкозы и глюкозо-фруктозных сиропов 149
 ПЕРЕРАБОТКА КРАХМАЛА Схема строения молекулы крахмала. Полимер имеет разветвленную структуру, в местах ветвления связи α-1, 6 (минорные). Сплошные стрелки – места атаки α-амилазой, пунктирные стрелки – места атаки глюкоамилазой, жирные сплошные стрелки – места атаки пуллуланазой. 150
ПЕРЕРАБОТКА КРАХМАЛА Схема строения молекулы крахмала. Полимер имеет разветвленную структуру, в местах ветвления связи α-1, 6 (минорные). Сплошные стрелки – места атаки α-амилазой, пунктирные стрелки – места атаки глюкоамилазой, жирные сплошные стрелки – места атаки пуллуланазой. 150
 ПЕРЕРАБОТКА КРАХМАЛА Гидролиз α-амилазой приводит к образованию олигосахаридов декстринов, гидролиз глюкоамилазой приводит к образованию глюкозы и мальтозы (короткие олигосахариды глюкозы), пуллуланаза необходима для разрушения полимера в точках ветвления. Для производства глюкозо-фруктозных сиропов проводится обработка глюкозоизомеразой. Получается смесь глюкозы и фруктозы – приблизительно в равных соотношениях. 151
ПЕРЕРАБОТКА КРАХМАЛА Гидролиз α-амилазой приводит к образованию олигосахаридов декстринов, гидролиз глюкоамилазой приводит к образованию глюкозы и мальтозы (короткие олигосахариды глюкозы), пуллуланаза необходима для разрушения полимера в точках ветвления. Для производства глюкозо-фруктозных сиропов проводится обработка глюкозоизомеразой. Получается смесь глюкозы и фруктозы – приблизительно в равных соотношениях. 151
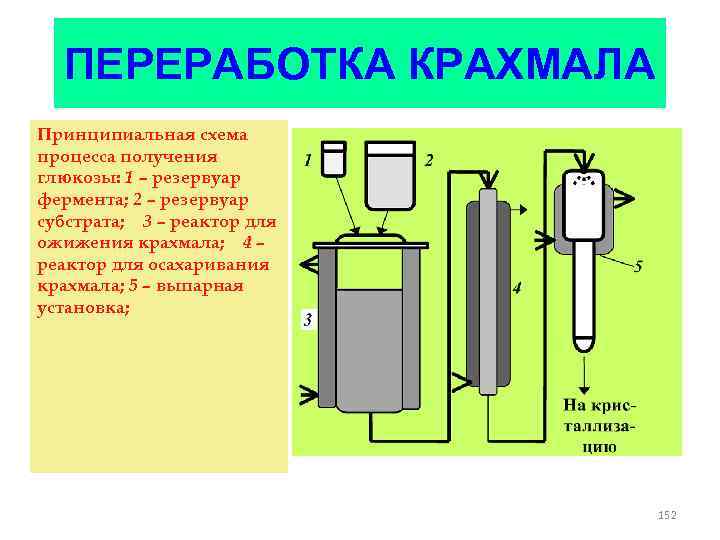 ПЕРЕРАБОТКА КРАХМАЛА Принципиальная схема процесса получения глюкозы: 1 – резервуар фермента; 2 – резервуар субстрата; 3 – реактор для ожижения крахмала; 4 – реактор для осахаривания крахмала; 5 – выпарная установка; 152
ПЕРЕРАБОТКА КРАХМАЛА Принципиальная схема процесса получения глюкозы: 1 – резервуар фермента; 2 – резервуар субстрата; 3 – реактор для ожижения крахмала; 4 – реактор для осахаривания крахмала; 5 – выпарная установка; 152
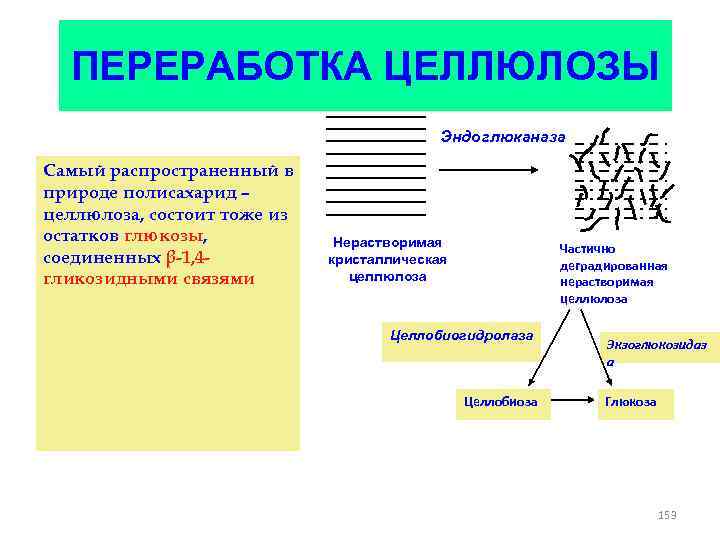 ПЕРЕРАБОТКА ЦЕЛЛЮЛОЗЫ Эндоглюканаза Самый распространенный в природе полисахарид – целлюлоза, состоит тоже из остатков глюкозы, соединенных β-1, 4 гликозидными связями Нерастворимая кристаллическая целлюлоза Частично деградированная нерастворимая целлюлоза Целлобиогидролаза Целлобиоза Экзоглюкозидаз а Глюкоза 153
ПЕРЕРАБОТКА ЦЕЛЛЮЛОЗЫ Эндоглюканаза Самый распространенный в природе полисахарид – целлюлоза, состоит тоже из остатков глюкозы, соединенных β-1, 4 гликозидными связями Нерастворимая кристаллическая целлюлоза Частично деградированная нерастворимая целлюлоза Целлобиогидролаза Целлобиоза Экзоглюкозидаз а Глюкоза 153
 ПОЛУЧЕНИЕ БЕЗЛАКТОЗНОГО МОЛОКА • Молочный сахар – лактоза – для многих детей оказывается трудно усваиваемым из-за отсутствия у них фермента, расщепляющего лактозу – βгалактозидазы (лактазы). Лактоза – глюкозил-4→ 1 -βгалактозид 154
ПОЛУЧЕНИЕ БЕЗЛАКТОЗНОГО МОЛОКА • Молочный сахар – лактоза – для многих детей оказывается трудно усваиваемым из-за отсутствия у них фермента, расщепляющего лактозу – βгалактозидазы (лактазы). Лактоза – глюкозил-4→ 1 -βгалактозид 154
 ПОЛУЧЕНИЕ БЕЗЛАКТОЗНОГО МОЛОКА • Для повышения усвояемости молока его обрабатывают иммобилизованной лактазой ( галактозидазой). Впервые этот процесс осуществлен итальянской фирмой «Чентрале дель Латте» . Молоко становится более сладким, поскольку глюкоза имеет большую сладость, чем лактоза. Иммобилизованная -галактозидаза достаточно стабильна – после 50 суток работы сохраняется 80 % первоначальной активности. • Эта же технология может использоваться для получения сахаров из молока: глюкозы и галактозы. 155
ПОЛУЧЕНИЕ БЕЗЛАКТОЗНОГО МОЛОКА • Для повышения усвояемости молока его обрабатывают иммобилизованной лактазой ( галактозидазой). Впервые этот процесс осуществлен итальянской фирмой «Чентрале дель Латте» . Молоко становится более сладким, поскольку глюкоза имеет большую сладость, чем лактоза. Иммобилизованная -галактозидаза достаточно стабильна – после 50 суток работы сохраняется 80 % первоначальной активности. • Эта же технология может использоваться для получения сахаров из молока: глюкозы и галактозы. 155
 ПОЛУЧЕНИЕ АКРИЛАМИДА • Акриламид – один из важнейших продуктов широкого потребления. Потребность в нем составляет 200 тыс. тонн в год (в мире). Используется как флоккулянт, компонент синтетических волокон, как кондиционер почвы и в других областях. • Обычный химический синтез акриламида включает гидратацию акрилонитрила в присутствии солей меди в качестве катализатора: • CH 2=CHCN + H 2 O → CH 2=CHCONH 2 • Неудобства процесса: • 1. Скорость параллельного образования акриловой кислоты выше, чем акриламида; • 2. Наличие двойной связи в субстрате и продукте приводит к образованию побочных продуктов (нитрило-трис-изопропионамид, этиленциангидрин, продукты полимеризации) 156
ПОЛУЧЕНИЕ АКРИЛАМИДА • Акриламид – один из важнейших продуктов широкого потребления. Потребность в нем составляет 200 тыс. тонн в год (в мире). Используется как флоккулянт, компонент синтетических волокон, как кондиционер почвы и в других областях. • Обычный химический синтез акриламида включает гидратацию акрилонитрила в присутствии солей меди в качестве катализатора: • CH 2=CHCN + H 2 O → CH 2=CHCONH 2 • Неудобства процесса: • 1. Скорость параллельного образования акриловой кислоты выше, чем акриламида; • 2. Наличие двойной связи в субстрате и продукте приводит к образованию побочных продуктов (нитрило-трис-изопропионамид, этиленциангидрин, продукты полимеризации) 156
 ПОЛУЧЕНИЕ АКРИЛАМИДА • Процесс получения акриламида может быть осуществлен ферментативно. Эффективная нитрилгидратаза была обнаружена у микроорганизма Pseudomonas chlororaphis. Однако, оказалось необходимым модифицировать продуцент из-за того, что исходный штамм микроорганизма продуцировал полисахарид, который приводил к высокой вязкости среды, что затрудняло выделение микробных клеток и ухудшало условия их роста за счет ослабления аэрации. • Полученный мутантный штамм обладал даже более высоким уровнем продукции фермента, так что в качестве катализатора можно было использовать неразрушенные клетки микроорганизма 157
ПОЛУЧЕНИЕ АКРИЛАМИДА • Процесс получения акриламида может быть осуществлен ферментативно. Эффективная нитрилгидратаза была обнаружена у микроорганизма Pseudomonas chlororaphis. Однако, оказалось необходимым модифицировать продуцент из-за того, что исходный штамм микроорганизма продуцировал полисахарид, который приводил к высокой вязкости среды, что затрудняло выделение микробных клеток и ухудшало условия их роста за счет ослабления аэрации. • Полученный мутантный штамм обладал даже более высоким уровнем продукции фермента, так что в качестве катализатора можно было использовать неразрушенные клетки микроорганизма 157
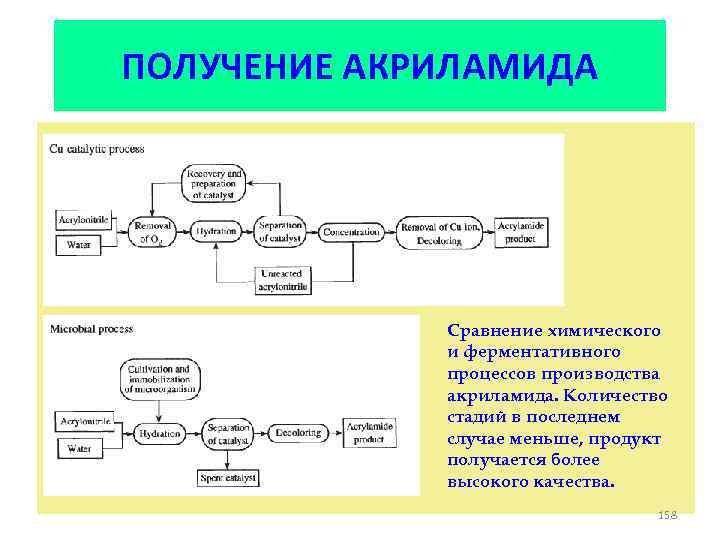 ПОЛУЧЕНИЕ АКРИЛАМИДА Сравнение химического и ферментативного процессов производства акриламида. Количество стадий в последнем случае меньше, продукт получается более высокого качества. 158
ПОЛУЧЕНИЕ АКРИЛАМИДА Сравнение химического и ферментативного процессов производства акриламида. Количество стадий в последнем случае меньше, продукт получается более высокого качества. 158
 ПОЛУЧЕНИЕ АКРИЛАМИДА Операционные параметры процесса Условия реакции Производительность р. Н 7, 5 – 8, 5 Температура 0 -5°С Концентрация акрилонитрила 1, 5 -2, 0% Конверсия акрилонитрила 99, 97% Выход акриламида 99, 99% Концентрация акрилонитрила на выходе из реактора 27 -30% Высокая степень превращения акрилонитрила позволяет исключить стадию выделения непрореагировавшего субстрата 159
ПОЛУЧЕНИЕ АКРИЛАМИДА Операционные параметры процесса Условия реакции Производительность р. Н 7, 5 – 8, 5 Температура 0 -5°С Концентрация акрилонитрила 1, 5 -2, 0% Конверсия акрилонитрила 99, 97% Выход акриламида 99, 99% Концентрация акрилонитрила на выходе из реактора 27 -30% Высокая степень превращения акрилонитрила позволяет исключить стадию выделения непрореагировавшего субстрата 159
 БИОТЕХНОЛОГИЯ Источники ферментов и перспективы развития инженерной энзимологии 160
БИОТЕХНОЛОГИЯ Источники ферментов и перспективы развития инженерной энзимологии 160
 ИСТОЧНИКИ ФЕРМЕНТОВ В подавляющем большинстве случаев источниками ферментов являются микроорганизмы. Выбор штаммов микроорганизмов осуществляется различными способами: 1. На основе имеющейся информации о свойствах ферментов из известных штаммов микроорганизмов; 2. На основе информации о физиологии известных микроорганизмов; 3. Путем направленного поиска микроорганизмов в природных экосистемах. 161
ИСТОЧНИКИ ФЕРМЕНТОВ В подавляющем большинстве случаев источниками ферментов являются микроорганизмы. Выбор штаммов микроорганизмов осуществляется различными способами: 1. На основе имеющейся информации о свойствах ферментов из известных штаммов микроорганизмов; 2. На основе информации о физиологии известных микроорганизмов; 3. Путем направленного поиска микроорганизмов в природных экосистемах. 161
 ИСТОЧНИКИ ФЕРМЕНТОВ Проблема поиска ферментов в микроорганизмах природного происхождения состоит в том, что подавляющее большинство микроорганизмов из образцов окружающей среды не удается перевести в культуру. В последние годы получает все большее распространение технология метагеномики – выделение суммарной ДНК из образцов окружающей среды, амплификация отдельных генов с праймерами, подобранными из баз данных по структуре генов определенных ферментов и клонирование полученного материала в удобных для культивирования хозяевах. 162
ИСТОЧНИКИ ФЕРМЕНТОВ Проблема поиска ферментов в микроорганизмах природного происхождения состоит в том, что подавляющее большинство микроорганизмов из образцов окружающей среды не удается перевести в культуру. В последние годы получает все большее распространение технология метагеномики – выделение суммарной ДНК из образцов окружающей среды, амплификация отдельных генов с праймерами, подобранными из баз данных по структуре генов определенных ферментов и клонирование полученного материала в удобных для культивирования хозяевах. 162
 ИСТОЧНИКИ ФЕРМЕНТОВ В необходимых случаях производится также конструирование штаммов микроорганизмов путем переноса генов из одних видов микроорганизмов в другие и объединения в одном штамме нескольких генов, кодирующих ферменты, необходимые для осуществления целевого процесса. 164
ИСТОЧНИКИ ФЕРМЕНТОВ В необходимых случаях производится также конструирование штаммов микроорганизмов путем переноса генов из одних видов микроорганизмов в другие и объединения в одном штамме нескольких генов, кодирующих ферменты, необходимые для осуществления целевого процесса. 164
 НЕКОТОРЫЕ НЕУДОБСТВА • Ферменты “настроены” на определенные субстраты, встречающиеся в системе метаболизма живых организмов • Промышленные технологии используют исходные продукты, не встречающиеся в живой природе • Часто возникает необходимость “подстройки” ферментов к использованию “незнакомых” субстратов 165
НЕКОТОРЫЕ НЕУДОБСТВА • Ферменты “настроены” на определенные субстраты, встречающиеся в системе метаболизма живых организмов • Промышленные технологии используют исходные продукты, не встречающиеся в живой природе • Часто возникает необходимость “подстройки” ферментов к использованию “незнакомых” субстратов 165
 ПЕРСПЕКТИВЫ РАЗВИТИЯ • Использование ферментов в органическом синтезе – интенсивно развивающаяся область биотехнологии • Ферменты помимо присущих им уникальных свойств – специфичности, стерео- и региоселективности имеют еще одну важную особенность: их можно конструировать, подстраивать под интересующий нас субстрат 166
ПЕРСПЕКТИВЫ РАЗВИТИЯ • Использование ферментов в органическом синтезе – интенсивно развивающаяся область биотехнологии • Ферменты помимо присущих им уникальных свойств – специфичности, стерео- и региоселективности имеют еще одну важную особенность: их можно конструировать, подстраивать под интересующий нас субстрат 166
 ПЕРСПЕКТИВЫ РАЗВИТИЯ • Основные направления модификации и дизайна биокатализаторов: • Молекулярная эволюция ферментов; • Конструирование каталитически активных антител (абзимов); • Разработка каталитически активных нуклеиновых кислот (рибозимов) 167
ПЕРСПЕКТИВЫ РАЗВИТИЯ • Основные направления модификации и дизайна биокатализаторов: • Молекулярная эволюция ферментов; • Конструирование каталитически активных антител (абзимов); • Разработка каталитически активных нуклеиновых кислот (рибозимов) 167
 МОЛЕКУЛЯРНАЯ ЭВОЛЮЦИЯ ФЕРМЕНТОВ • Под термином “молекулярная эволюция ферментов” подразумевается модификация генов ферментов и последующая селекция вариантов, в которых аминокислотные замены привели к улучшению свойств фермента в заданном направлении 168
МОЛЕКУЛЯРНАЯ ЭВОЛЮЦИЯ ФЕРМЕНТОВ • Под термином “молекулярная эволюция ферментов” подразумевается модификация генов ферментов и последующая селекция вариантов, в которых аминокислотные замены привели к улучшению свойств фермента в заданном направлении 168
 КАК МОДИФИЦИРУЮТ ГЕНЫ • Модификацию гена можно производить направленно, меняя природу аминокислоты в одном заданном участке белковой цепи, либо довериться случаю, создав для этого необходимые условия 169
КАК МОДИФИЦИРУЮТ ГЕНЫ • Модификацию гена можно производить направленно, меняя природу аминокислоты в одном заданном участке белковой цепи, либо довериться случаю, создав для этого необходимые условия 169
 КАК МОДИФИЦИРУЮТ ГЕНЫ • Современные знания о роли отдельных аминокислотных остатков в формировании структуры белка недостаточны для предсказания эффекта замены аминокислоты на функции белка • Именно по этой причине методы ввода случайных мутаций оказались более универсальными 170
КАК МОДИФИЦИРУЮТ ГЕНЫ • Современные знания о роли отдельных аминокислотных остатков в формировании структуры белка недостаточны для предсказания эффекта замены аминокислоты на функции белка • Именно по этой причине методы ввода случайных мутаций оказались более универсальными 170
 НАПРАВЛЕНИЯ “ПОДСТРОЙКИ” ФЕРМЕНТОВ • Повышение термостабильности ферментов • Повышение устойчивости к органическим растворителям • Изменение р. Н – оптимума • Изменение специфичности к субстрату • Повышение или изменение стереоселективности • Адаптация к условиям суперпродукции при получении рекомбинантных ферментов 171
НАПРАВЛЕНИЯ “ПОДСТРОЙКИ” ФЕРМЕНТОВ • Повышение термостабильности ферментов • Повышение устойчивости к органическим растворителям • Изменение р. Н – оптимума • Изменение специфичности к субстрату • Повышение или изменение стереоселективности • Адаптация к условиям суперпродукции при получении рекомбинантных ферментов 171
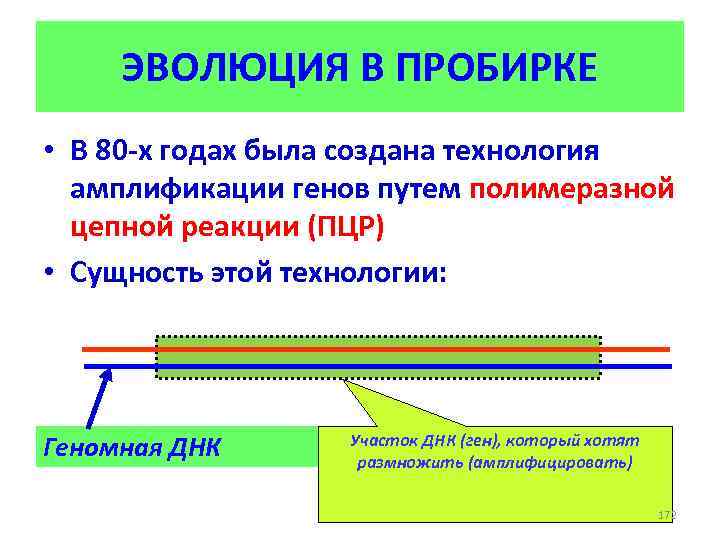 ЭВОЛЮЦИЯ В ПРОБИРКЕ • В 80 -х годах была создана технология амплификации генов путем полимеразной цепной реакции (ПЦР) • Сущность этой технологии: Геномная ДНК Участок ДНК (ген), который хотят размножить (амплифицировать) 172
ЭВОЛЮЦИЯ В ПРОБИРКЕ • В 80 -х годах была создана технология амплификации генов путем полимеразной цепной реакции (ПЦР) • Сущность этой технологии: Геномная ДНК Участок ДНК (ген), который хотят размножить (амплифицировать) 172
 ЭВОЛЮЦИЯ В ПРОБИРКЕ • Если первичная структура (последовательность нуклеотидных звеньев) в концевых областях гена известна, синтезируют праймеры короткие фрагменты, комплементарные концевым последовательностям обеих цепей. • Затем эти фрагменты добавляют к ДНК, нагревают смесь и медленно охлаждают (проводят «отжиг» ). 173
ЭВОЛЮЦИЯ В ПРОБИРКЕ • Если первичная структура (последовательность нуклеотидных звеньев) в концевых областях гена известна, синтезируют праймеры короткие фрагменты, комплементарные концевым последовательностям обеих цепей. • Затем эти фрагменты добавляют к ДНК, нагревают смесь и медленно охлаждают (проводят «отжиг» ). 173
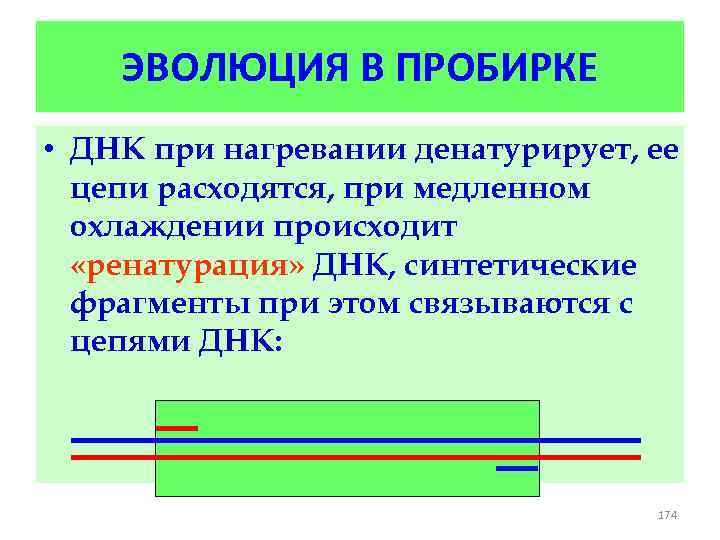 ЭВОЛЮЦИЯ В ПРОБИРКЕ • ДНК при нагревании денатурирует, ее цепи расходятся, при медленном охлаждении происходит «ренатурация» ДНК, синтетические фрагменты при этом связываются с цепями ДНК: 174
ЭВОЛЮЦИЯ В ПРОБИРКЕ • ДНК при нагревании денатурирует, ее цепи расходятся, при медленном охлаждении происходит «ренатурация» ДНК, синтетические фрагменты при этом связываются с цепями ДНК: 174
 ЭВОЛЮЦИЯ В ПРОБИРКЕ • К полученной смеси добавляют фермент – ДНК-полимеразу и субстраты – нуклеозидтрифосфаты, после чего происходит синтез цепей ДНК: 175
ЭВОЛЮЦИЯ В ПРОБИРКЕ • К полученной смеси добавляют фермент – ДНК-полимеразу и субстраты – нуклеозидтрифосфаты, после чего происходит синтез цепей ДНК: 175
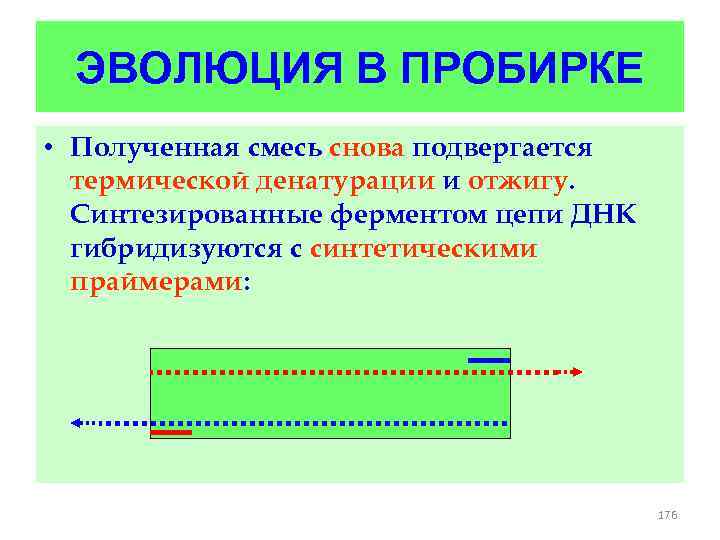 ЭВОЛЮЦИЯ В ПРОБИРКЕ • Полученная смесь снова подвергается термической денатурации и отжигу. Синтезированные ферментом цепи ДНК гибридизуются с синтетическими праймерами: 176
ЭВОЛЮЦИЯ В ПРОБИРКЕ • Полученная смесь снова подвергается термической денатурации и отжигу. Синтезированные ферментом цепи ДНК гибридизуются с синтетическими праймерами: 176
 ЭВОЛЮЦИЯ В ПРОБИРКЕ • Затем снова проводится ПЦР: Каждый раз при проведении цикла ПЦР – денатурация – отжиг происходит удвоение материала целевого гена. Таких циклов можно провести несколько десятков, в результате можно получить большое количество материала для дальнейших исследований 177
ЭВОЛЮЦИЯ В ПРОБИРКЕ • Затем снова проводится ПЦР: Каждый раз при проведении цикла ПЦР – денатурация – отжиг происходит удвоение материала целевого гена. Таких циклов можно провести несколько десятков, в результате можно получить большое количество материала для дальнейших исследований 177
 ЭВОЛЮЦИЯ В ПРОБИРКЕ • Многие термофильные полимеразы, используемые в ПЦР, менее точны, чем мезофильные. • Это оказалось возможным использовать для введения случайных мутаций (нуклеотидных замен) в копии генов. • Так возникла идея «управляемой» эволюции. 178
ЭВОЛЮЦИЯ В ПРОБИРКЕ • Многие термофильные полимеразы, используемые в ПЦР, менее точны, чем мезофильные. • Это оказалось возможным использовать для введения случайных мутаций (нуклеотидных замен) в копии генов. • Так возникла идея «управляемой» эволюции. 178
 УПРАВЛЯЕМАЯ ЭВОЛЮЦИЯ • Гены, кодирующие белки с одинаковыми функциями, встречаются в разных организмах; свойства белков из разных источников отличаются Библиотека родственных генов из разных организмов 179
УПРАВЛЯЕМАЯ ЭВОЛЮЦИЯ • Гены, кодирующие белки с одинаковыми функциями, встречаются в разных организмах; свойства белков из разных источников отличаются Библиотека родственных генов из разных организмов 179
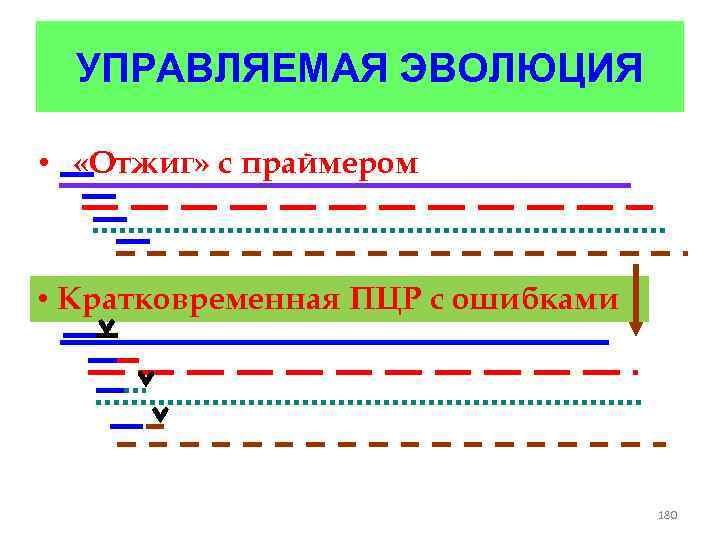 УПРАВЛЯЕМАЯ ЭВОЛЮЦИЯ • «Отжиг» с праймером • Кратковременная ПЦР с ошибками 180
УПРАВЛЯЕМАЯ ЭВОЛЮЦИЯ • «Отжиг» с праймером • Кратковременная ПЦР с ошибками 180
 УПРАВЛЯЕМАЯ ЭВОЛЮЦИЯ • После многократного повторения цикла отжиг – ПЦР – денатурация получается библиотека «мозаичных» генов с мутациями: 181
УПРАВЛЯЕМАЯ ЭВОЛЮЦИЯ • После многократного повторения цикла отжиг – ПЦР – денатурация получается библиотека «мозаичных» генов с мутациями: 181
 АДАПТАЦИЯ К ФИЗИКОХИМИЧЕСКИМ УСЛОВИЯМ • При использовании ферментов в органическом синтезе возникает проблема устойчивости ферментов в присутствии органических растворителей. Методами молекулярной эволюции получены варианты субтилизина, сохраняющие активность в 85%-ном диметилформамиде и имеющие более удобный оптимум р. Н. J. E. Ness et al. Nat. Biotech. , 17, 893, (1999) L. You et al. Protein Engng. , 9, 77 (1996) H. Zhao et al. Protein Engng. , 12, 47 (1999) 182
АДАПТАЦИЯ К ФИЗИКОХИМИЧЕСКИМ УСЛОВИЯМ • При использовании ферментов в органическом синтезе возникает проблема устойчивости ферментов в присутствии органических растворителей. Методами молекулярной эволюции получены варианты субтилизина, сохраняющие активность в 85%-ном диметилформамиде и имеющие более удобный оптимум р. Н. J. E. Ness et al. Nat. Biotech. , 17, 893, (1999) L. You et al. Protein Engng. , 9, 77 (1996) H. Zhao et al. Protein Engng. , 12, 47 (1999) 182
 ЭВОЛЮЦИЯ ТЕРМОСТАБИЛЬНОСТИ • Повышение активности термофильных ферментов при умеренных температурах – часто встречающаяся задача. Для глюкозоизомеразы – фермента, широко используемого в промышленном производстве глюкозо-фруктозных сиропов, эту задачу удалось решить. Мутации локализованы на удалении от каталитического центра и участка связывания металлов. A. Lönn et al. Eur. J. Biochem. , 89, 116 (2002) 183
ЭВОЛЮЦИЯ ТЕРМОСТАБИЛЬНОСТИ • Повышение активности термофильных ферментов при умеренных температурах – часто встречающаяся задача. Для глюкозоизомеразы – фермента, широко используемого в промышленном производстве глюкозо-фруктозных сиропов, эту задачу удалось решить. Мутации локализованы на удалении от каталитического центра и участка связывания металлов. A. Lönn et al. Eur. J. Biochem. , 89, 116 (2002) 183
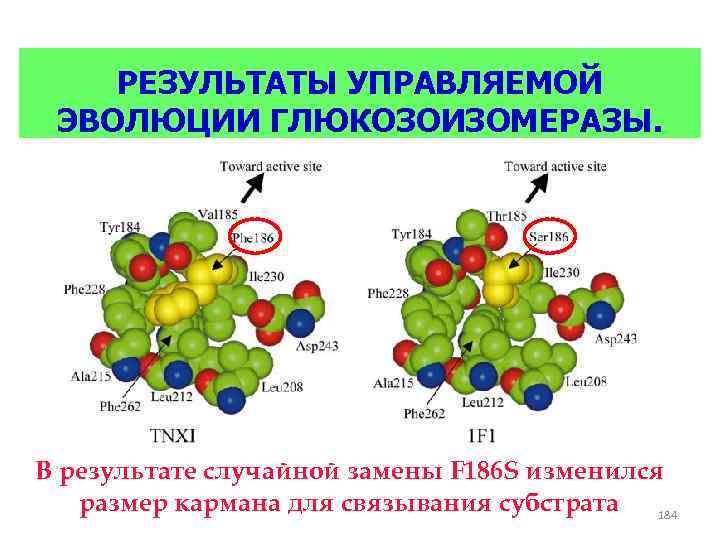 РЕЗУЛЬТАТЫ УПРАВЛЯЕМОЙ ЭВОЛЮЦИИ ГЛЮКОЗОИЗОМЕРАЗЫ. В результате случайной замены F 186 S изменился размер кармана для связывания субстрата 184
РЕЗУЛЬТАТЫ УПРАВЛЯЕМОЙ ЭВОЛЮЦИИ ГЛЮКОЗОИЗОМЕРАЗЫ. В результате случайной замены F 186 S изменился размер кармана для связывания субстрата 184
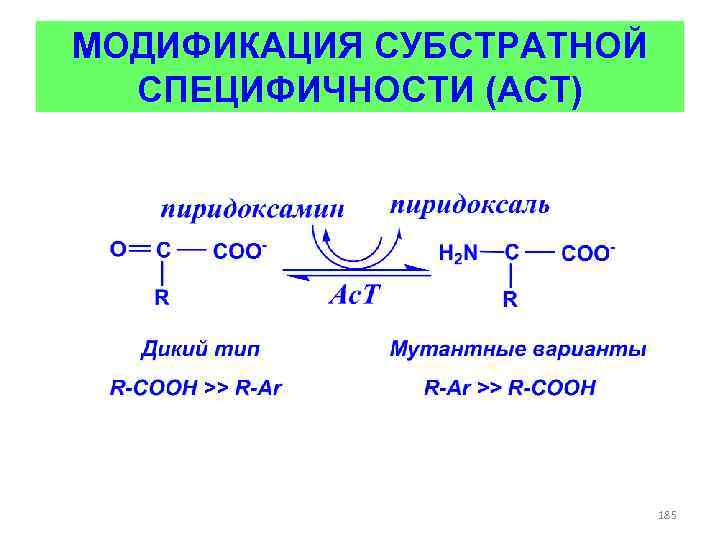 МОДИФИКАЦИЯ СУБСТРАТНОЙ СПЕЦИФИЧНОСТИ (АСТ) 185
МОДИФИКАЦИЯ СУБСТРАТНОЙ СПЕЦИФИЧНОСТИ (АСТ) 185
 МОДИФИКАЦИЯ СУБСТРАТНОЙ СПЕЦИФИЧНОСТИ • Для расширения круга используемых субстратов аспартатаминотрансферазу подвергли модификации путем молекулярной эволюции гена. Фермент дикого типа наиболее активен с кислыми субстратами, слабо активен с ароматическими 2 -кето- и -аминокислотами и субстратами с разветвлениями в β-положении боковой цепи. За пять раундов “перетасовки” гена получены варианты с повышенной в 105 раз активностью по отношению к β-разветвленным субстратам. T. Yano et al. PNAS, 95, pp 5511 -5515 (1998) 186
МОДИФИКАЦИЯ СУБСТРАТНОЙ СПЕЦИФИЧНОСТИ • Для расширения круга используемых субстратов аспартатаминотрансферазу подвергли модификации путем молекулярной эволюции гена. Фермент дикого типа наиболее активен с кислыми субстратами, слабо активен с ароматическими 2 -кето- и -аминокислотами и субстратами с разветвлениями в β-положении боковой цепи. За пять раундов “перетасовки” гена получены варианты с повышенной в 105 раз активностью по отношению к β-разветвленным субстратам. T. Yano et al. PNAS, 95, pp 5511 -5515 (1998) 186
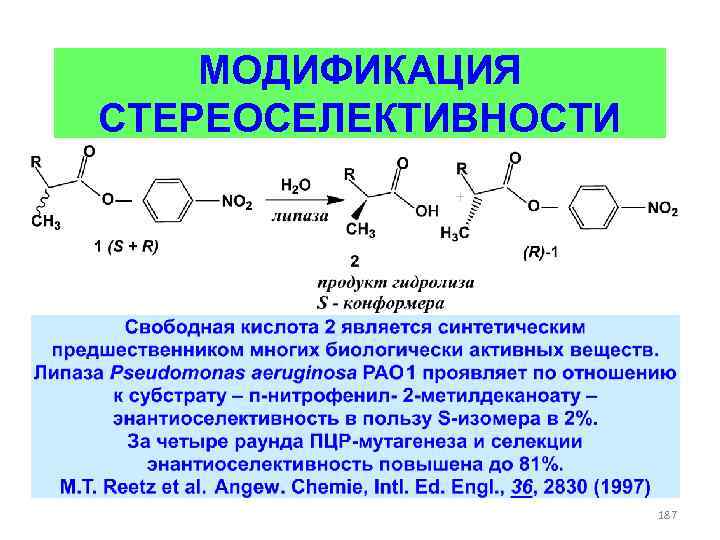 МОДИФИКАЦИЯ СТЕРЕОСЕЛЕКТИВНОСТИ 187
МОДИФИКАЦИЯ СТЕРЕОСЕЛЕКТИВНОСТИ 187
 КАТАЛИТИЧЕСКИ АКТИВНЫЕ АНТИТЕЛА (АБЗИМЫ) • Помимо использования природных катализаторов – ферментов возможно создание катализаторов путем их конструирования под определенные реакции. • Это направление развилось с момента появления идеи создания каталитически активных антител - абзимов 188
КАТАЛИТИЧЕСКИ АКТИВНЫЕ АНТИТЕЛА (АБЗИМЫ) • Помимо использования природных катализаторов – ферментов возможно создание катализаторов путем их конструирования под определенные реакции. • Это направление развилось с момента появления идеи создания каталитически активных антител - абзимов 188
 АБЗИМЫ 189
АБЗИМЫ 189
 АБЗИМЫ • Для получения антител, опознающих низкомолекулярные соединения, эти соединения присоединяют к какому-либо белку и иммунизируют животное. • Полученную после иммунизации антисыворотку истощают белкомносителем и получают иммуноглобулины, связывающие гаптен 190
АБЗИМЫ • Для получения антител, опознающих низкомолекулярные соединения, эти соединения присоединяют к какому-либо белку и иммунизируют животное. • Полученную после иммунизации антисыворотку истощают белкомносителем и получают иммуноглобулины, связывающие гаптен 190
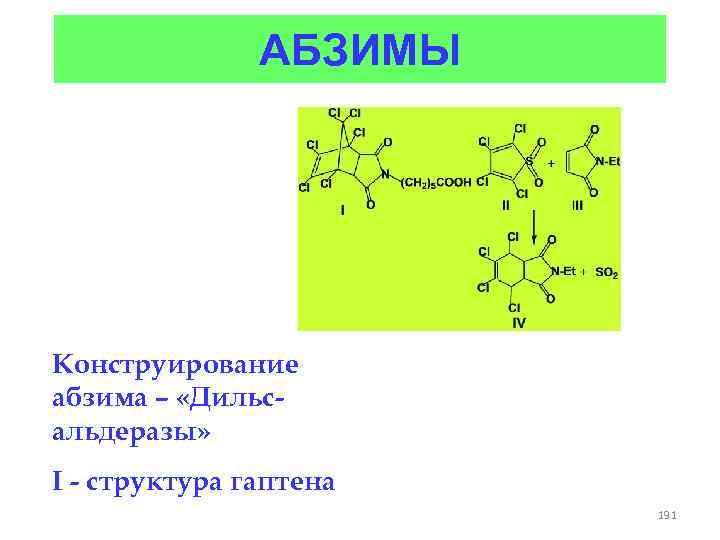 АБЗИМЫ Конструирование абзима – «Дильсальдеразы» I - структура гаптена 191
АБЗИМЫ Конструирование абзима – «Дильсальдеразы» I - структура гаптена 191
 РИБОЗИМЫ • В дальнейшем было обнаружено, что нуклеиновые кислоты могут проявлять активность не только по отношению к себе подобным. • Оказалось, что РНК (и ДНК) способны катализировать гидролиз сложных эфиров (например, эфиров холестерина) и даже реакцию Дильса – Альдера 192
РИБОЗИМЫ • В дальнейшем было обнаружено, что нуклеиновые кислоты могут проявлять активность не только по отношению к себе подобным. • Оказалось, что РНК (и ДНК) способны катализировать гидролиз сложных эфиров (например, эфиров холестерина) и даже реакцию Дильса – Альдера 192
 РИБОЗИМЫ • К нуклеиновым кислотам применимы приемы молекулярной эволюции • Схема селекции рибозимов: Пул РНК хроматографируют на сорбенте, содержащем в качестве аффинного лиганда аналог переходного состояния реакции, катализ которой хотят осуществить. Сорбирующиеся РНК – исходный материал для последующих раундов селекции на том же сорбенте. 193
РИБОЗИМЫ • К нуклеиновым кислотам применимы приемы молекулярной эволюции • Схема селекции рибозимов: Пул РНК хроматографируют на сорбенте, содержащем в качестве аффинного лиганда аналог переходного состояния реакции, катализ которой хотят осуществить. Сорбирующиеся РНК – исходный материал для последующих раундов селекции на том же сорбенте. 193


