interaction.ppt
- Количество слайдов: 59

INTERACTIONS OF BIOGEOCHEMICAL CYCLES These biogeochemical cycles are intimately interconnected and are ultimately powered by energy from the Sun via photosynthetic carbon fixation. Localized exceptions occur such as, for example, hydrothermal environments, where the energy for carbon fixation and biomaterial synthesis may be provided by inorganic reducing species emanating from rocks. The transformations within each biogeochemical cycle are reduction and oxidation reactions, each providing a basis for connection between biogeochemical cycles.

1. STOICHIOMETRIC ASPECTS OF NUTRIENT UPTAKE AND NUTRIENT LIMITATIONS OF LIVING MATTER PRODUCTION The various essential chemical nutrients are often determined in predicted proportions in living organisms. The C: N ratio in microbial plasma is between 4 to 10, in soil humus 6 to 35, and in forest biomass about 160. At the global level, we can consequently calculate how much nitrogen should be involved in biogeochemical cycling to provide the annual net primary productivity (NPP) of terrestrial ecosystems at this ratio for as much as 60 109 tons of carbon per year. Simple calculations show that at least 0, 4 109 tons of nitrogen should be supplied through biogeochemical cycling in global terrestrial ecosystems. Furthermore, as we have seen already, nitrogen and phosphorus are the most deficient elements, and their availability is the limiting factor of living matter productivity.

Organisms fixing carbon by photosynthesis also require a continual supply of nutrients such as N, P, K, Ca, Mg, etc, thus forming links in the biogeochemical food web and interactions between cycles of various nutrients. The availability of these elements in various terrestrial and aquatic ecosystems influences the heterogeneity of NPP values and spatial aspects of ecosystem productivity. The nitrogen biogeochemical cycle is similar to the carbon cycle and characterized by a rapid recycling within relatively small reservoirs in various compartments of the biosphere. Even smaller pools of nitrogen are in living organisms. Much larger and slower turnover rates are typical for interactions between nitrogen reservoirs in atmosphere and ocean bottom sediments, or between atmosphere and soil organic matter. The atomic carbon-tonitrogen ratio C: N in living biomass ranges from about 7 (marine microbes) to more than 100 for woody terrestrial materials. In dead organic matter, this ratio increases gradually during burial and diagenesis. This is accompanied with nitrogen release and recycling.

Phosphorus is even less abundant in biota than nitrogen. For marine organic matter, the atomic ratio of carbon-to-phosphorus (C: P) is 106: 1 (Redfield et al, 1963). Fossil fuels and fossil organic matter on the whole are depleted in phosphorus, consistent with rapid and efficient recycling of organic phosphorus species. The slowly cycling lithospheric phosphorus reservoir contains 0, 8 -1, 1 109 tons of P. Deficiency or availability of this nutrient is considered more likely to affect the productivity of many terrestrial and marine ecosystems than that of nitrogen. The biogeochemical carbon and sulfur cycles are tightly interrelated. The atomic C: S ratio in living biomass is 200: 1. However, fossil organic matter, particularly that deposited in certain ancient marine environments, contains significant amounts of organic sulfur, up to 10% w/w and atomic C: S ratio as much as 1: 1. This is far in excess of the normal sulfur content in living organisms, ranging from 0. 5 to 1. 5% by dry weight.

The biogeochemical sulfur cycle is one of the most important biogeochemical phenomena despite the relatively low content of this element in biota and the fact that sulfur compounds themselves are a quantitatively minor, albeit essential, component. Certain classes of bacteria, the sulfide-oxidizing bacteria and phototrophic sulfur bacteria, continually transform vast quantities of sulfur from sulfide to sulfate in energy transfer processes. Other groups of bacteria can utilize sulfate as an oxidant for respiration in the process of assimilatory sulfate reduction. These processes are not only for biogeochemical S cycle but also for interplay between many essential nutrients and their biogeochemical cycling in ecosystems.

Many elements are minor, in quantitative terms, but nevertheless essential constituents of living organisms. Some of them - Cu, Zn, Co, B, Se, Mo, Na, F, Cl, Br, I, Fe, Mn, Cr, and V. Distribution of these elements is affected, in various extent, by biochemical and physiological processes. Of these elements, Fe is a particularly significant chemical element. In living organisms, Fe is a constituent of a number of enzymes in cells, especially those related with respiration. Thiobacillus ferrooxidans and some other microbes can derive energy from the oxidation of Fe 2+. Furthermore, deposition of sedimentary pyrite and organic matter were the two principal reduced partners, which balanced atmospheric oxygen during biosphere evolution. These processes are important at present as well.
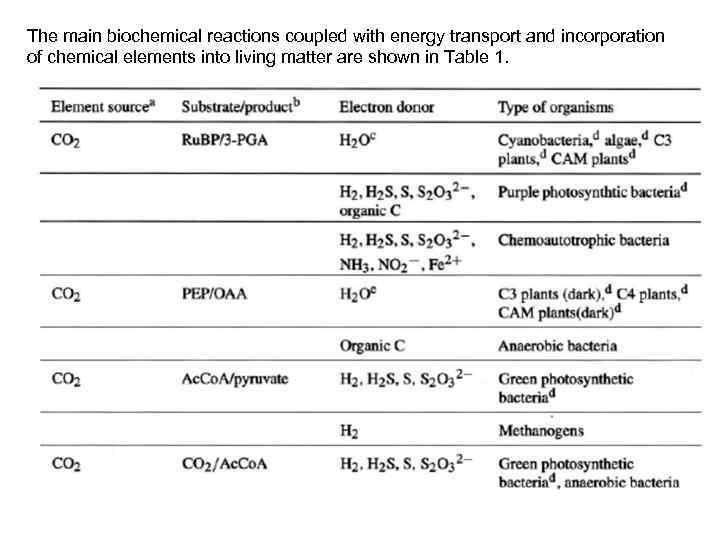
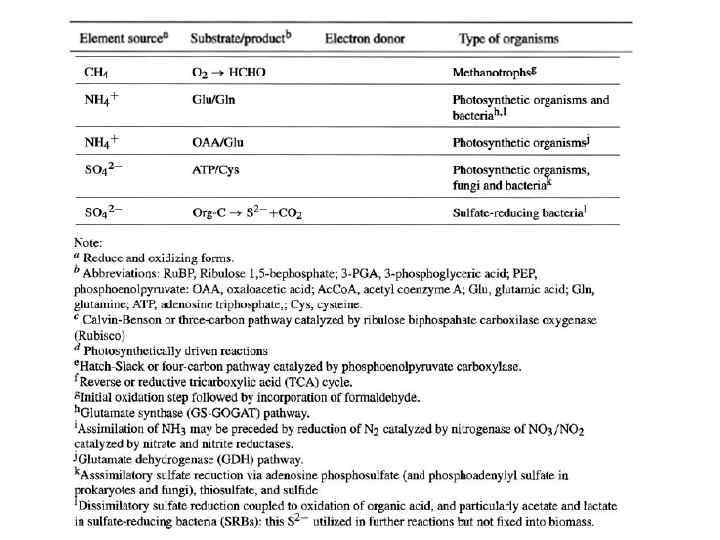
The main biochemical reactions coupled with energy transport and incorporation of chemical elements into living matter are shown in Table 1.
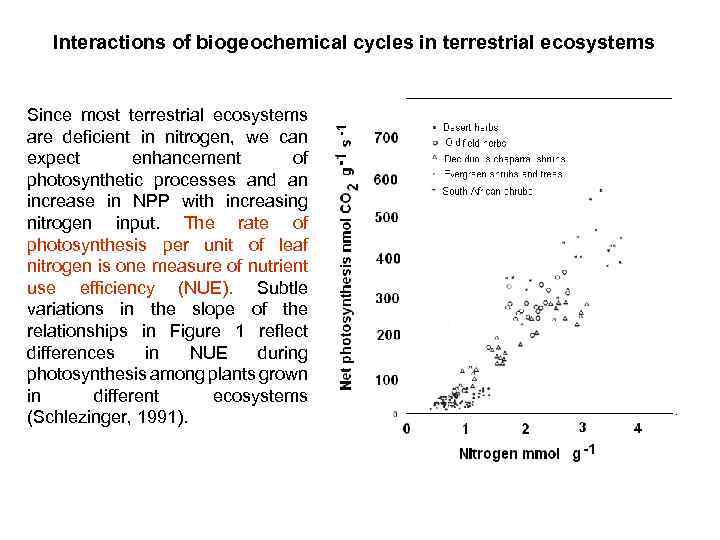
Interactions of biogeochemical cycles in terrestrial ecosystems Since most terrestrial ecosystems are deficient in nitrogen, we can expect enhancement of photosynthetic processes and an increase in NPP with increasing nitrogen input. The rate of photosynthesis per unit of leaf nitrogen is one measure of nutrient use efficiency (NUE). Subtle variations in the slope of the relationships in Figure 1 reflect differences in NUE during photosynthesis among plants grown in different ecosystems (Schlezinger, 1991).

This relationship is very important for modeling the possible greenhouse effects due to accumulation of carbon dioxide in the troposphere and the possible role of simultaneous increasing nitrogen supply due to air pollution by nitrogen oxides. It is reasonable that this artificial fertilization of natural ecosystems, forest ecosystems especially, will lead to increasing photosynthesis, increasing NPP and increasing sequestration of both C and P in plant biomass. The only open question is on the P deficiency, which may limit all the processes mentioned above. The typical ratios between essential nutrients in the plant biomass of the World’s terrestrial ecosystems are shown in Table 2.
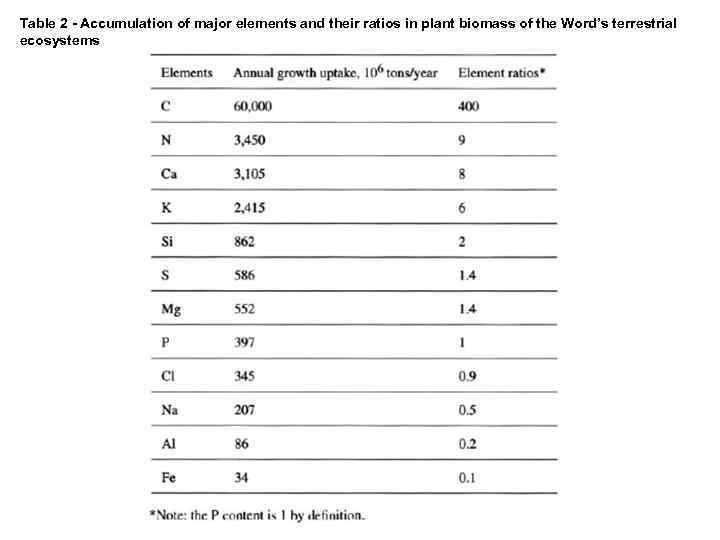
Table 2 - Accumulation of major elements and their ratios in plant biomass of the Word’s terrestrial ecosystems

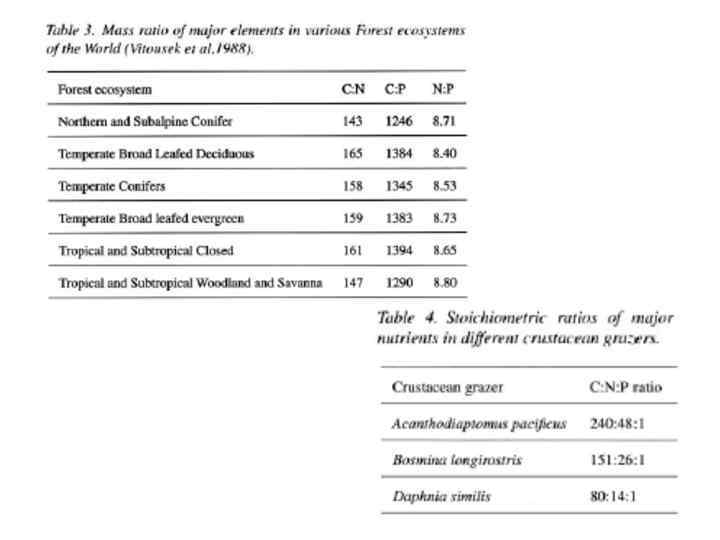
Taking into account the limiting role of phosphorus in many terrestrial ecosystems, the ratio between various elements is calculated assuming P content as a unit. In this case, the averaged ratio of main essential elements may be drawn as C: N: S: P=400: 9: 1. 4: 1 for plant biomass of the global terrestrial ecosystems. Vitousek et al (1988) have compiled results indicating the proportions of carbon and major essential nutrients in various Forest ecosystems of the World (Table 3). The nutrient ratios vary insignificantly, i. e. , 143 -165 for C: N, 1246– 1383 for C: P, and 8. 40– 8. 80 for N: P ratio for the total plant biomass. The content of nutrients in leaf tissues is higher and C: N and C: P ratios are correspondingly smaller. Thus, we should remember that nutrient ratios increase with time as the vegetation species become increasingly dominated by structural tissues with lower concentration of essential species (Schlezinger, 1991). Generally, in humus the ratio of C: N: P: S is close to 140: 1. 3: 1. 3 (Stevenson, 1986). As a result of its high nutrient content, humus plays a role of biogeochemical barrier in soil profile and dominates the storage of biogeochemical species in most ecosystems. For instance, in Temperate Forest ecosystems, the above ground biomass contains only 4– 8 % of the total pool of nitrogen accumulated in the whole ecosystem. Slightly higher percentages are monitored in Tropical Forest ecosystems, since the rates of biogeochemical cycling are very high in these ecosystems and the litterfall and dead organic matter mineralize very rapidly, during a month or so.

Eutrophication of natural waters In natural waters, phosphorus is usually the limiting element. This means that phosphorus limits the algal growth, but not, for instance, the supply of nitrogen or carbon. There are many monitoring results showing the relationship between input of various nutrients into surface waters, both freshwater and marine waters, and development of eutrophication processes, or accelerated aging of lakes. The uptake of nutrients into biomass occurs in the approximate ratio C: N: P = 100: 15: 1. However, phosphorus concentrations in natural waters are usually so much lower than those of nitrogen and carbon that phosphorus can be a limiting nutrient, even though only 0. 01 times as much phosphorus as carbon is needed for algal growth. In practice the measured content of P species in fresh and marine waters is higher than dissolved carbon species. This apparent inconsistency arises from sources of nutrient supply. We have seen, that carbonate can be re-supplied by atmospheric СО 2. A similar explanation applies to nitrogen since this element can be fixed by blue-green algae with corresponding increasing of dissolved nitrogen species in waters.

Thus we can see that the interactions of biogeochemical cycles in natural waters and relevant ratios between nutrients in various aquatic living organisms determine the productivity of freshwater and marine ecosystems. A. C. Redfield et al in 1963 first demonstrated a characteristic elemental ratio between N, P and C in marine phytoplankton, showing that this left a “fingerprint” on the cycling of major elements throughout oceanic and indeed biosphere biogeochemical food webs. This ratio was then shown to be relatively reliable in marine waters, whereas algal nutrient ratios in fact vary widely in fresh waters. Since then, there has also been considerable research work indicating that the nutrient stoichiometry of grazers is often very divergent from the typical “Redfield ratio” (Elser, 1999). Ratios for three typical crustacean grazers are given in Table 4 as illustration. Equally, many species have looked at grazer nutrient recycling, generally for N in marine waters and for P in freshwaters, but rarely were both nutrients taken into account or their relative recycling rates looked at.

Interactions of biogeochemical cycles in microbial mats Microbial mats are communities in surface water ecosystems where bacteria and bacterial processes dominate. In microbial mats dissolved nutrients and metabolites are transformed by one-dimensional (vertical) molecular diffusion. The distinction between microbial mats and biofilms is not sharp. By definition (Fenchel et al, 1998), microbial mats are typically stratified vertically with respect to different functional types of bacteria. Microbial mats are thicker (often several millimeters) than biofilms. In microbial mats various types of filamentous prokaryotes are the most conspicuous part and they are responsible for the mechanical coherence of the mat. The mechanical stability of microbial mats is reinforced by the bacterial excretion of mucous polymers, producing a gelatinous matrix. Requirements for the development of microbial mats include a sufficient energy supply and conditions that more or less exclude eukaryotic activity, especially grazing and mechanical disturbance (bioturbation). Microbial mats are widely distributed in spice of the somewhat special conditions required for their formation and integrity. In most places they are transient or seasonal phenomena of limited extension. They grow at most a few millimeters in thickness.

There are different types of microbial mats, based on colorless sulfur bacteria, purple sulfur bacteria, iron bacteria and cyanobacteria. The most studied mats are those represented by filamentous cyanobacteria. They are widely distributed in protected intertidal sand flats where periodic desiccation discourages colonization by marine invertebrates. Such shallow waters or intertidal mats have now been recorded in many places of the World. These mats are all ephemeral or seasonal, and only in some specific conditions of tropical and subtropical lagoons can they form permanently The major processes of cyanobacterial mats are shown in Figures 2 and 3. Cyanobacteria dominate oxygenic photosynthesis. It has been shown that almost all the activity in terms of energy flow, and both photosynthetic and heterotrophic element cycling, occurs in the surface layer, which thickness is less than 1 cm. The mat metabolism is driven by the rapid turnover of cyanobacterial photosynthesis. In the light, cyanobacterial mats are net producers of oxygen and accumulators of reduced carbon and sulfur species. During nighttime, the mat consumes oxygen. Accordingly, carbon dioxide is taken up during the day and released during the night. Most sulfur, carbon and oxygen is recycled within the mats implying relatively closed systems.
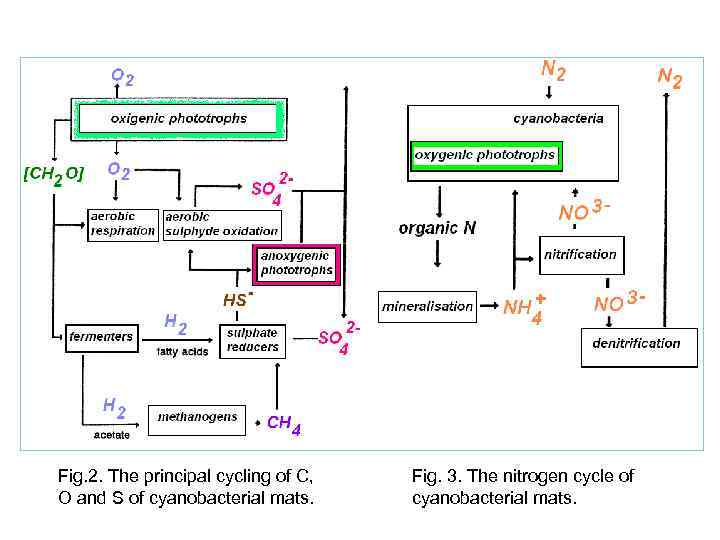
Fig. 2. The principal cycling of C, O and S of cyanobacterial mats. Fig. 3. The nitrogen cycle of cyanobacterial mats.

The nitrogen cycle is probably also largely internal. However, cyanobacteria, anoxygenic phototrophs and other anaerobic or microaerobic bacteria can fix nitrogen from the atmosphere. This N fixation compensates for the losses of nitrogen due to denitrification. The N cycle varies diurnally due to vertical migration of the oxicanoxic interface and the fact that N fixation is largely confined to darkness when conditions close to the surface are micro-oxic or anaerobic (Fenchel et al, 1998).

Биогеохимические механизмы азотного лимитирования в прибрежных морских экосистемах Эти экосистемы расположены внутри континентального шельфа. Они более соленые, чем эстуарии в большей степени влиянию океана. Вопрос о лимитировании прибрежных морских экосистем был проанализирован Howarth (1988) и Vitousek, Howarth (1991). Первичная продукция фитопланктона в условиях лимиторования азотом или фосфором является функцией их доступности. Выше было показано, что в отсутствии лимитирования фитоплантона между азотом и фосфором должно выполняться соотношение молей 16: 1. Когда отношение меньше, первичная продукция лимитирована азотом, в противном случае, наступает лимитирование по азоту.
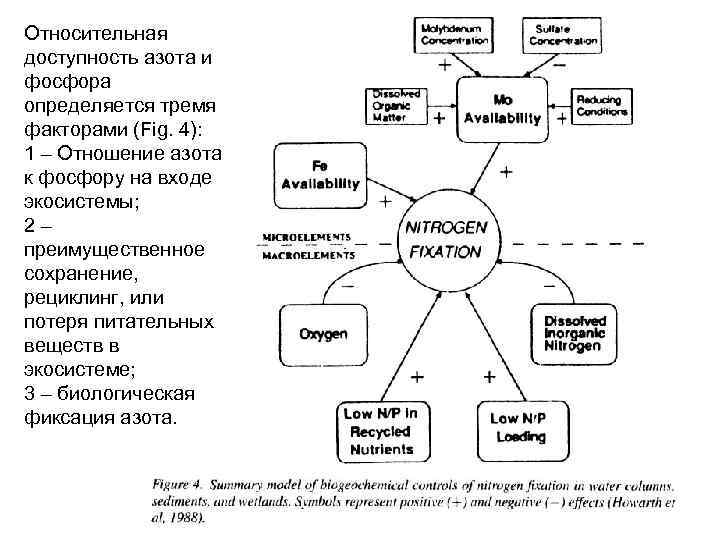
Относительная доступность азота и фосфора определяется тремя факторами (Fig. 4): 1 – Отношение азота к фосфору на входе экосистемы; 2 – преимущественное сохранение, рециклинг, или потеря питательных веществ в экосистеме; 3 – биологическая фиксация азота.

В каждом из указанных факторов возможны причины, по которым лимитирование азотом выражено в большей степени в прибрежных экосистемах по сравнению с озерами. Например, озера получают элементы за счет стока с наземных экосистем и из атмосферы, тогда как эстуарии и прибрежная зоны получают элементы из тех же источников, а также из соседних океанических водных масс. Эстуарии вдоль северо-восточного побережья США из океанской воды получают элементы питания (N: P) меньше указанного, это приводит к денитрификации континентальных шельфов (Nixon et al. 1995, 1996). Поэтому при равном поступлении с суши, эстуарии будут в большей степени ограничены по азоту, чем озера. Другой фактор, который необходимо отметить, это степень антропогенной нагрузки. При замене леса на агроценоз, а затем на промышленную зону, поток азота фосфора возрастают одновременно, но отношение N: P часто снижается. (Billen et al. 1991; Howarth et al. 1996).

Активность биогеохимических процессов в водных экосистемах зависит от доступности для фитопланктона питательных элементов. Процесс денитрифиикации при образовании донных отложений и абсорбция фосфатов представляются ведущими силами, которые влияют на соотношение азота и фосфора в годичном или более длительном цикле. Другие процессы, такие как преимущественное накопление фосфора в зоопланктоне (Sterner et al. 1992), влияют только в относительно короткий период. Денитрификация часто является главным стоком азота в водных экосистемах и это приводит к дефициту азота и к изменению в других процессах, таких как связывание фосфора. Величина денитрификации выше в эстуариях, чем в пресноводных экосистемах. Это может быть результатом большего потока азота через эстуарии. В процентном выражении поступление азота в систему и его потеря путем денитрификации отличаются незначительно, если сравнивать эстуарии и пресноводные экосистемы (Nixon et al. 1996). Может показаться, что денитрификация в равной степени снижает содержание азота в прибрежной зоне и в пресных экосистемах. В действительности, если лимитирование связано с денитрификацией, процесс идет быстрее в озерах, так как озерах, так как у них больше время удержания воды и соответственно процент потери азота при денитификации (Nixon et al. 1996; Howarth et al. 1996).
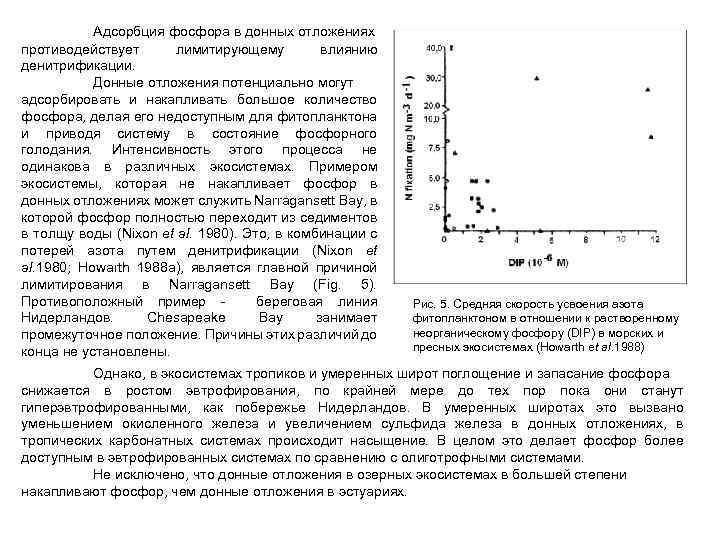
Адсорбция фосфора в донных отложениях противодействует лимитирующему влиянию денитрификации. Донные отложения потенциально могут адсорбировать и накапливать большое количество фосфора, делая его недоступным для фитопланктона и приводя систему в состояние фосфорного голодания. Интенсивность этого процесса не одинакова в различных экосистемах. Примером экосистемы, которая не накапливает фосфор в донных отложениях может служить Narragansett Bay, в которой фосфор полностью переходит из седиментов в толщу воды (Nixon et al. 1980). Это, в комбинации с потерей азота путем денитрификации (Nixon et al. 1980; Howarth 1988 a), является главной причиной лимитирования в Narragansett Bay (Fig. 5). Противоположный пример - береговая линия Нидерландов. Chesapeake Bay занимает промежуточное положение. Причины этих различий до конца не установлены. Рис. 5. Средняя скорость усвоения азота фитопланктоном в отношении к растворенному неорганическому фосфору (DIP) в морских и пресных экосистемах (Howarth et al. 1988) Однако, в экосистемах тропиков и умеренных широт поглощение и запасание фосфора снижается в ростом эвтрофирования, по крайней мере до тех пор пока они станут гиперэвтрофированными, как побережье Нидерландов. В умеренных широтах это вызвано уменьшением окисленного железа и увеличением сульфида железа в донных отложениях, в тропических карбонатных системах происходит насыщение. В целом это делает фосфор более доступным в эвтрофированных системах по сравнению с олиготрофными системами. Не исключено, что донные отложения в озерных экосистемах в большей степени накапливают фосфор, чем донные отложения в эстуариях.

Фиксирующие атмосферный азот цианобактерии (имеют гетероцисты) могут играть значительную роль в регуляции баланса между азотом и фосфором. Показателен эксперимент, проведенный на экспериментальном озере в США. В течение нескольких лет в нем искусственно поддерживали отношение N: P 16: 1 в мольном выражении. В развивающемся фитопланктоне отсутствовали виды, способные фиксировать азот. Затем отношение было снижено и вслед а этим появились нитчатые форма цманобактерий, способные фиксировать азот (Flett et al. , 1980). Различная степень развития фиксирующих азот цианобактерий в эстуариях и пресных экосистемах, является одной из причин их различной реакции на лимитирование азотом. Причины этих различий до конца не установлены. В эстуариях, возможно ограничение связано с комплексом физико-химических и годрологических условий, а в озерах с недостатком молибдена. Недостаток молибдена, в свою очередь, может возникать при избытке сульфатов. Вопрос о соотношении азота и фосфора продолжает оставаться актуальным и в отношении исторических глобальных моделей биогеохимического круговорота. Рис. 6. Обобщенная модель поглощения молибдена (р моль Мо/ мг Хл час) как функция концентрации молибдена и сульфата. Заштрихованная область показывает сочетание двух факторов, характерное для большинства озер.

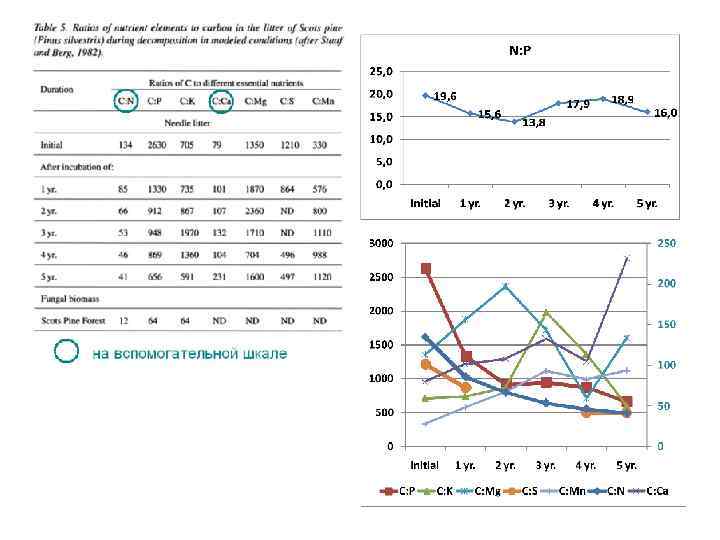
2. STOICHIOMETRIC ASPECTS OF NUTRIENT RECYCLING Рециклинг макроэлементов играет чрезвычайно важную роль в наземных и водных экосистемах. Скорость рециклинга зависит от многих биогеохимических особенностей экосистемы и климатических факторов. В этой ситуации важно определить стехиометрические соотношения сохраняющиеся в процессе рециклинга. НАЗЕМНЫЕ ЭКОСИСТЕМЫ Несмотря на возможность поступления питательных веществ из атмосферы или в процессе выветривания, основная масса питательных веществ в наземных экосистемах образуется в биогеохимических циклах из мертвых растительных и животных остатков и из почвы. Состав этой органики несомненно важен, так как от него зависит активность м. о. , принимающих участие в биогеохимических циклах. Растительный опад формируют целлюлоза, гемицеллюлоза, пектин и лигнин. Обычно отношение C: N в растительных остатках составляет величину 100 (см. выше табл. 3).
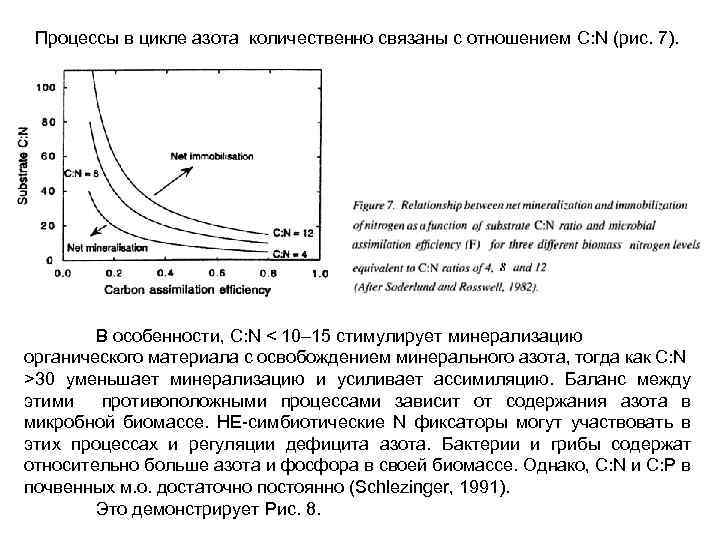
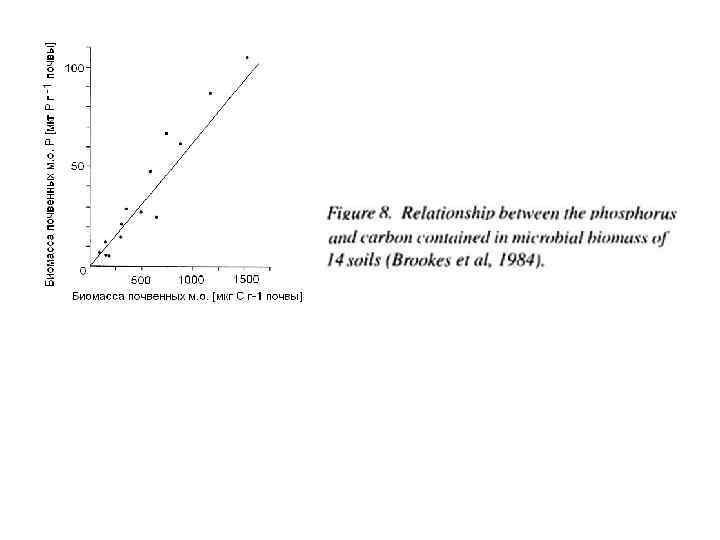
Процессы в цикле азота количественно связаны с отношением C: N (рис. 7). В особенности, C: N < 10– 15 стимулирует минерализацию органического материала с освобождением минерального азота, тогда как C: N >30 уменьшает минерализацию и усиливает ассимиляцию. Баланс между этими противоположными процессами зависит от содержания азота в микробной биомассе. НЕ-симбиотические N фиксаторы могут участвовать в этих процессах и регуляции дефицита азота. Бактерии и грибы содержат относительно больше азота и фосфора в своей биомассе. Однако, C: N и C: P в почвенных м. о. достаточно постоянно (Schlezinger, 1991). Это демонстрирует Рис. 8.

Stoichiometric aspects of nutrient recycling in aquatic ecosystems Фосфор играет важную роль в водных экосистемах (морских и пресных). Он содержится в неорганических и органических веществах. Минерализация фосфора происходит быстро. Фосфор быстро оказывается в составе донных отложений, но это не означает, что он также быстро из них освобождается. В окислительных условиях фосфаты образуют устойчивые комплексы с железом и освобождение фосфора возможно только при наступлении восстановительных (анаэробных) условий. Наличие м. о. в донных отложениях и в водной толще делает возможным рециклинг фосфора. В 80 -х годах прошлого века появились статьи, в которых обсуждались пищевые цепи в водных экосистемах при различных соотношениях углерода, азота и фосфора. Скорость рециклинга фосфора может зависеть от отношения С: Р в грэйзерах, таких как дафнии и копеподиды. Это, в свою очередь, может повлиять на видовой состав рыб. Соотношение С: Р в теле дафний оказалось стабильным при его варьировании в клетках фитопланктона.

БАКТЕРИАЛЬНАЯ ЭНЕРГЕТИКА Прогнозирование, которое должно связать биогеохимические процессы, происходящие с участием микроорганизмов, базируется на понимании энергетики диссипативных (катаболических) реакции. Необходимо обсудить два аспекта: 1 – кинетические ограничения химических реакций, 2 –основы химической термодинамики. Кинетическая ограничения означают, что процессы с большой энергией активации не могут происходить спонтанно. Теоретически можно предположить, что окисление N 2 кислородом способно обеспечить бактерии энергией, однако высокая энергия активации делает эту реакцию невыполнимой. Краткое рассмотрение бактериальной энергетики можно выполнить на основе равновесной термодинамики. Стандартная свободная энергия (ΔGo’) может быть определена на основе свободной энергии исходных соединений и продуктов: ΔGo’=ΣΔGo’(продукты) - ΣΔGo’(исходные вещества) Необходимые для определения величины можно найти в соответствующих таблицах.
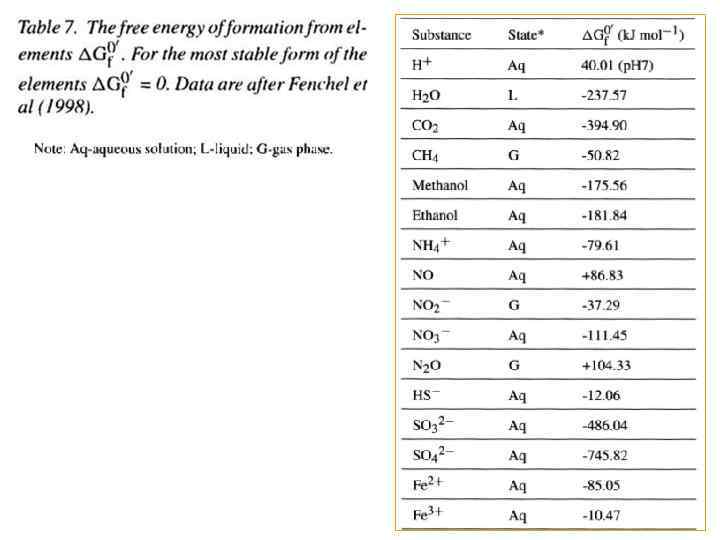

ПРИМЕРЫ РАСЧЕТА СВОБОДНОЙ ЭНЕРГИИ ОКИСЛЕНИЯ ВОДОРОДА Пример. На основе данных из таблицы 7 можно вычислить величину изменения свободной энергии (на 1 моль окисленного Н 2) в реакциях окисления водорода с различными акцепторами электронов. Для большинства стабильных форм элементов Go’ = 0. (определите самостоятельно изменение свободной энергии в реакции окисления водорода кислородом) Так как Н+ часто выступает в качестве реагента или продукта в биогеохимических реакциях в расчеты ΔGo’ обычно вносится поправка на его концентрацию 10 -7 М, что и выражается дополнительным «’» .
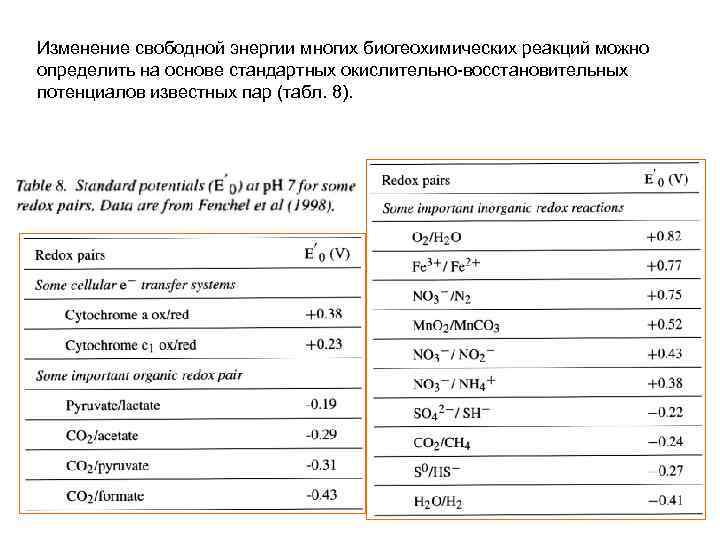
Изменение свободной энергии многих биогеохимических реакций можно определить на основе стандартных окислительно-восстановительных потенциалов известных пар (табл. 8).
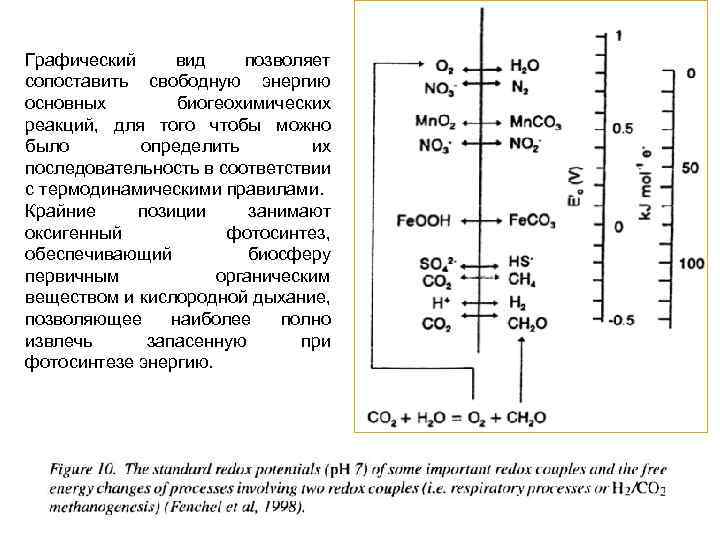
Графический вид позволяет сопоставить свободную энергию основных биогеохимических реакций, для того чтобы можно было определить их последовательность в соответствии с термодинамическими правилами. Крайние позиции занимают оксигенный фотосинтез, обеспечивающий биосферу первичным органическим веществом и кислородной дыхание, позволяющее наиболее полно извлечь запасенную при фотосинтезе энергию.

Часть энергии из органического вещества будет освобождена путем минерализации, но большинство пройдет через окислительно-восстановительные реакции дыхания с участием внешних акцепторов электронов. До тех пор пока кислород доступен, окислительное фосфорилирование будет обеспечивать энергией процесс минерализации. Когда кислород исчерпан, его место займет нитрат, затем марганец, нитрит и т. д. Эта термодинамическая последовательность окислительно-восстановительных реакций способна описать и объяснить временную и пространственную последовательность деградации органического вещества. Рисунок 10 показывает также, что при сокращении анаэробной минерализации, начнут действовать другие процессы с участием различных бактерий. В конце концов, может быть достигнуто новое равновесие на основе согласованного действия многих м. о. Мы можем также заключить, что знание этих термодинамических процессов позволяет понять количественные параметры взаимодействия различных биогеохимических циклов в наземных и водных экосистемах. Эти параметры могут быть также использованы при построении различных биогеохимических моделей.
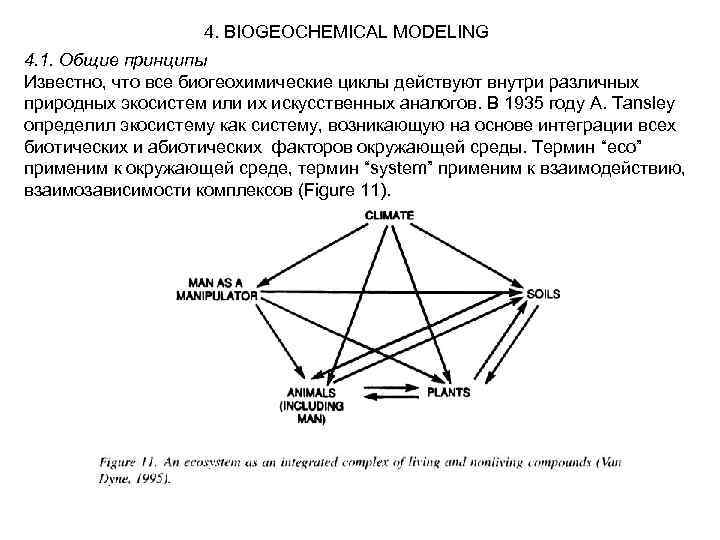
4. BIOGEOCHEMICAL MODELING 4. 1. Общие принципы Известно, что все биогеохимические циклы действуют внутри различных природных экосистем или их искусственных аналогов. В 1935 году A. Tansley определил экосистему как систему, возникающую на основе интеграции всех биотических и абиотических факторов окружающей среды. Термин “eco” применим к окружающей среде, термин “system” применим к взаимодействию, взаимозависимости комплексов (Figure 11).

На этой схеме каждый компонент, находится под влиянием других компонентов с возможным исключением микроклимата. Участие человека позволяет включить процесс трансформации экоситемы от ее естественного состояния к антропогенному. Можно видеть, что конкретная экосистема представляет собой единицу комплексного уровня организации. Она включает биотический и абиотический компоненты, которые объединены циклами миграции энергии и химических элементов, объединяемых понятием биогеохимического цикла. Итак биогеохимическая модель развивается как вариант общей экосистемной модели. Будем считать , что это модели после их создания станут мостом к созданию собственно биогеохимических моделей. Как и другие модели, экосистемная модель представляет собой математическую абстракцию реальной ситуации. В процессе их создания реальные ситуации абстрагируются до уровня математических моделей или математических систем (Figure 12). Математический анализ приобрел особую важность при описании поведения экосистем и их метаболизма, включая биогеохимические циклы в 40 -50 годы ХХ века после появления компьютеров. Последнее стало толчком в анализе сложных событий, происходящих в биосфере. Яркий пример – модель «Ядерной зимы» , разработанной Алексеевым.
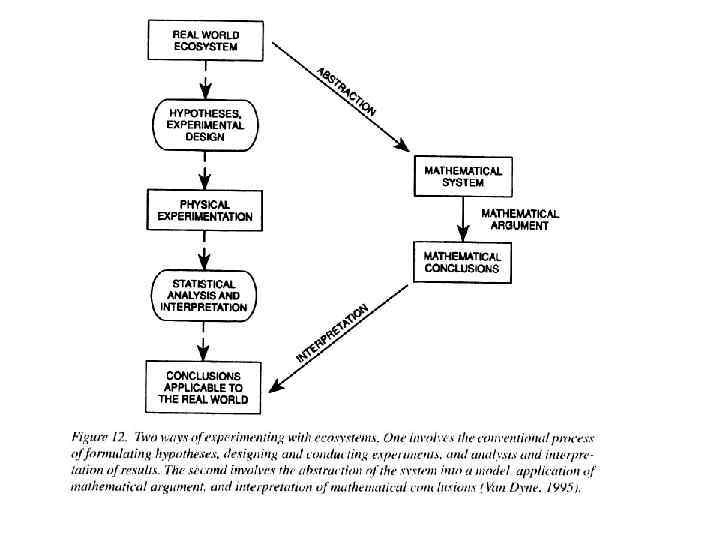

Теперь рассмотрим характеристики экосистемы на основе термодинамической теории. Структура термодинамической теории экосистем, которая развивает общие методы анализа применительно к экосистемам, показана на Figure 13. Ecosystems are open systems. Their boundaries are permeable, permitting energy and matter to cross them. Effects of environmental constraints and influences on the system play an important role in the regulation and maintenance of the system’s spatio-temporal as well as trophic organization and functioning. Indeed, ecosystems operate outside the realm of classical thermodynamics. Biological, chemical, and some physical processes inside of ecosystems are nonlinear. Stationary states of ecosystems are non-equilibrium states far from thermostatic equilibrium. In the course of time, entropy does not tend to a maximum value, or entropy production to a minimum. Entropy decreases when the order of organization and structure of the ecosystem increases. Entropy production is counterbalanced by export of entropy out of the system.
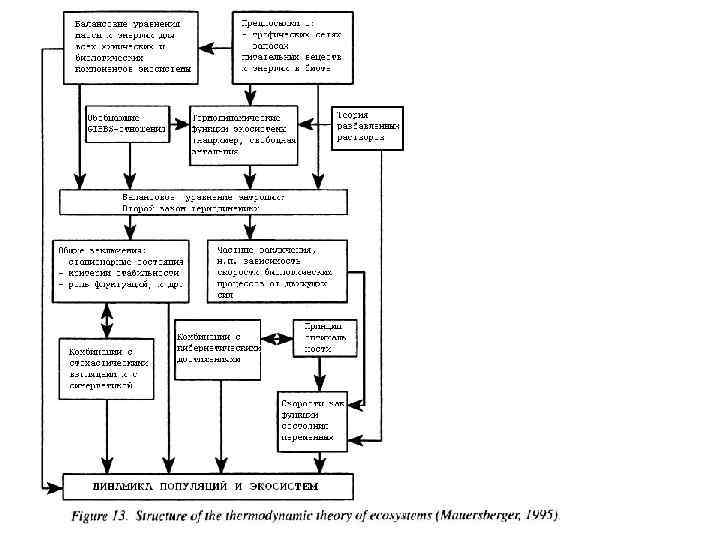

Экосистема является открытой системой. Она открыта для вещества и энергии. Факторы окружающей среды ограничивающие и влияющие на экосистему играют важную роль в регуляции и достижении ее пространственно-временной и трофической (функциональной) организации. В действительности, снаружи экосистема действует в рамках классической термодинамики, а внутри экосистема не линейна. Стационарное состояние системы не является равновесным, как этого требует классическая термодинамика. Энтропия складывается из баланса ее образования и экспорта из экосистемы. На основе формализма необратимой и неравновесной термодинамики экосистема как персистирующая биологическая структура, может быть представлена как конфигурация вещества и энергии, которые персистируют в состоянии далеком от равновесия за счет диссипации органического вещества, градиентов свободной энергии, образовании органического вещества из элементов окружающей среды. Таким образом, экосистема может быть представлена как функциональная биогеохимическая система (Figure 14), превращающая световую энергию солнца в энергию химических связей в процессе автотрофного фотосинтеза.
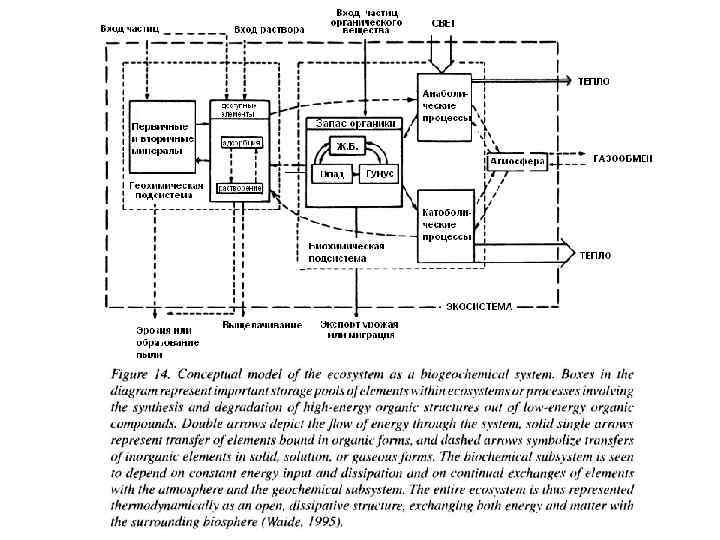

Химически связанная энергия представляет собой градиент свободной энергии между свободной энергией живых организмов свободной энергией окружающего геохимического матрикса. Органические структуры распадаются с освобождением энергии в виде тепла и структурных элементов, поступающих (возвращающихся) в геохимический матрикс в виде стабильных элементов с низким химическим потенциалом (Weide, 1995). Следовательно, экосистема может быть описана макроскопически как открытая диссипативная структура и как сохраняющаяся (персистированная) органическая конфигурация, сохраняющая неравновесное состояние с помощью сопряжения уровней диссипации энергии и биогеохимических циклов. Эти достаточно общие принципы используют при создании экосистемных и биогеохимических моделей. Представленные модели рассмотрены Jorgensen et al (1995).

4. 2 Модели. Математические модели глобальных экологических процессов (MMGEP). Цель этих биогеохимических моделей в объединении параметров иерархии биогеохимических, биоценотических и гидрологических процессов в биосфере. Они позволяют прогнозировать последствия антропогенных воздействий на эти процессы. MMGEP модели описывают взаимодействие атмосферы с сушей и океаном. В блоке, описывающем биогеохимические циклы, представлены углерод, азот, фосфор, сера и кислород; глобальный гидрологический баланс включает жидкую, газообразную и твердую фаы; почвенно-растительные образования разделены на 30 типов; фотосинтез в океанических экосистемах рассматривается как функция поверхности и глубины; включены демографические процессы и антропогенные изменения. Модели создаются в комплексе в глобальными климатическими моделями. MMGEP включает блоки для описания функции океанической пелагиали, арктических и шельфовых экосистем. Мировой океан разделен на четыре части: Arctic, Pacific, Atlantic и Indian. Пространственная структура определяется на основе доступных баз данных. Пространственная негомогенность характеризуется дискретностью, нанесенной на географическую координатную сетку с определенным шагом (km 2/pixel). MMGEP имеют порядка 50 управляющих функций, до 70 состояний и до 400 параметров. Модель проверяют более чем 30 ситуациях.

Мультиэлементные модели лимитирования (Multi-element limitation (MEL) model) Ответные реакции наземных экосистем на увеличение содержания диоксида углерода в атмосфере представляют в настоящее время наибольший интерес. Часть, происходящих дебатов, посвящены роли макроэлементов и незаменимых микроэлементов в лимитировании роста и накоплении биомассы наземными пастениями. Так как процесс вегетации должен обеспечиваться не просто элементами питания, но и их соотношением, можно ожидать, что лимитирование питательными элементами будет ключевым фактором, который будет сдерживать увеличение уровня продукции. С другой стороны, во многих областях Европы, Северной Америки и Азии (см. гл. 8 и 10) проблемой для окружающей среды является увеличение запасания азота. Увеличение СО 2 и N в атмосфере должно привести к негативным и позитивным эффектам: 1 - глобальному потеплению и повышению кислотности, 2 - дополнительному включению обоих элементов в биомассу растений.

Однако, ожидаемые ответы определяются способностью растений приспособиться к увеличению СО 2 путем увеличения биомассы и дополнительного получения элементов питания из почвы (Bastetter et al, 1997). В этом смысле, связывание (allocation) затрагивает множество процессов, действующих в различных временных шкалах, что может привести нарушению баланса питательных веществ во время вегетации. Это коснется и связей между биогеохимическими циклами в экосистеме и биохимии, морфологии, структуры сообщества и генетических адаптаций. Кроме ответов со стороны растений необходимо учитывать и изменение почвенного комплекса, в котором происходят процессы запасания и освобождения необходимых для жизни элементов и поддерживаются определенные физико-химические условия, важные для м. о. , растений и животных. Вывод: экспериментирования даже на локальном уровне требует громадных материальных затрат и может быть выполнено не в природе, а в модельной среде. Пример такой MEL модели показан на рисунке 15.
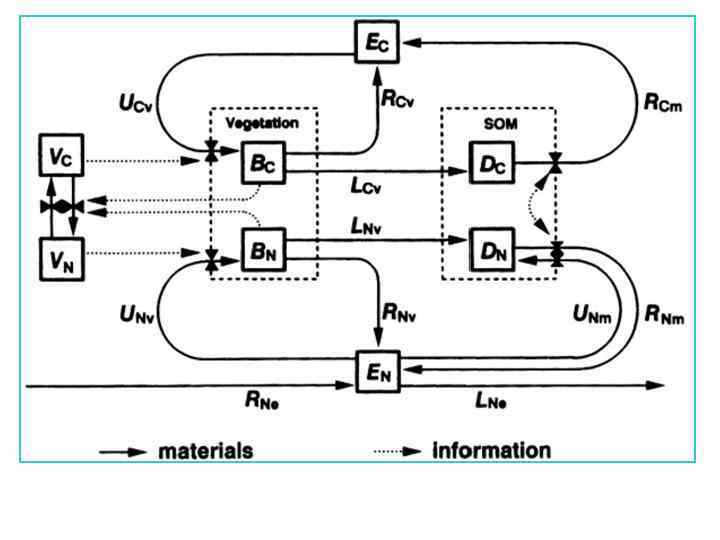

Рис. 15. MEL модель для С и N циклов в наземных экосистемах. Элементы перемещаются по вегетирующей массе , почвенному органическому веществу (SOM), неорганическим пулам и связаны через процессы вегетации и микробные процессы. Сплошные линии показывают потоки вещества, пунктирные линии – информации, которая описывает эти потоки. BС, BN – содержание углерода и азота в биомассе; DC, DN – содержание углерода и азота в почвенном детрите; ЕС, EN – поступление углерода и азота из атмосферы, LCv, LNv – потери с растительным опадом; LNe – выщелачивание неорганического азота; Rne – внешнее пополнение азота; RCm, RNm – общая (валовая) минерализация углерода и азота в почве; RCv, RNv – неорганическое освобождение углерода и азота из вегетирующей биомассы; UCm, UNm – валовое (gross) поглощение микробами углерода и азота; UCv, UNv – поглощение неорганического углерода и азота вегетирующей массой; VC, VN – поглотительная активность вегетирующей биомассы (Bastetter et al. , 1997).

Важной чертой MEL модели является «акклимация» вегетирующей массы к существующему балансу элементов питания, когда доступность ресурсов (VC, VN) изменяется. Под акклимацией понимают процессы, в результате которых происходит компенсаторное перераспределение активности поглощения адекватно изменению соотношения элементов в вегетирующей биомассе (Bastetter et al, 1997). Эти процессы включают не только физиологические и морфологические реакции отдельных растений, например, изменение концентрации ферментов в тканях, отношение корень: побег, но и генетические адаптации на уровне популяции и конкурентное замещение новыми видами с более благоприятными для поглощения характеристиками. Этот аспект наиболее важен определения временной шкалы ожидаемого ответа. Параметры для построения этой модели были определены на основе изучения 350 -ти летнего леса Hubbard Brook Experimental Forest, New Hampshire, USA.

В результате применения MEL модели стал понятен механизм, с помощью которого экосистема способна сокращать C при увеличении содержания СО 2 и N в атмосфере. Для перспективы сопряжения биогеохимических циклов углерода и азота, необходимые ограничения могут быть достигнуты только в комбинации с одним или более изменением в экосистеме: (1) Увеличение C: N отношения в компонентах экосистем; 2) Перераспределение N из компонентов с низким отношением C: N (например, почв) в компоненты с высоким отношением C: N (например, в древесину; Или (3) увеличение общего экосистемного азота. Применение модели показало, что потенциал лесных экосистем в резервировании С значительно увеличивается, если цикл N ускоряется за счет усиления запасания N или усиления его фиксации. Предварительный модельный анализ показал также, что парниковый эффект способен увеличить резервирование С леса в условиях лимитирования по N. Механизм запасания – это «чистое» движение азота из почвы (low C: N) в вегетирующую массу (high C: N). Увеличение температуры стимулирует одновременно освобождение и минерализацию азота из органического пула, увеличение скоростей освобождения в атмосферу. Минерализация приводит к усилению плодородия почвы и увеличению роста растений. Манипуляции с моделью Hubbard Brook ecosystem (предположением, что N цикл открыт) показали, что консервация углерода может увеличиться в два раза, когда концентрация СО 2 увеличится в 2 раза и температура возрастет на 5 °C (Bastetter et al, 1997).

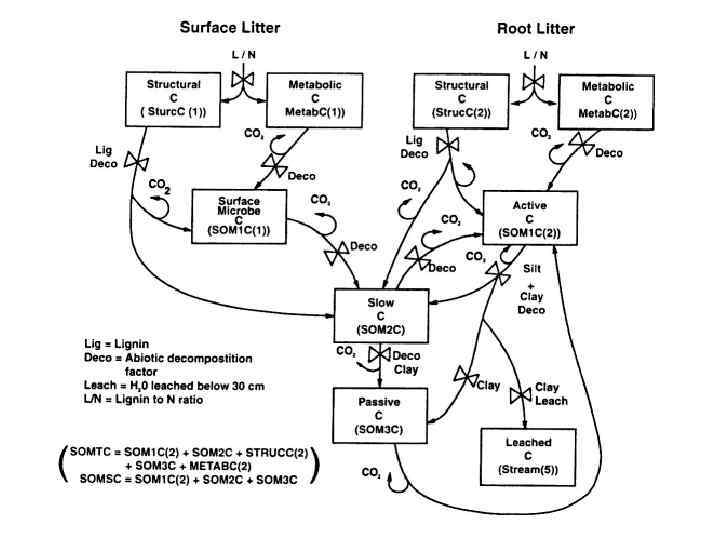
Century model (Soil Organic Matter Model) The Century биогеохимическая модель разработана для изучения влияния климата и движения атмосферы на почвенное органическое вещество и поведение экосистемы. Century представляет собой общую модель взаимодействия почвы и растения, которая позволяет получить основные представления о процессах ассимиляции углерода и его обороте (Figure 16). Century воспроизводит динамику углерода и азота в различных системах почва-растение. Продукция трав – функция температуры почвы и доступности воды, ограничения элементами питания и ценотическим эффектом «self-shading factor» . Модель включает возможность пожара и выедания «grazing» (Holland et al, 1992, Parton et al, 1993). К этой основной модели может быть присоединена субмодель, описывающая потоки органического вещества (азота и углерода) через различные органические и неорганические пулы почвы на коротких временных интервалах (месяц).

Macrophyte ecosystem model Модель предложена Kemp et al (1995). Концептуальная диаграмма модели показана на Figure 17. Модель применима к водной экосистеме, в которой фитопланктон, эпифлора, макрофиты и бентосны е микроводоросли конкурируют за элементы питания и свет. Конкуренция за свет выражается в прямом затенении, тогда как конкуренция за питание включает два независимых источника азота (вода и седименты), которые периодически сокращаются. Только сосудистые растения с их корневой системой имеют прямой доступ к питательным элементам. Модель описывает поведение экосистемы при различных физических и химических условиях среды: взаимодействия с эстуариями, эвтрофировании и т. п.
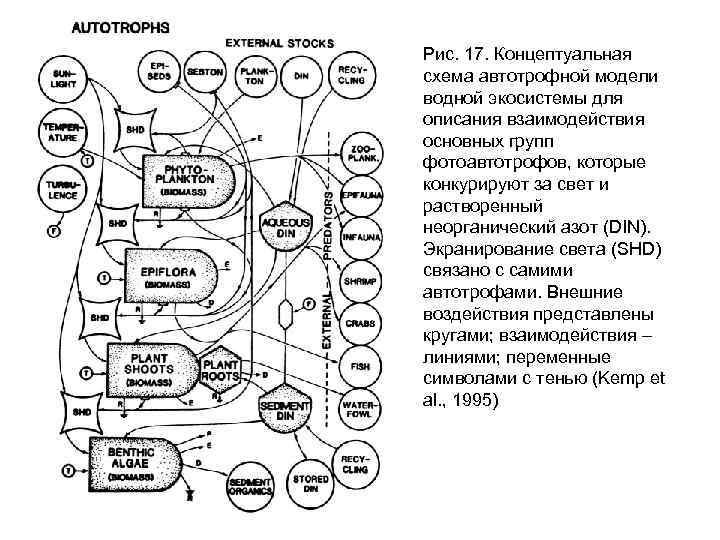
Рис. 17. Концептуальная схема автотрофной модели водной экосистемы для описания взаимодействия основных групп фотоавтотрофов, которые конкурируют за свет и растворенный неорганический азот (DIN). Экранирование света (SHD) связано с самими автотрофами. Внешние воздействия представлены кругами; взаимодействия – линиями; переменные символами с тенью (Kemp et al. , 1995)

Knowledge-based large scale aquatic ecosystem restoration model Цель этой биогеохимической модели заключается в оценке и выборе оптимального решения из некоторого числа существующих возможностей. Проблема выбора является чрезвычайно трудной. Необходимо получить доступ к влиянию различных факторов в условиях их взаимодействия и диффузности. Диффузность становится неотъемлемым свойством экосистемы. Поэтому возможно применение теории диффузности для описания свойств природного объекта и для применения соответствующих разделов и правил fuzzy математики (Frolova, 1999). Методология предполагает определенную последовательность в решении задач: предпринять первые шаги, направленные на защиту окружающей среды; создание группы функций измерений в отношении к различным параметрам в их условиях; создание функций параметров; измерение состояния окружающей среды; выполнение математических операций; получение соответствующих правил сокращающие рассеяние. Применение этой модели к восстановлению водной среды может потребовать следующих шагов: создание базы знаний об изучаемом объекте; сбор данных в различных частях объекта; ввод данных в экспертную систему; исключение выпадающих данных (ошибка 20– 40%); выполнение расчетов с помощью экспертной системы; анализ результата; использование рекомендаций экспертной системы для восстановления природного объекта. На практике экспертная система может применяться как анализирующая система и способна оптимизировать те или иные технологии.

Application of GIS techniques for calculation and mapping of critical loads Critical loads of pollutants at an ecosystem can be calculated on the basis of the Steady-State Mass Balance (SSMB) biogeochemical model (see Chapter 10). All equations of this model include a quantitative estimation of the greatest possible number of parameters describing pollutant circulation in ecosystems. However, direct use of this method is possible only for the areas in which it is possible directly to measure with necessary accuracy and spatial resolution all parameters, which are included in the equations. It is correct for the West European countries, which have rather small areas and a well advanced network of stations making an estimation of pollution of an environment by selection of tests with necessary accuracy and resolution. But there are regions for which it is impossible to determine with sufficient accuracy for accounting the inputting parameters of the SSMB equations. One such region is Russia. The absence of a regular network of stations on ecological monitoring is characteristic for vast Russian areas. Therefore it is necessary to apply the methods of the definition of inputting parameters of the SSMB model equations through indirect parameters.

One such method suggested by Bashkin et al. (1995), allows the researchers to determine critical loads through the internal ecosystem characteristics and their derivative parameters. The method is based on the suggestion that it is enough to calculate critical loads for small well investigated ecosystems (model systems) and then to distribute results of accounts to all mapping areas. All inputting parameters become dependent on internal ecosystem properties (soil type, soil texture, vegetation type, average annual temperature, river-network density etc. ). For realization of calculations, it is necessary to use various sources of a digital cartographic material of different manufacturers and different quality. Just this fact creates certain difficulties, which is necessary to take into account with GIS design. Accordingly the special GIS technology has been developed to run the calculations (Tankanag, 1999). Using this geoinformation system, mapping and quantitative estimation of critical loads of sulfur and nitrogen for a European part of Russia was carried out (see Chapter 10). As properties and thematic databases determining a situation of ecosystems in space of attributes, the following properties were taken: Soil types— FAO–UNESCO SOIL MAP OF THE WORLD, Lat/Long Temperature and Runoff— NASA, Lat/Long Land use—RIVM, EMEP Land cover and Digital Elevation Model— US Geological Survey, Deposition—Meteorological Synthesizing Center-East and Meteorological Synthesizing Center-West, EMEP 50 As a cartographic basis the data World Data Bank-2, 4 (US Department of State, CIA, 1989 -1990) were used. (градусградус; 50 км 2 обычное разрешение)
interaction.ppt