ДВС-синдром в акушерстве.ppt
- Количество слайдов: 84
 Интенсивная терапия ДВСсиндрома при критических состояниях в акушерскогинекологической практике Ткаченко Р. А. Национальный медицинский университет им. А. Богомольца
Интенсивная терапия ДВСсиндрома при критических состояниях в акушерскогинекологической практике Ткаченко Р. А. Национальный медицинский университет им. А. Богомольца
 n «Нить фибрина может оборвать нить жизни» Любарш
n «Нить фибрина может оборвать нить жизни» Любарш
 n Диссеминированное внутрисосудистое свертывание крови - сложный патологический синдром, в основе которого лежит активация сосудисто-тромбоцитарного гемостаза или коагуляционного гемостаза (внешнего или внутреннего), при котором во всем организме повышается протромбиназная активность, ведущая к образованию достаточно большого количества тромбина, фибриногена и образования сгустковтромбов в сосудистом русле.
n Диссеминированное внутрисосудистое свертывание крови - сложный патологический синдром, в основе которого лежит активация сосудисто-тромбоцитарного гемостаза или коагуляционного гемостаза (внешнего или внутреннего), при котором во всем организме повышается протромбиназная активность, ведущая к образованию достаточно большого количества тромбина, фибриногена и образования сгустковтромбов в сосудистом русле.
 Результатами этих двух процессов являются: 1) массивное потребление факторов свертывания крови; 2)чрезмерная активация фибринолиза. Следствием этого, в свою очередь, является частое возникновение кровотечений различной локализации. n
Результатами этих двух процессов являются: 1) массивное потребление факторов свертывания крови; 2)чрезмерная активация фибринолиза. Следствием этого, в свою очередь, является частое возникновение кровотечений различной локализации. n
 Летальность показатели летальности при ДВС-синдроме колеблются в пределах 30 - 76%, составляя в среднем около 50% Баркаган З. С. (1988); Spero J. A et al. , (1990).
Летальность показатели летальности при ДВС-синдроме колеблются в пределах 30 - 76%, составляя в среднем около 50% Баркаган З. С. (1988); Spero J. A et al. , (1990).
 Основные этиологические факторы, способствующие развитию ДВС-синдрома n n n n тяжелые формы позднего токсикоза беременных; преждевременная отслойка нормально расположенной плаценты; эмболия околоплодными водами; замершая беременность; шок различного генеза (геморрагический, септический, анафилактический); аллергические реакции; длительный прием контрацептивов; массивные переливания крови;
Основные этиологические факторы, способствующие развитию ДВС-синдрома n n n n тяжелые формы позднего токсикоза беременных; преждевременная отслойка нормально расположенной плаценты; эмболия околоплодными водами; замершая беременность; шок различного генеза (геморрагический, септический, анафилактический); аллергические реакции; длительный прием контрацептивов; массивные переливания крови;
 Основные этиологические факторы, способствующие развитию ДВС-синдрома n n n n конфликт матери и плода по системам АВ 0 и Rh; длительные и травматичные операции; сепсис; экстрагенитальная патология (заболевания сердечнососудистой системы, почек, печени, злокачественные новообразования); гемотрансфузионные осложнения (переливание несовместимой крови); анте- и интранатальная гибель плода; гнойно-воспалительные заболевания (метроэндометрит, септический аборт, хориоамнионит, мастит, перитонит); ятрогенные воздействия (массивная инфузионнотрансфузионная терапия (коагулопатия разведения), введение большого количества декстранов, бесконтрольное применение антикоагулянтов).
Основные этиологические факторы, способствующие развитию ДВС-синдрома n n n n конфликт матери и плода по системам АВ 0 и Rh; длительные и травматичные операции; сепсис; экстрагенитальная патология (заболевания сердечнососудистой системы, почек, печени, злокачественные новообразования); гемотрансфузионные осложнения (переливание несовместимой крови); анте- и интранатальная гибель плода; гнойно-воспалительные заболевания (метроэндометрит, септический аборт, хориоамнионит, мастит, перитонит); ятрогенные воздействия (массивная инфузионнотрансфузионная терапия (коагулопатия разведения), введение большого количества декстранов, бесконтрольное применение антикоагулянтов).
 Тромбогеморрагические осложнения являются постоянным спутником любой акушерско–гинекологической патологии и во многом определяют течение и исход беременности и родов. А. П. Колесниченко, Г. В. Грицан (2001) n
Тромбогеморрагические осложнения являются постоянным спутником любой акушерско–гинекологической патологии и во многом определяют течение и исход беременности и родов. А. П. Колесниченко, Г. В. Грицан (2001) n
 Высокая частота гемокоагуляционных расстройств в акушерской практике связана, прежде всего, с адаптационными изменениями в свертывающей системе, развивающимися у беременной и достигающего свого максимума к концу ІІІ триместра беременности. По данным А. П. Колесниченко и Г. В. Грицан (2001) в III триместре при физиологической беременности отмечается повышение суммарной активности факторов свертывания крови, составляющих внутренний путь активации гемостаза – VIII, IX, X, XII и как проявление этого укорочение хронометрических тестов (АЧТВ, АВР).
Высокая частота гемокоагуляционных расстройств в акушерской практике связана, прежде всего, с адаптационными изменениями в свертывающей системе, развивающимися у беременной и достигающего свого максимума к концу ІІІ триместра беременности. По данным А. П. Колесниченко и Г. В. Грицан (2001) в III триместре при физиологической беременности отмечается повышение суммарной активности факторов свертывания крови, составляющих внутренний путь активации гемостаза – VIII, IX, X, XII и как проявление этого укорочение хронометрических тестов (АЧТВ, АВР).
 n Уровень фибриногена в конце 3 триместра увеличивается на 20 -30% (в сравнении со средненормативными значениями), а возрастание количества факторов, составляющих внешний путь активации свертывания крови - незначительное, о чем свидетельствуют данные протромбинового комплекса (ПТИ в среднем 100– 110%).
n Уровень фибриногена в конце 3 триместра увеличивается на 20 -30% (в сравнении со средненормативными значениями), а возрастание количества факторов, составляющих внешний путь активации свертывания крови - незначительное, о чем свидетельствуют данные протромбинового комплекса (ПТИ в среднем 100– 110%).
 n Уровень растворимых фибрин-мономерных комплексов перед родами повышен в среднем в 1, 5 раза в сравнении с нормой, а в первые сутки послеродового периода их количество может увеличиваться в среднем на 50% от исходного. Такой уровень РФМК сохраняется в течение 3– 4 суток и имеет тенденцию к снижению лишь на 6– 7 сутки послеродового периода.
n Уровень растворимых фибрин-мономерных комплексов перед родами повышен в среднем в 1, 5 раза в сравнении с нормой, а в первые сутки послеродового периода их количество может увеличиваться в среднем на 50% от исходного. Такой уровень РФМК сохраняется в течение 3– 4 суток и имеет тенденцию к снижению лишь на 6– 7 сутки послеродового периода.
 n n В сосудисто–тромбоцитарном звене гемостаза отмечается повышение агрегационной способности тромбоцитов на 20 – 30%, при нормальном их количестве. Из–за высокой скорости обмена фибриногена в организме беременных, может наблюдаться небольшое увеличение ранних ПДФ по данным клампинг-теста, при отсутствии Д–димеров (поздних продуктов деградации фибрина) на фоне нормальной концентрации плазминогена. Данные изменения расцениваются как умеренная активация фибринолиза.
n n В сосудисто–тромбоцитарном звене гемостаза отмечается повышение агрегационной способности тромбоцитов на 20 – 30%, при нормальном их количестве. Из–за высокой скорости обмена фибриногена в организме беременных, может наблюдаться небольшое увеличение ранних ПДФ по данным клампинг-теста, при отсутствии Д–димеров (поздних продуктов деградации фибрина) на фоне нормальной концентрации плазминогена. Данные изменения расцениваются как умеренная активация фибринолиза.
 n ДВС-синдром неспецифичен и универсален, поэтому в настоящее время его рассматривают как общебиологический процесс, предназначенный природой как для остановки кровотечения при нарушении целостности сосуда, так и для отграничения пораженных тканей от всего организма.
n ДВС-синдром неспецифичен и универсален, поэтому в настоящее время его рассматривают как общебиологический процесс, предназначенный природой как для остановки кровотечения при нарушении целостности сосуда, так и для отграничения пораженных тканей от всего организма.
 Уменьшение кровопотери благодаря гиперкоагуляции в месте кровоточащего участка имеет жизнеспасающий потенциал при лечении травмы и во время тяжелых хирургических вмешательств
Уменьшение кровопотери благодаря гиперкоагуляции в месте кровоточащего участка имеет жизнеспасающий потенциал при лечении травмы и во время тяжелых хирургических вмешательств
 СИСТЕМА ГЕМОСТАЗА. Биологическая система, обеспечивающая, с одной стороны, сохранение жидкого состояния крови, а с другой - предупреждение и остановку кровотечений путем поддержания структурной целостности стенок кровеносных сосудов и достаточно быстрого тромбирования последних при повреждениях, называется системой гемостаза.
СИСТЕМА ГЕМОСТАЗА. Биологическая система, обеспечивающая, с одной стороны, сохранение жидкого состояния крови, а с другой - предупреждение и остановку кровотечений путем поддержания структурной целостности стенок кровеносных сосудов и достаточно быстрого тромбирования последних при повреждениях, называется системой гемостаза.
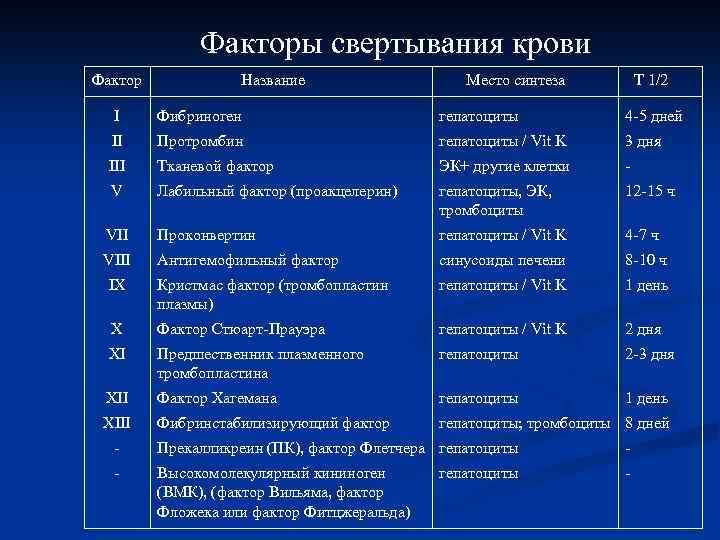 Факторы свертывания крови Фактор Название Место синтеза T 1/2 I Фибриноген гепатоциты 4 -5 дней II Протромбин гепатоциты / Vit K 3 дня III Тканевой фактор ЭК+ другие клетки - V Лабильный фактор (проакцелерин) гепатоциты, ЭК, тромбоциты 12 -15 ч VII Проконвертин гепатоциты / Vit K 4 -7 ч VIII Антигемофильный фактор синусоиды печени 8 -10 ч IX Кристмас фактор (тромбопластин плазмы) гепатоциты / Vit K 1 день X Фактор Стюарт-Прауэра гепатоциты / Vit K 2 дня XI Предшественник плазменного тромбопластина гепатоциты 2 -3 дня XII Фактор Хагемана гепатоциты 1 день XIII Фибринстабилизирующий фактор гепатоциты; тромбоциты 8 дней - Прекалликреин (ПК), фактор Флетчера гепатоциты - - Высокомолекулярный кининоген (ВМК), (фактор Вильяма, фактор Фложека или фактор Фитцжеральда) - гепатоциты
Факторы свертывания крови Фактор Название Место синтеза T 1/2 I Фибриноген гепатоциты 4 -5 дней II Протромбин гепатоциты / Vit K 3 дня III Тканевой фактор ЭК+ другие клетки - V Лабильный фактор (проакцелерин) гепатоциты, ЭК, тромбоциты 12 -15 ч VII Проконвертин гепатоциты / Vit K 4 -7 ч VIII Антигемофильный фактор синусоиды печени 8 -10 ч IX Кристмас фактор (тромбопластин плазмы) гепатоциты / Vit K 1 день X Фактор Стюарт-Прауэра гепатоциты / Vit K 2 дня XI Предшественник плазменного тромбопластина гепатоциты 2 -3 дня XII Фактор Хагемана гепатоциты 1 день XIII Фибринстабилизирующий фактор гепатоциты; тромбоциты 8 дней - Прекалликреин (ПК), фактор Флетчера гепатоциты - - Высокомолекулярный кининоген (ВМК), (фактор Вильяма, фактор Фложека или фактор Фитцжеральда) - гепатоциты
 СИСТЕМА ГЕМОСТАЗА. Активация свертывания крови in vivo модулируется рядом регуляторных механизмов, которые ограничивают реакцию местом повреждения и предотвращают возникновение массивного внутрисосудистого тромбоза.
СИСТЕМА ГЕМОСТАЗА. Активация свертывания крови in vivo модулируется рядом регуляторных механизмов, которые ограничивают реакцию местом повреждения и предотвращают возникновение массивного внутрисосудистого тромбоза.
 СИСТЕМА ГЕМОСТАЗА К регуляторным факторам относят: кровоток и гемодилюцию; n клиренс, осуществляемый печенью и РЭС; n протеолитическое действие тромбина (механизм обратной связи); n ингибиторы сериновых протеаз n
СИСТЕМА ГЕМОСТАЗА К регуляторным факторам относят: кровоток и гемодилюцию; n клиренс, осуществляемый печенью и РЭС; n протеолитическое действие тромбина (механизм обратной связи); n ингибиторы сериновых протеаз n
 Главными ингибиторами факторов свертывания являются: антитромбин III (AT-III), гепариновый кофактор II (ГК II), протеин С (ПС), протеин S (ПS), ингибитор пути тканевого фактора (ИПТФ), протеаза нексин-1 (ПН-1), С 1 ингибитор, α 1 -антитрипсин (α 1 -АТ) и α 2 -макроглобулин (α 2 -М). Ингибиторы, за исключением ИПТФ и α 2 -М, называются серпины, ИПТФ - относятся к группе апротеинов и называются кунины.
Главными ингибиторами факторов свертывания являются: антитромбин III (AT-III), гепариновый кофактор II (ГК II), протеин С (ПС), протеин S (ПS), ингибитор пути тканевого фактора (ИПТФ), протеаза нексин-1 (ПН-1), С 1 ингибитор, α 1 -антитрипсин (α 1 -АТ) и α 2 -макроглобулин (α 2 -М). Ингибиторы, за исключением ИПТФ и α 2 -М, называются серпины, ИПТФ - относятся к группе апротеинов и называются кунины.
 Нормальный эндотелий действует как мощная антикоагулянтная поверхность, которая не активирует белки свертывания крови и не привлекает к себе клеточные компоненты крови. «Гемостаз и тромбоз» , 2001 г.
Нормальный эндотелий действует как мощная антикоагулянтная поверхность, которая не активирует белки свертывания крови и не привлекает к себе клеточные компоненты крови. «Гемостаз и тромбоз» , 2001 г.
 После травмы или стимуляции эндотелий трансформируется в мощную прокоагулянтную поверхность. Это происходит за счет синтеза выделения или привлечения многих прокоагулянтных веществ: тканевой фактор (ТФ), фактор Виллебранда (ФВ), фактор V, ингибиторы активатора плазминогена (ИАП-1 и ИАП 2), интерлейкин-1 (ИЛ-1), фактор некроза ткани (ФНТ), эндотелин. «Гемостаз и тромбоз» , 2001 г.
После травмы или стимуляции эндотелий трансформируется в мощную прокоагулянтную поверхность. Это происходит за счет синтеза выделения или привлечения многих прокоагулянтных веществ: тканевой фактор (ТФ), фактор Виллебранда (ФВ), фактор V, ингибиторы активатора плазминогена (ИАП-1 и ИАП 2), интерлейкин-1 (ИЛ-1), фактор некроза ткани (ФНТ), эндотелин. «Гемостаз и тромбоз» , 2001 г.
 Продукты эндотелиальной клетки - Базальная мембрана - Коллаген (III, IV) - Микрофибриллы - Эластин - Ламилин - Витронектин - Ингибиторы протеаз - Фибронектин - Мукополисахариды - ФВ - Протеазы Продукты эндотелиальной клетки, секретируемые в субэндотелиальную зону и в просвет сосуда.
Продукты эндотелиальной клетки - Базальная мембрана - Коллаген (III, IV) - Микрофибриллы - Эластин - Ламилин - Витронектин - Ингибиторы протеаз - Фибронектин - Мукополисахариды - ФВ - Протеазы Продукты эндотелиальной клетки, секретируемые в субэндотелиальную зону и в просвет сосуда.
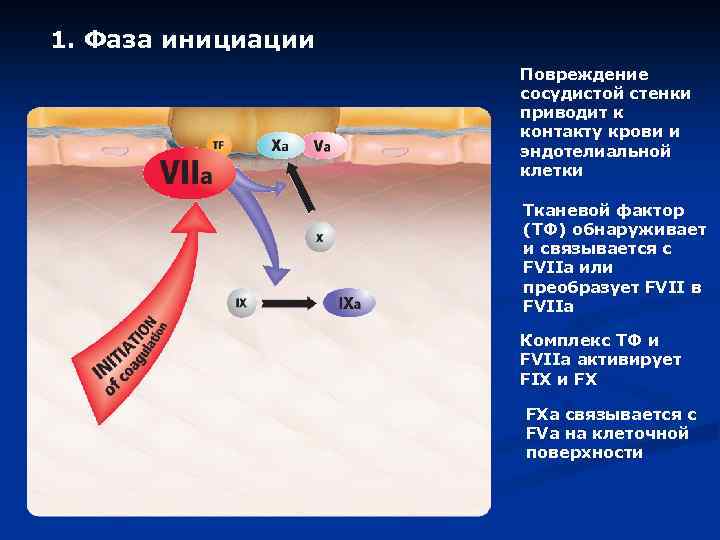 1. Фаза инициации Повреждение сосудистой стенки приводит к контакту крови и эндотелиальной клетки Тканевой фактор (ТФ) обнаруживает и связывается с FVIIa или преобразует FVII в FVIIa Комплекс ТФ и FVIIa активирует FIX и FX FXa связывается с FVa на клеточной поверхности
1. Фаза инициации Повреждение сосудистой стенки приводит к контакту крови и эндотелиальной клетки Тканевой фактор (ТФ) обнаруживает и связывается с FVIIa или преобразует FVII в FVIIa Комплекс ТФ и FVIIa активирует FIX и FX FXa связывается с FVa на клеточной поверхности
 Гемостаз: повреждение сосуда
Гемостаз: повреждение сосуда
 Патофизиология гемостаза На предыдущем слайде видна центральная роль ТФ в гемостазе при повреждении сосуда. В норме ТФ не циркулирует в крови, а связан с фибробластами и гладкомышечными клетками, при повреждении проникает в эндотелий, соединяется с факторами свертывания плазмы, что является начальным этапом образования фибрина.
Патофизиология гемостаза На предыдущем слайде видна центральная роль ТФ в гемостазе при повреждении сосуда. В норме ТФ не циркулирует в крови, а связан с фибробластами и гладкомышечными клетками, при повреждении проникает в эндотелий, соединяется с факторами свертывания плазмы, что является начальным этапом образования фибрина.
 Патофизиология гемостаза ТФ является мембрано-связанным гликопротеином, который продуцируют субэндотелиальные клетки в ответ на повреждение, т. е является также сигнальным рецептором. Недавно полученные данные свидетельствуют, что рожденный кровью тканевой фактор играет важную прокоагулянтную функцию при сепсисе, атеросклерозе и раке, а также выполняет другие негемостатические функции, типа иммунной функции и влияющей на метастазирование. (Price GC, Thompson SA, Kam PC. Anaesthesia. 2004; 59(5): 483 -92).
Патофизиология гемостаза ТФ является мембрано-связанным гликопротеином, который продуцируют субэндотелиальные клетки в ответ на повреждение, т. е является также сигнальным рецептором. Недавно полученные данные свидетельствуют, что рожденный кровью тканевой фактор играет важную прокоагулянтную функцию при сепсисе, атеросклерозе и раке, а также выполняет другие негемостатические функции, типа иммунной функции и влияющей на метастазирование. (Price GC, Thompson SA, Kam PC. Anaesthesia. 2004; 59(5): 483 -92).
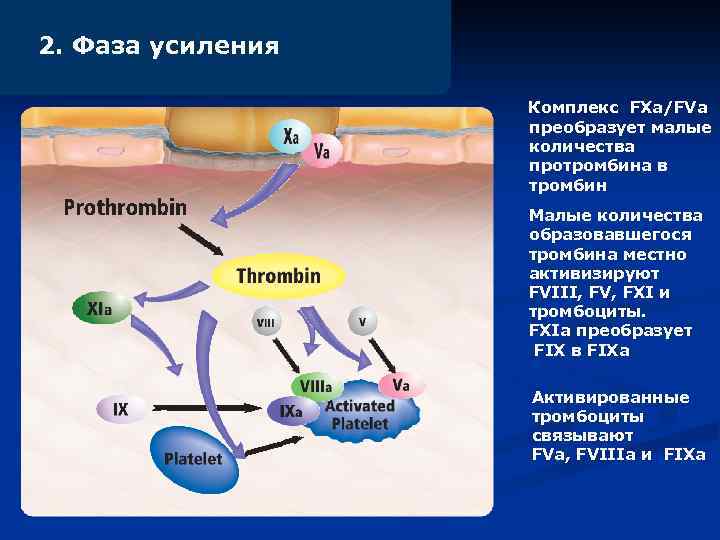 2. Фаза усиления Комплекс FXa/FVa преобразует малые количества протромбина в тромбин Малые количества образовавшегося тромбина местно активизируют FVIII, FV, FXI и тромбоциты. FXIa преобразует FIX в FIXa Активированные тромбоциты связывают FVa, FVIIIa и FIXa
2. Фаза усиления Комплекс FXa/FVa преобразует малые количества протромбина в тромбин Малые количества образовавшегося тромбина местно активизируют FVIII, FV, FXI и тромбоциты. FXIa преобразует FIX в FIXa Активированные тромбоциты связывают FVa, FVIIIa и FIXa
 2. Гемостаз: образование тромбоцитарного тромба Тромбоциты (показаны желтым цветом) «прилипают» к выделяющемуся коллагену в зоне повреждения и образуют тромбоцитарный тромб.
2. Гемостаз: образование тромбоцитарного тромба Тромбоциты (показаны желтым цветом) «прилипают» к выделяющемуся коллагену в зоне повреждения и образуют тромбоцитарный тромб.
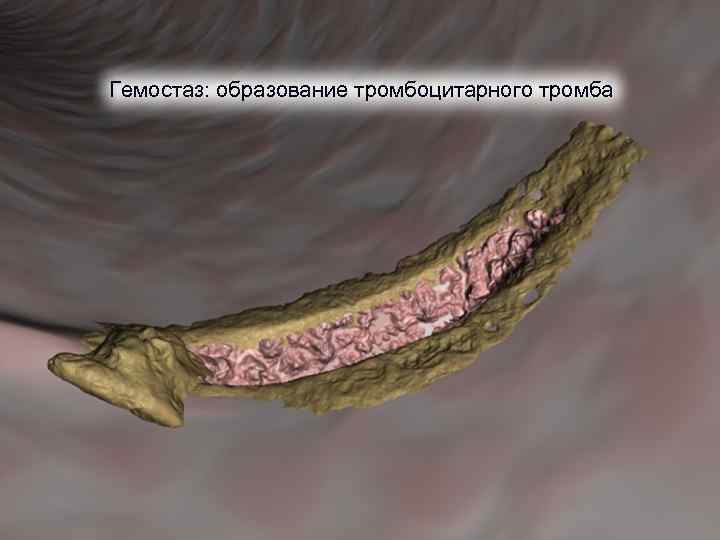 Гемостаз: образование тромбоцитарного тромба
Гемостаз: образование тромбоцитарного тромба
 3. Фаза распространения 3. Propagation phase Комплекс FVIIIa/FIXa активирует FX на поверхности активированных тромбоцитов FXa совместно с FVa преобразует большие количества протромбина в тромбин с образова нием «тромбинового импульса» «Тромбиновый импульс» приводит к образованию стабильного фибринового сгустка
3. Фаза распространения 3. Propagation phase Комплекс FVIIIa/FIXa активирует FX на поверхности активированных тромбоцитов FXa совместно с FVa преобразует большие количества протромбина в тромбин с образова нием «тромбинового импульса» «Тромбиновый импульс» приводит к образованию стабильного фибринового сгустка
 3. Гемостаз: образование тромбина и формирование тромба Механизм тромбообразования включает каскад протеолитических реакций, в которых неактивные ферменты активируют друга. В результате каждой реакции образуется активный компонент фермента, способный активировать последующие факторы. Центральное место занимает реакция расщепления протромбина с образованием тромбина (освещенные голубые образования на рисунке) - фактора, который не только усиливает формирование тромба за счет активации образования фибрина, но также резко увеличивает свой собственный синтез по механизму положительной обратной связи, активируя факторы V и VIII.
3. Гемостаз: образование тромбина и формирование тромба Механизм тромбообразования включает каскад протеолитических реакций, в которых неактивные ферменты активируют друга. В результате каждой реакции образуется активный компонент фермента, способный активировать последующие факторы. Центральное место занимает реакция расщепления протромбина с образованием тромбина (освещенные голубые образования на рисунке) - фактора, который не только усиливает формирование тромба за счет активации образования фибрина, но также резко увеличивает свой собственный синтез по механизму положительной обратной связи, активируя факторы V и VIII.
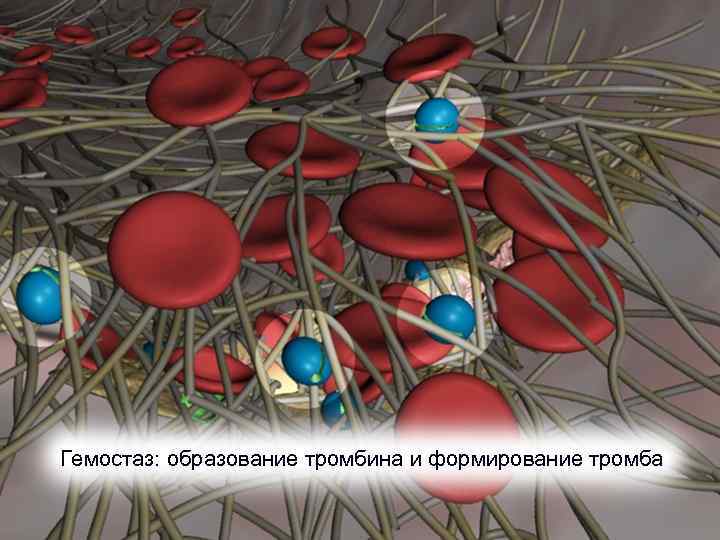 Гемостаз: образование тромбина и формирование тромба
Гемостаз: образование тромбина и формирование тромба
 4. Электронная микрограмма тромба Тромбин катализирует образование фибрина и также играет ключевую роль в стабилизации тромба, активируя фактор XIII (фибринстабилизирующий фактор).
4. Электронная микрограмма тромба Тромбин катализирует образование фибрина и также играет ключевую роль в стабилизации тромба, активируя фактор XIII (фибринстабилизирующий фактор).
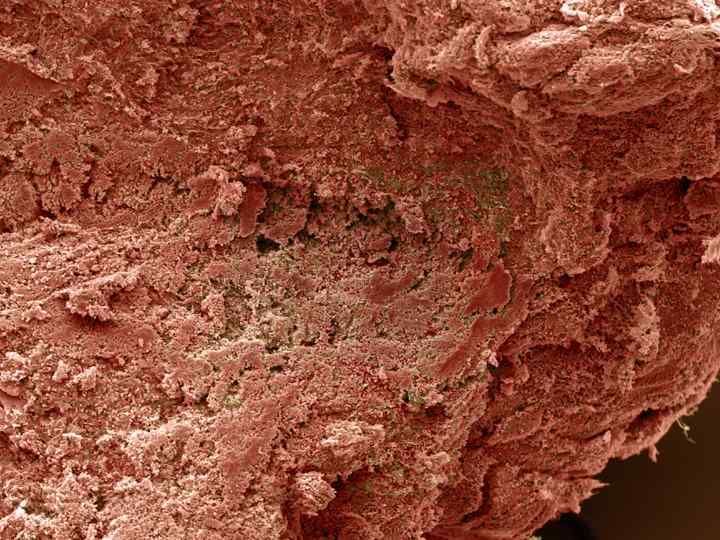
 5. Электронная микрограмма тромба, большее увеличение Тромб представляет собой желеобразную массу фибрина и эритроцитов, структура которой постоянно разрушается и перестраивается. Долговечность тромба зависит от баланса между тромбообразованием и фибринолизом.
5. Электронная микрограмма тромба, большее увеличение Тромб представляет собой желеобразную массу фибрина и эритроцитов, структура которой постоянно разрушается и перестраивается. Долговечность тромба зависит от баланса между тромбообразованием и фибринолизом.
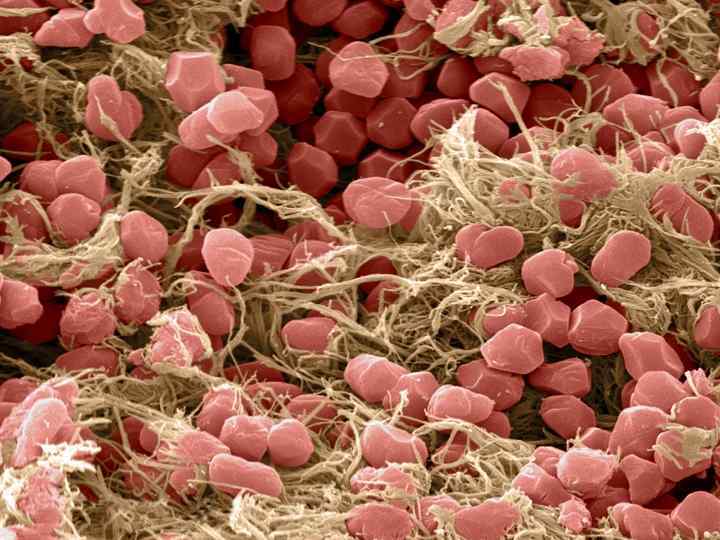
 Патофизиология гемостаза Откоррегированная модель коагуляции имеет значение в терапии и геморрагических и тромботических нарушений. Специфический интерес у анестезиологов вызывает совершенствование контроля за нарушением свертываемости до, во время и после операции.
Патофизиология гемостаза Откоррегированная модель коагуляции имеет значение в терапии и геморрагических и тромботических нарушений. Специфический интерес у анестезиологов вызывает совершенствование контроля за нарушением свертываемости до, во время и после операции.
 Патофизиология гемостаза Недавние достижения молекулярной биологии и клинические данные свидетельствуют, что взаимодействие тканевого фактора с фактором VII является первичным клеточным инициатором коагуляции в естественных условиях. Price GC, Thompson SA, Kam PC, Anaesthesia. 2004; 59(5): 483 -92)
Патофизиология гемостаза Недавние достижения молекулярной биологии и клинические данные свидетельствуют, что взаимодействие тканевого фактора с фактором VII является первичным клеточным инициатором коагуляции в естественных условиях. Price GC, Thompson SA, Kam PC, Anaesthesia. 2004; 59(5): 483 -92)
 Патофизиология гемостаза Пероксинитрит (OONO -), молекула, образующаяся при взаимодействии оксида азота (NO) и супероксида (O 2 -), уменьшает активность TF у больных в критических состояниях. В патогенез коагулопатии, которую связывают с печеночно-кишечной ишемиейреперфузией, вовлекается формирование OONO-. Обнаружено, что активность циркулирующего TF уменьшается после печеночно-кишечной ишемии-реперфузии (Nielsen VG, Crow JP. Anesth Analg. 2004; 98(3): 66871). Возможно, этот механизм ответственен за коагулопатию, развивающуюся при критических состояниях.
Патофизиология гемостаза Пероксинитрит (OONO -), молекула, образующаяся при взаимодействии оксида азота (NO) и супероксида (O 2 -), уменьшает активность TF у больных в критических состояниях. В патогенез коагулопатии, которую связывают с печеночно-кишечной ишемиейреперфузией, вовлекается формирование OONO-. Обнаружено, что активность циркулирующего TF уменьшается после печеночно-кишечной ишемии-реперфузии (Nielsen VG, Crow JP. Anesth Analg. 2004; 98(3): 66871). Возможно, этот механизм ответственен за коагулопатию, развивающуюся при критических состояниях.
 Патофизиология гемостаза Современные научные исследования подтверждают центральную роль FVIIa при многих коагулопатических состояниях: уремия, недостаточность печени, вследствие применения антикоагулянтов, при массивных восполнениях у больных с тяжелой травмой и обширными хирургическими вмешательствами. (Diprose P, Gill R, Herbertson M, 2003).
Патофизиология гемостаза Современные научные исследования подтверждают центральную роль FVIIa при многих коагулопатических состояниях: уремия, недостаточность печени, вследствие применения антикоагулянтов, при массивных восполнениях у больных с тяжелой травмой и обширными хирургическими вмешательствами. (Diprose P, Gill R, Herbertson M, 2003).
 Классификация ДВС - синдрома По клиническому течению выделяют (Лычев В. Г. , 1993): n острый; n подострый; n хронический; n рецидивирующий
Классификация ДВС - синдрома По клиническому течению выделяют (Лычев В. Г. , 1993): n острый; n подострый; n хронический; n рецидивирующий
 Классификация ДВС - синдрома n По стадиям течения (Барышев Б. А. , 1991): I стадия – гиперкоагуляция; n ІІ стадия – гипокоагуляция без генерализованной активации фибринолиза; n ІІІ стадия - гипокоагуляция с генерализованной активацией фибринолиза; n ІV стадия – полное несвертывание крови n
Классификация ДВС - синдрома n По стадиям течения (Барышев Б. А. , 1991): I стадия – гиперкоагуляция; n ІІ стадия – гипокоагуляция без генерализованной активации фибринолиза; n ІІІ стадия - гипокоагуляция с генерализованной активацией фибринолиза; n ІV стадия – полное несвертывание крови n
 диагностика Носит ситуационный характер и основана на выявлении заболеваний и состояний, при которых развитие ДВСсиндрома вполне закономерно. n Во всех этих случаях, необходимо начинать как можно раньше профилактическую терапию до появления выраженных клинических и лабораторных признаков ДВС-синдрома n
диагностика Носит ситуационный характер и основана на выявлении заболеваний и состояний, при которых развитие ДВСсиндрома вполне закономерно. n Во всех этих случаях, необходимо начинать как можно раньше профилактическую терапию до появления выраженных клинических и лабораторных признаков ДВС-синдрома n
 Диагностика должна основываться на: критическом анализе клиники; n тщательном исследовании системы гемостаза на предмет выяснения формы и стадии синдрома; n оценке реакции гемостаза на проводимую терапию противотромботическими препаратами n
Диагностика должна основываться на: критическом анализе клиники; n тщательном исследовании системы гемостаза на предмет выяснения формы и стадии синдрома; n оценке реакции гемостаза на проводимую терапию противотромботическими препаратами n
 Клиника ДВС-синдрома. n n Геморрагический синдром - частое, но не обязательное проявление ДВС-синдрома. По данным Лычева В. Г. (1993) отмечается в среднем у 50 - 75% больных. С клинической точки зрения важно разграничивать кровотечения локального типа - геморрагии из ран в связи с хирургическим вмешательством, послеродовые или послеабортные маточные кровотечения и др. Распространенный геморрагический синдром характеризуется появлением синяков, кровоподтеков, гематом в коже, подкожной и забрюшинной клетчатке, кровоизлияниями в различные органы (мозг и его оболочки, сердце, надпочечники, легкие, матку и др. ), диффузным пропотеванием крови в плевральную и брюшную полость, носовые, желудочно-кишечные кровотечения и т. Д.
Клиника ДВС-синдрома. n n Геморрагический синдром - частое, но не обязательное проявление ДВС-синдрома. По данным Лычева В. Г. (1993) отмечается в среднем у 50 - 75% больных. С клинической точки зрения важно разграничивать кровотечения локального типа - геморрагии из ран в связи с хирургическим вмешательством, послеродовые или послеабортные маточные кровотечения и др. Распространенный геморрагический синдром характеризуется появлением синяков, кровоподтеков, гематом в коже, подкожной и забрюшинной клетчатке, кровоизлияниями в различные органы (мозг и его оболочки, сердце, надпочечники, легкие, матку и др. ), диффузным пропотеванием крови в плевральную и брюшную полость, носовые, желудочно-кишечные кровотечения и т. Д.
 Легкие n в сосуды легочной системы из венозной системы заносится огромное количество микросгустков фибрина, агрегатов клеток крови, продуктов протеолиза (брадикинин, гистамин, фибринопептиды, ПДФ и др. ) В результате развивается острая легочно-цикуляторная недостаточность. При прогрессировании этого процесса развивается острый респираторный дистресс-синдром (ОРДС) взрослых. Интенсивная инфузионная терапия, нередко, усугубляет эти процессы.
Легкие n в сосуды легочной системы из венозной системы заносится огромное количество микросгустков фибрина, агрегатов клеток крови, продуктов протеолиза (брадикинин, гистамин, фибринопептиды, ПДФ и др. ) В результате развивается острая легочно-цикуляторная недостаточность. При прогрессировании этого процесса развивается острый респираторный дистресс-синдром (ОРДС) взрослых. Интенсивная инфузионная терапия, нередко, усугубляет эти процессы.
 Почки снижение диуреза, вплоть до полной анурии n Появление белка в моче, цилиндров, эритроцитов, n нарушение водно-электролитного баланса, кислотно-основного состояния, n нарастание уровня креатинина n прогрессирование симптомов острой почечной недостаточности. n
Почки снижение диуреза, вплоть до полной анурии n Появление белка в моче, цилиндров, эритроцитов, n нарушение водно-электролитного баланса, кислотно-основного состояния, n нарастание уровня креатинина n прогрессирование симптомов острой почечной недостаточности. n
 Печень развитие паренхиматозной желутхи n Повышение уровня ферментов (АЛТ, АСТ, ЩФ, ЛДГ) n прогрессирование печеночной недостаточности. n
Печень развитие паренхиматозной желутхи n Повышение уровня ферментов (АЛТ, АСТ, ЩФ, ЛДГ) n прогрессирование печеночной недостаточности. n
 ЖКТ n n развитие глубокой очаговой дистрофии слизистой двенадцатиперстной кишки и желудка микротромбирование и стаз в сосудах появление множественных геморрагий, превращающихся в тяжелых случаях в сплошное геморрагическое пропитывание слизистой желудка образование острых эрозий и язв. Они могут служить источником повторяющихся кровотечений
ЖКТ n n развитие глубокой очаговой дистрофии слизистой двенадцатиперстной кишки и желудка микротромбирование и стаз в сосудах появление множественных геморрагий, превращающихся в тяжелых случаях в сплошное геморрагическое пропитывание слизистой желудка образование острых эрозий и язв. Они могут служить источником повторяющихся кровотечений
 I стадия - гиперкоагуляции. n n n Продолжительность этой фазы различна. В ней наблюдают уменьшение времени свертывания крови, снижение фибринолитической и антикоагуляционной активности, укорочение тромбин-теста. Клинически в этой стадии наблюдают гиперемию кожных покровов, чередующуюся с цианозом, мраморность рисунка, особенно на верхних и нижних конечностях, иногда озноб, беспокойство больной, тахикардию. Кровотечение в этой стадии обусловлено некачественным хирургическим гемостазом, а не нарушениями свертывания крови.
I стадия - гиперкоагуляции. n n n Продолжительность этой фазы различна. В ней наблюдают уменьшение времени свертывания крови, снижение фибринолитической и антикоагуляционной активности, укорочение тромбин-теста. Клинически в этой стадии наблюдают гиперемию кожных покровов, чередующуюся с цианозом, мраморность рисунка, особенно на верхних и нижних конечностях, иногда озноб, беспокойство больной, тахикардию. Кровотечение в этой стадии обусловлено некачественным хирургическим гемостазом, а не нарушениями свертывания крови.
 I стадия - гиперкоагуляции. Кровь из матки свертывается на 3 -й мин. и быстрее. n Свертывание венозной крови нормальное n ДН I - ІI степени n Хронометрическая гиперкоагуляция Етаноловый тест (ЕТ) (+), n Фактор Виллебранда > 150 – 200 %, гиперагрегация тромбоцитов APACHE II < 20 баллов n
I стадия - гиперкоагуляции. Кровь из матки свертывается на 3 -й мин. и быстрее. n Свертывание венозной крови нормальное n ДН I - ІI степени n Хронометрическая гиперкоагуляция Етаноловый тест (ЕТ) (+), n Фактор Виллебранда > 150 – 200 %, гиперагрегация тромбоцитов APACHE II < 20 баллов n
 II стадия - гипокоагуляции. n n n По данным коагулограммы отмечается потребление факторов свертывания, появляются продукты деградации фибриногена и фибрина (ПДФ), уменьшается число тромбоцитов, увеличивается тромбиновое время, несколько уменьшается время лизиса сгустка фибрина, снижается активность антитромбина III. Клинически отмечают усиление кровотечения из родовых путей, раневых поверхностей, появляются кровоизлияния на коже, носовые кровотечения, петехиальные высыпания на боковых поверхностях грудной клетки, бедрах, верхнем веке. Кровь, изливающаяся из матки, содержит рыхлые сгустки, которые быстро лизируются. Возникновение кровотечения из матки обусловлено ее гипотонией или атонией, а не расстройствами в системе гемокоагуляции
II стадия - гипокоагуляции. n n n По данным коагулограммы отмечается потребление факторов свертывания, появляются продукты деградации фибриногена и фибрина (ПДФ), уменьшается число тромбоцитов, увеличивается тромбиновое время, несколько уменьшается время лизиса сгустка фибрина, снижается активность антитромбина III. Клинически отмечают усиление кровотечения из родовых путей, раневых поверхностей, появляются кровоизлияния на коже, носовые кровотечения, петехиальные высыпания на боковых поверхностях грудной клетки, бедрах, верхнем веке. Кровь, изливающаяся из матки, содержит рыхлые сгустки, которые быстро лизируются. Возникновение кровотечения из матки обусловлено ее гипотонией или атонией, а не расстройствами в системе гемокоагуляции
 II стадия - гипокоагуляции. Кровь из матки свертывается замедленно больше чем за 10 мин. n Петехиальный тип кровоточивости. Хронометрическая гиперкоагуляция, сгусток рыхлый Тромбоциты ≥ 100 тыс. Фибриноген - 1, 5 -3, 0 г/л, n APACHE II > 25 баллов ДН - II степень n
II стадия - гипокоагуляции. Кровь из матки свертывается замедленно больше чем за 10 мин. n Петехиальный тип кровоточивости. Хронометрическая гиперкоагуляция, сгусток рыхлый Тромбоциты ≥ 100 тыс. Фибриноген - 1, 5 -3, 0 г/л, n APACHE II > 25 баллов ДН - II степень n
 n ІІІ стадия – гипокоагуляция с генерализованой активацией фибринолиза Петехиально-пятнистый тип кровоточивости: экхимозы, петехии на коже и слизистых оболочках, кровотечение из мест инъекций и образование на их месте гематом, продолжительное кровотечение из послеоперационной раны, кровотечение в брюшную полость и забрюшинное пространство. . В этой стадии кровотечение из матки обусловлено уже нарушениями гемостаза.
n ІІІ стадия – гипокоагуляция с генерализованой активацией фибринолиза Петехиально-пятнистый тип кровоточивости: экхимозы, петехии на коже и слизистых оболочках, кровотечение из мест инъекций и образование на их месте гематом, продолжительное кровотечение из послеоперационной раны, кровотечение в брюшную полость и забрюшинное пространство. . В этой стадии кровотечение из матки обусловлено уже нарушениями гемостаза.
 n n n ІІІ стадия – гипокоагуляция с генерализованой активацией фибринолиза Кровь из матки не свертывается Кровь из вены свертывается довольно медленно, сгусток быстро растворяется Смешанный тип кровоточивости Хронометрическая гипокоагуляция, Тромбоциты 50 - 100 тыс. Фибриноген 0, 5 -1, 5 г/л АРАСНЕ II = 25 -30 баллов ДН - II -IIІ степени Олигоурия, гематурия
n n n ІІІ стадия – гипокоагуляция с генерализованой активацией фибринолиза Кровь из матки не свертывается Кровь из вены свертывается довольно медленно, сгусток быстро растворяется Смешанный тип кровоточивости Хронометрическая гипокоагуляция, Тромбоциты 50 - 100 тыс. Фибриноген 0, 5 -1, 5 г/л АРАСНЕ II = 25 -30 баллов ДН - II -IIІ степени Олигоурия, гематурия
 ІV стадия – полное несвертывание крови. n Клиническая картина геморрагического синдрома характеризуется смешанным типом кровоточивости: профузное кровотечение из тканей, желудочно-кишечного тракта, дыхательных путей и носо-глотки, макрогематурия.
ІV стадия – полное несвертывание крови. n Клиническая картина геморрагического синдрома характеризуется смешанным типом кровоточивости: профузное кровотечение из тканей, желудочно-кишечного тракта, дыхательных путей и носо-глотки, макрогематурия.
 ІV стадия – полное несвертывание крови. n n n Тотальная геморрагия Кровь из матки и вены не свертывается Выраженная хронометрическая гипокоагуляция Фибриноген – не определяется или следы Тромбоциты < 50 тыс. , Фактор Виллебранда < 100% Анурия, макрогематурия АРАСНЕ II > 30 баллов ДН III – IV степени
ІV стадия – полное несвертывание крови. n n n Тотальная геморрагия Кровь из матки и вены не свертывается Выраженная хронометрическая гипокоагуляция Фибриноген – не определяется или следы Тромбоциты < 50 тыс. , Фактор Виллебранда < 100% Анурия, макрогематурия АРАСНЕ II > 30 баллов ДН III – IV степени
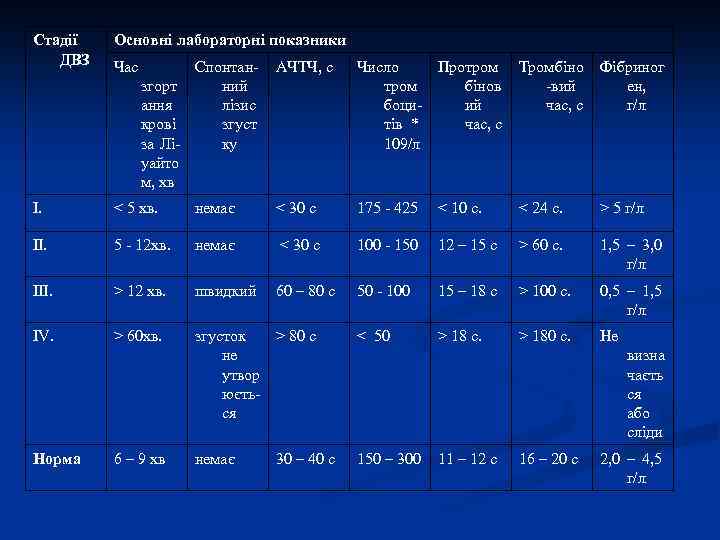 Стадії ДВЗ Основні лабораторні показники І. < 5 хв. ІІ. АЧТЧ, с Число Протром бінов боциий тів * час, с 109/л Тромбіно -вий час, с Фібриног ен, г/л немає < 30 с 175 - 425 < 10 с. < 24 с. > 5 г/л 5 - 12 хв. немає < 30 с 100 - 150 12 – 15 с > 60 с. 1, 5 – 3, 0 г/л ІІІ. > 12 хв. швидкий 60 – 80 с 50 - 100 15 – 18 с > 100 с. 0, 5 – 1, 5 г/л ІV. > 60 хв. згусток > 80 с не утвор юється < 50 > 18 с. > 180 с. Не немає 150 – 300 Норма Час Спонтанзгорт ний ання лізис крові згуст за Ліку уайто м, хв 6 – 9 хв 30 – 40 с визна чаєть ся або сліди 11 – 12 с 16 – 20 с 2, 0 – 4, 5 г/л
Стадії ДВЗ Основні лабораторні показники І. < 5 хв. ІІ. АЧТЧ, с Число Протром бінов боциий тів * час, с 109/л Тромбіно -вий час, с Фібриног ен, г/л немає < 30 с 175 - 425 < 10 с. < 24 с. > 5 г/л 5 - 12 хв. немає < 30 с 100 - 150 12 – 15 с > 60 с. 1, 5 – 3, 0 г/л ІІІ. > 12 хв. швидкий 60 – 80 с 50 - 100 15 – 18 с > 100 с. 0, 5 – 1, 5 г/л ІV. > 60 хв. згусток > 80 с не утвор юється < 50 > 18 с. > 180 с. Не немає 150 – 300 Норма Час Спонтанзгорт ний ання лізис крові згуст за Ліку уайто м, хв 6 – 9 хв 30 – 40 с визна чаєть ся або сліди 11 – 12 с 16 – 20 с 2, 0 – 4, 5 г/л
 Профилактика ДВС-синдрома. n n Своевременно оценить кровопотерю и адекватно проводить восстановление ОЦК благодаря использование кристаллоидных и коллоидных растворов. Из коллоидных растворов преимущество следует отдавать препаратам желатины, которые не влияют на систему гемостаза (гелофузин), а при их отсутствии – производным гидроксиэтилкрахмала (рефортан, стабизол). По возможности, избегать применение реополиглюкина и 5% альбумина. При развитии угрожающего состояния выполнить хирургическое вмешательство в максимально короткие сроки.
Профилактика ДВС-синдрома. n n Своевременно оценить кровопотерю и адекватно проводить восстановление ОЦК благодаря использование кристаллоидных и коллоидных растворов. Из коллоидных растворов преимущество следует отдавать препаратам желатины, которые не влияют на систему гемостаза (гелофузин), а при их отсутствии – производным гидроксиэтилкрахмала (рефортан, стабизол). По возможности, избегать применение реополиглюкина и 5% альбумина. При развитии угрожающего состояния выполнить хирургическое вмешательство в максимально короткие сроки.
 Профилактика ДВС-синдрома. n n n Избегать эпизодов гипоксии и гипотонии во время родов, в том числе и медикаментозно индуцированных. Системно не использовать препараты повышающие коагуляционный потенциал крови (дицинон, аминокапроновую кислоту и др. ). Не применять без насущной необходимости препараты, которые вызывают тромбоцитопению или повышают функциональную активность тромбоцитов (гепарин, реополиглюкин, дипиридамол, полусинтетические пенициллины).
Профилактика ДВС-синдрома. n n n Избегать эпизодов гипоксии и гипотонии во время родов, в том числе и медикаментозно индуцированных. Системно не использовать препараты повышающие коагуляционный потенциал крови (дицинон, аминокапроновую кислоту и др. ). Не применять без насущной необходимости препараты, которые вызывают тромбоцитопению или повышают функциональную активность тромбоцитов (гепарин, реополиглюкин, дипиридамол, полусинтетические пенициллины).
 Интенсивная терапия ДВСсиндрома. n n Лечение основного заболевания. Внутривенное струйное введение 700 – 1000 мл подогретой до 37° С свежезамороженной плазмы. Если кровотечение не останавливается – необходимо дополнительное введение 1000 мл свежезамороженной плазмы. В последующие вторые – третьи сутки, свежезамороженную плазму используют в дозе 400 – 600 мл/сут. При возможности - введение антитромбина ІІІ в дозе 100 ЕД/кг каждые 3 часа
Интенсивная терапия ДВСсиндрома. n n Лечение основного заболевания. Внутривенное струйное введение 700 – 1000 мл подогретой до 37° С свежезамороженной плазмы. Если кровотечение не останавливается – необходимо дополнительное введение 1000 мл свежезамороженной плазмы. В последующие вторые – третьи сутки, свежезамороженную плазму используют в дозе 400 – 600 мл/сут. При возможности - введение антитромбина ІІІ в дозе 100 ЕД/кг каждые 3 часа
 Лечение n Учитывая скорость перехода у акушерских больных стадии гиперкоагуляции в стадию гипокоагуляции, и отсутствии возможности (в большинстве случаев) четкой лабораторной диагностики стадии синдрома ДВС от рутинного применения гепарина следует отказаться. Если после операции прошло 8 -12 часов и отсутствуют признаки кровотечения, то целесообразно назначение гепарина и его производных в профилактических дозах (гепарин – подкожно 10 -20 тыс. ЕД/сут, фраксипарин - 0, 30, 6 мг/сут, клексан - 0, 4 мг/сут.
Лечение n Учитывая скорость перехода у акушерских больных стадии гиперкоагуляции в стадию гипокоагуляции, и отсутствии возможности (в большинстве случаев) четкой лабораторной диагностики стадии синдрома ДВС от рутинного применения гепарина следует отказаться. Если после операции прошло 8 -12 часов и отсутствуют признаки кровотечения, то целесообразно назначение гепарина и его производных в профилактических дозах (гепарин – подкожно 10 -20 тыс. ЕД/сут, фраксипарин - 0, 30, 6 мг/сут, клексан - 0, 4 мг/сут.
 Лечение n Начиная со 2 -й стадии показано введение ингибиторов протеолиза. Контрикал (или другие препараты в эквивалентных дозах) вводят в дозе в зависимости от стадии путем капельной внутривенной инфузии за 1 -2 часа. Введение небольших доз контрикала (50000 – 100000 ЕД) усиливает гиперкоагуляцию.
Лечение n Начиная со 2 -й стадии показано введение ингибиторов протеолиза. Контрикал (или другие препараты в эквивалентных дозах) вводят в дозе в зависимости от стадии путем капельной внутривенной инфузии за 1 -2 часа. Введение небольших доз контрикала (50000 – 100000 ЕД) усиливает гиперкоагуляцию.
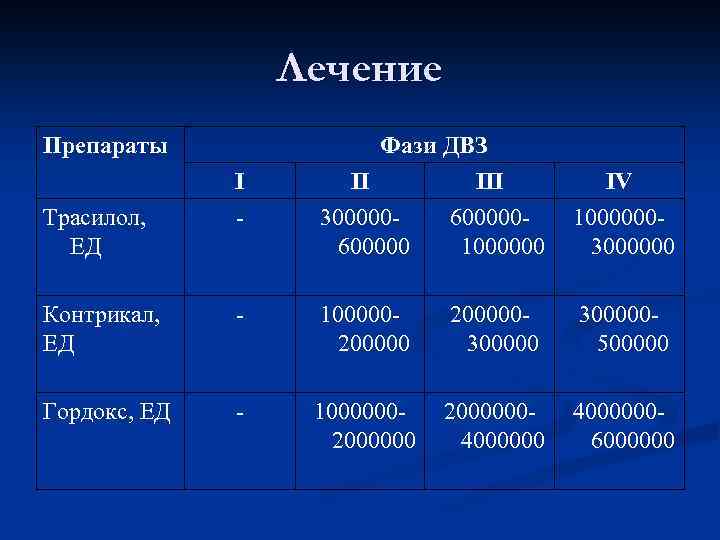 Лечение Препараты Трасилол, ЕД І - Фази ДВЗ ІІ ІІІ 300000600000 1000000 ІV 10000003000000 Контрикал, ЕД - 100000200000300000500000 Гордокс, ЕД - 1000000200000040000006000000
Лечение Препараты Трасилол, ЕД І - Фази ДВЗ ІІ ІІІ 300000600000 1000000 ІV 10000003000000 Контрикал, ЕД - 100000200000300000500000 Гордокс, ЕД - 1000000200000040000006000000
 Лечение n n Восстановление факторов свертывания крови путем введения криопреципитата плазмы (200 ЕД – ІІ стадия, 400 ЕД – ІІІ стадия, 600 ЕД – ІV стадия). При возможности, рекомендуется внутривенное введение рекомбинантного VIIа фактора (новосевен) – 90 мкг/кг. В крайних случаях (дальнейшее прогрессирование гипокоагуляции и кровотечения (Hb < 60 г/л, Ht < 0, 25 л/л), нарастание признаков полиорганной недостаточности), только по жизненным и с согласия больной, а при безсознательном состоянии пациентки – решением консилиума врачей, возможно введение теплой донорской крови в половинной дозе от объема кровопотери.
Лечение n n Восстановление факторов свертывания крови путем введения криопреципитата плазмы (200 ЕД – ІІ стадия, 400 ЕД – ІІІ стадия, 600 ЕД – ІV стадия). При возможности, рекомендуется внутривенное введение рекомбинантного VIIа фактора (новосевен) – 90 мкг/кг. В крайних случаях (дальнейшее прогрессирование гипокоагуляции и кровотечения (Hb < 60 г/л, Ht < 0, 25 л/л), нарастание признаков полиорганной недостаточности), только по жизненным и с согласия больной, а при безсознательном состоянии пациентки – решением консилиума врачей, возможно введение теплой донорской крови в половинной дозе от объема кровопотери.
 Лечение n n n Тромбоцитарная масса используется при снижении тромбоцитов менее 50000/л и при повышении продолжительности кровотечения более чем в 2 раза. Местная остановка кровотечения должна проводиться во всех случаях. Достигается разными методами и способами: коагуляцией и перевязкой сосудов, тампонада раны, применением местных гемостатических средств. Лечение синдрома полиорганной недостаточности.
Лечение n n n Тромбоцитарная масса используется при снижении тромбоцитов менее 50000/л и при повышении продолжительности кровотечения более чем в 2 раза. Местная остановка кровотечения должна проводиться во всех случаях. Достигается разными методами и способами: коагуляцией и перевязкой сосудов, тампонада раны, применением местных гемостатических средств. Лечение синдрома полиорганной недостаточности.
 Препарат Ново. Севен® - рекомбинантный VII активированный фактор человека
Препарат Ново. Севен® - рекомбинантный VII активированный фактор человека
 Механизм действия препарата Ново. Севен®: Образуя комплекс с тканевым фактором (ТФ) запускает эффективный гемостаз непосредственно в месте повреждения n Благодаря высокой концентрации и наличию специфических рецепторов действует независимо от присутствия факторов: V, VIII, IX, XI n За счет наличия на тромбоцитах рецепторов к комплексу VIIa-ТФ эффективен при тромбоцитопении (тромбоцитопатии)
Механизм действия препарата Ново. Севен®: Образуя комплекс с тканевым фактором (ТФ) запускает эффективный гемостаз непосредственно в месте повреждения n Благодаря высокой концентрации и наличию специфических рецепторов действует независимо от присутствия факторов: V, VIII, IX, XI n За счет наличия на тромбоцитах рецепторов к комплексу VIIa-ТФ эффективен при тромбоцитопении (тромбоцитопатии)
 В 1999 г. Израильский хирург Martinovitz с соавт. Описали случай успешного применения препарата Ново. Севен у 19 -летнего солдата с огнестрельным ранением нижней полой вены. Несмотря на повторные оперативные вмешательства и переливание большого количества гемостатических препаратов продолжалось массивное кровотечение и только после введения препарата Ново. Севен (120 мг/кг) оно прекратилось Kenet G, Walden R, Eldad A, Martinowitz U. Treatment of traumatic bleeding with recombinant factor VIIa. Lancet. 1999; 354: 1897).
В 1999 г. Израильский хирург Martinovitz с соавт. Описали случай успешного применения препарата Ново. Севен у 19 -летнего солдата с огнестрельным ранением нижней полой вены. Несмотря на повторные оперативные вмешательства и переливание большого количества гемостатических препаратов продолжалось массивное кровотечение и только после введения препарата Ново. Севен (120 мг/кг) оно прекратилось Kenet G, Walden R, Eldad A, Martinowitz U. Treatment of traumatic bleeding with recombinant factor VIIa. Lancet. 1999; 354: 1897).
 Впоследствии препарат Ново. Севен применяли у других умирающих, гипотермических коагулопатических пациентов, когда с помощью стандартных терапевтических и хирургических методик не удавалось остановить массивное кровотечение. После введения r. FVIIa коррекция коагулопатии и значительное уменьшение скорости кровотечения наблюдалось практически у всех пациентов Martinowitz U, Kenet G, Segal E et al. Recombinant activated factor VII (r. FVIIa) for adjunctive hemorrhage control in trauma. J Trauma. 2001. 31. 431 -439.
Впоследствии препарат Ново. Севен применяли у других умирающих, гипотермических коагулопатических пациентов, когда с помощью стандартных терапевтических и хирургических методик не удавалось остановить массивное кровотечение. После введения r. FVIIa коррекция коагулопатии и значительное уменьшение скорости кровотечения наблюдалось практически у всех пациентов Martinowitz U, Kenet G, Segal E et al. Recombinant activated factor VII (r. FVIIa) for adjunctive hemorrhage control in trauma. J Trauma. 2001. 31. 431 -439.
 Рекомбинантный фактор VIIа(r. FVIIa) был разработан в качестве прогемостатического средства для лечения кровотечений у пациентов с гемофилией А и В с дефицитом факторов VIII и IX, соответственно. r. FVIIa идентичен по структуре и действию к человеческому фактору VIIa. (Bernstein D. E, Jeffers L, Erhardtsen E, et al. Recombinant factor VIIa corrects prothrombin time in cirrhotic patients: a preliminary study. Gastroenterology. 1997; 113: 1930 -1937).
Рекомбинантный фактор VIIа(r. FVIIa) был разработан в качестве прогемостатического средства для лечения кровотечений у пациентов с гемофилией А и В с дефицитом факторов VIII и IX, соответственно. r. FVIIa идентичен по структуре и действию к человеческому фактору VIIa. (Bernstein D. E, Jeffers L, Erhardtsen E, et al. Recombinant factor VIIa corrects prothrombin time in cirrhotic patients: a preliminary study. Gastroenterology. 1997; 113: 1930 -1937).
 Патофизиология гемостаза Ново. Севен может быть эффективным прокоагулянтным агентом при неконтролируемом кровотечении, при этом не вызывая системную гиперкоагуляцию и микротромбообразование (Schreiber MA, Holcomb JB, et al. J Trauma, 2002, 53: 252259). Особенность препарата Ново. Севен в том, что он совместно с ТФ активирует в основном местный гемостаз в поврежденном сосуде, мало влияя на системную реакцию. (Diprose P, Gill R, Herbertson M, 2003)
Патофизиология гемостаза Ново. Севен может быть эффективным прокоагулянтным агентом при неконтролируемом кровотечении, при этом не вызывая системную гиперкоагуляцию и микротромбообразование (Schreiber MA, Holcomb JB, et al. J Trauma, 2002, 53: 252259). Особенность препарата Ново. Севен в том, что он совместно с ТФ активирует в основном местный гемостаз в поврежденном сосуде, мало влияя на системную реакцию. (Diprose P, Gill R, Herbertson M, 2003)
 Лабораторные показатели После применения препарата Ново. Севен нормализовались показатели тромбина и АЧ, а также большинство показателей тромбоэластограммы.
Лабораторные показатели После применения препарата Ново. Севен нормализовались показатели тромбина и АЧ, а также большинство показателей тромбоэластограммы.
 Дозировка Фармакодинамический эффект r. FVIIa является дозозависимым: в дозе 120 мкг/кг концентрация его в плазме составляет 2 -3 мкг/мл, что соответствует нормальному уровню его в плазме 60 -90 ЕД/мл. При гемофилии рекомендуют 90 мкг/кг, однако у хирургических больных сообщают об эффективности более низких доз: • 30 – 45 мкг/кг – Martinovitz et al, 2001; Tanaka et al, 2003; Al Douri et al, 2000 • 70 мкг/ кг – Gielen-Wijffels et al, 2004 Для определения оптимальной дозировки препарата Ново. Севен необходимы дополнительные рандомизированные исследования.
Дозировка Фармакодинамический эффект r. FVIIa является дозозависимым: в дозе 120 мкг/кг концентрация его в плазме составляет 2 -3 мкг/мл, что соответствует нормальному уровню его в плазме 60 -90 ЕД/мл. При гемофилии рекомендуют 90 мкг/кг, однако у хирургических больных сообщают об эффективности более низких доз: • 30 – 45 мкг/кг – Martinovitz et al, 2001; Tanaka et al, 2003; Al Douri et al, 2000 • 70 мкг/ кг – Gielen-Wijffels et al, 2004 Для определения оптимальной дозировки препарата Ново. Севен необходимы дополнительные рандомизированные исследования.
 Введение препарата Ново. Сэвен® n Внутривенно болюсно n Универсальная доза 90 мкг/кг массы тела
Введение препарата Ново. Сэвен® n Внутривенно болюсно n Универсальная доза 90 мкг/кг массы тела
 Безопасность применения препарата Ново. Сэвен® n n n Все побочные эффекты < 3% Все тяжелые побочные эффекты <0, 8% Тромботические осложнения <0, 5% Гемотрансмиссивных вирусов (ВИЧ, гепатит и др. ) нет. В течение последних 6 лет по данным мировой литературы было применено 230 000 доз r. FVIIa, но сообщается только о 24 случаях тромботических осложнений (Erhardsen E. Intensive Care Med, 2002, 28(suppl 2): S 248 -S 256). Причем все больные были пожилого возраста или имели другие факторы риска.
Безопасность применения препарата Ново. Сэвен® n n n Все побочные эффекты < 3% Все тяжелые побочные эффекты <0, 8% Тромботические осложнения <0, 5% Гемотрансмиссивных вирусов (ВИЧ, гепатит и др. ) нет. В течение последних 6 лет по данным мировой литературы было применено 230 000 доз r. FVIIa, но сообщается только о 24 случаях тромботических осложнений (Erhardsen E. Intensive Care Med, 2002, 28(suppl 2): S 248 -S 256). Причем все больные были пожилого возраста или имели другие факторы риска.
 Безопасность Не отмечено побочных эффектов препарата, однако Moore EE et al (2004) указывают на то, что у выживших во многом благодаря препарату Ново. Севен больных с тяжелыми кровотечениями, существует риск развития ПОН, и нельзя исключить какую-то роль препарата Ново. Севен в этом процессе.
Безопасность Не отмечено побочных эффектов препарата, однако Moore EE et al (2004) указывают на то, что у выживших во многом благодаря препарату Ново. Севен больных с тяжелыми кровотечениями, существует риск развития ПОН, и нельзя исключить какую-то роль препарата Ново. Севен в этом процессе.
 Контроль гемостаза применении препарата Ново. Севен® n Протромбиновое время (ПВ) n Активированное частичное тромбопластиновое время (АЧТВ)
Контроль гемостаза применении препарата Ново. Севен® n Протромбиновое время (ПВ) n Активированное частичное тромбопластиновое время (АЧТВ)
 Опыт применения препарата Ново. Севен® Женщина 31 год, беременность 38 недель, развитие HELLP синдрома, экстренное кесарево сечение. Через 2 часа после операции массивное кровотечение с геморрагическим шоком. Проводилась интенсивная заместительная терапия (СЗП, эр-масса, криопреципитат, тромбоциты) Эр-1, 87 х1012/л; Hb-52 г/л; Ht-0, 15; Plt- 76 х109/л; АЧТВ >50 сек; фибриноген <0, 1 г/л; позитивные мономеры фибрина
Опыт применения препарата Ново. Севен® Женщина 31 год, беременность 38 недель, развитие HELLP синдрома, экстренное кесарево сечение. Через 2 часа после операции массивное кровотечение с геморрагическим шоком. Проводилась интенсивная заместительная терапия (СЗП, эр-масса, криопреципитат, тромбоциты) Эр-1, 87 х1012/л; Hb-52 г/л; Ht-0, 15; Plt- 76 х109/л; АЧТВ >50 сек; фибриноген <0, 1 г/л; позитивные мономеры фибрина
 Опыт применения препарата Ново. Севен® Развитие ДВС синдрома. Введение препарата Ново. Севен® 90 мкг/кг внутривенно болюсно. Прекращение кровотечения, нормализация показателей гемостаза. Выписана из клиники через 5 дней. Zupancic et al. Croatia, Univ hospital, Zagreb (данные не опубликованы)
Опыт применения препарата Ново. Севен® Развитие ДВС синдрома. Введение препарата Ново. Севен® 90 мкг/кг внутривенно болюсно. Прекращение кровотечения, нормализация показателей гемостаза. Выписана из клиники через 5 дней. Zupancic et al. Croatia, Univ hospital, Zagreb (данные не опубликованы)
 Опыт применения препарата Ново. Севен® Больная Г. , 20 лет, поступила в НИИ ПАГ, г. Киев Диагноз при поступлении: беременность I, 33 -34 недели, гипопроконвертенемия средней тяжести Клинический диагноз: беременность І, 34 недели, ягодичное предлежание; ГП средней тяжести; гестационный пиелонефрит Тактика ведения родов – при начале спонтанной родовой деятельности, роды вести через естественные родовые пути. С введением СЗП по 200, 0 мл каждые 2 часа – в 1 -ом периоде родов
Опыт применения препарата Ново. Севен® Больная Г. , 20 лет, поступила в НИИ ПАГ, г. Киев Диагноз при поступлении: беременность I, 33 -34 недели, гипопроконвертенемия средней тяжести Клинический диагноз: беременность І, 34 недели, ягодичное предлежание; ГП средней тяжести; гестационный пиелонефрит Тактика ведения родов – при начале спонтанной родовой деятельности, роды вести через естественные родовые пути. С введением СЗП по 200, 0 мл каждые 2 часа – в 1 -ом периоде родов
 Опыт применения препарата Ново. Севен® n Роды начались преждевременным излитием околоплодных вод в сроке 38 недель n В связи со слабостью родовой деятельности и к 6 часам безводного периода – принято решение о проведении кесаревого сечения n Общая кровопотеря – 700, 0 мл n К концу первых суток – геморрагический синдром (внутреннее кровотечение в брюшную полость, маточное, из ослоперационной раны и явления ОПН
Опыт применения препарата Ново. Севен® n Роды начались преждевременным излитием околоплодных вод в сроке 38 недель n В связи со слабостью родовой деятельности и к 6 часам безводного периода – принято решение о проведении кесаревого сечения n Общая кровопотеря – 700, 0 мл n К концу первых суток – геморрагический синдром (внутреннее кровотечение в брюшную полость, маточное, из ослоперационной раны и явления ОПН
 Опыт применения препарата Ново. Севен® n Было перелито 2790, 0 мл СЗП n Проведена релапаротомия на фоне препарата Ново. Севен, который был введен в дозе 60 мкг/кг внутривенно n Проведена экстирпация матки без придатков, дренирование брюшной полости Дашкевич, Перехрестенко и др. – НИИ ПАГ и ИГТ, г. Киев (4(12) 2002 «Здоровье Женщины» )
Опыт применения препарата Ново. Севен® n Было перелито 2790, 0 мл СЗП n Проведена релапаротомия на фоне препарата Ново. Севен, который был введен в дозе 60 мкг/кг внутривенно n Проведена экстирпация матки без придатков, дренирование брюшной полости Дашкевич, Перехрестенко и др. – НИИ ПАГ и ИГТ, г. Киев (4(12) 2002 «Здоровье Женщины» )
 Универсальность Diprose P et al (2003) поставили вопрос: является ли r. FVIIa (Ново. Севен) универсальным гемостатиком? И после тщательного мета-анализа утверждают: ДА. Хотя необходимы дальнейшие исследования для подтверждения этого положения.
Универсальность Diprose P et al (2003) поставили вопрос: является ли r. FVIIa (Ново. Севен) универсальным гемостатиком? И после тщательного мета-анализа утверждают: ДА. Хотя необходимы дальнейшие исследования для подтверждения этого положения.


