011a37adc069d20540e61f50ea25826a.ppt
- Количество слайдов: 51
 Интегрированный урок Учитель: Климова Г. Р.
Интегрированный урок Учитель: Климова Г. Р.
 Алюминий и его соединения.
Алюминий и его соединения.
 ® Знать области применения алюминия и его соединений, нахождение алюминия в природе; ® Уметь давать характеристику алюминия как химического элемента и простого вещества; ® Закрепить понятие амфотерности на примере алюминия и его соединений.
® Знать области применения алюминия и его соединений, нахождение алюминия в природе; ® Уметь давать характеристику алюминия как химического элемента и простого вещества; ® Закрепить понятие амфотерности на примере алюминия и его соединений.
 «Мыслящий ум не чувствует себя счастливым, пока не удастся связать воедино разрозненные факты, им наблюдаемые» (Д. Хевеши)
«Мыслящий ум не чувствует себя счастливым, пока не удастся связать воедино разрозненные факты, им наблюдаемые» (Д. Хевеши)
 Можно ли утверждать, что алюминий является металлом настоящего и будущего?
Можно ли утверждать, что алюминий является металлом настоящего и будущего?
 Что вы знаете об истории открытия алюминия?
Что вы знаете об истории открытия алюминия?
 Алюминий открыт в 1825 году Х. К. Эрстедом. Название этого элемента происходит от латинского alumen. Так в древности назывались квасцы, которые использовали для крашения тканей.
Алюминий открыт в 1825 году Х. К. Эрстедом. Название этого элемента происходит от латинского alumen. Так в древности назывались квасцы, которые использовали для крашения тканей.
 Содержание в земной коре 8, 8% по массе (3 место после кислорода и кремния)
Содержание в земной коре 8, 8% по массе (3 место после кислорода и кремния)
 Природные соединения алюминия: l l Алюмосиликаты (входят в состав полевых шпатов – наиболее распространенных минералов и глин); Боксит (горная порода, из которой получают алюминий. Она содержит Al 2 O 3); Корунд; Глинозем.
Природные соединения алюминия: l l Алюмосиликаты (входят в состав полевых шпатов – наиболее распространенных минералов и глин); Боксит (горная порода, из которой получают алюминий. Она содержит Al 2 O 3); Корунд; Глинозем.
 Посмотрите на географическую карту и найдите залежи перечисленных минералов.
Посмотрите на географическую карту и найдите залежи перечисленных минералов.
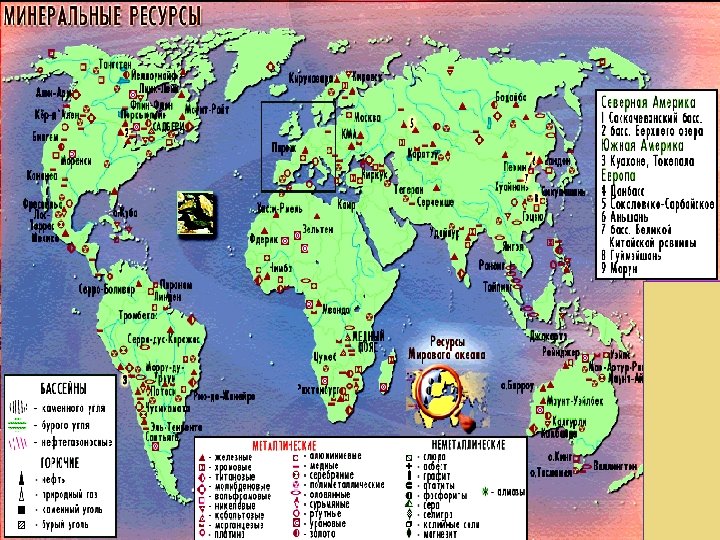
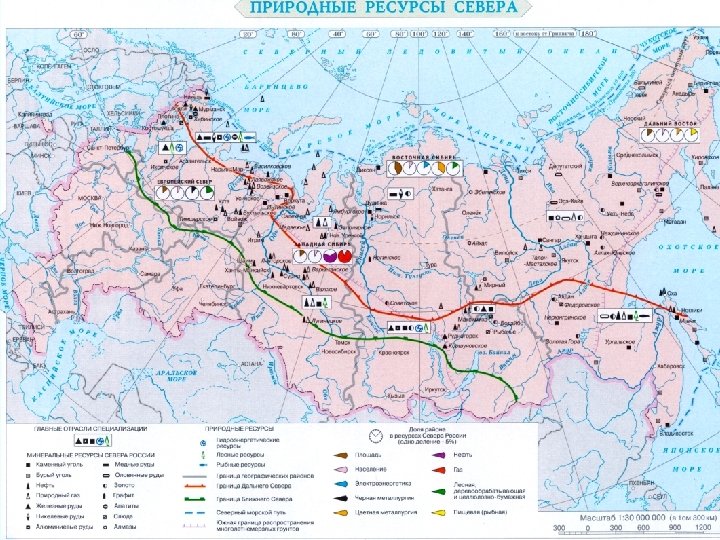
 Получают алюминий Ø разложением электрическим током расплава оксида алюминия (в криолите) 2 Al 2 O 3 = 4 Al + 3 O 2 – 3352 к. Дж Ш Получают на алюминиевых заводах. Мировое производство постоянно растет.
Получают алюминий Ø разложением электрическим током расплава оксида алюминия (в криолите) 2 Al 2 O 3 = 4 Al + 3 O 2 – 3352 к. Дж Ш Получают на алюминиевых заводах. Мировое производство постоянно растет.
 Производство алюминия.
Производство алюминия.
 Способ получения алюминия Алюминий получают электролизом раствора оксида алюминия в расплавленном криолите при температуре 9500 С.
Способ получения алюминия Алюминий получают электролизом раствора оксида алюминия в расплавленном криолите при температуре 9500 С.
 Процесс электролиза изображается следующей схемой: На катоде: На аноде: Al³++3 е→Al° О²ˉ-2 е→О° О+О → 2 О°
Процесс электролиза изображается следующей схемой: На катоде: На аноде: Al³++3 е→Al° О²ˉ-2 е→О° О+О → 2 О°
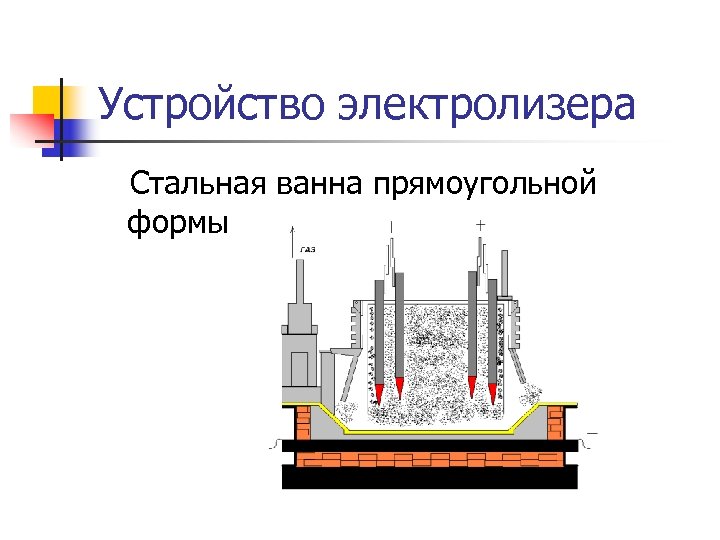 Устройство электролизера Стальная ванна прямоугольной формы
Устройство электролизера Стальная ванна прямоугольной формы
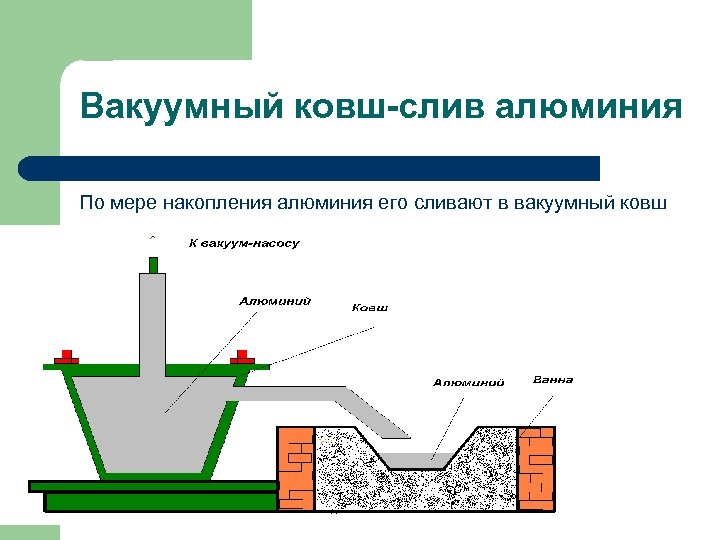 Вакуумный ковш-слив алюминия По мере накопления алюминия его сливают в вакуумный ковш
Вакуумный ковш-слив алюминия По мере накопления алюминия его сливают в вакуумный ковш
 Энергоемкость процесса Для получения одной тонны алюминия расходуется около 17 тыс. квт/ч электроэнергии.
Энергоемкость процесса Для получения одной тонны алюминия расходуется около 17 тыс. квт/ч электроэнергии.
 Из истории алюминиевого производства Первый алюминиевый завод в нашей стране был пущен в 1932 г. На базе Волховской электростанции на тихвинских бокситах.
Из истории алюминиевого производства Первый алюминиевый завод в нашей стране был пущен в 1932 г. На базе Волховской электростанции на тихвинских бокситах.

 27 Al +13 2)8)3) 13 1 S 22 P 63 S 23 P 1 3 S 2 Валентность в соединениях III. Амфотерный металл.
27 Al +13 2)8)3) 13 1 S 22 P 63 S 23 P 1 3 S 2 Валентность в соединениях III. Амфотерный металл.
 Он яркой звездой загорится, Белый и легкий металл, В тринадцатой клетке таблицы Почетное место занял. Для легкости в сплавы дается, Мощь самолета создал. Тягуч и пластичен, отлично куется Серебряный этот металл. В составе багровых рубинов, В сапфировой сини огней, В серой обыденной глине В виде наждачных камней – Всюду металл тот я вижу В отчетливой клетке из линий. К веку легчайших металлов идет Наш чудесный металл «Алюминий» .
Он яркой звездой загорится, Белый и легкий металл, В тринадцатой клетке таблицы Почетное место занял. Для легкости в сплавы дается, Мощь самолета создал. Тягуч и пластичен, отлично куется Серебряный этот металл. В составе багровых рубинов, В сапфировой сини огней, В серой обыденной глине В виде наждачных камней – Всюду металл тот я вижу В отчетливой клетке из линий. К веку легчайших металлов идет Наш чудесный металл «Алюминий» .

 р(Аl) = 2, 7 г/см 3 2500°С 660°С
р(Аl) = 2, 7 г/см 3 2500°С 660°С
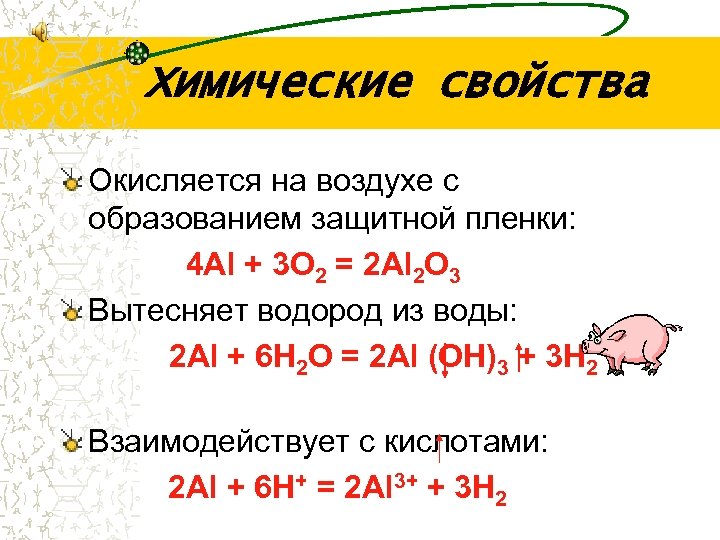 Химические свойства Окисляется на воздухе с образованием защитной пленки: 4 Al + 3 O 2 = 2 Al 2 O 3 Вытесняет водород из воды: 2 Al + 6 H 2 O = 2 Al (OH)3 + 3 H 2 Взаимодействует с кислотами: 2 Al + 6 H+ = 2 Al 3+ + 3 H 2
Химические свойства Окисляется на воздухе с образованием защитной пленки: 4 Al + 3 O 2 = 2 Al 2 O 3 Вытесняет водород из воды: 2 Al + 6 H 2 O = 2 Al (OH)3 + 3 H 2 Взаимодействует с кислотами: 2 Al + 6 H+ = 2 Al 3+ + 3 H 2
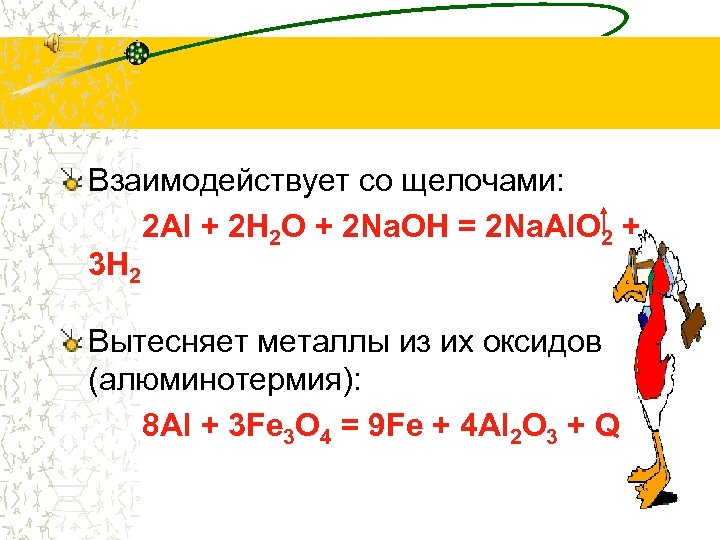 Взаимодействует со щелочами: 2 Al + 2 H 2 O + 2 Na. OH = 2 Na. Al. O 2 + 3 H 2 Вытесняет металлы из их оксидов (алюминотермия): 8 Al + 3 Fe 3 O 4 = 9 Fe + 4 Al 2 O 3 + Q
Взаимодействует со щелочами: 2 Al + 2 H 2 O + 2 Na. OH = 2 Na. Al. O 2 + 3 H 2 Вытесняет металлы из их оксидов (алюминотермия): 8 Al + 3 Fe 3 O 4 = 9 Fe + 4 Al 2 O 3 + Q
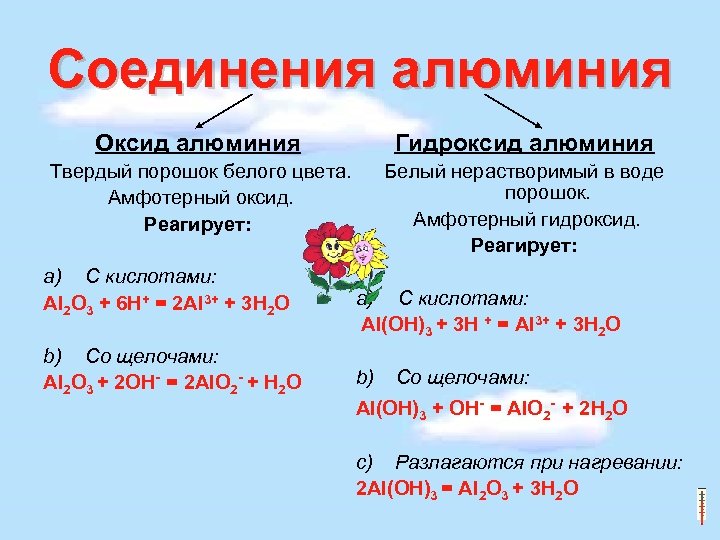 Соединения алюминия Оксид алюминия Гидроксид алюминия Твердый порошок белого цвета. Амфотерный оксид. Реагирует: Белый нерастворимый в воде порошок. Амфотерный гидроксид. Реагирует: a) С кислотами: Al 2 O 3 + 6 H+ = 2 Al 3+ + 3 H 2 O b) Со щелочами: Al 2 O 3 + 2 OH- = 2 Al. O 2 - + H 2 O a) С кислотами: Al(OH)3 + 3 Н + = Al 3+ + 3 H 2 O b) Со щелочами: Al(OH)3 + OH- = Al. O 2 - + 2 H 2 O c) Разлагаются при нагревании: 2 Al(OH)3 = Al 2 O 3 + 3 H 2 O
Соединения алюминия Оксид алюминия Гидроксид алюминия Твердый порошок белого цвета. Амфотерный оксид. Реагирует: Белый нерастворимый в воде порошок. Амфотерный гидроксид. Реагирует: a) С кислотами: Al 2 O 3 + 6 H+ = 2 Al 3+ + 3 H 2 O b) Со щелочами: Al 2 O 3 + 2 OH- = 2 Al. O 2 - + H 2 O a) С кислотами: Al(OH)3 + 3 Н + = Al 3+ + 3 H 2 O b) Со щелочами: Al(OH)3 + OH- = Al. O 2 - + 2 H 2 O c) Разлагаются при нагревании: 2 Al(OH)3 = Al 2 O 3 + 3 H 2 O
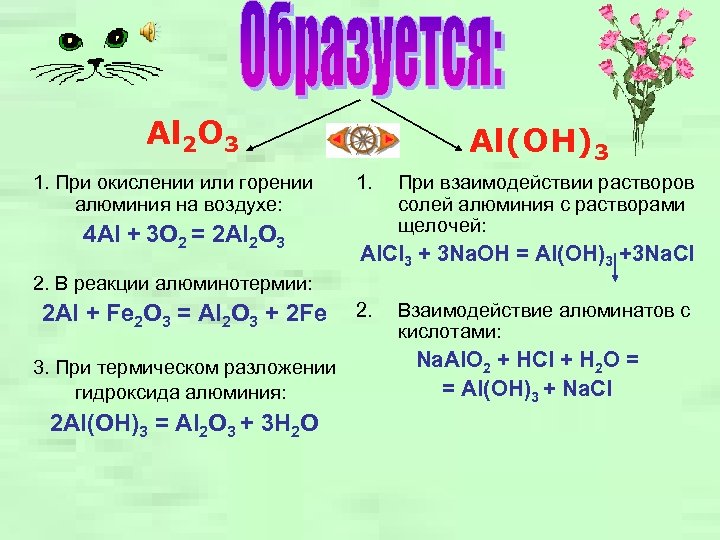 Al 2 O 3 1. При окислении или горении алюминия на воздухе: 4 Al + 3 O 2 = 2 Al 2 O 3 Al(OH)3 1. При взаимодействии растворов солей алюминия с растворами щелочей: Al. Cl 3 + 3 Na. OH = Al(OH)3 +3 Na. Cl 2. В реакции алюминотермии: 2 Al + Fe 2 O 3 = Al 2 O 3 + 2 Fe 3. При термическом разложении гидроксида алюминия: 2 Al(OH)3 = Al 2 O 3 + 3 H 2 O 2. Взаимодействие алюминатов с кислотами: Na. Al. O 2 + HCl + H 2 O = = Al(OH)3 + Na. Cl
Al 2 O 3 1. При окислении или горении алюминия на воздухе: 4 Al + 3 O 2 = 2 Al 2 O 3 Al(OH)3 1. При взаимодействии растворов солей алюминия с растворами щелочей: Al. Cl 3 + 3 Na. OH = Al(OH)3 +3 Na. Cl 2. В реакции алюминотермии: 2 Al + Fe 2 O 3 = Al 2 O 3 + 2 Fe 3. При термическом разложении гидроксида алюминия: 2 Al(OH)3 = Al 2 O 3 + 3 H 2 O 2. Взаимодействие алюминатов с кислотами: Na. Al. O 2 + HCl + H 2 O = = Al(OH)3 + Na. Cl

 Задание № 1 В математике действует правило – «От перемены мест слагаемых сумма не изменяется» . Справедливо ли оно для химии? Проверьте это на примере следующего опыта. Получите гидроксид алюминия по реакции обмена и докажите его амфотерный характер.
Задание № 1 В математике действует правило – «От перемены мест слагаемых сумма не изменяется» . Справедливо ли оно для химии? Проверьте это на примере следующего опыта. Получите гидроксид алюминия по реакции обмена и докажите его амфотерный характер.
 Для этого вы можете использовать реакцию: Al. Cl 3 + 3 Na. OH = Al(OH)3 + 3 Na. Cl Проведите эту реакцию в двух вариантах: сначала к раствору одного из исходных веществ (реагенту) прибавляйте по каплям раствор другого реагента, затем поменяйте последовательность введения в реакцию реагентов. Наблюдайте, в каком случае выпадает осадок, а в каком – нет. Объясните результаты и запишите уравнения проведенных реакций в молекулярной и ионной формах.
Для этого вы можете использовать реакцию: Al. Cl 3 + 3 Na. OH = Al(OH)3 + 3 Na. Cl Проведите эту реакцию в двух вариантах: сначала к раствору одного из исходных веществ (реагенту) прибавляйте по каплям раствор другого реагента, затем поменяйте последовательность введения в реакцию реагентов. Наблюдайте, в каком случае выпадает осадок, а в каком – нет. Объясните результаты и запишите уравнения проведенных реакций в молекулярной и ионной формах.
 Задание № 2 Определите р. Н в растворах некоторых солей алюминия, используя цифровую лабораторию Архимеда. Результаты исследования объясните. Задание № 3 Создайте самостоятельно минибатарейку используя: медную монету, лист пластмассы, алюминиевую фольгу, фильтровальную бумагу, медные изолированные провода, гальванометр, раствор кислоты. Объясните результат эксперимента.
Задание № 2 Определите р. Н в растворах некоторых солей алюминия, используя цифровую лабораторию Архимеда. Результаты исследования объясните. Задание № 3 Создайте самостоятельно минибатарейку используя: медную монету, лист пластмассы, алюминиевую фольгу, фильтровальную бумагу, медные изолированные провода, гальванометр, раствор кислоты. Объясните результат эксперимента.

 Поверхность алюминиевых изделий покрыта тонкой пленкой оксида, который является амфотерным и растворяется в щелочах. Поэтому в бачке будет протекать реакция: Al 2 O 3 + 2 Ca(OH)2 + H 2 O = 2[Ca. Al. O 2 · H 2 O] В результате материал бачка будет постепенно растворяться.
Поверхность алюминиевых изделий покрыта тонкой пленкой оксида, который является амфотерным и растворяется в щелочах. Поэтому в бачке будет протекать реакция: Al 2 O 3 + 2 Ca(OH)2 + H 2 O = 2[Ca. Al. O 2 · H 2 O] В результате материал бачка будет постепенно растворяться.
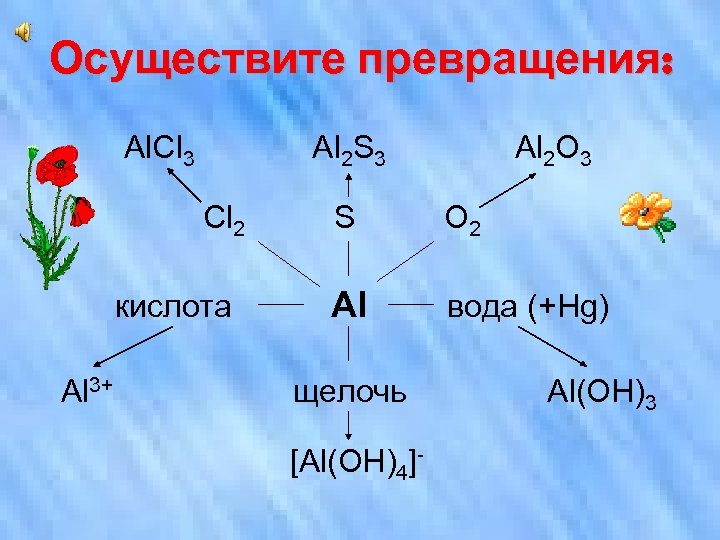 Осуществите превращения: Al. Cl 3 Al 2 S 3 Cl 2 кислота Al 3+ Al 2 O 3 S O 2 Al вода (+Hg) щелочь [Al(OH)4]- Al(OH)3
Осуществите превращения: Al. Cl 3 Al 2 S 3 Cl 2 кислота Al 3+ Al 2 O 3 S O 2 Al вода (+Hg) щелочь [Al(OH)4]- Al(OH)3
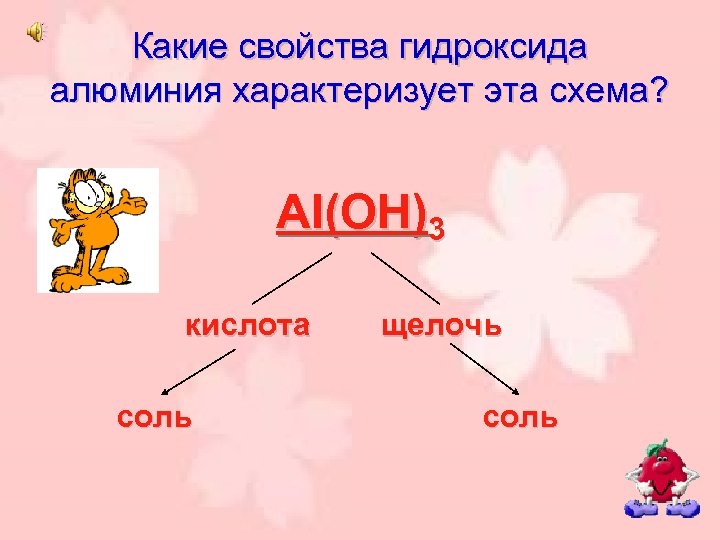 Какие свойства гидроксида алюминия характеризует эта схема? Al(OH)3 кислота соль щелочь соль
Какие свойства гидроксида алюминия характеризует эта схема? Al(OH)3 кислота соль щелочь соль
 Щелочные и щелочноземельные элементы окрашивают пламя в разные цвета. Какие металлы нужно взять для получения этой радуги?
Щелочные и щелочноземельные элементы окрашивают пламя в разные цвета. Какие металлы нужно взять для получения этой радуги?
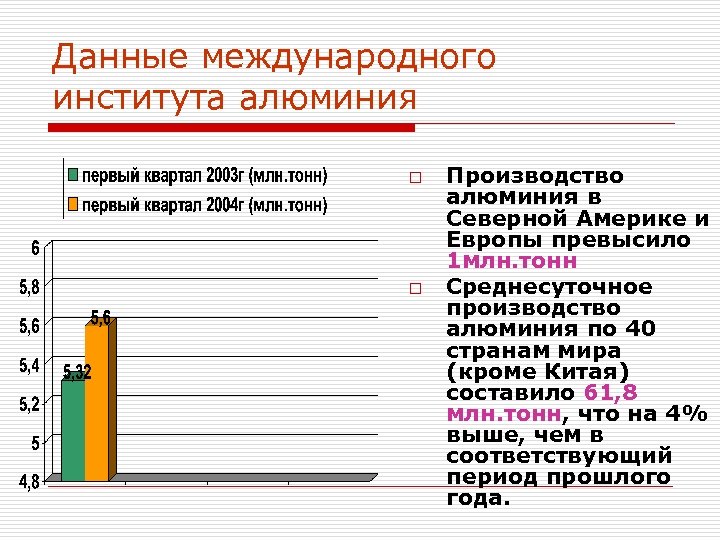 Данные международного института алюминия o o Производство алюминия в Северной Америке и Европы превысило 1 млн. тонн Среднесуточное производство алюминия по 40 странам мира (кроме Китая) составило 61, 8 млн. тонн, что на 4% выше, чем в соответствующий период прошлого года.
Данные международного института алюминия o o Производство алюминия в Северной Америке и Европы превысило 1 млн. тонн Среднесуточное производство алюминия по 40 странам мира (кроме Китая) составило 61, 8 млн. тонн, что на 4% выше, чем в соответствующий период прошлого года.
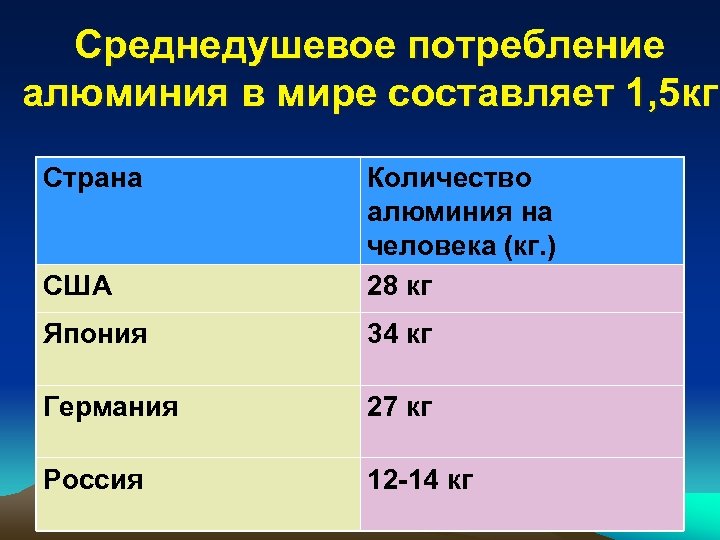 Среднедушевое потребление алюминия в мире составляет 1, 5 кг Страна США Количество алюминия на человека (кг. ) 28 кг Япония 34 кг Германия 27 кг Россия 12 -14 кг
Среднедушевое потребление алюминия в мире составляет 1, 5 кг Страна США Количество алюминия на человека (кг. ) 28 кг Япония 34 кг Германия 27 кг Россия 12 -14 кг
 • В автомобиле сейчас 50 -60 кг алюминия (будет 130 кг). 13 Al 27
• В автомобиле сейчас 50 -60 кг алюминия (будет 130 кг). 13 Al 27
 В России • В ближайшие 5 -6 лет внутреннее потребление вырастает в 5 -6 раз и достигает 3 -3, 5 млн. тонн первичного алюминия. Наиболее важные отрасли потребления: v. Строительство v. Военно-промышленный комплекс v. Самолетостроение и ракетостроение
В России • В ближайшие 5 -6 лет внутреннее потребление вырастает в 5 -6 раз и достигает 3 -3, 5 млн. тонн первичного алюминия. Наиболее важные отрасли потребления: v. Строительство v. Военно-промышленный комплекс v. Самолетостроение и ракетостроение
 ОАО «Русский алюминий» входит в первую тройку мировых производителей алюминия – около 10% мирового производства первичного алюминия и около 70% алюминиевого производства в России.
ОАО «Русский алюминий» входит в первую тройку мировых производителей алюминия – около 10% мирового производства первичного алюминия и около 70% алюминиевого производства в России.
 ТЕСТЫ 1. Химическому элементу с порядковым номером 13 в Периодической системе соответствует конфигурация внешнего энергетического уровня, формула оксида и гидроксида: a) b) c) d) 3 S 23 P 1; R 2 O 3; R(OH)3 3 S 23 P 2; RO 2; R(OH)4 3 S 23 P 2; RO 2; H 2 RO 3 3 S 23 P 4; R 2 O 3; HRO 2 1. Найдите формулу оксида и гидроксида алюминия с порядковым номером 13: a) b) c) d) R 2 O 3; R(OH)3 R 2 O; ROH RO; R(OH)2 R 2 O; R(OH)2
ТЕСТЫ 1. Химическому элементу с порядковым номером 13 в Периодической системе соответствует конфигурация внешнего энергетического уровня, формула оксида и гидроксида: a) b) c) d) 3 S 23 P 1; R 2 O 3; R(OH)3 3 S 23 P 2; RO 2; R(OH)4 3 S 23 P 2; RO 2; H 2 RO 3 3 S 23 P 4; R 2 O 3; HRO 2 1. Найдите формулу оксида и гидроксида алюминия с порядковым номером 13: a) b) c) d) R 2 O 3; R(OH)3 R 2 O; ROH RO; R(OH)2 R 2 O; R(OH)2
 2. Степень окисления алюминия в соединениях: a) b) c) d) +1 +3 +2 +1, +2, +3 3. Определите роль алюминия в алюмотермических процессах: a) b) c) d) Действует как окислитель Обеспечивает необходимое тепло Действует как восстановитель Действует как катализатор 2. Оксид, образованный элементом с порядковым номером 13 относится к: a) b) c) d) Кислотным оксидам Амфотерным оксидам Основным оксидам Безразличным оксидам 3. Защитный слой на поверхности алюминия состоит из: a) b) c) d) Al(OH)3 Na. Al. O 2 Al 2 O 3 Al. N
2. Степень окисления алюминия в соединениях: a) b) c) d) +1 +3 +2 +1, +2, +3 3. Определите роль алюминия в алюмотермических процессах: a) b) c) d) Действует как окислитель Обеспечивает необходимое тепло Действует как восстановитель Действует как катализатор 2. Оксид, образованный элементом с порядковым номером 13 относится к: a) b) c) d) Кислотным оксидам Амфотерным оксидам Основным оксидам Безразличным оксидам 3. Защитный слой на поверхности алюминия состоит из: a) b) c) d) Al(OH)3 Na. Al. O 2 Al 2 O 3 Al. N
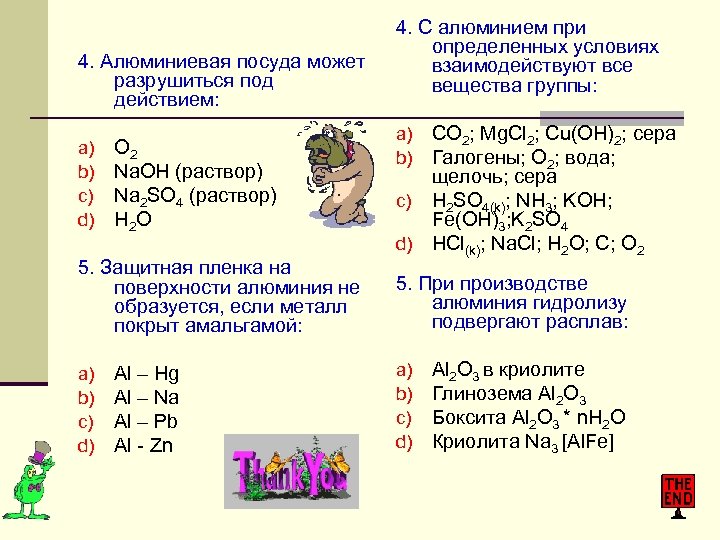 4. Алюминиевая посуда может разрушиться под действием: a) b) c) d) О 2 Na. OH (раствор) Na 2 SO 4 (раствор) H 2 O 5. Защитная пленка на поверхности алюминия не образуется, если металл покрыт амальгамой: a) b) c) d) Al – Hg Al – Na Al – Pb Al - Zn 4. С алюминием при определенных условиях взаимодействуют все вещества группы: CO 2; Mg. Cl 2; Cu(OH)2; сера Галогены; O 2; вода; щелочь; сера c) H 2 SO 4(k); NH 3; KOH; Fe(OH)3; K 2 SO 4 d) HCl(k); Na. Cl; H 2 O; C; O 2 a) b) 5. При производстве алюминия гидролизу подвергают расплав: a) b) c) d) Al 2 O 3 в криолите Глинозема Al 2 O 3 Боксита Al 2 O 3 * n. H 2 O Криолита Na 3 [Al. Fe]
4. Алюминиевая посуда может разрушиться под действием: a) b) c) d) О 2 Na. OH (раствор) Na 2 SO 4 (раствор) H 2 O 5. Защитная пленка на поверхности алюминия не образуется, если металл покрыт амальгамой: a) b) c) d) Al – Hg Al – Na Al – Pb Al - Zn 4. С алюминием при определенных условиях взаимодействуют все вещества группы: CO 2; Mg. Cl 2; Cu(OH)2; сера Галогены; O 2; вода; щелочь; сера c) H 2 SO 4(k); NH 3; KOH; Fe(OH)3; K 2 SO 4 d) HCl(k); Na. Cl; H 2 O; C; O 2 a) b) 5. При производстве алюминия гидролизу подвергают расплав: a) b) c) d) Al 2 O 3 в криолите Глинозема Al 2 O 3 Боксита Al 2 O 3 * n. H 2 O Криолита Na 3 [Al. Fe]
 Полученный код рисуем на лице по точкам
Полученный код рисуем на лице по точкам
 Почему он его так назвал? Если честно, то я и не знаю… Может быть потому что, красивый металл, Может быть потому, что на солнце играет. Может бабушку звали у химика так, Может так подзывал свою кошку. Тем не менее Он так решил И назвал алюминиевой ложку. Я на кухне сижу о Нём рассуждая, Алюминиевой ложкою сахар мешая. Алюминиевую кружку за ручку держа, Алюминиевой вилкой пельмень подцепляя, Рассуждая о Нём не спеша. Он очень старый для меня, Он всем давно известен. Когда мне будет тридцать пять, Ему уж будет двести.
Почему он его так назвал? Если честно, то я и не знаю… Может быть потому что, красивый металл, Может быть потому, что на солнце играет. Может бабушку звали у химика так, Может так подзывал свою кошку. Тем не менее Он так решил И назвал алюминиевой ложку. Я на кухне сижу о Нём рассуждая, Алюминиевой ложкою сахар мешая. Алюминиевую кружку за ручку держа, Алюминиевой вилкой пельмень подцепляя, Рассуждая о Нём не спеша. Он очень старый для меня, Он всем давно известен. Когда мне будет тридцать пять, Ему уж будет двести.
 Мы все знакомы с детства с ним. А кто-то может быть и позже, Но много-много лет назад Он был намного золота дороже! За честь считалось королям И разным феодалам Испить игристого вина Из алюминиевых бокалов. Прошли года, Сменились нравы Из алюминиевой посуды Едят уже не феодалы.
Мы все знакомы с детства с ним. А кто-то может быть и позже, Но много-много лет назад Он был намного золота дороже! За честь считалось королям И разным феодалам Испить игристого вина Из алюминиевых бокалов. Прошли года, Сменились нравы Из алюминиевой посуды Едят уже не феодалы.
 Его так много на Земле Что больше вдвое, чем железа Он применяется везде От вилки до протеза. Ракеты в космос улетают, Идут по морю корабли. Быть может кто-то и не знает, Но Алюминий есть внутри! Он мягкий, лёгкий, серебристый Его и девочка согнёт, Но кремний с магнием добавить И можно строить вертолёт. Когда-то полвека назад, В огромной, Великой Стране Чеканили деньги, Его добавляя Про это отец рассказывал мне. Хотелось бы больше о нём узнать Я жду с нетерпением урок, Когда учитель расскажет всем нам Какой есть ещё в алюминии прок!
Его так много на Земле Что больше вдвое, чем железа Он применяется везде От вилки до протеза. Ракеты в космос улетают, Идут по морю корабли. Быть может кто-то и не знает, Но Алюминий есть внутри! Он мягкий, лёгкий, серебристый Его и девочка согнёт, Но кремний с магнием добавить И можно строить вертолёт. Когда-то полвека назад, В огромной, Великой Стране Чеканили деньги, Его добавляя Про это отец рассказывал мне. Хотелось бы больше о нём узнать Я жду с нетерпением урок, Когда учитель расскажет всем нам Какой есть ещё в алюминии прок!
 1. Массовая доля кислорода в оксиде трехвалентного металла равна 47, 06%. Определите этот металл и составьте формулу оксида. 2. Определите объем водорода, выделенный при взаимодействии с соляной кислотой 5 г алюминия.
1. Массовая доля кислорода в оксиде трехвалентного металла равна 47, 06%. Определите этот металл и составьте формулу оксида. 2. Определите объем водорода, выделенный при взаимодействии с соляной кислотой 5 г алюминия.


