579f2bc03e3b0005be5ef302ae821c8e.ppt
- Количество слайдов: 24
 Инструменты генетического анализа Классическая генетика: Метод Меллер-5 - детекция леталей хромосомные компаунды – детекция нерасхождения хромосом Y-аутосомные транслокации – сегментная анеуплоидия T(A, Y)1 T(A, Y)2 С помощью этого метода была получена анеуплоидия по всем участкам хромосом дрозофилы Были обнаружены все локусы, которые в гаплоидном состоянии приводят к летальности – гапло-чувствительные локусы. Исторически это первый случай, когда было выполнено полногеномное исследование.
Инструменты генетического анализа Классическая генетика: Метод Меллер-5 - детекция леталей хромосомные компаунды – детекция нерасхождения хромосом Y-аутосомные транслокации – сегментная анеуплоидия T(A, Y)1 T(A, Y)2 С помощью этого метода была получена анеуплоидия по всем участкам хромосом дрозофилы Были обнаружены все локусы, которые в гаплоидном состоянии приводят к летальности – гапло-чувствительные локусы. Исторически это первый случай, когда было выполнено полногеномное исследование.
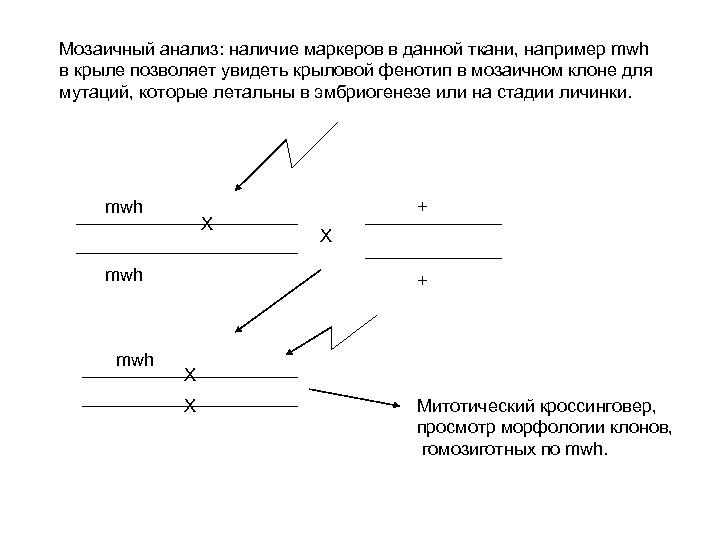 Мозаичный анализ: наличие маркеров в данной ткани, например mwh в крыле позволяет увидеть крыловой фенотип в мозаичном клоне для мутаций, которые летальны в эмбриогенезе или на стадии личинки. mwh X mwh + X X Митотический кроссинговер, просмотр морфологии клонов, гомозиготных по mwh.
Мозаичный анализ: наличие маркеров в данной ткани, например mwh в крыле позволяет увидеть крыловой фенотип в мозаичном клоне для мутаций, которые летальны в эмбриогенезе или на стадии личинки. mwh X mwh + X X Митотический кроссинговер, просмотр морфологии клонов, гомозиготных по mwh.
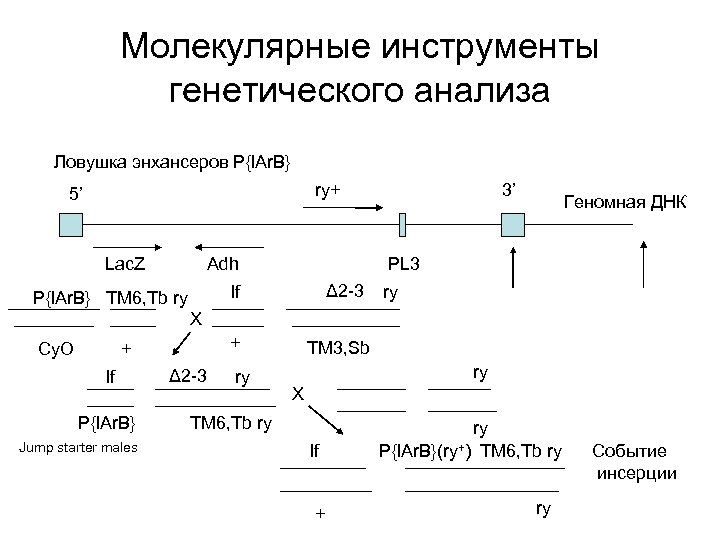 Молекулярные инструменты генетического анализа Ловушка энхансеров P{l. Ar. B} ry+ 5’ Lac. Z Adh Геномная ДНК PL 3 Δ 2 -3 If P{l. Ar. B} TM 6, Tb ry 3’ ry X Cy. O + + If P{l. Ar. B} Jump starter males Δ 2 -3 ry TM 3, Sb ry X TM 6, Tb ry If + ry P{l. Ar. B}(ry+) TM 6, Tb ry ry Событие инсерции
Молекулярные инструменты генетического анализа Ловушка энхансеров P{l. Ar. B} ry+ 5’ Lac. Z Adh Геномная ДНК PL 3 Δ 2 -3 If P{l. Ar. B} TM 6, Tb ry 3’ ry X Cy. O + + If P{l. Ar. B} Jump starter males Δ 2 -3 ry TM 3, Sb ry X TM 6, Tb ry If + ry P{l. Ar. B}(ry+) TM 6, Tb ry ry Событие инсерции
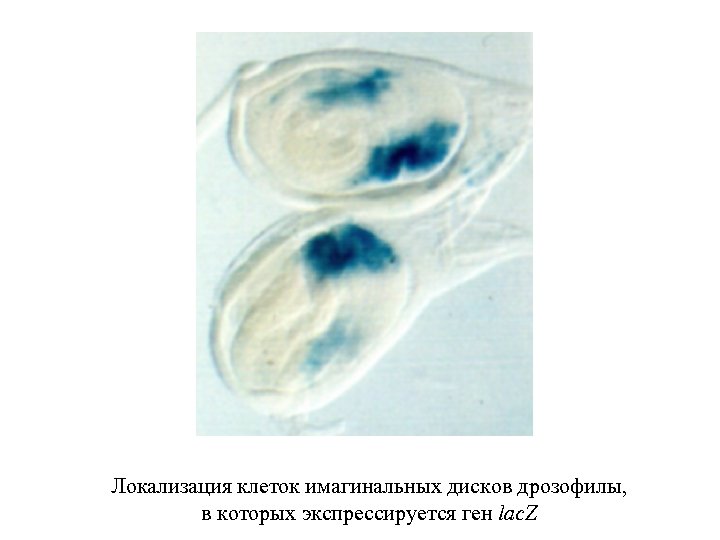 Локализация клеток имагинальных дисков дрозофилы, в которых экспрессируется ген lac. Z
Локализация клеток имагинальных дисков дрозофилы, в которых экспрессируется ген lac. Z
 Структура плазмиды (а) и метод «спасения» плазмиды (б)
Структура плазмиды (а) и метод «спасения» плазмиды (б)
 Частота перемещений энхансерной ловушки у дрозофилы ~ 1%, это не много. Но перемещать ловушку по геному в скрещиваниях много проще, чем заново проводить трансформацию. Именно этим путем было проведено насыщение инсерциями генома дрозофилы в геномном проекте. Энхансерная ловушка у растений Arabidopsis thaliana является наиболее развитым в отношении генной инженерии растительным объектом. У этого растения достаточно легко можно проводить получение новых трансформантов с помощью агробактериального переноса. Но энхансерная ловушка тоже была сконструирована, поскольку не для всех растительных объектов агроперенос возможен. Ac транспозаза под контролем убиквитиного промотора, в Ds элемент вставлен GUS (-glucuronidase) под контролем миниамльного Ca. MV 35 S промотора. Частота транспозиций у риса 1%-15% в зависимости от используемых линий.
Частота перемещений энхансерной ловушки у дрозофилы ~ 1%, это не много. Но перемещать ловушку по геному в скрещиваниях много проще, чем заново проводить трансформацию. Именно этим путем было проведено насыщение инсерциями генома дрозофилы в геномном проекте. Энхансерная ловушка у растений Arabidopsis thaliana является наиболее развитым в отношении генной инженерии растительным объектом. У этого растения достаточно легко можно проводить получение новых трансформантов с помощью агробактериального переноса. Но энхансерная ловушка тоже была сконструирована, поскольку не для всех растительных объектов агроперенос возможен. Ac транспозаза под контролем убиквитиного промотора, в Ds элемент вставлен GUS (-glucuronidase) под контролем миниамльного Ca. MV 35 S промотора. Частота транспозиций у риса 1%-15% в зависимости от используемых линий.
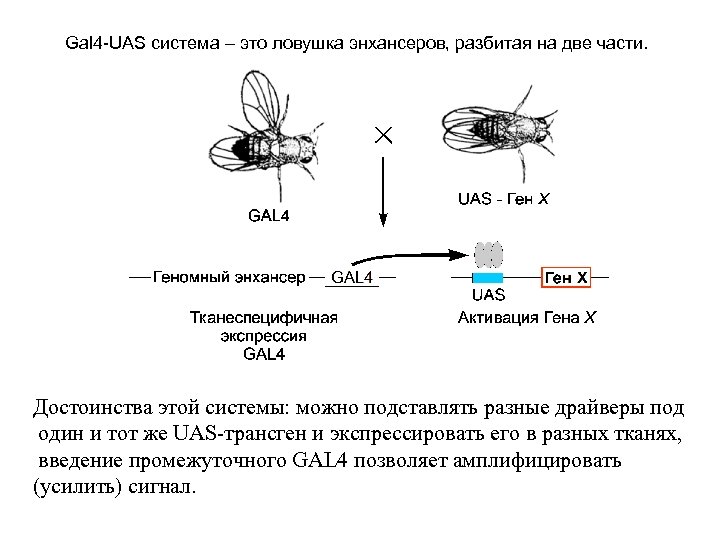 Gal 4 -UAS система – это ловушка энхансеров, разбитая на две части. Достоинства этой системы: можно подставлять разные драйверы под один и тот же UAS-трансген и экспрессировать его в разных тканях, введение промежуточного GAL 4 позволяет амплифицировать (усилить) сигнал.
Gal 4 -UAS система – это ловушка энхансеров, разбитая на две части. Достоинства этой системы: можно подставлять разные драйверы под один и тот же UAS-трансген и экспрессировать его в разных тканях, введение промежуточного GAL 4 позволяет амплифицировать (усилить) сигнал.
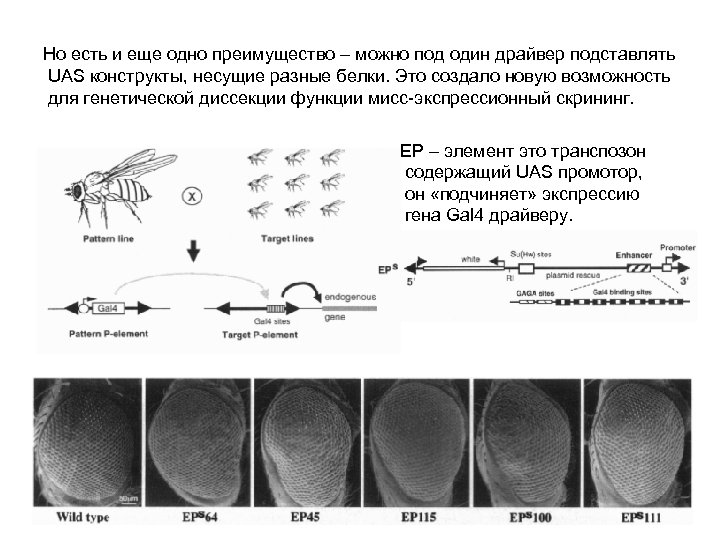 Но есть и еще одно преимущество – можно под один драйвер подставлять UAS конструкты, несущие разные белки. Это создало новую возможность для генетической диссекции функции мисс-экспрессионный скрининг. EP – элемент это транспозон содержащий UAS промотор, он «подчиняет» экспрессию гена Gal 4 драйверу.
Но есть и еще одно преимущество – можно под один драйвер подставлять UAS конструкты, несущие разные белки. Это создало новую возможность для генетической диссекции функции мисс-экспрессионный скрининг. EP – элемент это транспозон содержащий UAS промотор, он «подчиняет» экспрессию гена Gal 4 драйверу.
 Попытка создания Gal 4 -UAS системы на растения (табак) встретилась с трудностями. Как оказалось, сайт связавания Gal 4 в UAS промоторе, метилируется у этого вида, что предотвращает работу этой системы. На Arabidopsis эта проблема менее значима, что дает возможность проводить работы по созданию коллекций драйверов, аналогичных имеющимся у дрозофилы. EP элементы у растений пока не созданы.
Попытка создания Gal 4 -UAS системы на растения (табак) встретилась с трудностями. Как оказалось, сайт связавания Gal 4 в UAS промоторе, метилируется у этого вида, что предотвращает работу этой системы. На Arabidopsis эта проблема менее значима, что дает возможность проводить работы по созданию коллекций драйверов, аналогичных имеющимся у дрозофилы. EP элементы у растений пока не созданы.
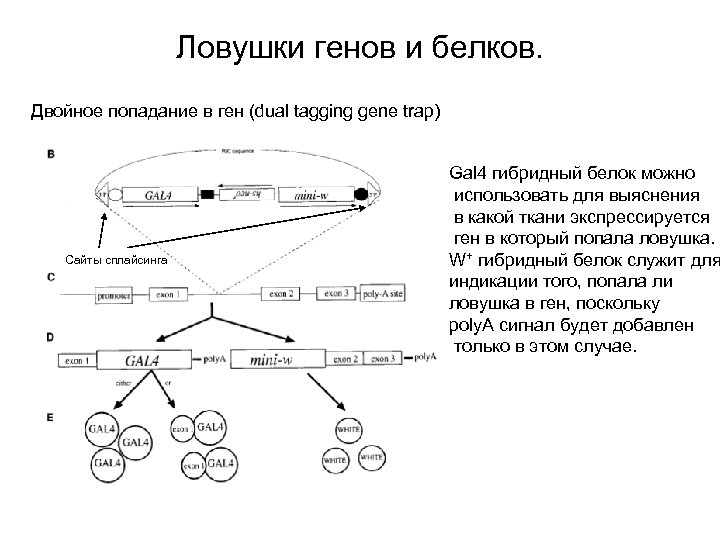 Ловушки генов и белков. Двойное попадание в ген (dual tagging gene trap) Сайты сплайсинга Gal 4 гибридный белок можно использовать для выяснения в какой ткани экспрессируется ген в который попала ловушка. W+ гибридный белок служит для индикации того, попала ли ловушка в ген, поскольку poly. A сигнал будет добавлен только в этом случае.
Ловушки генов и белков. Двойное попадание в ген (dual tagging gene trap) Сайты сплайсинга Gal 4 гибридный белок можно использовать для выяснения в какой ткани экспрессируется ген в который попала ловушка. W+ гибридный белок служит для индикации того, попала ли ловушка в ген, поскольку poly. A сигнал будет добавлен только в этом случае.
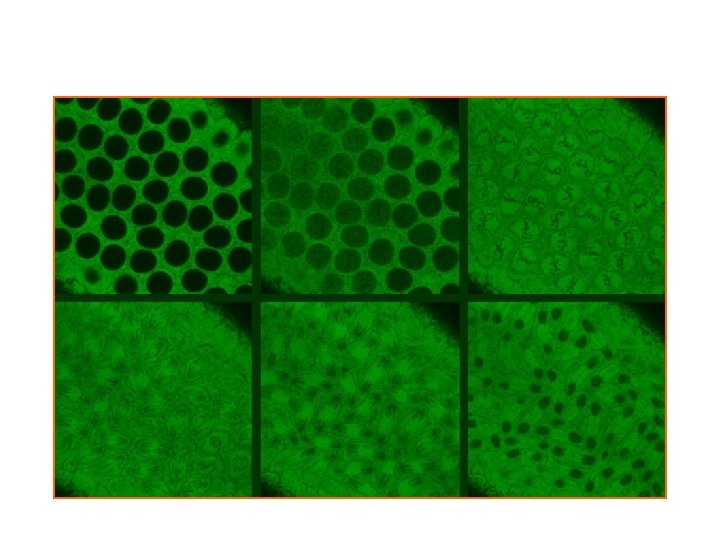
 Метод GFP-белковой ловушки Экзон 1 Интрон 1 Экзон 2 Интрон 2 сайты сплайсинга Копия экзона 1 GFP Копия экзона 2 Копия экзона 3 GFP PDI Экзон 3
Метод GFP-белковой ловушки Экзон 1 Интрон 1 Экзон 2 Интрон 2 сайты сплайсинга Копия экзона 1 GFP Копия экзона 2 Копия экзона 3 GFP PDI Экзон 3
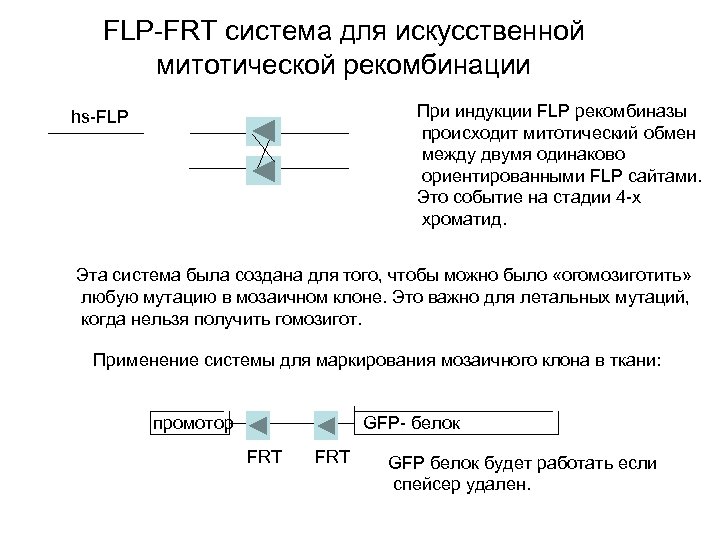 FLP-FRT система для искусственной митотической рекомбинации При индукции FLP рекомбиназы происходит митотический обмен между двумя одинаково ориентированными FLP сайтами. Это событие на стадии 4 -х хроматид. hs-FLP Эта система была создана для того, чтобы можно было «огомозиготить» любую мутацию в мозаичном клоне. Это важно для летальных мутаций, когда нельзя получить гомозигот. Применение системы для маркирования мозаичного клона в ткани: промотор GFP- белок FRT GFP белок будет работать если спейсер удален.
FLP-FRT система для искусственной митотической рекомбинации При индукции FLP рекомбиназы происходит митотический обмен между двумя одинаково ориентированными FLP сайтами. Это событие на стадии 4 -х хроматид. hs-FLP Эта система была создана для того, чтобы можно было «огомозиготить» любую мутацию в мозаичном клоне. Это важно для летальных мутаций, когда нельзя получить гомозигот. Применение системы для маркирования мозаичного клона в ткани: промотор GFP- белок FRT GFP белок будет работать если спейсер удален.
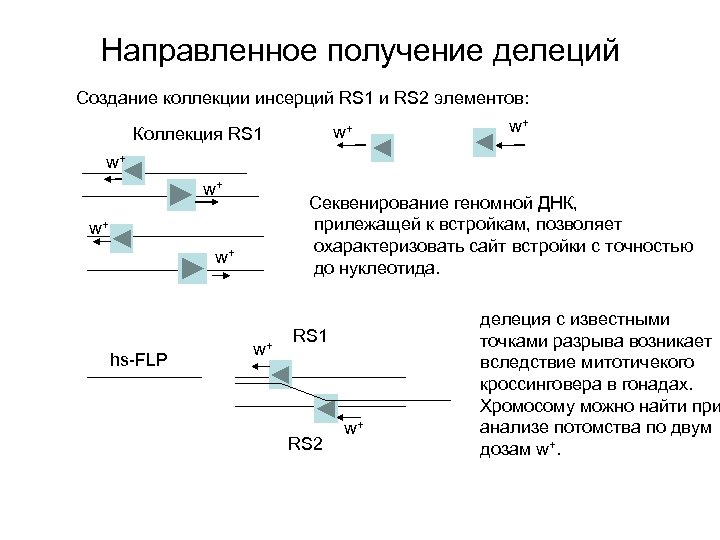 Направленное получение делеций Создание коллекции инсерций RS 1 и RS 2 элементов: w+ Коллекция RS 1 w+ w+ w+ Секвенирование геномной ДНК, прилежащей к встройкам, позволяет охарактеризовать сайт встройки с точностью до нуклеотида. w+ w+ hs-FLP w+ RS 1 RS 2 w+ делеция с известными точками разрыва возникает вследствие митотичекого кроссинговера в гонадах. Хромосому можно найти при анализе потомства по двум дозам w+.
Направленное получение делеций Создание коллекции инсерций RS 1 и RS 2 элементов: w+ Коллекция RS 1 w+ w+ w+ Секвенирование геномной ДНК, прилежащей к встройкам, позволяет охарактеризовать сайт встройки с точностью до нуклеотида. w+ w+ hs-FLP w+ RS 1 RS 2 w+ делеция с известными точками разрыва возникает вследствие митотичекого кроссинговера в гонадах. Хромосому можно найти при анализе потомства по двум дозам w+.
 Получение направленных делеций у растений началось раньше, чем у дрозофилы. Использовали Ds транспозон, содержащий Lox-P сайт. Перемещения внутри генома вызывали с помощью Ac транспозазы. Вместо FLP рекомбиназы была использована Cre рекомбиназа.
Получение направленных делеций у растений началось раньше, чем у дрозофилы. Использовали Ds транспозон, содержащий Lox-P сайт. Перемещения внутри генома вызывали с помощью Ac транспозазы. Вместо FLP рекомбиназы была использована Cre рекомбиназа.
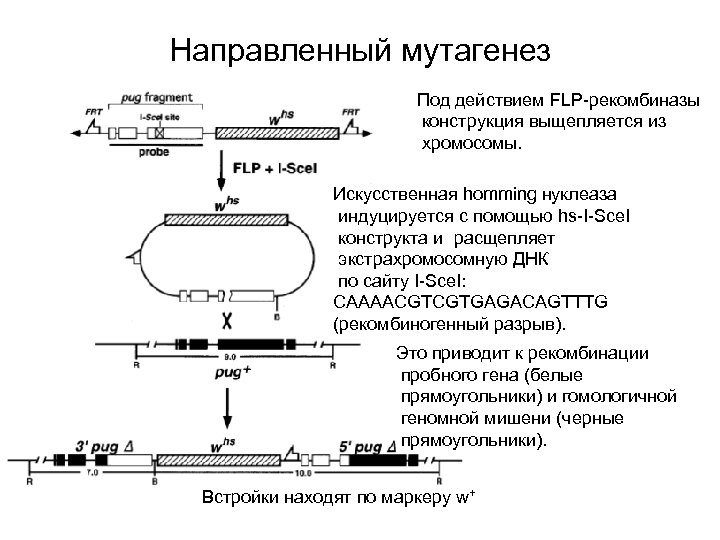 Направленный мутагенез Под действием FLP-рекомбиназы конструкция выщепляется из хромосомы. Искусственная homming нуклеаза индуцируется с помощью hs-I-Sce. I конструкта и расщепляет экстрахромосомную ДНК по сайту I-Sce. I: CAAAACGTCGTGAGACAGTTTG (рекомбиногенный разрыв). Это приводит к рекомбинации пробного гена (белые прямоугольники) и гомологичной геномной мишени (черные прямоугольники). Встройки находят по маркеру w+
Направленный мутагенез Под действием FLP-рекомбиназы конструкция выщепляется из хромосомы. Искусственная homming нуклеаза индуцируется с помощью hs-I-Sce. I конструкта и расщепляет экстрахромосомную ДНК по сайту I-Sce. I: CAAAACGTCGTGAGACAGTTTG (рекомбиногенный разрыв). Это приводит к рекомбинации пробного гена (белые прямоугольники) и гомологичной геномной мишени (черные прямоугольники). Встройки находят по маркеру w+
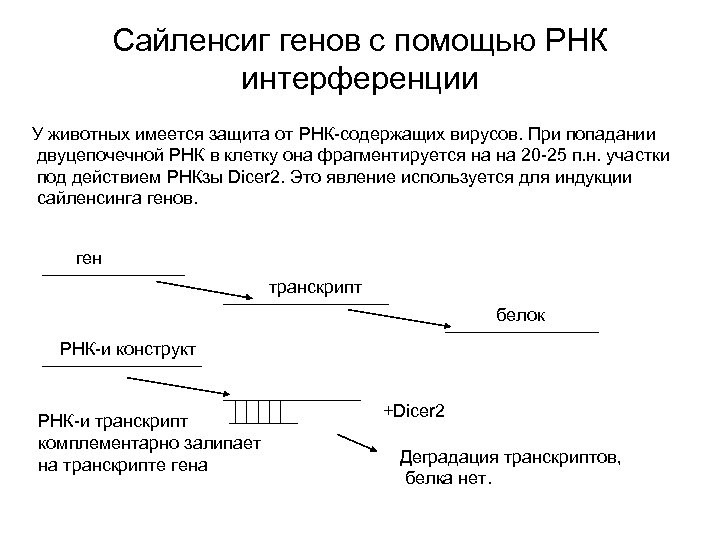 Сайленсиг генов с помощью РНК интерференции У животных имеется защита от РНК-содержащих вирусов. При попадании двуцепочечной РНК в клетку она фрагментируется на на 20 -25 п. н. участки под действием РНКзы Dicer 2. Это явление используется для индукции сайленсинга генов. ген транскрипт белок РНК-и конструкт РНК-и транскрипт комплементарно залипает на транскрипте гена +Dicer 2 Деградация транскриптов, белка нет.
Сайленсиг генов с помощью РНК интерференции У животных имеется защита от РНК-содержащих вирусов. При попадании двуцепочечной РНК в клетку она фрагментируется на на 20 -25 п. н. участки под действием РНКзы Dicer 2. Это явление используется для индукции сайленсинга генов. ген транскрипт белок РНК-и конструкт РНК-и транскрипт комплементарно залипает на транскрипте гена +Dicer 2 Деградация транскриптов, белка нет.
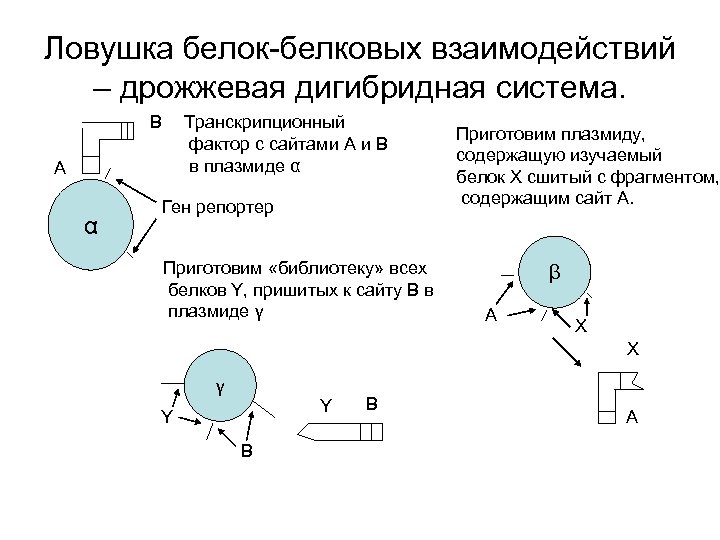 Ловушка белок-белковых взаимодействий – дрожжевая дигибридная система. B Транскрипционный фактор с сайтами A и B в плазмиде α A α Ген репортер Приготовим «библиотеку» всех белков Y, пришитых к сайту B в плазмиде γ Приготовим плазмиду, cодержащую изучаемый белок X сшитый с фрагментом, содержащим сайт A. β A X X γ Y Y B B A
Ловушка белок-белковых взаимодействий – дрожжевая дигибридная система. B Транскрипционный фактор с сайтами A и B в плазмиде α A α Ген репортер Приготовим «библиотеку» всех белков Y, пришитых к сайту B в плазмиде γ Приготовим плазмиду, cодержащую изучаемый белок X сшитый с фрагментом, содержащим сайт A. β A X X γ Y Y B B A
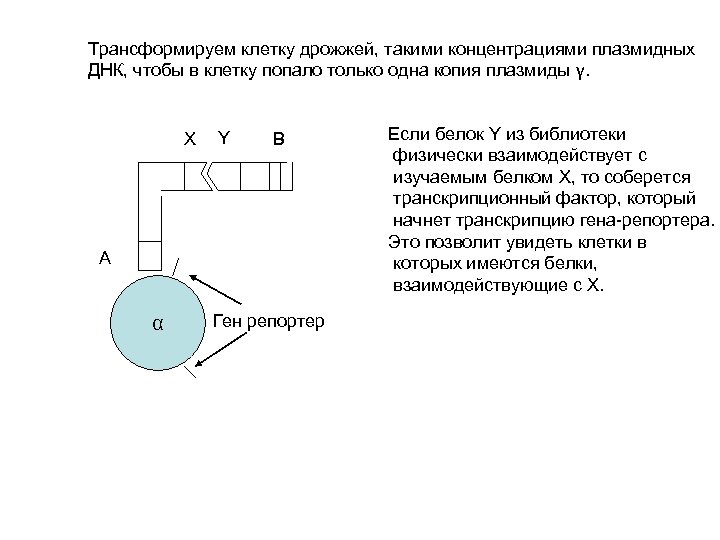 Трансформируем клетку дрожжей, такими концентрациями плазмидных ДНК, чтобы в клетку попало только одна копия плазмиды γ. X Y B A α Ген репортер Если белок Y из библиотеки физически взаимодействует с изучаемым белком X, то соберется транскрипционный фактор, который начнет транскрипцию гена-репортера. Это позволит увидеть клетки в которых имеются белки, взаимодействующие с X.
Трансформируем клетку дрожжей, такими концентрациями плазмидных ДНК, чтобы в клетку попало только одна копия плазмиды γ. X Y B A α Ген репортер Если белок Y из библиотеки физически взаимодействует с изучаемым белком X, то соберется транскрипционный фактор, который начнет транскрипцию гена-репортера. Это позволит увидеть клетки в которых имеются белки, взаимодействующие с X.
 Фаговый дисплей В ген, кодирующий белок оболочки p. III вставляют библиотеку случайных последовательностей из 12 нуклеотидов. После заражения E. coli фагом с низкой плотностью получают библиотек фагов. Каждый фаг несет свой вариант оболочечного белка. Все пептиды представлены частицами фага. Библиотеку используют для отбора фагов связывающихся с определенным субстратом.
Фаговый дисплей В ген, кодирующий белок оболочки p. III вставляют библиотеку случайных последовательностей из 12 нуклеотидов. После заражения E. coli фагом с низкой плотностью получают библиотек фагов. Каждый фаг несет свой вариант оболочечного белка. Все пептиды представлены частицами фага. Библиотеку используют для отбора фагов связывающихся с определенным субстратом.
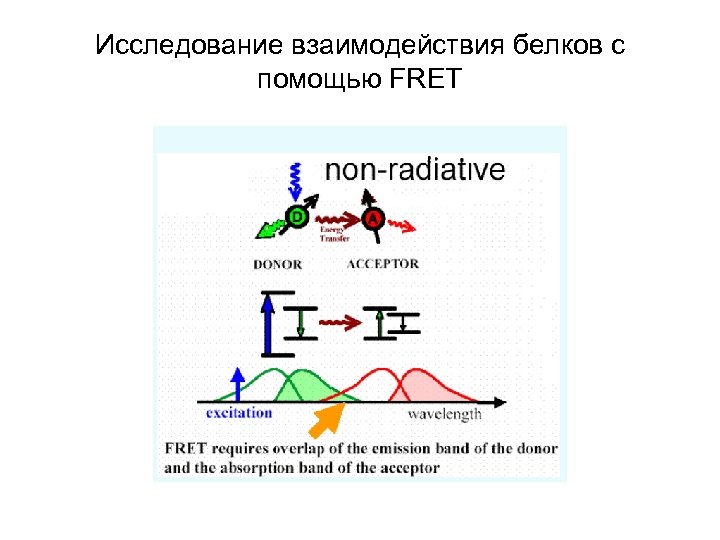 Исследование взаимодействия белков с помощью FRET
Исследование взаимодействия белков с помощью FRET
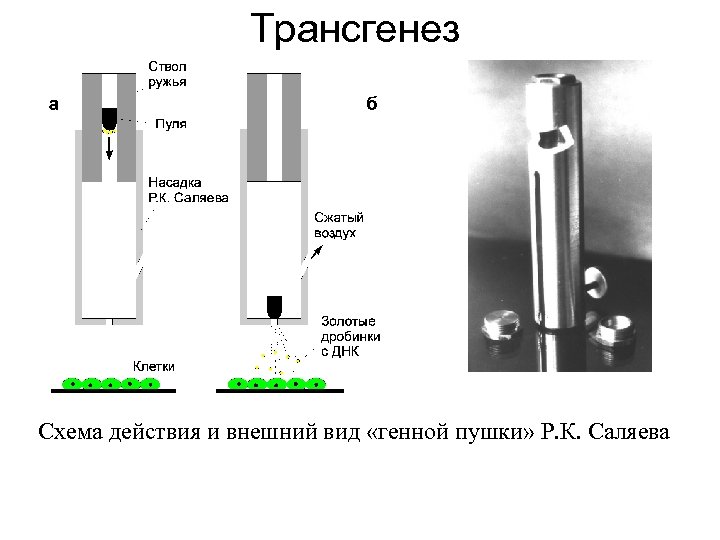 Трансгенез Схема действия и внешний вид «генной пушки» Р. К. Саляева
Трансгенез Схема действия и внешний вид «генной пушки» Р. К. Саляева
 Ускорение роста осины в результате совместного введения генов ugt и acb в ее геном
Ускорение роста осины в результате совместного введения генов ugt и acb в ее геном
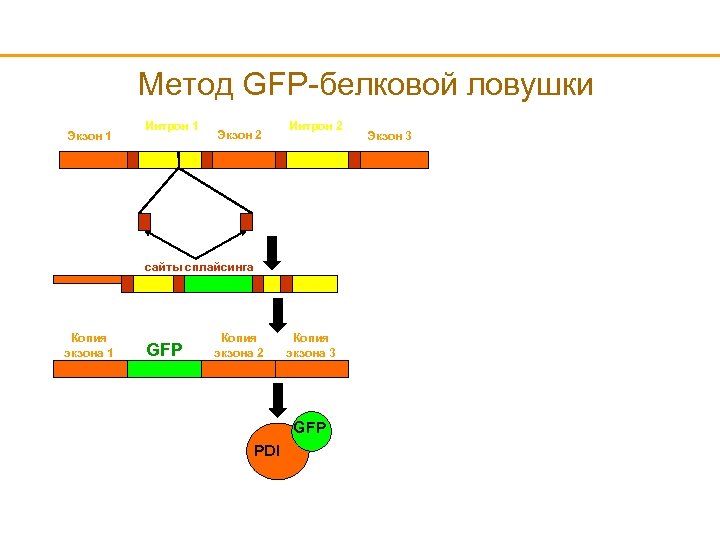 Метод GFP-белковой ловушки Экзон 1 Интрон 1 Экзон 2 Интрон 2 сайты сплайсинга Копия экзона 1 GFP Копия экзона 2 Копия экзона 3 GFP PDI Экзон 3
Метод GFP-белковой ловушки Экзон 1 Интрон 1 Экзон 2 Интрон 2 сайты сплайсинга Копия экзона 1 GFP Копия экзона 2 Копия экзона 3 GFP PDI Экзон 3


