ХГ(168)-27.11.12.ppt
- Количество слайдов: 168
 Институт полиомиелита и вирусных энцефалитов имени М. П. Чумакова РАМН Отдел вирусных гепатитов Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Кафедра госпитальной терапии № 2 лечебного факультета Хронические вирусные гепатиты: клиника, диагностика и лечение Людмила Юрьевна Ильченко 27. 11. 2012
Институт полиомиелита и вирусных энцефалитов имени М. П. Чумакова РАМН Отдел вирусных гепатитов Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Кафедра госпитальной терапии № 2 лечебного факультета Хронические вирусные гепатиты: клиника, диагностика и лечение Людмила Юрьевна Ильченко 27. 11. 2012
 Первым описал признаки гепатита Гиппократ в V веке до нашей эры
Первым описал признаки гепатита Гиппократ в V веке до нашей эры
 Сергей Петрович Боткин С. П. Боткин (1888 г. ) пришел к выводу, что «…катаральная желтуха — специфическое инфекционное заболевание, поражающее не только печень, но и весь организм. . . » Он сделал предположение об общности спорадической катаральной и эпидемической желтухи, а также острой атрофии печени. 5 (17) сентября 1832 г. , Москва – 12 (24) декабря 1889 г. , Ментона
Сергей Петрович Боткин С. П. Боткин (1888 г. ) пришел к выводу, что «…катаральная желтуха — специфическое инфекционное заболевание, поражающее не только печень, но и весь организм. . . » Он сделал предположение об общности спорадической катаральной и эпидемической желтухи, а также острой атрофии печени. 5 (17) сентября 1832 г. , Москва – 12 (24) декабря 1889 г. , Ментона
 Е. М. Тареев совместно с П. Г. Сергиевым, А. А. Гонтаевой и др. описали вспышку желтухи у лиц, вакцинированных против желтой лихорадки Это первое в нашей стране описание клиники сывороточного гепатита «Вирусная желтуха» , 1940 г. Впервые в мировой науке ученые представили доказательство передачи заболевания «безбактериальным фильтратом сыворотки крови» Евгений Михайлович Тареев 13 (25) мая 1895 г. , Псков — 17 августа 1986 г. , Москва «…острый гепатит – хронический гепатит – цирроз печени – цирроз-рак печени"
Е. М. Тареев совместно с П. Г. Сергиевым, А. А. Гонтаевой и др. описали вспышку желтухи у лиц, вакцинированных против желтой лихорадки Это первое в нашей стране описание клиники сывороточного гепатита «Вирусная желтуха» , 1940 г. Впервые в мировой науке ученые представили доказательство передачи заболевания «безбактериальным фильтратом сыворотки крови» Евгений Михайлович Тареев 13 (25) мая 1895 г. , Псков — 17 августа 1986 г. , Москва «…острый гепатит – хронический гепатит – цирроз печени – цирроз-рак печени"
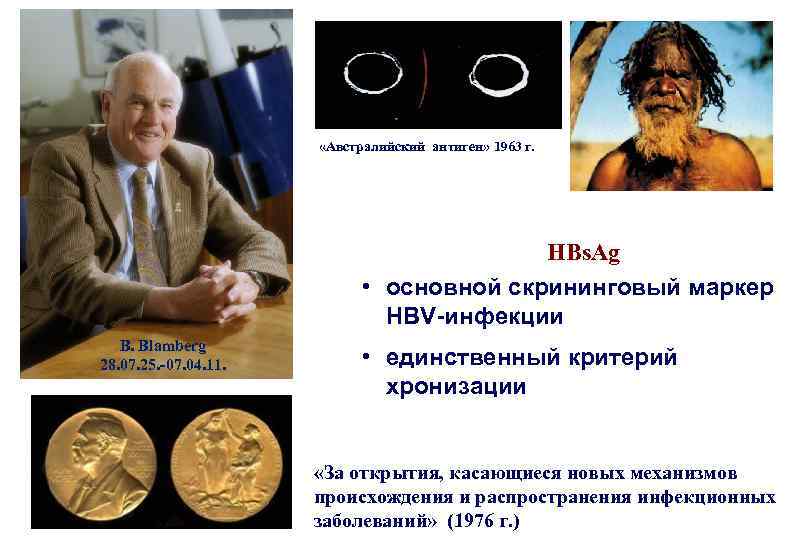 «Австралийский антиген» 1963 г. HBs. Ag • основной скрининговый маркер HBV-инфекции B. Blamberg 28. 07. 25. -07. 04. 11. • единственный критерий хронизации «За открытия, касающиеся новых механизмов происхождения и распространения инфекционных заболеваний» (1976 г. )
«Австралийский антиген» 1963 г. HBs. Ag • основной скрининговый маркер HBV-инфекции B. Blamberg 28. 07. 25. -07. 04. 11. • единственный критерий хронизации «За открытия, касающиеся новых механизмов происхождения и распространения инфекционных заболеваний» (1976 г. )
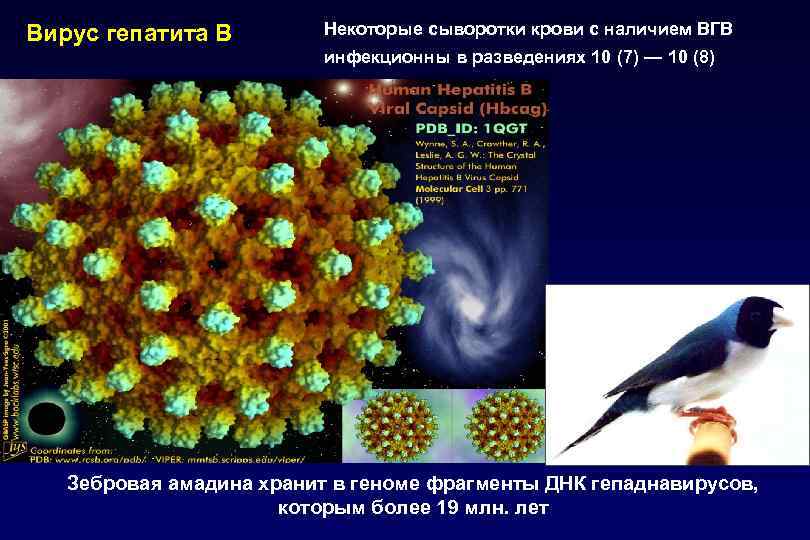 Вирус гепатита В Некоторые сыворотки крови с наличием ВГВ инфекционны в разведениях 10 (7) — 10 (8) Зебровая амадина хранит в геноме фрагменты ДНК гепаднавирусов, которым более 19 млн. лет
Вирус гепатита В Некоторые сыворотки крови с наличием ВГВ инфекционны в разведениях 10 (7) — 10 (8) Зебровая амадина хранит в геноме фрагменты ДНК гепаднавирусов, которым более 19 млн. лет
 Гепатотропные вирусы А, В, С, D, E, G, TT, SEN, NFV …? Герпетическая группа Вирусы кори Вирус краснухи Парвовирусы ВИЧ… Коинфекция Суперинфекция Число возможных сочетаний вирусов – до 5000
Гепатотропные вирусы А, В, С, D, E, G, TT, SEN, NFV …? Герпетическая группа Вирусы кори Вирус краснухи Парвовирусы ВИЧ… Коинфекция Суперинфекция Число возможных сочетаний вирусов – до 5000
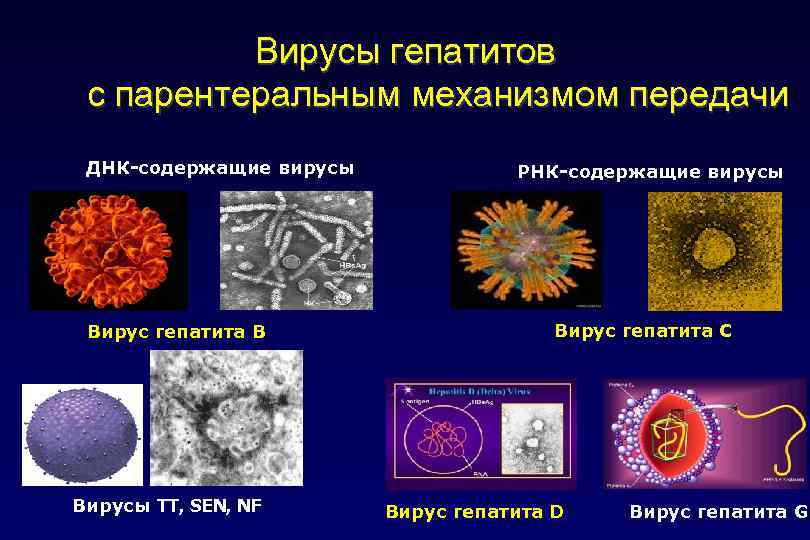 Вирусы гепатитов с парентеральным механизмом передачи ДНК-содержащие вирусы Вирус гепатита В Вирусы TT, SEN, NF РНК-содержащие вирусы Вирус гепатита С Вирус гепатита D Вируc гепатита G
Вирусы гепатитов с парентеральным механизмом передачи ДНК-содержащие вирусы Вирус гепатита В Вирусы TT, SEN, NF РНК-содержащие вирусы Вирус гепатита С Вирус гепатита D Вируc гепатита G
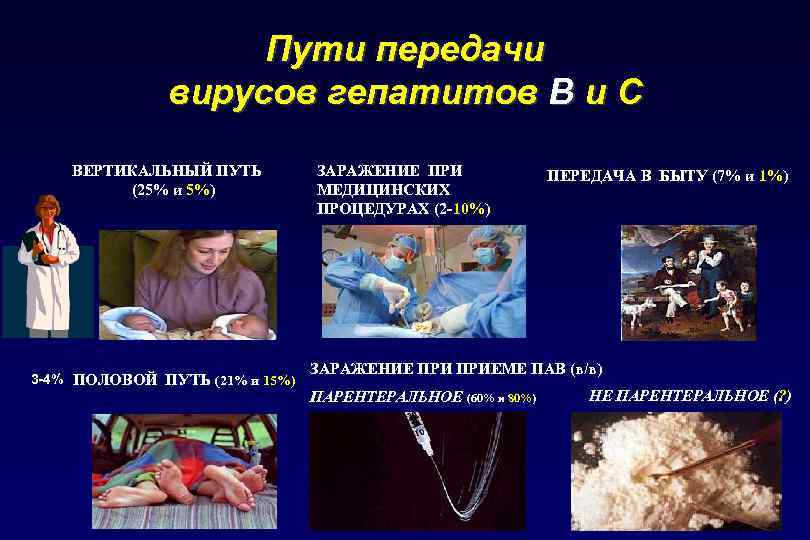 Пути передачи вирусов гепатитов В и С ВЕРТИКАЛЬНЫЙ ПУТЬ (25% и 5%) 3 -4% ПОЛОВОЙ ПУТЬ (21% и 15%) ЗАРАЖЕНИЕ ПРИ МЕДИЦИНСКИХ ПРОЦЕДУРАХ (2 -10%) ПЕРЕДАЧА В БЫТУ (7% и 1%) ЗАРАЖЕНИЕ ПРИЕМЕ ПАВ (в/в) ПАРЕНТЕРАЛЬНОЕ (60% и 80%) НЕ ПАРЕНТЕРАЛЬНОЕ (? )
Пути передачи вирусов гепатитов В и С ВЕРТИКАЛЬНЫЙ ПУТЬ (25% и 5%) 3 -4% ПОЛОВОЙ ПУТЬ (21% и 15%) ЗАРАЖЕНИЕ ПРИ МЕДИЦИНСКИХ ПРОЦЕДУРАХ (2 -10%) ПЕРЕДАЧА В БЫТУ (7% и 1%) ЗАРАЖЕНИЕ ПРИЕМЕ ПАВ (в/в) ПАРЕНТЕРАЛЬНОЕ (60% и 80%) НЕ ПАРЕНТЕРАЛЬНОЕ (? )
 Пирсинг Тату
Пирсинг Тату
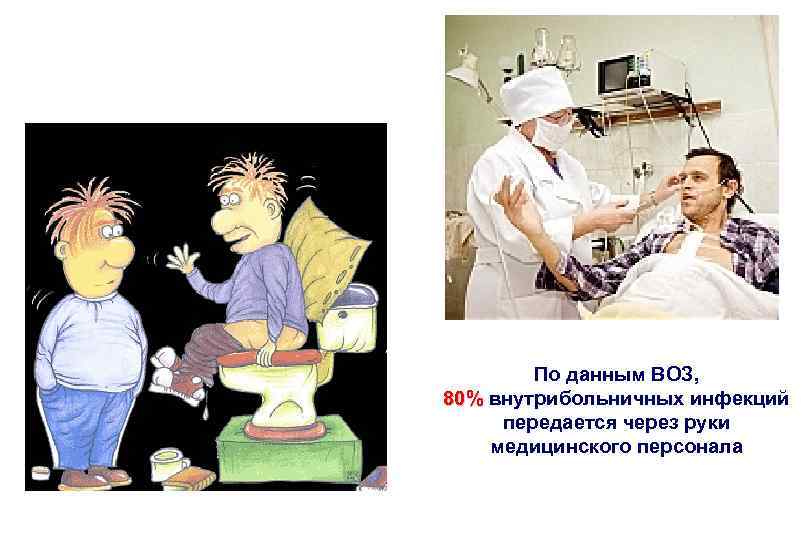 По данным ВОЗ, 80% внутрибольничных инфекций передается через руки медицинского персонала
По данным ВОЗ, 80% внутрибольничных инфекций передается через руки медицинского персонала
 Хронический вирусный гепатит - синдром, характеризуемый постоянными и неустойчивыми болевыми сигналами печени с гистологическими признаками воспаления и гепатоцеллюлярным некрозом. Он определяется как хронический, если клинические симптомы наблюдаются в течение 6 месяцев или более и вызывается, прежде всего, гепатотропными вирусами B, C и D Морозов И. А. , 2010
Хронический вирусный гепатит - синдром, характеризуемый постоянными и неустойчивыми болевыми сигналами печени с гистологическими признаками воспаления и гепатоцеллюлярным некрозом. Он определяется как хронический, если клинические симптомы наблюдаются в течение 6 месяцев или более и вызывается, прежде всего, гепатотропными вирусами B, C и D Морозов И. А. , 2010
 Критерии диагностики вирусных гепатитов • Этиологический фактор • Степень активности • Стадия печеночного процесса IWP. WCG – 1994 J. G. Desmet, M. Gerber, J. H. Hoofnagele, et al. Hepat; 1994; 14: 1513 -1520 • Спектр внепеченочных проявлений
Критерии диагностики вирусных гепатитов • Этиологический фактор • Степень активности • Стадия печеночного процесса IWP. WCG – 1994 J. G. Desmet, M. Gerber, J. H. Hoofnagele, et al. Hepat; 1994; 14: 1513 -1520 • Спектр внепеченочных проявлений
 КЛАССИФИКАЦИЯ ХГ (IWP. WCG – 1994) I Этиология • аутоиммунный гепатит • • хронический вирусный гепатит В хронический вирусный гепатит С хронический вирусный гепатит D хронический вирусный гепатит, не характеризуемый иным образом • хронический гепатит, не классифицируемый как вирусный или как аутоиммунный хронический лекарственный гепатит первичный билиарный цирроз первичный склерозирующий холангит болезнь Вильсона-Коновалова болезнь недостаточности альфа-антитрипсина печени • • •
КЛАССИФИКАЦИЯ ХГ (IWP. WCG – 1994) I Этиология • аутоиммунный гепатит • • хронический вирусный гепатит В хронический вирусный гепатит С хронический вирусный гепатит D хронический вирусный гепатит, не характеризуемый иным образом • хронический гепатит, не классифицируемый как вирусный или как аутоиммунный хронический лекарственный гепатит первичный билиарный цирроз первичный склерозирующий холангит болезнь Вильсона-Коновалова болезнь недостаточности альфа-антитрипсина печени • • •
 КЛАССИФИКАЦИЯ ХГ (IWP. WCG – 1994) II Степень активности патологического процесса • • минимальная (1 -3 балла) слабо выраженная (4 -8 баллов) умеренно выраженная (9 -12 баллов) резко выраженная (13 -18 баллов) АЛТ - 1 -5 N – минимальная активность АЛТ – от 5 N до 10 N – умеренная активность АЛТ > 10 N – высокая активность Индекс гистологической активности (ИГА), R. G. Knodell и соавт. , 1981 А 2 А 3 METAVIR
КЛАССИФИКАЦИЯ ХГ (IWP. WCG – 1994) II Степень активности патологического процесса • • минимальная (1 -3 балла) слабо выраженная (4 -8 баллов) умеренно выраженная (9 -12 баллов) резко выраженная (13 -18 баллов) АЛТ - 1 -5 N – минимальная активность АЛТ – от 5 N до 10 N – умеренная активность АЛТ > 10 N – высокая активность Индекс гистологической активности (ИГА), R. G. Knodell и соавт. , 1981 А 2 А 3 METAVIR
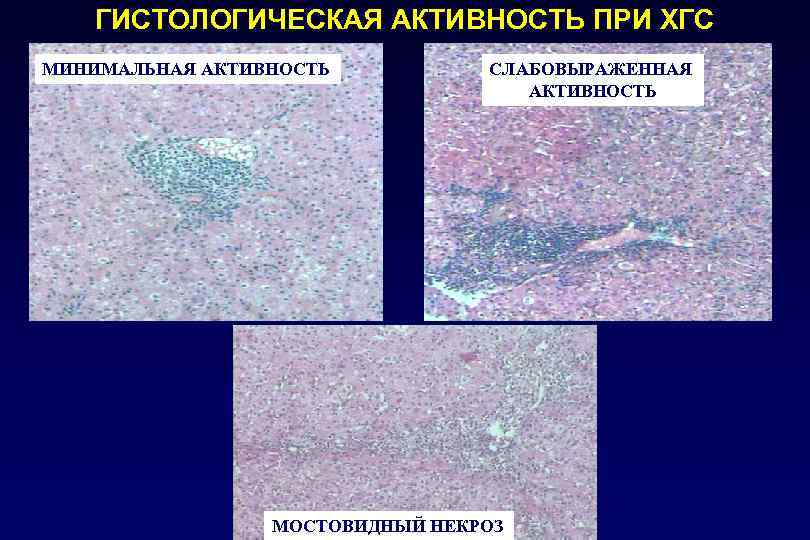 ГИСТОЛОГИЧЕСКАЯ АКТИВНОСТЬ ПРИ ХГС МИНИМАЛЬНАЯ АКТИВНОСТЬ СЛАБОВЫРАЖЕННАЯ АКТИВНОСТЬ МОСТОВИДНЫЙ НЕКРОЗ
ГИСТОЛОГИЧЕСКАЯ АКТИВНОСТЬ ПРИ ХГС МИНИМАЛЬНАЯ АКТИВНОСТЬ СЛАБОВЫРАЖЕННАЯ АКТИВНОСТЬ МОСТОВИДНЫЙ НЕКРОЗ
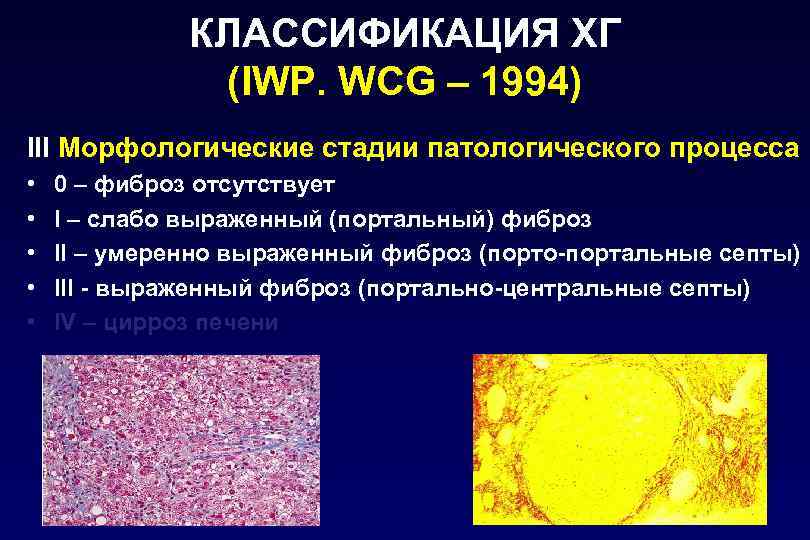 КЛАССИФИКАЦИЯ ХГ (IWP. WCG – 1994) III Морфологические стадии патологического процесса • • • 0 – фиброз отсутствует I – слабо выраженный (портальный) фиброз II – умеренно выраженный фиброз (порто-портальные септы) III - выраженный фиброз (портально-центральные септы) IV – цирроз печени
КЛАССИФИКАЦИЯ ХГ (IWP. WCG – 1994) III Морфологические стадии патологического процесса • • • 0 – фиброз отсутствует I – слабо выраженный (портальный) фиброз II – умеренно выраженный фиброз (порто-портальные септы) III - выраженный фиброз (портально-центральные септы) IV – цирроз печени
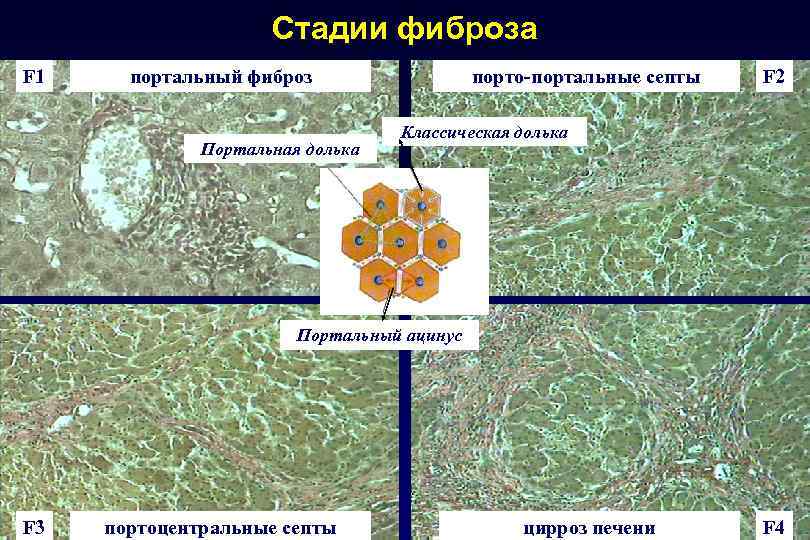 Стадии фиброза F 1 портальный фиброз Портальная долька порто-портальные септы F 2 Классическая долька Портальный ацинус F 3 портоцентральные септы цирроз печени F 4
Стадии фиброза F 1 портальный фиброз Портальная долька порто-портальные септы F 2 Классическая долька Портальный ацинус F 3 портоцентральные септы цирроз печени F 4
 КЛАССИФИКАЦИЯ ХГ (IWP. WCG – 1994) IV Фазы патологического процесса • для неверифицированных ХГ – обострение или ремиссия • для верифицированных вирусных гепатитов репликация или ее отсутствие Фаза репликации - активную продукцию вируса в гепатоцитах
КЛАССИФИКАЦИЯ ХГ (IWP. WCG – 1994) IV Фазы патологического процесса • для неверифицированных ХГ – обострение или ремиссия • для верифицированных вирусных гепатитов репликация или ее отсутствие Фаза репликации - активную продукцию вируса в гепатоцитах
 Патогенез ВГВ- и ВГС-инфекций «хроническая инфекция» ü Репликация вируса в печени и вне ее ü Мутации геномов вируса, гетерогенность генотипов, наличие квазивидов (ВГС), рекомбинантные формы ü Прямой цитопатический эффект (при ВГС) ü Иммунологические и иммунопатологические нарушения В. В. Серов, Н. А. Мухин, 2000; M. R. Gopal et al. , 1990
Патогенез ВГВ- и ВГС-инфекций «хроническая инфекция» ü Репликация вируса в печени и вне ее ü Мутации геномов вируса, гетерогенность генотипов, наличие квазивидов (ВГС), рекомбинантные формы ü Прямой цитопатический эффект (при ВГС) ü Иммунологические и иммунопатологические нарушения В. В. Серов, Н. А. Мухин, 2000; M. R. Gopal et al. , 1990
 Критерии диагностики вирусных гепатитов • Этиологический фактор • Степень активности • Стадия печеночного процесса IWP. WCG – 1994 J. G. Desmet, M. Gerber, J. H. Hoofnagele, et al. Hepat; 1994; 14: 1513 -1520 • Спектр внепеченочных проявлений
Критерии диагностики вирусных гепатитов • Этиологический фактор • Степень активности • Стадия печеночного процесса IWP. WCG – 1994 J. G. Desmet, M. Gerber, J. H. Hoofnagele, et al. Hepat; 1994; 14: 1513 -1520 • Спектр внепеченочных проявлений
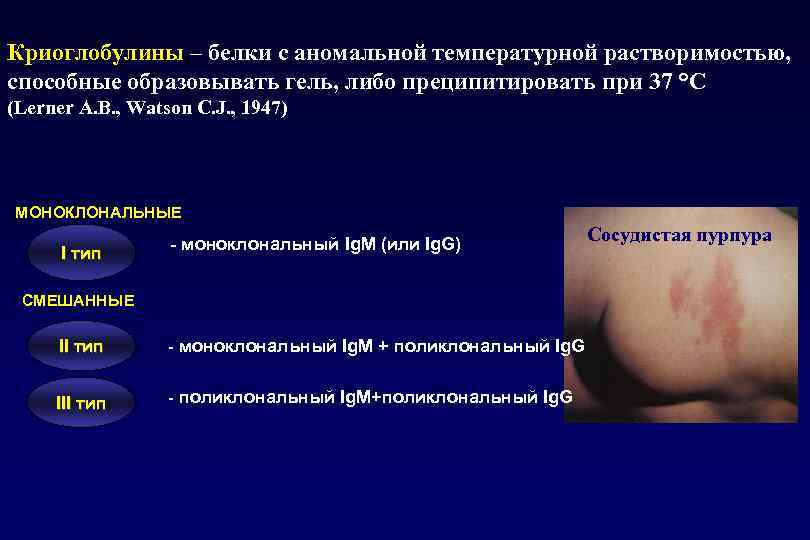 Криоглобулины – белки с аномальной температурной растворимостью, способные образовывать гель, либо преципитировать при 37 °С (Lerner A. B. , Watson C. J. , 1947) МОНОКЛОНАЛЬНЫЕ I тип - моноклональный Ig. M (или Ig. G) СМЕШАННЫЕ II тип - моноклональный Ig. M + поликлональный Ig. G III тип - поликлональный Ig. M+поликлональный Ig. G Сосудистая пурпура
Криоглобулины – белки с аномальной температурной растворимостью, способные образовывать гель, либо преципитировать при 37 °С (Lerner A. B. , Watson C. J. , 1947) МОНОКЛОНАЛЬНЫЕ I тип - моноклональный Ig. M (или Ig. G) СМЕШАННЫЕ II тип - моноклональный Ig. M + поликлональный Ig. G III тип - поликлональный Ig. M+поликлональный Ig. G Сосудистая пурпура
 Внепеченочные поражения, для которых доказана роль HCV в качестве одного из этиологических факторов В-клеточная неходжкинская лимфома Моноклональная иммуноглобулинопатия Узелковый полиартериит Синдром Шегрена Иммунная цитопения Поздняя кожная порфирия (спорадическая форма) Красный плоский лишай Сахарный диабет II типа Аутоиммунный тиреоидит
Внепеченочные поражения, для которых доказана роль HCV в качестве одного из этиологических факторов В-клеточная неходжкинская лимфома Моноклональная иммуноглобулинопатия Узелковый полиартериит Синдром Шегрена Иммунная цитопения Поздняя кожная порфирия (спорадическая форма) Красный плоский лишай Сахарный диабет II типа Аутоиммунный тиреоидит
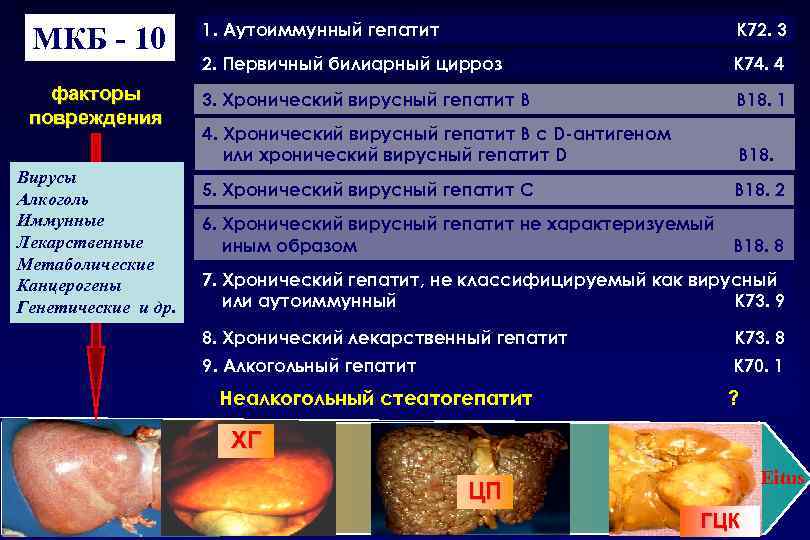 МКБ - 10 факторы повреждения Вирусы Алкоголь Иммунные Лекарственные Метаболические Канцерогены Генетические и др. 1. Аутоиммунный гепатит К 72. 3 2. Первичный билиарный цирроз К 74. 4 3. Хронический вирусный гепатит В В 18. 1 4. Хронический вирусный гепатит В с D-антигеном или хронический вирусный гепатит D 0 5. Хронический вирусный гепатит С В 18. 2 6. Хронический вирусный гепатит не характеризуемый иным образом В 18. 8 7. Хронический гепатит, не классифицируемый как вирусный или аутоиммунный К 73. 9 8. Хронический лекарственный гепатит К 73. 8 9. Алкогольный гепатит К 70. 1 Неалкогольный стеатогепатит ? ХГ Еitus ЦП ГЦК
МКБ - 10 факторы повреждения Вирусы Алкоголь Иммунные Лекарственные Метаболические Канцерогены Генетические и др. 1. Аутоиммунный гепатит К 72. 3 2. Первичный билиарный цирроз К 74. 4 3. Хронический вирусный гепатит В В 18. 1 4. Хронический вирусный гепатит В с D-антигеном или хронический вирусный гепатит D 0 5. Хронический вирусный гепатит С В 18. 2 6. Хронический вирусный гепатит не характеризуемый иным образом В 18. 8 7. Хронический гепатит, не классифицируемый как вирусный или аутоиммунный К 73. 9 8. Хронический лекарственный гепатит К 73. 8 9. Алкогольный гепатит К 70. 1 Неалкогольный стеатогепатит ? ХГ Еitus ЦП ГЦК
 Методы исследований ЭГДС, ЭРХПГ, КТ, МРТХ БИОХИМИЧЕСКИЕ ТЕСТЫ УЗИ ИММУНОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ МОРФОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ МАРКЕРЫ ВИРУСНЫХ ГЕПАТИТОВ IFA PCR
Методы исследований ЭГДС, ЭРХПГ, КТ, МРТХ БИОХИМИЧЕСКИЕ ТЕСТЫ УЗИ ИММУНОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ МОРФОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ МАРКЕРЫ ВИРУСНЫХ ГЕПАТИТОВ IFA PCR
 Маркеры инфицирования вирусами гепатитов ВГВ ВГС ВГD репликации HBe. Ag HBc. Ab Ig. M HBV DNA anti-HCVс Ig. M HCV RNA anti-HDV Ig. M HDV RNA инфицирования HBs. Ag anti-HCV свидетельствуют о перенесенном ОВГ HBs. Ab HBc. Ab HBe. Ab anti-HCV anti-HDV Ig. G
Маркеры инфицирования вирусами гепатитов ВГВ ВГС ВГD репликации HBe. Ag HBc. Ab Ig. M HBV DNA anti-HCVс Ig. M HCV RNA anti-HDV Ig. M HDV RNA инфицирования HBs. Ag anti-HCV свидетельствуют о перенесенном ОВГ HBs. Ab HBc. Ab HBe. Ab anti-HCV anti-HDV Ig. G
 Биохимические тесты для оценки фиброза Тесты Биохимические параметры Fibro. Test α 2 -макроглобулин, гаптоглобин, ГГТП, общий билирубин, аполипопротеин A 1 Fibro. Spect II α 2 -макроглобулин, гиалуроновая кислота, тканевые ингибиторы металлопротеиназ Fibro. SURE α 2 -макроглобулин, гаптоглобин, ГГТП, общий билирубин, аполипопротеин A 1, АЛТ, АСТ, холестерин, триглицериды, глюкоза APRI АСТ / тромбоциты Forns индекс Возраст, тромбоциты, ГГТП, холестерин FIB-4 Тромбоциты, АЛТ, АСТ, возраст Hepa. Score α 2 -макроглобулин, гиалуроновая кислота, ГГТП, общий билирубин Fibrometer Возраст, пол, α 2 -макроглобулин, гиалуроновая кислота, тромбоциты, протромбиновый индекс, АСТ, мочевина
Биохимические тесты для оценки фиброза Тесты Биохимические параметры Fibro. Test α 2 -макроглобулин, гаптоглобин, ГГТП, общий билирубин, аполипопротеин A 1 Fibro. Spect II α 2 -макроглобулин, гиалуроновая кислота, тканевые ингибиторы металлопротеиназ Fibro. SURE α 2 -макроглобулин, гаптоглобин, ГГТП, общий билирубин, аполипопротеин A 1, АЛТ, АСТ, холестерин, триглицериды, глюкоза APRI АСТ / тромбоциты Forns индекс Возраст, тромбоциты, ГГТП, холестерин FIB-4 Тромбоциты, АЛТ, АСТ, возраст Hepa. Score α 2 -макроглобулин, гиалуроновая кислота, ГГТП, общий билирубин Fibrometer Возраст, пол, α 2 -макроглобулин, гиалуроновая кислота, тромбоциты, протромбиновый индекс, АСТ, мочевина
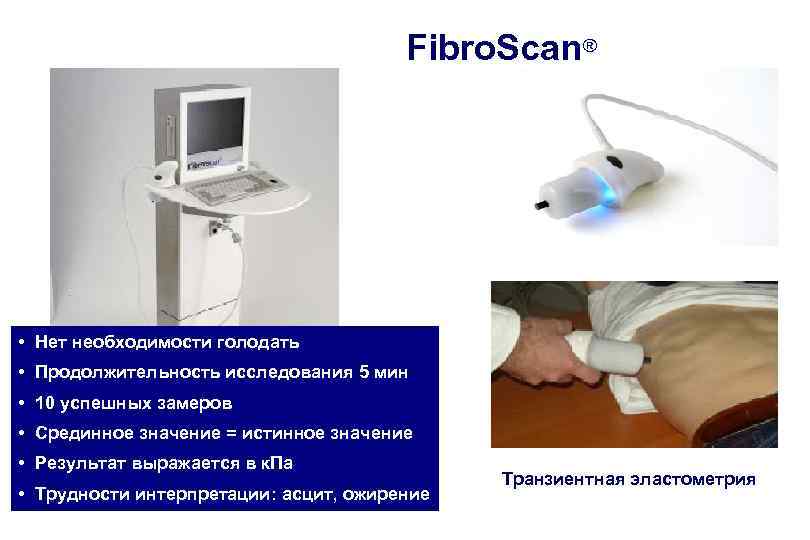 Fibro. Scan® • Нет необходимости голодать • Продолжительность исследования 5 мин • 10 успешных замеров • Срединное значение = истинное значение • Результат выражается в к. Па • Трудности интерпретации: асцит, ожирение Транзиентная эластометрия
Fibro. Scan® • Нет необходимости голодать • Продолжительность исследования 5 мин • 10 успешных замеров • Срединное значение = истинное значение • Результат выражается в к. Па • Трудности интерпретации: асцит, ожирение Транзиентная эластометрия
 Транзиентная эластометрия при хроническом гепатите Эластичность 7, 7 к. Па F 2 по METAVIR Хронический гепатит С Порто-портальные септы
Транзиентная эластометрия при хроническом гепатите Эластичность 7, 7 к. Па F 2 по METAVIR Хронический гепатит С Порто-портальные септы
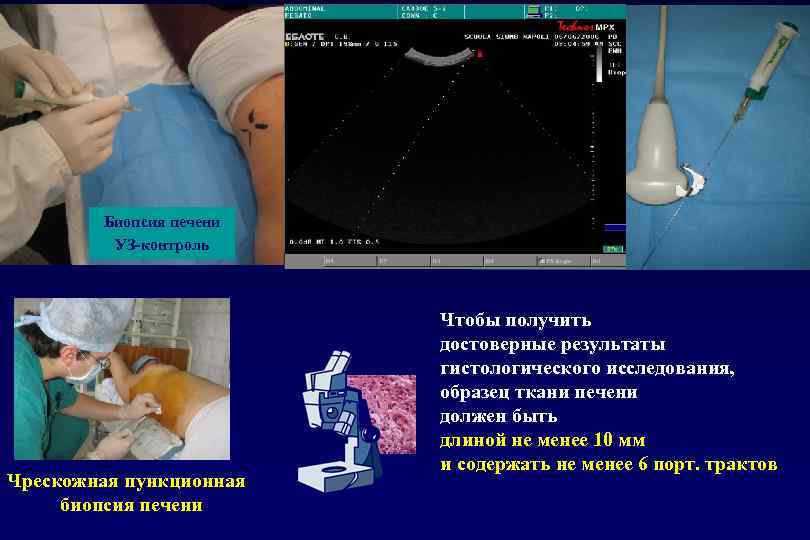 Биопсия печени УЗ-контроль Чрескожная пункционная биопсия печени Чтобы получить достоверные результаты гистологического исследования, образец ткани печени должен быть длиной не менее 10 мм и содержать не менее 6 порт. трактов
Биопсия печени УЗ-контроль Чрескожная пункционная биопсия печени Чтобы получить достоверные результаты гистологического исследования, образец ткани печени должен быть длиной не менее 10 мм и содержать не менее 6 порт. трактов
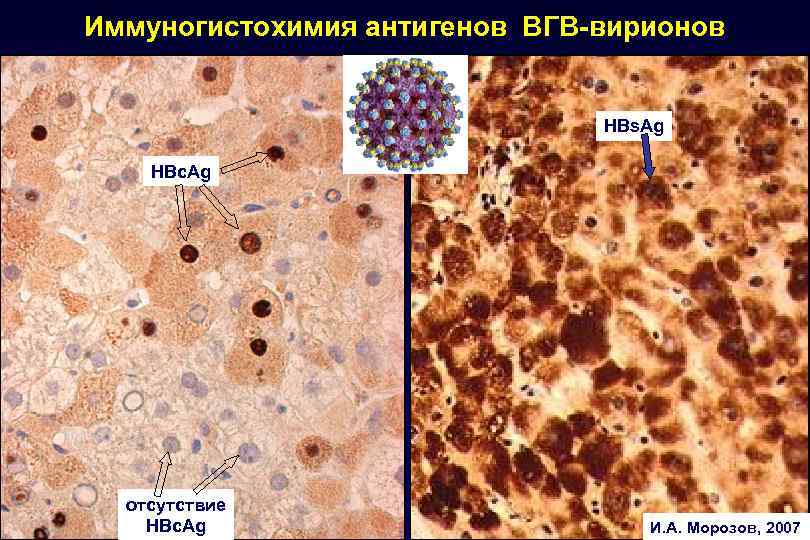 Иммуногистохимия антигенов ВГВ-вирионов HBs. Ag HBc. Ag отсутствие HBc. Ag И. А. Морозов, 2007
Иммуногистохимия антигенов ВГВ-вирионов HBs. Ag HBc. Ag отсутствие HBc. Ag И. А. Морозов, 2007
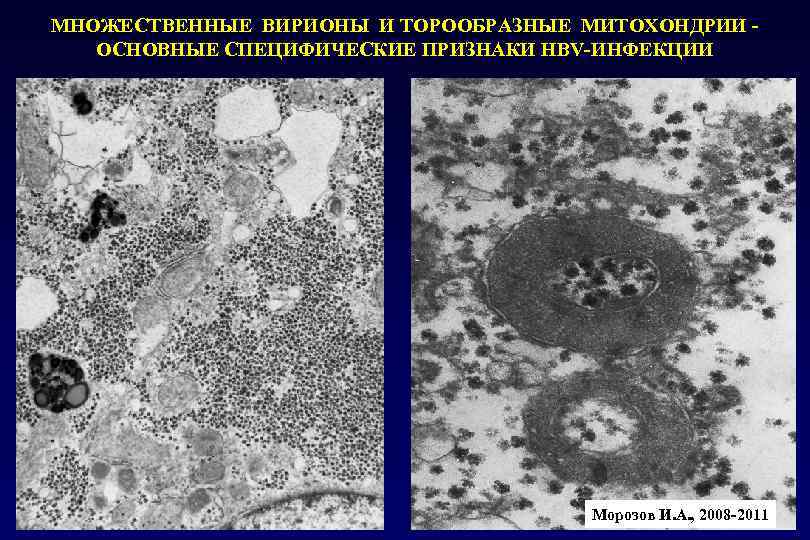 МНОЖЕСТВЕННЫЕ ВИРИОНЫ И ТОРООБРАЗНЫЕ МИТОХОНДРИИ - ОСНОВНЫЕ СПЕЦИФИЧЕСКИЕ ПРИЗНАКИ HBV-ИНФЕКЦИИ Морозов И. А. , 2008 -2011
МНОЖЕСТВЕННЫЕ ВИРИОНЫ И ТОРООБРАЗНЫЕ МИТОХОНДРИИ - ОСНОВНЫЕ СПЕЦИФИЧЕСКИЕ ПРИЗНАКИ HBV-ИНФЕКЦИИ Морозов И. А. , 2008 -2011
 Хронический вирусный гепатит В
Хронический вирусный гепатит В
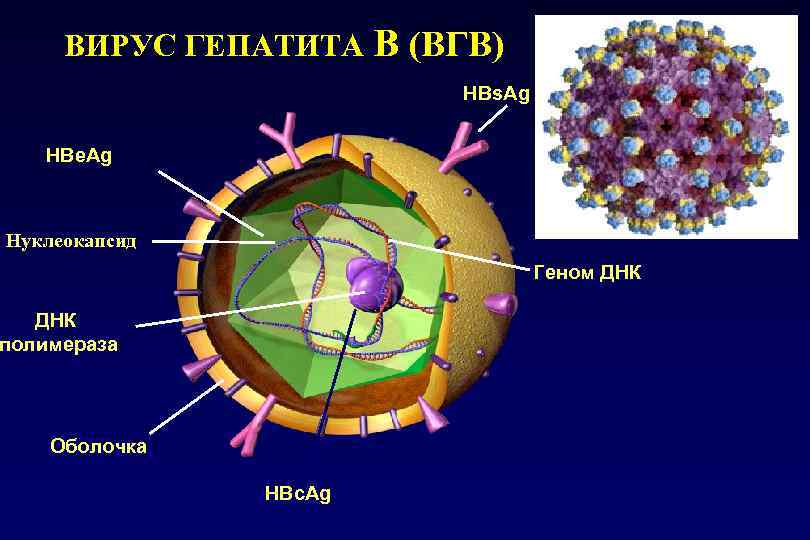 ВИРУС ГЕПАТИТА В (ВГВ) HBs. Ag HBе. Ag Нуклеокапсид Геном ДНК полимераза Оболочка HBс. Ag
ВИРУС ГЕПАТИТА В (ВГВ) HBs. Ag HBе. Ag Нуклеокапсид Геном ДНК полимераза Оболочка HBс. Ag
 Характеристика вирусагепатита В В Характеристика вируса гепатита Семейство Hepadnaviridae • двухцепочечная ДНК • 3200 нуклеотидов • 4 гена (S, C, P, X) • 42 нм (40 -48 нм) • 10 генотипов A-J 150 субтипов • Т½ - 24 ч • синтез – 1011 вирионов/сут
Характеристика вирусагепатита В В Характеристика вируса гепатита Семейство Hepadnaviridae • двухцепочечная ДНК • 3200 нуклеотидов • 4 гена (S, C, P, X) • 42 нм (40 -48 нм) • 10 генотипов A-J 150 субтипов • Т½ - 24 ч • синтез – 1011 вирионов/сут
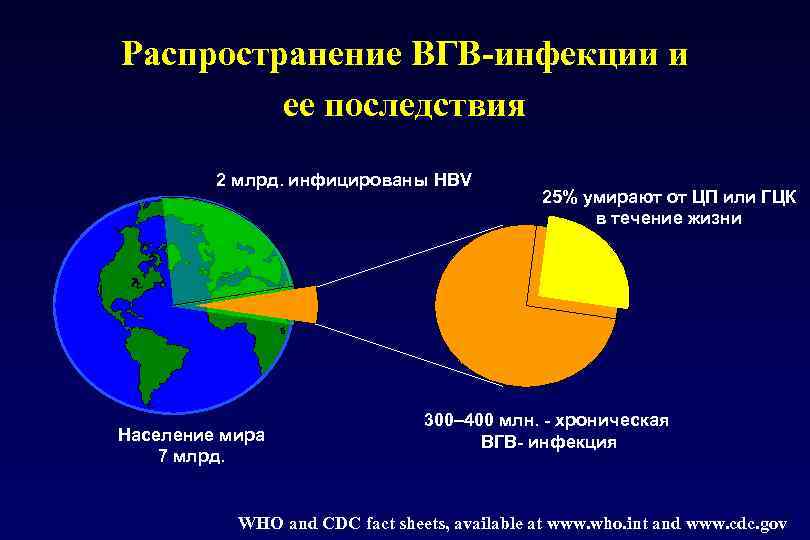 Распространение ВГВ-инфекции и ее последствия 2 млрд. инфицированы HBV Население мира 7 млрд. 25% умирают от ЦП или ГЦК в течение жизни 300– 400 млн. - хроническая ВГВ- инфекция WHO and CDC fact sheets, available at www. who. int and www. cdc. gov
Распространение ВГВ-инфекции и ее последствия 2 млрд. инфицированы HBV Население мира 7 млрд. 25% умирают от ЦП или ГЦК в течение жизни 300– 400 млн. - хроническая ВГВ- инфекция WHO and CDC fact sheets, available at www. who. int and www. cdc. gov
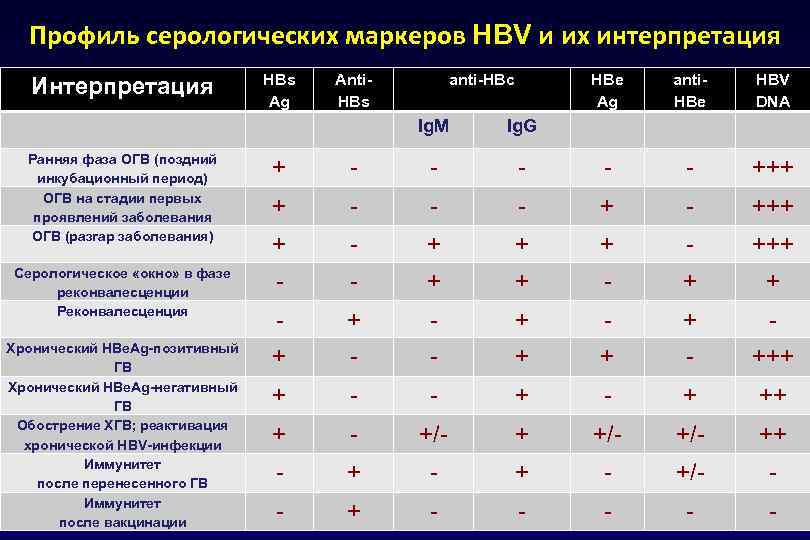 Профиль серологических маркеров HBV и их интерпретация Интерпретация HBs Ag Anti. HBs anti-HBc HBe Ag Ig. M anti. HBe HBV DNA Ig. G Ранняя фаза ОГВ (поздний инкубационный период) ОГВ на стадии первых проявлений заболевания ОГВ (разгар заболевания) + - - - +++ + - + + + - +++ Серологическое «окно» в фазе реконвалесценции Реконвалесценция - - + + - + - + - Хронический HBe. Ag-позитивный ГВ Хронический HBe. Ag-негативный ГВ Обострение ХГВ; реактивация хронической HBV-инфекции Иммунитет после перенесенного ГВ Иммунитет после вакцинации + - - + + - +++ + - - + ++ + - +/- +/- ++ - + - +/- - - + - - -
Профиль серологических маркеров HBV и их интерпретация Интерпретация HBs Ag Anti. HBs anti-HBc HBe Ag Ig. M anti. HBe HBV DNA Ig. G Ранняя фаза ОГВ (поздний инкубационный период) ОГВ на стадии первых проявлений заболевания ОГВ (разгар заболевания) + - - - +++ + - + + + - +++ Серологическое «окно» в фазе реконвалесценции Реконвалесценция - - + + - + - + - Хронический HBe. Ag-позитивный ГВ Хронический HBe. Ag-негативный ГВ Обострение ХГВ; реактивация хронической HBV-инфекции Иммунитет после перенесенного ГВ Иммунитет после вакцинации + - - + + - +++ + - - + ++ + - +/- +/- ++ - + - +/- - - + - - -
 Клинические формы HBV-инфекции ● острый самолимитирующийся ГВ (ОГВ) ● хронический гепатит В (ХГВ) ● «носительство» HBs. Ag в отсутствие выраженных симптомов гепатита ~ хронический гепатит В низкой активности с нормальным уровнем трансаминаз
Клинические формы HBV-инфекции ● острый самолимитирующийся ГВ (ОГВ) ● хронический гепатит В (ХГВ) ● «носительство» HBs. Ag в отсутствие выраженных симптомов гепатита ~ хронический гепатит В низкой активности с нормальным уровнем трансаминаз
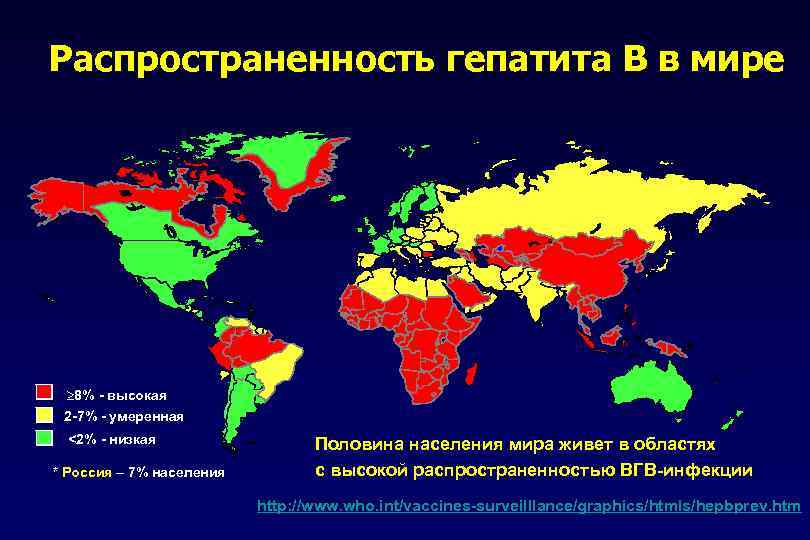 Распространенность гепатита В в мире ³ 8% - высокая 2 -7% - умеренная <2% - низкая * Россия – 7% населения Половина населения мира живет в областях с высокой распространенностью ВГВ-инфекции http: //www. who. int/vaccines-surveilllance/graphics/htmls/hepbprev. htm
Распространенность гепатита В в мире ³ 8% - высокая 2 -7% - умеренная <2% - низкая * Россия – 7% населения Половина населения мира живет в областях с высокой распространенностью ВГВ-инфекции http: //www. who. int/vaccines-surveilllance/graphics/htmls/hepbprev. htm
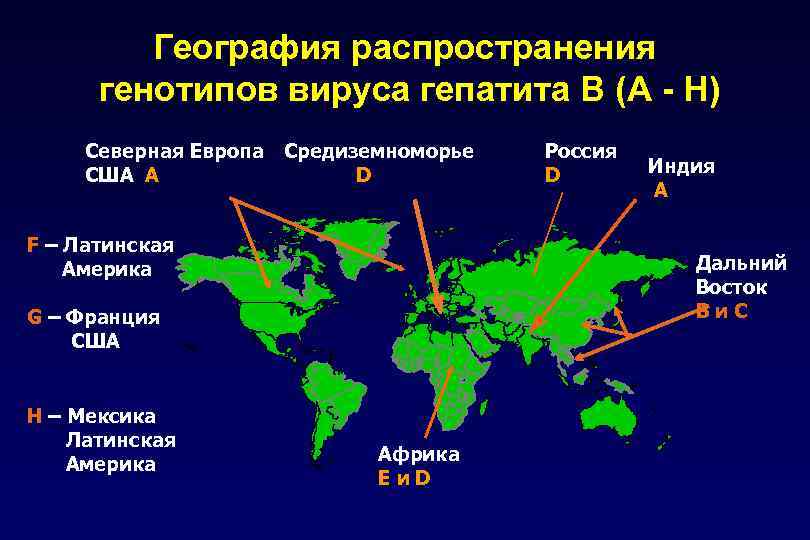 География распространения генотипов вируса гепатита В (A - H) Северная Европа США A Средиземноморье D F – Латинская Америка Индия A Дальний Восток Bи. C G – Франция США H – Мексика Латинская Америка Россия D Африка Eи. D
География распространения генотипов вируса гепатита В (A - H) Северная Европа США A Средиземноморье D F – Латинская Америка Индия A Дальний Восток Bи. C G – Франция США H – Мексика Латинская Америка Россия D Африка Eи. D
 Генотипы ВГВ Различия между генотипами >8% D. Glebe 2007 Различия между субтипами >4% D. Glebe 2007 Коинфекция разными генотипами От 4, 4% (Япония) До 17, 5% (Зап. Африка) H. Kato et al. , 2003 C. M. Olinger et al. , 2006 Рекомбинация между генотипами До 16% (22/136) между генотипами В и С в Китае K. Luo et al. , 2004 Клиническое значение Генотип С связан с более тяжелым заболеванием печени по сравнению с генотипами B и D Генотип А связан с HBe. Ag+, ответ на ИФН; генотип D – с анти-НВе+ T. N. Duonq et al. , 2004 H. B. Kong et al. , 2007 P. Halfon et al. , 2006
Генотипы ВГВ Различия между генотипами >8% D. Glebe 2007 Различия между субтипами >4% D. Glebe 2007 Коинфекция разными генотипами От 4, 4% (Япония) До 17, 5% (Зап. Африка) H. Kato et al. , 2003 C. M. Olinger et al. , 2006 Рекомбинация между генотипами До 16% (22/136) между генотипами В и С в Китае K. Luo et al. , 2004 Клиническое значение Генотип С связан с более тяжелым заболеванием печени по сравнению с генотипами B и D Генотип А связан с HBe. Ag+, ответ на ИФН; генотип D – с анти-НВе+ T. N. Duonq et al. , 2004 H. B. Kong et al. , 2007 P. Halfon et al. , 2006
 Динамика заболеваемости хроническими гепатитами В и С в России Заболеваемость ХГВ превзошла показатель заболеваемости ОГВ более чем в 6 раз, а заболеваемость ХГС и ОГС различались почти в 20 раз
Динамика заболеваемости хроническими гепатитами В и С в России Заболеваемость ХГВ превзошла показатель заболеваемости ОГВ более чем в 6 раз, а заболеваемость ХГС и ОГС различались почти в 20 раз
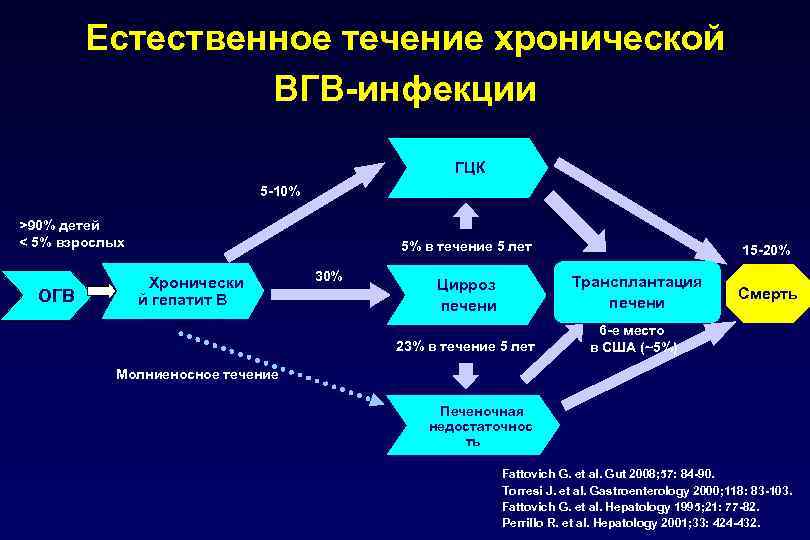 Естественное течение хронической ВГВ-инфекции ГЦК 5 -10% >90% детей < 5% взрослых ОГВ 5% в течение 5 лет 30% 15 -20% Цирроз печени Трансплантация печени 23% в течение 5 лет Хронически й гепатит В 6 -е место в США (~5%) Смерть Молниеносное течение Печеночная недостаточнос ть Fattovich G. et al. Gut 2008; 57: 84 -90. Torresi J. et al. Gastroenterology 2000; 118: 83 -103. Fattovich G. et al. Hepatology 1995; 21: 77 -82. Perrillo R. et al. Hepatology 2001; 33: 424 -432.
Естественное течение хронической ВГВ-инфекции ГЦК 5 -10% >90% детей < 5% взрослых ОГВ 5% в течение 5 лет 30% 15 -20% Цирроз печени Трансплантация печени 23% в течение 5 лет Хронически й гепатит В 6 -е место в США (~5%) Смерть Молниеносное течение Печеночная недостаточнос ть Fattovich G. et al. Gut 2008; 57: 84 -90. Torresi J. et al. Gastroenterology 2000; 118: 83 -103. Fattovich G. et al. Hepatology 1995; 21: 77 -82. Perrillo R. et al. Hepatology 2001; 33: 424 -432.
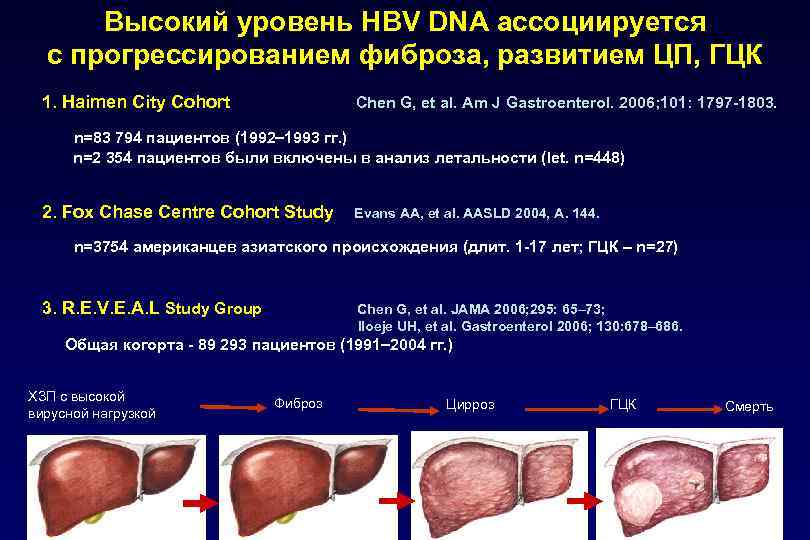 Высокий уровень HBV DNA ассоциируется с прогрессированием фиброза, развитием ЦП, ГЦК 1. Haimen City Cohort Chen G, et al. Am J Gastroenterol. 2006; 101: 1797 -1803. n=83 794 пациентов (1992 1993 гг. ) n=2 354 пациентов были включены в анализ летальности (let. n=448) 2. Fox Chase Centre Cohort Study Evans AA, et al. AASLD 2004, А. 144. n=3754 американцев азиатского происхождения (длит. 1 -17 лет; ГЦК – n=27) 3. R. E. V. E. A. L Study Group Chen G, et al. JAMA 2006; 295: 65– 73; Iloeje UH, et al. Gastroenterol 2006; 130: 678– 686. Общая когорта - 89 293 пациентов (1991 2004 гг. ) ХЗП с высокой вирусной нагрузкой Фиброз ГЦК Цирроз ГЦК Смерть
Высокий уровень HBV DNA ассоциируется с прогрессированием фиброза, развитием ЦП, ГЦК 1. Haimen City Cohort Chen G, et al. Am J Gastroenterol. 2006; 101: 1797 -1803. n=83 794 пациентов (1992 1993 гг. ) n=2 354 пациентов были включены в анализ летальности (let. n=448) 2. Fox Chase Centre Cohort Study Evans AA, et al. AASLD 2004, А. 144. n=3754 американцев азиатского происхождения (длит. 1 -17 лет; ГЦК – n=27) 3. R. E. V. E. A. L Study Group Chen G, et al. JAMA 2006; 295: 65– 73; Iloeje UH, et al. Gastroenterol 2006; 130: 678– 686. Общая когорта - 89 293 пациентов (1991 2004 гг. ) ХЗП с высокой вирусной нагрузкой Фиброз ГЦК Цирроз ГЦК Смерть
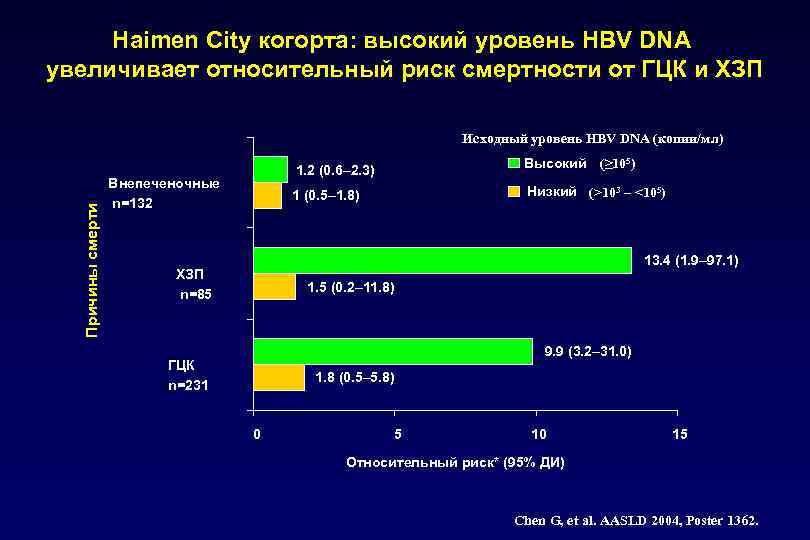 Haimen City когорта: высокий уровень HBV DNA увеличивает относительный риск смертности от ГЦК и ХЗП Причины смерти Исходный уровень HBV DNA (копии/мл) 1. 2 (0. 6– 2. 3) 1 (0. 5– 1. 8) Внепеченочные n=132 Высокий (≥ 105) Низкий (>103 – <105) 13. 4 (1. 9– 97. 1) ХЗП n=85 1. 5 (0. 2– 11. 8) 9. 9 (3. 2– 31. 0) ГЦК n=231 1. 8 (0. 5– 5. 8) 0 5 10 15 Относительный риск* (95% ДИ) Chen G, et al. AASLD 2004, Poster 1362.
Haimen City когорта: высокий уровень HBV DNA увеличивает относительный риск смертности от ГЦК и ХЗП Причины смерти Исходный уровень HBV DNA (копии/мл) 1. 2 (0. 6– 2. 3) 1 (0. 5– 1. 8) Внепеченочные n=132 Высокий (≥ 105) Низкий (>103 – <105) 13. 4 (1. 9– 97. 1) ХЗП n=85 1. 5 (0. 2– 11. 8) 9. 9 (3. 2– 31. 0) ГЦК n=231 1. 8 (0. 5– 5. 8) 0 5 10 15 Относительный риск* (95% ДИ) Chen G, et al. AASLD 2004, Poster 1362.
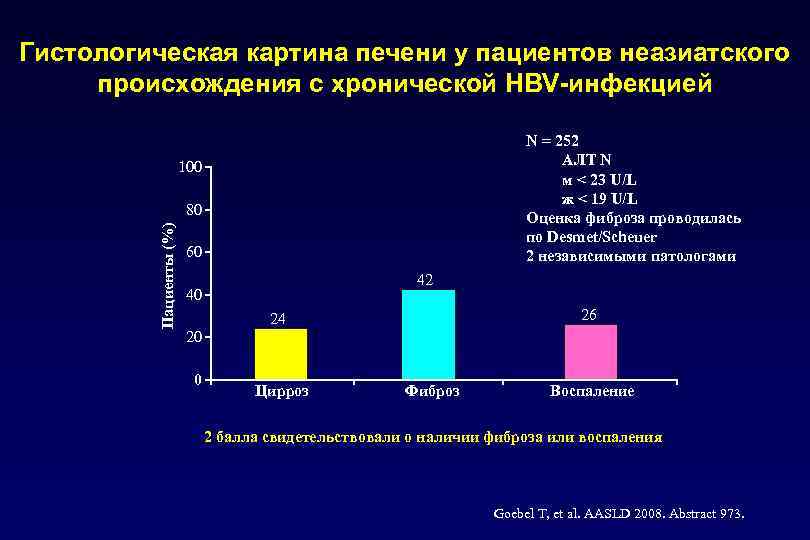 Гистологическая картина печени у пациентов неазиатского происхождения с хронической HBV-инфекцией N = 252 АЛТ N м < 23 U/L ж < 19 U/L Оценка фиброза проводилась по Desmet/Scheuer 2 независимыми патологами 100 Пациенты (%) 80 60 42 40 26 24 20 0 Цирроз Фиброз Воспаление 2 балла свидетельствовали о наличии фиброза или воспаления Goebel T, et al. AASLD 2008. Abstract 973.
Гистологическая картина печени у пациентов неазиатского происхождения с хронической HBV-инфекцией N = 252 АЛТ N м < 23 U/L ж < 19 U/L Оценка фиброза проводилась по Desmet/Scheuer 2 независимыми патологами 100 Пациенты (%) 80 60 42 40 26 24 20 0 Цирроз Фиброз Воспаление 2 балла свидетельствовали о наличии фиброза или воспаления Goebel T, et al. AASLD 2008. Abstract 973.
 Естественное течение хронического гепатита В HBe. Ag- позитивный HBe. Ag-негативный/ анти. HBe-позитивный ДНК HBV АЛТ Фазы хронической Репликативная, или фаза Клиренс HBV- иммунной толерантности HBe. Ag инфекции Фаза низкого уровня Реактивация HBV репликации Оптимальное время для лечения Brunetto MR J Hepatol 1991
Естественное течение хронического гепатита В HBe. Ag- позитивный HBe. Ag-негативный/ анти. HBe-позитивный ДНК HBV АЛТ Фазы хронической Репликативная, или фаза Клиренс HBV- иммунной толерантности HBe. Ag инфекции Фаза низкого уровня Реактивация HBV репликации Оптимальное время для лечения Brunetto MR J Hepatol 1991
 Фазы хронической HBV-инфекции Фаза HBVинфекции HBe. Ag АЛТ HBV DNA Степень воспаления и фиброза Лечение показано Иммунная толерантность + до ВГН ≥ 10 млн. МЕ/мл (оч. высокий) От отсутствия до минимальной Нет Иммунная активность + / - > 20 000 МЕ/мл (высокий) От умеренной до выраженной Да Неактивная фаза - до ВГН < 2000 МЕ/мл (низкий) От отсутствия до умеренной Нет Клиренс HBe. Ag - до ВГН < 2000 МЕ/мл (низкий) От отсутствия до умеренной Нет
Фазы хронической HBV-инфекции Фаза HBVинфекции HBe. Ag АЛТ HBV DNA Степень воспаления и фиброза Лечение показано Иммунная толерантность + до ВГН ≥ 10 млн. МЕ/мл (оч. высокий) От отсутствия до минимальной Нет Иммунная активность + / - > 20 000 МЕ/мл (высокий) От умеренной до выраженной Да Неактивная фаза - до ВГН < 2000 МЕ/мл (низкий) От отсутствия до умеренной Нет Клиренс HBe. Ag - до ВГН < 2000 МЕ/мл (низкий) От отсутствия до умеренной Нет
 Спонтанная HBe. Ag и HBs. Ag сероконверсия в разные фазы HBV-инфекции HBe. Ag-позитивный ХГВ: частота HBe. Ag сероконверсии – 8%-15% в год (G. Fattovich, Semin Liver Dis 2003) HBe. Ag-негативный ХГВ: спонтанная элиминация HBs. Ag – 0, 5% в год (S. Hadziyannis, Hepatology 2001; G. Papathedoridis, J Hepatol 2001; YS Hsu, Hepatology 2002)
Спонтанная HBe. Ag и HBs. Ag сероконверсия в разные фазы HBV-инфекции HBe. Ag-позитивный ХГВ: частота HBe. Ag сероконверсии – 8%-15% в год (G. Fattovich, Semin Liver Dis 2003) HBe. Ag-негативный ХГВ: спонтанная элиминация HBs. Ag – 0, 5% в год (S. Hadziyannis, Hepatology 2001; G. Papathedoridis, J Hepatol 2001; YS Hsu, Hepatology 2002)
 Латентная (occult, silent) HBV-инфекция «присутствие DNA HBV в печени пациентов (независимо от наличия DNA HBV в крови), в сыворотке крови которых доступными методами не определяется HBs. Ag» EASL, 2008 Raimondo G. Navarra G. , Mondello S. et al. Occult hepatitis B virus in liver tissue of individuals without hepatic disease Hepatology 2008; 48: 743 -746.
Латентная (occult, silent) HBV-инфекция «присутствие DNA HBV в печени пациентов (независимо от наличия DNA HBV в крови), в сыворотке крови которых доступными методами не определяется HBs. Ag» EASL, 2008 Raimondo G. Navarra G. , Mondello S. et al. Occult hepatitis B virus in liver tissue of individuals without hepatic disease Hepatology 2008; 48: 743 -746.
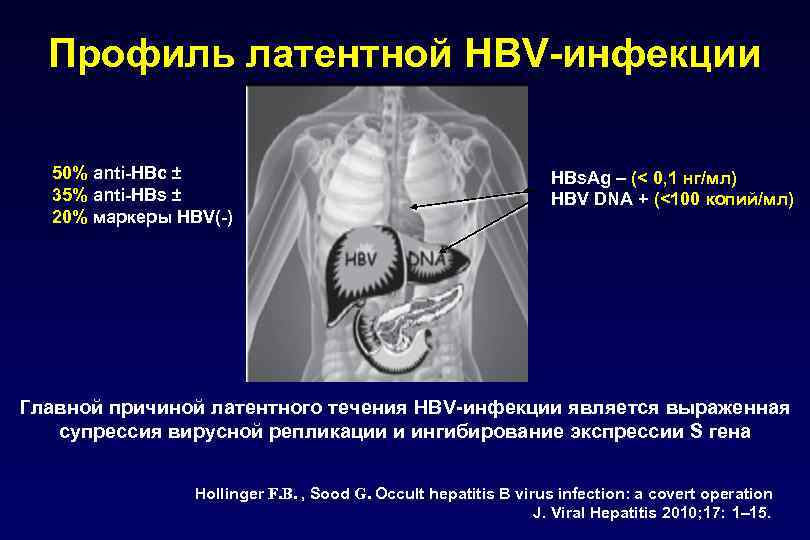 Профиль латентной HBV-инфекции 50% аnti-HBc ± 35% anti-HBs ± 20% маркеры HBV(-) HBs. Ag – (< 0, 1 нг/мл) HBV DNA + (<100 копий/мл) Главной причиной латентного течения HBV-инфекции является выраженная супрессия вирусной репликации и ингибирование экспрессии S гена Hollinger F. B. , Sood G. Occult hepatitis B virus infection: a covert operation J. Viral Hepatitis 2010; 17: 1– 15.
Профиль латентной HBV-инфекции 50% аnti-HBc ± 35% anti-HBs ± 20% маркеры HBV(-) HBs. Ag – (< 0, 1 нг/мл) HBV DNA + (<100 копий/мл) Главной причиной латентного течения HBV-инфекции является выраженная супрессия вирусной репликации и ингибирование экспрессии S гена Hollinger F. B. , Sood G. Occult hepatitis B virus infection: a covert operation J. Viral Hepatitis 2010; 17: 1– 15.
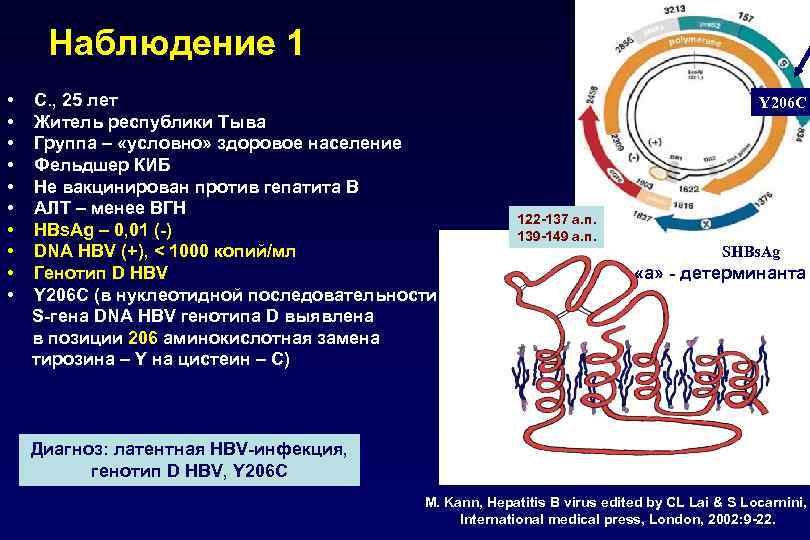 Наблюдение 1 • • • С. , 25 лет Житель республики Тыва Группа – «условно» здоровое население Фельдшер КИБ Не вакцинирован против гепатита В АЛТ – менее ВГН HBs. Ag – 0, 01 (-) DNA HBV (+), < 1000 копий/мл Генотип D HBV Y 206 C (в нуклеотидной последовательности S-гена DNA HBV генотипа D выявлена в позиции 206 аминокислотная замена тирозина – Y на циcтеин – C) Y 206 C 122 -137 а. п. 139 -149 а. п. SHBs. Ag «а» - детерминанта Диагноз: латентная HBV-инфекция, генотип D HBV, Y 206 C M. Kann, Hepatitis B virus edited by CL Lai & S Locarnini, International medical press, London, 2002: 9 -22.
Наблюдение 1 • • • С. , 25 лет Житель республики Тыва Группа – «условно» здоровое население Фельдшер КИБ Не вакцинирован против гепатита В АЛТ – менее ВГН HBs. Ag – 0, 01 (-) DNA HBV (+), < 1000 копий/мл Генотип D HBV Y 206 C (в нуклеотидной последовательности S-гена DNA HBV генотипа D выявлена в позиции 206 аминокислотная замена тирозина – Y на циcтеин – C) Y 206 C 122 -137 а. п. 139 -149 а. п. SHBs. Ag «а» - детерминанта Диагноз: латентная HBV-инфекция, генотип D HBV, Y 206 C M. Kann, Hepatitis B virus edited by CL Lai & S Locarnini, International medical press, London, 2002: 9 -22.
 Наблюдение 2 • • Пациентка М. , 62 лет Жалобы – тянущие боли в правом подреберье На догоспитальном этапе АЛТ – 2 -3 ВГН ХГ н/э, гипертоническая болезнь, сахарный диабет 2 • • Госпитализация – неалкогольный стеатогепатит? ИМТ – 27 кг/м 2 Печень – незначительно увеличена АЛТ – 1, 5 ВГН Anti-HCV (-), HBs. Ag (-), anti-HBc (+), HCV RNA(-), HBV DNA (-) Биопсия печени – стеатогепатит А 1, ИФ – 1 балл НАСГ Диагноз: неалкогольный стеатогепатит
Наблюдение 2 • • Пациентка М. , 62 лет Жалобы – тянущие боли в правом подреберье На догоспитальном этапе АЛТ – 2 -3 ВГН ХГ н/э, гипертоническая болезнь, сахарный диабет 2 • • Госпитализация – неалкогольный стеатогепатит? ИМТ – 27 кг/м 2 Печень – незначительно увеличена АЛТ – 1, 5 ВГН Anti-HCV (-), HBs. Ag (-), anti-HBc (+), HCV RNA(-), HBV DNA (-) Биопсия печени – стеатогепатит А 1, ИФ – 1 балл НАСГ Диагноз: неалкогольный стеатогепатит
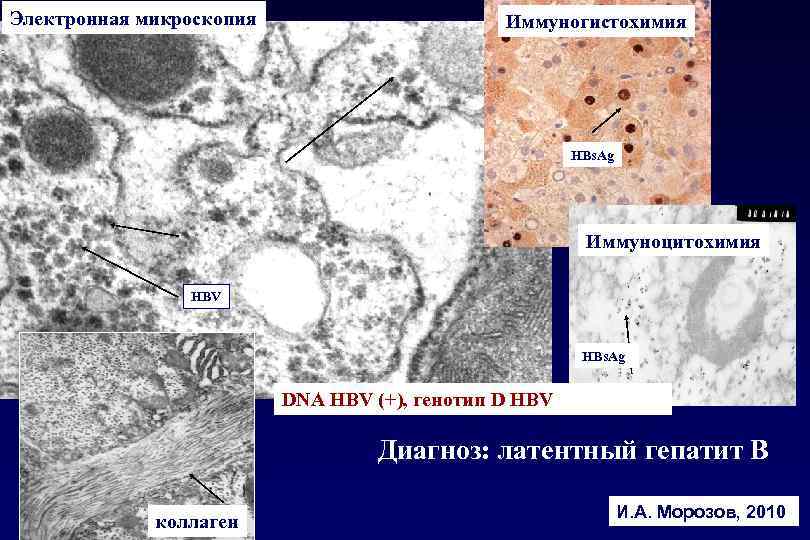 Электронная микроскопия Иммуногистохимия HBs. Ag Иммуноцитохимия HBV HBs. Ag DNA HBV (+), генотип D HBV Диагноз: латентный гепатит В коллаген И. А. Морозов, 2010
Электронная микроскопия Иммуногистохимия HBs. Ag Иммуноцитохимия HBV HBs. Ag DNA HBV (+), генотип D HBV Диагноз: латентный гепатит В коллаген И. А. Морозов, 2010
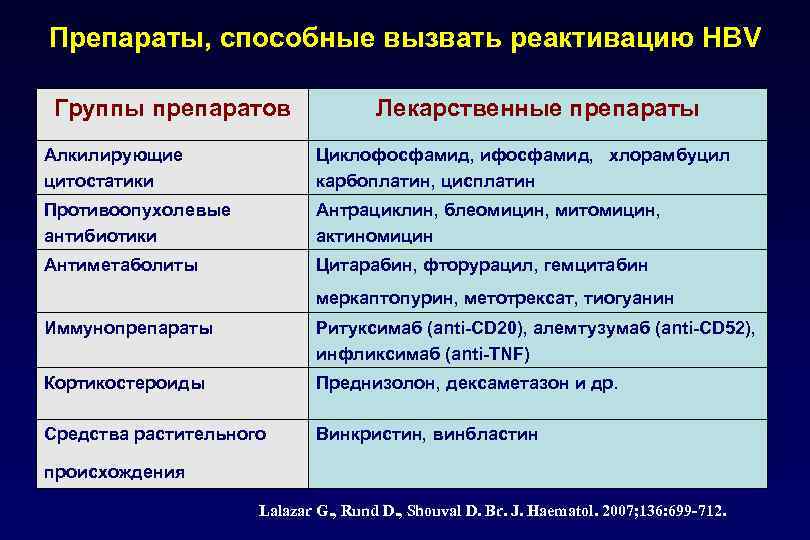 Препараты, способные вызвать реактивацию HBV Группы препаратов Лекарственные препараты Алкилирующие цитостатики Циклофосфамид, ифосфамид, хлорамбуцил карбоплатин, цисплатин Противоопухолевые антибиотики Антрациклин, блеомицин, митомицин, актиномицин Антиметаболиты Цитарабин, фторурацил, гемцитабин меркаптопурин, метотрексат, тиогуанин Иммунопрепараты Ритуксимаб (anti-CD 20), алемтузумаб (anti-CD 52), инфликсимаб (anti-TNF) Кортикостероиды Преднизолон, дексаметазон и др. Средства растительного Винкристин, винбластин происхождения Lalazar G. , Rund D. , Shouval D. Br. J. Haematol. 2007; 136: 699 -712.
Препараты, способные вызвать реактивацию HBV Группы препаратов Лекарственные препараты Алкилирующие цитостатики Циклофосфамид, ифосфамид, хлорамбуцил карбоплатин, цисплатин Противоопухолевые антибиотики Антрациклин, блеомицин, митомицин, актиномицин Антиметаболиты Цитарабин, фторурацил, гемцитабин меркаптопурин, метотрексат, тиогуанин Иммунопрепараты Ритуксимаб (anti-CD 20), алемтузумаб (anti-CD 52), инфликсимаб (anti-TNF) Кортикостероиды Преднизолон, дексаметазон и др. Средства растительного Винкристин, винбластин происхождения Lalazar G. , Rund D. , Shouval D. Br. J. Haematol. 2007; 136: 699 -712.
 Хронический гепатит дельта
Хронический гепатит дельта
 Марио Риззетто
Марио Риззетто
 «Новый антиген сначала считали маркером вируса гепатита B (HBV) и ввиду его замысловатого истинного характера, было возможно, что он умрет как еще один странный антигенный подтип HBV, как и многие другие, которые были описаны в 1970 -х годах. К счастью, вместо этого, сотрудничество, которое началась в 1978 году, между группой из Турина, национальным институтом здравоохранения и Джорджтаунским университетом США привело только спустя год ( 1979 г. ), к неожиданным и удивительным открытиям в вирусологии. Эксперименты на шимпанзе показали, что Дельта антиген не компонент HBV, а отдельный дефектный вирус, требующий вирус гепатита В для развития инфекции» Марио Риззетто
«Новый антиген сначала считали маркером вируса гепатита B (HBV) и ввиду его замысловатого истинного характера, было возможно, что он умрет как еще один странный антигенный подтип HBV, как и многие другие, которые были описаны в 1970 -х годах. К счастью, вместо этого, сотрудничество, которое началась в 1978 году, между группой из Турина, национальным институтом здравоохранения и Джорджтаунским университетом США привело только спустя год ( 1979 г. ), к неожиданным и удивительным открытиям в вирусологии. Эксперименты на шимпанзе показали, что Дельта антиген не компонент HBV, а отдельный дефектный вирус, требующий вирус гепатита В для развития инфекции» Марио Риззетто
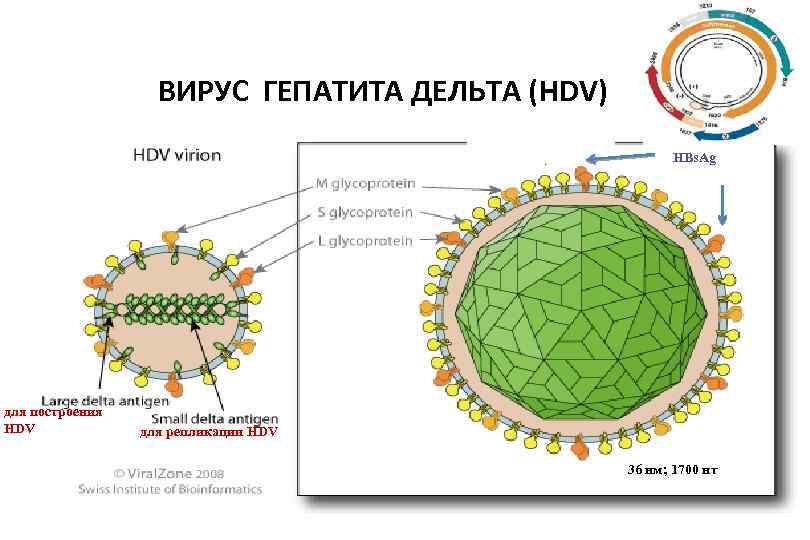 ВИРУС ГЕПАТИТА ДЕЛЬТА (HDV) HBs. Ag для построения HDV для репликации HDV 36 нм; 1700 нт
ВИРУС ГЕПАТИТА ДЕЛЬТА (HDV) HBs. Ag для построения HDV для репликации HDV 36 нм; 1700 нт
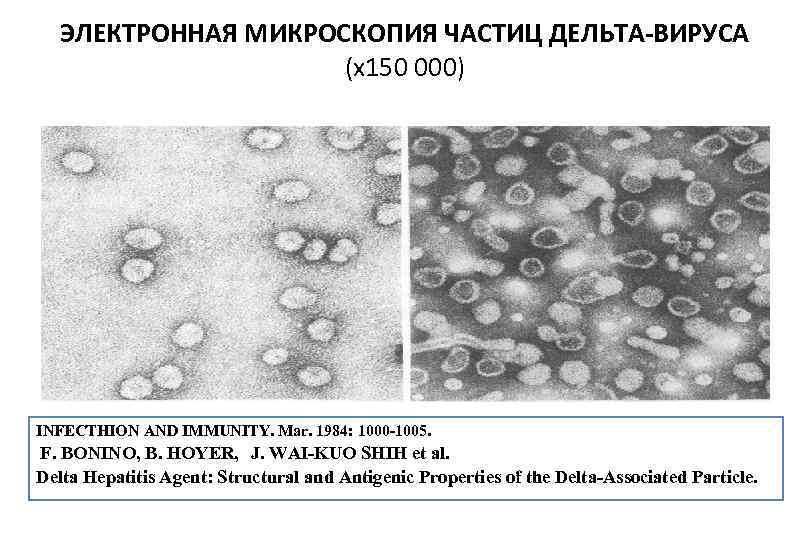 ЭЛЕКТРОННАЯ МИКРОСКОПИЯ ЧАСТИЦ ДЕЛЬТА-ВИРУСА (x 150 000) INFECTHION AND IMMUNITY. Mar. 1984: 1000 -1005. F. BONINO, B. HOYER, J. WAI-KUO SHIH et al. Delta Hepatitis Agent: Structural and Antigenic Properties of the Delta-Associated Particle.
ЭЛЕКТРОННАЯ МИКРОСКОПИЯ ЧАСТИЦ ДЕЛЬТА-ВИРУСА (x 150 000) INFECTHION AND IMMUNITY. Mar. 1984: 1000 -1005. F. BONINO, B. HOYER, J. WAI-KUO SHIH et al. Delta Hepatitis Agent: Structural and Antigenic Properties of the Delta-Associated Particle.
 Вирус гепатита дельта и вироиды HDV Вироиды (Т. О. Diener, 1971) Сходства 1. Геном представлен кольцевой, одноцепочечной РНК HDV (-) одноцепочечной РНК (300 -400 1700 нуклеотидов) 2. Не имеет специфического 2. Не имеют специфического фермента репликации (использует РНК полимеразу II (использует РНК полимеразу клетки человека) клетки растений) 3. Геномные и антигеномные нити 3. РНК содержат рибозим (репликация HDV) Отличия 1. РНК (только 1 из 6 ORF) кодирует белок HDAg. 2. Имеет белковую оболочку (HDAg) 3. Репликация происходит с участием вируса-помощника (HBV). 4. Вызывает заболевание у человека (поражение печени). 1. РНК не кодирует собственных белков 2. Не имеют белковой оболочки 3. Реплицируются самостоятельно, без участия вируса-помощника. 4. Вызывают болезни растений
Вирус гепатита дельта и вироиды HDV Вироиды (Т. О. Diener, 1971) Сходства 1. Геном представлен кольцевой, одноцепочечной РНК HDV (-) одноцепочечной РНК (300 -400 1700 нуклеотидов) 2. Не имеет специфического 2. Не имеют специфического фермента репликации (использует РНК полимеразу II (использует РНК полимеразу клетки человека) клетки растений) 3. Геномные и антигеномные нити 3. РНК содержат рибозим (репликация HDV) Отличия 1. РНК (только 1 из 6 ORF) кодирует белок HDAg. 2. Имеет белковую оболочку (HDAg) 3. Репликация происходит с участием вируса-помощника (HBV). 4. Вызывает заболевание у человека (поражение печени). 1. РНК не кодирует собственных белков 2. Не имеют белковой оболочки 3. Реплицируются самостоятельно, без участия вируса-помощника. 4. Вызывают болезни растений
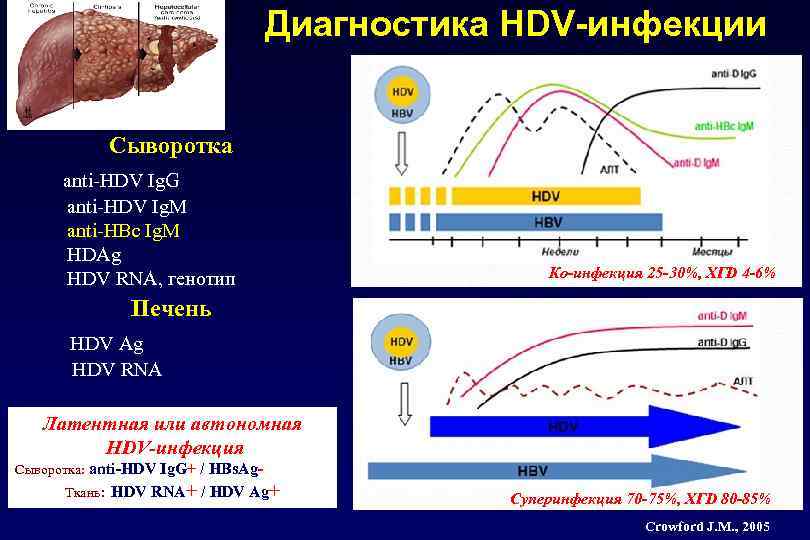 Диагностика HDV-инфекции Сыворотка anti-HDV Ig. G anti-HDV Ig. M anti-HBc Ig. M HDAg HDV RNA, генотип Ко-инфекция 25 -30%, ХГD 4 -6% Печень HDV Ag HDV RNA Латентная или автономная HDV-инфекция Сыворотка: anti-HDV Ig. G+ / HBs. Ag. Ткань: HDV RNA+ / HDV Ag+ Суперинфекция 70 -75%, ХГD 80 -85% Crowford J. M. , 2005
Диагностика HDV-инфекции Сыворотка anti-HDV Ig. G anti-HDV Ig. M anti-HBc Ig. M HDAg HDV RNA, генотип Ко-инфекция 25 -30%, ХГD 4 -6% Печень HDV Ag HDV RNA Латентная или автономная HDV-инфекция Сыворотка: anti-HDV Ig. G+ / HBs. Ag. Ткань: HDV RNA+ / HDV Ag+ Суперинфекция 70 -75%, ХГD 80 -85% Crowford J. M. , 2005
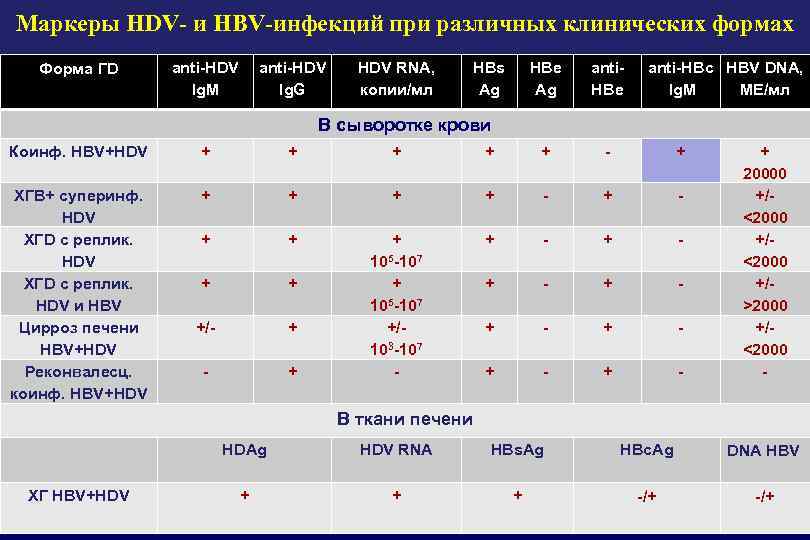 Маркеры HDV- и HBV-инфекций при различных клинических формах Форма ГD anti-HDV Ig. M anti-HDV Ig. G HDV RNA, копии/мл HBs Ag HВe Ag anti. HBe anti-HBc HBV DNA, Ig. M МЕ/мл В сыворотке крови Коинф. HBV+HDV + + + - + ХГВ+ суперинф. HDV ХГD c реплик. HDV ХГD с реплик. HDV и HBV Цирроз печени HBV+HDV Реконвалесц. коинф. HBV+HDV + + - + - + + + - +/- + + - - + + 105 -107 +/103 -107 - + - + 20000 +/<2000 +/>2000 +/<2000 - В ткани печени HDAg ХГ HBV+HDV RNA HBs. Ag HBc. Ag DNA HBV + + + -/+
Маркеры HDV- и HBV-инфекций при различных клинических формах Форма ГD anti-HDV Ig. M anti-HDV Ig. G HDV RNA, копии/мл HBs Ag HВe Ag anti. HBe anti-HBc HBV DNA, Ig. M МЕ/мл В сыворотке крови Коинф. HBV+HDV + + + - + ХГВ+ суперинф. HDV ХГD c реплик. HDV ХГD с реплик. HDV и HBV Цирроз печени HBV+HDV Реконвалесц. коинф. HBV+HDV + + - + - + + + - +/- + + - - + + 105 -107 +/103 -107 - + - + 20000 +/<2000 +/>2000 +/<2000 - В ткани печени HDAg ХГ HBV+HDV RNA HBs. Ag HBc. Ag DNA HBV + + + -/+
 «Санта-Марта» гепатит был признан, как необычно тяжелый тип гепатита, регистрируемый на севере Колумбии, начиная с 30 -х годов ХХ века
«Санта-Марта» гепатит был признан, как необычно тяжелый тип гепатита, регистрируемый на севере Колумбии, начиная с 30 -х годов ХХ века
 Вирусы гепатита В и гепатита дельта, как причина вспышки фульминантного гепатита (черная лихорадка Лабреа) в западной части бразильской Амазонии
Вирусы гепатита В и гепатита дельта, как причина вспышки фульминантного гепатита (черная лихорадка Лабреа) в западной части бразильской Амазонии
 Гепатит дельта в Амазонии …Гепатит дельта может быстро распространяться, возможно, через контакт с инфицированными выделениями из открытых повреждений кожи, при обмене игл или шипов для удаления личинок из кожи, или, возможно, существует механическая передача через неизвестных насекомых…
Гепатит дельта в Амазонии …Гепатит дельта может быстро распространяться, возможно, через контакт с инфицированными выделениями из открытых повреждений кожи, при обмене игл или шипов для удаления личинок из кожи, или, возможно, существует механическая передача через неизвестных насекомых…
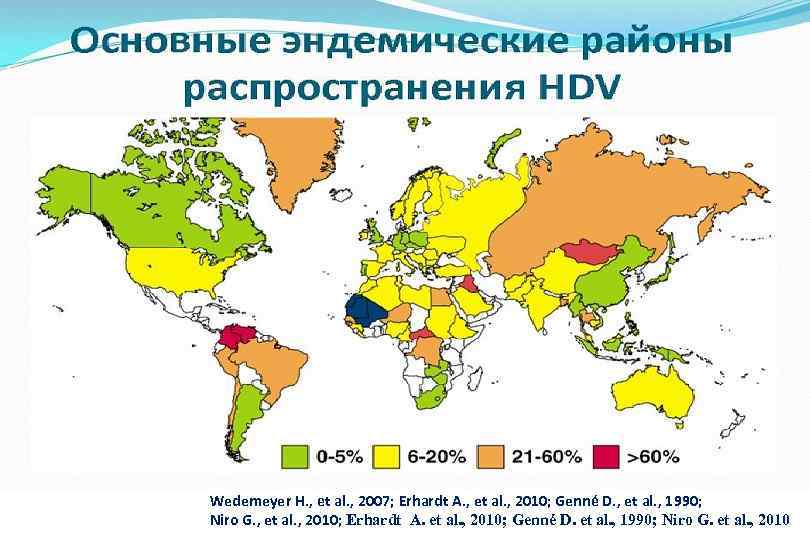 Wedemeyer H. , еt al. , 2007; Erhardt A. , et al. , 2010; Genné D. , et al. , 1990; Niro G. , et al. , 2010; Erhardt A. et al. , 2010; Genné D. et al. , 1990; Niro G. et al. , 2010
Wedemeyer H. , еt al. , 2007; Erhardt A. , et al. , 2010; Genné D. , et al. , 1990; Niro G. , et al. , 2010; Erhardt A. et al. , 2010; Genné D. et al. , 1990; Niro G. et al. , 2010
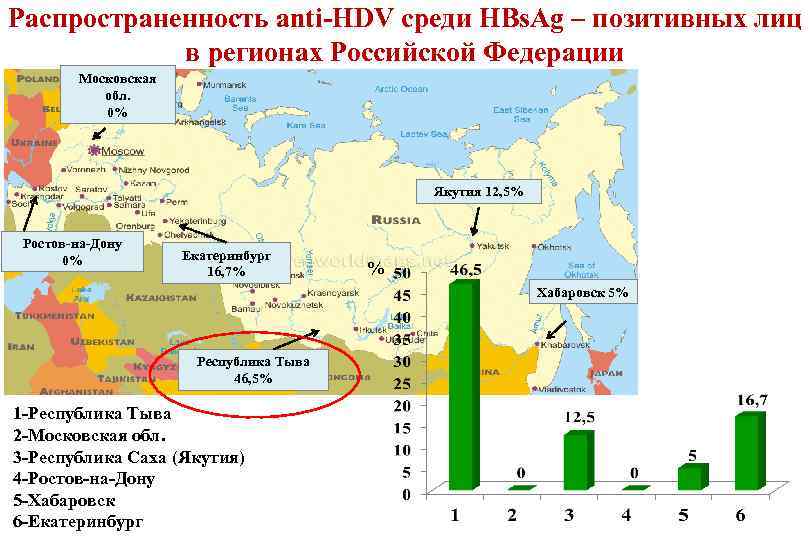 Распространенность anti-HDV среди HBs. Ag – позитивных лиц в регионах Российской Федерации Московская обл. 0% Якутия 12, 5% Ростов-на-Дону 0% Екатеринбург 16, 7% % Хабаровск 5% Республика Тыва 46, 5% 1 -Республика Тыва 2 -Московская обл. 3 -Республика Саха (Якутия) 4 -Ростов-на-Дону 5 -Хабаровск 6 -Екатеринбург
Распространенность anti-HDV среди HBs. Ag – позитивных лиц в регионах Российской Федерации Московская обл. 0% Якутия 12, 5% Ростов-на-Дону 0% Екатеринбург 16, 7% % Хабаровск 5% Республика Тыва 46, 5% 1 -Республика Тыва 2 -Московская обл. 3 -Республика Саха (Якутия) 4 -Ростов-на-Дону 5 -Хабаровск 6 -Екатеринбург
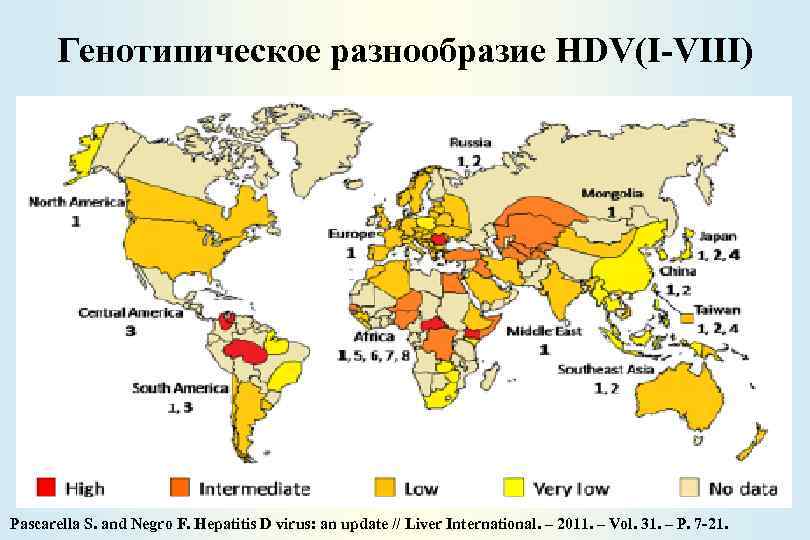 Генотипическое разнообразие HDV(I-VIII) Pascarella S. and Negro F. Hepatitis D virus: an update // Liver International. – 2011. – Vol. 31. – P. 7 -21.
Генотипическое разнообразие HDV(I-VIII) Pascarella S. and Negro F. Hepatitis D virus: an update // Liver International. – 2011. – Vol. 31. – P. 7 -21.
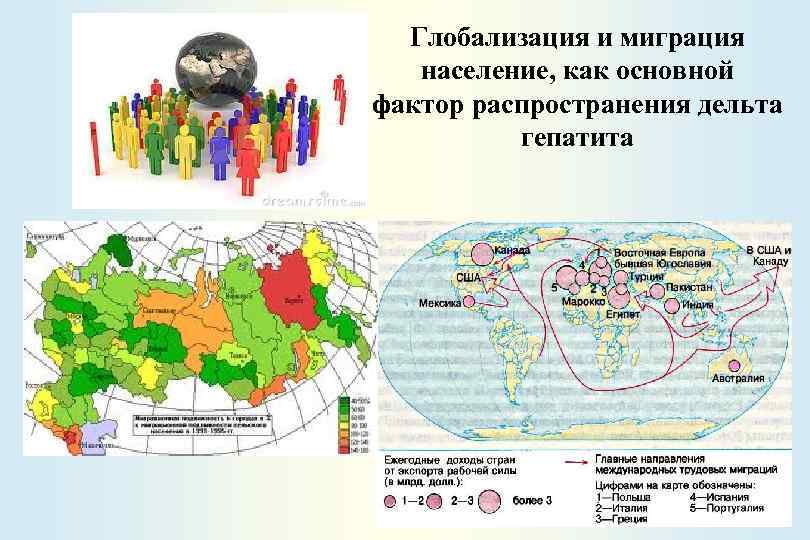 Глобализация и миграция население, как основной фактор распространения дельта гепатита
Глобализация и миграция население, как основной фактор распространения дельта гепатита
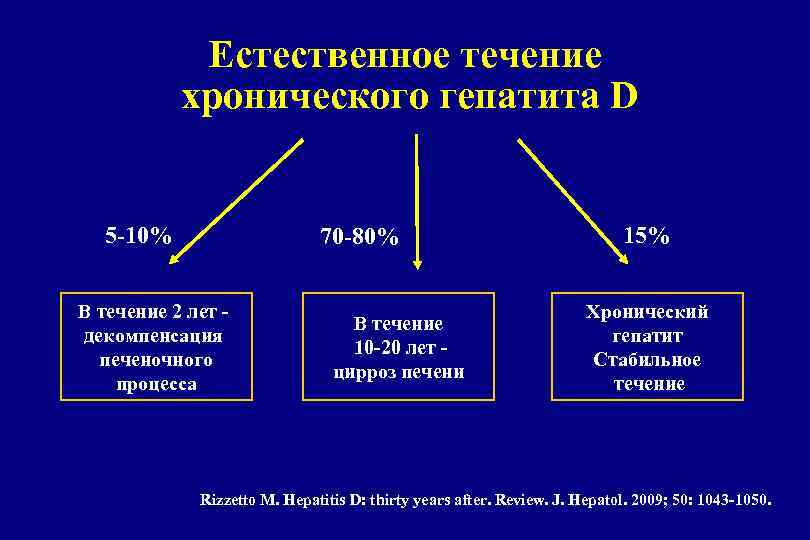 Естественное течение хронического гепатита D 5 -10% 70 -80% В течение 2 лет - декомпенсация печеночного процесса В течение 10 -20 лет цирроз печени 15% Хронический гепатит Стабильное течение Rizzetto M. Hepatitis D: thirty years after. Review. J. Hepatol. 2009; 50: 1043 -1050.
Естественное течение хронического гепатита D 5 -10% 70 -80% В течение 2 лет - декомпенсация печеночного процесса В течение 10 -20 лет цирроз печени 15% Хронический гепатит Стабильное течение Rizzetto M. Hepatitis D: thirty years after. Review. J. Hepatol. 2009; 50: 1043 -1050.
 Клиническое наблюдение • • Пациент К. , 21 год Жалобы – ноющие боли в правом подреберье, выраженная слабость, желтушность склер и кожных покровов Острый вирусный гепатит в детстве (этиология не уточнена) Вакцинирован против гепатита В в 2008 г. (3 дозы) • • Госпитализация 24. 07. 2009 г. Состояние тяжелое: интенсивная желтуха, заторможен Печень не увеличена, селезенка – у реберной дуги Печеночная кома IV (25. 07. – 01. 08. 2009 г. ) • • • АЛТ – 9, 5 ВГН; билирубин – 19 ВГН; о. белок – 57, 2 г/л; ПИ – 33% Пребывание в стационаре – 52 дня При выписке: АЛТ – 2 ВГН; билирубин – 24, 76 мкмоль/л • HBs. Ag (+), anti- HBc (+), HBe. Ag (-), anti-HBe (+), HBV DNA (-), anti-HDV (+), HDV RNA (+), генотип 1, anti-HCV (-), RNA HCV (-) Диагноз: суперинфекция HDV, генотип 1 HDV, желтушная форма, фульминантное течение (печеночная кома)
Клиническое наблюдение • • Пациент К. , 21 год Жалобы – ноющие боли в правом подреберье, выраженная слабость, желтушность склер и кожных покровов Острый вирусный гепатит в детстве (этиология не уточнена) Вакцинирован против гепатита В в 2008 г. (3 дозы) • • Госпитализация 24. 07. 2009 г. Состояние тяжелое: интенсивная желтуха, заторможен Печень не увеличена, селезенка – у реберной дуги Печеночная кома IV (25. 07. – 01. 08. 2009 г. ) • • • АЛТ – 9, 5 ВГН; билирубин – 19 ВГН; о. белок – 57, 2 г/л; ПИ – 33% Пребывание в стационаре – 52 дня При выписке: АЛТ – 2 ВГН; билирубин – 24, 76 мкмоль/л • HBs. Ag (+), anti- HBc (+), HBe. Ag (-), anti-HBe (+), HBV DNA (-), anti-HDV (+), HDV RNA (+), генотип 1, anti-HCV (-), RNA HCV (-) Диагноз: суперинфекция HDV, генотип 1 HDV, желтушная форма, фульминантное течение (печеночная кома)
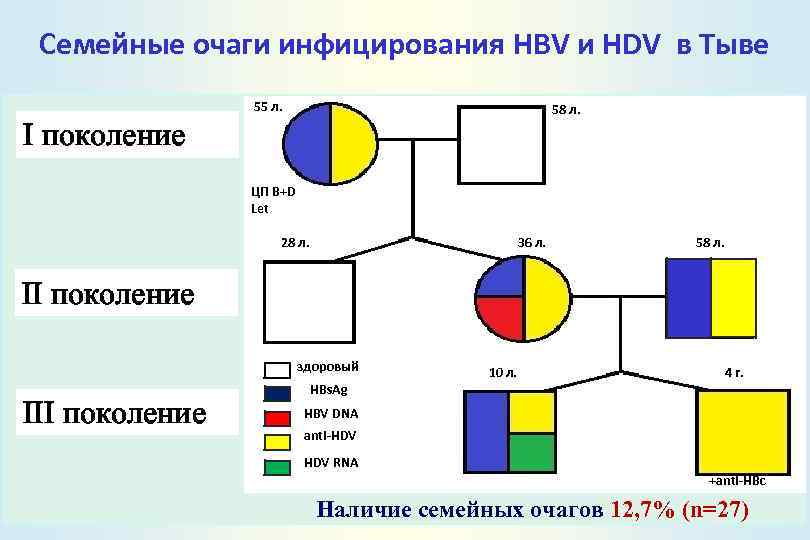 Семейные очаги инфицирования HBV и HDV в Тыве 55 л. 58 л. I поколение ЦП B+D Let 36 л. 28 л. 58 л. II поколение здоровый III поколение 10 л. 4 г. HBs. Ag HBV DNA anti-HDV RNA +anti-HBc Наличие семейных очагов 12, 7% (n=27)
Семейные очаги инфицирования HBV и HDV в Тыве 55 л. 58 л. I поколение ЦП B+D Let 36 л. 28 л. 58 л. II поколение здоровый III поколение 10 л. 4 г. HBs. Ag HBV DNA anti-HDV RNA +anti-HBc Наличие семейных очагов 12, 7% (n=27)
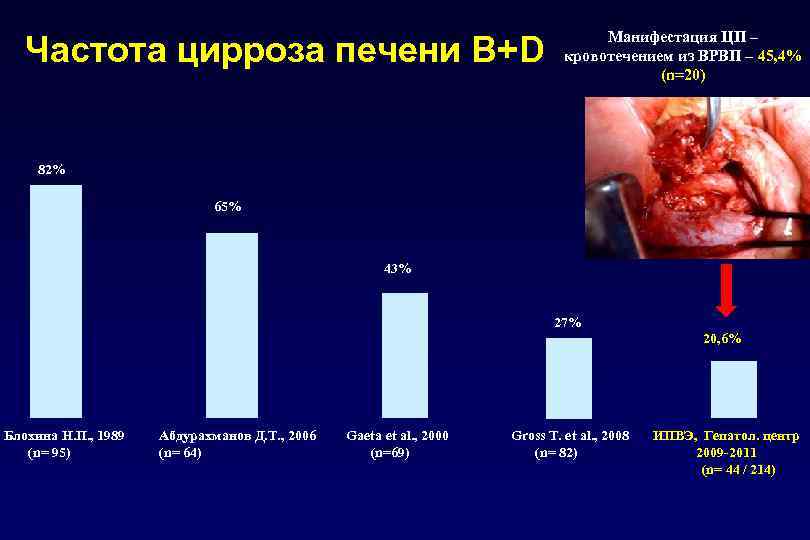 Частота цирроза печени В+D Манифестация ЦП – кровотечением из ВРВП – 45, 4% (n=20) 82% 65% 43% 27% 20, 6% Блохина Н. П. , 1989 (n= 95) Абдурахманов Д. Т. , 2006 (n= 64) Gaeta et al. , 2000 (n=69) Gross T. et al. , 2008 (n= 82) ИПВЭ, Гепатол. центр 2009 -2011 (n= 44 / 214)
Частота цирроза печени В+D Манифестация ЦП – кровотечением из ВРВП – 45, 4% (n=20) 82% 65% 43% 27% 20, 6% Блохина Н. П. , 1989 (n= 95) Абдурахманов Д. Т. , 2006 (n= 64) Gaeta et al. , 2000 (n=69) Gross T. et al. , 2008 (n= 82) ИПВЭ, Гепатол. центр 2009 -2011 (n= 44 / 214)
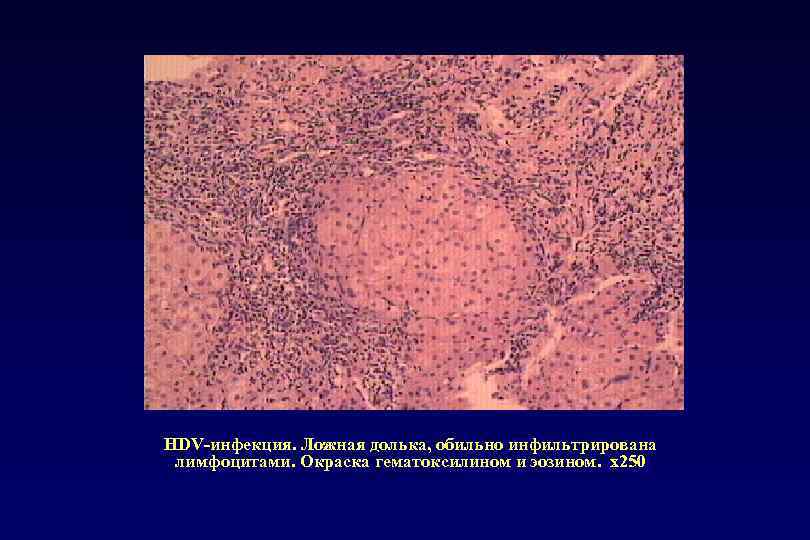 HDV-инфекция. Ложная долька, обильно инфильтрирована лимфоцитами. Окраска гематоксилином и эозином. х250
HDV-инфекция. Ложная долька, обильно инфильтрирована лимфоцитами. Окраска гематоксилином и эозином. х250
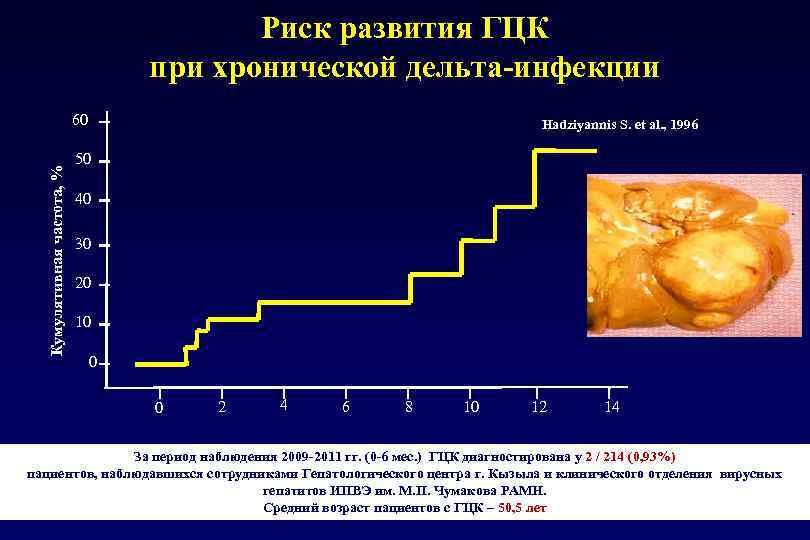 Риск развития ГЦК при хронической дельта-инфекции Кумулятивная частота, % 60 Hadziyannis S. et al. , 1996 50 40 30 20 10 0 0 2 4 6 8 10 12 14 За период наблюдения 2009 -2011 гг. (0 -6 мес. ) ГЦК диагностирована у 2 / 214 (0, 93%) пациентов, наблюдавшихся сотрудниками Гепатологического центра г. Кызыла и клинического отделения вирусных гепатитов ИПВЭ им. М. П. Чумакова РАМН. Средний возраст пациентов с ГЦК – 50, 5 лет
Риск развития ГЦК при хронической дельта-инфекции Кумулятивная частота, % 60 Hadziyannis S. et al. , 1996 50 40 30 20 10 0 0 2 4 6 8 10 12 14 За период наблюдения 2009 -2011 гг. (0 -6 мес. ) ГЦК диагностирована у 2 / 214 (0, 93%) пациентов, наблюдавшихся сотрудниками Гепатологического центра г. Кызыла и клинического отделения вирусных гепатитов ИПВЭ им. М. П. Чумакова РАМН. Средний возраст пациентов с ГЦК – 50, 5 лет
 Особенности течения хронического гепатита D (1) • преобладание мужчин молодого и зрелого возраста • у половины пациентов в анамнезе наличие острого вирусного гепатита • тяжелое течение в случаях суперинфекции ВГD, включая фульминантный вариант • нередко установление хронического поражения печени (ХГ и ЦП) при первом обращении • преобладание HBe. Ag-негативного варианта ХГ В+D • связь клинических проявлений с сочетанием генотипов HBV HDV (наиболее неблагоприятный - HBV F + HDV 3) • полиморфизм клинической симптоматики • наличие семейных очагов HDV-инфекции
Особенности течения хронического гепатита D (1) • преобладание мужчин молодого и зрелого возраста • у половины пациентов в анамнезе наличие острого вирусного гепатита • тяжелое течение в случаях суперинфекции ВГD, включая фульминантный вариант • нередко установление хронического поражения печени (ХГ и ЦП) при первом обращении • преобладание HBe. Ag-негативного варианта ХГ В+D • связь клинических проявлений с сочетанием генотипов HBV HDV (наиболее неблагоприятный - HBV F + HDV 3) • полиморфизм клинической симптоматики • наличие семейных очагов HDV-инфекции
 Особенности течения хронического гепатита D (II) • высокая активность печеночного процесса • большая частота аутоиммунных нарушений • резистентность к противовирусной терапии • быстро прогрессирующее течение с исходом в ЦП, особенно у детей рожденных от инфицированных ВГВ матерей • высокий уровень летальности вследствие развития кровотечения из ВРВП • высокая частота формирования ГЦК • высокая частота билиарной патологии (ЖКБ, бил. сладж, холестероз)
Особенности течения хронического гепатита D (II) • высокая активность печеночного процесса • большая частота аутоиммунных нарушений • резистентность к противовирусной терапии • быстро прогрессирующее течение с исходом в ЦП, особенно у детей рожденных от инфицированных ВГВ матерей • высокий уровень летальности вследствие развития кровотечения из ВРВП • высокая частота формирования ГЦК • высокая частота билиарной патологии (ЖКБ, бил. сладж, холестероз)
 Хронический вирусный гепатит С
Хронический вирусный гепатит С
 1989 г. Методами молекулярной биологии выделен геном вируса гепатита С Michael Houghton Qui-Lim Choo George Kuo Daniel Bradley Получены иммунореактивные олигопептиды, реагирующие с антителами, циркулирующими в крови больных хроническим гепатитом ни А, ни В, что стало основой диагностических препаратов для выявления антител к HCV
1989 г. Методами молекулярной биологии выделен геном вируса гепатита С Michael Houghton Qui-Lim Choo George Kuo Daniel Bradley Получены иммунореактивные олигопептиды, реагирующие с антителами, циркулирующими в крови больных хроническим гепатитом ни А, ни В, что стало основой диагностических препаратов для выявления антител к HCV
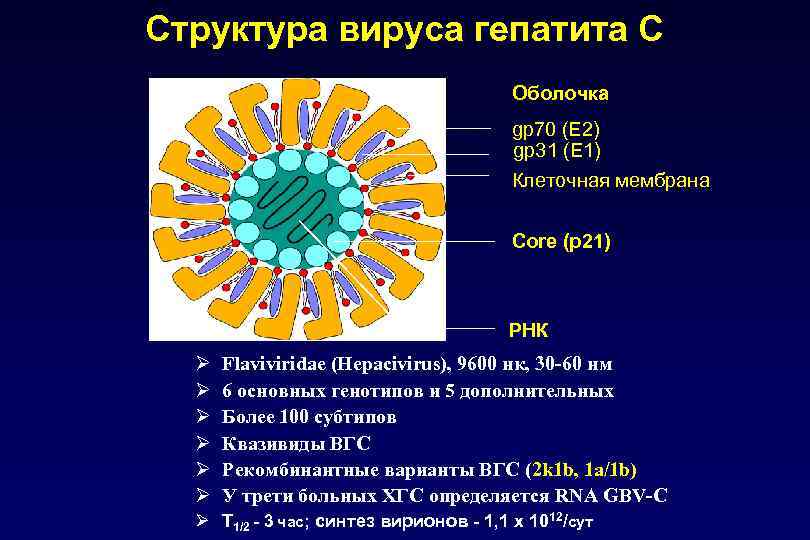 Структура вируса гепатита С Оболочка gp 70 (E 2) gp 31 (E 1) Клеточная мембрана Core (p 21) РНК Ø Ø Ø Flaviviridae (Hepacivirus), 9600 нк, 30 -60 нм 6 основных генотипов и 5 дополнительных Более 100 субтипов Квазивиды ВГС Рекомбинантные варианты ВГС (2 k 1 b, 1 а/1 b) У трети больных ХГС определяется RNA GBV-C Ø Т 1/2 - 3 час; синтез вирионов - 1, 1 х 1012/сут
Структура вируса гепатита С Оболочка gp 70 (E 2) gp 31 (E 1) Клеточная мембрана Core (p 21) РНК Ø Ø Ø Flaviviridae (Hepacivirus), 9600 нк, 30 -60 нм 6 основных генотипов и 5 дополнительных Более 100 субтипов Квазивиды ВГС Рекомбинантные варианты ВГС (2 k 1 b, 1 а/1 b) У трети больных ХГС определяется RNA GBV-C Ø Т 1/2 - 3 час; синтез вирионов - 1, 1 х 1012/сут
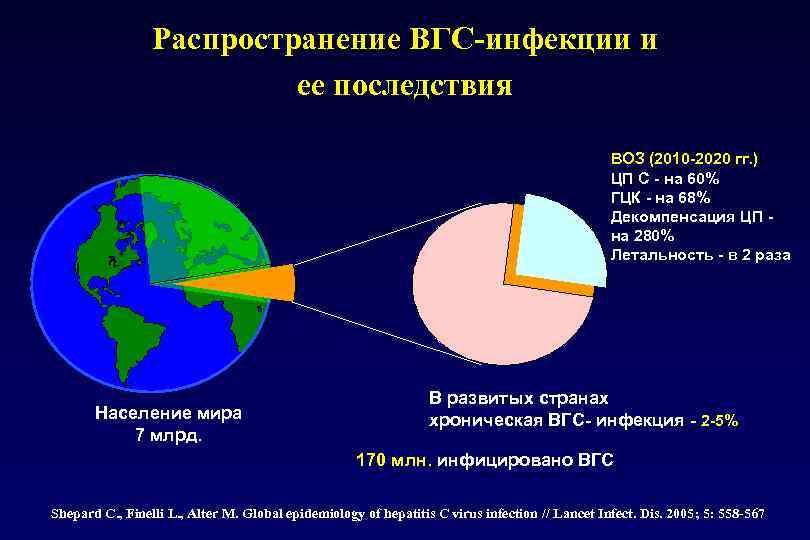 Распространение ВГС-инфекции и ее последствия ВОЗ (2010 -2020 гг. ) ЦП С - на 60% ГЦК - на 68% Декомпенсация ЦП на 280% Летальность - в 2 раза Население мира 7 млрд. В развитых странах хроническая ВГС- инфекция - 2 -5% 170 млн. инфицировано ВГС Shepard C. , Finelli L. , Alter M. Global epidemiology of hepatitis C virus infection // Lancet Infect. Dis. 2005; 5: 558 -567
Распространение ВГС-инфекции и ее последствия ВОЗ (2010 -2020 гг. ) ЦП С - на 60% ГЦК - на 68% Декомпенсация ЦП на 280% Летальность - в 2 раза Население мира 7 млрд. В развитых странах хроническая ВГС- инфекция - 2 -5% 170 млн. инфицировано ВГС Shepard C. , Finelli L. , Alter M. Global epidemiology of hepatitis C virus infection // Lancet Infect. Dis. 2005; 5: 558 -567
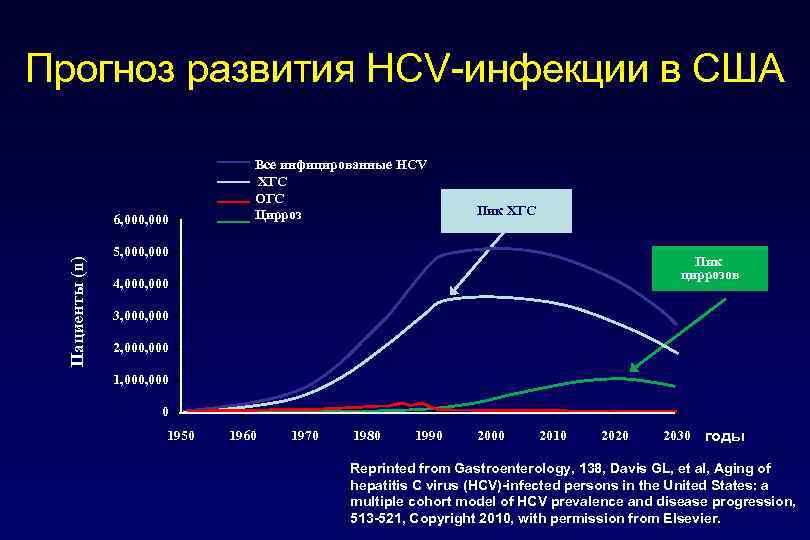 Прогноз развития НСV-инфекции в США Пациенты (n) 6, 000 Все инфицированные HCV ХГС ОГС Цирроз Пик ХГС 5, 000 Пик циррозов 4, 000 3, 000 2, 000 1, 000 0 1950 1960 1970 1980 1990 2000 2010 2020 2030 годы Reprinted from Gastroenterology, 138, Davis GL, et al, Aging of hepatitis C virus (HCV)-infected persons in the United States: a multiple cohort model of HCV prevalence and disease progression, 513 -521, Copyright 2010, with permission from Elsevier.
Прогноз развития НСV-инфекции в США Пациенты (n) 6, 000 Все инфицированные HCV ХГС ОГС Цирроз Пик ХГС 5, 000 Пик циррозов 4, 000 3, 000 2, 000 1, 000 0 1950 1960 1970 1980 1990 2000 2010 2020 2030 годы Reprinted from Gastroenterology, 138, Davis GL, et al, Aging of hepatitis C virus (HCV)-infected persons in the United States: a multiple cohort model of HCV prevalence and disease progression, 513 -521, Copyright 2010, with permission from Elsevier.
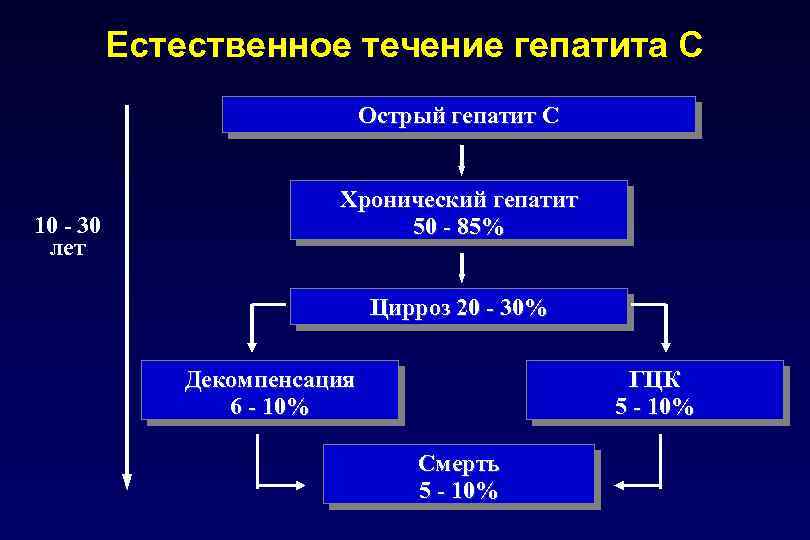 Естественное течение гепатита С Острый гепатит C 10 - 30 лет Хронический гепатит 50 - 85% Цирроз 20 - 30% Декомпенсация 6 - 10% ГЦК 5 - 10% Смерть 5 - 10%
Естественное течение гепатита С Острый гепатит C 10 - 30 лет Хронический гепатит 50 - 85% Цирроз 20 - 30% Декомпенсация 6 - 10% ГЦК 5 - 10% Смерть 5 - 10%
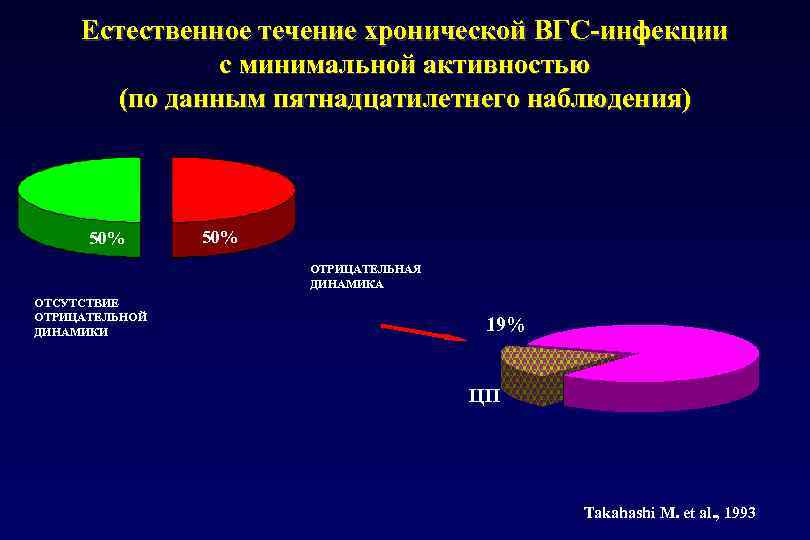 Естественное течение хронической ВГС-инфекции c минимальной активностью (по данным пятнадцатилетнего наблюдения) 50% ОТРИЦАТЕЛЬНАЯ ДИНАМИКА ОТСУТСТВИЕ ОТРИЦАТЕЛЬНОЙ ДИНАМИКИ 19% ЦП Takahashi М. et al. , 1993
Естественное течение хронической ВГС-инфекции c минимальной активностью (по данным пятнадцатилетнего наблюдения) 50% ОТРИЦАТЕЛЬНАЯ ДИНАМИКА ОТСУТСТВИЕ ОТРИЦАТЕЛЬНОЙ ДИНАМИКИ 19% ЦП Takahashi М. et al. , 1993
 Сывороточные маркеры ВГВ ВГС ВГD anti-HDV Ig. M HDV RNA репликации HBe. Ag HBc. Ab Ig. M HBV DNA anti-HCVс Ig. M HCV RNA инфицирования HBs. Ag anti-HCV свидетельствуют о перенесенном ОВГ HBs. Ab HBc. Ab HBe. Ab anti-HCV anti-HDV Ig. G “Изолированные” HBc. Ab и HBe. Ab требуют исследования HBV DNA и маркеров HCV
Сывороточные маркеры ВГВ ВГС ВГD anti-HDV Ig. M HDV RNA репликации HBe. Ag HBc. Ab Ig. M HBV DNA anti-HCVс Ig. M HCV RNA инфицирования HBs. Ag anti-HCV свидетельствуют о перенесенном ОВГ HBs. Ab HBc. Ab HBe. Ab anti-HCV anti-HDV Ig. G “Изолированные” HBc. Ab и HBe. Ab требуют исследования HBV DNA и маркеров HCV
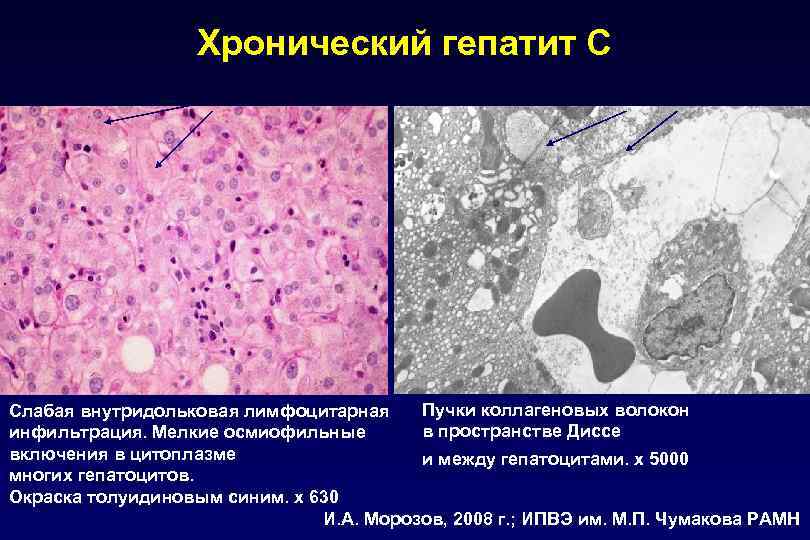 Хронический гепатит С Пучки коллагеновых волокон Слабая внутридольковая лимфоцитарная в пространстве Диссе инфильтрация. Мелкие осмиофильные включения в цитоплазме и между гепатоцитами. х 5000 многих гепатоцитов. Окраска толуидиновым синим. х 630 И. А. Морозов, 2008 г. ; ИПВЭ им. М. П. Чумакова РАМН
Хронический гепатит С Пучки коллагеновых волокон Слабая внутридольковая лимфоцитарная в пространстве Диссе инфильтрация. Мелкие осмиофильные включения в цитоплазме и между гепатоцитами. х 5000 многих гепатоцитов. Окраска толуидиновым синим. х 630 И. А. Морозов, 2008 г. ; ИПВЭ им. М. П. Чумакова РАМН
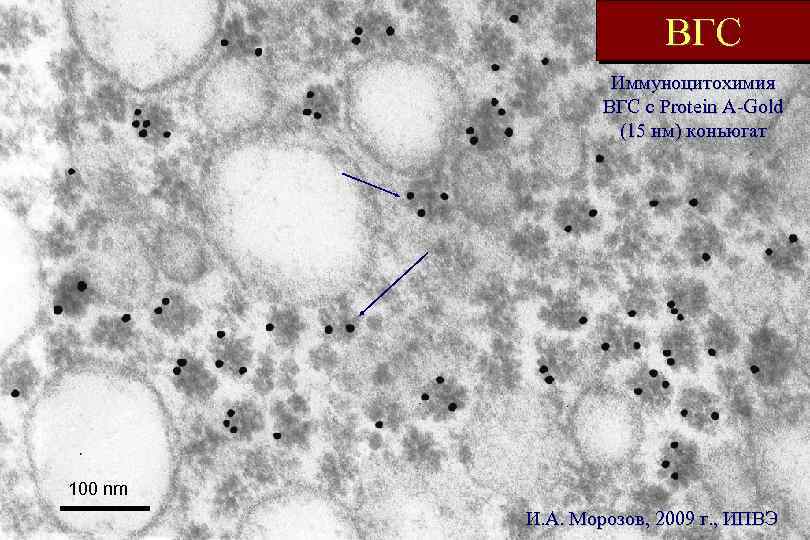 ВГС Иммуноцитохимия ВГС с Protein A-Gold (15 нм) коньюгат 100 nm И. А. Морозов, 2009 г. , ИПВЭ
ВГС Иммуноцитохимия ВГС с Protein A-Gold (15 нм) коньюгат 100 nm И. А. Морозов, 2009 г. , ИПВЭ
 Вирусный микст-гепатит HVB + HСV + HDV ~1% HBV + HDV 5 -10% HCV 170 млн. HDV ~20 -50 млн. HBV 300 -400 млн. HBV + HСV 7 -17% http: //www. who. int/topics/hepatitis/ru/
Вирусный микст-гепатит HVB + HСV + HDV ~1% HBV + HDV 5 -10% HCV 170 млн. HDV ~20 -50 млн. HBV 300 -400 млн. HBV + HСV 7 -17% http: //www. who. int/topics/hepatitis/ru/
 Лечение хронических вирусных гепатитов
Лечение хронических вирусных гепатитов
 Электронный опрос - У специалистов какой специальности должны лечиться больные хроническим вирусным гепатитом? 60% - у инфекционистов 30% - у гастроэнтерологов 10% - затруднились ответить Профессор Шейла Шерлок - А я голосовала за гастроэнтерологов Впрочем, все равно, был бы врач хороший – Профессор Шейла Шерлок 1918 -2001
Электронный опрос - У специалистов какой специальности должны лечиться больные хроническим вирусным гепатитом? 60% - у инфекционистов 30% - у гастроэнтерологов 10% - затруднились ответить Профессор Шейла Шерлок - А я голосовала за гастроэнтерологов Впрочем, все равно, был бы врач хороший – Профессор Шейла Шерлок 1918 -2001
 Терапия хронического гепатита С
Терапия хронического гепатита С
 Показания к лечению HCV-инфекции • Острый гепатит С • Хронический гепатит С • Компенсированный цирроз печени С • Декомпенсированный цирроз печени С (перед трансплантацией печени) • Возвратная HCV-инфекция у пациентов, перенесших трансплантацию печени NIH Consensus Conference Hepatol. , 2002; 36 (5, Suppl. 1): 3 -19 Thomas R. M. et al. Liver Transpl. 2003; 9: 905 -915 Strader D. B. et al. Hepatol. , 2004; 39 (4): 1147 -1171 Рекомендации Американской гастроэнтерологической ассоциации, 2006 Сhany M. G. et al. Hepatol. , 2009; 49: 1335 -1374
Показания к лечению HCV-инфекции • Острый гепатит С • Хронический гепатит С • Компенсированный цирроз печени С • Декомпенсированный цирроз печени С (перед трансплантацией печени) • Возвратная HCV-инфекция у пациентов, перенесших трансплантацию печени NIH Consensus Conference Hepatol. , 2002; 36 (5, Suppl. 1): 3 -19 Thomas R. M. et al. Liver Transpl. 2003; 9: 905 -915 Strader D. B. et al. Hepatol. , 2004; 39 (4): 1147 -1171 Рекомендации Американской гастроэнтерологической ассоциации, 2006 Сhany M. G. et al. Hepatol. , 2009; 49: 1335 -1374
 Реальная клиническая практика Противовирусные препараты для лечения хронического гепатита С (стандарты МЗ и СФ РФ, международные рекомендации) • Интерферон альфа 2 a, интерферон альфа 2 b • Пэгинтерферон альфа 2 а, пэгинтерферон альфа 2 b • Рибавирин
Реальная клиническая практика Противовирусные препараты для лечения хронического гепатита С (стандарты МЗ и СФ РФ, международные рекомендации) • Интерферон альфа 2 a, интерферон альфа 2 b • Пэгинтерферон альфа 2 а, пэгинтерферон альфа 2 b • Рибавирин
 Препараты интерферона, разрешенные к применению в Российской Федерации Интерферон-альфа (3 млн МЕ) Интрон А (США) Роферон (Швейцария) Реальдирон (Израиль) Альфаферон (Италия) Реаферон (Россия) Интераль (Россия) Альтевир (Россия) Альфарона (Россия) Эбирон (Куба)
Препараты интерферона, разрешенные к применению в Российской Федерации Интерферон-альфа (3 млн МЕ) Интрон А (США) Роферон (Швейцария) Реальдирон (Израиль) Альфаферон (Италия) Реаферон (Россия) Интераль (Россия) Альтевир (Россия) Альфарона (Россия) Эбирон (Куба)
 Пэг. ИФНновое поколение пегилированных интерферонов Пэг. ИФН альфа-2 а (180 мкг/нед) Пэг. ИФН альфа-2 b (1, 5 мкг/кг/нед)
Пэг. ИФНновое поколение пегилированных интерферонов Пэг. ИФН альфа-2 а (180 мкг/нед) Пэг. ИФН альфа-2 b (1, 5 мкг/кг/нед)
 Ограничение традиционной ИФН - терапии • Быстрый распад после инъекции • Короткий период полужизни (3– 8 ч) • Низкое накопление в органе-мишени • Быстрое выведение почками • Ограниченная эффективность • Частое введение • Тяжелые побочные эффекты
Ограничение традиционной ИФН - терапии • Быстрый распад после инъекции • Короткий период полужизни (3– 8 ч) • Низкое накопление в органе-мишени • Быстрое выведение почками • Ограниченная эффективность • Частое введение • Тяжелые побочные эффекты
 Противопоказания к проведению ИФН-терапии 1. Сопутствующие тяжелые заболевания (сердечно-сосудистые, легких, почек, неврологические, психические, сахарный диабет) 2. Декомпенсированные циррозы печени (Child-Pugh B, C) 3. Аутоиммунные нарушения (в т. ч. HCV-ассоциированный аутоиммунный гепатит) 4. Наркомания, алкоголизм, ВИЧ 5. Цитопения: лейкопения (< 1, 5 тыс. ), тромбоцитопения (< 100 тыс. ) 6. Анемия (Hb < 120 г/л) 7. Беременность
Противопоказания к проведению ИФН-терапии 1. Сопутствующие тяжелые заболевания (сердечно-сосудистые, легких, почек, неврологические, психические, сахарный диабет) 2. Декомпенсированные циррозы печени (Child-Pugh B, C) 3. Аутоиммунные нарушения (в т. ч. HCV-ассоциированный аутоиммунный гепатит) 4. Наркомания, алкоголизм, ВИЧ 5. Цитопения: лейкопения (< 1, 5 тыс. ), тромбоцитопения (< 100 тыс. ) 6. Анемия (Hb < 120 г/л) 7. Беременность
 Лечение острого гепатита С • Американская коллегия врачей и Американская ассоциация по изучению заболеваний печени (AASLD) предлагает рассмотреть назначение ПВТ через 8 -12 недель от установления диагноза ОГС. • Рекомендуется применение больших доз ИФН-α короткого действия (5 -10 млн. МЕ ежедневно в течение 4 нед. , затем 20 нед по 5 млн. МЕ ч/д в течение 20 нед. ). При этом УВО и нормализация АЛТ достигается в 83 -100% случаев • Применение ПЕГ-ИФН-α-2 b в течение 12 недель позволяет достичь УВО у 90% пациентов в случаях начала терапии через 8 -12 недель против 76% - при начале ПВТ через 20 недель от установления диагноза ОГС
Лечение острого гепатита С • Американская коллегия врачей и Американская ассоциация по изучению заболеваний печени (AASLD) предлагает рассмотреть назначение ПВТ через 8 -12 недель от установления диагноза ОГС. • Рекомендуется применение больших доз ИФН-α короткого действия (5 -10 млн. МЕ ежедневно в течение 4 нед. , затем 20 нед по 5 млн. МЕ ч/д в течение 20 нед. ). При этом УВО и нормализация АЛТ достигается в 83 -100% случаев • Применение ПЕГ-ИФН-α-2 b в течение 12 недель позволяет достичь УВО у 90% пациентов в случаях начала терапии через 8 -12 недель против 76% - при начале ПВТ через 20 недель от установления диагноза ОГС
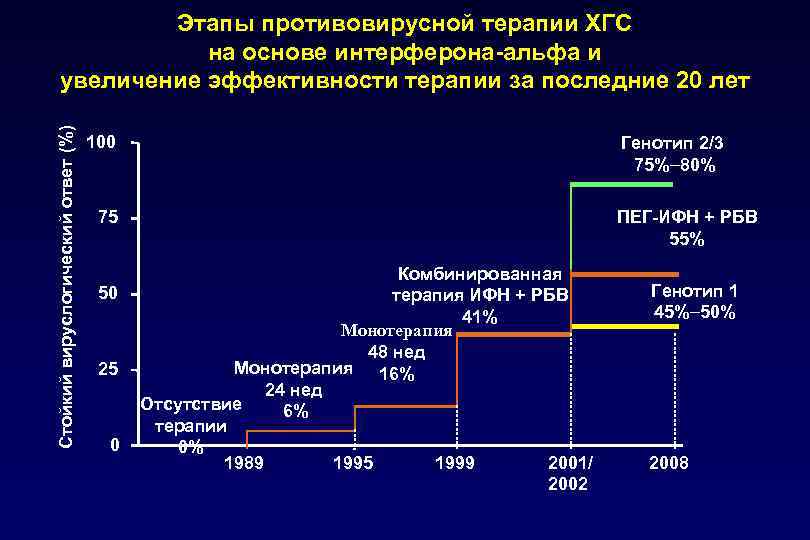 Стойкий вируслогический ответ (%) Этапы противовирусной терапии ХГС на основе интерферона-альфа и увеличение эффективности терапии за последние 20 лет 100 Генотип 2/3 75%− 80% ПЕГ-ИФН + РБВ 55% 75 50 25 0 Комбинированная терапия ИФН + РБВ 41% Монотерапия 48 нед Монотерапия 16% 24 нед Отсутствие 6% терапии 0% 1989 1995 1999 2001/ 2002 Генотип 1 45%− 50% 2008
Стойкий вируслогический ответ (%) Этапы противовирусной терапии ХГС на основе интерферона-альфа и увеличение эффективности терапии за последние 20 лет 100 Генотип 2/3 75%− 80% ПЕГ-ИФН + РБВ 55% 75 50 25 0 Комбинированная терапия ИФН + РБВ 41% Монотерапия 48 нед Монотерапия 16% 24 нед Отсутствие 6% терапии 0% 1989 1995 1999 2001/ 2002 Генотип 1 45%− 50% 2008
 Рибавирин (РБВ) Синтетический аналог нуклеозидов с выраженным противовирусным действием Обладает широким спектром активности против РНК-содержащих вирусов
Рибавирин (РБВ) Синтетический аналог нуклеозидов с выраженным противовирусным действием Обладает широким спектром активности против РНК-содержащих вирусов
 Механизмы действия рибавирина § рибавирин-монофосфат ингибирует инозинмонофосфат-дегидрогеназу, что приводит к синтезу РНК ВГС с аномальными 5’-концами § рибавирин обладает прямым ингибирующим действием на вирусную РНК-полимеразу § подавляет синтез белка и нуклеиновых кислот, снижает выработку провоспалительных цитокинов § индуцирует апоптоз инфицированных клеток
Механизмы действия рибавирина § рибавирин-монофосфат ингибирует инозинмонофосфат-дегидрогеназу, что приводит к синтезу РНК ВГС с аномальными 5’-концами § рибавирин обладает прямым ингибирующим действием на вирусную РНК-полимеразу § подавляет синтез белка и нуклеиновых кислот, снижает выработку провоспалительных цитокинов § индуцирует апоптоз инфицированных клеток
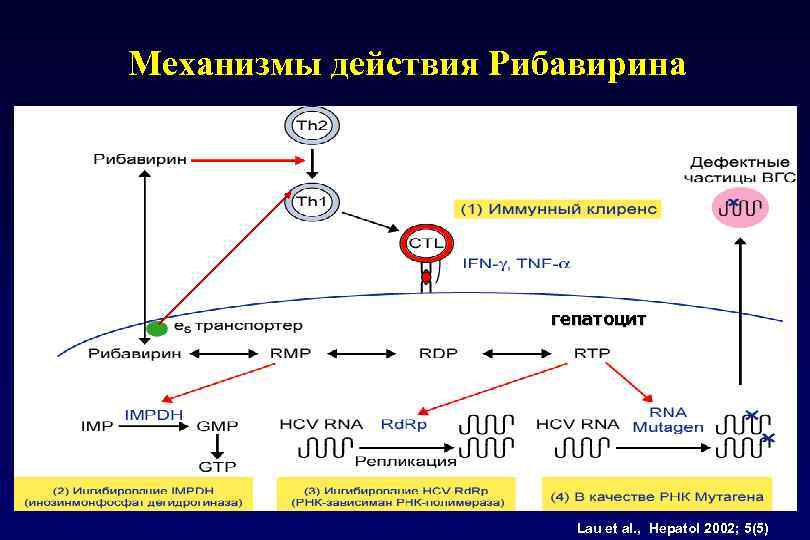 Механизмы действия Рибавирина гепатоцит Lau et al. , Hepatol 2002; 5(5)
Механизмы действия Рибавирина гепатоцит Lau et al. , Hepatol 2002; 5(5)
 Препараты рибавирина, разрешенные к применению в Российской Федерации Ребетол Рибавирин-Медуна Рибавин Веро-рибавирин Рибапег Рибамидил Арвирон Рибавирин-верте США Германия Индия Россия, Россия
Препараты рибавирина, разрешенные к применению в Российской Федерации Ребетол Рибавирин-Медуна Рибавин Веро-рибавирин Рибапег Рибамидил Арвирон Рибавирин-верте США Германия Индия Россия, Россия
 • AASLD PRACTICE GUIDELINES Diagnosis, Management, and Treatment of Hepatitis C: An Update M. G. Ghany, D. B. Strader, D. L. Thomas, L. B. Seeff Hepatology, 2009; 49 (4): 1335 -1374 • EASL Clinical Practice Guidelines: Management of hepatitis C virus Infection. A. Craxi et al. Hepatology, 2011; 55(2): 245 -64 • AASLD PRACTICE GUIDELINE: An Update on Treatment of Genotype 1 Chronic Hepatitis C Virus Infection: 2011 Practice Guideline by the American Association for the Study of Liver Diseases. M. G. Ghany, D. R. Nelson, D. B. Strader, D. L. Thomas, L. B. Seeff. Hepatology, 2011; 54: 1433 -1444. • Методические рекомендации Диагностика, ведение и лечение HCV-инфекции Российский журнал гастроэнтерологии, гепатологии, колопроктологии (РЖГГК) -2010; 1: 61 -68 (часть 1); 2010; 2: 66 -72 (часть 2)
• AASLD PRACTICE GUIDELINES Diagnosis, Management, and Treatment of Hepatitis C: An Update M. G. Ghany, D. B. Strader, D. L. Thomas, L. B. Seeff Hepatology, 2009; 49 (4): 1335 -1374 • EASL Clinical Practice Guidelines: Management of hepatitis C virus Infection. A. Craxi et al. Hepatology, 2011; 55(2): 245 -64 • AASLD PRACTICE GUIDELINE: An Update on Treatment of Genotype 1 Chronic Hepatitis C Virus Infection: 2011 Practice Guideline by the American Association for the Study of Liver Diseases. M. G. Ghany, D. R. Nelson, D. B. Strader, D. L. Thomas, L. B. Seeff. Hepatology, 2011; 54: 1433 -1444. • Методические рекомендации Диагностика, ведение и лечение HCV-инфекции Российский журнал гастроэнтерологии, гепатологии, колопроктологии (РЖГГК) -2010; 1: 61 -68 (часть 1); 2010; 2: 66 -72 (часть 2)
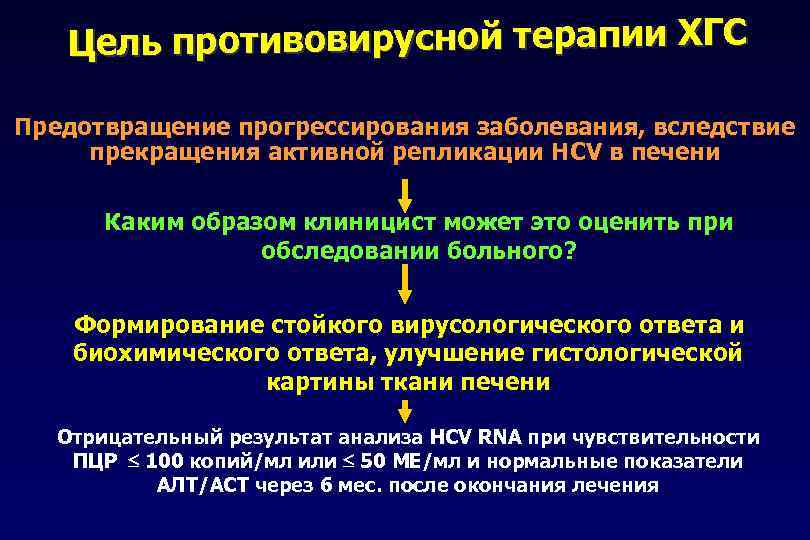 Цель противовирусной терапии ХГС Предотвращение прогрессирования заболевания, вследствие прекращения активной репликации HCV в печени Каким образом клиницист может это оценить при обследовании больного? Формирование стойкого вирусологического ответа и биохимического ответа, улучшение гистологической картины ткани печени Отрицательный результат анализа HCV RNA при чувствительности ПЦР 100 копий/мл или 50 МЕ/мл и нормальные показатели АЛТ/АСТ через 6 мес. после окончания лечения
Цель противовирусной терапии ХГС Предотвращение прогрессирования заболевания, вследствие прекращения активной репликации HCV в печени Каким образом клиницист может это оценить при обследовании больного? Формирование стойкого вирусологического ответа и биохимического ответа, улучшение гистологической картины ткани печени Отрицательный результат анализа HCV RNA при чувствительности ПЦР 100 копий/мл или 50 МЕ/мл и нормальные показатели АЛТ/АСТ через 6 мес. после окончания лечения
 Стратегия лечения хронического гепатита C Определение генотипа HCV Генотипы 2, 3 (24 нед. ) Пег-ИФН-a 2 а 180 мкг/нед + рибавирин 800 мг/сут или Пег-ИФН-a 2 b 1, 5 мкг/кг/нед + рибавирин - 800 мг/сут Генотипы 1, 4, 5, 6 (48 нед. ) Пег-ИФН-a 2 а 180 мкг /нед + рибавирин 10001200 мг/сут или Пег-ИФН-a 2 b 1, 5 мкг/кг/нед + рибавирин ( 800 мг и более) Рибавирин менее 65 кг – 800 мг/сут 65 -85 кг – 1000 - мг/сут более 85 – 105 кг -1200 мг/сут более 105 кг – 1400 мг/сут AASLD 2009 Ghany M. G. et al. Hepatol. , 2009; 49: 1335 -137
Стратегия лечения хронического гепатита C Определение генотипа HCV Генотипы 2, 3 (24 нед. ) Пег-ИФН-a 2 а 180 мкг/нед + рибавирин 800 мг/сут или Пег-ИФН-a 2 b 1, 5 мкг/кг/нед + рибавирин - 800 мг/сут Генотипы 1, 4, 5, 6 (48 нед. ) Пег-ИФН-a 2 а 180 мкг /нед + рибавирин 10001200 мг/сут или Пег-ИФН-a 2 b 1, 5 мкг/кг/нед + рибавирин ( 800 мг и более) Рибавирин менее 65 кг – 800 мг/сут 65 -85 кг – 1000 - мг/сут более 85 – 105 кг -1200 мг/сут более 105 кг – 1400 мг/сут AASLD 2009 Ghany M. G. et al. Hepatol. , 2009; 49: 1335 -137
 Вирусологический мониторинг при ХГС 8 РНК ВГС, МЕ/мл 7 Пег-ИФН- + рибавирин 6 5 4 Отсутствие ответа БВО 3 2 Снижение 2 log 10 РВО Рецидив Обострение во время ПВТ МВО УВО Чувствительность ПЦР 1 0 -6 0 6 12 18 24 30 36 42 48 Недели лечения УВО – устойчивыц вирусологический ответ МВО – медленный вирусологический ответ РВО – ранний вирусологический ответ БВО – быстрый вирусологический ответ 4 8 12 24 Недели наблюдения Индивидуализация терапии – вирусологический ответ на 4 и 12 неделе противовирусного лечени
Вирусологический мониторинг при ХГС 8 РНК ВГС, МЕ/мл 7 Пег-ИФН- + рибавирин 6 5 4 Отсутствие ответа БВО 3 2 Снижение 2 log 10 РВО Рецидив Обострение во время ПВТ МВО УВО Чувствительность ПЦР 1 0 -6 0 6 12 18 24 30 36 42 48 Недели лечения УВО – устойчивыц вирусологический ответ МВО – медленный вирусологический ответ РВО – ранний вирусологический ответ БВО – быстрый вирусологический ответ 4 8 12 24 Недели наблюдения Индивидуализация терапии – вирусологический ответ на 4 и 12 неделе противовирусного лечени
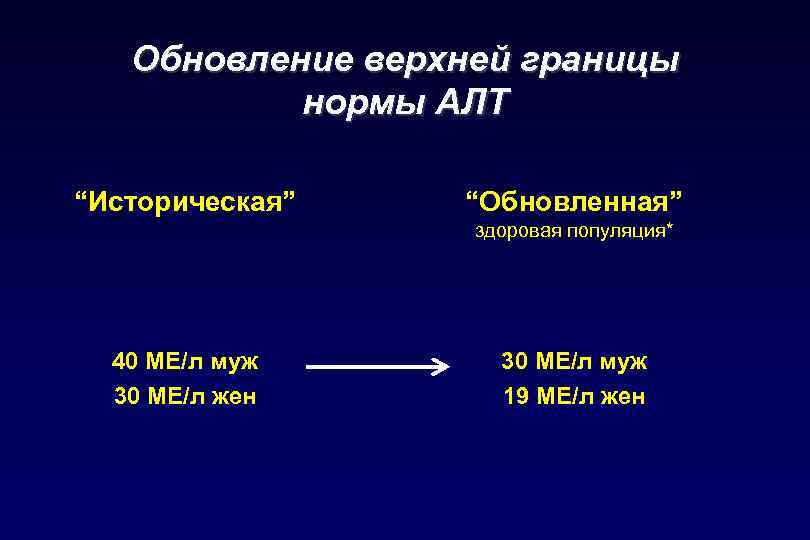 Обновление верхней границы нормы АЛТ “Историческая” “Обновленная” здоровая популяция* 40 МЕ/л муж 30 МЕ/л жен 30 МЕ/л муж 19 МЕ/л жен
Обновление верхней границы нормы АЛТ “Историческая” “Обновленная” здоровая популяция* 40 МЕ/л муж 30 МЕ/л жен 30 МЕ/л муж 19 МЕ/л жен
 Факторы, определяющие эффективность противовирусной терапии Пег-ИФН/PБВ Факторы вируса: - генотип HCV - вирусная нагрузка - квазивиды - мутации - резистентность Факторы заболевания: - стадия фиброза - внепеченочные проявления - синдром перегрузки железом - уровень АЛТ - стеатоз, стеатогепатит, ИР - HIV/HCV, HBV/HCV Факторы внешней среды: - алкоголь - наркотики - лекарства Факторы больного: - масса тела - возраст - раса - пол - генетические факторы (IL 28 B) - приверженность Факторы лечения: - длительность терапии - нежелательные явления
Факторы, определяющие эффективность противовирусной терапии Пег-ИФН/PБВ Факторы вируса: - генотип HCV - вирусная нагрузка - квазивиды - мутации - резистентность Факторы заболевания: - стадия фиброза - внепеченочные проявления - синдром перегрузки железом - уровень АЛТ - стеатоз, стеатогепатит, ИР - HIV/HCV, HBV/HCV Факторы внешней среды: - алкоголь - наркотики - лекарства Факторы больного: - масса тела - возраст - раса - пол - генетические факторы (IL 28 B) - приверженность Факторы лечения: - длительность терапии - нежелательные явления
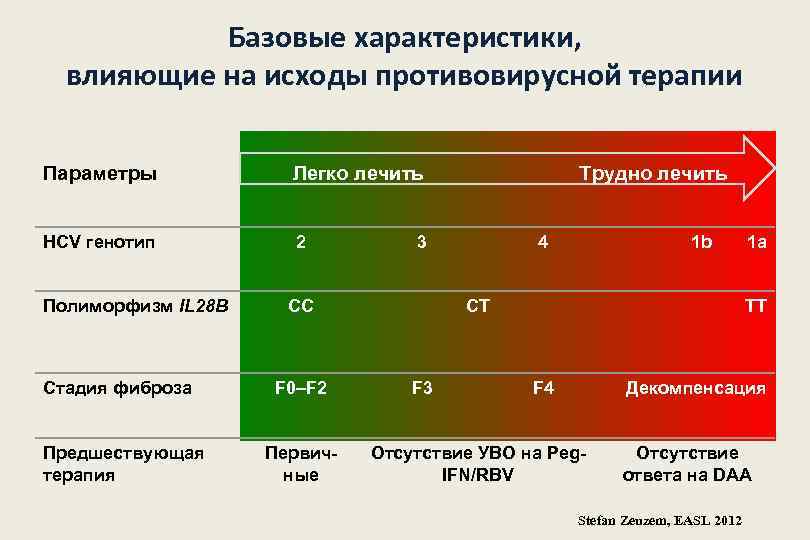 Базовые характеристики, влияющие на исходы противовирусной терапии Параметры Легко лечить HCV генотип 2 Полиморфизм IL 28 B Стадия фиброза Предшествующая терапия 3 CC F 0–F 2 Первичные Трудно лечить 4 1 b CT F 3 1 a TT F 4 Декомпенсация Отсутствие УВО на Peg. IFN/RBV Отсутствие ответа на DAA Stefan Zeuzem, EASL 2012
Базовые характеристики, влияющие на исходы противовирусной терапии Параметры Легко лечить HCV генотип 2 Полиморфизм IL 28 B Стадия фиброза Предшествующая терапия 3 CC F 0–F 2 Первичные Трудно лечить 4 1 b CT F 3 1 a TT F 4 Декомпенсация Отсутствие УВО на Peg. IFN/RBV Отсутствие ответа на DAA Stefan Zeuzem, EASL 2012
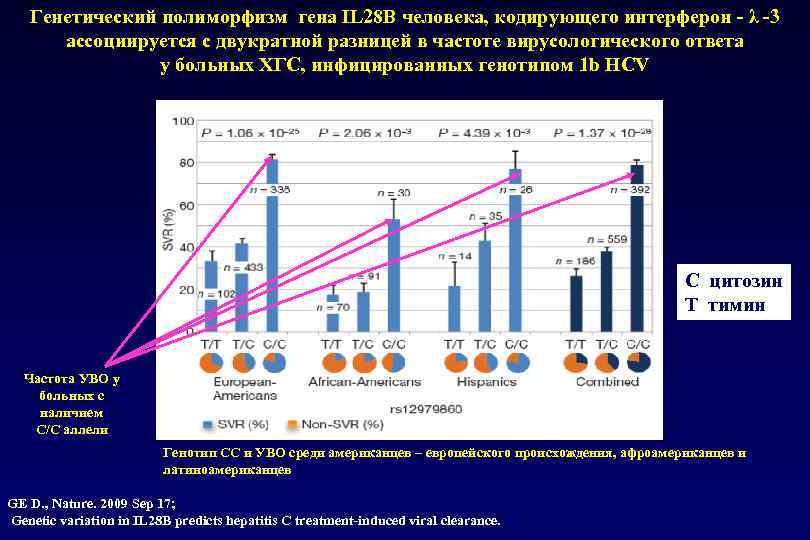 Генетический полиморфизм гена IL 28 B человека, кодирующего интерферон - λ -3 ассоциируется с двукратной разницей в частоте вирусологического ответа у больных ХГС, инфицированных генотипом 1 b HCV С цитозин Т тимин Частота УВО у больных с наличием С/C аллели Генотип СС и УВО среди американцев – европейского происхождения, афроамериканцев и латиноамериканцев GE D. , Nature. 2009 Sep 17; Genetic variation in IL 28 B predicts hepatitis C treatment-induced viral clearance.
Генетический полиморфизм гена IL 28 B человека, кодирующего интерферон - λ -3 ассоциируется с двукратной разницей в частоте вирусологического ответа у больных ХГС, инфицированных генотипом 1 b HCV С цитозин Т тимин Частота УВО у больных с наличием С/C аллели Генотип СС и УВО среди американцев – европейского происхождения, афроамериканцев и латиноамериканцев GE D. , Nature. 2009 Sep 17; Genetic variation in IL 28 B predicts hepatitis C treatment-induced viral clearance.
 Побочные эффекты терапии интерфероном-α (классификация по G. Dusheiko, 1997 г. ) • Частые (>20%) - нетяжелые побочные эффекты, не требующие изменения терапии • Относительно нечастые (<10%) - побочные эффекты, которые могут потребовать снижения дозы и/или отмены лечения • Редкие тяжелые (<1%) или опасные для жизни (<0, 1%) побочные эффекты, требующие отмены лечения • Необратимые побочные эффекты
Побочные эффекты терапии интерфероном-α (классификация по G. Dusheiko, 1997 г. ) • Частые (>20%) - нетяжелые побочные эффекты, не требующие изменения терапии • Относительно нечастые (<10%) - побочные эффекты, которые могут потребовать снижения дозы и/или отмены лечения • Редкие тяжелые (<1%) или опасные для жизни (<0, 1%) побочные эффекты, требующие отмены лечения • Необратимые побочные эффекты
 Наиболее частые побочные эффекты интерферона-α • Гриппоподобный синдром лихорадка, озноб, слабость, головная боль, миалгии, артралгии, тахикардия • Симптомы со стороны ЖКТ снижение аппетита, тошнота, рвота, диарея • Изменения со стороны ЦНС нарушение концентрации, бессонница, раздражительность, депрессия • Система дыхания кашель, одышка • Кожа • Общие симптомы астенический синдром, снижение массы тела • Аутоиммунные расстройства поражение щитовидной железы, выработка АТ и др. • Лабораторные показатели тромбоцитопения, нейтропения, анемия алопеция, зуд, сыпь, сухость кожи и др.
Наиболее частые побочные эффекты интерферона-α • Гриппоподобный синдром лихорадка, озноб, слабость, головная боль, миалгии, артралгии, тахикардия • Симптомы со стороны ЖКТ снижение аппетита, тошнота, рвота, диарея • Изменения со стороны ЦНС нарушение концентрации, бессонница, раздражительность, депрессия • Система дыхания кашель, одышка • Кожа • Общие симптомы астенический синдром, снижение массы тела • Аутоиммунные расстройства поражение щитовидной железы, выработка АТ и др. • Лабораторные показатели тромбоцитопения, нейтропения, анемия алопеция, зуд, сыпь, сухость кожи и др.
 Основные побочные эффекты терапии рибавирином • Анемия (гемолиз) • Кашель • Тератогенные и эмбриотоксические эффекты • Диспепсические явления • Гиперурикемия • Нарушения функции щитовидной железы • Аллергические реакции
Основные побочные эффекты терапии рибавирином • Анемия (гемолиз) • Кашель • Тератогенные и эмбриотоксические эффекты • Диспепсические явления • Гиперурикемия • Нарушения функции щитовидной железы • Аллергические реакции
 Редкие побочные эффекты ПВТ • • • Саркоидоз Ретинопатия Сахарный диабет Волчаночноподобный синдром Аутоиммунная гемолитическая анемия Иммунная тромбоцитопения Аутоиммунный гепатит Периферическая нейропатия Нейросенсорная тугоухость Язвенный колит Энцефалопатия Хашимото Обострение псориаза
Редкие побочные эффекты ПВТ • • • Саркоидоз Ретинопатия Сахарный диабет Волчаночноподобный синдром Аутоиммунная гемолитическая анемия Иммунная тромбоцитопения Аутоиммунный гепатит Периферическая нейропатия Нейросенсорная тугоухость Язвенный колит Энцефалопатия Хашимото Обострение псориаза
 Коррекция нежелательных эффектов при ХГС Лабораторный контроль Старт (0)-2 -4 -8 -12 -16 -24 -28 -32 -36 -40 -44 -48 ---72 ----96 нед Стимуляторы нейтропоэза гранулоцитарный колониестимулирующий фактор, 300 мкг 3 р/нед Стимуляторы эритропоэза осторожно (образ. антител, апласт. анемия) эритропоэтин-а, 30 -100 МЕ/кг 3 р/нед Стимуляторы тромбопоэза элтромбопаг (тромбопаг) 30 -75 мг/сут в течение 4 нед Коррекция гипотиреоза (контроль 0 -12 -24 -48 -24 нед) тироксин 25 -50 мг/сут Коррекция депрессии ИОЗС, пароксетин, 20 мг/сут Профилактика и лечение энцефалопатии орнитин-аспартат 18 г/сут, лактулоза 30 -90 мл/сут, рифаксимин 1200 мг/сут
Коррекция нежелательных эффектов при ХГС Лабораторный контроль Старт (0)-2 -4 -8 -12 -16 -24 -28 -32 -36 -40 -44 -48 ---72 ----96 нед Стимуляторы нейтропоэза гранулоцитарный колониестимулирующий фактор, 300 мкг 3 р/нед Стимуляторы эритропоэза осторожно (образ. антител, апласт. анемия) эритропоэтин-а, 30 -100 МЕ/кг 3 р/нед Стимуляторы тромбопоэза элтромбопаг (тромбопаг) 30 -75 мг/сут в течение 4 нед Коррекция гипотиреоза (контроль 0 -12 -24 -48 -24 нед) тироксин 25 -50 мг/сут Коррекция депрессии ИОЗС, пароксетин, 20 мг/сут Профилактика и лечение энцефалопатии орнитин-аспартат 18 г/сут, лактулоза 30 -90 мл/сут, рифаксимин 1200 мг/сут
 LADR - Low-Accelerating-Dose Regimen – технология увеличения низких доз Стратегия антивирусной терапии у больных с декомпенсированным ЦПС Начальные дозы: ИФН alfa-2 b или Пег-ИФН alfa-2 b в сочетании с Рибавирином ежедневная доза соответствует 50% от полной дозы Увеличение дозы через 2 недели до 75% при переносимости Увеличение дозы через 4 недели до 100 % при переносимости 13. 5% Thomas R. M. et al. Liver Transpl. 2003; 9: 905 -915 Everson G. T. et al. Hepatology 2005; 42: 255 -262.
LADR - Low-Accelerating-Dose Regimen – технология увеличения низких доз Стратегия антивирусной терапии у больных с декомпенсированным ЦПС Начальные дозы: ИФН alfa-2 b или Пег-ИФН alfa-2 b в сочетании с Рибавирином ежедневная доза соответствует 50% от полной дозы Увеличение дозы через 2 недели до 75% при переносимости Увеличение дозы через 4 недели до 100 % при переносимости 13. 5% Thomas R. M. et al. Liver Transpl. 2003; 9: 905 -915 Everson G. T. et al. Hepatology 2005; 42: 255 -262.
 Методы коррекции неблагоприятных факторов ХГС + НАСГ (стеатоз) Метаболический синдром • • Избыточная масса тела Гиперлипидемия НТГ, гипергликемия Артериальная гипертензия • Гипокалорийная диета (2200 ккал/сут) • Аэробные дозированные физические нагрузки (40 -60 мин/сут) • Хирургические методы снижения массы тела (установление баллона в желудке, наложение желудочнокишечного анастомоза) • Антиоксиданты (витамин Е, бетаин) Патогенез ХГС + НАСГ • Снижение инсулинорезистентности (метформин, пиоглитазон, розиглитазон) Инсулинорезистентность • Гепатопротекторы • Лептинемия (УДХК, ЭФЛ) • Повышенный синтез TNFa • Гиполипидемическая терапия • HVC, G 1 a (HGV ? ? ? ) (ингибиторы-ГМГ-Ко. А-редуктазы) • Снижение синтеза ТНФa (пентоксифиллин)
Методы коррекции неблагоприятных факторов ХГС + НАСГ (стеатоз) Метаболический синдром • • Избыточная масса тела Гиперлипидемия НТГ, гипергликемия Артериальная гипертензия • Гипокалорийная диета (2200 ккал/сут) • Аэробные дозированные физические нагрузки (40 -60 мин/сут) • Хирургические методы снижения массы тела (установление баллона в желудке, наложение желудочнокишечного анастомоза) • Антиоксиданты (витамин Е, бетаин) Патогенез ХГС + НАСГ • Снижение инсулинорезистентности (метформин, пиоглитазон, розиглитазон) Инсулинорезистентность • Гепатопротекторы • Лептинемия (УДХК, ЭФЛ) • Повышенный синтез TNFa • Гиполипидемическая терапия • HVC, G 1 a (HGV ? ? ? ) (ингибиторы-ГМГ-Ко. А-редуктазы) • Снижение синтеза ТНФa (пентоксифиллин)
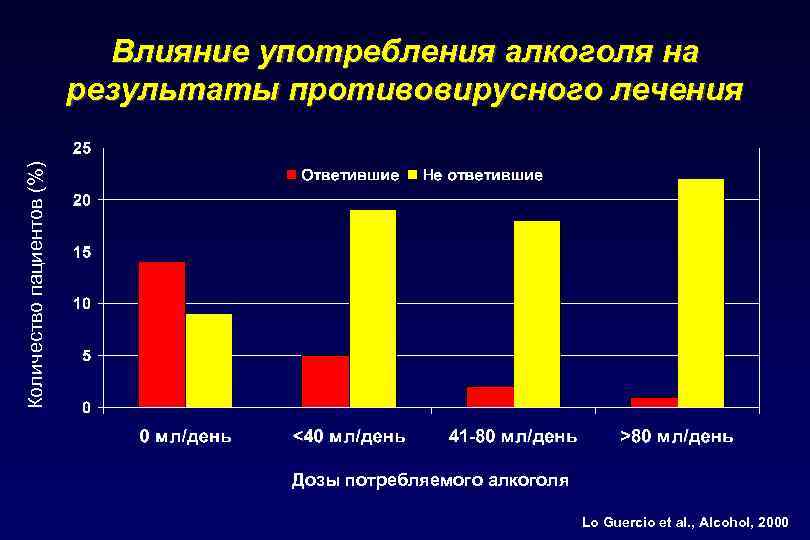 Количество пациентов (%) Влияние употребления алкоголя на результаты противовирусного лечения Дозы потребляемого алкоголя Lo Guercio et al. , Alcohol, 2000
Количество пациентов (%) Влияние употребления алкоголя на результаты противовирусного лечения Дозы потребляемого алкоголя Lo Guercio et al. , Alcohol, 2000
 Синдром перегрузки железом при ХГС Определение мутаций HFE-гена (C 282 Y, H 63 D) Кровопускания до начала лечения / десферал, эксиджат Гепатобиоптат. Включения железа в цитоплазме отдельных клеток ретикулоэндотелиальной системы. Окраска по Перлсу. х 250
Синдром перегрузки железом при ХГС Определение мутаций HFE-гена (C 282 Y, H 63 D) Кровопускания до начала лечения / десферал, эксиджат Гепатобиоптат. Включения железа в цитоплазме отдельных клеток ретикулоэндотелиальной системы. Окраска по Перлсу. х 250
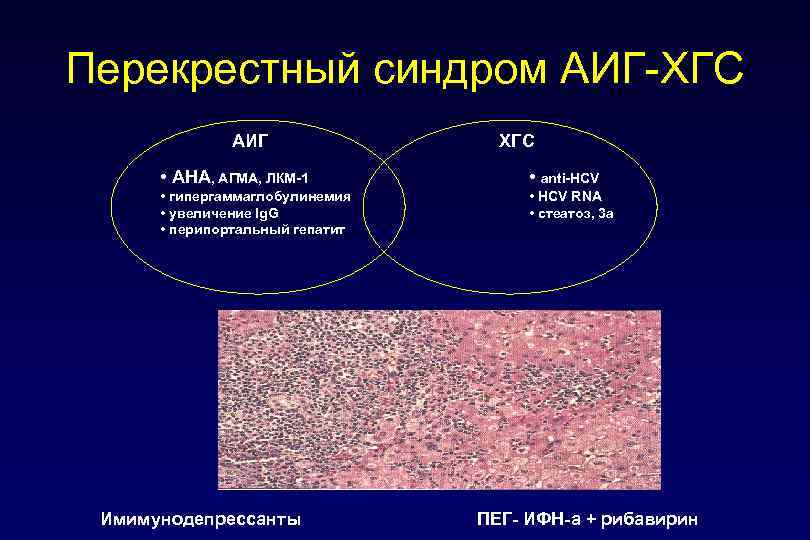 Перекрестный синдром АИГ-ХГС АИГ ХГС • АНА, АГМА, ЛКМ-1 • anti-HCV • гипергаммаглобулинемия • увеличение Ig. G • перипортальный гепатит • HCV RNA • стеатоз, 3 а Имимунодепрессанты ПЕГ- ИФН-a + рибавирин
Перекрестный синдром АИГ-ХГС АИГ ХГС • АНА, АГМА, ЛКМ-1 • anti-HCV • гипергаммаглобулинемия • увеличение Ig. G • перипортальный гепатит • HCV RNA • стеатоз, 3 а Имимунодепрессанты ПЕГ- ИФН-a + рибавирин
 Жизненный цикл ВГС и возможные мишени направленного воздействия противовирусных препаратов Связывание с рецептором и эндоцитоз Нейтрализующие антитела, Ингибиторы входа вируса Транспорт и высвобождение Ингибиторы гликозилирования Слияние и «раздевание» Вирусная сборка (+) RNA Антисмысловые олигонуклеотиды Ингибиторы циклофилина Трансляция и полипротеиновый процессинг Репликация РНК Ингибиторы NS 3/4 протеазы Ингибиторы NS 5 B полимеразы Нуклеоз(т)идные Ненуклеоз(т)идные Ингибиторы NS 5 A* * Роль в ЖЦ ВГС точно не установлена 5 – Core E 1 E 2 P 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A NS 5 B – 3 Asselah T et al. Liver International 2012
Жизненный цикл ВГС и возможные мишени направленного воздействия противовирусных препаратов Связывание с рецептором и эндоцитоз Нейтрализующие антитела, Ингибиторы входа вируса Транспорт и высвобождение Ингибиторы гликозилирования Слияние и «раздевание» Вирусная сборка (+) RNA Антисмысловые олигонуклеотиды Ингибиторы циклофилина Трансляция и полипротеиновый процессинг Репликация РНК Ингибиторы NS 3/4 протеазы Ингибиторы NS 5 B полимеразы Нуклеоз(т)идные Ненуклеоз(т)идные Ингибиторы NS 5 A* * Роль в ЖЦ ВГС точно не установлена 5 – Core E 1 E 2 P 7 NS 2 NS 3 NS 4 A NS 4 B NS 5 A NS 5 B – 3 Asselah T et al. Liver International 2012
 Первая генерация ингибиторов NS 3/4 A протеазы HCV: телапревир и боцепревир в тройной терапии Peg-IFN Ribavirin Ингибиторы протеазы
Первая генерация ингибиторов NS 3/4 A протеазы HCV: телапревир и боцепревир в тройной терапии Peg-IFN Ribavirin Ингибиторы протеазы
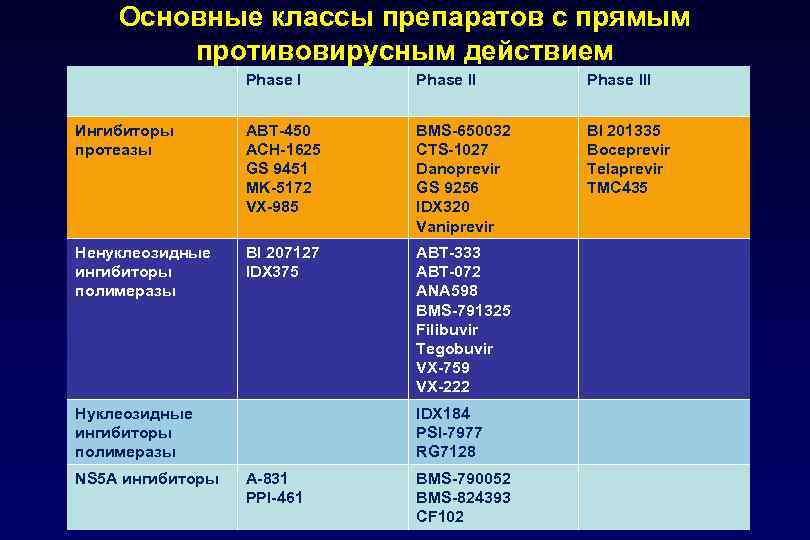 Основные классы препаратов с прямым противовирусным действием Phase III Ингибиторы протеазы ABT-450 ACH-1625 GS 9451 MK-5172 VX-985 BMS-650032 CTS-1027 Danoprevir GS 9256 IDX 320 Vaniprevir BI 201335 Boceprevir Telaprevir TMC 435 Ненуклеозидные ингибиторы полимеразы BI 207127 IDX 375 ABT-333 ABT-072 ANA 598 BMS-791325 Filibuvir Tegobuvir VX-759 VX-222 Нуклеозидные ингибиторы полимеразы NS 5 A ингибиторы IDX 184 PSI-7977 RG 7128 A-831 PPI-461 BMS-790052 BMS-824393 CF 102
Основные классы препаратов с прямым противовирусным действием Phase III Ингибиторы протеазы ABT-450 ACH-1625 GS 9451 MK-5172 VX-985 BMS-650032 CTS-1027 Danoprevir GS 9256 IDX 320 Vaniprevir BI 201335 Boceprevir Telaprevir TMC 435 Ненуклеозидные ингибиторы полимеразы BI 207127 IDX 375 ABT-333 ABT-072 ANA 598 BMS-791325 Filibuvir Tegobuvir VX-759 VX-222 Нуклеозидные ингибиторы полимеразы NS 5 A ингибиторы IDX 184 PSI-7977 RG 7128 A-831 PPI-461 BMS-790052 BMS-824393 CF 102
 Терапия хронического гепатита В
Терапия хронического гепатита В
 Терапия хронического гепатита В «Цель - улучшение качества и продолжительности жизни за счет предотвращения прогрессирования болезни в ЦП (декомпенсирнованный) и ГЦК. … может быть достигнута в результате устойчивого подавления вирусной репликации … Однако полная вирусная эрадикация не наступает вследствие персистенции в ядре гепатоцита ccc. DNA (В 1)» Конечные точки терапии: 1. Элиминация HBs. Ag (+/- HBs. Ag сероконверсия) (А 1) 2. Длительная HBe. Ag сероконверсия (А 1) 3. Уровень ДНК ВГВ неопределяемый или < 2000 МЕ/мл (А 1)
Терапия хронического гепатита В «Цель - улучшение качества и продолжительности жизни за счет предотвращения прогрессирования болезни в ЦП (декомпенсирнованный) и ГЦК. … может быть достигнута в результате устойчивого подавления вирусной репликации … Однако полная вирусная эрадикация не наступает вследствие персистенции в ядре гепатоцита ccc. DNA (В 1)» Конечные точки терапии: 1. Элиминация HBs. Ag (+/- HBs. Ag сероконверсия) (А 1) 2. Длительная HBe. Ag сероконверсия (А 1) 3. Уровень ДНК ВГВ неопределяемый или < 2000 МЕ/мл (А 1)
 Рекомендации по лечению ХГВ • Keeffe EB, Dieterich DT, Han SH et al. A treatment algorithm for the management of chronic hepatitis B virus infection in the United States: an update. Clin Gastroenter Hepatol. 2006; 4: 936 -962. • AASLD - Lok AS, Mc. Mahon BJ. Chronic hepatitis B. Hepatol. 2007; 45: 507 -539. - Lok AS, Mc. Mahon BJ. Chronic hepatitis B: Update 2009. Hepatol. 2009; 50: 661 -662. • APASL - Liaw YF, Leung N, Kao JH et al. Chronic hepatitis B. Hepatol Int. 2008; 2: 263 -83. • EASL - Management of chronic hepatitis B virus infection. Hepatol. 2012; 57: 167– 185. • РГА - Рекомендации по ведению больных ХГВ 2009; 50 HBe. Ag (+) / HBe. Ag (-) ДНК ВГВ > 2 000 МЕ/мл АЛТ > ВГН A 2 -A 3 F 2 -F 4
Рекомендации по лечению ХГВ • Keeffe EB, Dieterich DT, Han SH et al. A treatment algorithm for the management of chronic hepatitis B virus infection in the United States: an update. Clin Gastroenter Hepatol. 2006; 4: 936 -962. • AASLD - Lok AS, Mc. Mahon BJ. Chronic hepatitis B. Hepatol. 2007; 45: 507 -539. - Lok AS, Mc. Mahon BJ. Chronic hepatitis B: Update 2009. Hepatol. 2009; 50: 661 -662. • APASL - Liaw YF, Leung N, Kao JH et al. Chronic hepatitis B. Hepatol Int. 2008; 2: 263 -83. • EASL - Management of chronic hepatitis B virus infection. Hepatol. 2012; 57: 167– 185. • РГА - Рекомендации по ведению больных ХГВ 2009; 50 HBe. Ag (+) / HBe. Ag (-) ДНК ВГВ > 2 000 МЕ/мл АЛТ > ВГН A 2 -A 3 F 2 -F 4
 Препараты для лечения хронического гепатита В - 2012 Peginterferon alfa-2 a 180 Peginterferon alfa-2 b 100 Lamivudine 100 1998 Interferon-alfa-2 b 5 -6 млн Tenofovir 245 Entecavir 0, 5; 1, 0 2002 Adefovir 10 2005 2006 Telbivudine 600 2008
Препараты для лечения хронического гепатита В - 2012 Peginterferon alfa-2 a 180 Peginterferon alfa-2 b 100 Lamivudine 100 1998 Interferon-alfa-2 b 5 -6 млн Tenofovir 245 Entecavir 0, 5; 1, 0 2002 Adefovir 10 2005 2006 Telbivudine 600 2008
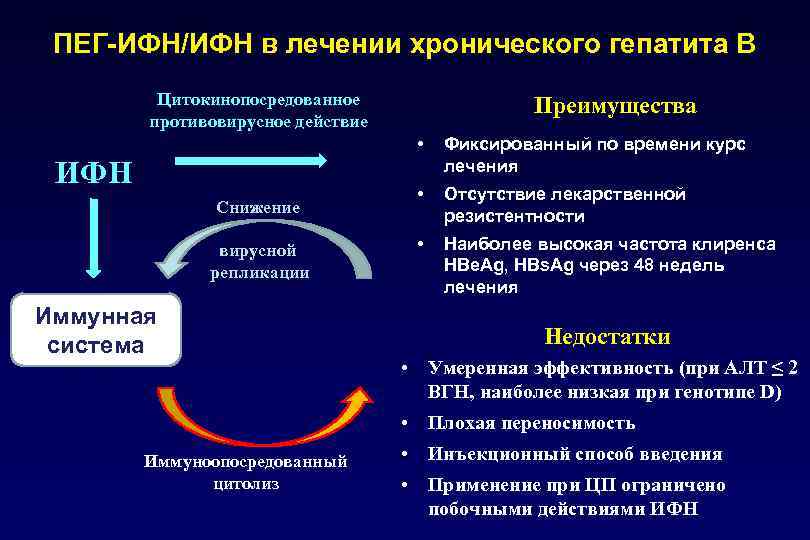 ПЕГ-ИФН/ИФН в лечении хронического гепатита В Цитокинопосредованное противовирусное действие Преимущества • ИФН Снижение вирусной репликации Иммунная система Фиксированный по времени курс лечения • Отсутствие лекарственной резистентности • Наиболее высокая частота клиренса HBe. Ag, HBs. Ag через 48 недель лечения Недостатки • Умеренная эффективность (при АЛТ ≤ 2 ВГН, наиболее низкая при генотипе D) • Плохая переносимость Иммуноопосредованный цитолиз • Инъекционный способ введения • Применение при ЦП ограничено побочными действиями ИФН
ПЕГ-ИФН/ИФН в лечении хронического гепатита В Цитокинопосредованное противовирусное действие Преимущества • ИФН Снижение вирусной репликации Иммунная система Фиксированный по времени курс лечения • Отсутствие лекарственной резистентности • Наиболее высокая частота клиренса HBe. Ag, HBs. Ag через 48 недель лечения Недостатки • Умеренная эффективность (при АЛТ ≤ 2 ВГН, наиболее низкая при генотипе D) • Плохая переносимость Иммуноопосредованный цитолиз • Инъекционный способ введения • Применение при ЦП ограничено побочными действиями ИФН
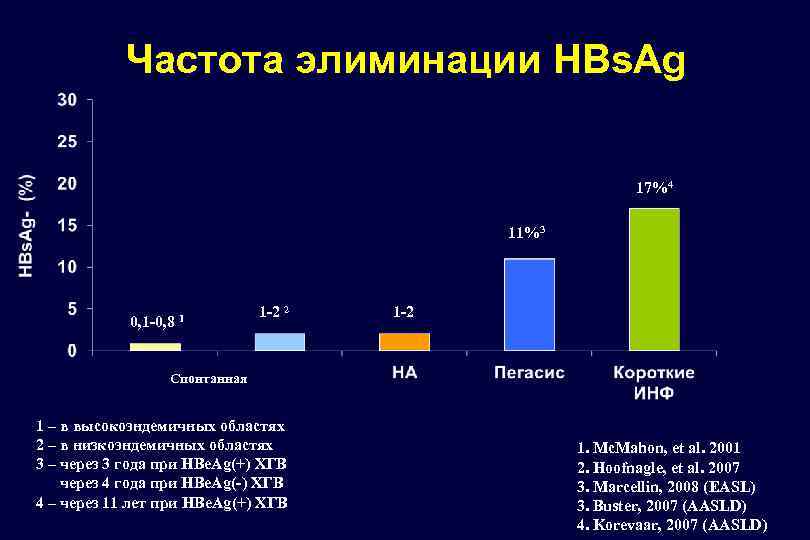 Частота элиминации HBs. Ag 17%4 11%3 0, 1 -0, 8 1 1 -2 2 1 -2 Спонтанная 1 – в высокоэндемичных областях 2 – в низкоэндемичных областях 3 – через 3 гoда при HBe. Ag(+) ХГВ через 4 года при HBe. Ag(-) ХГВ 4 – через 11 лет при HBe. Ag(+) ХГВ 1. Mc. Mahon, et al. 2001 2. Hoofnagle, et al. 2007 3. Marcellin, 2008 (EASL) 3. Buster, 2007 (AASLD) 4. Korevaar, 2007 (AASLD)
Частота элиминации HBs. Ag 17%4 11%3 0, 1 -0, 8 1 1 -2 2 1 -2 Спонтанная 1 – в высокоэндемичных областях 2 – в низкоэндемичных областях 3 – через 3 гoда при HBe. Ag(+) ХГВ через 4 года при HBe. Ag(-) ХГВ 4 – через 11 лет при HBe. Ag(+) ХГВ 1. Mc. Mahon, et al. 2001 2. Hoofnagle, et al. 2007 3. Marcellin, 2008 (EASL) 3. Buster, 2007 (AASLD) 4. Korevaar, 2007 (AASLD)
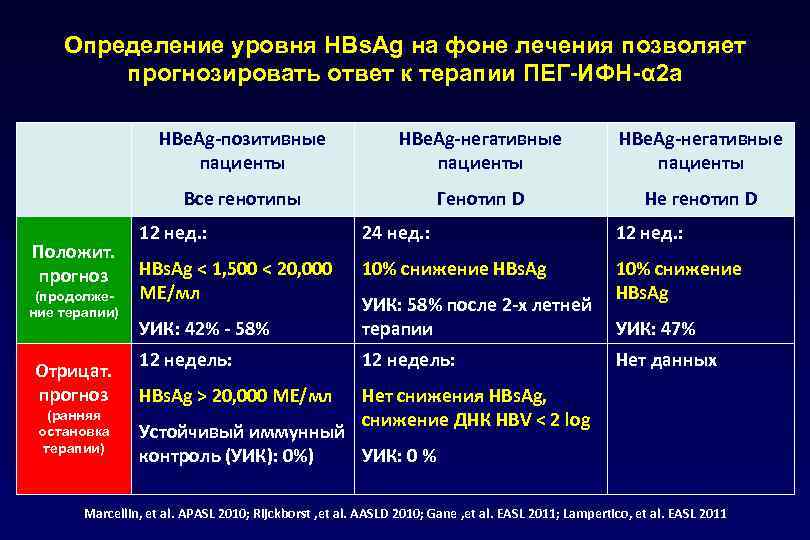 Определение уровня HBs. Ag на фоне лечения позволяет прогнозировать ответ к терапии ПЕГ-ИФН-α 2 a HBe. Ag-позитивные пациенты (продолжение терапии) Отрицат. прогноз (ранняя остановка терапии) HBe. Ag-негативные пациенты Все генотипы Положит. прогноз HBe. Ag-негативные пациенты Генотип D Не генотип D 12 нед. : 24 нед. : 12 нед. : HBs. Ag < 1, 500 < 20, 000 МЕ/мл 10% снижение HBs. Ag УИК: 42% - 58% УИК: 58% после 2 -х летней терапии 12 недель: HBs. Ag > 20, 000 МЕ/мл Нет снижения HBs. Ag, снижение ДНК HBV < 2 log УИК: 47% Нет данных Устойчивый иммунный контроль (УИК): 0%) УИК: 0 % Marcellin, et al. APASL 2010; Rijckborst , et al. AASLD 2010; Gane , et al. EASL 2011; Lampertico, et al. EASL 2011
Определение уровня HBs. Ag на фоне лечения позволяет прогнозировать ответ к терапии ПЕГ-ИФН-α 2 a HBe. Ag-позитивные пациенты (продолжение терапии) Отрицат. прогноз (ранняя остановка терапии) HBe. Ag-негативные пациенты Все генотипы Положит. прогноз HBe. Ag-негативные пациенты Генотип D Не генотип D 12 нед. : 24 нед. : 12 нед. : HBs. Ag < 1, 500 < 20, 000 МЕ/мл 10% снижение HBs. Ag УИК: 42% - 58% УИК: 58% после 2 -х летней терапии 12 недель: HBs. Ag > 20, 000 МЕ/мл Нет снижения HBs. Ag, снижение ДНК HBV < 2 log УИК: 47% Нет данных Устойчивый иммунный контроль (УИК): 0%) УИК: 0 % Marcellin, et al. APASL 2010; Rijckborst , et al. AASLD 2010; Gane , et al. EASL 2011; Lampertico, et al. EASL 2011
 Аналоги нуклеозидов в лечении ХГВ Преимущества • Высокая противовирусная эффективность на фоне лечения НА Прямое противовирусное действие (ИОТ) • Пероральный прием • Хорошая переносимость • Могут использоваться у пациентов с – декомпенсированным циррозом печени – после трансплантации органов – на фоне иммуносупрессивной /химиотерапии Синтетические молекулы, копирующие природные нуклеозиды и нуклеотиды (фосфорные эфиры нуклеотидов) Недостатки • Долгосрочная терапия • Существует риск развития резистентности • Меньшая частота клиренса HBe. Ag, HBs. Ag в течение 48 нед. лечения в сравнении с ИФН
Аналоги нуклеозидов в лечении ХГВ Преимущества • Высокая противовирусная эффективность на фоне лечения НА Прямое противовирусное действие (ИОТ) • Пероральный прием • Хорошая переносимость • Могут использоваться у пациентов с – декомпенсированным циррозом печени – после трансплантации органов – на фоне иммуносупрессивной /химиотерапии Синтетические молекулы, копирующие природные нуклеозиды и нуклеотиды (фосфорные эфиры нуклеотидов) Недостатки • Долгосрочная терапия • Существует риск развития резистентности • Меньшая частота клиренса HBe. Ag, HBs. Ag в течение 48 нед. лечения в сравнении с ИФН
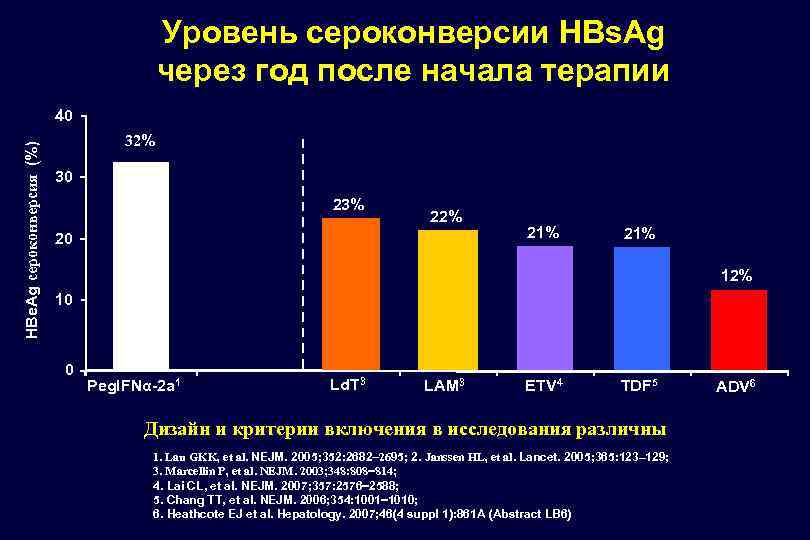 Уровень сероконверсии HBs. Ag через год после начала терапии HBe. Ag сероконверсия (%) 40 32% 30 23% 22% 20 21% 12% 10 0 Peg. IFNα-2 a 1 Ld. T 3 LAM 3 ETV 4 TDF 5 Дизайн и критерии включения в исследования различны 1. Lau GKK, et al. NEJM. 2005; 352: 2682− 2695; 2. Janssen HL, et al. Lancet. 2005; 365: 123– 129; 3. Marcellin P, et al. NEJM. 2003; 348: 808− 814; 4. Lai CL, et al. NEJM. 2007; 357: 2576− 2588; 5. Chang TT, et al. NEJM. 2006; 354: 1001− 1010; 6. Heathcote EJ et al. Hepatology. 2007; 46(4 suppl 1): 861 A (Abstract LB 6) ADV 6
Уровень сероконверсии HBs. Ag через год после начала терапии HBe. Ag сероконверсия (%) 40 32% 30 23% 22% 20 21% 12% 10 0 Peg. IFNα-2 a 1 Ld. T 3 LAM 3 ETV 4 TDF 5 Дизайн и критерии включения в исследования различны 1. Lau GKK, et al. NEJM. 2005; 352: 2682− 2695; 2. Janssen HL, et al. Lancet. 2005; 365: 123– 129; 3. Marcellin P, et al. NEJM. 2003; 348: 808− 814; 4. Lai CL, et al. NEJM. 2007; 357: 2576− 2588; 5. Chang TT, et al. NEJM. 2006; 354: 1001− 1010; 6. Heathcote EJ et al. Hepatology. 2007; 46(4 suppl 1): 861 A (Abstract LB 6) ADV 6
 Длительный мониторинг кинетики HBs. Ag и прогнозирование его элиминации у пациентов с ХГВ при лечении НА 30 пациентов получили различные схемы НА в среднем в течение 93 мес (49 – 123 мес) 3/26 5/26 13/26 S. Chevaliez, C. Hezode, M. Grare, J-M. Pawlotsky, AASLD 2010
Длительный мониторинг кинетики HBs. Ag и прогнозирование его элиминации у пациентов с ХГВ при лечении НА 30 пациентов получили различные схемы НА в среднем в течение 93 мес (49 – 123 мес) 3/26 5/26 13/26 S. Chevaliez, C. Hezode, M. Grare, J-M. Pawlotsky, AASLD 2010
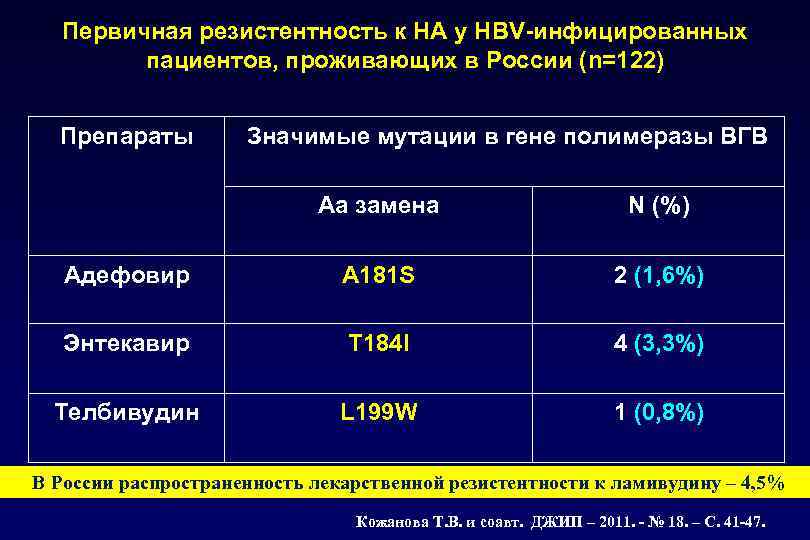 Первичная резистентность к НА у HBV-инфицированных пациентов, проживающих в России (n=122) Препараты Значимые мутации в гене полимеразы ВГВ Аа замена N (%) Адефовир A 181 S 2 (1, 6%) Энтекавир T 184 I 4 (3, 3%) Телбивудин L 199 W 1 (0, 8%) В России распространенность лекарственной резистентности к ламивудину – 4, 5% Кожанова Т. В. и соавт. ДЖИП – 2011. - № 18. – С. 41 -47.
Первичная резистентность к НА у HBV-инфицированных пациентов, проживающих в России (n=122) Препараты Значимые мутации в гене полимеразы ВГВ Аа замена N (%) Адефовир A 181 S 2 (1, 6%) Энтекавир T 184 I 4 (3, 3%) Телбивудин L 199 W 1 (0, 8%) В России распространенность лекарственной резистентности к ламивудину – 4, 5% Кожанова Т. В. и соавт. ДЖИП – 2011. - № 18. – С. 41 -47.
 Когда необходимо прекращать лечение? • ИФН/ПЕГ-ИФН - определенная длительность лечения – 12 мес. - устойчивость ответа: HBe. Ag (+) ~ 80 -90% HBs. Ag (-) ~ 15 -25% • НУКЛЕОЗ(Т)ИДНЫЕ АНАЛОГИ - HBe. Ag+ до наступления сероконверсии HBe. Ag + ≥ 12 мес (консолидирующая терапия) устойчивость ответа ~ 80% - HBe. Ag-: до наступления клиренса HBs. Ag? - цирроз печени: пожизненно?
Когда необходимо прекращать лечение? • ИФН/ПЕГ-ИФН - определенная длительность лечения – 12 мес. - устойчивость ответа: HBe. Ag (+) ~ 80 -90% HBs. Ag (-) ~ 15 -25% • НУКЛЕОЗ(Т)ИДНЫЕ АНАЛОГИ - HBe. Ag+ до наступления сероконверсии HBe. Ag + ≥ 12 мес (консолидирующая терапия) устойчивость ответа ~ 80% - HBe. Ag-: до наступления клиренса HBs. Ag? - цирроз печени: пожизненно?
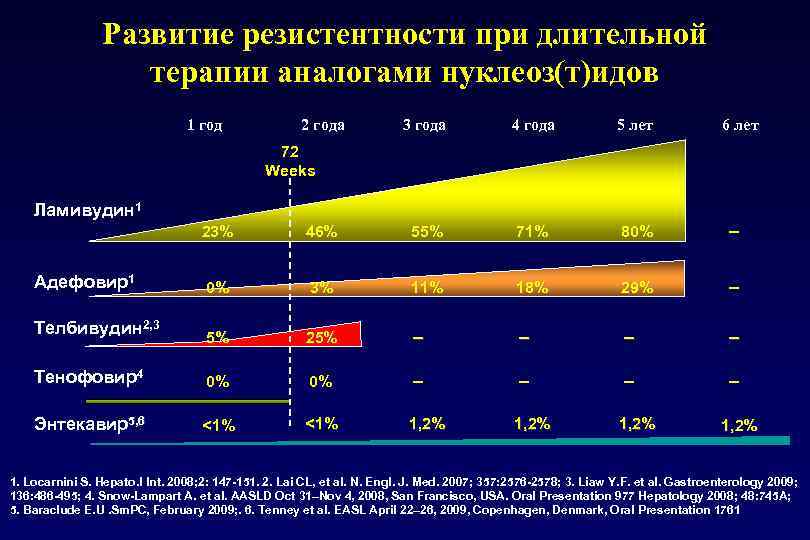 Развитие резистентности при длительной терапии аналогами нуклеоз(т)идов 1 год 2 года 3 года 4 года 5 лет 6 лет 72 Weeks Ламивудин 1 23% Tенофовир4 Энтекавир5, 6 71% 80% – 3% 11% 18% 29% – 5% Телбивудин 2, 3 55% 0% Адефовир1 46% 25% – – 0% 0% – – <1% 1, 2% 1. Locarnini S. Hepato. l Int. 2008; 2: 147 -151. 2. Lai CL, et al. N. Engl. J. Med. 2007; 357: 2576 -2578; 3. Liaw Y. F. et al. Gastroenterology 2009; 136: 486 -495; 4. Snow-Lampart A. et al. AASLD Oct 31–Nov 4, 2008, San Francisco, USA. Oral Presentation 977 Hepatology 2008; 48: 745 A; 5. Baraclude E. U. Sm. PC, February 2009; . 6. Tenney et al. EASL April 22– 26, 2009, Copenhagen, Denmark, Oral Presentation 1761
Развитие резистентности при длительной терапии аналогами нуклеоз(т)идов 1 год 2 года 3 года 4 года 5 лет 6 лет 72 Weeks Ламивудин 1 23% Tенофовир4 Энтекавир5, 6 71% 80% – 3% 11% 18% 29% – 5% Телбивудин 2, 3 55% 0% Адефовир1 46% 25% – – 0% 0% – – <1% 1, 2% 1. Locarnini S. Hepato. l Int. 2008; 2: 147 -151. 2. Lai CL, et al. N. Engl. J. Med. 2007; 357: 2576 -2578; 3. Liaw Y. F. et al. Gastroenterology 2009; 136: 486 -495; 4. Snow-Lampart A. et al. AASLD Oct 31–Nov 4, 2008, San Francisco, USA. Oral Presentation 977 Hepatology 2008; 48: 745 A; 5. Baraclude E. U. Sm. PC, February 2009; . 6. Tenney et al. EASL April 22– 26, 2009, Copenhagen, Denmark, Oral Presentation 1761
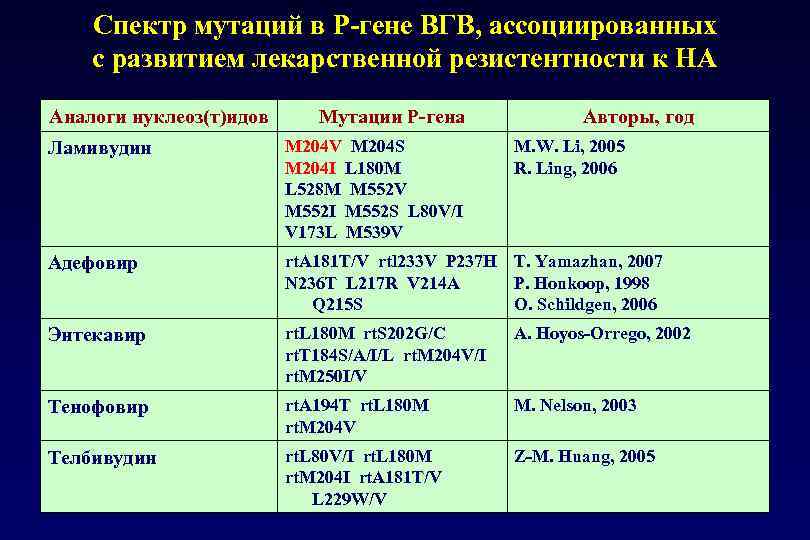 Спектр мутаций в Р-гене ВГВ, ассоциированных с развитием лекарственной резистентности к НА Аналоги нуклеоз(т)идов Мутации Р-гена Авторы, год Ламивудин M 204 V M 204 S M 204 I L 180 M L 528 M M 552 V M 552 I M 552 S L 80 V/I V 173 L M 539 V M. W. Li, 2005 R. Ling, 2006 Адефовир rt. A 181 T/V rtl 233 V P 237 H T. Yamazhan, 2007 N 236 T L 217 R V 214 A P. Honkoop, 1998 Q 215 S O. Schildgen, 2006 Энтекавир rt. L 180 M rt. S 202 G/C rt. T 184 S/A/I/L rt. M 204 V/I rt. M 250 I/V A. Hoyos-Orrego, 2002 Тенофовир rt. A 194 T rt. L 180 M rt. M 204 V М. Nelson, 2003 Телбивудин rt. L 80 V/I rt. L 180 M rt. M 204 I rt. A 181 T/V L 229 W/V Z-M. Huang, 2005
Спектр мутаций в Р-гене ВГВ, ассоциированных с развитием лекарственной резистентности к НА Аналоги нуклеоз(т)идов Мутации Р-гена Авторы, год Ламивудин M 204 V M 204 S M 204 I L 180 M L 528 M M 552 V M 552 I M 552 S L 80 V/I V 173 L M 539 V M. W. Li, 2005 R. Ling, 2006 Адефовир rt. A 181 T/V rtl 233 V P 237 H T. Yamazhan, 2007 N 236 T L 217 R V 214 A P. Honkoop, 1998 Q 215 S O. Schildgen, 2006 Энтекавир rt. L 180 M rt. S 202 G/C rt. T 184 S/A/I/L rt. M 204 V/I rt. M 250 I/V A. Hoyos-Orrego, 2002 Тенофовир rt. A 194 T rt. L 180 M rt. M 204 V М. Nelson, 2003 Телбивудин rt. L 80 V/I rt. L 180 M rt. M 204 I rt. A 181 T/V L 229 W/V Z-M. Huang, 2005
 АЛГОРИТМ МОНИТОРИРОВАНИЯ БОЛЬНЫХ ХГВ, ПОЛУЧАЮЩИХ ТЕРАПИЮ АНАЛОГАМИ НУКЛЕОЗ(Т)ИДОВ Оценка вирусологического ответа на 12 нед. (смена терапии если нет снижения на 1 log 10 МЕ/мл) Оценка вирусологического ответа на 24 неделе Полный вирусологический ответ Продолжить лечение с оценкой уровня виремии каждые 24 нед. Частичный вирусологич. ответ (60 < ДНК ВГВ < 2000 МЕ/мл) Препарат с низким генетическим барьером резистентности: добавить не имеющий перекрестной резистентности второй препарат или заменить на него Препарат с высоким генетическим барьером резистентности: продолжать лечение до 48 нед. и более Недостаточный вирусол. ответ (ДНК ВГВ > 2000 МЕ/мл) Препарат с субоптимальным противовирусным действием: продолжать лечение до 48 нед. Есть полный ответ: продолжить лечение Keeffe EB, et al. Clin Gastroenterol Hepatol 2008; 6: 1314 -39. Сменить препарат или добавить не имеющий перекрестной резистентности второй препарат Нет полного ответа: добавить не имеющий перекрестной резистентности более мощный препарат
АЛГОРИТМ МОНИТОРИРОВАНИЯ БОЛЬНЫХ ХГВ, ПОЛУЧАЮЩИХ ТЕРАПИЮ АНАЛОГАМИ НУКЛЕОЗ(Т)ИДОВ Оценка вирусологического ответа на 12 нед. (смена терапии если нет снижения на 1 log 10 МЕ/мл) Оценка вирусологического ответа на 24 неделе Полный вирусологический ответ Продолжить лечение с оценкой уровня виремии каждые 24 нед. Частичный вирусологич. ответ (60 < ДНК ВГВ < 2000 МЕ/мл) Препарат с низким генетическим барьером резистентности: добавить не имеющий перекрестной резистентности второй препарат или заменить на него Препарат с высоким генетическим барьером резистентности: продолжать лечение до 48 нед. и более Недостаточный вирусол. ответ (ДНК ВГВ > 2000 МЕ/мл) Препарат с субоптимальным противовирусным действием: продолжать лечение до 48 нед. Есть полный ответ: продолжить лечение Keeffe EB, et al. Clin Gastroenterol Hepatol 2008; 6: 1314 -39. Сменить препарат или добавить не имеющий перекрестной резистентности второй препарат Нет полного ответа: добавить не имеющий перекрестной резистентности более мощный препарат
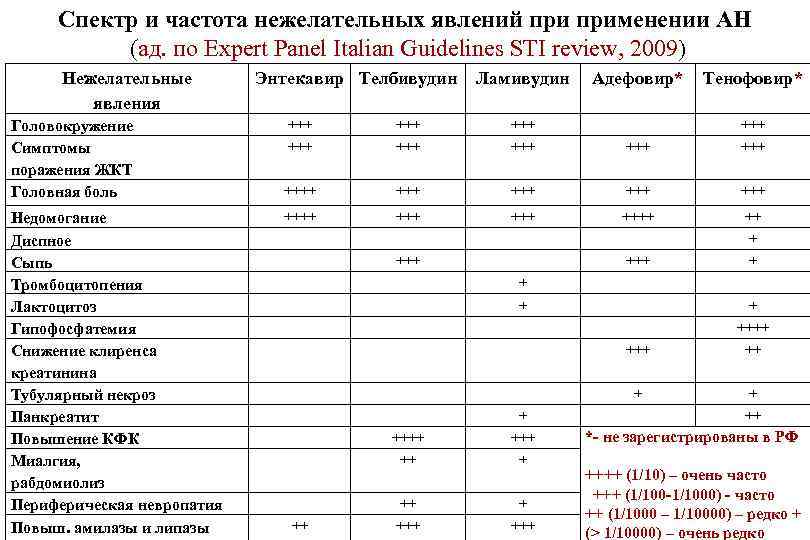 Спектр и частота нежелательных явлений применении АН (ад. по Expert Panel Italian Guidelines STI review, 2009) Нежелательные явления Головокружение Симптомы поражения ЖКТ Головная боль Недомогание Диспное Сыпь Тромбоцитопения Лактоцитоз Гипофосфатемия Снижение клиренса креатинина Тубулярный некроз Панкреатит Повышение КФК Миалгия, рабдомиолиз Периферическая невропатия Повыш. амилазы и липазы Энтекавир Телбивудин Ламивудин Адефовир* Тенофовир* +++ +++ ++++ +++ ++++ +++ + + ++++ ++ +++ ++ *- не зарегистрированы в РФ ++++ (1/10) – очень часто +++ (1/100 -1/1000) - часто ++ (1/1000 – 1/10000) – редко + (> 1/10000) – очень редко
Спектр и частота нежелательных явлений применении АН (ад. по Expert Panel Italian Guidelines STI review, 2009) Нежелательные явления Головокружение Симптомы поражения ЖКТ Головная боль Недомогание Диспное Сыпь Тромбоцитопения Лактоцитоз Гипофосфатемия Снижение клиренса креатинина Тубулярный некроз Панкреатит Повышение КФК Миалгия, рабдомиолиз Периферическая невропатия Повыш. амилазы и липазы Энтекавир Телбивудин Ламивудин Адефовир* Тенофовир* +++ +++ ++++ +++ ++++ +++ + + ++++ ++ +++ ++ *- не зарегистрированы в РФ ++++ (1/10) – очень часто +++ (1/100 -1/1000) - часто ++ (1/1000 – 1/10000) – редко + (> 1/10000) – очень редко
 Нуклеотидные/зидные аналоги в целом безопасны, но не совершенны Ламивудин − Были описаны случаи мышечных расстройств, включая рабдомиолиз Адефовир − Риск почечных нарушений Энтекавир − Выявлен риск развития опухоли у мышей и крыс в 2 -годичном исследовании Телбивудин − Случаи миопатии − Комбинированная терапия с ПЕГ-ИНФ – повышенный риск периферической нейропатии Zeffix® (lamivudine) Sm. PC 2007 Hepsera® (adefovir dipivoxil) Sm. PC 2007 Baraclude® (entecavir) Sm. PC 2007 Sebivo® (telbivudine) Sm. PC 2008 Viread® (Tenofovir DF) HIV Sm. PC 2007
Нуклеотидные/зидные аналоги в целом безопасны, но не совершенны Ламивудин − Были описаны случаи мышечных расстройств, включая рабдомиолиз Адефовир − Риск почечных нарушений Энтекавир − Выявлен риск развития опухоли у мышей и крыс в 2 -годичном исследовании Телбивудин − Случаи миопатии − Комбинированная терапия с ПЕГ-ИНФ – повышенный риск периферической нейропатии Zeffix® (lamivudine) Sm. PC 2007 Hepsera® (adefovir dipivoxil) Sm. PC 2007 Baraclude® (entecavir) Sm. PC 2007 Sebivo® (telbivudine) Sm. PC 2008 Viread® (Tenofovir DF) HIV Sm. PC 2007
 Профили безопасности НА Исследования генотоксичности (in vitro) Исследования канцерогенности (в эксперименте) Категория препаратов по применению у беременных * Показан риск генотоксичности Риск канцерогенеза не выявлен C Энтекавир Показан риск генотоксичности Показан риск канцерогенеза C Телбивудин Генотоксичность не выявлена Риск канцерогенеза не выявлен B Ламивудин 1. 2. 3. 4. Entecavir (BMS-200475) Antiviral drugs advisory committee (AVDAC) briefing document: 11 Mar 2005; Bridges E. D. Shanghai-Hong Kong Intern Liver Congress, 2006, Poster 179; Watts DH. Amer J Obstetrics Gynecology, 2004, 191, 985 -992; Bryant ML Antimicrob Agents Chemother. , 2001, 45(1): 229 -235. * Категория В означает, что в исследованиях данного препарата у животных доказано отсутствие риска, исследования у человека не проводились (утверждено FDA) Категория С означает, что исследования на животных показали риск для плода, необходимо соотносить пользу и риск применения данного препарата у беременной женщины
Профили безопасности НА Исследования генотоксичности (in vitro) Исследования канцерогенности (в эксперименте) Категория препаратов по применению у беременных * Показан риск генотоксичности Риск канцерогенеза не выявлен C Энтекавир Показан риск генотоксичности Показан риск канцерогенеза C Телбивудин Генотоксичность не выявлена Риск канцерогенеза не выявлен B Ламивудин 1. 2. 3. 4. Entecavir (BMS-200475) Antiviral drugs advisory committee (AVDAC) briefing document: 11 Mar 2005; Bridges E. D. Shanghai-Hong Kong Intern Liver Congress, 2006, Poster 179; Watts DH. Amer J Obstetrics Gynecology, 2004, 191, 985 -992; Bryant ML Antimicrob Agents Chemother. , 2001, 45(1): 229 -235. * Категория В означает, что в исследованиях данного препарата у животных доказано отсутствие риска, исследования у человека не проводились (утверждено FDA) Категория С означает, что исследования на животных показали риск для плода, необходимо соотносить пользу и риск применения данного препарата у беременной женщины
 Рекомендации беременным женщинам, инфицированным HBV Умеренная активность ХГВ, низкий уровень виремии - ПВТ до беременности Умеренная активность ХГВ (но не ЦП) - ПВТ до беременности, при получении ответа прекращение терапии до беременности Прогрессирующее течение ХГВ – ПВТ до и во время беременности, продолжение после родов Умеренная активность ХГВ, высокий уровень виремии – ПВТ в 3 -м триместре беременности препаратами категории «В» (телбивудин, тенофовир) Wedemeyer H, et al. Dtsch Med Wochenschr. 2007; 132: 1775 -1782. EASL Clinical Practice Guidelines. J Hepatol.
Рекомендации беременным женщинам, инфицированным HBV Умеренная активность ХГВ, низкий уровень виремии - ПВТ до беременности Умеренная активность ХГВ (но не ЦП) - ПВТ до беременности, при получении ответа прекращение терапии до беременности Прогрессирующее течение ХГВ – ПВТ до и во время беременности, продолжение после родов Умеренная активность ХГВ, высокий уровень виремии – ПВТ в 3 -м триместре беременности препаратами категории «В» (телбивудин, тенофовир) Wedemeyer H, et al. Dtsch Med Wochenschr. 2007; 132: 1775 -1782. EASL Clinical Practice Guidelines. J Hepatol.
 ХВГ и беременность • Все новорожденные от матерей, позитивных по HBs. Ag, подлежат обязательной иммунопрофилактике ВГВ-инфекции • Первое введение вакцины (а у детей от матерей, позитивных по HBs. Ag и/или HBe. Ag, в сочетании с введением HBIg) должно проводиться в первые 12 часов после рождения, последующие - через 1 и 6 мес. , либо через 1, 2, 6 (12) мес. после введения первой дозы (быстрая схема) • HBIg - «Антигеп» ( «Биомед» , Пермь) и «Гепатект» ( «Biotest Pharma» , Германия). Оба препарата предназначены для внутривенного введения и содержат анти-НBs в концентрациях не менее 100 МЕ и 50 МЕ на 100 мг белков плазмы человека
ХВГ и беременность • Все новорожденные от матерей, позитивных по HBs. Ag, подлежат обязательной иммунопрофилактике ВГВ-инфекции • Первое введение вакцины (а у детей от матерей, позитивных по HBs. Ag и/или HBe. Ag, в сочетании с введением HBIg) должно проводиться в первые 12 часов после рождения, последующие - через 1 и 6 мес. , либо через 1, 2, 6 (12) мес. после введения первой дозы (быстрая схема) • HBIg - «Антигеп» ( «Биомед» , Пермь) и «Гепатект» ( «Biotest Pharma» , Германия). Оба препарата предназначены для внутривенного введения и содержат анти-НBs в концентрациях не менее 100 МЕ и 50 МЕ на 100 мг белков плазмы человека
 Traditional Chinese Medicines (200 растений) Лекарственные средства традиционной китайской медицины могут быть эффективнее дорогостоящих препаратов для лечения ХГВ Zhang L. , Wang G. , Hou W. et al. Contemporary Clinical Research of Traditional Chinese Medicines for Chronic Hepatitis B in China: An Analytical Review Hepatology, 2010; 51(2): 690– 698. Ивашкин В. Т. , Морозова М. А. , Маевская М. В. , Федосьина Е. А. Препараты растительного происхождения в лечении гепатита С. РЖГГК – 2— 9; 9: 70 -75.
Traditional Chinese Medicines (200 растений) Лекарственные средства традиционной китайской медицины могут быть эффективнее дорогостоящих препаратов для лечения ХГВ Zhang L. , Wang G. , Hou W. et al. Contemporary Clinical Research of Traditional Chinese Medicines for Chronic Hepatitis B in China: An Analytical Review Hepatology, 2010; 51(2): 690– 698. Ивашкин В. Т. , Морозова М. А. , Маевская М. В. , Федосьина Е. А. Препараты растительного происхождения в лечении гепатита С. РЖГГК – 2— 9; 9: 70 -75.
 Терапия хронического гепатита D
Терапия хронического гепатита D
 I. Терапия хронического гепатита D EASL Clinical Practice Guidelinees: management of chronic hepatitis B J. Hepatol. 2009; Vol. 50: 227 -242. • • • Тимозин Рибавирин Ламивудин Фамцикловир Адефовир не эффективны ИФН-альфа 5 МЕ ежедневно или 9 МЕ три раза/нед (СВО 23%) Пег. ИФН-альфа 180 мкг/нед (СВО 25 -27%) 48 -72 -96 нед
I. Терапия хронического гепатита D EASL Clinical Practice Guidelinees: management of chronic hepatitis B J. Hepatol. 2009; Vol. 50: 227 -242. • • • Тимозин Рибавирин Ламивудин Фамцикловир Адефовир не эффективны ИФН-альфа 5 МЕ ежедневно или 9 МЕ три раза/нед (СВО 23%) Пег. ИФН-альфа 180 мкг/нед (СВО 25 -27%) 48 -72 -96 нед
 II. Терапия хронического гепатита дельта • HIDIT I - Peg. IFN-alfa 2 a (СВО 28%) - Аdefovir Германия, Турция, Греция 92 больных Wedemeyer H. , Yurdaydin C. , Dalekos G. et al. Peginterferon plus Adefovir versus either drug alone for hepatitis delta // NEJM. 2011; 364: 322 -331. • HIDIT II – The Hep-Net International Delta Hepatitis Interventional Trial II (HIDIT-II) - Июнь 2009 г. - май 2017 г. Phase II: 96 нед. 70 пациентов 1: 1 Peg. IFN-alfa 2 a (180 мкг) + placebo versus Peg. IFN-alfa 2 a (180 мкг) + Tenofovir (245 мг) Наблюдение 358 нед.
II. Терапия хронического гепатита дельта • HIDIT I - Peg. IFN-alfa 2 a (СВО 28%) - Аdefovir Германия, Турция, Греция 92 больных Wedemeyer H. , Yurdaydin C. , Dalekos G. et al. Peginterferon plus Adefovir versus either drug alone for hepatitis delta // NEJM. 2011; 364: 322 -331. • HIDIT II – The Hep-Net International Delta Hepatitis Interventional Trial II (HIDIT-II) - Июнь 2009 г. - май 2017 г. Phase II: 96 нед. 70 пациентов 1: 1 Peg. IFN-alfa 2 a (180 мкг) + placebo versus Peg. IFN-alfa 2 a (180 мкг) + Tenofovir (245 мг) Наблюдение 358 нед.
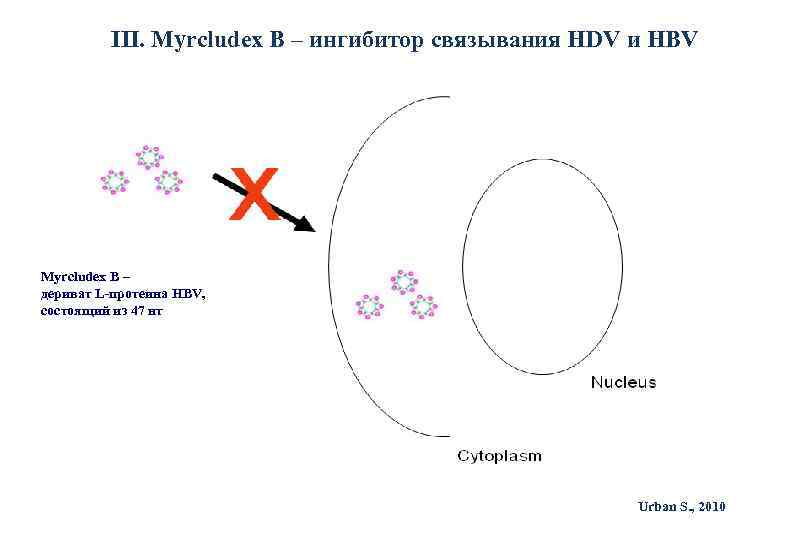 III. Myrcludex B – ингибитор связывания HDV и HBV Myrcludex B – дериват L-протеина HBV, состоящий из 47 нт Urban S. , 2010
III. Myrcludex B – ингибитор связывания HDV и HBV Myrcludex B – дериват L-протеина HBV, состоящий из 47 нт Urban S. , 2010
 IV. Биологически активные добавки, разработанные на основе рецептов тибетской народной медицины Миробаланхебула «Золотистый» Миробаланхебула Гранат Эмблика Ластовник Краснодев Латук степной Цветки шиповника Мумие Шафран Мордовник Мускатный орех………. .
IV. Биологически активные добавки, разработанные на основе рецептов тибетской народной медицины Миробаланхебула «Золотистый» Миробаланхебула Гранат Эмблика Ластовник Краснодев Латук степной Цветки шиповника Мумие Шафран Мордовник Мускатный орех………. .
 Адъювантная (вспомогательная, дополняющая) терапия хронических вирусных гепатитов
Адъювантная (вспомогательная, дополняющая) терапия хронических вирусных гепатитов
 Адъювантная терапия • Имеет самостоятельное значение на различных этапах ведения пациента • Используется как дополнительное средство в период проведения противовирусной терапии • Является единственным способом лечения при невозможности проведения противовирусной терапии • Применяется для лечения сопутствующих заболеваний, в том числе печени 154
Адъювантная терапия • Имеет самостоятельное значение на различных этапах ведения пациента • Используется как дополнительное средство в период проведения противовирусной терапии • Является единственным способом лечения при невозможности проведения противовирусной терапии • Применяется для лечения сопутствующих заболеваний, в том числе печени 154
 УРСОДЕОКСИХОЛЕВАЯ КИСЛОТА 3 a, 7 b-дигидрокси-5 b-холановая кислота СOOH 13 -15 мг/кг D А HO 1. Цитопротективное 2. Литолитическое 3. Антиоксидантное 4. Антиапоптотическое 5. Холеретическое 6. Гипохолестеринемическое 7. Иммуносупрессивное OH 7 üУДХК – 7 -бета-эпимер хенодеоксихолевой кислоты üУДХК – третичная желчная кислота, образуется эндогенным путем в организме человека; 3% всего пула желчных кислот üУДХК – наиболее гидрофильная из желчных кислот üУДХК – первое сообщение об использовании при ХЗП в 1961 г.
УРСОДЕОКСИХОЛЕВАЯ КИСЛОТА 3 a, 7 b-дигидрокси-5 b-холановая кислота СOOH 13 -15 мг/кг D А HO 1. Цитопротективное 2. Литолитическое 3. Антиоксидантное 4. Антиапоптотическое 5. Холеретическое 6. Гипохолестеринемическое 7. Иммуносупрессивное OH 7 üУДХК – 7 -бета-эпимер хенодеоксихолевой кислоты üУДХК – третичная желчная кислота, образуется эндогенным путем в организме человека; 3% всего пула желчных кислот üУДХК – наиболее гидрофильная из желчных кислот üУДХК – первое сообщение об использовании при ХЗП в 1961 г.
 Фосфоглив и ВГС-инфекция Глицирризиновая кислота оказывает - противовоспалительное действие - влияет на выживаемость пациентов с подострой печеночной недостаточностью (в сочетании с глицином и цистеином) - улучшает функцию печени при циррозе с признаками активности - может предупреждать развитие ГЦК ФОСФАТИДИЛХОЛИН – мембраностабилизирующее д-е Соль ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ - противовирусное действие Капсулы – 65 мг фосфатидилхолина и 35 мг тринатриевой соли глицирризина Лиофилизат (2, 5 г) : 500 мг фосфатидилхолина и 200 мг глицирризина (в 10 мл апирогенной воды, 3/нед (6 -12 мес. ) Dhiman R. K. , Chawla Y. K. Dig. Dis. Sci. 2005 Oct; 50(10): 1807 -1812
Фосфоглив и ВГС-инфекция Глицирризиновая кислота оказывает - противовоспалительное действие - влияет на выживаемость пациентов с подострой печеночной недостаточностью (в сочетании с глицином и цистеином) - улучшает функцию печени при циррозе с признаками активности - может предупреждать развитие ГЦК ФОСФАТИДИЛХОЛИН – мембраностабилизирующее д-е Соль ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ - противовирусное действие Капсулы – 65 мг фосфатидилхолина и 35 мг тринатриевой соли глицирризина Лиофилизат (2, 5 г) : 500 мг фосфатидилхолина и 200 мг глицирризина (в 10 мл апирогенной воды, 3/нед (6 -12 мес. ) Dhiman R. K. , Chawla Y. K. Dig. Dis. Sci. 2005 Oct; 50(10): 1807 -1812
 Препараты, содержащие силимарин основное действующее вещество – силибинин, получаемый из расторопши пятнистой – чертополоха Антиоксидантное действие - связывает свободные радикалы - снижает уровень ПОЛ Антифибротическое действие - тормозит синтез и отложение коллагена Антитоксическое действие - препятствует проникновению в клетку ядов бледной поганки: фаллоидина и а-аманитина 140 мг х 3 не менее 3 мес.
Препараты, содержащие силимарин основное действующее вещество – силибинин, получаемый из расторопши пятнистой – чертополоха Антиоксидантное действие - связывает свободные радикалы - снижает уровень ПОЛ Антифибротическое действие - тормозит синтез и отложение коллагена Антитоксическое действие - препятствует проникновению в клетку ядов бледной поганки: фаллоидина и а-аманитина 140 мг х 3 не менее 3 мес.
 Спектр лекарственных эффектов гепатопротекторов
Спектр лекарственных эффектов гепатопротекторов
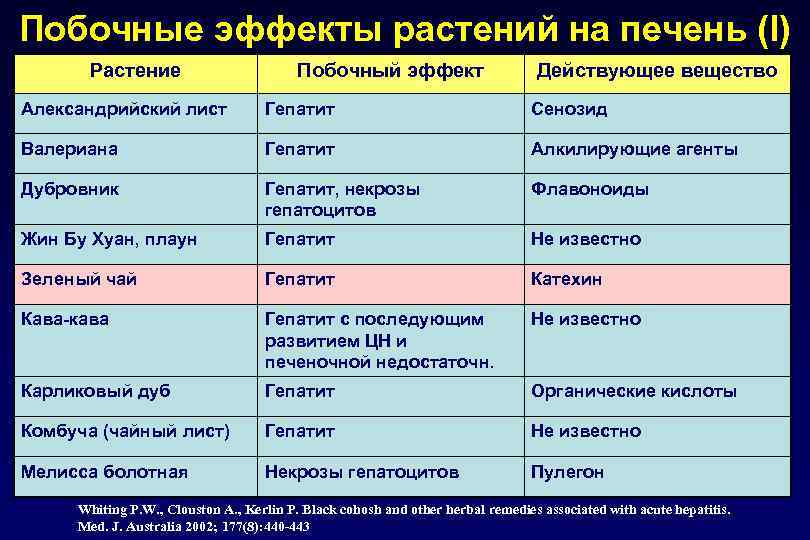 Побочные эффекты растений на печень (I) Растение Побочный эффект Действующее вещество Александрийский лист Гепатит Сенозид Валериана Гепатит Алкилирующие агенты Дубровник Гепатит, некрозы гепатоцитов Флавоноиды Жин Бу Хуан, плаун Гепатит Не известно Зеленый чай Гепатит Катехин Кава-кава Гепатит с последующим развитием ЦН и печеночной недостаточн. Не известно Карликовый дуб Гепатит Органические кислоты Комбуча (чайный лист) Гепатит Не известно Мелисса болотная Некрозы гепатоцитов Пулегон Whiting P. W. , Clouston A. , Kerlin P. Black cohosh and other herbal remedies associated with acute hepatitis. Med. J. Australia 2002; 177(8): 440 -443
Побочные эффекты растений на печень (I) Растение Побочный эффект Действующее вещество Александрийский лист Гепатит Сенозид Валериана Гепатит Алкилирующие агенты Дубровник Гепатит, некрозы гепатоцитов Флавоноиды Жин Бу Хуан, плаун Гепатит Не известно Зеленый чай Гепатит Катехин Кава-кава Гепатит с последующим развитием ЦН и печеночной недостаточн. Не известно Карликовый дуб Гепатит Органические кислоты Комбуча (чайный лист) Гепатит Не известно Мелисса болотная Некрозы гепатоцитов Пулегон Whiting P. W. , Clouston A. , Kerlin P. Black cohosh and other herbal remedies associated with acute hepatitis. Med. J. Australia 2002; 177(8): 440 -443
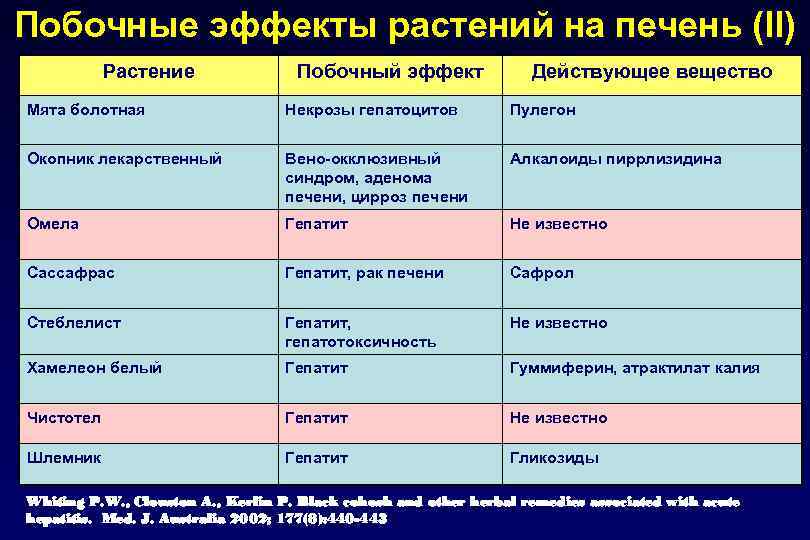 Побочные эффекты растений на печень (II) Растение Побочный эффект Действующее вещество Мята болотная Некрозы гепатоцитов Пулегон Окопник лекарственный Вено-окклюзивный синдром, аденома печени, цирроз печени Алкалоиды пиррлизидина Омела Гепатит Не известно Сассафрас Гепатит, рак печени Сафрол Стеблелист Гепатит, гепатотоксичность Не известно Хамелеон белый Гепатит Гуммиферин, атрактилат калия Чистотел Гепатит Не известно Шлемник Гепатит Гликозиды Whiting P. W. , Clouston A. , Kerlin P. Black cohosh and other herbal remedies associated with acute hepatitis. Med. J. Australia 2002; 177(8): 440 -443
Побочные эффекты растений на печень (II) Растение Побочный эффект Действующее вещество Мята болотная Некрозы гепатоцитов Пулегон Окопник лекарственный Вено-окклюзивный синдром, аденома печени, цирроз печени Алкалоиды пиррлизидина Омела Гепатит Не известно Сассафрас Гепатит, рак печени Сафрол Стеблелист Гепатит, гепатотоксичность Не известно Хамелеон белый Гепатит Гуммиферин, атрактилат калия Чистотел Гепатит Не известно Шлемник Гепатит Гликозиды Whiting P. W. , Clouston A. , Kerlin P. Black cohosh and other herbal remedies associated with acute hepatitis. Med. J. Australia 2002; 177(8): 440 -443
 Вакцинопрофилактика вирусных гепатитов
Вакцинопрофилактика вирусных гепатитов
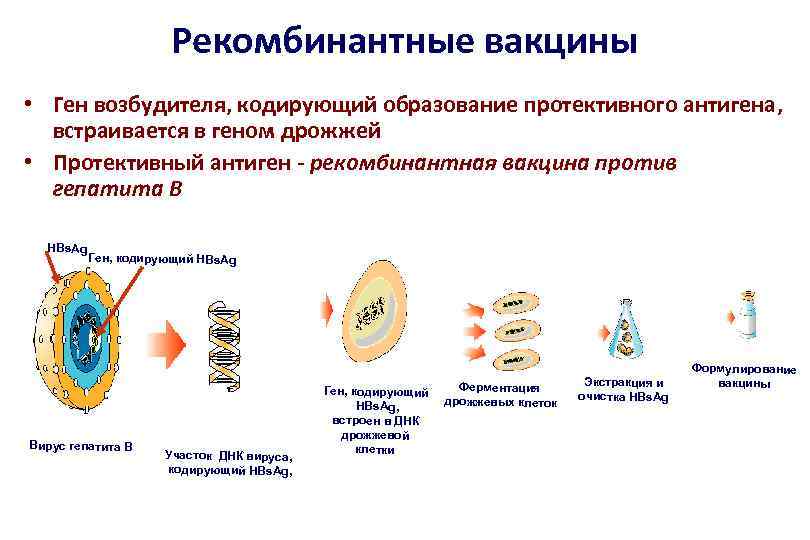 Рекомбинантные вакцины • Ген возбудителя, кодирующий образование протективного антигена, встраивается в геном дрожжей • Протективный антиген - рекомбинантная вакцина против гепатита В HBs. Ag Ген, кодирующий HBs. Ag Вирус гепатита В Участок ДНК вируса, кодирующий HBs. Ag, Ген, кодирующий HBs. Ag, встроен в ДНК дрожжевой клетки Ферментация дрожжевых клеток Экстракция и очистка HBs. Ag Формулирование вакцины
Рекомбинантные вакцины • Ген возбудителя, кодирующий образование протективного антигена, встраивается в геном дрожжей • Протективный антиген - рекомбинантная вакцина против гепатита В HBs. Ag Ген, кодирующий HBs. Ag Вирус гепатита В Участок ДНК вируса, кодирующий HBs. Ag, Ген, кодирующий HBs. Ag, встроен в ДНК дрожжевой клетки Ферментация дрожжевых клеток Экстракция и очистка HBs. Ag Формулирование вакцины
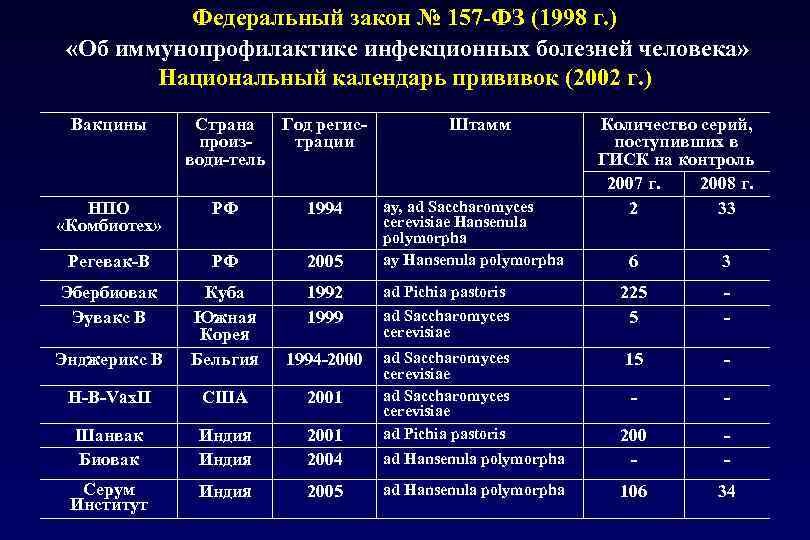 Федеральный закон № 157 -ФЗ (1998 г. ) «Об иммунопрофилактике инфекционных болезней человека» Национальный календарь прививок (2002 г. ) Вакцины Страна Год региспроизтрации води-тель Штамм НПО «Комбиотех» РФ 1994 Регевак-В РФ 2005 Эбербиовак Эувакс В 1992 1999 ad Pichia pastoris Энджерикс В Куба Южная Корея Бельгия 1994 -2000 Н-В-Vax. II США 2001 Шанвак Биовак Индия 2001 2004 ad Saccharomyces cerevisiae ad Pichia pastoris Серум Институт Индия 2005 ay, ad Saccharomyces cerevisiae Hansenula polymorpha ay Hansenula polymorpha Количество серий, поступивших в ГИСК на контроль 2007 г. 2008 г. 2 33 6 3 225 5 - 15 - - - ad Hansenula polymorpha 200 - - ad Hansenula polymorpha 106 34 ad Saccharomyces cerevisiae
Федеральный закон № 157 -ФЗ (1998 г. ) «Об иммунопрофилактике инфекционных болезней человека» Национальный календарь прививок (2002 г. ) Вакцины Страна Год региспроизтрации води-тель Штамм НПО «Комбиотех» РФ 1994 Регевак-В РФ 2005 Эбербиовак Эувакс В 1992 1999 ad Pichia pastoris Энджерикс В Куба Южная Корея Бельгия 1994 -2000 Н-В-Vax. II США 2001 Шанвак Биовак Индия 2001 2004 ad Saccharomyces cerevisiae ad Pichia pastoris Серум Институт Индия 2005 ay, ad Saccharomyces cerevisiae Hansenula polymorpha ay Hansenula polymorpha Количество серий, поступивших в ГИСК на контроль 2007 г. 2008 г. 2 33 6 3 225 5 - 15 - - - ad Hansenula polymorpha 200 - - ad Hansenula polymorpha 106 34 ad Saccharomyces cerevisiae
 ВАКЦИНАЦИЯ ПРОТИВ ГЕПАТИТА В (национальный проект «Здоровье» , 2006 г. ) В СРЕДНЕМ уже ПРОДЛИЛА ЖИЗНЬ КАЖДОМУ ЧЕЛОВЕКУ в Российской Федерации на 3, 5 месяца Материалы ИПВЭ им. М. П. Чумакова РАМН, 2007
ВАКЦИНАЦИЯ ПРОТИВ ГЕПАТИТА В (национальный проект «Здоровье» , 2006 г. ) В СРЕДНЕМ уже ПРОДЛИЛА ЖИЗНЬ КАЖДОМУ ЧЕЛОВЕКУ в Российской Федерации на 3, 5 месяца Материалы ИПВЭ им. М. П. Чумакова РАМН, 2007
 Схемы вакцинации против гепатита В • Стандартная схема вакцинации 0, 1, 6 мес. • Быстрая схема вакцинации 0, 1, 2 и 6 (12) мес. • Эстренная схема вакцинации 0, 7, 21 день и 12 мес. 10 м. МЕ/мл
Схемы вакцинации против гепатита В • Стандартная схема вакцинации 0, 1, 6 мес. • Быстрая схема вакцинации 0, 1, 2 и 6 (12) мес. • Эстренная схема вакцинации 0, 7, 21 день и 12 мес. 10 м. МЕ/мл
 Вакцина против гепатита В защищает против гепатита D
Вакцина против гепатита В защищает против гепатита D
 Вакцинопрофилактика ГА 20 м. МЕ/мл 1. ГЕП-А-ин-ВАК-вакцина против гепатита А культуральная очищенная концентрированная адсорбированная инактивированная жидкая, Россия 2. ГЕП-А-ин-ВАК-ПОЛ-вакцина против гепатита А культуральная очищенная концентрированная адсорбированная инактивированная жидкая с полиоксидонием, Россия 3. Аваксим фирмы Санофи Пастер, Франция 4. Вакта 50 Ед. фирмы Мерк, Шарп и Доум, США 5. Вакта 25 Ед. фирмы Мерк, Шарп и Доум, США 6. Хаврикс1440 фирмы Глаксо. Смит. Кляйн, Англия 7. Хаврикс720 фирмы Глаксо. Смит. Кляйн, Англия 8. ГЕП-А+В-ин-ВАК-вакцина гепатитов А+В, Россия 9. Твинрикс-вакцина гепатитов А и В, Глаксо. Смит. Кляйн, Англия 10. Эпаксал-вакцина гепатита А фирмы Берна, Швейцария Схема вакцинации 0, 6 (12) мес.
Вакцинопрофилактика ГА 20 м. МЕ/мл 1. ГЕП-А-ин-ВАК-вакцина против гепатита А культуральная очищенная концентрированная адсорбированная инактивированная жидкая, Россия 2. ГЕП-А-ин-ВАК-ПОЛ-вакцина против гепатита А культуральная очищенная концентрированная адсорбированная инактивированная жидкая с полиоксидонием, Россия 3. Аваксим фирмы Санофи Пастер, Франция 4. Вакта 50 Ед. фирмы Мерк, Шарп и Доум, США 5. Вакта 25 Ед. фирмы Мерк, Шарп и Доум, США 6. Хаврикс1440 фирмы Глаксо. Смит. Кляйн, Англия 7. Хаврикс720 фирмы Глаксо. Смит. Кляйн, Англия 8. ГЕП-А+В-ин-ВАК-вакцина гепатитов А+В, Россия 9. Твинрикс-вакцина гепатитов А и В, Глаксо. Смит. Кляйн, Англия 10. Эпаксал-вакцина гепатита А фирмы Берна, Швейцария Схема вакцинации 0, 6 (12) мес.
 Хронические вирусные гепатиты – серьезная проблема! Edvard Munch Крик
Хронические вирусные гепатиты – серьезная проблема! Edvard Munch Крик


