8188c9aef362a35a97c3c278184bdcbd.ppt
- Количество слайдов: 58
 Институт органической химии им. Н. Д. Зелинского РАН, г. Москва
Институт органической химии им. Н. Д. Зелинского РАН, г. Москва
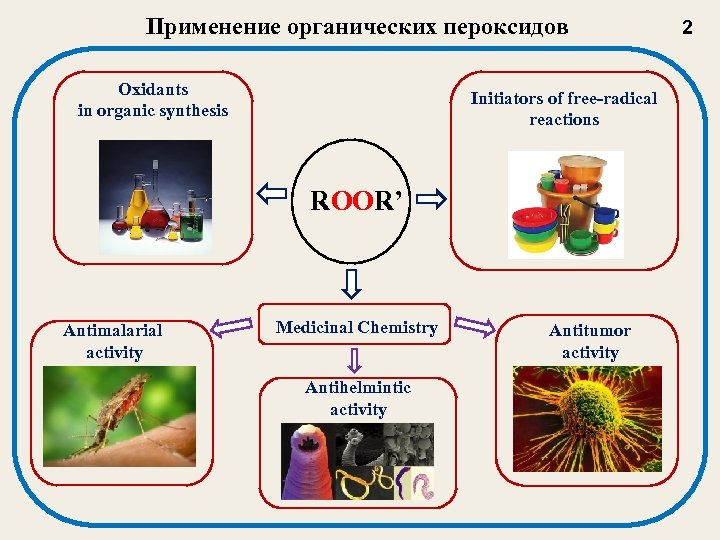 Применение органических пероксидов Oxidants in organic synthesis Initiators of free-radical reactions ROOR’ Antimalarial activity Medicinal Chemistry Antihelmintic activity Antitumor activity 2
Применение органических пероксидов Oxidants in organic synthesis Initiators of free-radical reactions ROOR’ Antimalarial activity Medicinal Chemistry Antihelmintic activity Antitumor activity 2
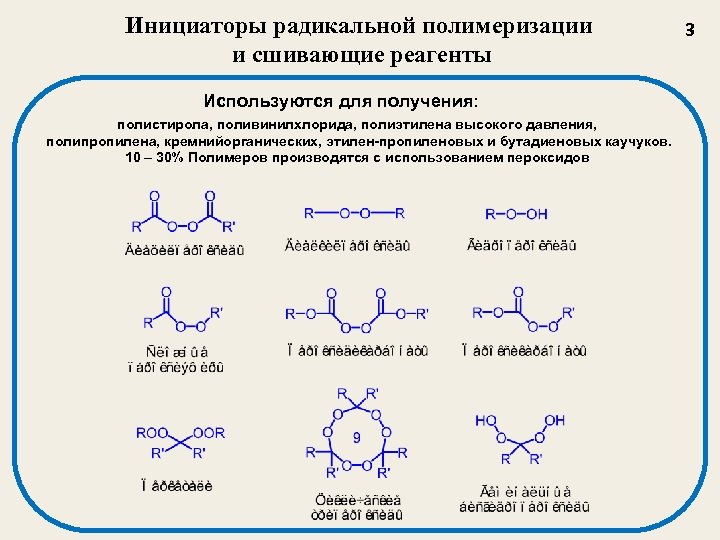 Инициаторы радикальной полимеризации и сшивающие реагенты Используются для получения: полистирола, поливинилхлорида, полиэтилена высокого давления, полипропилена, кремнийорганических, этилен-пропиленовых и бутадиеновых каучуков. 10 – 30% Полимеров производятся с использованием пероксидов 3
Инициаторы радикальной полимеризации и сшивающие реагенты Используются для получения: полистирола, поливинилхлорида, полиэтилена высокого давления, полипропилена, кремнийорганических, этилен-пропиленовых и бутадиеновых каучуков. 10 – 30% Полимеров производятся с использованием пероксидов 3
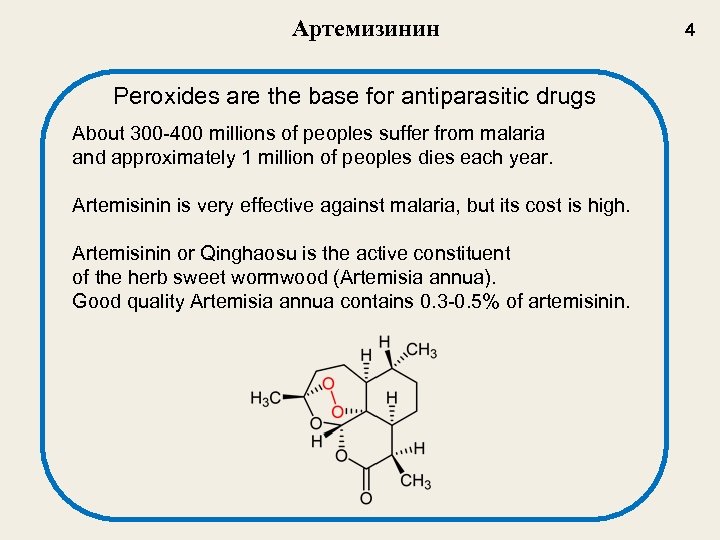 Артемизинин Peroxides are the base for antiparasitic drugs About 300 -400 millions of peoples suffer from malaria and approximately 1 million of peoples dies each year. Artemisinin is very effective against malaria, but its cost is high. Artemisinin or Qinghaosu is the active constituent of the herb sweet wormwood (Artemisia annua). Good quality Artemisia annua contains 0. 3 -0. 5% of artemisinin. 4
Артемизинин Peroxides are the base for antiparasitic drugs About 300 -400 millions of peoples suffer from malaria and approximately 1 million of peoples dies each year. Artemisinin is very effective against malaria, but its cost is high. Artemisinin or Qinghaosu is the active constituent of the herb sweet wormwood (Artemisia annua). Good quality Artemisia annua contains 0. 3 -0. 5% of artemisinin. 4
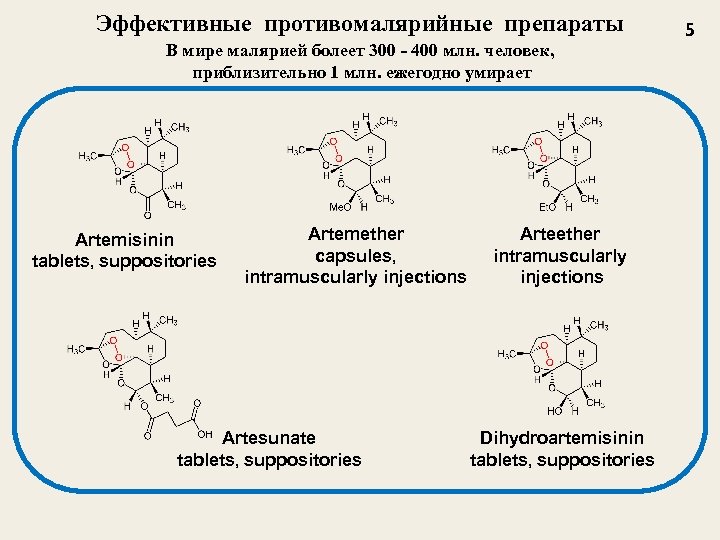 Эффективные противомалярийные препараты В мире малярией болеет 300 - 400 млн. человек, приблизительно 1 млн. ежегодно умирает Artemisinin tablets, suppositories Artemether capsules, intramuscularly injections Artesunate tablets, suppositories Arteether intramuscularly injections Dihydroartemisinin tablets, suppositories 5
Эффективные противомалярийные препараты В мире малярией болеет 300 - 400 млн. человек, приблизительно 1 млн. ежегодно умирает Artemisinin tablets, suppositories Artemether capsules, intramuscularly injections Artesunate tablets, suppositories Arteether intramuscularly injections Dihydroartemisinin tablets, suppositories 5
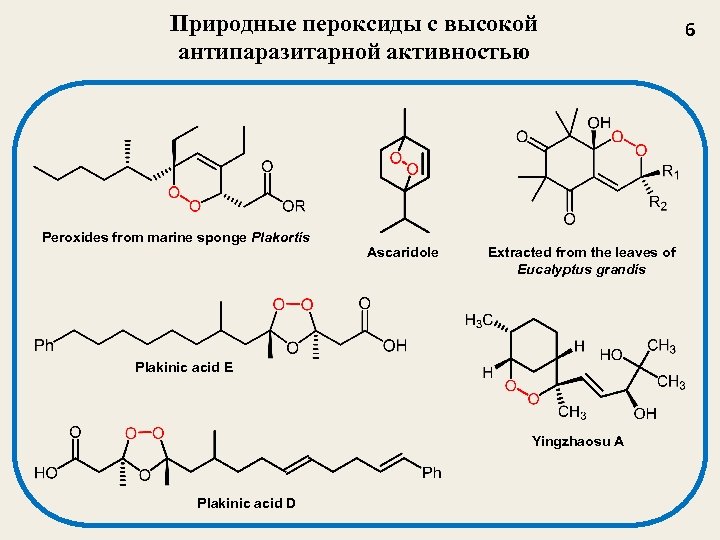 Природные пероксиды с высокой антипаразитарной активностью Peroxides from marine sponge Plakortis Ascaridole Extracted from the leaves of Eucalyptus grandis Plakinic acid E Yingzhaosu A Plakinic acid D 6
Природные пероксиды с высокой антипаразитарной активностью Peroxides from marine sponge Plakortis Ascaridole Extracted from the leaves of Eucalyptus grandis Plakinic acid E Yingzhaosu A Plakinic acid D 6
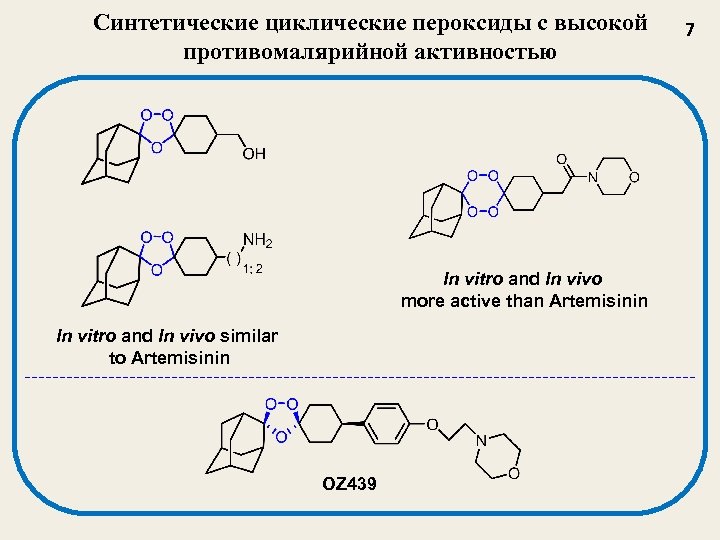 Синтетические циклические пероксиды с высокой противомалярийной активностью In vitro and In vivo more active than Artemisinin In vitro and In vivo similar to Artemisinin OZ 439 7
Синтетические циклические пероксиды с высокой противомалярийной активностью In vitro and In vivo more active than Artemisinin In vitro and In vivo similar to Artemisinin OZ 439 7
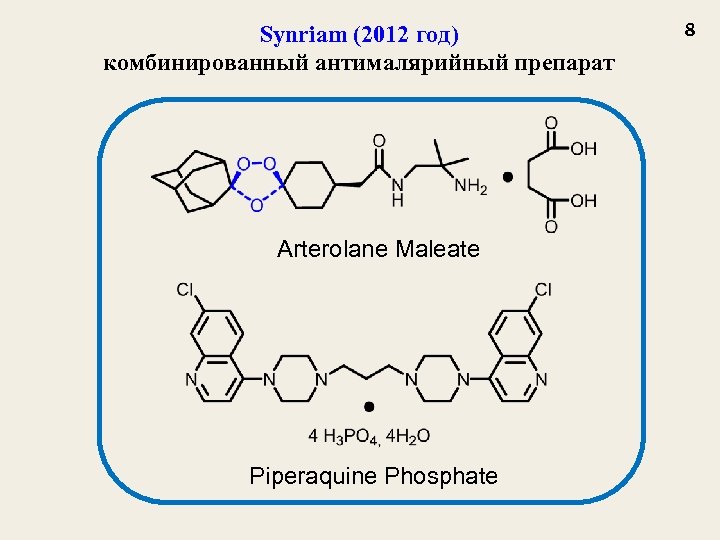 Synriam (2012 год) комбинированный антималярийный препарат Arterolane Maleate Piperaquine Phosphate 8
Synriam (2012 год) комбинированный антималярийный препарат Arterolane Maleate Piperaquine Phosphate 8
 Основные направления развития химии органических пероксидов - Селективные методы получения пероксидов - Селективные превращения пероксидов - Поиск биологически активных пероксидов - Поиск эффективных окислителей и инициаторов радикальной полимеризации 9
Основные направления развития химии органических пероксидов - Селективные методы получения пероксидов - Селективные превращения пероксидов - Поиск биологически активных пероксидов - Поиск эффективных окислителей и инициаторов радикальной полимеризации 9
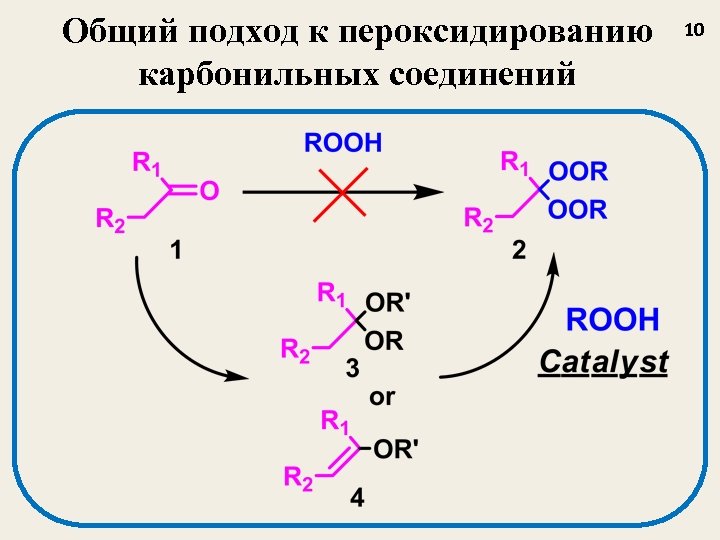 Общий подход к пероксидированию карбонильных соединений 10
Общий подход к пероксидированию карбонильных соединений 10
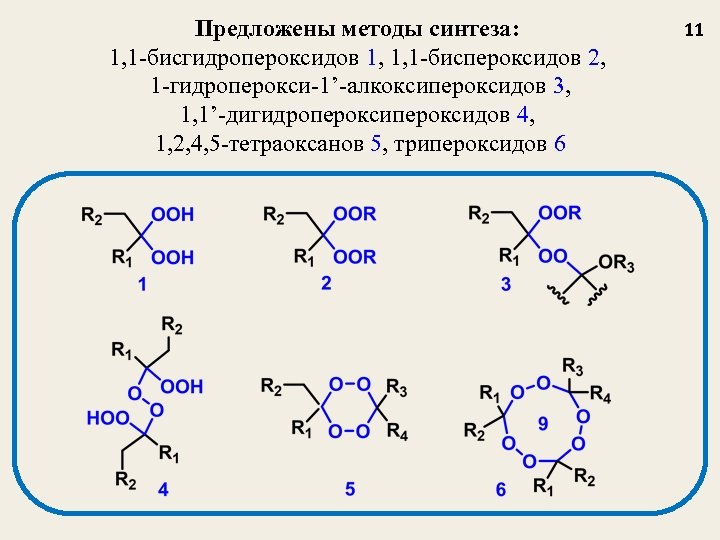 Предложены методы синтеза: 1, 1 -бисгидропероксидов 1, 1, 1 -биспероксидов 2, 1 -гидроперокси-1’-алкоксипероксидов 3, 1, 1’-дигидропероксидов 4, 1, 2, 4, 5 -тетраоксанов 5, трипероксидов 6 11
Предложены методы синтеза: 1, 1 -бисгидропероксидов 1, 1, 1 -биспероксидов 2, 1 -гидроперокси-1’-алкоксипероксидов 3, 1, 1’-дигидропероксидов 4, 1, 2, 4, 5 -тетраоксанов 5, трипероксидов 6 11
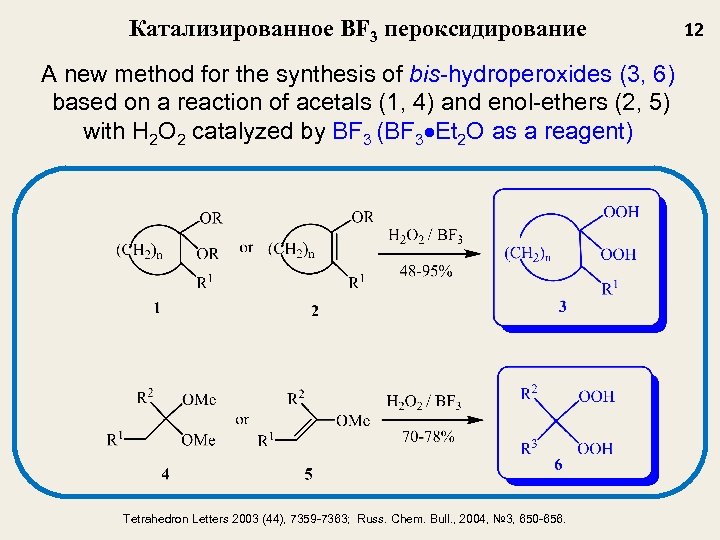 Катализированное BF 3 пероксидирование A new method for the synthesis of bis-hydroperoxides (3, 6) based on a reaction of acetals (1, 4) and enol-ethers (2, 5) with H 2 O 2 catalyzed by BF 3 (BF 3 Et 2 O as a reagent) Tetrahedron Letters 2003 (44), 7359 -7363; Russ. Chem. Bull. , 2004, № 3, 650 -656. 12
Катализированное BF 3 пероксидирование A new method for the synthesis of bis-hydroperoxides (3, 6) based on a reaction of acetals (1, 4) and enol-ethers (2, 5) with H 2 O 2 catalyzed by BF 3 (BF 3 Et 2 O as a reagent) Tetrahedron Letters 2003 (44), 7359 -7363; Russ. Chem. Bull. , 2004, № 3, 650 -656. 12
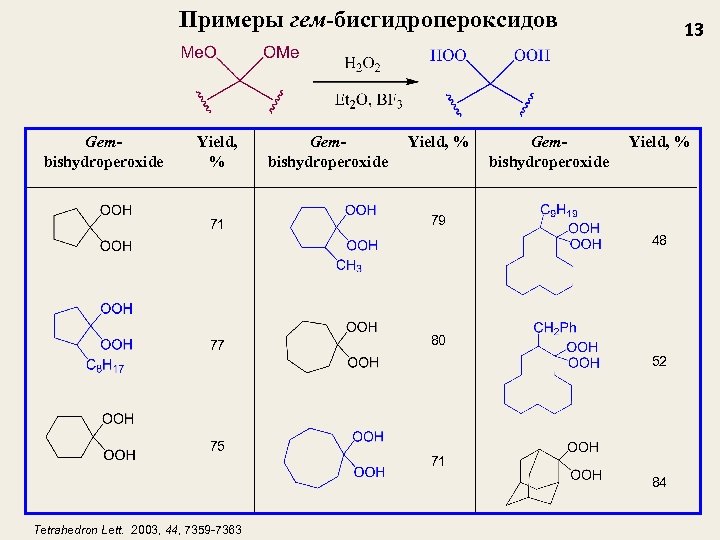 Примеры гем-бисгидропероксидов Gembishydroperoxide Yield, % 71 Yield, % 79 77 Gembishydroperoxide 13 80 75 48 52 71 84 Tetrahedron Lett. 2003, 44, 7359 -7363
Примеры гем-бисгидропероксидов Gembishydroperoxide Yield, % 71 Yield, % 79 77 Gembishydroperoxide 13 80 75 48 52 71 84 Tetrahedron Lett. 2003, 44, 7359 -7363
 Предполагаемый механизм получения 14 гем-бисгидропероксидов B и побочных продуктов C и D
Предполагаемый механизм получения 14 гем-бисгидропероксидов B и побочных продуктов C и D
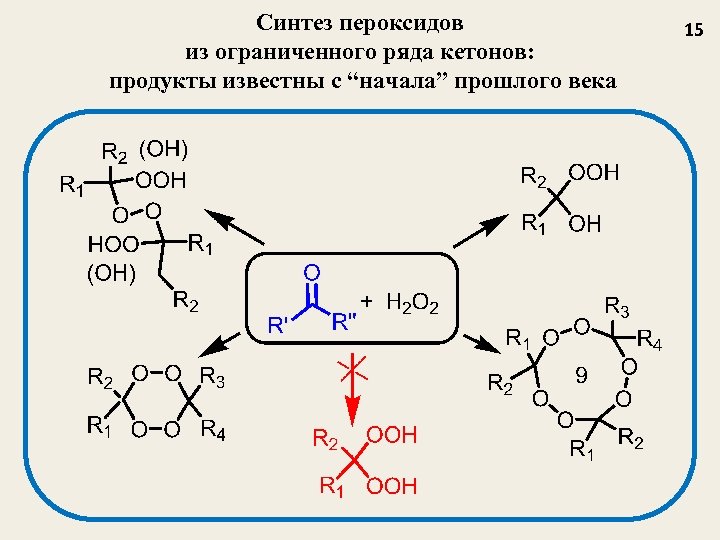 Синтез пероксидов из ограниченного ряда кетонов: продукты известны с “начала” прошлого века 15
Синтез пероксидов из ограниченного ряда кетонов: продукты известны с “начала” прошлого века 15
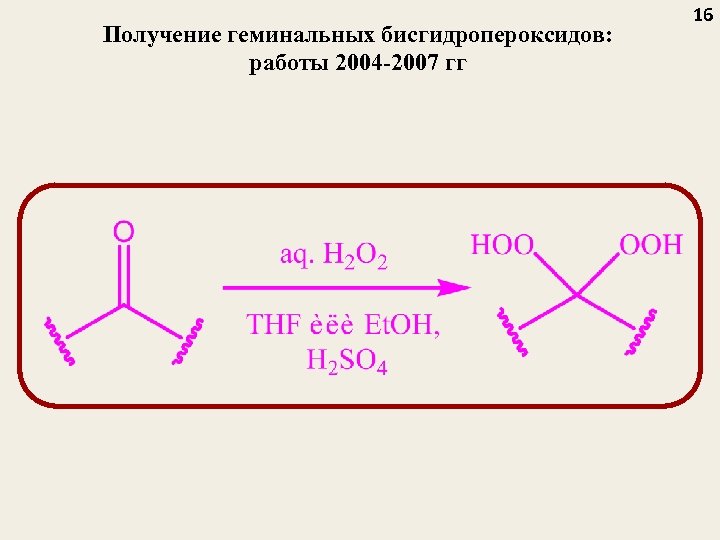 Получение геминальных бисгидропероксидов: работы 2004 -2007 гг 16
Получение геминальных бисгидропероксидов: работы 2004 -2007 гг 16
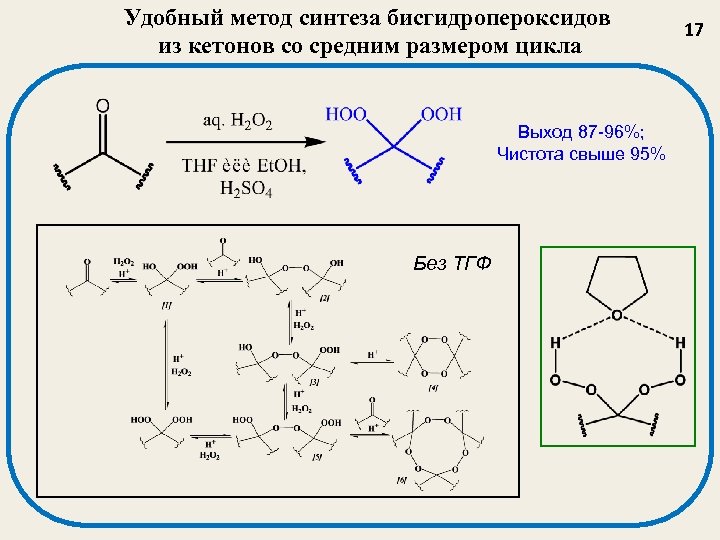 Удобный метод синтеза бисгидропероксидов из кетонов со средним размером цикла Выход 87 -96%; Чистота свыше 95% Без ТГФ 17
Удобный метод синтеза бисгидропероксидов из кетонов со средним размером цикла Выход 87 -96%; Чистота свыше 95% Без ТГФ 17
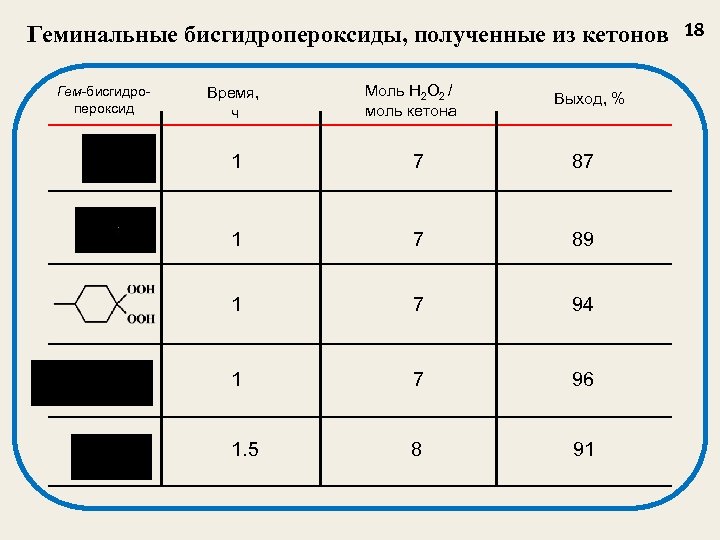 Геминальные бисгидропероксиды, полученные из кетонов 18 Гем-бисгидропероксид Время, ч Моль H 2 O 2 / моль кетона Выход, % 1 7 87 1 7 89 1 7 94 1 7 96 1. 5 8 91
Геминальные бисгидропероксиды, полученные из кетонов 18 Гем-бисгидропероксид Время, ч Моль H 2 O 2 / моль кетона Выход, % 1 7 87 1 7 89 1 7 94 1 7 96 1. 5 8 91
 Геминальные бисгидропероксиды – 19 эффективные инициаторы радикальной полимеризации метилакрилата, стирола и акрилонитрила в массе Впервые показано, что геминальные бисгидропероксиды являются инициаторами радикальной полимеризации Способ получения геминальных дигидропероксидов. // патент РФ № 2395494, 27. 12. 2006. Способ получения полиметилметакрилата. // патент РФ № 2352587, 25. 12. 2007. Способ получения полиакрилонитрила. // патент РФ № 2393173, 01. 04. 2008. ГК от « 25» июня 2007 г. № 02. 513. 11. 3302 (ИОХ РАН – ИНЭОС РАН) Компания Акзо-Нобель (Akzo. Nobel) производит пероксид циклогексанона под торговыми марками CYCLONOX 11; CYCLONOX GT-50 LP; CYCLONOX LE-50; CYCLONOX LR-50 BA для применения в получении КУЗОВНЫХ ШПАКЛЕВОК и НАРУЖНЫХ ПОКРЫТИЙ
Геминальные бисгидропероксиды – 19 эффективные инициаторы радикальной полимеризации метилакрилата, стирола и акрилонитрила в массе Впервые показано, что геминальные бисгидропероксиды являются инициаторами радикальной полимеризации Способ получения геминальных дигидропероксидов. // патент РФ № 2395494, 27. 12. 2006. Способ получения полиметилметакрилата. // патент РФ № 2352587, 25. 12. 2007. Способ получения полиакрилонитрила. // патент РФ № 2393173, 01. 04. 2008. ГК от « 25» июня 2007 г. № 02. 513. 11. 3302 (ИОХ РАН – ИНЭОС РАН) Компания Акзо-Нобель (Akzo. Nobel) производит пероксид циклогексанона под торговыми марками CYCLONOX 11; CYCLONOX GT-50 LP; CYCLONOX LE-50; CYCLONOX LR-50 BA для применения в получении КУЗОВНЫХ ШПАКЛЕВОК и НАРУЖНЫХ ПОКРЫТИЙ
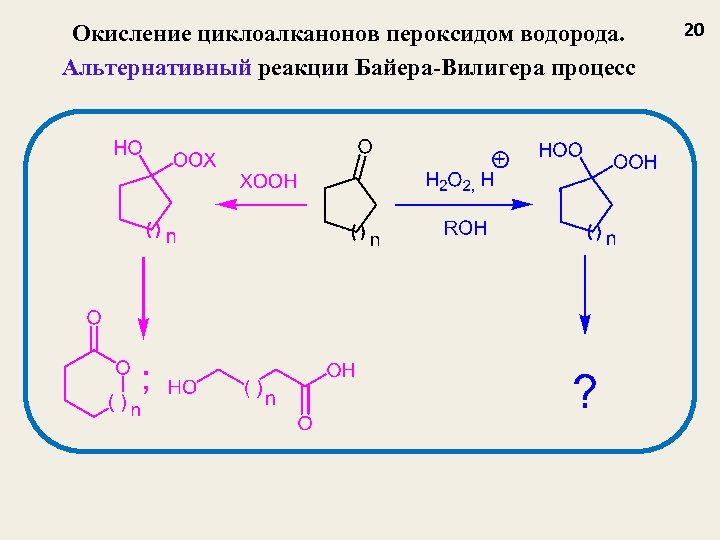 Окисление циклоалканонов пероксидом водорода. Альтернативный реакции Байера-Вилигера процесс 20
Окисление циклоалканонов пероксидом водорода. Альтернативный реакции Байера-Вилигера процесс 20
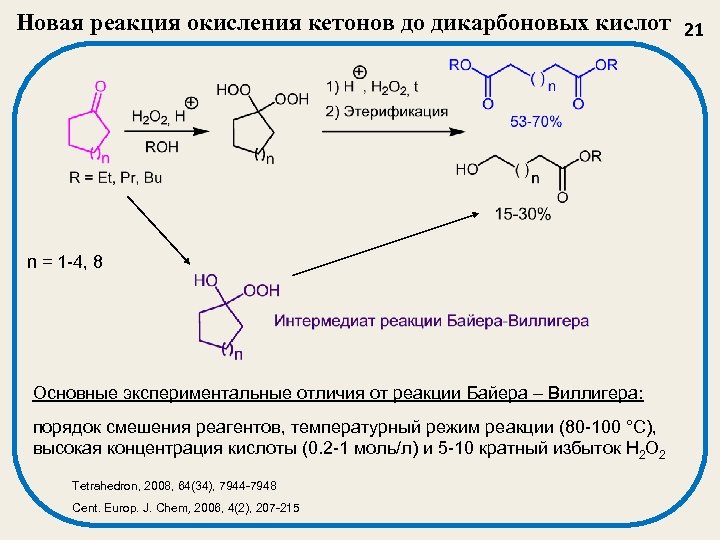 Новая реакция окисления кетонов до дикарбоновых кислот 21 n = 1 -4, 8 Основные экспериментальные отличия от реакции Байера – Виллигера: порядок смешения реагентов, температурный режим реакции (80 -100 °С), высокая концентрация кислоты (0. 2 -1 моль/л) и 5 -10 кратный избыток H 2 O 2 Tetrahedron, 2008, 64(34), 7944 -7948 Cent. Europ. J. Chem, 2006, 4(2), 207 -215
Новая реакция окисления кетонов до дикарбоновых кислот 21 n = 1 -4, 8 Основные экспериментальные отличия от реакции Байера – Виллигера: порядок смешения реагентов, температурный режим реакции (80 -100 °С), высокая концентрация кислоты (0. 2 -1 моль/л) и 5 -10 кратный избыток H 2 O 2 Tetrahedron, 2008, 64(34), 7944 -7948 Cent. Europ. J. Chem, 2006, 4(2), 207 -215
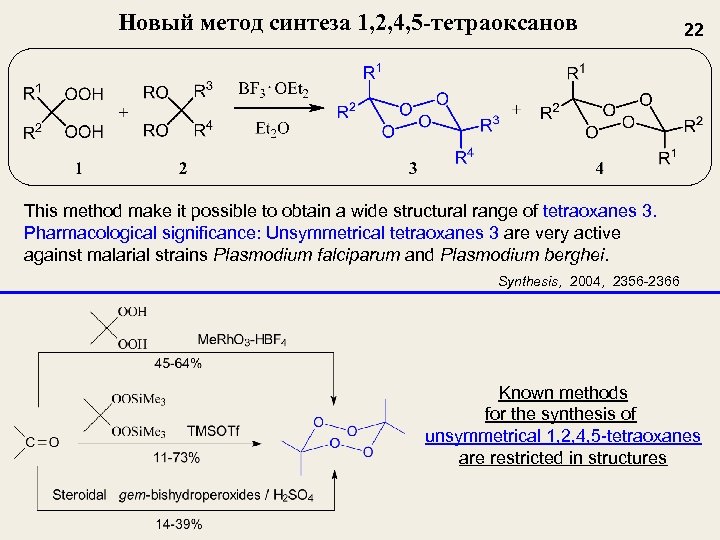 Новый метод синтеза 1, 2, 4, 5 -тетраоксанов 22 This method make it possible to obtain a wide structural range of tetraoxanes 3. Pharmacological significance: Unsymmetrical tetraoxanes 3 are very active against malarial strains Plasmodium falciparum and Plasmodium berghei. Synthesis, 2004, 2356 -2366 Known methods for the synthesis of unsymmetrical 1, 2, 4, 5 -tetraoxanes are restricted in structures
Новый метод синтеза 1, 2, 4, 5 -тетраоксанов 22 This method make it possible to obtain a wide structural range of tetraoxanes 3. Pharmacological significance: Unsymmetrical tetraoxanes 3 are very active against malarial strains Plasmodium falciparum and Plasmodium berghei. Synthesis, 2004, 2356 -2366 Known methods for the synthesis of unsymmetrical 1, 2, 4, 5 -tetraoxanes are restricted in structures
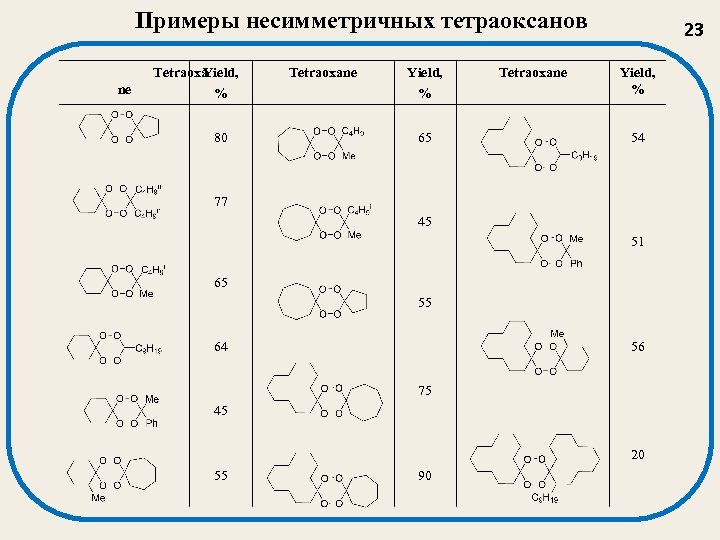 Примеры несимметричных тетраоксанов ne Tetraoxa Yield, % 80 Tetraoxane Yield, % 65 Tetraoxane 23 Yield, % 54 77 45 51 65 55 64 56 75 45 20 55 90
Примеры несимметричных тетраоксанов ne Tetraoxa Yield, % 80 Tetraoxane Yield, % 65 Tetraoxane 23 Yield, % 54 77 45 51 65 55 64 56 75 45 20 55 90
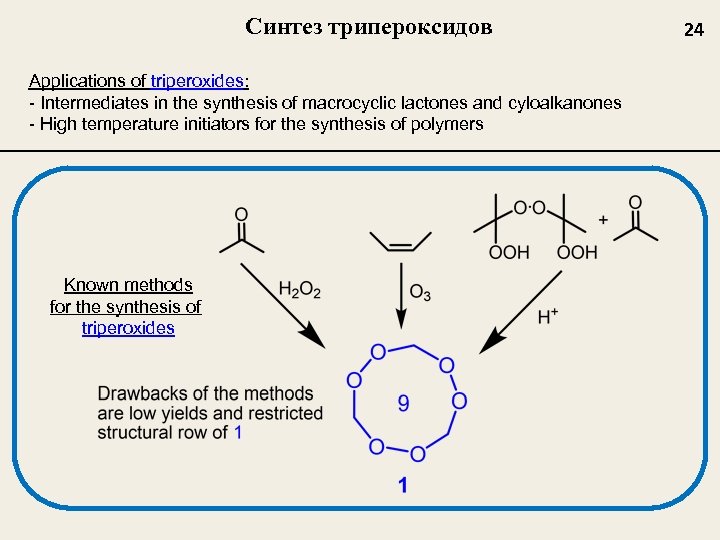 Синтез трипероксидов Applications of triperoxides: - Intermediates in the synthesis of macrocyclic lactones and cyloalkanones - High temperature initiators for the synthesis of polymers Known methods for the synthesis of triperoxides 24
Синтез трипероксидов Applications of triperoxides: - Intermediates in the synthesis of macrocyclic lactones and cyloalkanones - High temperature initiators for the synthesis of polymers Known methods for the synthesis of triperoxides 24
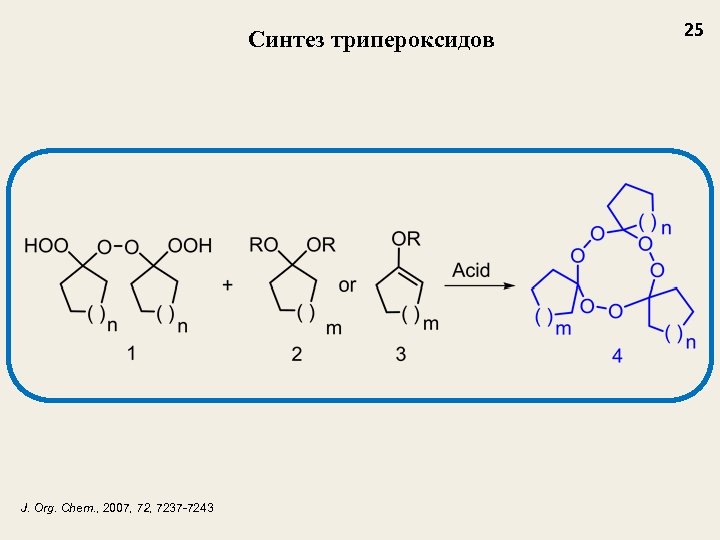 Синтез трипероксидов J. Org. Chem. , 2007, 7237 -7243 25
Синтез трипероксидов J. Org. Chem. , 2007, 7237 -7243 25
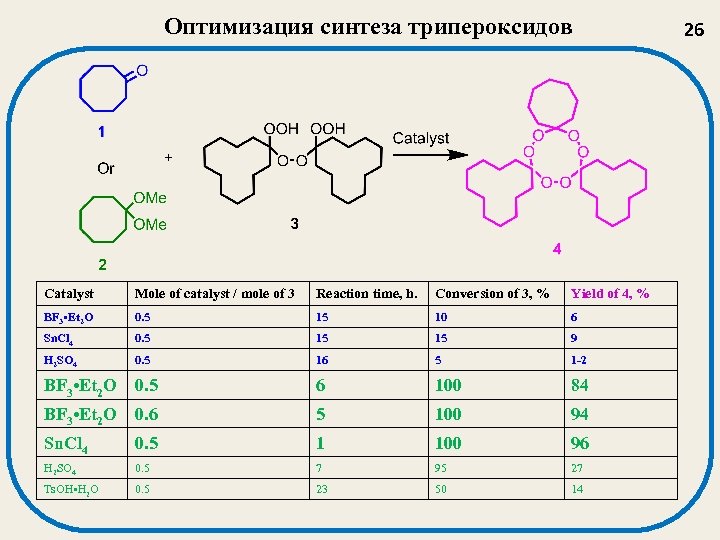 Оптимизация синтеза трипероксидов Catalyst Mole of catalyst / mole of 3 Reaction time, h. Conversion of 3, % Yield of 4, % BF 3 • Et 2 O 0. 5 15 10 6 Sn. Cl 4 0. 5 15 15 9 H 2 SO 4 0. 5 16 5 1 -2 BF 3 • Et 2 O 0. 5 6 100 84 BF 3 • Et 2 O 0. 6 5 100 94 Sn. Cl 4 0. 5 1 100 96 H 2 SO 4 0. 5 7 95 27 Ts. OH • H 2 O 0. 5 23 50 14 26
Оптимизация синтеза трипероксидов Catalyst Mole of catalyst / mole of 3 Reaction time, h. Conversion of 3, % Yield of 4, % BF 3 • Et 2 O 0. 5 15 10 6 Sn. Cl 4 0. 5 15 15 9 H 2 SO 4 0. 5 16 5 1 -2 BF 3 • Et 2 O 0. 5 6 100 84 BF 3 • Et 2 O 0. 6 5 100 94 Sn. Cl 4 0. 5 1 100 96 H 2 SO 4 0. 5 7 95 27 Ts. OH • H 2 O 0. 5 23 50 14 26
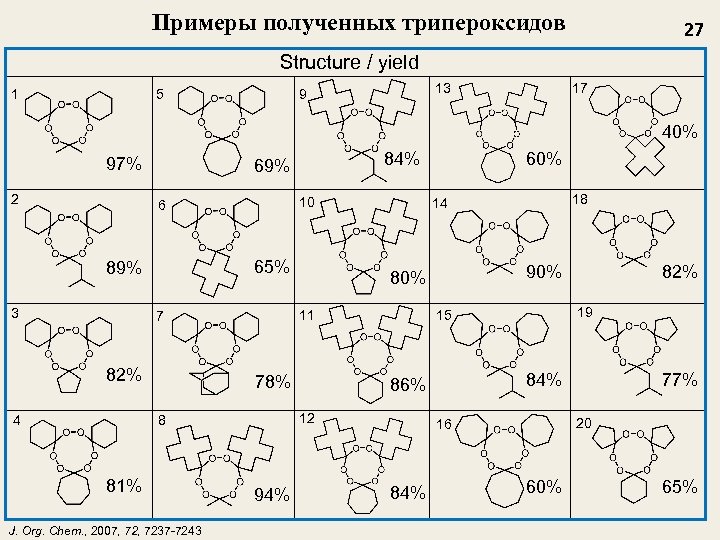 Примеры полученных трипероксидов 27 Structure / yield 1 5 97% 2 6 7 84% 10 81% J. Org. Chem. , 2007, 7237 -7243 94% 84% 16 84% 82% 19 15 90% 86% 12 40% 18 14 11 60% 80% 78% 8 17 13 65% 82% 4 69% 89% 3 9 77% 20 60% 65%
Примеры полученных трипероксидов 27 Structure / yield 1 5 97% 2 6 7 84% 10 81% J. Org. Chem. , 2007, 7237 -7243 94% 84% 16 84% 82% 19 15 90% 86% 12 40% 18 14 11 60% 80% 78% 8 17 13 65% 82% 4 69% 89% 3 9 77% 20 60% 65%
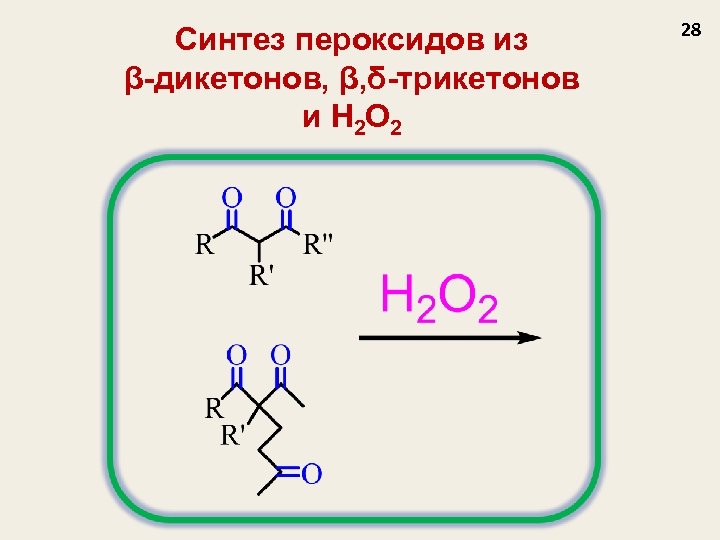 Синтез пероксидов из β-дикетонов, β, δ-трикетонов и H 2 O 2 28
Синтез пероксидов из β-дикетонов, β, δ-трикетонов и H 2 O 2 28
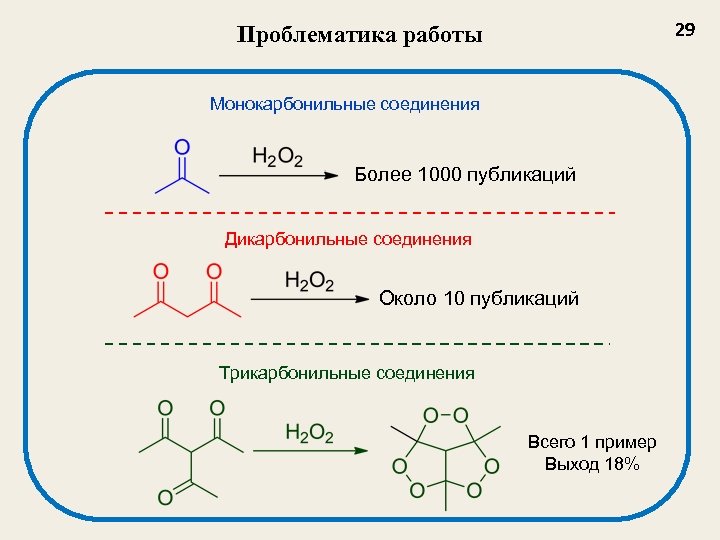 29 Проблематика работы Монокарбонильные соединения Более 1000 публикаций Дикарбонильные соединения Около 10 публикаций Трикарбонильные соединения Всего 1 пример Выход 18%
29 Проблематика работы Монокарбонильные соединения Более 1000 публикаций Дикарбонильные соединения Около 10 публикаций Трикарбонильные соединения Всего 1 пример Выход 18%
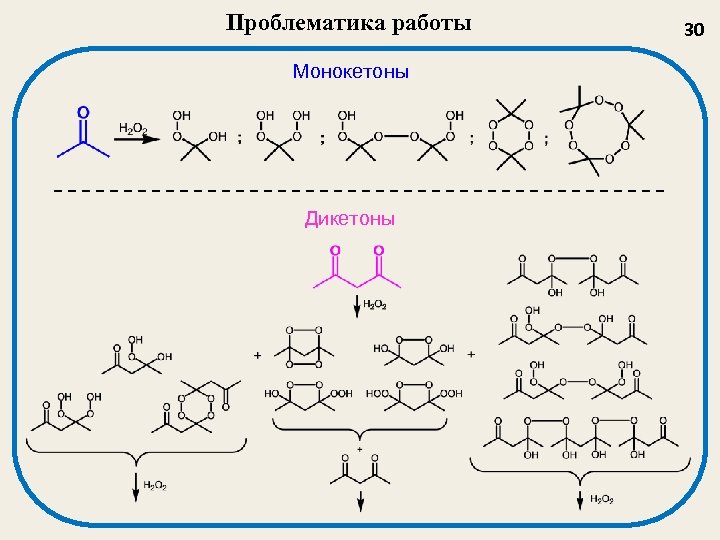 Проблематика работы Монокетоны Дикетоны 30
Проблематика работы Монокетоны Дикетоны 30
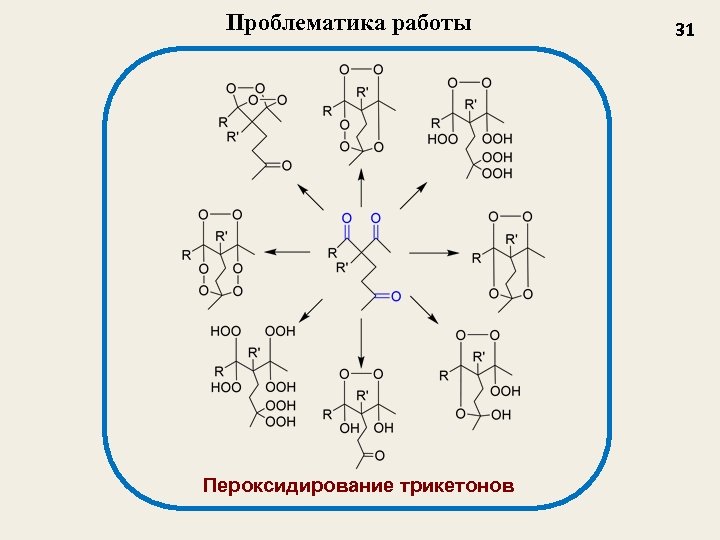 Проблематика работы Пероксидирование трикетонов 31
Проблематика работы Пероксидирование трикетонов 31
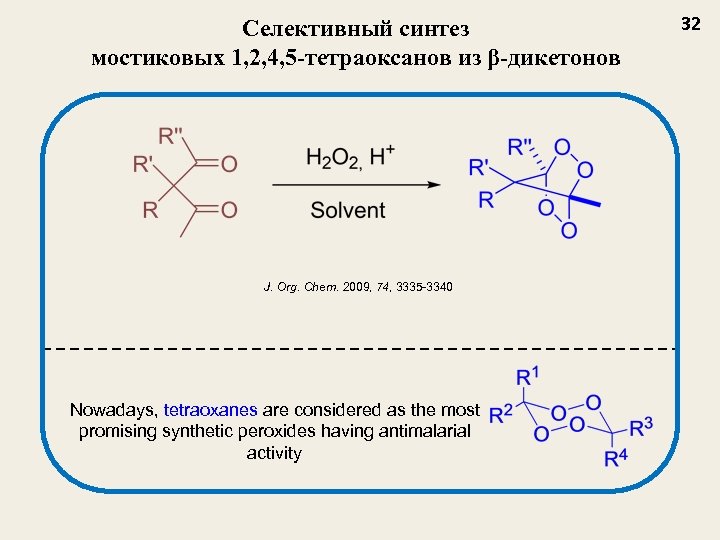 Селективный синтез мостиковых 1, 2, 4, 5 -тетраоксанов из β-дикетонов J. Org. Chem. 2009, 74, 3335 -3340 Nowadays, tetraoxanes are considered as the most promising synthetic peroxides having antimalarial activity 32
Селективный синтез мостиковых 1, 2, 4, 5 -тетраоксанов из β-дикетонов J. Org. Chem. 2009, 74, 3335 -3340 Nowadays, tetraoxanes are considered as the most promising synthetic peroxides having antimalarial activity 32
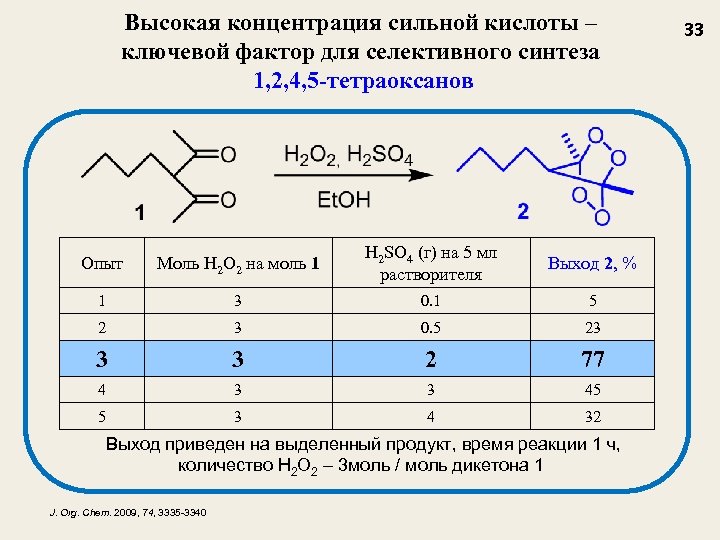 Высокая концентрация сильной кислоты – ключевой фактор для селективного синтеза 1, 2, 4, 5 -тетраоксанов Опыт Моль H 2 O 2 на моль 1 H 2 SO 4 (г) на 5 мл растворителя Выход 2, % 1 3 0. 1 5 2 3 0. 5 23 3 3 2 77 4 3 3 45 5 3 4 32 Выход приведен на выделенный продукт, время реакции 1 ч, количество H 2 O 2 – 3 моль / моль дикетона 1 J. Org. Chem. 2009, 74, 3335 -3340 33
Высокая концентрация сильной кислоты – ключевой фактор для селективного синтеза 1, 2, 4, 5 -тетраоксанов Опыт Моль H 2 O 2 на моль 1 H 2 SO 4 (г) на 5 мл растворителя Выход 2, % 1 3 0. 1 5 2 3 0. 5 23 3 3 2 77 4 3 3 45 5 3 4 32 Выход приведен на выделенный продукт, время реакции 1 ч, количество H 2 O 2 – 3 моль / моль дикетона 1 J. Org. Chem. 2009, 74, 3335 -3340 33
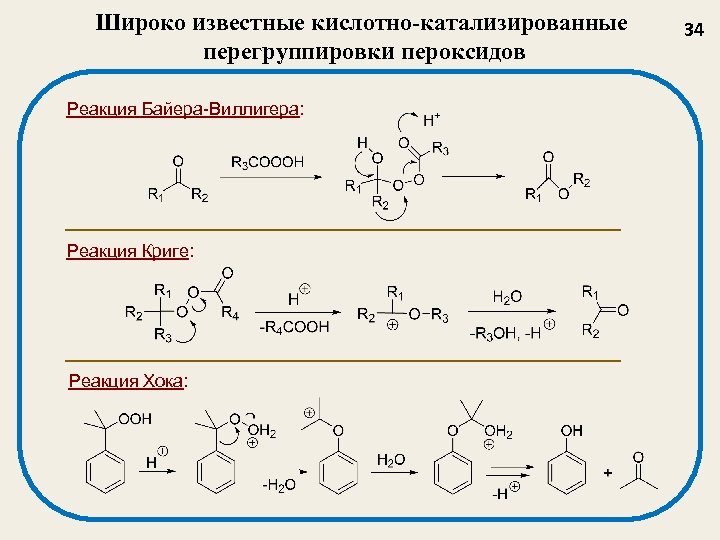 Широко известные кислотно-катализированные перегруппировки пероксидов Реакция Байера-Виллигера: Реакция Криге: Реакция Хока: 34
Широко известные кислотно-катализированные перегруппировки пероксидов Реакция Байера-Виллигера: Реакция Криге: Реакция Хока: 34
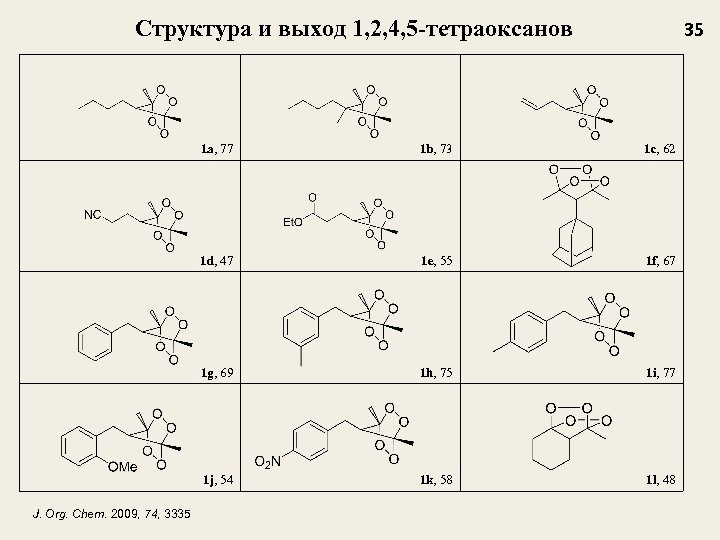 Структура и выход 1, 2, 4, 5 -тетраоксанов 35 1 a, 77 1 c, 62 1 d, 47 1 e, 55 1 f, 67 1 g, 69 1 h, 75 1 i, 77 1 j, 54 J. Org. Chem. 2009, 74, 3335 1 b, 73 1 k, 58 1 l, 48
Структура и выход 1, 2, 4, 5 -тетраоксанов 35 1 a, 77 1 c, 62 1 d, 47 1 e, 55 1 f, 67 1 g, 69 1 h, 75 1 i, 77 1 j, 54 J. Org. Chem. 2009, 74, 3335 1 b, 73 1 k, 58 1 l, 48
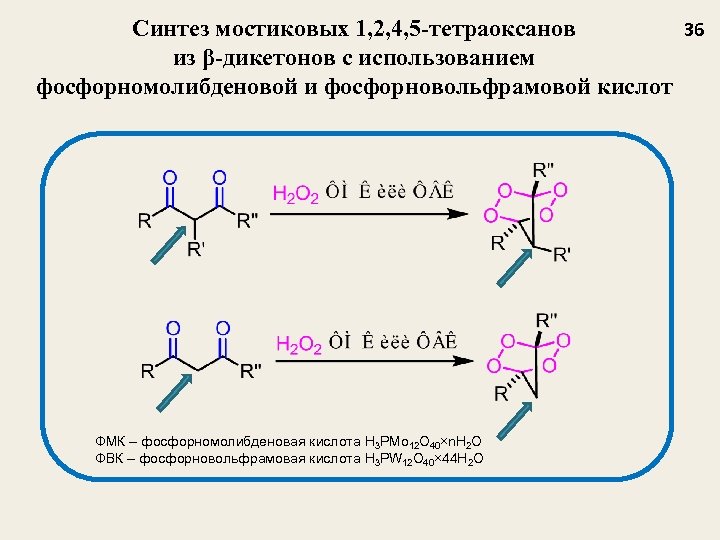 Синтез мостиковых 1, 2, 4, 5 -тетраоксанов 36 из β-дикетонов с использованием фосфорномолибденовой и фосфорновольфрамовой кислот ФМК – фосфорномолибденовая кислота H 3 PMo 12 O 40×n. H 2 O ФВК – фосфорновольфрамовая кислота H 3 PW 12 O 40× 44 H 2 O
Синтез мостиковых 1, 2, 4, 5 -тетраоксанов 36 из β-дикетонов с использованием фосфорномолибденовой и фосфорновольфрамовой кислот ФМК – фосфорномолибденовая кислота H 3 PMo 12 O 40×n. H 2 O ФВК – фосфорновольфрамовая кислота H 3 PW 12 O 40× 44 H 2 O
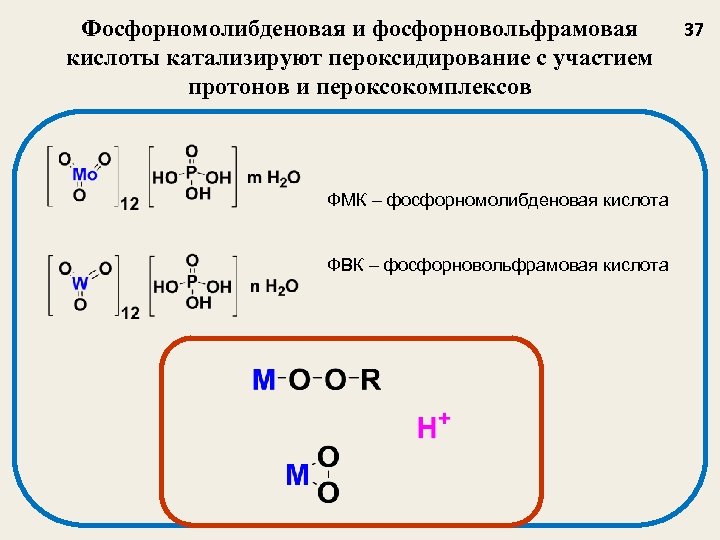 Фосфорномолибденовая и фосфорновольфрамовая кислоты катализируют пероксидирование с участием протонов и пероксокомплексов ФМК – фосфорномолибденовая кислота ФВК – фосфорновольфрамовая кислота 37
Фосфорномолибденовая и фосфорновольфрамовая кислоты катализируют пероксидирование с участием протонов и пероксокомплексов ФМК – фосфорномолибденовая кислота ФВК – фосфорновольфрамовая кислота 37
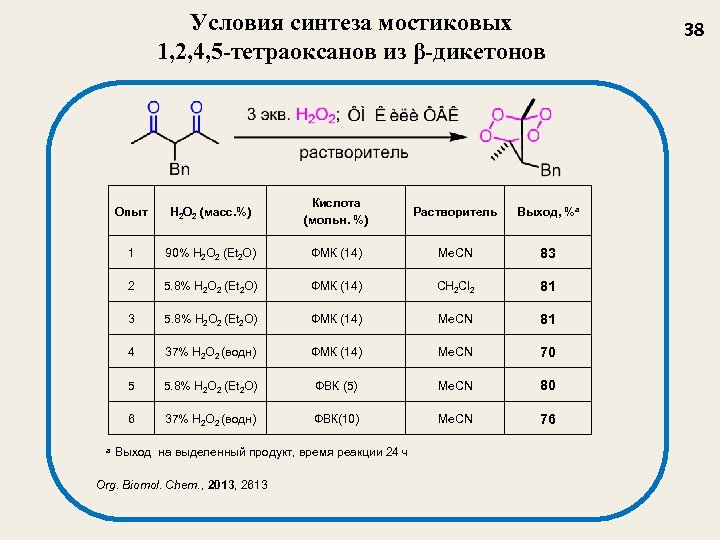 Условия синтеза мостиковых 1, 2, 4, 5 -тетраоксанов из β-дикетонов Опыт H 2 O 2 (масс. %) Кислота (мольн. %) Растворитель Выход, %a 1 90% H 2 O 2 (Et 2 O) ФМК (14) Me. CN 83 2 5. 8% H 2 O 2 (Et 2 O) ФМК (14) CH 2 Cl 2 81 3 5. 8% H 2 O 2 (Et 2 O) ФМК (14) Me. CN 81 4 37% H 2 O 2 (водн) ФМК (14) Me. CN 70 5 5. 8% H 2 O 2 (Et 2 O) ФВК (5) Me. CN 80 6 37% H 2 O 2 (водн) ФВК(10) Me. CN 76 а Выход на выделенный продукт, время реакции 24 ч Org. Biomol. Chem. , 2013, 2613 38
Условия синтеза мостиковых 1, 2, 4, 5 -тетраоксанов из β-дикетонов Опыт H 2 O 2 (масс. %) Кислота (мольн. %) Растворитель Выход, %a 1 90% H 2 O 2 (Et 2 O) ФМК (14) Me. CN 83 2 5. 8% H 2 O 2 (Et 2 O) ФМК (14) CH 2 Cl 2 81 3 5. 8% H 2 O 2 (Et 2 O) ФМК (14) Me. CN 81 4 37% H 2 O 2 (водн) ФМК (14) Me. CN 70 5 5. 8% H 2 O 2 (Et 2 O) ФВК (5) Me. CN 80 6 37% H 2 O 2 (водн) ФВК(10) Me. CN 76 а Выход на выделенный продукт, время реакции 24 ч Org. Biomol. Chem. , 2013, 2613 38
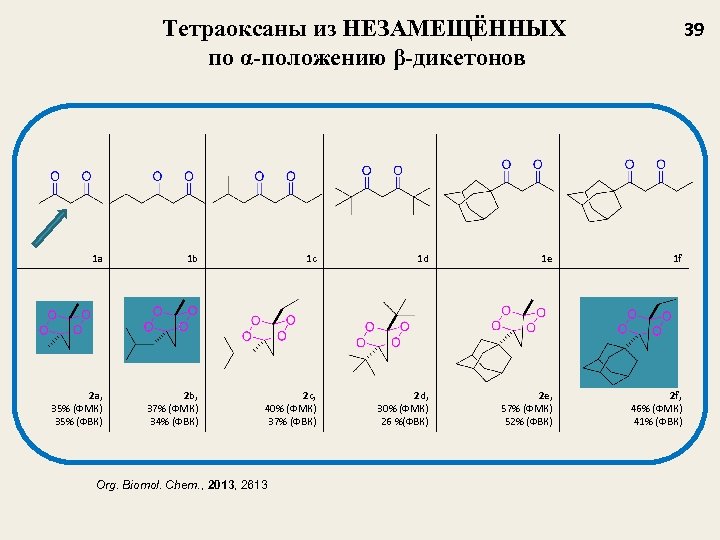 Тетраоксаны из НЕЗАМЕЩЁННЫХ по α-положению β-дикетонов 39 1 a 1 b 1 c 1 d 1 e 1 f 2 a, 35% (ФМК) 35% (ФВК) 2 b, 37% (ФМК) 34% (ФВК) 2 c, 40% (ФМК) 37% (ФВК) 2 d, 30% (ФМК) 26 %(ФВК) 2 e, 57% (ФМК) 52% (ФВК) 2 f, 46% (ФМК) 41% (ФВК) Org. Biomol. Chem. , 2013, 2613
Тетраоксаны из НЕЗАМЕЩЁННЫХ по α-положению β-дикетонов 39 1 a 1 b 1 c 1 d 1 e 1 f 2 a, 35% (ФМК) 35% (ФВК) 2 b, 37% (ФМК) 34% (ФВК) 2 c, 40% (ФМК) 37% (ФВК) 2 d, 30% (ФМК) 26 %(ФВК) 2 e, 57% (ФМК) 52% (ФВК) 2 f, 46% (ФМК) 41% (ФВК) Org. Biomol. Chem. , 2013, 2613
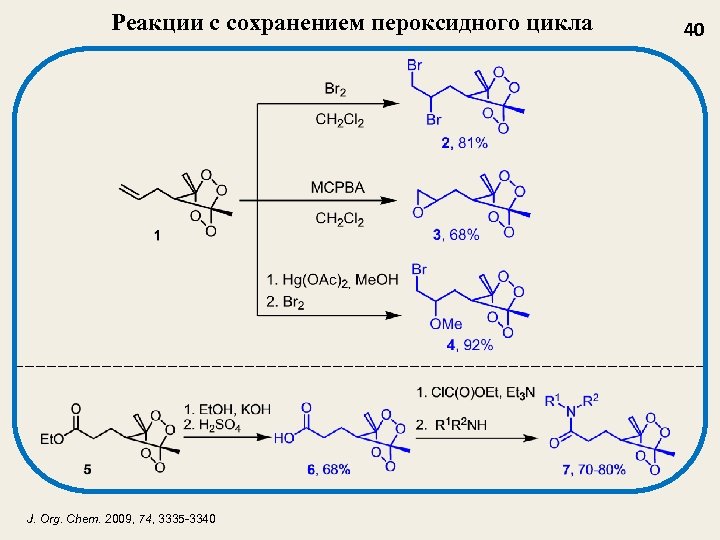 Реакции с сохранением пероксидного цикла J. Org. Chem. 2009, 74, 3335 -3340 40
Реакции с сохранением пероксидного цикла J. Org. Chem. 2009, 74, 3335 -3340 40
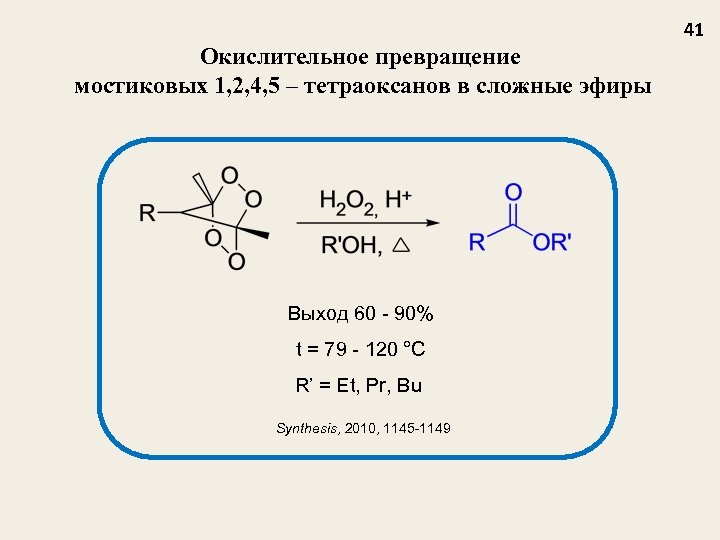 41 Окислительное превращение мостиковых 1, 2, 4, 5 – тетраоксанов в сложные эфиры Выход 60 - 90% t = 79 - 120 °С R’ = Et, Pr, Bu Synthesis, 2010, 1145 -1149
41 Окислительное превращение мостиковых 1, 2, 4, 5 – тетраоксанов в сложные эфиры Выход 60 - 90% t = 79 - 120 °С R’ = Et, Pr, Bu Synthesis, 2010, 1145 -1149
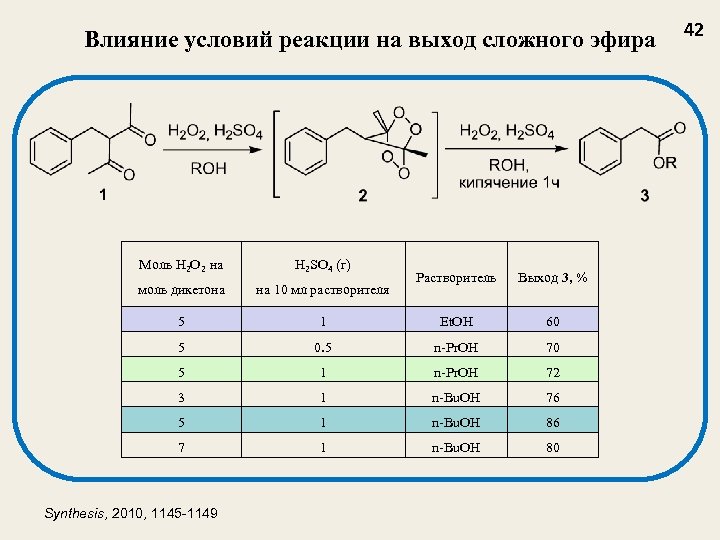 Влияние условий реакции на выход сложного эфира Моль H 2 O 2 на H 2 SO 4 (г) моль дикетона на 10 мл растворителя 5 Растворитель Выход 3, % 1 Et. OH 60 5 0. 5 n-Pr. OH 70 5 1 n-Pr. OH 72 3 1 n-Bu. OH 76 5 1 n-Bu. OH 86 7 1 n-Bu. OH 80 Synthesis, 2010, 1145 -1149 42
Влияние условий реакции на выход сложного эфира Моль H 2 O 2 на H 2 SO 4 (г) моль дикетона на 10 мл растворителя 5 Растворитель Выход 3, % 1 Et. OH 60 5 0. 5 n-Pr. OH 70 5 1 n-Pr. OH 72 3 1 n-Bu. OH 76 5 1 n-Bu. OH 86 7 1 n-Bu. OH 80 Synthesis, 2010, 1145 -1149 42
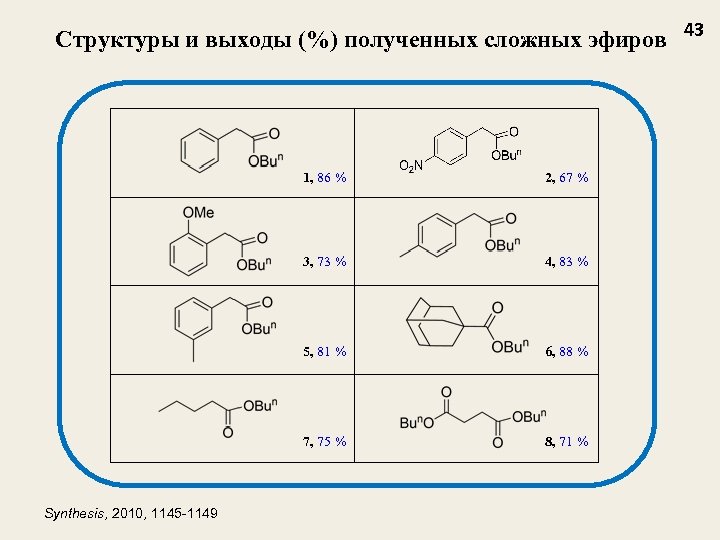 Структуры и выходы (%) полученных сложных эфиров 43 1, 86 % 3, 73 % 4, 83 % 5, 81 % 6, 88 % 7, 75 % Synthesis, 2010, 1145 -1149 2, 67 % 8, 71 %
Структуры и выходы (%) полученных сложных эфиров 43 1, 86 % 3, 73 % 4, 83 % 5, 81 % 6, 88 % 7, 75 % Synthesis, 2010, 1145 -1149 2, 67 % 8, 71 %
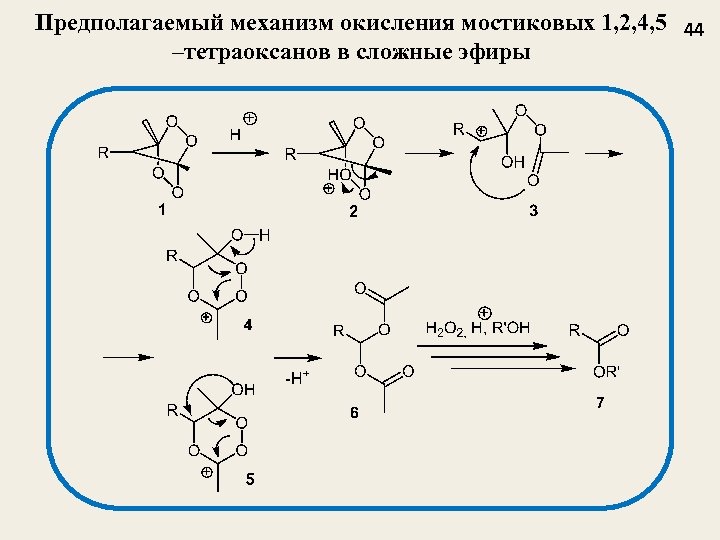 Предполагаемый механизм окисления мостиковых 1, 2, 4, 5 44 –тетраоксанов в сложные эфиры
Предполагаемый механизм окисления мостиковых 1, 2, 4, 5 44 –тетраоксанов в сложные эфиры
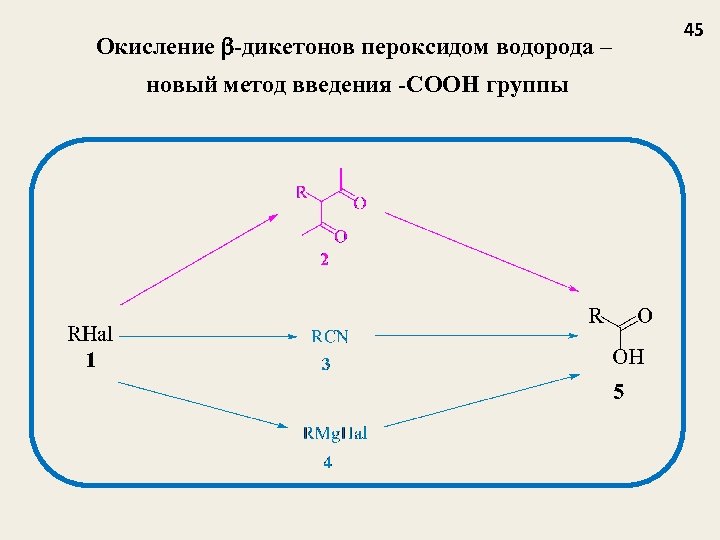 Окисление -дикетонов пероксидом водорода – новый метод введения -COOH группы 45
Окисление -дикетонов пероксидом водорода – новый метод введения -COOH группы 45
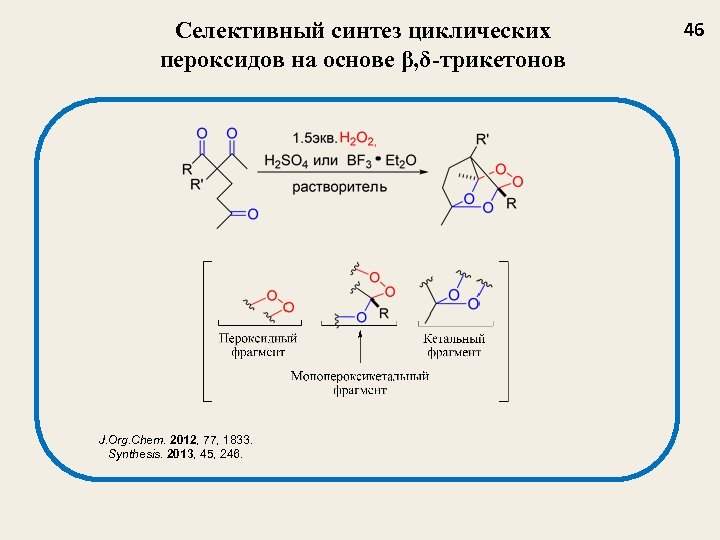 Селективный синтез циклических пероксидов на основе β, δ-трикетонов J. Org. Chem. 2012, 77, 1833. Synthesis. 2013, 45, 246. 46
Селективный синтез циклических пероксидов на основе β, δ-трикетонов J. Org. Chem. 2012, 77, 1833. Synthesis. 2013, 45, 246. 46
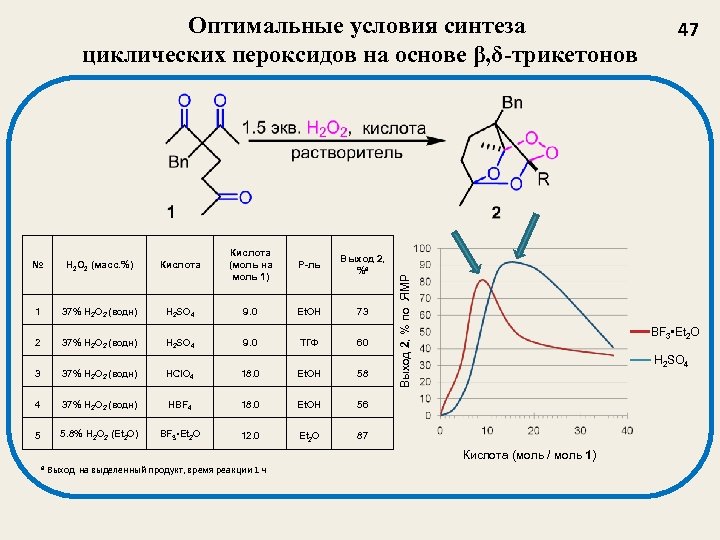 № Н 2 O 2 (масс. %) Кислота (моль на моль 1) Р-ль Выход 2, %a 1 37% H 2 O 2 (водн) H 2 SO 4 9. 0 Et. OH 73 2 37% H 2 O 2 (водн) H 2 SO 4 9. 0 ТГФ 60 3 37% H 2 O 2 (водн) HCl. O 4 18. 0 Et. OH 58 4 37% H 2 O 2 (водн) HBF 4 18. 0 Et. OH 5. 8% H 2 O 2 (Et 2 O) BF 3 • Et 2 O 12. 0 Et 2 O H 2 SO 4 87 Кислота (моль / моль 1) а Выход на выделенный продукт, время реакции 1 ч 47 BF 3 • Et 2 O 56 5 Выход 2, % по ЯМР Оптимальные условия синтеза циклических пероксидов на основе β, δ-трикетонов
№ Н 2 O 2 (масс. %) Кислота (моль на моль 1) Р-ль Выход 2, %a 1 37% H 2 O 2 (водн) H 2 SO 4 9. 0 Et. OH 73 2 37% H 2 O 2 (водн) H 2 SO 4 9. 0 ТГФ 60 3 37% H 2 O 2 (водн) HCl. O 4 18. 0 Et. OH 58 4 37% H 2 O 2 (водн) HBF 4 18. 0 Et. OH 5. 8% H 2 O 2 (Et 2 O) BF 3 • Et 2 O 12. 0 Et 2 O H 2 SO 4 87 Кислота (моль / моль 1) а Выход на выделенный продукт, время реакции 1 ч 47 BF 3 • Et 2 O 56 5 Выход 2, % по ЯМР Оптимальные условия синтеза циклических пероксидов на основе β, δ-трикетонов
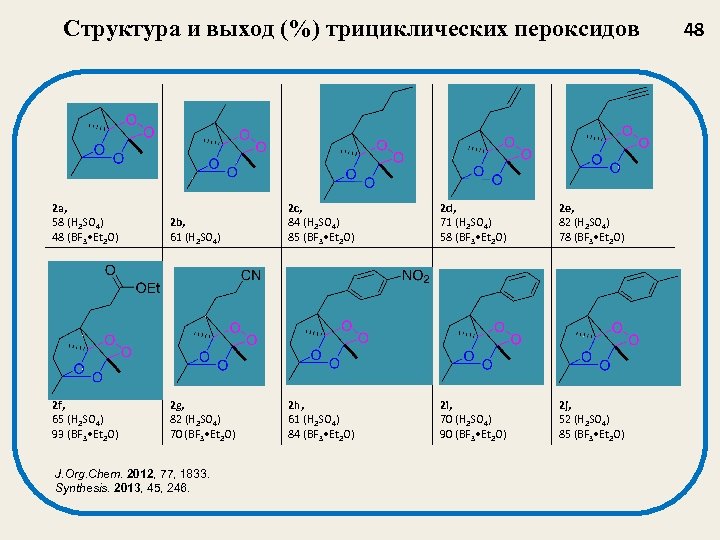 Структура и выход (%) трициклических пероксидов 2 a, 58 (H 2 SO 4) 48 (BF 3 • Et 2 O) 2 f, 65 (H 2 SO 4) 93 (BF 3 • Et 2 O) 2 b, 61 (H 2 SO 4) 2 c, 84 (H 2 SO 4) 85 (BF 3 • Et 2 O) 2 d, 71 (H 2 SO 4) 58 (BF 3 • Et 2 O) 2 e, 82 (H 2 SO 4) 78 (BF 3 • Et 2 O) 2 g, 82 (H 2 SO 4) 70 (BF 3 • Et 2 O) 2 h, 61 (H 2 SO 4) 84 (BF 3 • Et 2 O) 2 i, 70 (H 2 SO 4) 90 (BF 3 • Et 2 O) 2 j, 52 (H 2 SO 4) 85 (BF 3 • Et 2 O) J. Org. Chem. 2012, 77, 1833. Synthesis. 2013, 45, 246. 48
Структура и выход (%) трициклических пероксидов 2 a, 58 (H 2 SO 4) 48 (BF 3 • Et 2 O) 2 f, 65 (H 2 SO 4) 93 (BF 3 • Et 2 O) 2 b, 61 (H 2 SO 4) 2 c, 84 (H 2 SO 4) 85 (BF 3 • Et 2 O) 2 d, 71 (H 2 SO 4) 58 (BF 3 • Et 2 O) 2 e, 82 (H 2 SO 4) 78 (BF 3 • Et 2 O) 2 g, 82 (H 2 SO 4) 70 (BF 3 • Et 2 O) 2 h, 61 (H 2 SO 4) 84 (BF 3 • Et 2 O) 2 i, 70 (H 2 SO 4) 90 (BF 3 • Et 2 O) 2 j, 52 (H 2 SO 4) 85 (BF 3 • Et 2 O) J. Org. Chem. 2012, 77, 1833. Synthesis. 2013, 45, 246. 48
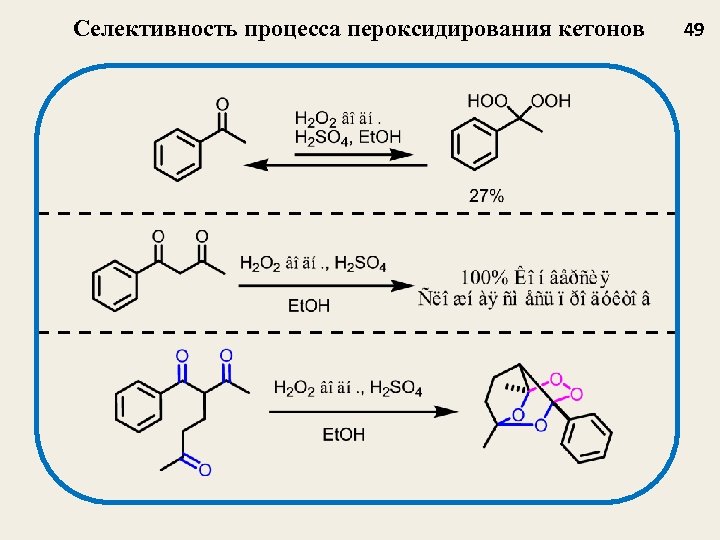 Селективность процесса пероксидирования кетонов 49
Селективность процесса пероксидирования кетонов 49
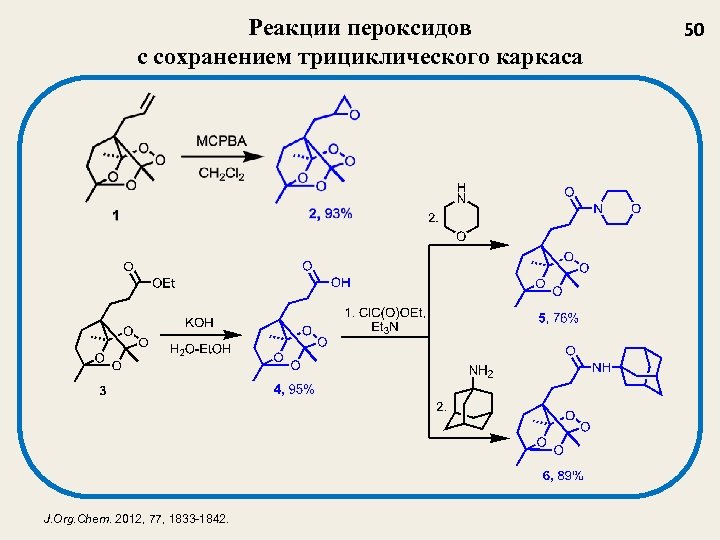 Реакции пероксидов с сохранением трициклического каркаса J. Org. Chem. 2012, 77, 1833 -1842. 50
Реакции пероксидов с сохранением трициклического каркаса J. Org. Chem. 2012, 77, 1833 -1842. 50
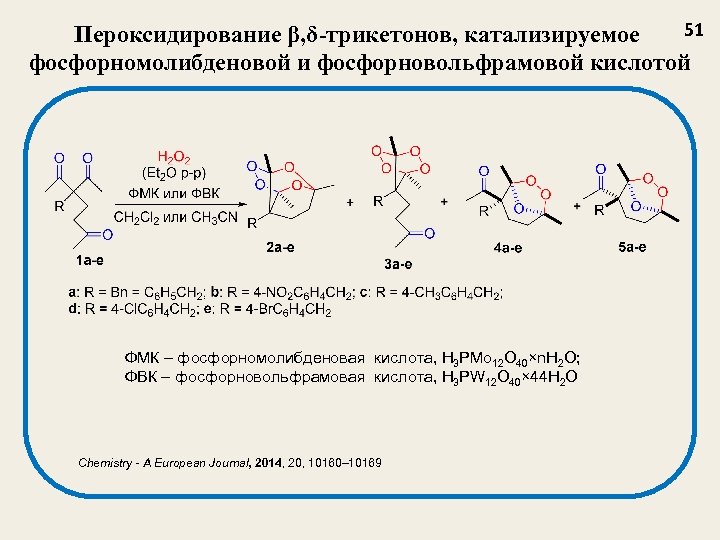 51 Пероксидирование β, δ-трикетонов, катализируемое фосфорномолибденовой и фосфорновольфрамовой кислотой ФМК – фосфорномолибденовая кислота, H 3 PMo 12 O 40×n. H 2 O; ФВК – фосфорновольфрамовая кислота, H 3 PW 12 O 40× 44 H 2 O Chemistry - A European Journal, 2014, 20, 10160– 10169
51 Пероксидирование β, δ-трикетонов, катализируемое фосфорномолибденовой и фосфорновольфрамовой кислотой ФМК – фосфорномолибденовая кислота, H 3 PMo 12 O 40×n. H 2 O; ФВК – фосфорновольфрамовая кислота, H 3 PW 12 O 40× 44 H 2 O Chemistry - A European Journal, 2014, 20, 10160– 10169
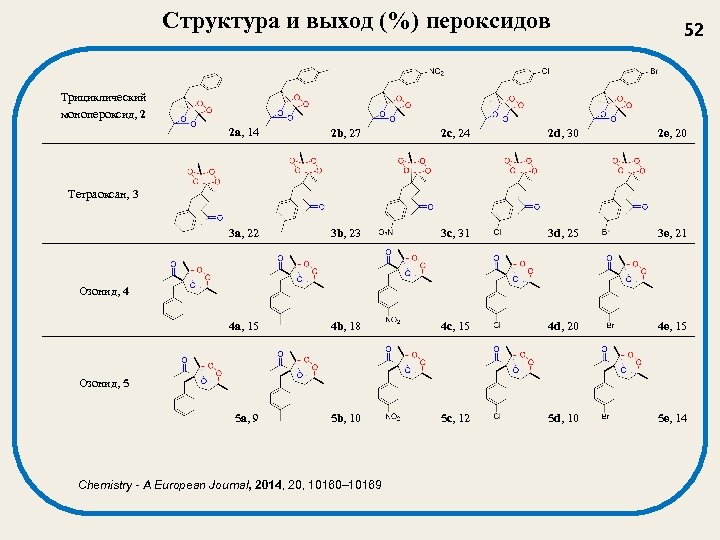 Структура и выход (%) пероксидов 52 Трициклический монопероксид, 2 2 a, 14 2 b, 27 2 c, 24 2 d, 30 2 e, 20 3 a, 22 3 b, 23 3 c, 31 3 d, 25 3 e, 21 4 a, 15 4 b, 18 4 c, 15 4 d, 20 4 e, 15 5 a, 9 5 b, 10 5 c, 12 5 d, 10 5 e, 14 Тетраоксан, 3 Озонид, 4 Озонид, 5 Chemistry - A European Journal, 2014, 20, 10160– 10169
Структура и выход (%) пероксидов 52 Трициклический монопероксид, 2 2 a, 14 2 b, 27 2 c, 24 2 d, 30 2 e, 20 3 a, 22 3 b, 23 3 c, 31 3 d, 25 3 e, 21 4 a, 15 4 b, 18 4 c, 15 4 d, 20 4 e, 15 5 a, 9 5 b, 10 5 c, 12 5 d, 10 5 e, 14 Тетраоксан, 3 Озонид, 4 Озонид, 5 Chemistry - A European Journal, 2014, 20, 10160– 10169
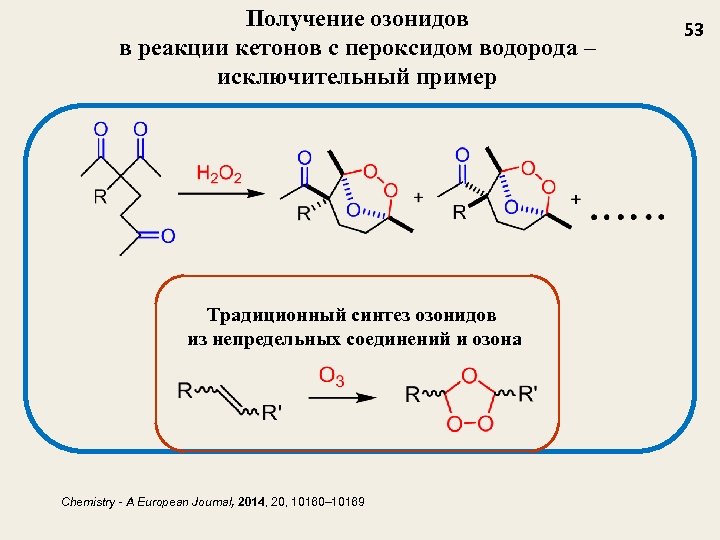 Получение озонидов в реакции кетонов с пероксидом водорода – исключительный пример Традиционный синтез озонидов из непредельных соединений и озона Chemistry - A European Journal, 2014, 20, 10160– 10169 53
Получение озонидов в реакции кетонов с пероксидом водорода – исключительный пример Традиционный синтез озонидов из непредельных соединений и озона Chemistry - A European Journal, 2014, 20, 10160– 10169 53
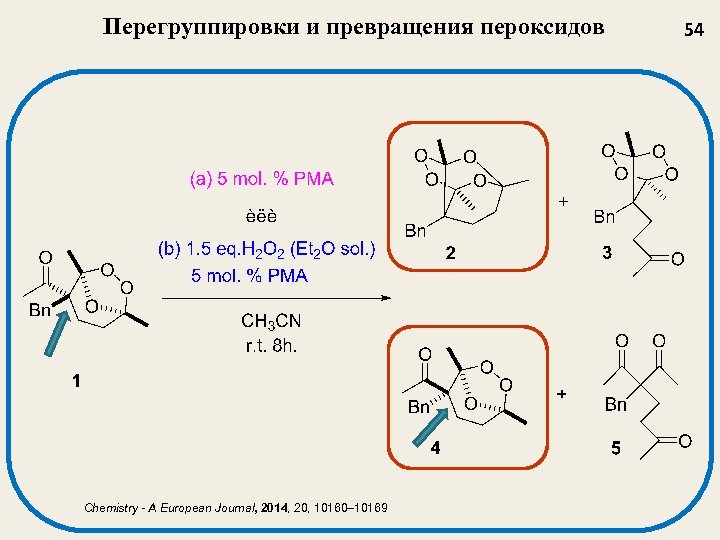 Перегруппировки и превращения пероксидов Chemistry - A European Journal, 2014, 20, 10160– 10169 54
Перегруппировки и превращения пероксидов Chemistry - A European Journal, 2014, 20, 10160– 10169 54
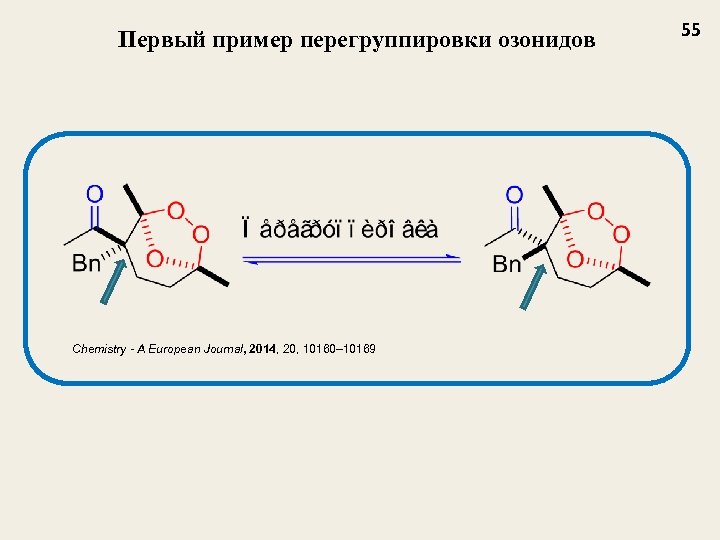 Первый пример перегруппировки озонидов Chemistry - A European Journal, 2014, 20, 10160– 10169 55
Первый пример перегруппировки озонидов Chemistry - A European Journal, 2014, 20, 10160– 10169 55
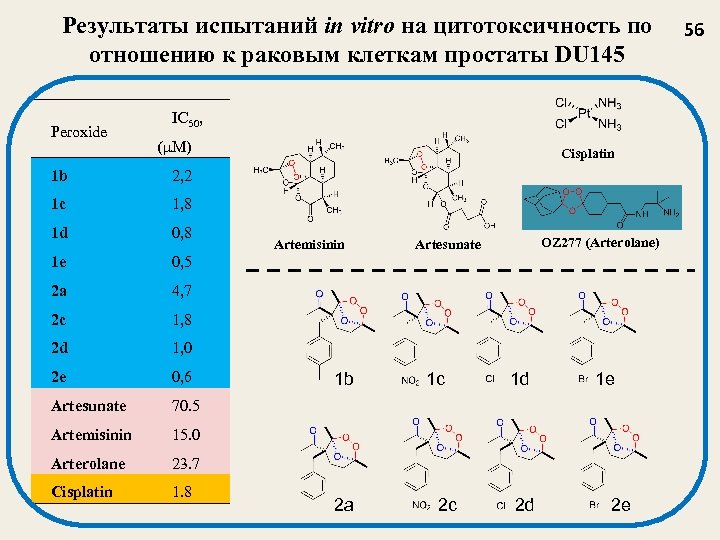 Результаты испытаний in vitro на цитотоксичность по отношению к раковым клеткам простаты DU 145 Peroxide IC 50, (μM) 1 b 2, 2 1 c 1, 8 1 d 0, 8 1 e 0, 5 2 a 4, 7 2 c 1, 8 2 d 1, 0 2 e 0, 6 Artesunate 70. 5 Artemisinin 15. 0 Arterolane 23. 7 Cisplatin 1. 8 Cisplatin Artemisinin 1 b 2 a OZ 277 (Arterolane) Artesunate 1 c 2 c 1 d 2 d 1 e 2 e 56
Результаты испытаний in vitro на цитотоксичность по отношению к раковым клеткам простаты DU 145 Peroxide IC 50, (μM) 1 b 2, 2 1 c 1, 8 1 d 0, 8 1 e 0, 5 2 a 4, 7 2 c 1, 8 2 d 1, 0 2 e 0, 6 Artesunate 70. 5 Artemisinin 15. 0 Arterolane 23. 7 Cisplatin 1. 8 Cisplatin Artemisinin 1 b 2 a OZ 277 (Arterolane) Artesunate 1 c 2 c 1 d 2 d 1 e 2 e 56
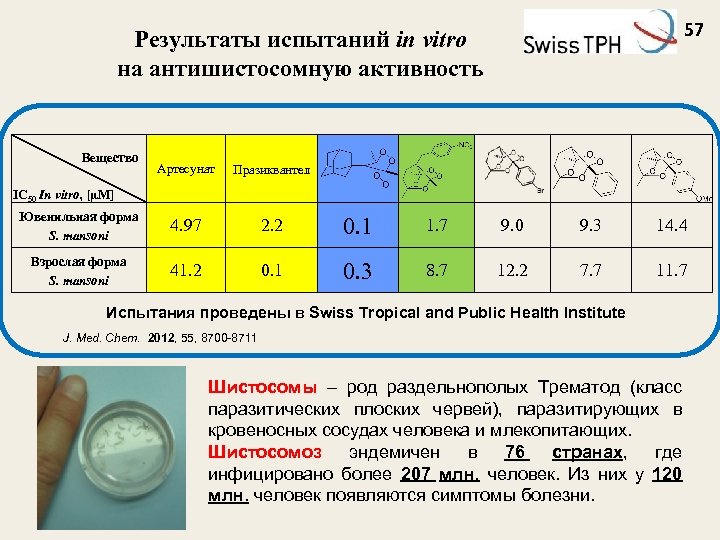 57 Результаты испытаний in vitro на антишистосомную активность Вещество Артесунат Празиквантел Ювенильная форма S. mansoni 4. 97 2. 2 0. 1 1. 7 9. 0 9. 3 14. 4 Взрослая форма S. mansoni 41. 2 0. 1 0. 3 8. 7 12. 2 7. 7 11. 7 IC 50 In vitro, [µM] Испытания проведены в Swiss Tropical and Public Health Institute J. Med. Chem. 2012, 55, 8700 -8711 Шистосомы – род раздельнополых Трематод (класс паразитических плоских червей), паразитирующих в кровеносных сосудах человека и млекопитающих. Шистосомоз эндемичен в 76 странах, где инфицировано более 207 млн. человек. Из них у 120 млн. человек появляются симптомы болезни.
57 Результаты испытаний in vitro на антишистосомную активность Вещество Артесунат Празиквантел Ювенильная форма S. mansoni 4. 97 2. 2 0. 1 1. 7 9. 0 9. 3 14. 4 Взрослая форма S. mansoni 41. 2 0. 1 0. 3 8. 7 12. 2 7. 7 11. 7 IC 50 In vitro, [µM] Испытания проведены в Swiss Tropical and Public Health Institute J. Med. Chem. 2012, 55, 8700 -8711 Шистосомы – род раздельнополых Трематод (класс паразитических плоских червей), паразитирующих в кровеносных сосудах человека и млекопитающих. Шистосомоз эндемичен в 76 странах, где инфицировано более 207 млн. человек. Из них у 120 млн. человек появляются симптомы болезни.
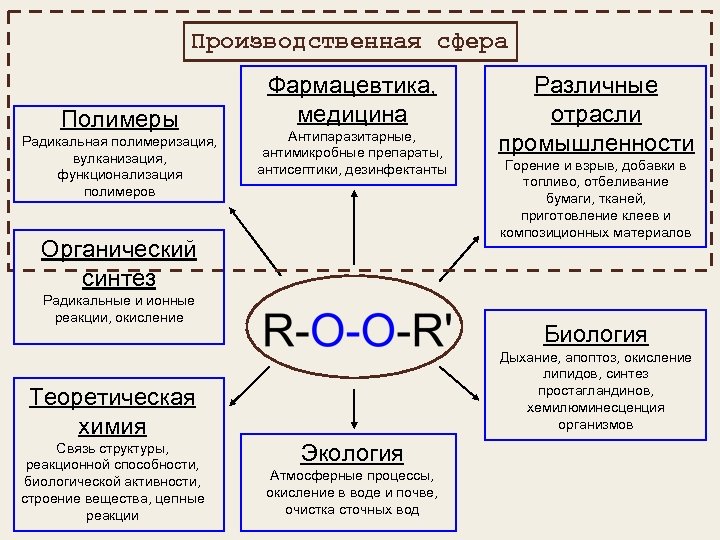 Производственная сфера Полимеры Радикальная полимеризация, вулканизация, функционализация полимеров Фармацевтика, медицина Антипаразитарные, антимикробные препараты, антисептики, дезинфектанты Органический синтез Радикальные и ионные реакции, окисление Горение и взрыв, добавки в топливо, отбеливание бумаги, тканей, приготовление клеев и композиционных материалов Биология Дыхание, апоптоз, окисление липидов, синтез простагландинов, хемилюминесценция организмов Теоретическая химия Связь структуры, реакционной способности, биологической активности, строение вещества, цепные реакции Различные отрасли промышленности Экология Атмосферные процессы, окисление в воде и почве, очистка сточных вод
Производственная сфера Полимеры Радикальная полимеризация, вулканизация, функционализация полимеров Фармацевтика, медицина Антипаразитарные, антимикробные препараты, антисептики, дезинфектанты Органический синтез Радикальные и ионные реакции, окисление Горение и взрыв, добавки в топливо, отбеливание бумаги, тканей, приготовление клеев и композиционных материалов Биология Дыхание, апоптоз, окисление липидов, синтез простагландинов, хемилюминесценция организмов Теоретическая химия Связь структуры, реакционной способности, биологической активности, строение вещества, цепные реакции Различные отрасли промышленности Экология Атмосферные процессы, окисление в воде и почве, очистка сточных вод


