143.ppt
- Количество слайдов: 13

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Лекция Металлы VIБ подгруппы

Цель лекции: ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА изложение основных химических свойств и реакций элементов VIБ подгруппы Компетенции, формируемые у студента: Умения: прогнозировать на основе современных представлений о строении атомов и химической связи, возможность протекания ОВР реакций, химические свойства соединений элементов VIБ подгруппы Модуль V. Лекция. Металлы Vi. Б подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Природные соединения Содержание Cr в земной коре составляет около 0, 01 % Элементы Mo, W – достаточно распространенные элементы их содержание в земной коре оценивается в 10 -4%. Важнейшими минералами являются хромистый железняк Fe. Cr 2 O 4. Модуль V. Лекция. Металлы Vi. Б подгруппы Mo. S 2 – молибденит, Pb. Mo. O 4 – вульфенит, Ca. Mo. O 4 – повелит и (Fe, Mn)WO 4 – вольфрамит
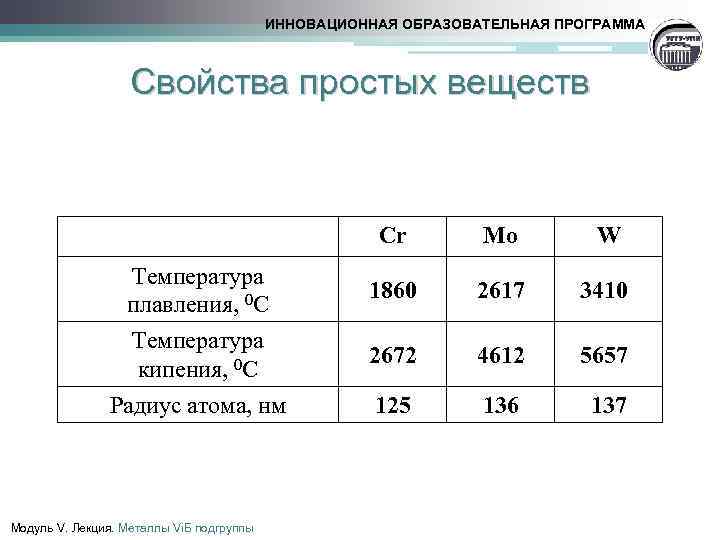
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Свойства простых веществ Cr Температура плавления, 0 С Температура кипения, 0 С Радиус атома, нм Модуль V. Лекция. Металлы Vi. Б подгруппы Mo W 1860 2617 3410 2672 4612 5657 125 136 137

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Соединения хрома Диаграмма Латимера (р. H<7) Модуль V. Лекция. Металлы Vi. Б подгруппы
![ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Получение и свойства хроматов 2 Na 3[Cr(OH)6] + 3 H 2 ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Получение и свойства хроматов 2 Na 3[Cr(OH)6] + 3 H 2](https://present5.com/presentation/27360963_132774657/image-6.jpg)
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Получение и свойства хроматов 2 Na 3[Cr(OH)6] + 3 H 2 O 2 = 2 Na 2 Cr. O 4 + 8 H 2 O + 2 Na. OH K 2 Cr. O 4 + 2 Н 2 SO 4(конц) = 2 KHSO 4 + 2 Cr. O 3 + H 2 O Сr 2 O 72– + 14 H+ +6 e– = 2 Cr 3+ + 7 H 2 O; (E 0= +1, 33 В) Cr. O 42– + 4 H 2 O +3 e– = Cr(OH)3 + 5 OН– ; (E 0= +0, 13 В) Модуль V. Лекция. Металлы Vi. Б подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Хроматы и бихроматы Модуль V. Лекция. Металлы Vi. Б подгруппы
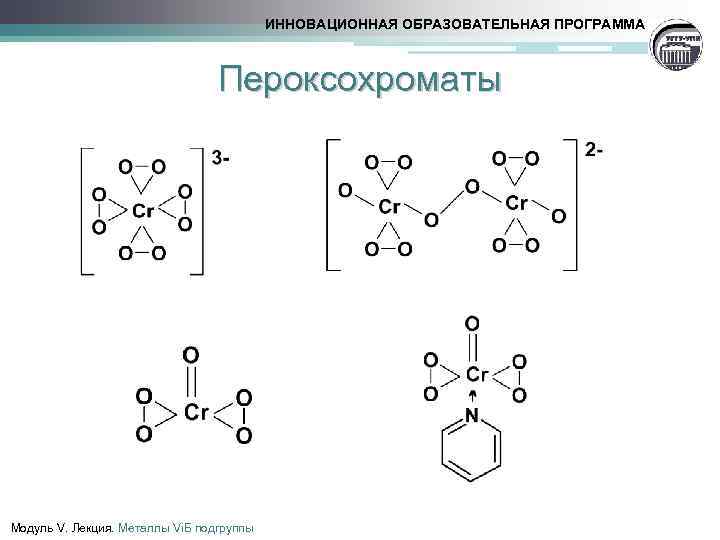
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Пероксохроматы Модуль V. Лекция. Металлы Vi. Б подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Соединения хрома (+3) Cr(OH)3 + 3 Na. OН = 2 Na 3[Cr(OH)6] Cr(OH)3 + 3 НCl = Cr. Cl 3 + 3 H 2 O [Cr(H 2 O)6]Cl 3 – фиолетового цвета [Cr. Сl(H 2 O)5]Cl 2 • H 2 O – бледно-зеленого цвета [Cr. Сl 2(H 2 O)4]Cl • 2 H 2 O – темно-зеленого цвета Модуль V. Лекция. Металлы Vi. Б подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Соединения хрома (+2) Cr + 2 HX = Cr. X 2 + H 2 Cr. X 3 + 1/2 H 2 = Cr. X 2 + HX Cr + I 2 = Cr. I 2 [Cr 2(CH 3 COO)4(H 2 O)2] 2 Cr. Cl 2 + 2 HCl + 1/2 O 2 = 2 Cr. Cl 3 + H 2 O Модуль V. Лекция. Металлы Vi. Б подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Полимеризация молибдатов и вольфраматов Mo 7 O 246– + 4 H 2 O 7 Mo. O 42– +8 H+ 12 WO 42– +14 H+ Модуль V. Лекция. Металлы Vi. Б подгруппы W 12 O 4110– + 7 H 2 O

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА § § § Заключение Наиболеее распространенными степенями окисления у Cr являются +2, +3, +6 Кислотно–основной характер оксидов и гидроксидов Cr закономерно изменяется в зависимости от степени окисления: в степени окисления+2 оксид и гидроксид являются основными, а в высшей степени окисления – кислотными, причем, H 2 Cr. O 4 – это сильная кислота. В щелочных растворах более устойчив Cr. O 42– (желтого цвета), в интервале р. Н от 2 до 6 сосуществует в равновесии с Cr 2 O 72– (оранжевого цвета) и HCr. O 4– Бихроматы и хроматы являются сильными окислителями В водных растворах соединения Cr(+2) сильные и быстродействующие восстановители. Молибдаты Mo. O 42– и вольфраматы WO 42– при подкислении склонны к полимеризации Модуль V. Лекция. Металлы Vi. Б подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Рекомендуемая литература § § Никольский А. Б. , Суворов А. В. Химия. - СПб: Химиздат, 2001 § Карапетьянц М. Х. Общая и неорганическая химия. - М. : Химия, 2000 § Угай Я. А. Общая и неорганическая химия. - М. : Высш. шк. , 2007 § Неорганическая химия. В 3 т. Т. 1: Физико-химические основы неорганической химии. Под ред. Ю. Д. Третьякова. - М. : Академия, 2004 § Гаршин А. П. Неорганическая химия в схемах, рисунках, таблицах, формулах, химических реакциях. - СПб. : Лань, 2000 Степин Б. Д. , Цветков А. А. Неорганическая химия. - М. : Высш. шк. , 1994 Модуль V. Лекция. Металлы Vi. Б подгруппы
143.ppt