144.ppt
- Количество слайдов: 13

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Лекция Металлы VБ–подгруппы

Цель лекции: ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА изложение основных химических свойств и реакций элементов VБ-подгруппы Компетенции, формируемые у студента: Умения: прогнозировать на основе современных представлений о строении атомов и химической связи, возможность протекания ОВР реакций, химические свойства соединений элементов VБ подгруппы Модуль V. Лекция. Металлы IA и IA подгрупп

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Природные соединения Содержание V в земной коре составляет около 0, 015 % Элементы Nb, Ta – достаточно распространенные элементы их содержание в земной коре оценивается в 103 - 10 -4%. Важнейшими минералами являются Минерал ванадит 3 Pb 3(VО 4)2 • Pb. Cl 2 Модуль V. Лекция. Металлы VБ подгруппы Fe(Ta. O 3)2 – танталит Fe(Nb. O 3)2– колумбит, V(S 2)2 – патронит
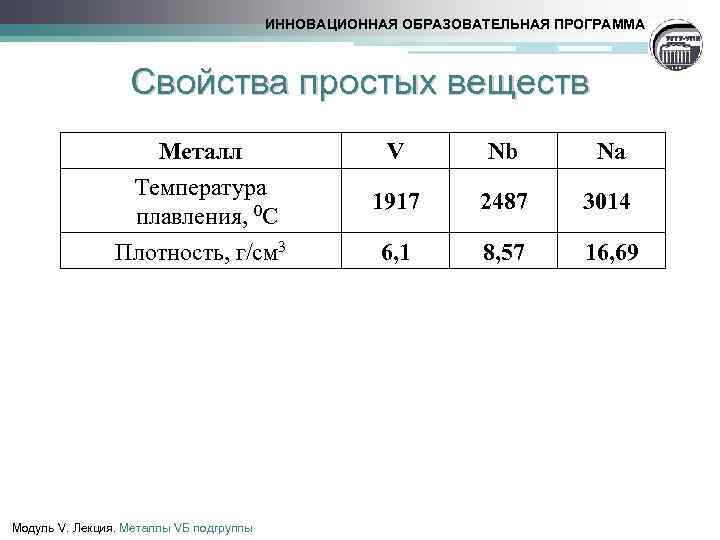
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Свойства простых веществ Металл Температура плавления, 0 С Плотность, г/cм 3 Модуль V. Лекция. Металлы VБ подгруппы V Nb Na 1917 2487 3014 6, 1 8, 57 16, 69

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Свойства простых веществ 2 V + 12 HF = 2 H 3[VF 6] + 3 Н 2 3 Ta + 5 HNO 3 + 21 HF = 3 H 2[Ta. F 7] + 5 NO+ 10 Н 2 O V + 3 H 2 SO 4 (к. ) = VOSO 4 + 2 SO 2 + 3 H 2 O V + 6 HNO 3 (к. ) = (VO 2)NO 3 + 5 NO 2 + 3 H 2 O 3 V + 12 НС 1 + 4 HNO 3 = 3 VC 14 + 4 NO + 8 Н 2 О 4 Nb + 12 Na. OH (ж. ) + 5 O 2 = 4 Na 3 Nb. O 4(ж. ) + 6 Н 2 О Модуль V. Лекция. Металлы VБ подгруппы
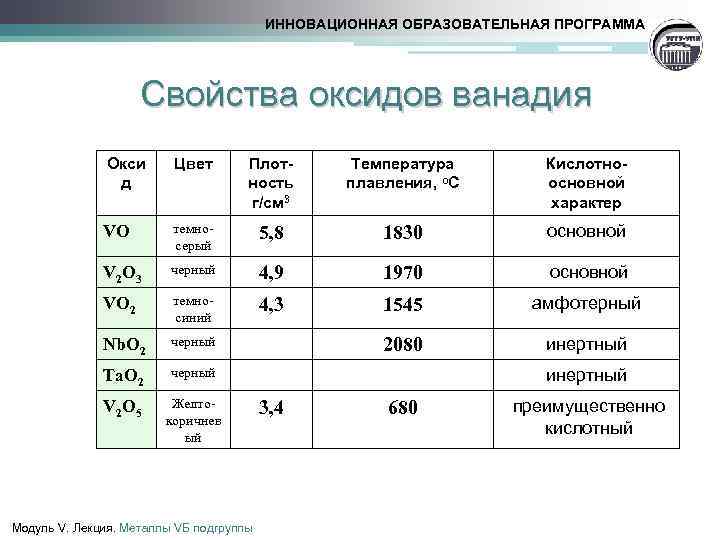
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Cвойства оксидов ванадия Окси д Цвет Плотность г/см 3 Температура плавления, о. С Кислотноосновной характер VO темносерый 5, 8 1830 основной V 2 O 3 черный 4, 9 1970 основной VO 2 темносиний 4, 3 1545 амфотерный Nb. O 2 черный 2080 инертный Ta. O 2 черный V 2 O 5 Желтокоричнев ый Модуль V. Лекция. Металлы VБ подгруппы инертный 3, 4 680 преимущественно кислотный

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Свойства VO 2 Амфотерность 4 VO 2 + 2 Na. OH = Na 2 V 4 O 9 + H 2 O VO 2 + 2 Na. OH = Na 2 VO 3 + H 2 O VO 2 + 2 H 2 SO 4 = (VO)SO 4 + H 2 O Катион VO 2+ окрашен в красивый синий цвет Модуль V. Лекция. Металлы VБ подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Свойства оксидов металлов(+5) Ta 2 O 5 + 6 Na. OH = 2 Na 3 Ta. O 4 + 3 H 2 O (г. ) Nb 2 O 5 + 3 Na 2 CO 3 = 2 Na 3 Nb. O 4 + 3 CO 2 Оксид V 2 O 5 взаимодействует с расплавами и с растворами щелочей с образованием: ортованадата – Na 3 VO 4 пированадата – Na 4 V 2 O 7 триметаванадата – Na 3 V 3 O 9 Модуль V. Лекция. Металлы VБ подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Окислительно-воостановительные свойства V(+5) + восста новитель + кислота Степень окисления +5 +4 +3 +2 {VO 3–} VO 2+ V 3+ V 2+ Модуль V. Лекция. Металлы VБ подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Окислительно-воостановительные свойства V(+5) Соединения V(+5) проявляют окислительные свойства 2 NH 4 VO 3 + Zn + 2 H 2 SO 4 = VOSO 4 + Zn. SO 4 + (NH 4)2 SO 4 + 2 H 2 O 2 VOSO 4 + Zn + 2 H 2 SO 4 = V 2(SO 4)3 + Zn. SO 4 + 2 H 2 O V 2(SO 4)3 + Zn = 2 VSO 4 + Zn. SO 4 Модуль V. Лекция. Металлы VБ подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Полимеризация ванадатов при р. Н больше 13 существует ортованадат – VO 43– при понижении р. Н последовательно образуются: V 2 O 74– Модуль V. Лекция. Металлы VБ подгруппы V 3 O 93– V 10 O 286–

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Заключение § Наиболеее распространенными степенями окисления у V являются +2, +3, +4 и +5. § Кислотно–основной характер оксидов и гидроксидов М(V, Nb, Ta) закономерно изменяется в зависимости Ta от степени окисления: в степени окисления+2 оксид и гидроксид являются основными, а в высшей степени окисления – кислотными. § Ванадаты являются сильными окислителями. § В водных растворах соединения V(+2) сильные и быстродействующие восстановители. § Ванадат VO 3–при подкислении склонен к 4 полимеризации Модуль V. Лекция. Металлы VБ подгруппы

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Рекомендуемая литература § § Никольский А. Б. , Суворов А. В. Химия. - СПб: Химиздат, 2001 § Карапетьянц М. Х. Общая и неорганическая химия. - М. : Химия, 2000 § Угай Я. А. Общая и неорганическая химия. - М. : Высш. шк. , 2007 § Неорганическая химия. В 3 т. Т. 1: Физико-химические основы неорганической химии. Под ред. Ю. Д. Третьякова. - М. : Академия, 2004 § Гаршин А. П. Неорганическая химия в схемах, рисунках, таблицах, формулах, химических реакциях. - СПб. : Лань, 2000 Степин Б. Д. , Цветков А. А. Неорганическая химия. - М. : Высш. шк. , 1994 Модуль V. Лекция. Металлы VБ подгруппы
144.ppt