L2_Entropia_Energia_Gibbsa.ppt
- Количество слайдов: 17

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Лекция 2 ЭНЕРГЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ. ЭНТРОПИЯ И ЭНЕРГИЯ ГИББСА

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Содержание § Энтропия § Второе начало термодинамики § Энергия Гиббса. Термодинамическая возможность прохождения химической реакции § Влияние температуры на направление химической реакции § Расчет стандартной энергии Гиббса химической реакции Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Энтропия (S) Предложена Клаузиусом как функция, изменение которой равно отношению теплоты, поглощенной системой, к абсолютной температуре: Q – количество теплоты, получаемое системой при температуре T Подведенная к системе при постоянной температуре теплота расходуется на увеличение энтропии Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Термодинамическая вероятность состояния Состояние системы можно характеризовать § значениями параметров (температура, давление, объем), которые определяют макросостояние системы § совокупностью микросостояний системы, которые определяются распределением частиц по доступным уровням энергии Число микросостояний, соответствующее данному макросостоянию системы при заданных объеме и внутренней энергии, называют термодинамической вероятностью состояния (W) Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса
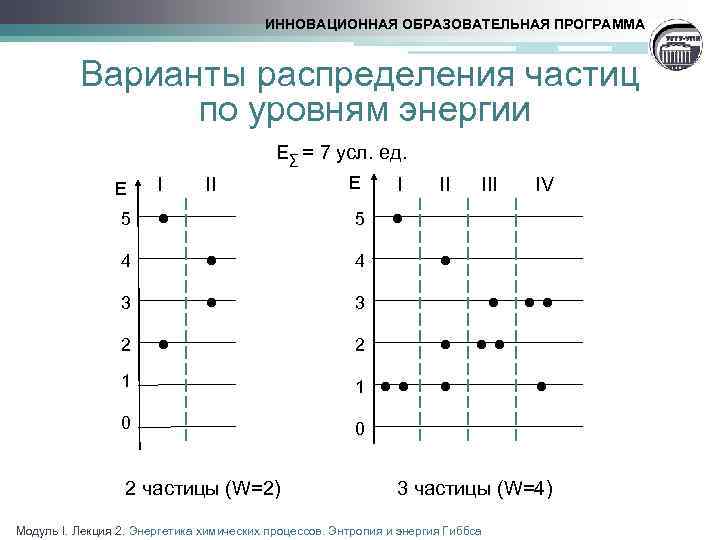
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Варианты распределения частиц по уровням энергии I Е 5 • • 3 • Е I 5 II • 4 2 E∑ = 7 усл. ед. • 4 3 2 1 1 0 II IV • • • 0 2 частицы (W=2) 3 частицы (W=4) Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Энтропия - мера термодинамической вероятности состояния системы Формула Больцмана: k – постоянная Больцмана R – универсальная газовая постоянная NA – число Авогадро Размерность энтропии Дж/(моль∙К) Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Закономерности изменения энтропии § Увеличением энтропии § сопровождаются процессы, связанные с увеличением неупорядоченности: нагревание, плавление, сублимация, испарение, растворение твердых веществ; реакции с увеличением объема системы и др. Уменьшением энтропии сопровождаются процессы, связанные с увеличением упорядоченности: охлаждение, кристаллизация, конденсация веществ; реакции с уменьшением объема системы и др. Пример. При переходе твердое вещество жидкость газ происходит увеличение неупорядоченности системы и возрастание энтропии: Вещество H 2 O(к) H 2 O(ж) H 2 O(г) S 0298, Дж/(моль. К) 44, 8 70, 1 188, 7 Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Второе начало термодинамики: самопроизвольные процессы в изолированных системах сопровождаются увеличением энтропии Пример. Теплообмен в изолированной системе между соприкасающимися телами A и B TA>TB S>0, энтропия увеличивается Условие самопроизвольного прохождения процесса в закрытых системах: Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Расчет изменения энтропии химической реакции в стандартных условиях Энтропия реакции равна разности сумм энтропий продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов: S 0 исх, S 0 прод - стандартные энтропии исходных веществ и продуктов реакции (справочные данные) nисх, nпрод - стехиометрические коэффициенты Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Энергия Гиббса Самопроизвольное прохождение химической реакции в закрытой системе (р, Т = const) возможно при условии T S > Qp Qp = H T S > H или H - T S<0 При переходе системы из состояния 1 в состояние 2: H = H 2 – H 1 S = S 2 – S 1 (H 2 – H 1) – T(S 2 – S 1) < 0 (H 2 – TS 2) – (H 1 – TS 1) < 0 Mатематическое определение энергии Гиббса: G = H – TS при p, T = const ∆G = ∆H – T∆S при р, Т = const Значение G<0 - условие возможности самопроизвольного прохождения реакции в закрытой системе при р, Т = const Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Энергия Гиббса – критерий возможности самопроизвольного прохождения химических реакций Процессы, для которых G<0 – термодинамически возможные G>0 – термодинамически невозможные Для обратимых химических процессов: § G<0 возможна самопроизвольная прямая реакция § G>0 возможна самопроизвольная обратная реакция § G=0 состояние химического равновесия (прямая и обратная реакции равновероятны) Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Влияние температуры на направление химической реакции 1. H<0, S<0 реакции термодинамически возможны ( G<0) при низких температурах, при высоких температурах возможны обратные реакции ∆G, к. Дж 3 1 Пример: N 2 + 3 H 2 = 2 NH 3 2. H>0, S>0 реакции термодинамически возможны ( G<0) при высоких температурах, при низких температурах возможны обратные реакции Пример: Ca. CO 3 = Ca. O + CO 2 3. H>0, S<0 G>0, реакции при любых температурах термодинамически невозможны Пример: N 2 + 2 O 2 = 2 NO 2 4. H<0, S>0 G<0, реакции при любых температурах термодинамически возможны. Пример: 2 C + O 2 = 2 CO Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса Т, К 2 4

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Расчет стандартной энергии Гиббса химической реакции В справочниках – значения стандартных энергий Гиббса образования веществ ( G 0 обр, к. Дж/моль). Стандартной энергией Гиббса образования называют энергию Гиббса реакции образования одного моля данного вещества из простых веществ, устойчивых в стандартных условиях. Способ 1 ( G 0 обр G 0) G 0 = Σ nпрод G 0 обр. прод ‑ Σ nисх G 0 обр. исх nисх, nпрод ‑ стехиометрические коэффициенты Способ 2 ( H 0 обр H 0; S 0 S 0) H 0 = Σ nпрод H 0 обр. прод ‑ Σ nисх H 0 обр. исх G 0 = H 0 ‑ T S 0 = Σ nпрод. S 0 прод ‑ Σ nисх. S 0 исх Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса
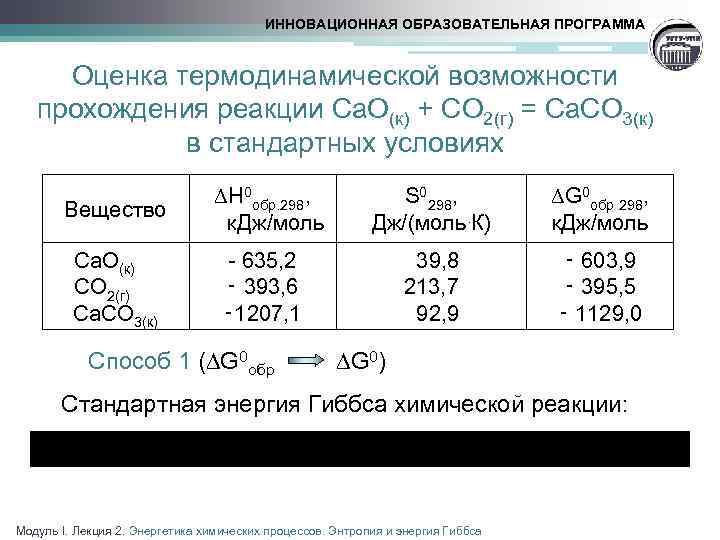
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Оценка термодинамической возможности прохождения реакции Ca. O(к) + CO 2(г) = Ca. CO 3(к) в стандартных условиях Вещество Ca. O(к) CO 2(г) Ca. CO 3(к) H 0 обр. 298, к. Дж/моль - 635, 2 ‑ 393, 6 ‑ 1207, 1 S 0298, Дж/(моль. К) 39, 8 213, 7 92, 9 G 0 обр 298, к. Дж/моль ‑ 603, 9 ‑ 395, 5 ‑ 1129, 0 Способ 1 ( G 0 обр G 0) Стандартная энергия Гиббса химической реакции: Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса
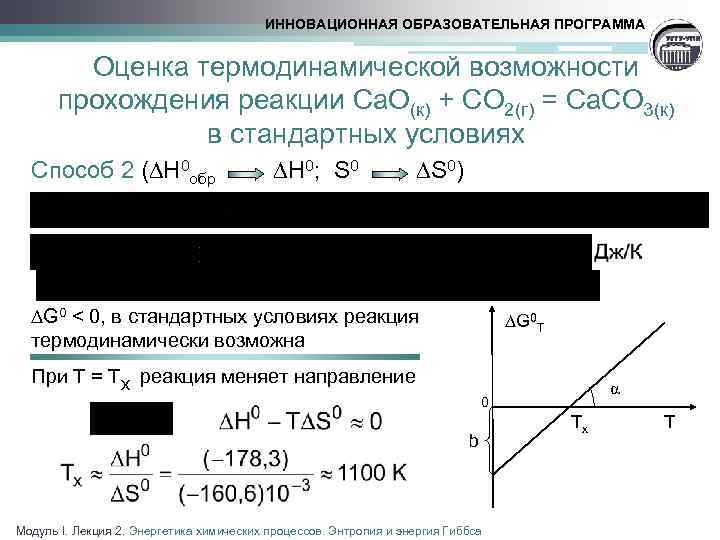
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Оценка термодинамической возможности прохождения реакции Ca. O(к) + CO 2(г) = Ca. CO 3(к) в стандартных условиях Способ 2 ( H 0 обр H 0; S 0) ∆G 0 < 0, в стандартных условиях реакция термодинамически возможна ∆G 0 Т При Т = Тх реакция меняет направление α 0 b Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса Tx T

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Заключение § Согласно II началу термодинамики самопроизвольные процессы в изолированных системах сопровождаются увеличением энтропии § Энтропия по своему физическому смыслу является мерой неупорядоченности системы § В закрытых системах осуществление химических реакций определяется стремлением системы перейти в состояние с большей неупорядоченностью ( S>0) и наименьшей внутренней энергией, с выделением ее части в форме теплоты ( H<0) или работы. Самопроизвольно протекают процессы, в которых G < 0 § Энергия Гиббса ‑ термодинамическая функция состояния, определяется соотношением: G = H ‑ T S при р, Т = const § Критерием возможности самопроизвольного прохождения химических реакций в закрытых системах является уменьшение энергии Гиббса G<0 Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Рекомендуемая литература § § Никольский А. Б. , Суворов А. В. Химия. - СПб: Химиздат, 2001 § Карапетьянц М. Х. Общая и неорганическая химия. - М. : Химия, 2000 § § Угай Я. А. Общая и неорганическая химия. - М. : Высш. шк. , 2007 § Гаршин А. П. Неорганическая химия в схемах, рисунках, таблицах, формулах, химических реакциях. - СПб. : Лань, 2000 Степин Б. Д. , Цветков А. А. Неорганическая химия. - М. : Высш. шк. , 1994 Неорганическая химия. В 3 т. Т. 1: Физико-химические основы неорганической химии. Под ред. Ю. Д. Третьякова. - М. : Академия, 2004 Модуль I. Лекция 2. Энергетика химических процессов. Энтропия и энергия Гиббса
L2_Entropia_Energia_Gibbsa.ppt