74.ppt
- Количество слайдов: 21

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Лекция 10 ГИДРОЛИЗ СОЛЕЙ

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Содержание § Общие понятия § Количественные характеристики гидролиза солей q q Константа гидролиза Степень гидролиза § Расчет степени гидролиза и р. Н водных растворов солей § Примеры гидролиза солей q Гидролиз солей слабых кислот и сильных оснований q Гидролиз солей слабых оснований и сильных кислот q Гидролиз солей слабых оснований и слабых кислот § Необратимый гидролиз Модуль 2. Лекция 10. Гидролиз солей
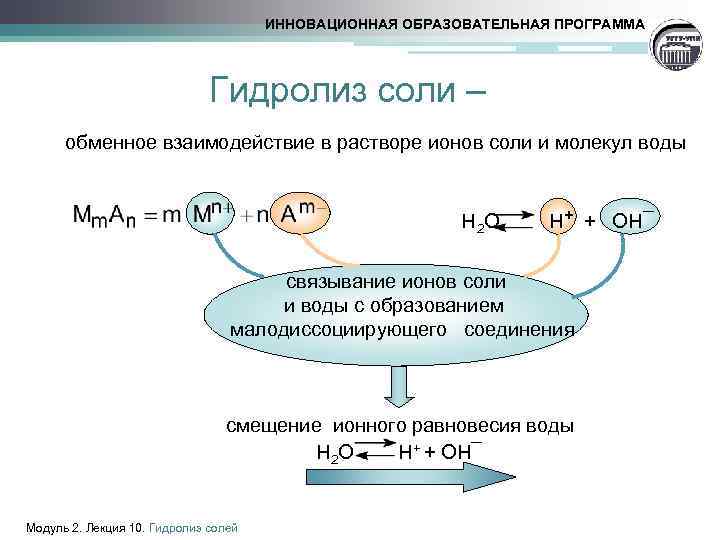
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Гидролиз соли – обменное взаимодействие в растворе ионов соли и молекул воды Н 2 О Н+ + ОН¯ связывание ионов соли и воды с образованием малодиссоциирующего соединения смещение ионного равновесия воды Н 2 О Н+ + ОН¯ Модуль 2. Лекция 10. Гидролиз солей
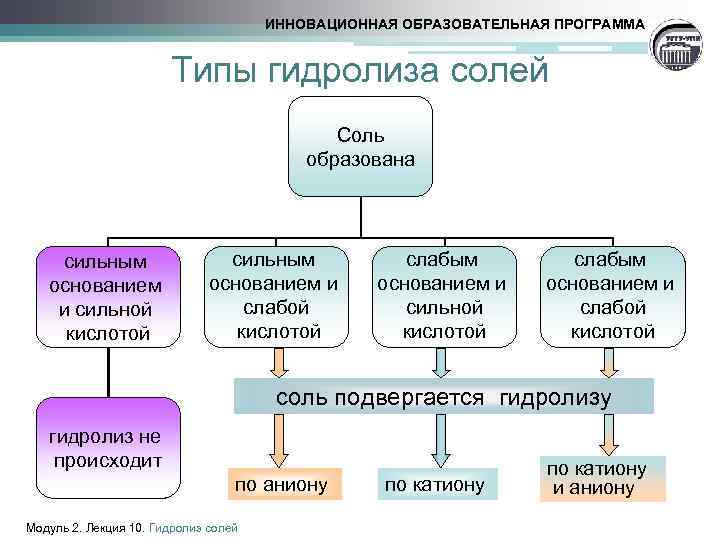
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Типы гидролиза солей Соль образована сильным основанием и сильной кислотой сильным основанием и слабой кислотой слабым основанием и сильной кислотой слабым основанием и слабой кислотой соль подвергается гидролизу гидролиз не происходит по аниону Модуль 2. Лекция 10. Гидролиз солей по катиону и аниону
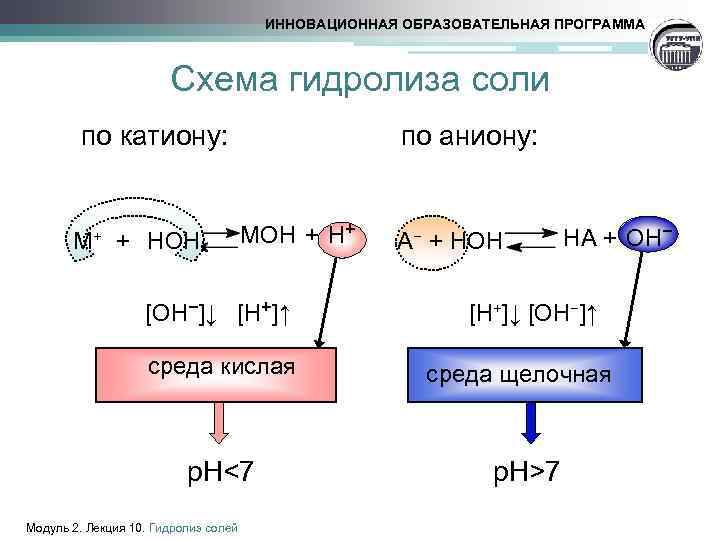
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Схема гидролиза соли по катиону: по аниону: М + НОН MOH + H+ + [ОН−]↓ [H+]↑ среда кислая p. H<7 Модуль 2. Лекция 10. Гидролиз солей А− + НОН HА + OH− [H+]↓ [ОН−]↑ cреда щелочная p. H>7
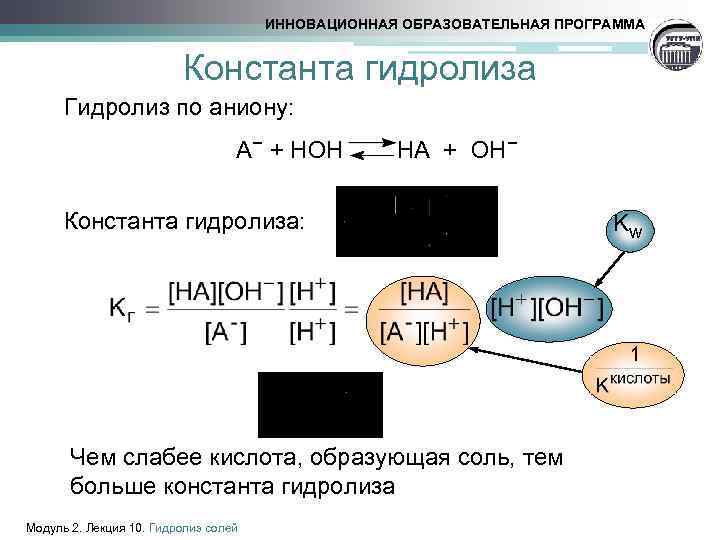
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Константа гидролиза Гидролиз по аниону: А− + НОН НА + ОН− Константа гидролиза: Чем слабее кислота, образующая соль, тем больше константа гидролиза Модуль 2. Лекция 10. Гидролиз солей Kw
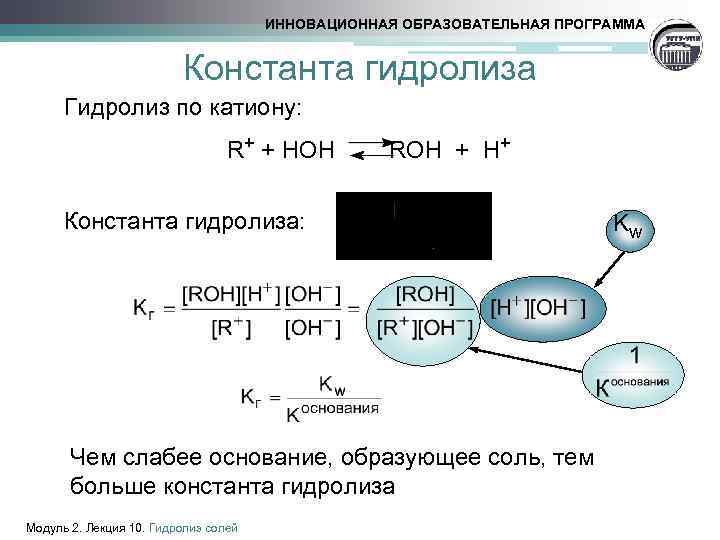
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Константа гидролиза Гидролиз по катиону: R+ + НОН ROН + Н+ Константа гидролиза: Чем слабее основание, образующее соль, тем больше константа гидролиза Модуль 2. Лекция 10. Гидролиз солей Kw
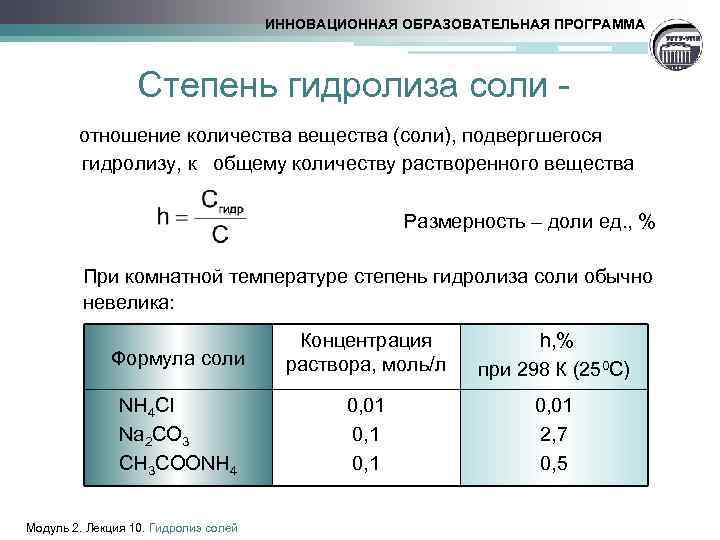
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Степень гидролиза соли - отношение количества вещества (соли), подвергшегося гидролизу, к общему количеству растворенного вещества Размерность – доли ед. , % При комнатной температуре степень гидролиза соли обычно невелика: Формула соли NH 4 Cl Na 2 CO 3 CН 3 СООNH 4 Модуль 2. Лекция 10. Гидролиз солей Концентрация раствора, моль/л h, % при 298 К (250 С) 0, 01 0, 01 2, 7 0, 5
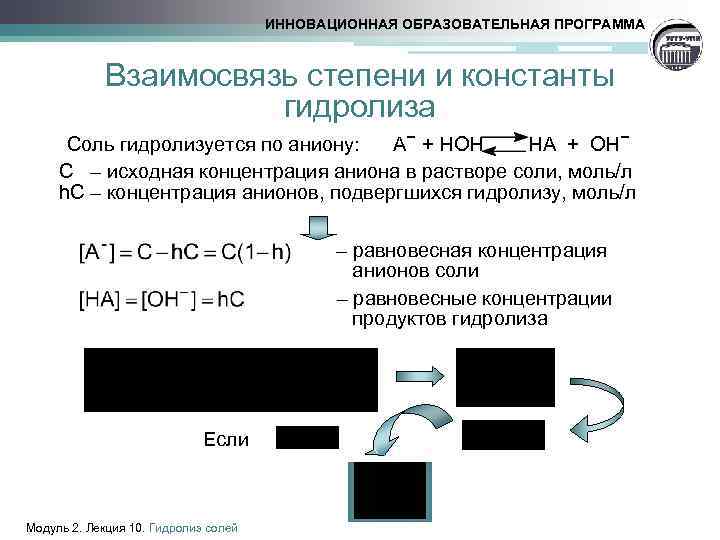
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Взаимосвязь степени и константы гидролиза Соль гидролизуется по аниону: А− + НОН НА + ОН− С – исходная концентрация аниона в растворе соли, моль/л h. С – концентрация анионов, подвергшихся гидролизу, моль/л – равновесная концентрация анионов соли – равновесные концентрации продуктов гидролиза Если Модуль 2. Лекция 10. Гидролиз солей

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Зависимость степени гидролиза от различных факторов § Влияние природы соли слабее основание или кислота, образующие соль меньше значение К - константы диссоциации больше h § Влияние концентрации раствора увеличение концентрации (С ↑ ) h ↓ уменьшение концентрации (С ↑ ) h ↑ § Влияние температуры нагревание h ↑ Гидролиз – процесс эндотермический охлаждение h ↓ Модуль 2. Лекция 10. Гидролиз солей
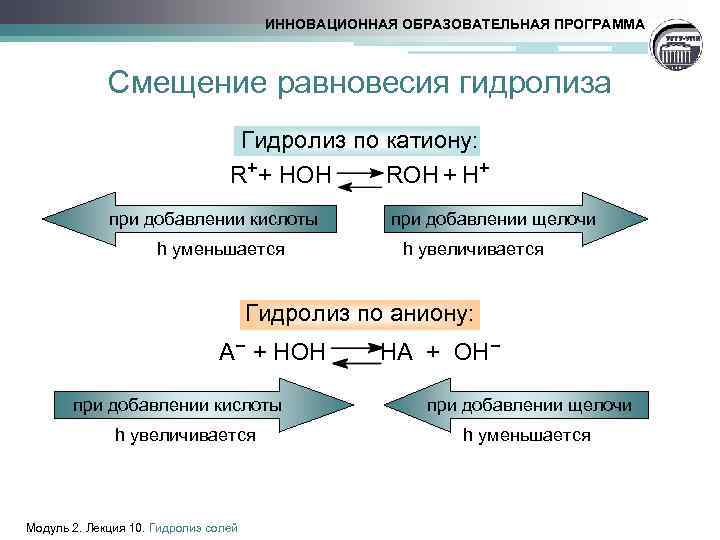
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Смещение равновесия гидролиза Гидролиз по катиону: R++ HOH ROH + H+ при добавлении кислоты h уменьшается при добавлении щелочи h увеличивается Гидролиз по аниону: А− + НОН НА + ОН− при добавлении кислоты h увеличивается Модуль 2. Лекция 10. Гидролиз солей при добавлении щелочи h уменьшается

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА § Расчет степени гидролиза CH 3 COONa в 0, 1 М растворе и p. H раствора Ионное уравнение гидролиза СH 3 COO + HOH СH 3 COOH + OH § Степень гидролиза § Концентрация ионов Н+ и р. Н Модуль 2. Лекция 10. Гидролиз солей

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Гидролиз соли Na. NO 2 соль образована сильным основанием и слабой одноосновной кислотой, гидролиз идет по аниону Na. NO 2 = Na+ + NO 2 + HOH HNO 2 + OH Na. NO 2 + H 2 O HNO 2 + Na. OH Среда щелочная, р. Н>7 Константа гидролиза Кг <<1 равновесие смещено в направлении обратной реакции Модуль 2. Лекция 10. Гидролиз солей

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Гидролиз соли К 2 СО 3 K 2 CO 3 = 2 K+ + CO 32 Соль образована сильным основанием и слабой двухосновной кислотой. Гидролиз идет по аниону, возможны две ступени гидролиза Уравнения гидролиза по I ступени: CO 32 + HOH HCO 3 + OH K 2 CO 3 + H 2 O KHCO 3 + KOH Уравнения гидролиза по II ступени: HCO 3 + HOH H 2 CO 3 + OH KHCO 3 + HOH H 2 CO 3 + KOH Среда щелочная, р. Н>7 Модуль 2. Лекция 10. Гидролиз солей
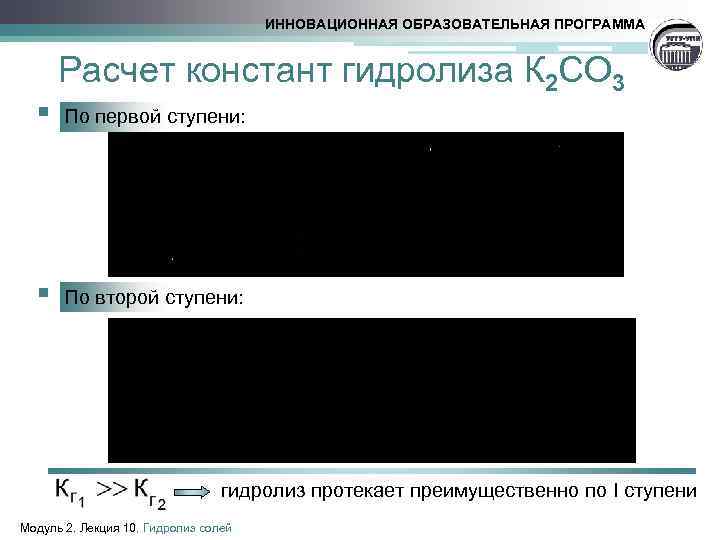
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА § § Расчет констант гидролиза К 2 СО 3 По первой ступени: По второй ступени: гидролиз протекает преимущественно по I ступени Модуль 2. Лекция 10. Гидролиз солей

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Гидролиз соли Cd(NO 3)2 = Cd 2+ + 2 NO 3 Соль образована слабым основанием и сильной кислотой. Гидролиз идет по катиону Уравнение гидролиза по I ступени: Cd 2+ + HOH Cd. OH+ + H+ Cd(NO 3)2 + H 2 O Cd. OHNO 3 + HNO 3 Уравнение гидролиза по II ступени: Cd. OH+ + HOH Cd(OH)2 + H+ Cd. OHNO 3 + H 2 O Cd(OH)2 + HNO 3 Среда кислая, p. H<7 Гидролиз идет преимущественно по I ступени Модуль 2. Лекция 10. Гидролиз солей
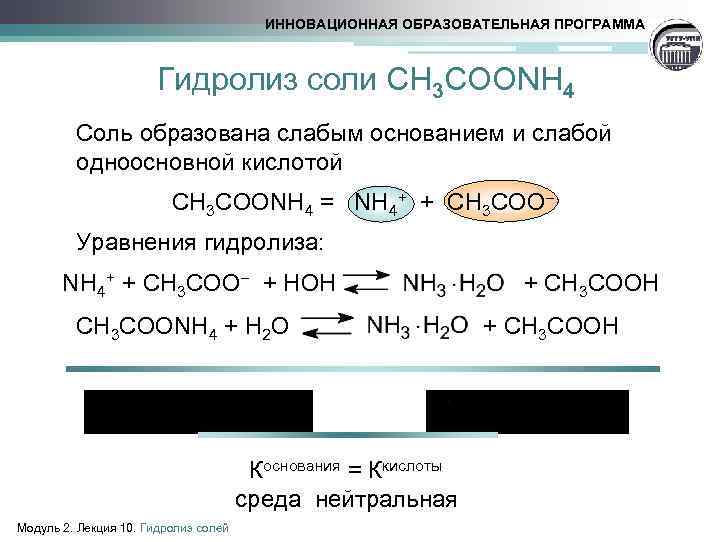
ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Гидролиз соли CH 3 COONH 4 Соль образована слабым основанием и слабой одноосновной кислотой CH 3 COONH 4 = NH 4+ + CH 3 COO Уравнения гидролиза: NH 4+ + CH 3 COO + HOH + CH 3 COOH CH 3 COONH 4 + H 2 O + CH 3 COOH Коснования = Ккислоты среда нейтральная Модуль 2. Лекция 10. Гидролиз солей

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА § Гидролиз солей слабых кислот и слабых оснований Соли слабого основания и слабой многоосновной кислоты в растворе полностью гидролизованы (NH 4)2 S + H 2 O NH 4 HS + HOH + H 2 S § Соли слабых одноосновных кислот и слабых оснований при гидролизе образуют осадки основных солей: Al(CH 3 COO)3 + HOH Al(OH)(CH 3 COO)2↓ + CH 3 COOH Al(OH)(CH 3 COO)2 + HOH Al(OH)2 CH 3 COO↓ + CH 3 COOH § Гидролиз некоторых солей, образованных летучими или малорастворимыми слабыми кислотами и слабыми основаниями протекает необратимо: Al 2 S 3 + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑ Такие соли в водных растворах не существуют Модуль 2. Лекция 10. Гидролиз солей

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Необратимый совместный гидролиз § - с участием катионов Al 3+, Fe 3+, Cr 3+, NH 4+ и анионов проходит с образованием слабого основания и кислоты 2 Al. Cl 3 + 3 Na 2 S + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑+ 6 Na. Cl 2 Al 3+ + 3 S 2 + 6 H 2 O = 2 Al(OH)3 + 3 H 2 S 2 NH 4 Cl + Na 2 Si. O 3 + (H 2 O) = 2 NH 3↑ + H 2 Si. O 3↓ + 2 Na. Cl 2 NH 4+ + Si. O 32 + (H 2 O) = 2 NH 3 + H 2 Si. O 3 § - солей слабых оснований типа M(OH)2 и солей угольной кислоты проходит с образованием основных солей и угольной кислоты 2 Cu. SO 4 + 2 Na 2 CO 3 + H 2 O = (Cu. OH)2 CO 3↓ + CO 2↑ + 2 Na 2 SO 4 2 Cu 2+ + 2 CO 32 + H 2 O = (Cu. OH)2 CO 3 + CO 2 Модуль 2. Лекция 10. Гидролиз солей

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА § § § Заключение Гидролиз соли ‑ процесс обменного взаимодействия ионов соли с молекулами воды Гидролизу подвергаются соли, образованные – слабыми кислотами и сильными основаниями – слабыми основаниями и сильными кислотами – слабыми кислотами и слабыми основаниями Количественные характеристики гидролиза солей ‑ константа гидролиза и степень гидролиза Чем слабее основание или кислота, образующие соль, тем больше степень гидролиза соли Степень гидролиза увеличивается при повышении температуры и разбавлении раствора Гидролиз солей, образованных многоосновными слабыми кислотами (летучими или малорастворимыми) и слабыми основаниями, протекает необратимо Модуль 2. Лекция 10. Гидролиз солей

ИННОВАЦИОННАЯ ОБРАЗОВАТЕЛЬНАЯ ПРОГРАММА Рекомендуемая литература § § Никольский А. Б. , Суворов А. В. Химия. - СПб: Химиздат, 2001 § Карапетьянц М. Х. Общая и неорганическая химия. - М. : Химия, 2000 § Угай Я. А. Общая и неорганическая химия. - М. : Высш. шк. , 2007 § Неорганическая химия. В 3 т. Т. 1: Физико-химические основы неорганической химии. Под ред. Ю. Д. Третьякова. - М. : Академия, 2004 § Гаршин А. П. Неорганическая химия в схемах, рисунках, таблицах, формулах, химических реакциях. - СПб. : Лань, 2000 Степин Б. Д. , Цветков А. А. Неорганическая химия. - М. : Высш. шк. , 1994 Модуль 2. Лекция 10. Гидролиз солей
74.ppt