Инфракрасная Фурье-спектроскопия (лекционно-практическое занятие) План лекции


















Лекция по ИКС для студентов1.ppt
- Количество слайдов: 23
 Инфракрасная Фурье-спектроскопия (лекционно-практическое занятие)
Инфракрасная Фурье-спектроскопия (лекционно-практическое занятие)
 План лекции Введение Инфракрасная спектроскопия Молекулярные спектры веществ Инфракрасный спектр Типы ИК спектрометров Инфракрасная Фурье-спектроскопия Подготовка проб Интерпретация ИК спектров Области применения ИК спектроскопии 2
План лекции Введение Инфракрасная спектроскопия Молекулярные спектры веществ Инфракрасный спектр Типы ИК спектрометров Инфракрасная Фурье-спектроскопия Подготовка проб Интерпретация ИК спектров Области применения ИК спектроскопии 2
 Введение Спектроскопия — раздел физики и аналитической химии, посвящённый изучению спектров взаимодействия электромагнитного излучения с веществом. Физика ⇒ изучение всевозможных свойств взаимодействий электромагнитного излучения с веществом. Аналитическая химия ⇒ обнаружение и определение веществ при помощи измерения их характеристических спектров. Характер процессов, протекающих при взаимодействии излучения с веществом, различен в разных спектральных областях. В связи с чем, спектроскопические методы анализа классифицируют по длине волны (энергии) используемого излучения: оптическая, рентгеновская, инфракрасная, масс- спектроскопия и др. 3
Введение Спектроскопия — раздел физики и аналитической химии, посвящённый изучению спектров взаимодействия электромагнитного излучения с веществом. Физика ⇒ изучение всевозможных свойств взаимодействий электромагнитного излучения с веществом. Аналитическая химия ⇒ обнаружение и определение веществ при помощи измерения их характеристических спектров. Характер процессов, протекающих при взаимодействии излучения с веществом, различен в разных спектральных областях. В связи с чем, спектроскопические методы анализа классифицируют по длине волны (энергии) используемого излучения: оптическая, рентгеновская, инфракрасная, масс- спектроскопия и др. 3
 Инфракрасная спектроскопия (ИКС) Раздел оптической спектроскопии, включающий получение, исследование и применение спектров испускания, поглощения и отражения в инфракрасной (ИК) области спектра. ИКС занимается изучением молекулярных спектров веществ и основана на исследовании колебательных и вращательных переходов в молекулах. Инфракрасная спектроскопия является одним из основных методов анализа структурных особенностей органических соединений. Методами ИКС изучают внутри- и межмолекулярные взаимодействия, например, образование водородных связей. 4
Инфракрасная спектроскопия (ИКС) Раздел оптической спектроскопии, включающий получение, исследование и применение спектров испускания, поглощения и отражения в инфракрасной (ИК) области спектра. ИКС занимается изучением молекулярных спектров веществ и основана на исследовании колебательных и вращательных переходов в молекулах. Инфракрасная спектроскопия является одним из основных методов анализа структурных особенностей органических соединений. Методами ИКС изучают внутри- и межмолекулярные взаимодействия, например, образование водородных связей. 4
 Спектр Молекула, как и атом, имеет большое число различных энергетических состояний, в которых она может находиться в зависимости от величины поглощенной ею энергии. Переход молекулы из одного энергетического состояния в другое связан с поглощением или излучением квантов света, с энергией Е = hcν , где Е — разность энергии квантовых уровней; h - постоянная Планка; с - скорость света; ν — волновое число. Совокупность всевозможных энергетических переходов в молекуле, сопровождаемых поглощением (или выделением) различных квантов, образует спектр. Электронные переходы обычно сопровождаются изменением колебательного и вращательного состояний. Спектр – последовательность квантов энергии электромагнитных колебаний, поглощенных, выделившихся или рассеянных при переходах атомов или молекул из одних энергетических состояний в другие. Рис. 1. Схема энергетических переходов в молекуле: W’W” - электронные состояния; V’V” - колебательные состояния; - J’J” вращательные состояния. 5
Спектр Молекула, как и атом, имеет большое число различных энергетических состояний, в которых она может находиться в зависимости от величины поглощенной ею энергии. Переход молекулы из одного энергетического состояния в другое связан с поглощением или излучением квантов света, с энергией Е = hcν , где Е — разность энергии квантовых уровней; h - постоянная Планка; с - скорость света; ν — волновое число. Совокупность всевозможных энергетических переходов в молекуле, сопровождаемых поглощением (или выделением) различных квантов, образует спектр. Электронные переходы обычно сопровождаются изменением колебательного и вращательного состояний. Спектр – последовательность квантов энергии электромагнитных колебаний, поглощенных, выделившихся или рассеянных при переходах атомов или молекул из одних энергетических состояний в другие. Рис. 1. Схема энергетических переходов в молекуле: W’W” - электронные состояния; V’V” - колебательные состояния; - J’J” вращательные состояния. 5
 Вращательные спектры Обусловлены вращением молекулы, как единого целого. Вращательный спектр представляет собой совокупность спектральных линий, возникающих при изменении вращательного состояния молекул. Линии вращательного спектра возникают в результате переходов молекулы между двумя возможными вращательными состояниями. Частота соответствующая вращательному переходу: νвр. =(Евр. кон. - Евр. нач. )/h=h/4π2 I. Момент инерции этой молекулы: I=m. Аr. А 2+m. Вr. В 2=m. Аm. В/(m. А+m. В)·r. АВ 2, где m. А, m. В – массы обоих атомов, а r. АВ – расстояние между ними. Рис. 3. Вращательный спектр: B – Рис. 2. Вращательные движения двухатомной вращательная константа, по оси ординат молекулы AB: S – центр тяжести молекулы. отложена интенсивность, по оси абсцисс волновое число. 6
Вращательные спектры Обусловлены вращением молекулы, как единого целого. Вращательный спектр представляет собой совокупность спектральных линий, возникающих при изменении вращательного состояния молекул. Линии вращательного спектра возникают в результате переходов молекулы между двумя возможными вращательными состояниями. Частота соответствующая вращательному переходу: νвр. =(Евр. кон. - Евр. нач. )/h=h/4π2 I. Момент инерции этой молекулы: I=m. Аr. А 2+m. Вr. В 2=m. Аm. В/(m. А+m. В)·r. АВ 2, где m. А, m. В – массы обоих атомов, а r. АВ – расстояние между ними. Рис. 3. Вращательный спектр: B – Рис. 2. Вращательные движения двухатомной вращательная константа, по оси ординат молекулы AB: S – центр тяжести молекулы. отложена интенсивность, по оси абсцисс волновое число. 6
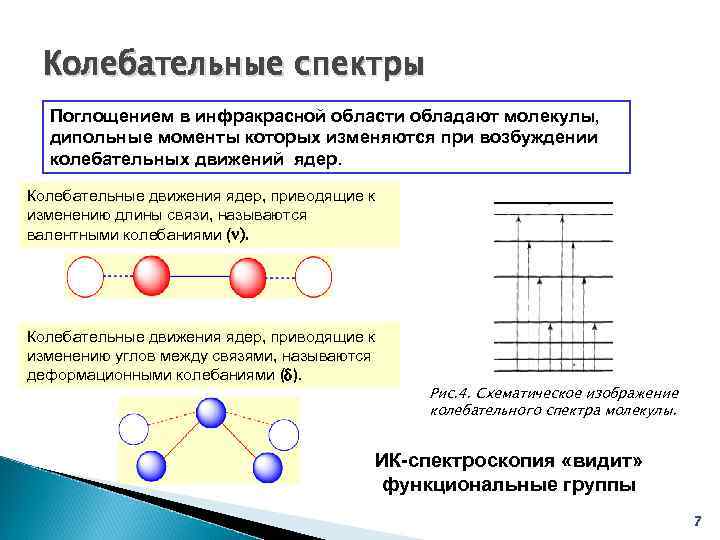
 Колебательные спектры Поглощением в инфракрасной области обладают молекулы, дипольные моменты которых изменяются при возбуждении колебательных движений ядер. Колебательные движения ядер, приводящие к изменению длины связи, называются валентными колебаниями ( ). Колебательные движения ядер, приводящие к изменению углов между связями, называются деформационными колебаниями (d). Рис. 4. Схематическое изображение колебательного спектра молекулы. ИК-спектроскопия «видит» функциональные группы 7
Колебательные спектры Поглощением в инфракрасной области обладают молекулы, дипольные моменты которых изменяются при возбуждении колебательных движений ядер. Колебательные движения ядер, приводящие к изменению длины связи, называются валентными колебаниями ( ). Колебательные движения ядер, приводящие к изменению углов между связями, называются деформационными колебаниями (d). Рис. 4. Схематическое изображение колебательного спектра молекулы. ИК-спектроскопия «видит» функциональные группы 7
 Инфракрасное излучение Электромагнитное излучение, занимающее спектральную область между красным концом видимого излучения ( с длиной волны λ ≈0, 74 мкм) и коротковолновым радиоизлучением (λ≈1 -2 мм) Инфракрасную область спектра условно разделяют на ближнюю (0, 74 – 2, 5 мкм), среднюю (2, 5 – 50 мкм) и далекую (50 – 2000 мкм). 8
Инфракрасное излучение Электромагнитное излучение, занимающее спектральную область между красным концом видимого излучения ( с длиной волны λ ≈0, 74 мкм) и коротковолновым радиоизлучением (λ≈1 -2 мм) Инфракрасную область спектра условно разделяют на ближнюю (0, 74 – 2, 5 мкм), среднюю (2, 5 – 50 мкм) и далекую (50 – 2000 мкм). 8
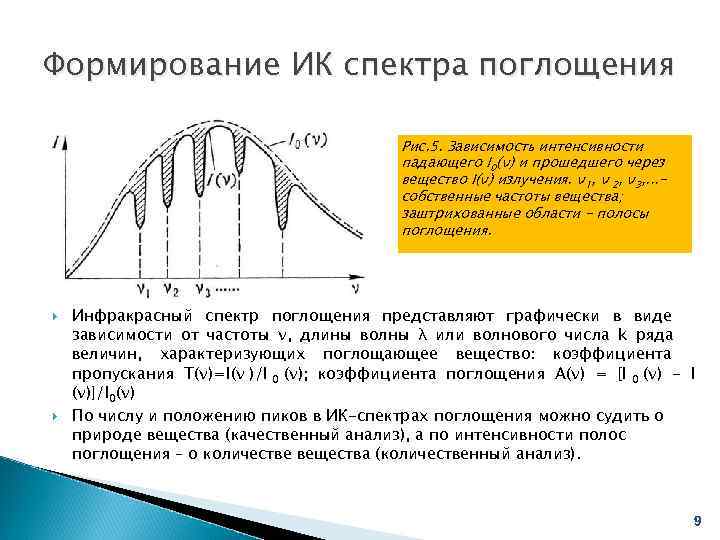
 Формирование ИК спектра поглощения Рис. 5. Зависимость интенсивности падающего I 0(ʋ) и прошедшего через вещество I(ʋ) излучения. ʋ1, ʋ 2, ʋ3, . . . - собственные частоты вещества; заштрихованные области - полосы поглощения. Инфракрасный спектр поглощения представляют графически в виде зависимости от частоты ν, длины волны λ или волнового числа k ряда величин, характеризующих поглощающее вещество: коэффициента пропускания T(ν)=I(ν )/I 0 (ν); коэффициента поглощения А(ν) = [I 0 (ν) - I (ν)]/I 0(ν) По числу и положению пиков в ИК-спектрах поглощения можно судить о природе вещества (качественный анализ), а по интенсивности полос поглощения – о количестве вещества (количественный анализ). 9
Формирование ИК спектра поглощения Рис. 5. Зависимость интенсивности падающего I 0(ʋ) и прошедшего через вещество I(ʋ) излучения. ʋ1, ʋ 2, ʋ3, . . . - собственные частоты вещества; заштрихованные области - полосы поглощения. Инфракрасный спектр поглощения представляют графически в виде зависимости от частоты ν, длины волны λ или волнового числа k ряда величин, характеризующих поглощающее вещество: коэффициента пропускания T(ν)=I(ν )/I 0 (ν); коэффициента поглощения А(ν) = [I 0 (ν) - I (ν)]/I 0(ν) По числу и положению пиков в ИК-спектрах поглощения можно судить о природе вещества (качественный анализ), а по интенсивности полос поглощения – о количестве вещества (количественный анализ). 9
 Волновое число (пространственная частота) – это отношение 2 π радиан к длине волны: Единица измерения - рад·м− 1, физическая размерность м− 1, см− 1. В спектроскопии волновым числом часто называют просто величину, обратную длине волны (1/λ) , измеряемую обычно в обратных сантиметрах (см − 1 ). Такое определение отличается от обычного отсутствием множителя 2π. Рис. 6. Длина волны соответствует расстоянию АВ; волновое число – число волн, приходящееся на 1 см, CD ; частота – число волн, проходящих через фиксированную точку С в единицу времени. 10
Волновое число (пространственная частота) – это отношение 2 π радиан к длине волны: Единица измерения - рад·м− 1, физическая размерность м− 1, см− 1. В спектроскопии волновым числом часто называют просто величину, обратную длине волны (1/λ) , измеряемую обычно в обратных сантиметрах (см − 1 ). Такое определение отличается от обычного отсутствием множителя 2π. Рис. 6. Длина волны соответствует расстоянию АВ; волновое число – число волн, приходящееся на 1 см, CD ; частота – число волн, проходящих через фиксированную точку С в единицу времени. 10
 Регистрация ИК спектров Каждое вещество имеет определённый набор собственных колебательных и вращательных частот, поэтому ИК-спектр поглощения являет ся индивидуальной характеристикой вещества. Измерение спектра ИК-поглощения сводится к измерению интенсивности ИК-излучения, прошедшего через вещество, в зависимости от частоты излучения ν или длины волны λ. Регистрация спектров поглощения осуществляется с помощью специальных устройств – инфракрасных спектрометров (инфракрасных Фурье-спектрометров). Рис. 7. Общий вид и оптическая схема инфракрасного Фурье -спектрометра. 11
Регистрация ИК спектров Каждое вещество имеет определённый набор собственных колебательных и вращательных частот, поэтому ИК-спектр поглощения являет ся индивидуальной характеристикой вещества. Измерение спектра ИК-поглощения сводится к измерению интенсивности ИК-излучения, прошедшего через вещество, в зависимости от частоты излучения ν или длины волны λ. Регистрация спектров поглощения осуществляется с помощью специальных устройств – инфракрасных спектрометров (инфракрасных Фурье-спектрометров). Рис. 7. Общий вид и оптическая схема инфракрасного Фурье -спектрометра. 11
 12
12
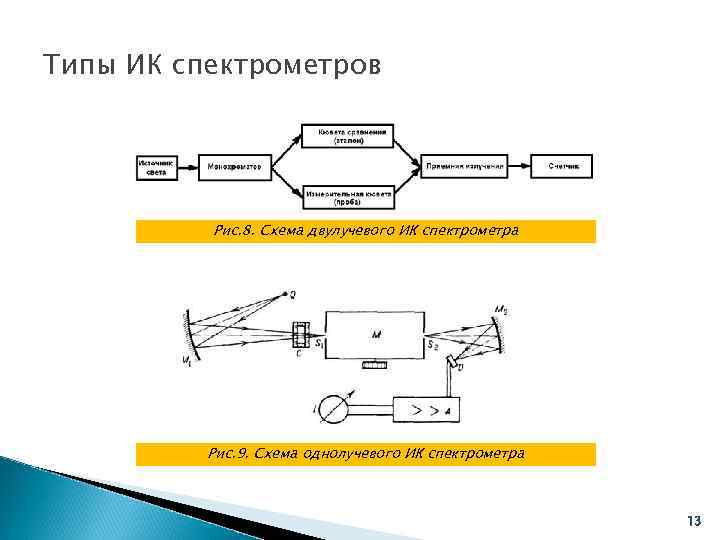
 Типы ИК спектрометров Рис. 8. Схема двулучевого ИК спектрометра Рис. 9. Схема однолучевого ИК спектрометра 13
Типы ИК спектрометров Рис. 8. Схема двулучевого ИК спектрометра Рис. 9. Схема однолучевого ИК спектрометра 13
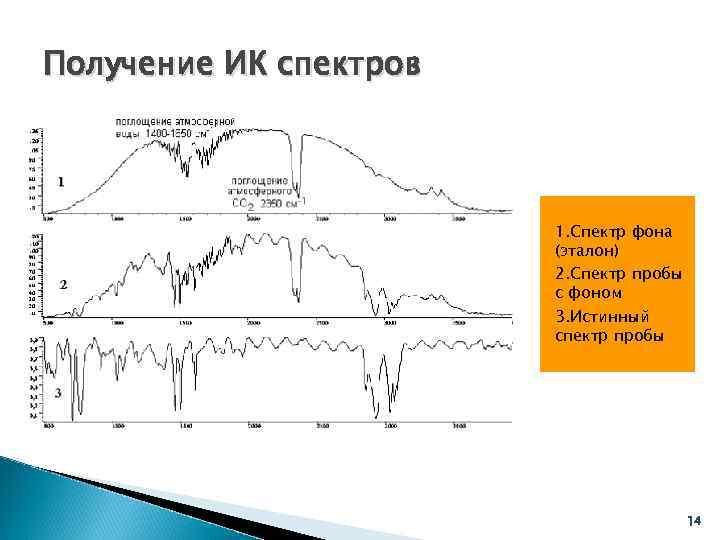
 Получение ИК спектров 1. Спектр фона (эталон) 2. Спектр пробы с фоном 3. Истинный спектр пробы 14
Получение ИК спектров 1. Спектр фона (эталон) 2. Спектр пробы с фоном 3. Истинный спектр пробы 14
 Преимущества ИК-Фурье спектрометров 1. Высокая точность определения волнового числа. 2. Преимущество пропускания - площадь круглой щели, значительно больше, чем у узкой щели дифракционных спектрометров, что позволяет получить на детекторе световые потоки большей мощности. 3. В процессе сканирования получается информация одновременно обо всем исследуемом спектральном диапазоне, а не как в обычном спектрометре в разные моменты времени получается информация только об узких спектральных полосах исследуемого диапазона, в следствии чего уменьшается время регистрации спектра. 4. Отсутствие ограничений в спектральном разрешении за счет размеров оптических элементов, в настоящее время производятся ИК Фурье спектрометры с разрешением до 0, 002 см-1. 15
Преимущества ИК-Фурье спектрометров 1. Высокая точность определения волнового числа. 2. Преимущество пропускания - площадь круглой щели, значительно больше, чем у узкой щели дифракционных спектрометров, что позволяет получить на детекторе световые потоки большей мощности. 3. В процессе сканирования получается информация одновременно обо всем исследуемом спектральном диапазоне, а не как в обычном спектрометре в разные моменты времени получается информация только об узких спектральных полосах исследуемого диапазона, в следствии чего уменьшается время регистрации спектра. 4. Отсутствие ограничений в спектральном разрешении за счет размеров оптических элементов, в настоящее время производятся ИК Фурье спектрометры с разрешением до 0, 002 см-1. 15
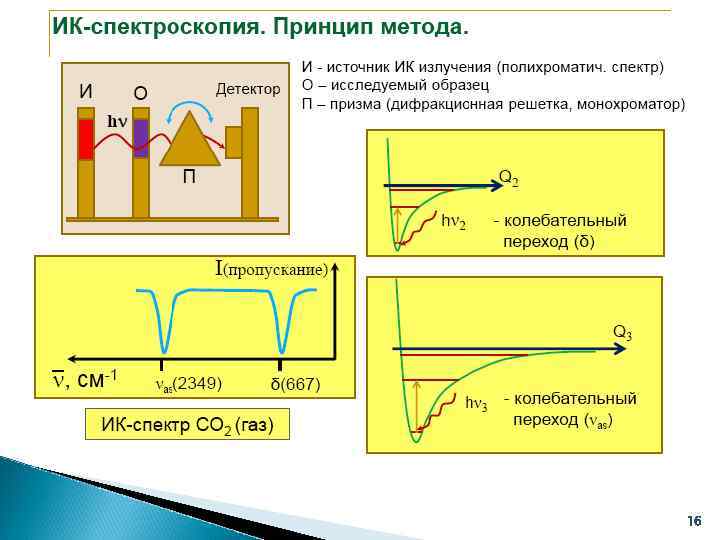
 16
16
 Подготовка образцов для снятия ИК-спектров Инфракрасные спектры можно измерить для газообразных, жидких и твердых веществ Подготовка образцов: 1. Для твердых веществ 2. Для жидких веществ а) Пасты: 10 -20 мг тв. вещества с 1 -2 в пленке исследуемого вещества каплями иммерсионной жидкости. 3. Растворы б) Диски с KBr (спектроскопически 0, 5 -1, 5% р-р тв. или жидкого вещества чистый): смесь 1 -3 мг тв. вещества и 150 -200 мг KBr И вазелиновое масло, и растворители не полностью прозрачны по всей области спектра вазелиновое масло (нуйлон) поглощает: 3000 – 2800 см-1, 1460 и 1380 см-1 СCl 4 поглощает: 1600, 800 см-1 Оформление записи ИК-спектра: ИК-спектр ( , вазелин, см-1): 1680 (С=О), 650 (С-Вr) 17
Подготовка образцов для снятия ИК-спектров Инфракрасные спектры можно измерить для газообразных, жидких и твердых веществ Подготовка образцов: 1. Для твердых веществ 2. Для жидких веществ а) Пасты: 10 -20 мг тв. вещества с 1 -2 в пленке исследуемого вещества каплями иммерсионной жидкости. 3. Растворы б) Диски с KBr (спектроскопически 0, 5 -1, 5% р-р тв. или жидкого вещества чистый): смесь 1 -3 мг тв. вещества и 150 -200 мг KBr И вазелиновое масло, и растворители не полностью прозрачны по всей области спектра вазелиновое масло (нуйлон) поглощает: 3000 – 2800 см-1, 1460 и 1380 см-1 СCl 4 поглощает: 1600, 800 см-1 Оформление записи ИК-спектра: ИК-спектр ( , вазелин, см-1): 1680 (С=О), 650 (С-Вr) 17
 18
18
 19
19
 1 5 2 20
1 5 2 20
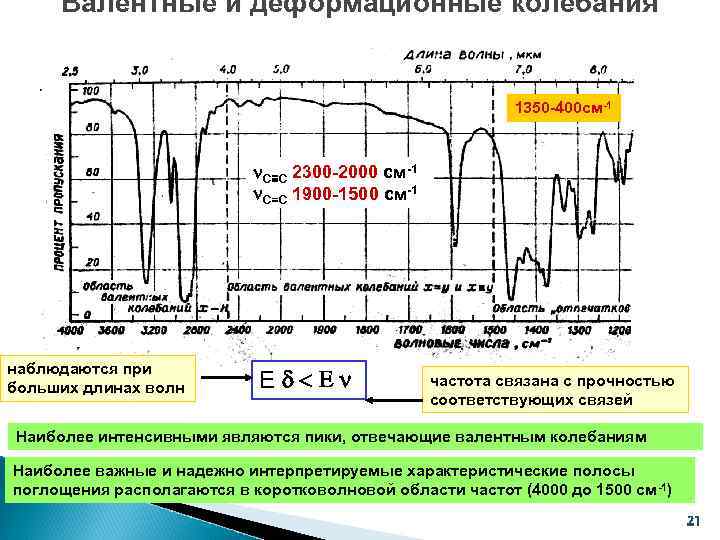
 Валентные и деформационные колебания 1350 -400 см-1 С≡С 2300 -2000 см-1 С=С 1900 -1500 см-1 наблюдаются при больших длинах волн Ed
Валентные и деформационные колебания 1350 -400 см-1 С≡С 2300 -2000 см-1 С=С 1900 -1500 см-1 наблюдаются при больших длинах волн Ed
 Области применения ИК- спектроскопии 22
Области применения ИК- спектроскопии 22
 Спасибо за внимание! 23
Спасибо за внимание! 23

