
 • Информация к размышлению • Русская примета гласит: «Двадцать лет ума нет и не будет, тридцать лет жены нет и не будет, сорок лет денег нет и не будет» • • Ответьте такие вопросы: Кто я? Что буду делать в жизни? Кого буду любить? Как буду строить отношения с людьми? Какие у меня политические взгляды? Что входит в мою систему убеждений? В чем мой долг? • Какими поступками я утверждаю свои ценности?
• Информация к размышлению • Русская примета гласит: «Двадцать лет ума нет и не будет, тридцать лет жены нет и не будет, сорок лет денег нет и не будет» • • Ответьте такие вопросы: Кто я? Что буду делать в жизни? Кого буду любить? Как буду строить отношения с людьми? Какие у меня политические взгляды? Что входит в мою систему убеждений? В чем мой долг? • Какими поступками я утверждаю свои ценности?
 «Не знать, значит жить в опасности» (Януш Вишневский «Одиночество в сети» ) ХИМИЯ
«Не знать, значит жить в опасности» (Януш Вишневский «Одиночество в сети» ) ХИМИЯ
 ТЕМА 1. Атомный уровень организации вещества • 1. 1. Определение атома: атом – это микросистема, состоящая из ядра и электронов, движущихся в поле ядра • 1. 2. Строение атомов: H Орбитали: 1 s He 1 2 1 s Li 2 1 1 s 2 s Be B 2 2 1 s 2 s 2 2 1 1 s 2 s 2 p
ТЕМА 1. Атомный уровень организации вещества • 1. 1. Определение атома: атом – это микросистема, состоящая из ядра и электронов, движущихся в поле ядра • 1. 2. Строение атомов: H Орбитали: 1 s He 1 2 1 s Li 2 1 1 s 2 s Be B 2 2 1 s 2 s 2 2 1 1 s 2 s 2 p
 • 1. 3. Взаимодействия в атомах: • Притяжение (ядро-электрон) и отталкивание (электрон) уравновешены и не дают атому распасться на составные части.
• 1. 3. Взаимодействия в атомах: • Притяжение (ядро-электрон) и отталкивание (электрон) уравновешены и не дают атому распасться на составные части.
 • 1. 4. Свойства атомов: • 1) Обмениваться энергией с окружающей средой: Н Н* 1 1 s 1 2 p Пример: свечение возбужденных атомов ртути в ртутных люминесцентных лампах: Hg + энергия потока электронов Hg* (возбужденный атом) Hg* Hg + электромагнитное излучение (видимый свет)
• 1. 4. Свойства атомов: • 1) Обмениваться энергией с окружающей средой: Н Н* 1 1 s 1 2 p Пример: свечение возбужденных атомов ртути в ртутных люминесцентных лампах: Hg + энергия потока электронов Hg* (возбужденный атом) Hg* Hg + электромагнитное излучение (видимый свет)
 2) Отдавать и присоединять электроны Li Li атом лития e + электрон + ион лития F атом фтора + е электрон F ион фтора
2) Отдавать и присоединять электроны Li Li атом лития e + электрон + ион лития F атом фтора + е электрон F ион фтора
 3) Изменять геометрическую конфигурацию Н Li Н* + Li
3) Изменять геометрическую конфигурацию Н Li Н* + Li
 3) Изменять геометрическую конфигурацию Н Li Н* + Li
3) Изменять геометрическую конфигурацию Н Li Н* + Li
 • 4) образовывать химические связи: Н Li Н Н 2 F Li. F
• 4) образовывать химические связи: Н Li Н Н 2 F Li. F
 • • 1. 5. Количество вещества Моль – это количество вещества (безразмерная величина). Один моль насчитывает 6. 02· 1023 атомов, молекул, ионов или электронов. n моль N частиц 1 6. 02· 1023 1 1 6. 02· 10 23 Молярная масса атомов химического элемента равна количеству граммов вещества, которое содержится в 1 моль атомов данного элемента. 24 Например, масса атома водорода равна 1. 674· 10 г. В 1 моль 23 водорода содержится 6. 02· 10 атомов, следовательно молярная 24 23 масса атома водорода М = 1. 674· 10 · 6. 02· 10 = 1. 008 г/моль. Молярная масса молекулы Н 2: М = 2. 016 г/моль.
• • 1. 5. Количество вещества Моль – это количество вещества (безразмерная величина). Один моль насчитывает 6. 02· 1023 атомов, молекул, ионов или электронов. n моль N частиц 1 6. 02· 1023 1 1 6. 02· 10 23 Молярная масса атомов химического элемента равна количеству граммов вещества, которое содержится в 1 моль атомов данного элемента. 24 Например, масса атома водорода равна 1. 674· 10 г. В 1 моль 23 водорода содержится 6. 02· 10 атомов, следовательно молярная 24 23 масса атома водорода М = 1. 674· 10 · 6. 02· 10 = 1. 008 г/моль. Молярная масса молекулы Н 2: М = 2. 016 г/моль.
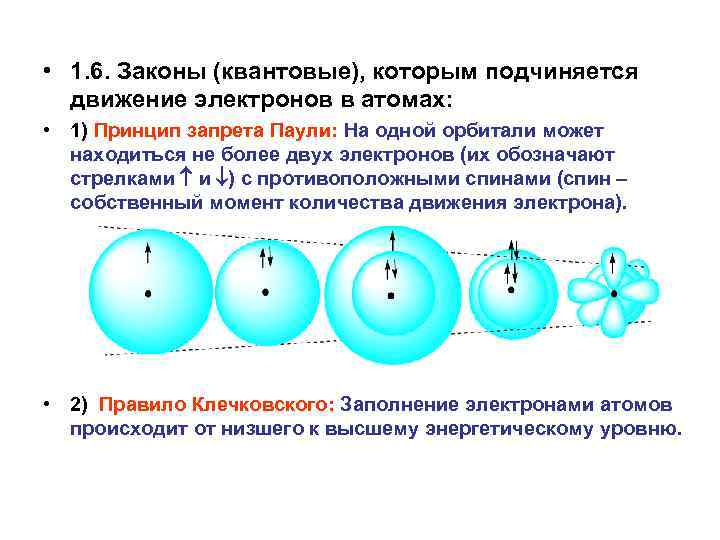 • 1. 6. Законы (квантовые), которым подчиняется движение электронов в атомах: • 1) Принцип запрета Паули: На одной орбитали может находиться не более двух электронов (их обозначают стрелками и ) с противоположными спинами (спин – собственный момент количества движения электрона). • 2) Правило Клечковского: Заполнение электронами атомов происходит от низшего к высшему энергетическому уровню.
• 1. 6. Законы (квантовые), которым подчиняется движение электронов в атомах: • 1) Принцип запрета Паули: На одной орбитали может находиться не более двух электронов (их обозначают стрелками и ) с противоположными спинами (спин – собственный момент количества движения электрона). • 2) Правило Клечковского: Заполнение электронами атомов происходит от низшего к высшему энергетическому уровню.
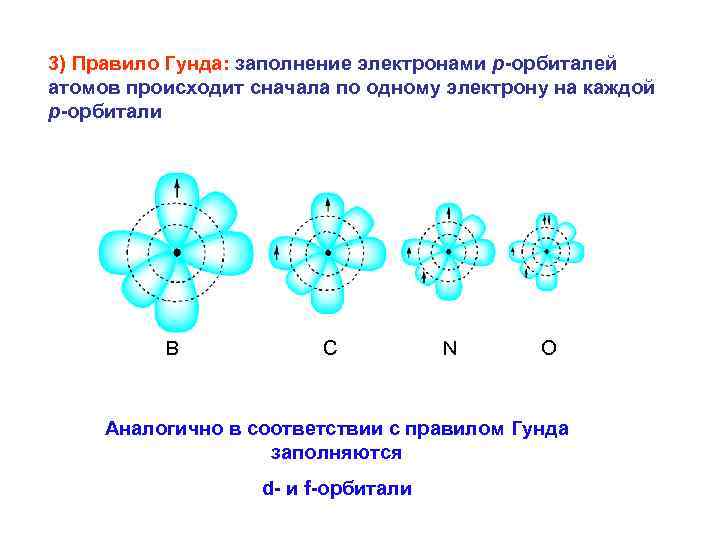 3) Правило Гунда: заполнение электронами р-орбиталей атомов происходит сначала по одному электрону на каждой р-орбитали B C N O Аналогично в соответствии с правилом Гунда заполняются d- и f-орбитали
3) Правило Гунда: заполнение электронами р-орбиталей атомов происходит сначала по одному электрону на каждой р-орбитали B C N O Аналогично в соответствии с правилом Гунда заполняются d- и f-орбитали
 • Как запоминать прочитанное • 1. Читаю лекцию или учебник • 2. Запоминаю термины и понятия по двум-трем ключевым словам. • 3. Воспроизвожу прочитанное письменно. • 4. Если есть затруднения в написании терминов, понятий, рисунков, схем, графиков, химических формул и уравнений – буду повторять операции 1, 2 и 3 столько раз, чтобы воспроизвести прочитанное.
• Как запоминать прочитанное • 1. Читаю лекцию или учебник • 2. Запоминаю термины и понятия по двум-трем ключевым словам. • 3. Воспроизвожу прочитанное письменно. • 4. Если есть затруднения в написании терминов, понятий, рисунков, схем, графиков, химических формул и уравнений – буду повторять операции 1, 2 и 3 столько раз, чтобы воспроизвести прочитанное.


