Инфекции иммунной системы.pptx
- Количество слайдов: 51
 Инфекции иммунной системы Несмиянов П. П. , кафедра иммунологии и аллергологии Волг. ГМУ
Инфекции иммунной системы Несмиянов П. П. , кафедра иммунологии и аллергологии Волг. ГМУ

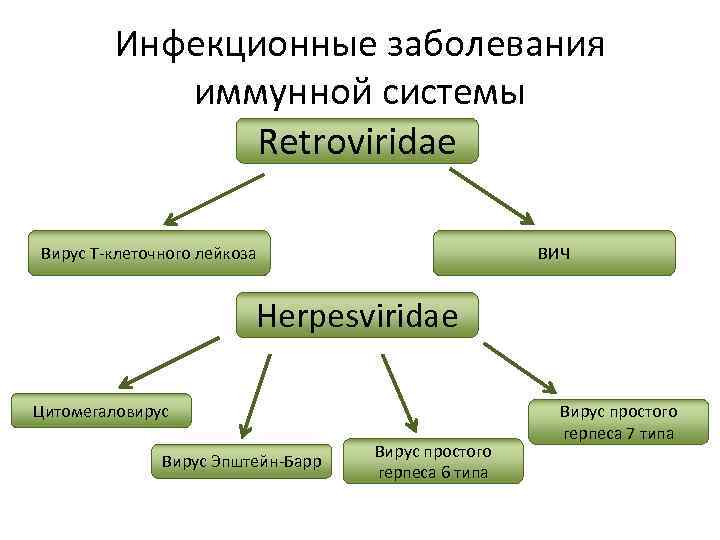 Инфекционные заболевания иммунной системы Retroviridae Вирус Т-клеточного лейкоза ВИЧ Herpesviridae Цитомегаловирус Вирус Эпштейн-Барр Вирус простого герпеса 6 типа Вирус простого герпеса 7 типа
Инфекционные заболевания иммунной системы Retroviridae Вирус Т-клеточного лейкоза ВИЧ Herpesviridae Цитомегаловирус Вирус Эпштейн-Барр Вирус простого герпеса 6 типа Вирус простого герпеса 7 типа
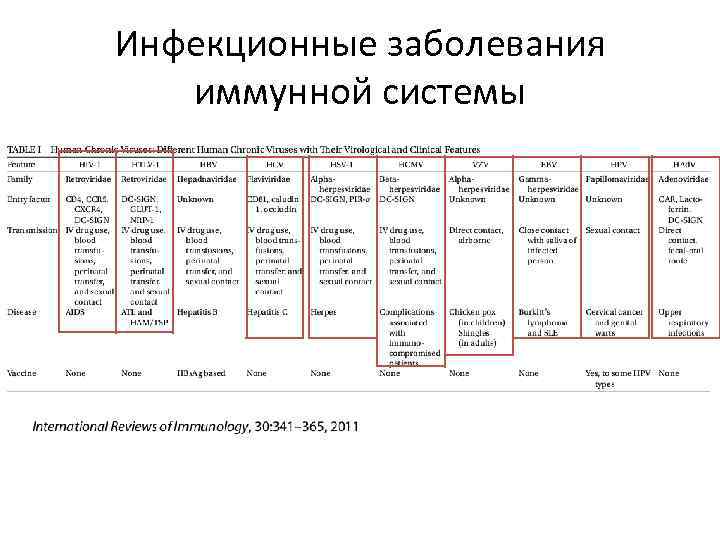 Инфекционные заболевания иммунной системы
Инфекционные заболевания иммунной системы
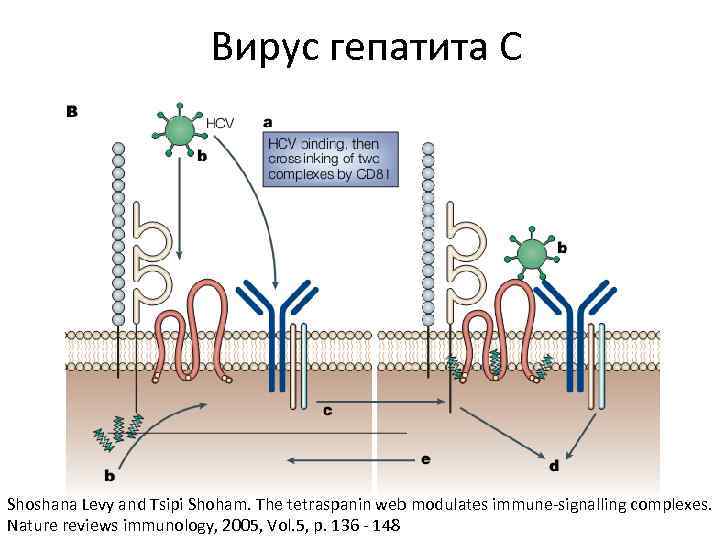 Вирус гепатита С Shoshana Levy and Tsipi Shoham. The tetraspanin web modulates immune-signalling complexes. Nature reviews immunology, 2005, Vol. 5, p. 136 - 148
Вирус гепатита С Shoshana Levy and Tsipi Shoham. The tetraspanin web modulates immune-signalling complexes. Nature reviews immunology, 2005, Vol. 5, p. 136 - 148
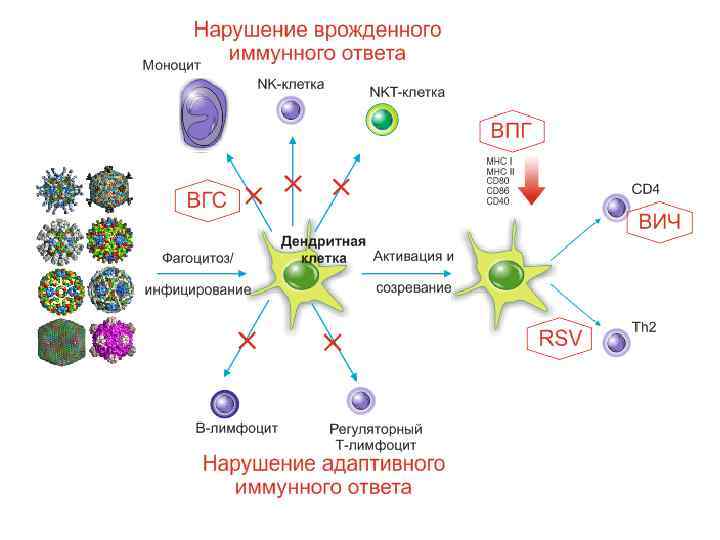
 Вирусы герпеса EAACI Newsletter, Issue 20, February 2010, P. 12 – 14, Am Fam Physician. 2003 Feb 1; 67(3): 519 -524
Вирусы герпеса EAACI Newsletter, Issue 20, February 2010, P. 12 – 14, Am Fam Physician. 2003 Feb 1; 67(3): 519 -524
 Цитомегаловирус: биология Семейство герпесвирусы, подсемейство бета-герпесвирусы Образует гигантские клетки Имеет необычайно большой геном Поражает все органы и ткани, имеет сродство к клеткам слюнных желез, почек Пути передачи: воздушно-капельный, половой, трансплацентарный, переливание органов и пересадка тканей Способен к реактивации после длительного латентного периода
Цитомегаловирус: биология Семейство герпесвирусы, подсемейство бета-герпесвирусы Образует гигантские клетки Имеет необычайно большой геном Поражает все органы и ткани, имеет сродство к клеткам слюнных желез, почек Пути передачи: воздушно-капельный, половой, трансплацентарный, переливание органов и пересадка тканей Способен к реактивации после длительного латентного периода
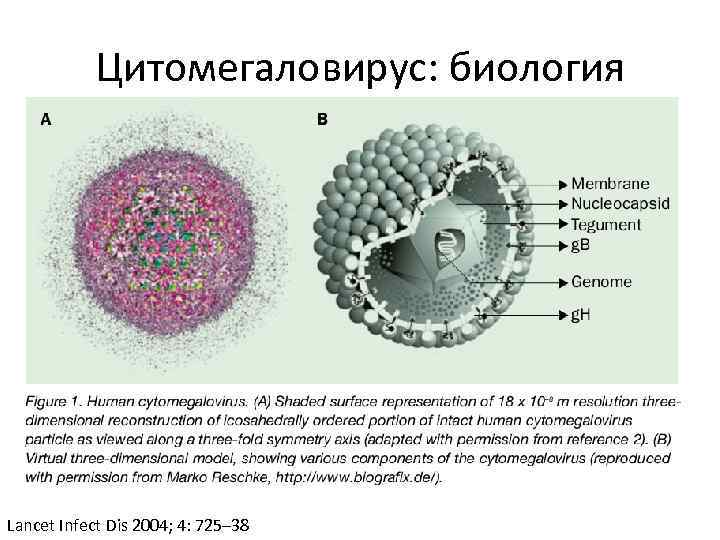 Цитомегаловирус: биология Семейство герпесвирусы, подсемейство бета-герпесвирусы Lancet Infect Dis 2004; 4: 725– 38
Цитомегаловирус: биология Семейство герпесвирусы, подсемейство бета-герпесвирусы Lancet Infect Dis 2004; 4: 725– 38
 Цитомегаловирус: эпидемиология К возрасту 30 лет инфицированы 60 -100% населения В течение беременности заражается около 2% новорожденных 10% из них умирает в течение первого года жизни у 2 -5% развивается глухота у 5 -10% развивается гепатоспленомегалия, микроцефалия, ретинит, тромбоцитопения, желтуха 10 -16% детей заражаются при родах и в первые 6 месяцев с молоком матери Значительная часть населения заражается в подростковом периоде ( «болезнь поцелуев» )
Цитомегаловирус: эпидемиология К возрасту 30 лет инфицированы 60 -100% населения В течение беременности заражается около 2% новорожденных 10% из них умирает в течение первого года жизни у 2 -5% развивается глухота у 5 -10% развивается гепатоспленомегалия, микроцефалия, ретинит, тромбоцитопения, желтуха 10 -16% детей заражаются при родах и в первые 6 месяцев с молоком матери Значительная часть населения заражается в подростковом периоде ( «болезнь поцелуев» )
 Цитомегаловирус: репликация
Цитомегаловирус: репликация
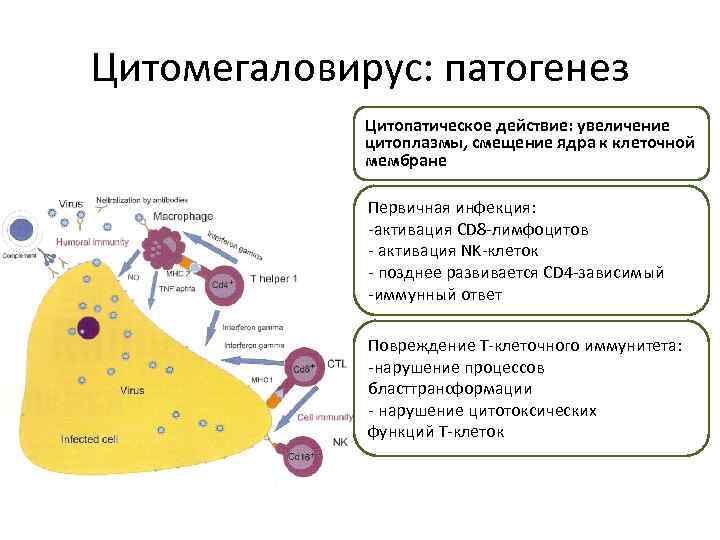 Цитомегаловирус: патогенез Цитопатическое действие: увеличение цитоплазмы, смещение ядра к клеточной мембране Первичная инфекция: -активация CD 8 -лимфоцитов - активация NK-клеток - позднее развивается CD 4 -зависимый -иммунный ответ Повреждение Т-клеточного иммунитета: -нарушение процессов бласттрансформации - нарушение цитотоксических функций Т-клеток
Цитомегаловирус: патогенез Цитопатическое действие: увеличение цитоплазмы, смещение ядра к клеточной мембране Первичная инфекция: -активация CD 8 -лимфоцитов - активация NK-клеток - позднее развивается CD 4 -зависимый -иммунный ответ Повреждение Т-клеточного иммунитета: -нарушение процессов бласттрансформации - нарушение цитотоксических функций Т-клеток
 Цитомегаловирус: иммунный ответ Иммунокомпетентные лица: –Т-клеточное звено восстанавливается в течение нескольких месяцев –может наблюдаться остаточная репликация вируса Иммунокомпроментированные лица (ВИЧинфицированные, реципиенты трансплантатов и лица после противоопухолевой химиотерапии) –Отсутствует элиминация вируса –Существует риск диссеминированной инфекции
Цитомегаловирус: иммунный ответ Иммунокомпетентные лица: –Т-клеточное звено восстанавливается в течение нескольких месяцев –может наблюдаться остаточная репликация вируса Иммунокомпроментированные лица (ВИЧинфицированные, реципиенты трансплантатов и лица после противоопухолевой химиотерапии) –Отсутствует элиминация вируса –Существует риск диссеминированной инфекции
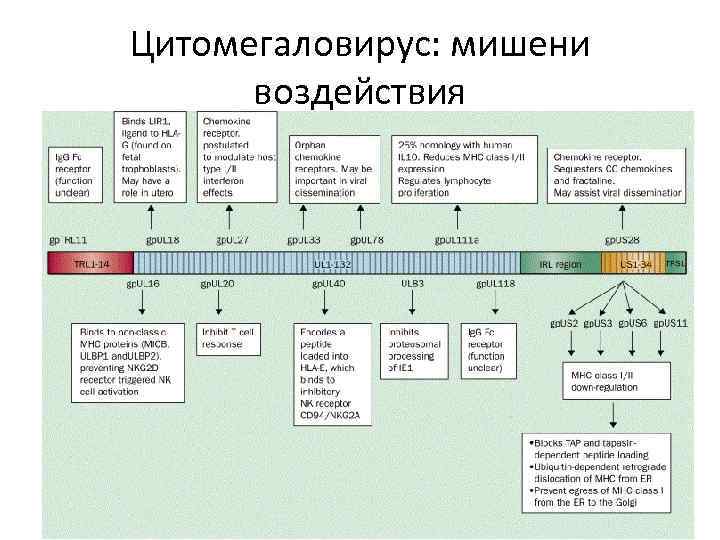 Цитомегаловирус: мишени воздействия
Цитомегаловирус: мишени воздействия
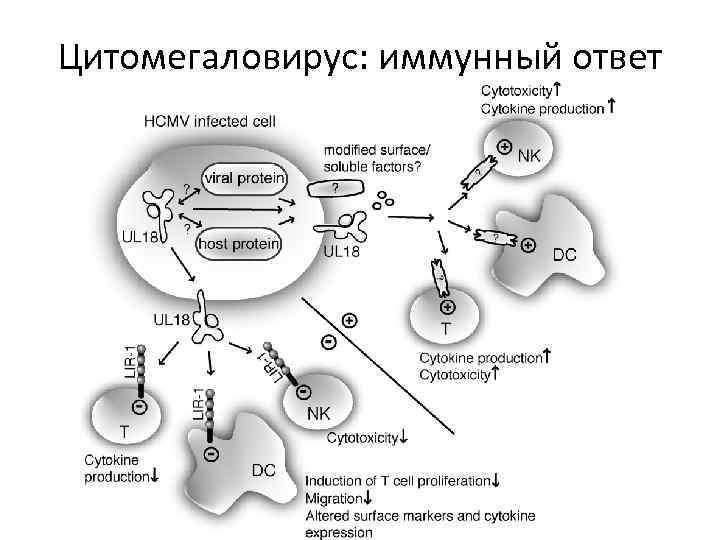 Цитомегаловирус: иммунный ответ
Цитомегаловирус: иммунный ответ
 Цитомегаловирус: мишени воздействия
Цитомегаловирус: мишени воздействия
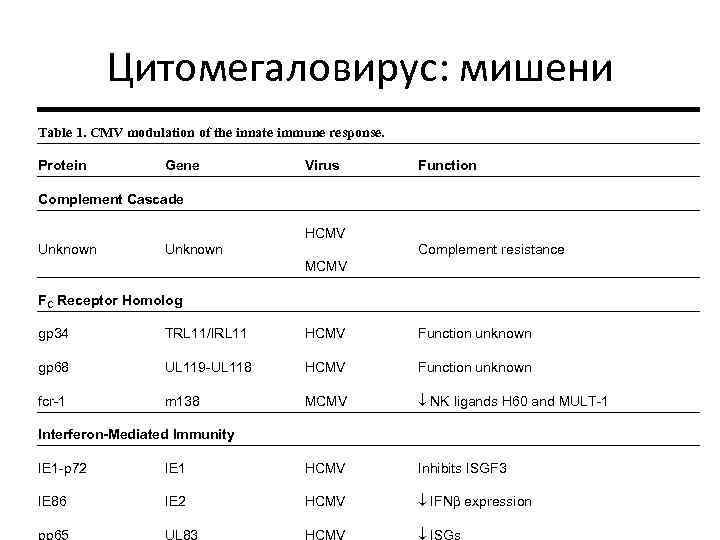 Цитомегаловирус: мишени Table 1. CMV modulation of the innate immune response. Protein Gene Virus Function Complement Cascade HCMV Unknown Complement resistance MCMV FC Receptor Homolog gp 34 TRL 11/IRL 11 HCMV Function unknown gp 68 UL 119 -UL 118 HCMV Function unknown fcr-1 m 138 MCMV NK ligands H 60 and MULT-1 Interferon-Mediated Immunity IE 1 -p 72 IE 1 HCMV Inhibits ISGF 3 IE 86 IE 2 HCMV IFN expression
Цитомегаловирус: мишени Table 1. CMV modulation of the innate immune response. Protein Gene Virus Function Complement Cascade HCMV Unknown Complement resistance MCMV FC Receptor Homolog gp 34 TRL 11/IRL 11 HCMV Function unknown gp 68 UL 119 -UL 118 HCMV Function unknown fcr-1 m 138 MCMV NK ligands H 60 and MULT-1 Interferon-Mediated Immunity IE 1 -p 72 IE 1 HCMV Inhibits ISGF 3 IE 86 IE 2 HCMV IFN expression
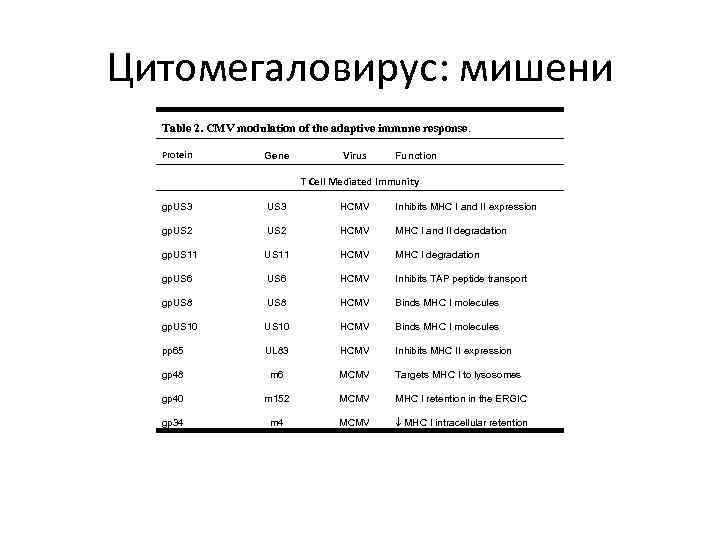 Цитомегаловирус: мишени Table 2. CMV modulation of the adaptive immune response. Protein Gene Virus Function T Cell Mediated Immunity gp. US 3 HCMV Inhibits MHC I and II expression gp. US 2 HCMV MHC I and II degradation gp. US 11 HCMV MHC I degradation gp. US 6 HCMV Inhibits TAP peptide transport gp. US 8 HCMV Binds MHC I molecules gp. US 10 HCMV Binds MHC I molecules pp 65 UL 83 HCMV Inhibits MHC II expression gp 48 m 6 MCMV Targets MHC I to lysosomes gp 40 m 152 MCMV MHC I retention in the ERGIC gp 34 m 4 MCMV MHC I intracellular retention
Цитомегаловирус: мишени Table 2. CMV modulation of the adaptive immune response. Protein Gene Virus Function T Cell Mediated Immunity gp. US 3 HCMV Inhibits MHC I and II expression gp. US 2 HCMV MHC I and II degradation gp. US 11 HCMV MHC I degradation gp. US 6 HCMV Inhibits TAP peptide transport gp. US 8 HCMV Binds MHC I molecules gp. US 10 HCMV Binds MHC I molecules pp 65 UL 83 HCMV Inhibits MHC II expression gp 48 m 6 MCMV Targets MHC I to lysosomes gp 40 m 152 MCMV MHC I retention in the ERGIC gp 34 m 4 MCMV MHC I intracellular retention
 Цитомегаловирус: клинические проявления Клинические формы: По происхождению: врожденная/приобретенная По форме: клинически выраженная и бессимптомная По тяжести: легкая, среднетяжелая, тяжелая По течению: острое, затяжное, хроническое, непрерывно рецидивирующее По распространенности: локализованная, генерализованная Пренатальная инфекция: врожденные пороки, нарушения зрения и слуха, дефекты развития ЦНС Пост(интра)натальная инфекция: от отсутствия симптомов до развития пневмонии Дети: мононуклеоз Иммунокомпетентные взрослые: ОРВИ-подобные симптомы, лихорадка Иммунокомпроментированные взрослые: тяжелые инфекции
Цитомегаловирус: клинические проявления Клинические формы: По происхождению: врожденная/приобретенная По форме: клинически выраженная и бессимптомная По тяжести: легкая, среднетяжелая, тяжелая По течению: острое, затяжное, хроническое, непрерывно рецидивирующее По распространенности: локализованная, генерализованная Пренатальная инфекция: врожденные пороки, нарушения зрения и слуха, дефекты развития ЦНС Пост(интра)натальная инфекция: от отсутствия симптомов до развития пневмонии Дети: мононуклеоз Иммунокомпетентные взрослые: ОРВИ-подобные симптомы, лихорадка Иммунокомпроментированные взрослые: тяжелые инфекции
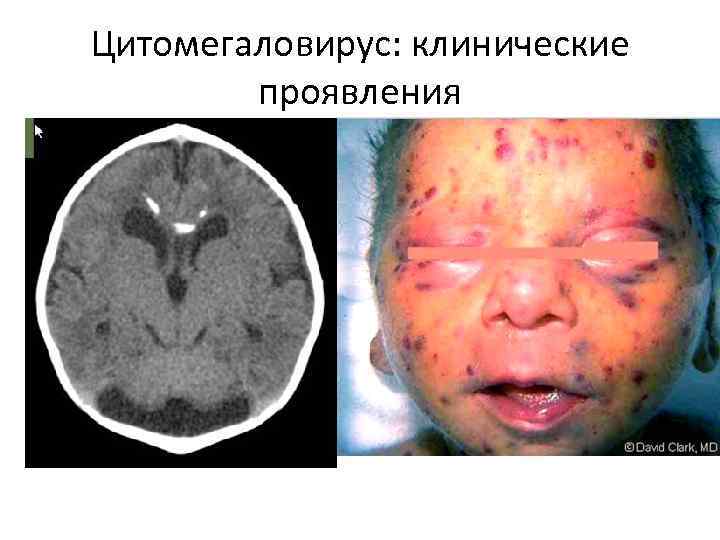 Цитомегаловирус: клинические проявления
Цитомегаловирус: клинические проявления
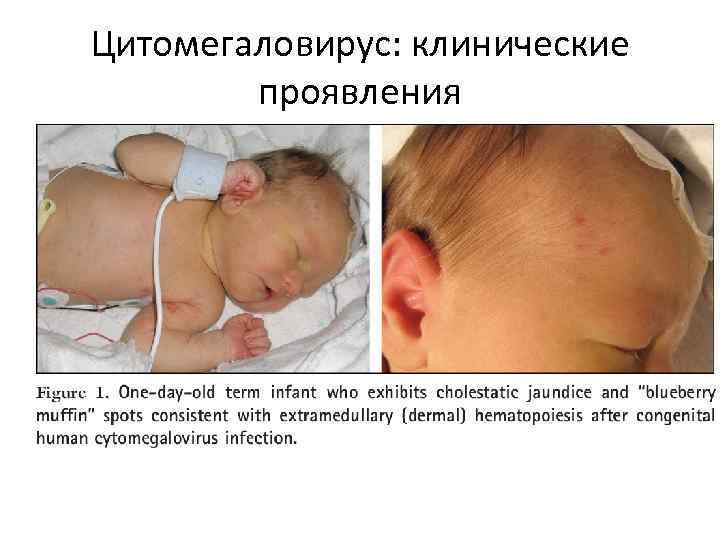 Цитомегаловирус: клинические проявления
Цитомегаловирус: клинические проявления
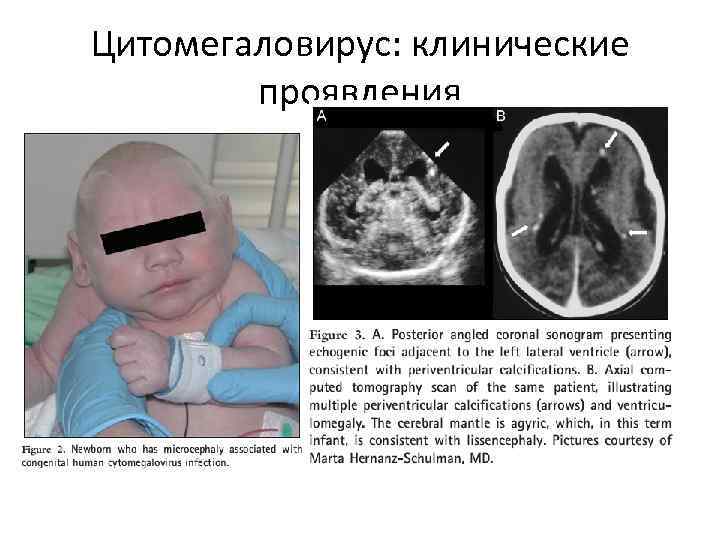 Цитомегаловирус: клинические проявления
Цитомегаловирус: клинические проявления
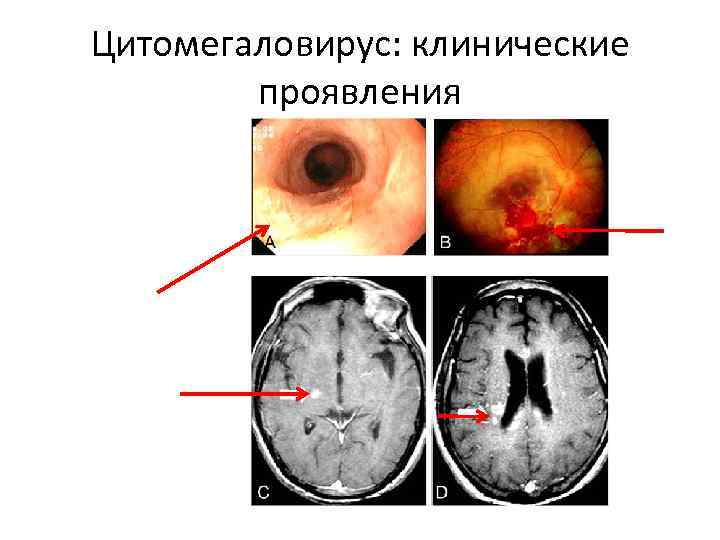 Цитомегаловирус: клинические проявления
Цитомегаловирус: клинические проявления
 Цитомегаловирус: диагностика Выделение вируса или определение его компонентов: Культуральный метод – выделение вируса на культуре фибробластов Морфологические изменения клеток (не менее 10%) Иммунофлюоресцентная детекция антигена в клетках Определение вирусных белков в биологических жидкостях ДНК-исследования (ПЦР)
Цитомегаловирус: диагностика Выделение вируса или определение его компонентов: Культуральный метод – выделение вируса на культуре фибробластов Морфологические изменения клеток (не менее 10%) Иммунофлюоресцентная детекция антигена в клетках Определение вирусных белков в биологических жидкостях ДНК-исследования (ПЦР)
 Цитомегаловирус: бляшкообразование в культуре фибробластов
Цитомегаловирус: бляшкообразование в культуре фибробластов
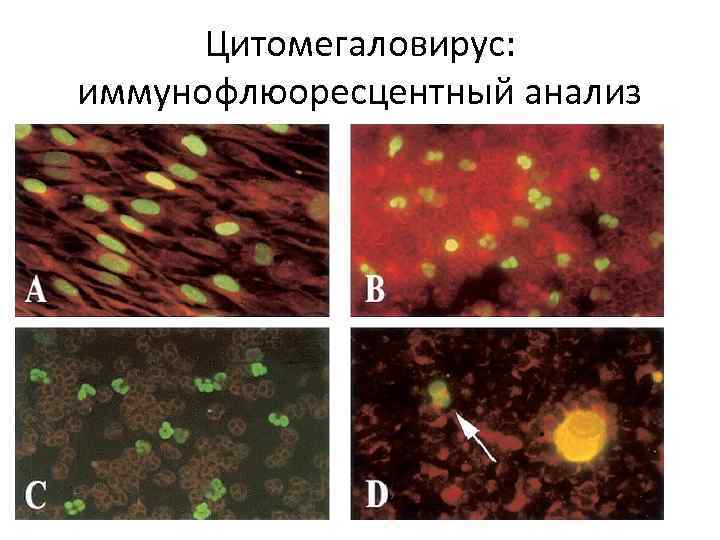 Цитомегаловирус: иммунофлюоресцентный анализ
Цитомегаловирус: иммунофлюоресцентный анализ
 Цитомегаловирус: диагностика Серологическая диагностика: Определение Ig. G – определение латентной инфекции – определение групп риска среди беременных (Ig. G -отсутствует!) Определение Ig. M – диагностика острой ЦМВ-инфекции – определение первичной инфекции/сероконверсии – низкая чувствительность метода – риск ложноположительных результатов
Цитомегаловирус: диагностика Серологическая диагностика: Определение Ig. G – определение латентной инфекции – определение групп риска среди беременных (Ig. G -отсутствует!) Определение Ig. M – диагностика острой ЦМВ-инфекции – определение первичной инфекции/сероконверсии – низкая чувствительность метода – риск ложноположительных результатов
 Цитомегаловирус: лечение Острая инфекция - введение специфического иммуноглобулина - противовирусные препараты (ганцикловир, фоскарнет, цидофовир) в случае тяжелой инфекции - противовирусная терапия в сочетании с интерферонами (рибавирин+α-интерферон) (не применятся в РФ) Хроническая инфекция При обострении: противовирусная терапия
Цитомегаловирус: лечение Острая инфекция - введение специфического иммуноглобулина - противовирусные препараты (ганцикловир, фоскарнет, цидофовир) в случае тяжелой инфекции - противовирусная терапия в сочетании с интерферонами (рибавирин+α-интерферон) (не применятся в РФ) Хроническая инфекция При обострении: противовирусная терапия
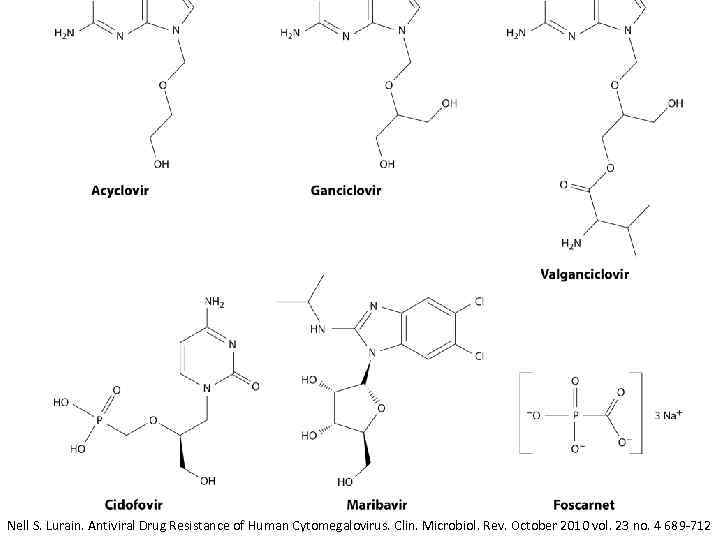 Цитомегаловирус: лечение Nell S. Lurain. Antiviral Drug Resistance of Human Cytomegalovirus. Clin. Microbiol. Rev. October 2010 vol. 23 no. 4 689 -712
Цитомегаловирус: лечение Nell S. Lurain. Antiviral Drug Resistance of Human Cytomegalovirus. Clin. Microbiol. Rev. October 2010 vol. 23 no. 4 689 -712
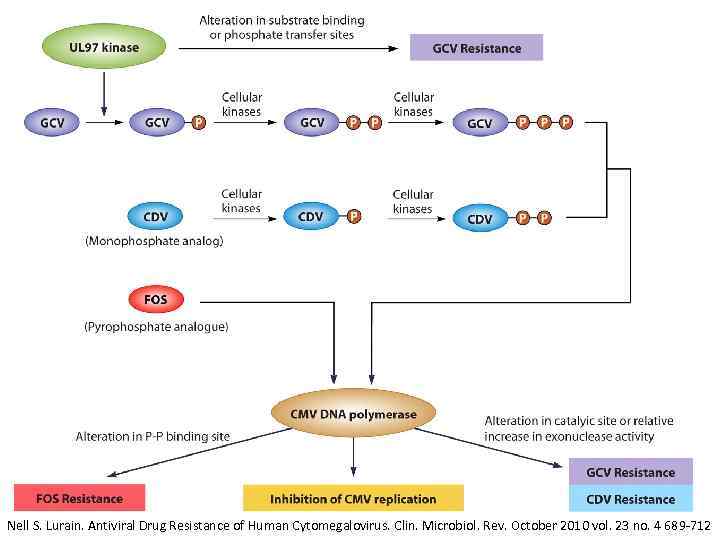 Цитомегаловирус: лечение Nell S. Lurain. Antiviral Drug Resistance of Human Cytomegalovirus. Clin. Microbiol. Rev. October 2010 vol. 23 no. 4 689 -712
Цитомегаловирус: лечение Nell S. Lurain. Antiviral Drug Resistance of Human Cytomegalovirus. Clin. Microbiol. Rev. October 2010 vol. 23 no. 4 689 -712
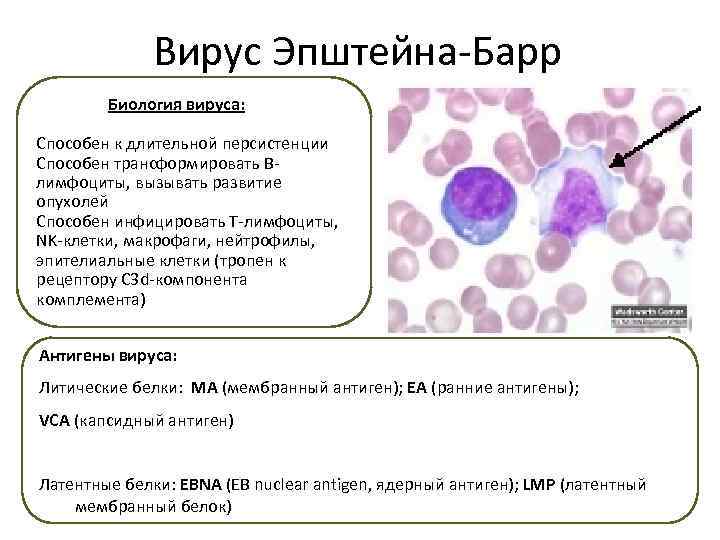 Вирус Эпштейна-Барр Биология вируса: Способен к длительной персистенции Способен трансформировать Влимфоциты, вызывать развитие опухолей Способен инфицировать Т-лимфоциты, NK-клетки, макрофаги, нейтрофилы, эпителиальные клетки (тропен к рецептору C 3 d-компонента комплемента) Антигены вируса: Литические белки: МА (мембранный антиген); ЕА (ранние антигены); VCA (капсидный антиген) Латентные белки: EBNA (EB nuclear antigen, ядерный антиген); LMP (латентный мембранный белок)
Вирус Эпштейна-Барр Биология вируса: Способен к длительной персистенции Способен трансформировать Влимфоциты, вызывать развитие опухолей Способен инфицировать Т-лимфоциты, NK-клетки, макрофаги, нейтрофилы, эпителиальные клетки (тропен к рецептору C 3 d-компонента комплемента) Антигены вируса: Литические белки: МА (мембранный антиген); ЕА (ранние антигены); VCA (капсидный антиген) Латентные белки: EBNA (EB nuclear antigen, ядерный антиген); LMP (латентный мембранный белок)
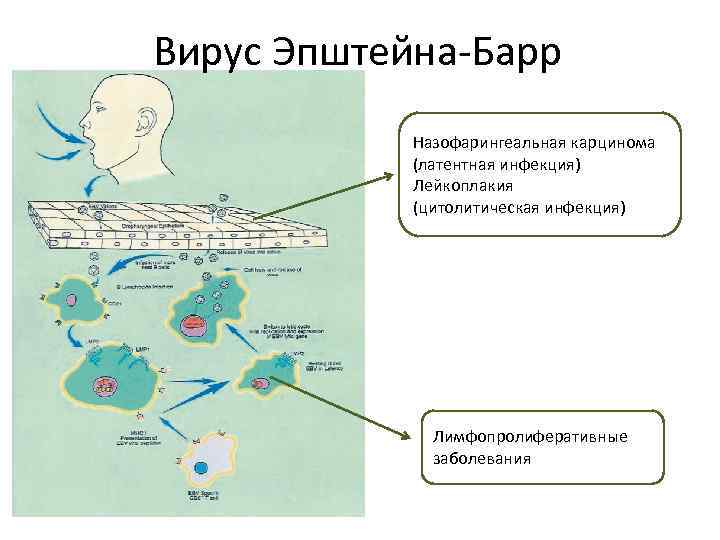 Вирус Эпштейна-Барр Назофарингеальная карцинома (латентная инфекция) Лейкоплакия (цитолитическая инфекция) Лимфопролиферативные заболевания
Вирус Эпштейна-Барр Назофарингеальная карцинома (латентная инфекция) Лейкоплакия (цитолитическая инфекция) Лимфопролиферативные заболевания
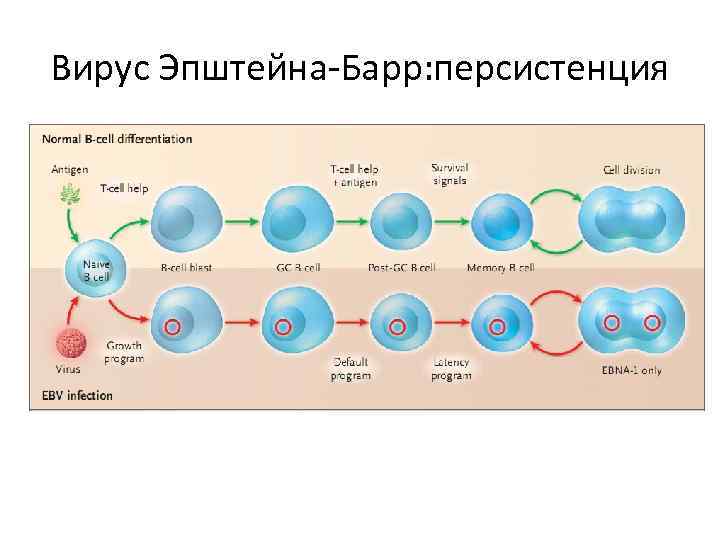 Вирус Эпштейна-Барр: персистенция
Вирус Эпштейна-Барр: персистенция
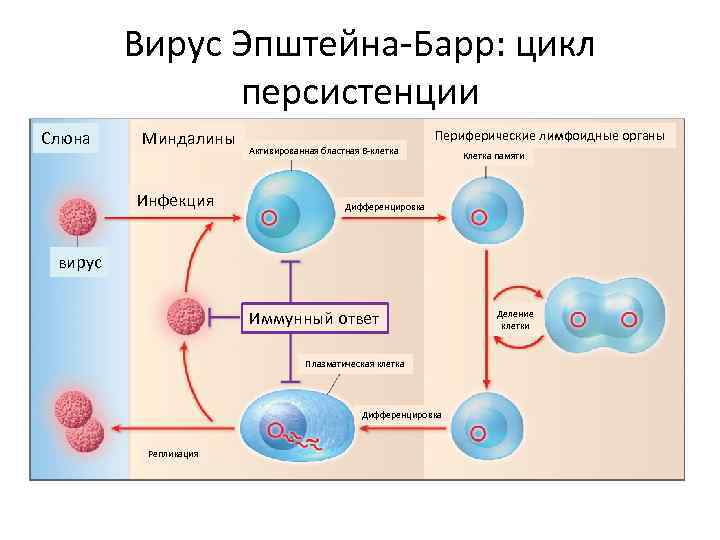 Вирус Эпштейна-Барр: цикл персистенции Слюна Миндалины Инфекция Активированная бластная В-клетка Периферические лимфоидные органы Клетка памяти Дифференцировка вирус Иммунный ответ Плазматическая клетка Дифференцировка Репликация Деление клетки
Вирус Эпштейна-Барр: цикл персистенции Слюна Миндалины Инфекция Активированная бластная В-клетка Периферические лимфоидные органы Клетка памяти Дифференцировка вирус Иммунный ответ Плазматическая клетка Дифференцировка Репликация Деление клетки
 Вирус Эпштейна-Барр: цикл персистенции
Вирус Эпштейна-Барр: цикл персистенции
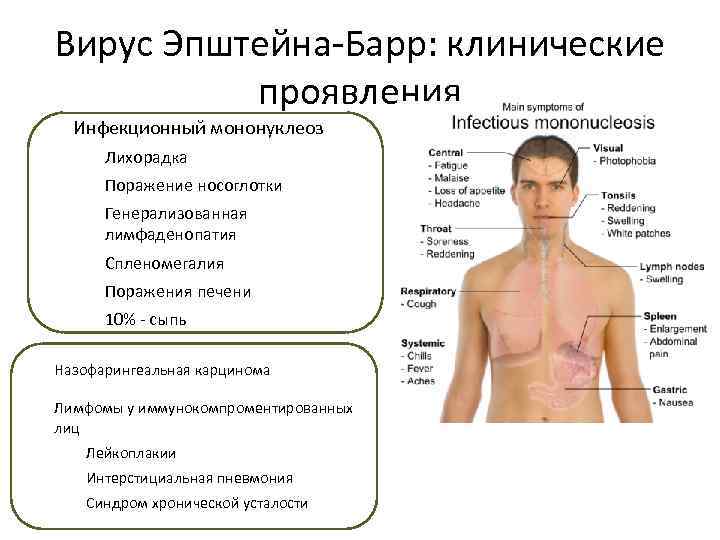 Вирус Эпштейна-Барр: клинические проявления Инфекционный мононуклеоз Лихорадка Поражение носоглотки Генерализованная лимфаденопатия Спленомегалия Поражения печени 10% - сыпь Назофарингеальная карцинома Лимфомы у иммунокомпроментированных лиц Лейкоплакии Интерстициальная пневмония Синдром хронической усталости
Вирус Эпштейна-Барр: клинические проявления Инфекционный мононуклеоз Лихорадка Поражение носоглотки Генерализованная лимфаденопатия Спленомегалия Поражения печени 10% - сыпь Назофарингеальная карцинома Лимфомы у иммунокомпроментированных лиц Лейкоплакии Интерстициальная пневмония Синдром хронической усталости
 Вирус Эпштейна-Барр: клинические проявления хроническая рецидивирующая инфекция: а) хроническая активная ВЭБ-инфекция; б) генерализованная форма хронической активной ВЭБ-инфекции; в) ВЭБ-ассоциированный гемофагоцитарный синдром; г) стертые или атипичные формы ВЭБ-инфекции: длительный субфебрилитет неясного генеза, клиника вторичного иммунодефицита; развитие онкологического (лимфопролиферативного) процесса (лимфомы, назофарингеальная карцинома, лейкоплакии, рак желудка и кишечника и др. ); развитие аутоиммунного заболевания.
Вирус Эпштейна-Барр: клинические проявления хроническая рецидивирующая инфекция: а) хроническая активная ВЭБ-инфекция; б) генерализованная форма хронической активной ВЭБ-инфекции; в) ВЭБ-ассоциированный гемофагоцитарный синдром; г) стертые или атипичные формы ВЭБ-инфекции: длительный субфебрилитет неясного генеза, клиника вторичного иммунодефицита; развитие онкологического (лимфопролиферативного) процесса (лимфомы, назофарингеальная карцинома, лейкоплакии, рак желудка и кишечника и др. ); развитие аутоиммунного заболевания.
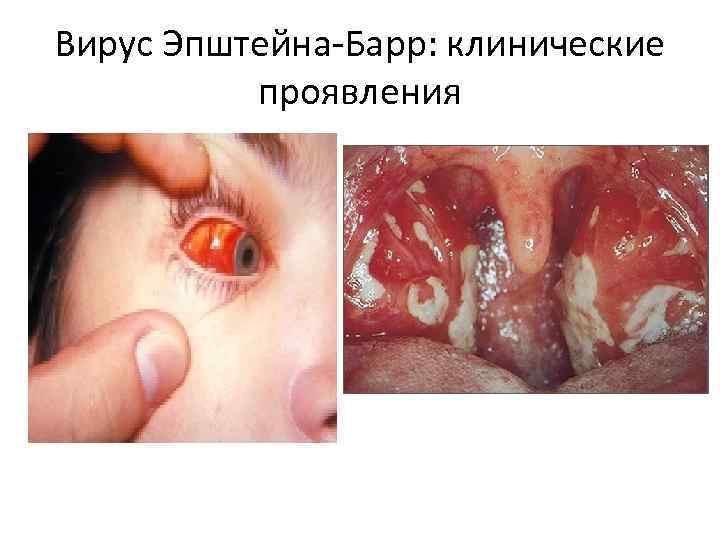 Вирус Эпштейна-Барр: клинические проявления
Вирус Эпштейна-Барр: клинические проявления
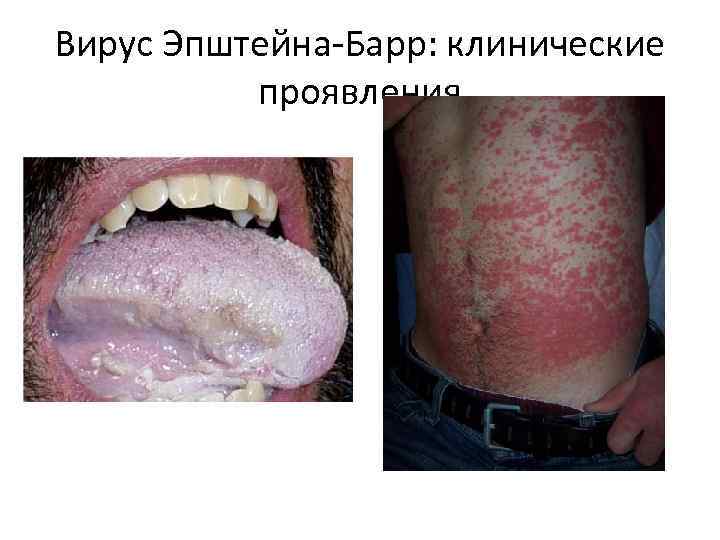 Вирус Эпштейна-Барр: клинические проявления
Вирус Эпштейна-Барр: клинические проявления
 Вирус Эпштейна-Барр: лабораторная диагностика 2 -3 недели: лейкоцитоз, абсолютный лимфоцитоз Увеличение АЛТ, АСТ, С-реактивного белка Обнаружение ДНК ВЭБ или его антигенов На ранних стадиях – обнаружением Ig. M к антигенам вируса Затем – обнаружение Ig. G
Вирус Эпштейна-Барр: лабораторная диагностика 2 -3 недели: лейкоцитоз, абсолютный лимфоцитоз Увеличение АЛТ, АСТ, С-реактивного белка Обнаружение ДНК ВЭБ или его антигенов На ранних стадиях – обнаружением Ig. M к антигенам вируса Затем – обнаружение Ig. G
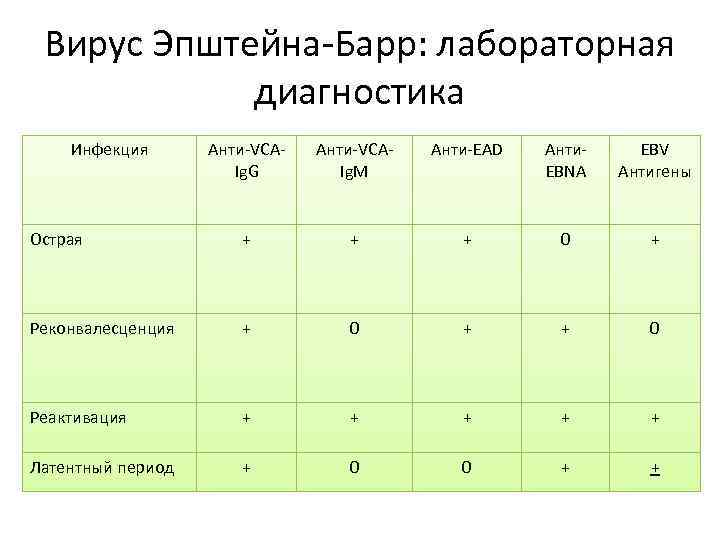 Вирус Эпштейна-Барр: лабораторная диагностика Инфекция Анти-VCAIg. G Анти-VCAIg. M Анти-EAD Анти. EBNA EBV Антигены Острая + + + 0 + Реконвалесценция + 0 + + 0 Реактивация + + + Латентный период + 0 0 + +
Вирус Эпштейна-Барр: лабораторная диагностика Инфекция Анти-VCAIg. G Анти-VCAIg. M Анти-EAD Анти. EBNA EBV Антигены Острая + + + 0 + Реконвалесценция + 0 + + 0 Реактивация + + + Латентный период + 0 0 + +
 Вирус Эпштейна-Барр: лабораторная диагностика Антигены вируса: Литические белки: МА (мембранный антиген); ЕА (ранние антигены); VCA (капсидный антиген) Латентные белки: EBNA (EB nuclear antigen, ядерный антиген); LMP (латентный мембранный белок)
Вирус Эпштейна-Барр: лабораторная диагностика Антигены вируса: Литические белки: МА (мембранный антиген); ЕА (ранние антигены); VCA (капсидный антиген) Латентные белки: EBNA (EB nuclear antigen, ядерный антиген); LMP (латентный мембранный белок)
 Вирус Эпштейна-Барр: лечение Цель лечения – редуцировать симптомы: Гидратация Антипиретики (кроме аспирина детям [синдром Рейе]) Анальгетики Антивирусные препараты (Ацикловир, Ганцикловир, Фоскарнет – неэффективны!!!) В тяжелых случаях – короткие курсы кортикостероидов (5 -7 дней) (при обструкции дыхательных путей [нет доказанной эффективности], тяжелой тромбоцитопении (<20. 000/мкл) , гемолитической анемии
Вирус Эпштейна-Барр: лечение Цель лечения – редуцировать симптомы: Гидратация Антипиретики (кроме аспирина детям [синдром Рейе]) Анальгетики Антивирусные препараты (Ацикловир, Ганцикловир, Фоскарнет – неэффективны!!!) В тяжелых случаях – короткие курсы кортикостероидов (5 -7 дней) (при обструкции дыхательных путей [нет доказанной эффективности], тяжелой тромбоцитопении (<20. 000/мкл) , гемолитической анемии
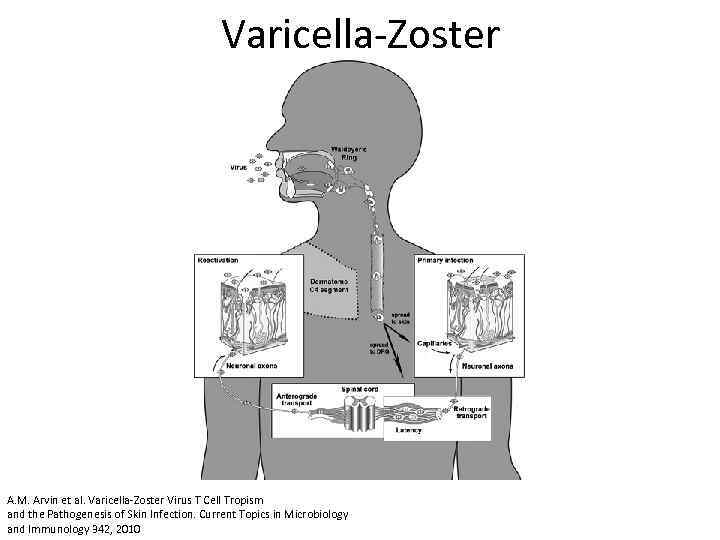 Varicella-Zoster A. M. Arvin et al. Varicella-Zoster Virus T Cell Tropism and the Pathogenesis of Skin Infection. Current Topics in Microbiology and Immunology 342, 2010
Varicella-Zoster A. M. Arvin et al. Varicella-Zoster Virus T Cell Tropism and the Pathogenesis of Skin Infection. Current Topics in Microbiology and Immunology 342, 2010
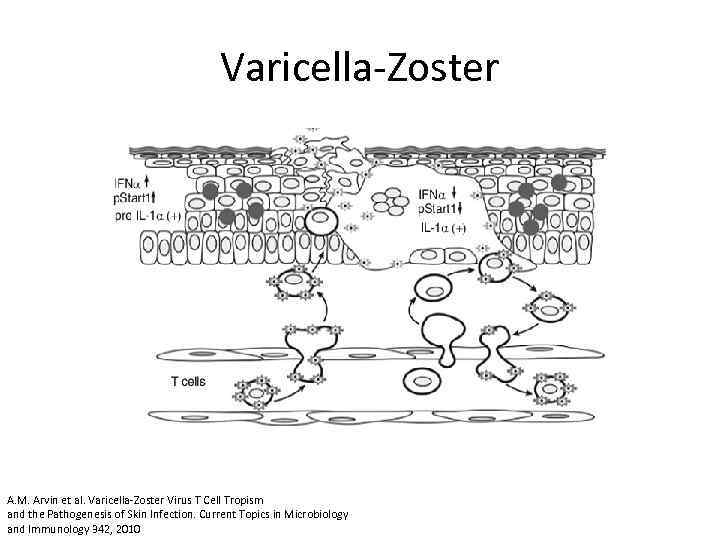 Varicella-Zoster A. M. Arvin et al. Varicella-Zoster Virus T Cell Tropism and the Pathogenesis of Skin Infection. Current Topics in Microbiology and Immunology 342, 2010
Varicella-Zoster A. M. Arvin et al. Varicella-Zoster Virus T Cell Tropism and the Pathogenesis of Skin Infection. Current Topics in Microbiology and Immunology 342, 2010
 Вирус герпеса 6 типа • Описан в 1980 году • Инфицированность - 35 -90% населения • Мишень – В-лимфоциты • В случае коинфекции ВИЧ вирусы – синергисты в отношении деструктивного влияния на лимфоциты Первичная острая инфекция: СХУ (? Не подтверждено) Внезапная экзантема новорожденных Инфекционный мононуклеоз Гистиоцитарный некротический лимфаденит Персистирующая инфекция: Лимфопролиферативные заболевания Злокачественные лимфомы
Вирус герпеса 6 типа • Описан в 1980 году • Инфицированность - 35 -90% населения • Мишень – В-лимфоциты • В случае коинфекции ВИЧ вирусы – синергисты в отношении деструктивного влияния на лимфоциты Первичная острая инфекция: СХУ (? Не подтверждено) Внезапная экзантема новорожденных Инфекционный мононуклеоз Гистиоцитарный некротический лимфаденит Персистирующая инфекция: Лимфопролиферативные заболевания Злокачественные лимфомы
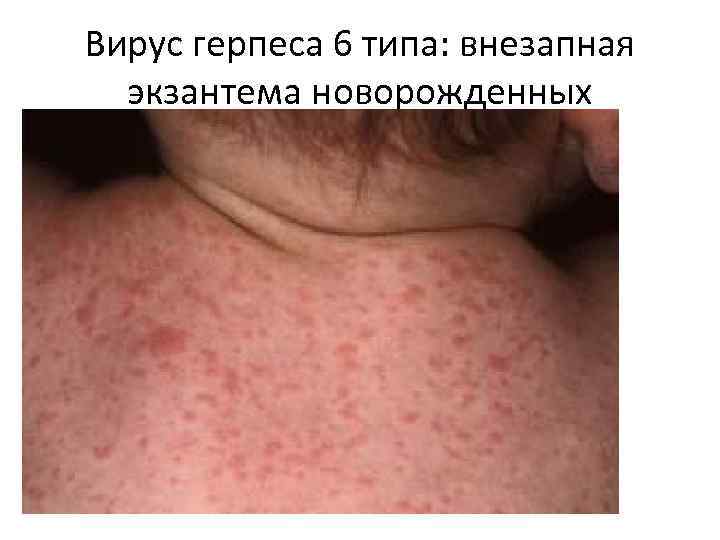 Вирус герпеса 6 типа: внезапная экзантема новорожденных
Вирус герпеса 6 типа: внезапная экзантема новорожденных
 Вирус герпеса 7 типа Впервые описан в 1990 Рецептор – CD 4. В течение инфекции наблюдается снижение количества Т -хелперов Патогенез неизвестен. Является возможной причиной заболеваний: Лимфопролиферативные заболевания СХУ Иммунодефициты Клинические признаки: лихорадка, гепатоспленомегалия, панцитопения Лечение: симптоматическое, коррекция иммунитета Профилактика: срининг донорской крови, органов и тканей
Вирус герпеса 7 типа Впервые описан в 1990 Рецептор – CD 4. В течение инфекции наблюдается снижение количества Т -хелперов Патогенез неизвестен. Является возможной причиной заболеваний: Лимфопролиферативные заболевания СХУ Иммунодефициты Клинические признаки: лихорадка, гепатоспленомегалия, панцитопения Лечение: симптоматическое, коррекция иммунитета Профилактика: срининг донорской крови, органов и тканей
 Ретровирусы (вирус Т-клеточного лейкоза, HTLV) Впервые выделен в 1977 (B. Poiesz и F. Ruscetti) Рецептор – IL-2 R. Клинические проявления: Т-клеточный лейкоз Регионы распространения – Япония, страны Карибского бассейна, Центральная и западная Африка Пути передачи: материнское молоко, половой, переливание крови Этиотропного лечения не существует
Ретровирусы (вирус Т-клеточного лейкоза, HTLV) Впервые выделен в 1977 (B. Poiesz и F. Ruscetti) Рецептор – IL-2 R. Клинические проявления: Т-клеточный лейкоз Регионы распространения – Япония, страны Карибского бассейна, Центральная и западная Африка Пути передачи: материнское молоко, половой, переливание крови Этиотропного лечения не существует
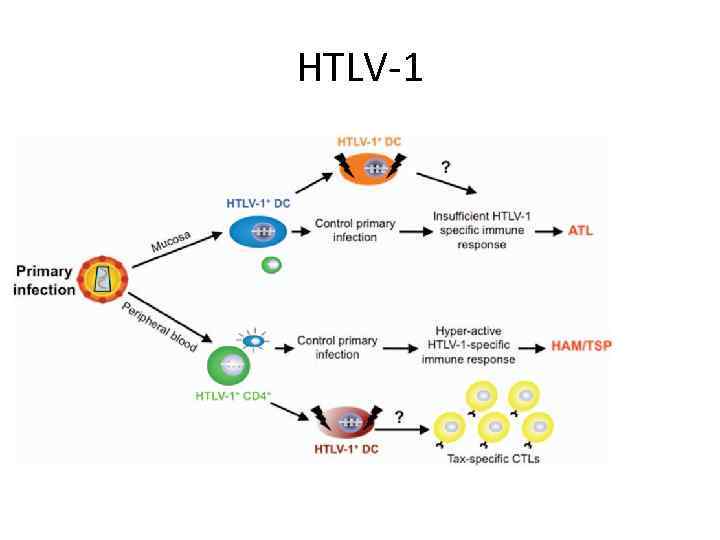 HTLV-1
HTLV-1
 Спасибо за внимание!
Спасибо за внимание!


