гидролиз.ppt
- Количество слайдов: 13

![ИНДИКАТОРЫ Среда раствора нейтральная щелочная кислая [OH-] = [H+] [OH-] > [H+] [OH-] < ИНДИКАТОРЫ Среда раствора нейтральная щелочная кислая [OH-] = [H+] [OH-] > [H+] [OH-] <](https://present5.com/presentation/3/-33033369_31468702.pdf-img/-33033369_31468702.pdf-2.jpg) ИНДИКАТОРЫ Среда раствора нейтральная щелочная кислая [OH-] = [H+] [OH-] > [H+] [OH-] < [H+] лакмус метилоранж фенолфталеин
ИНДИКАТОРЫ Среда раствора нейтральная щелочная кислая [OH-] = [H+] [OH-] > [H+] [OH-] < [H+] лакмус метилоранж фенолфталеин
 Понятие о во. Дородном показателе ввел датский биохимик С. П. Серенсен (1868 -1939), разрабатывавший в это время способы контроля за качеством пива. Водородный показатель [ р. Н ] р. Н = - lg[H+] Среда раствора [H+]↔[OH-] [H+] p. H нейтральная [H+]=[OH-] [H+]=10 -7 моль/л 7 [H+]>[OH-] [H+]<10 -7 моль/л <7 [H+]<[OH-] [H+]>10 -7 моль/л кислая щелочная >7
Понятие о во. Дородном показателе ввел датский биохимик С. П. Серенсен (1868 -1939), разрабатывавший в это время способы контроля за качеством пива. Водородный показатель [ р. Н ] р. Н = - lg[H+] Среда раствора [H+]↔[OH-] [H+] p. H нейтральная [H+]=[OH-] [H+]=10 -7 моль/л 7 [H+]>[OH-] [H+]<10 -7 моль/л <7 [H+]<[OH-] [H+]>10 -7 моль/л кислая щелочная >7
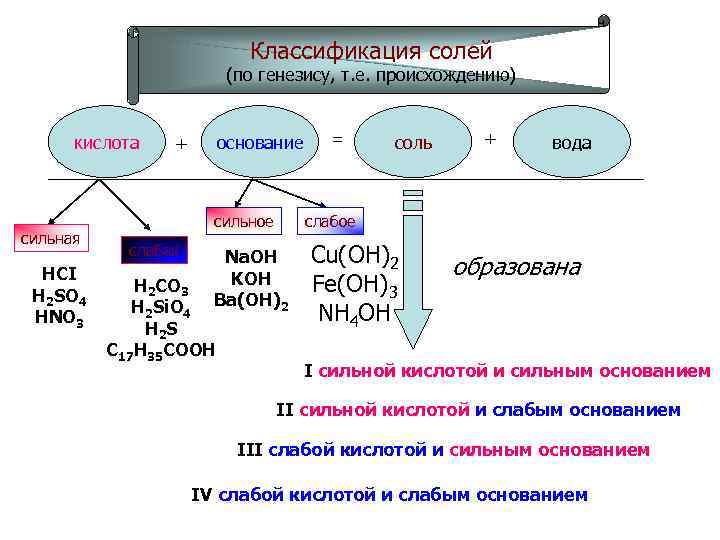 Классификация солей (по генезису, т. е. происхождению) кислота сильная HCI H 2 SO 4 HNO 3 основание + сильное слабая соль + вода слабое Na. OH KOH Ba(OH)2 H 2 CO 3 H 2 Si. O 4 H 2 S C 17 H 35 COOH = Сu(OH)2 Fe(OH)3 NH 4 OH образована I cильной кислотой и сильным основанием II сильной кислотой и слабым основанием III слабой кислотой и сильным основанием IV cлабой кислотой и слабым основанием
Классификация солей (по генезису, т. е. происхождению) кислота сильная HCI H 2 SO 4 HNO 3 основание + сильное слабая соль + вода слабое Na. OH KOH Ba(OH)2 H 2 CO 3 H 2 Si. O 4 H 2 S C 17 H 35 COOH = Сu(OH)2 Fe(OH)3 NH 4 OH образована I cильной кислотой и сильным основанием II сильной кислотой и слабым основанием III слабой кислотой и сильным основанием IV cлабой кислотой и слабым основанием
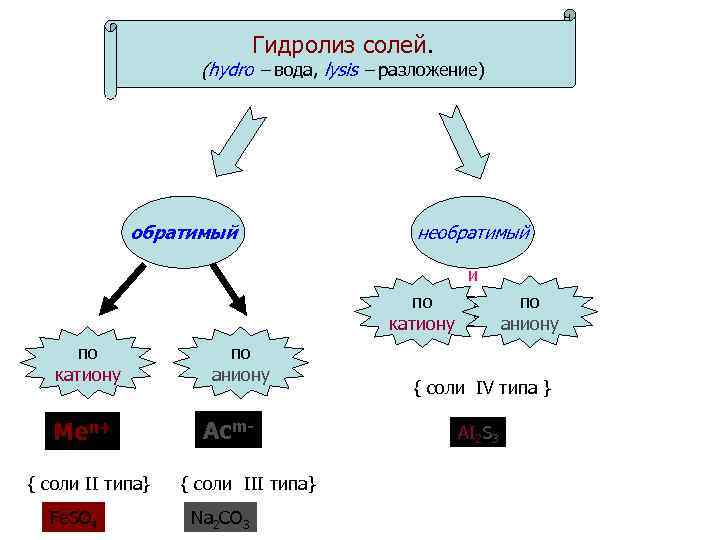 Гидролиз солей. (hydro – вода, lysis – разложение) обратимый необратимый и по катиону Меn+ { соли II типа} Fe. SO 4 по аниону Асm{ соли III типа} Na 2 CO 3 по аниону { соли IV типа } AI 2 S 3
Гидролиз солей. (hydro – вода, lysis – разложение) обратимый необратимый и по катиону Меn+ { соли II типа} Fe. SO 4 по аниону Асm{ соли III типа} Na 2 CO 3 по аниону { соли IV типа } AI 2 S 3
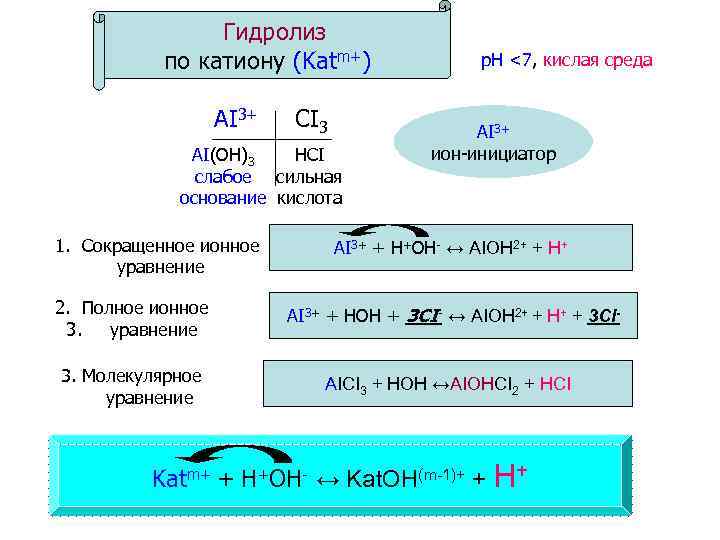 Гидролиз по катиону (Katm+) АI 3+ CI 3 AI(OH)3 HCI слабое сильная основание кислота 1. Сокращенное ионное уравнение 2. Полное ионное 3. уравнение 3. Молекулярное уравнение р. Н <7, кислая среда AI 3+ ион-инициатор AI 3+ + H+OH- ↔ AIOH 2+ + H+ AI 3+ + HOH + 3 CI- ↔ AIOH 2+ + H+ + 3 CI- AICI 3 + HOH ↔AIOHCI 2 + HCI Katm+ + H+OH- ↔ Kat. OH(m-1)+ + H+
Гидролиз по катиону (Katm+) АI 3+ CI 3 AI(OH)3 HCI слабое сильная основание кислота 1. Сокращенное ионное уравнение 2. Полное ионное 3. уравнение 3. Молекулярное уравнение р. Н <7, кислая среда AI 3+ ион-инициатор AI 3+ + H+OH- ↔ AIOH 2+ + H+ AI 3+ + HOH + 3 CI- ↔ AIOH 2+ + H+ + 3 CI- AICI 3 + HOH ↔AIOHCI 2 + HCI Katm+ + H+OH- ↔ Kat. OH(m-1)+ + H+
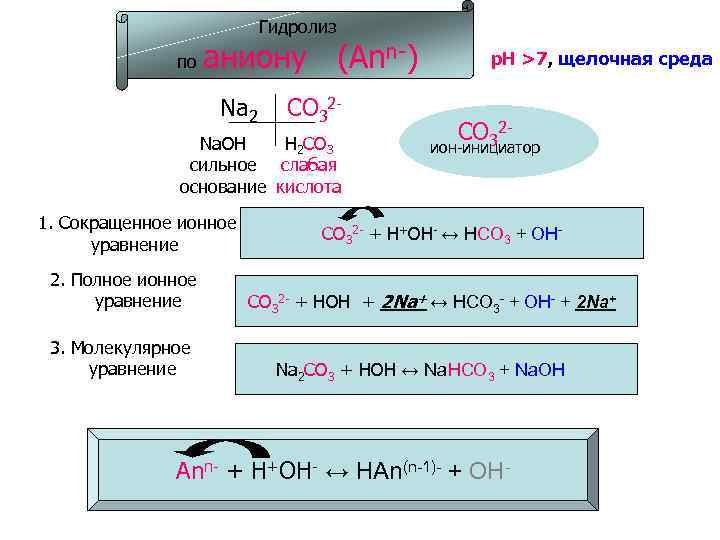 Гидролиз по аниону (Ann-) Na 2 CO 32 - Na. OH Н 2 СО 3 сильное слабая основание кислота 1. Сокращенное ионное уравнение 2. Полное ионное уравнение 3. Молекулярное уравнение p. H >7, щелочная среда СО 32 - ион-инициатор CO 32 - + H+OH- ↔ HCO 3 + OHCO 32 - + HOH + 2 Na+ ↔ HCO 3 - + OH- + 2 Na+ Na 2 CO 3 + HOH ↔ Na. HCO 3 + Na. OH Ann- + H+OH- ↔ HAn(n-1)- + OH-
Гидролиз по аниону (Ann-) Na 2 CO 32 - Na. OH Н 2 СО 3 сильное слабая основание кислота 1. Сокращенное ионное уравнение 2. Полное ионное уравнение 3. Молекулярное уравнение p. H >7, щелочная среда СО 32 - ион-инициатор CO 32 - + H+OH- ↔ HCO 3 + OHCO 32 - + HOH + 2 Na+ ↔ HCO 3 - + OH- + 2 Na+ Na 2 CO 3 + HOH ↔ Na. HCO 3 + Na. OH Ann- + H+OH- ↔ HAn(n-1)- + OH-
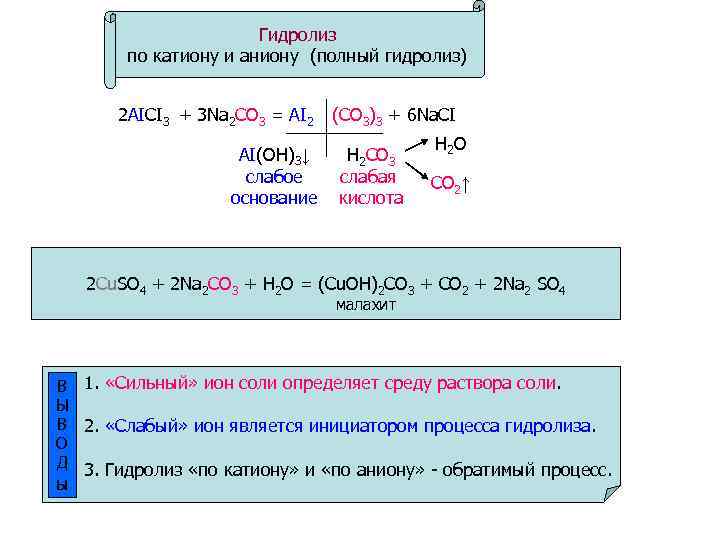 Гидролиз по катиону и аниону (полный гидролиз) 2 AICI 3 + 3 Na 2 CO 3 = AI 2 AI(OH)3↓ слабое основание (CO 3)3 + 6 Na. CI H 2 CO 3 слабая кислота H 2 O CO 2↑ 2 Cu. SO 4 + 2 Na 2 CO 3 + H 2 O = (Cu. OH)2 CO 3 + CO 2 + 2 Na 2 SO 4 малахит В 1. «Сильный» ион соли определяет среду раствора соли. Ы В 2. «Слабый» ион является инициатором процесса гидролиза. О Д 3. Гидролиз «по катиону» и «по аниону» - обратимый процесс. ы
Гидролиз по катиону и аниону (полный гидролиз) 2 AICI 3 + 3 Na 2 CO 3 = AI 2 AI(OH)3↓ слабое основание (CO 3)3 + 6 Na. CI H 2 CO 3 слабая кислота H 2 O CO 2↑ 2 Cu. SO 4 + 2 Na 2 CO 3 + H 2 O = (Cu. OH)2 CO 3 + CO 2 + 2 Na 2 SO 4 малахит В 1. «Сильный» ион соли определяет среду раствора соли. Ы В 2. «Слабый» ион является инициатором процесса гидролиза. О Д 3. Гидролиз «по катиону» и «по аниону» - обратимый процесс. ы
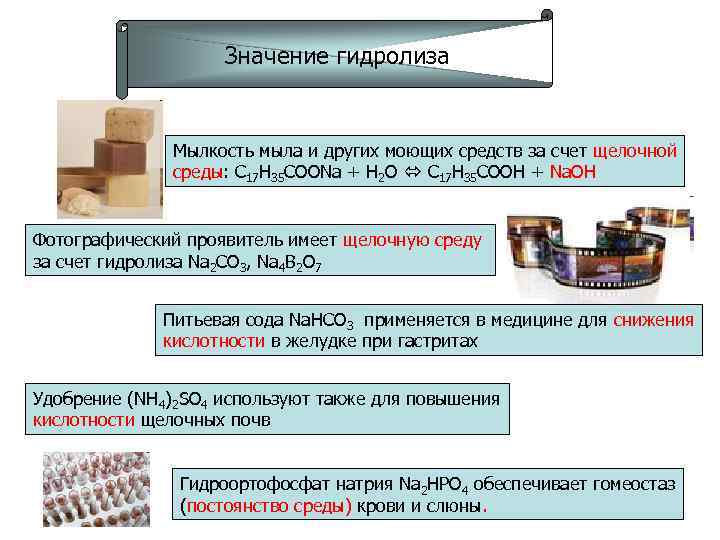 Значение гидролиза Мылкость мыла и других моющих средств за счет щелочной среды: С 17 Н 35 СООNa + H 2 O C 17 H 35 COOH + Na. OH Фотографический проявитель имеет щелочную среду за счет гидролиза Na 2 CO 3, Na 4 B 2 O 7 Питьевая сода Na. HCO 3 применяется в медицине для снижения кислотности в желудке при гастритах Удобрение (NH 4)2 SO 4 используют также для повышения кислотности щелочных почв Гидроортофосфат натрия Nа 2 НРО 4 обеспечивает гомеостаз (постоянство среды) крови и слюны.
Значение гидролиза Мылкость мыла и других моющих средств за счет щелочной среды: С 17 Н 35 СООNa + H 2 O C 17 H 35 COOH + Na. OH Фотографический проявитель имеет щелочную среду за счет гидролиза Na 2 CO 3, Na 4 B 2 O 7 Питьевая сода Na. HCO 3 применяется в медицине для снижения кислотности в желудке при гастритах Удобрение (NH 4)2 SO 4 используют также для повышения кислотности щелочных почв Гидроортофосфат натрия Nа 2 НРО 4 обеспечивает гомеостаз (постоянство среды) крови и слюны.
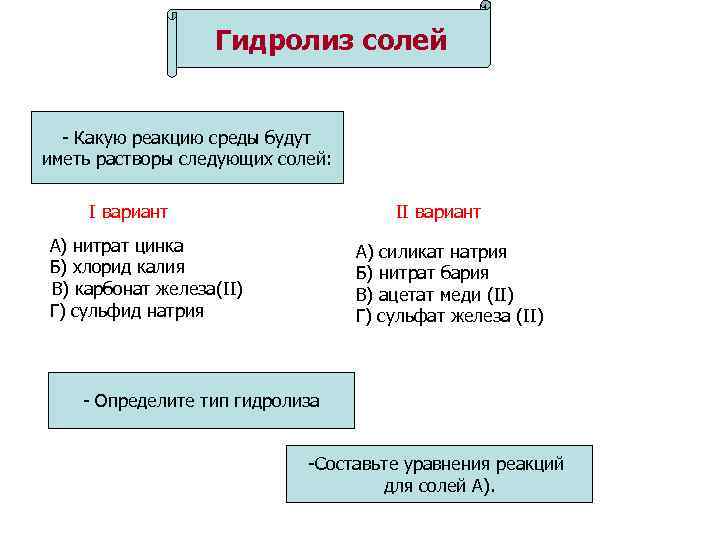 Гидролиз солей - Какую реакцию среды будут иметь растворы следующих солей: I вариант II вариант А) нитрат цинка Б) хлорид калия В) карбонат железа(II) Г) сульфид натрия А) силикат натрия Б) нитрат бария В) ацетат меди (II) Г) сульфат железа (II) - Определите тип гидролиза -Составьте уравнения реакций для солей А).
Гидролиз солей - Какую реакцию среды будут иметь растворы следующих солей: I вариант II вариант А) нитрат цинка Б) хлорид калия В) карбонат железа(II) Г) сульфид натрия А) силикат натрия Б) нитрат бария В) ацетат меди (II) Г) сульфат железа (II) - Определите тип гидролиза -Составьте уравнения реакций для солей А).
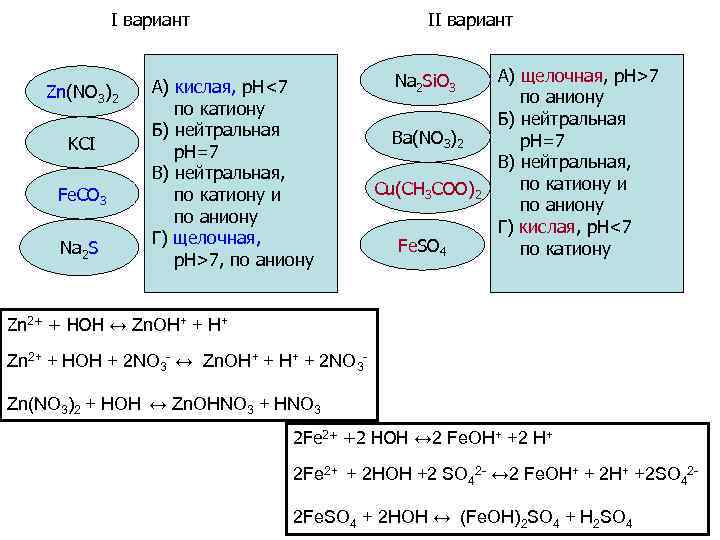 I вариант Zn(NO 3)2 KCI Fe. CO 3 Na 2 S II вариант А) кислая, р. Н<7 по катиону Б) нейтральная р. Н=7 В) нейтральная, по катиону и по аниону Г) щелочная, р. Н>7, по аниону Na 2 Si. O 3 Ba(NO 3)2 Cu(CH 3 COO)2 Fe. SO 4 А) щелочная, р. Н>7 по аниону Б) нейтральная р. Н=7 В) нейтральная, по катиону и по аниону Г) кислая, р. Н<7 по катиону Zn 2+ + HOH ↔ Zn. OH+ + H+ Zn 2+ + HOH + 2 NO 3 - ↔ Zn. OH+ + 2 NO 3 Zn(NO 3)2 + HOH ↔ Zn. OHNO 3 + HNO 3 2 Fe 2+ +2 HOH ↔ 2 Fe. OH+ +2 H+ 2 Fe 2+ + 2 HOH +2 SO 42 - ↔ 2 Fe. OH+ + 2 H+ +2 SO 422 Fe. SO 4 + 2 HOH ↔ (Fe. OH)2 SO 4 + H 2 SO 4
I вариант Zn(NO 3)2 KCI Fe. CO 3 Na 2 S II вариант А) кислая, р. Н<7 по катиону Б) нейтральная р. Н=7 В) нейтральная, по катиону и по аниону Г) щелочная, р. Н>7, по аниону Na 2 Si. O 3 Ba(NO 3)2 Cu(CH 3 COO)2 Fe. SO 4 А) щелочная, р. Н>7 по аниону Б) нейтральная р. Н=7 В) нейтральная, по катиону и по аниону Г) кислая, р. Н<7 по катиону Zn 2+ + HOH ↔ Zn. OH+ + H+ Zn 2+ + HOH + 2 NO 3 - ↔ Zn. OH+ + 2 NO 3 Zn(NO 3)2 + HOH ↔ Zn. OHNO 3 + HNO 3 2 Fe 2+ +2 HOH ↔ 2 Fe. OH+ +2 H+ 2 Fe 2+ + 2 HOH +2 SO 42 - ↔ 2 Fe. OH+ + 2 H+ +2 SO 422 Fe. SO 4 + 2 HOH ↔ (Fe. OH)2 SO 4 + H 2 SO 4
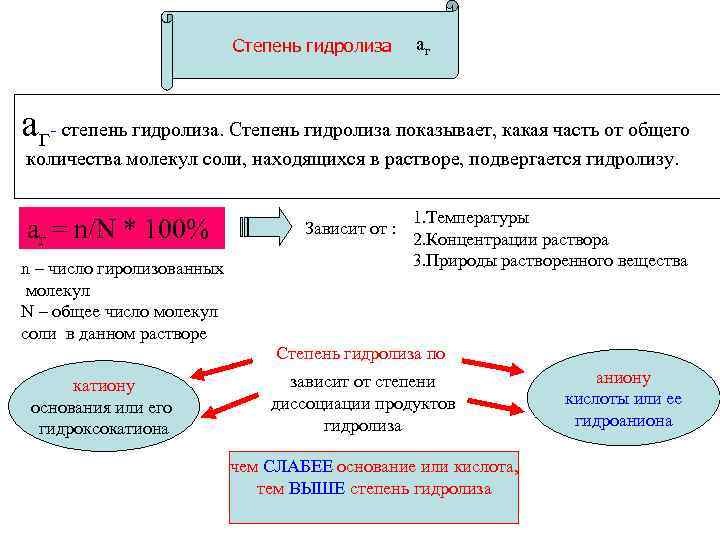 Степень гидролиза аг аг- степень гидролиза. Степень гидролиза показывает, какая часть от общего количества молекул соли, находящихся в растворе, подвергается гидролизу. аг = n/N * 100% n – число гиролизованных молекул N – общее число молекул соли в данном растворе Зависит от : 1. Температуры 2. Концентрации раствора 3. Природы растворенного вещества Степень гидролиза по катиону основания или его гидроксокатиона зависит от степени диссоциации продуктов гидролиза чем СЛАБЕЕ основание или кислота, тем ВЫШЕ степень гидролиза аниону кислоты или ее гидроаниона
Степень гидролиза аг аг- степень гидролиза. Степень гидролиза показывает, какая часть от общего количества молекул соли, находящихся в растворе, подвергается гидролизу. аг = n/N * 100% n – число гиролизованных молекул N – общее число молекул соли в данном растворе Зависит от : 1. Температуры 2. Концентрации раствора 3. Природы растворенного вещества Степень гидролиза по катиону основания или его гидроксокатиона зависит от степени диссоциации продуктов гидролиза чем СЛАБЕЕ основание или кислота, тем ВЫШЕ степень гидролиза аниону кислоты или ее гидроаниона
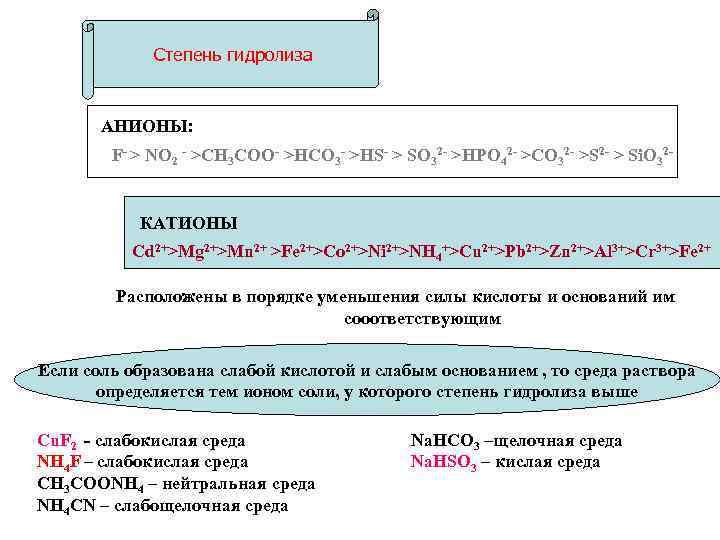 Степень гидролиза АНИОНЫ: F- > NO 2 - >CH 3 COO- >HCO 3 - >HS- > SO 32 - >HPO 42 - >CO 32 - >S 2 - > Si. O 32 КАТИОНЫ Cd 2+>Mg 2+>Mn 2+ >Fe 2+>Co 2+>Ni 2+>NH 4+>Cu 2+>Pb 2+>Zn 2+>Al 3+>Cr 3+>Fe 2+ Расположены в порядке уменьшения силы кислоты и оснований им сооответствующим Если соль образована слабой кислотой и слабым основанием , то среда раствора определяется тем ионом соли, у которого степень гидролиза выше Сu. F 2 - слабокислая среда NH 4 F – cлабокислая среда CH 3 COONH 4 – нейтральная среда NH 4 CN – слабощелочная среда Na. HCO 3 –щелочная среда Na. HSO 3 – кислая среда
Степень гидролиза АНИОНЫ: F- > NO 2 - >CH 3 COO- >HCO 3 - >HS- > SO 32 - >HPO 42 - >CO 32 - >S 2 - > Si. O 32 КАТИОНЫ Cd 2+>Mg 2+>Mn 2+ >Fe 2+>Co 2+>Ni 2+>NH 4+>Cu 2+>Pb 2+>Zn 2+>Al 3+>Cr 3+>Fe 2+ Расположены в порядке уменьшения силы кислоты и оснований им сооответствующим Если соль образована слабой кислотой и слабым основанием , то среда раствора определяется тем ионом соли, у которого степень гидролиза выше Сu. F 2 - слабокислая среда NH 4 F – cлабокислая среда CH 3 COONH 4 – нейтральная среда NH 4 CN – слабощелочная среда Na. HCO 3 –щелочная среда Na. HSO 3 – кислая среда


