Иммунопрофилактика.ppt
- Количество слайдов: 75

Иммунопрофилактика. Вакцины нового поколения профессор Бажукова Т. А. зав. каф. микробиологии, вирусологии и иммунологии

Иммунизация против инфекций • Иммунизация - создание эффективного антигенспецифического иммунитета, препятствующего развитию болезни в результате контакта иммунизированного человека с патогенным микроорганизмом.
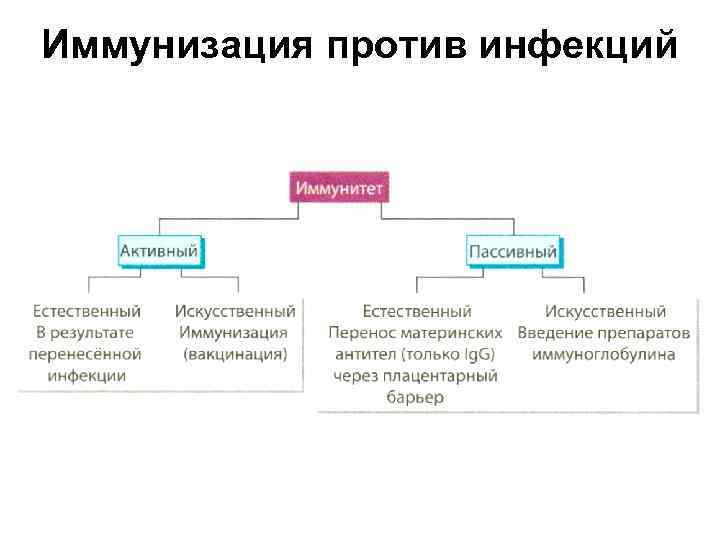
Иммунизация против инфекций

Основы иммунизации • Формирование активного иммунитета подразумевает развитие в организме всех последовательных стадий иммунных реакций. Это происходит в результате непосредственного контакта с инфекционным агентом и может сопровождаться развитием клинических признаков болезни. • Другим способом приобретения активного иммунитета является вакцинация. Введение вакцин не сопровождается развитием клинических симптомов болезни.

Основы иммунизации • В настоящее время создано несколько разновидностей вакцин, используемых для создания протективного иммунного ответа: • живые —ослабленные (аттенуированные) микроорганизмы; • убитые — инактивированные микроорганизмы или их компоненты, обладающие иммуногенностью; обработанные и очищенные продукты жизнедеятельности микроорганизмов (анатоксины — инактивированные токсины).

Основы иммунизации • Существует группа вакцин, основанных на белках, синтезированных с помощью метода рекомбинантных ДНК. • Идеальной вакциной следует считать ту, которая способна вызывать иммунный ответ, идентичный таковому при попадании патогенного микроорганизма, но не сопровождающийся развитием клинических симптомов заболевания или побочных эффектов.

Основы иммунизации Основные требования, предъявляемые к вакцинам Способность обеспечить адекватную презентацию антигена для последующего запуска иммунных реакций. Формирование иммунологической памяти (как Т-, так и В-звена иммунной системы). Образование Т-клеток, специфичных к различным эпитопам из-за: • антигенной вариабельности патогенов; • индивидуальных различий в формировании иммунного ответа по причине выраженного полиморфязма МНС. Для формирования В-клеточной памяти необходима экспрессия антигена на фолликулярных дендритных клетках лимфоидной ткани.

Основы иммунизации • Использование вакцин, содержащих живой патоген, — наиболее эффективный способ индукции иммунного ответа. • Однако использование живых вакцин небезопасно и сопровождается риском развития заболевания. • Инактивация патогенного микроорганизма часто приводит к ослаблению его иммуногенных свойств, что делает вакцины на основе убитых микроорганизмов менее эффективными в создании протективного иммунного ответа.

Основы иммунизации • Иммунитет, генерируемый убитыми вакцинами, даже при их совместном введении с адъювантами, слабее, чем иммунитет, вырабатывающийся в результате вакцинации живыми аттенуированными вакцинами или после перенесённого инфекционного заболевания. • При размножении живых патогенов организм хозяина сталкивается с более высокими концентрациями антигена.

Основы иммунизации • Достижение аналогичной антигенной нагрузки при введении убитых микроорганизмов является трудновыполнимой задачей, так как требует существенного повышения дозы вводимого препарата, а это, в свою очередь, сопряжено с высоким риском развития побочных эффектов. • Кроме того, для установления хорошей Тклеточной памяти (особенно, противовирусной) требуется контакт иммунокомпетентных клеток с заражёнными клетками, что невозможно при вакцинации убитыми вакцинами.

Основы иммунизации • Убитые микроорганизмы не способны инициировать полноценный Т-клеточный иммунный ответ из-за недостаточной степени включения экзогенных антигенов, содержащихся в вакцинах, в механизм презентации. • Иммуногенность убитых вакцин повышают путём одновременного их введения с адъювантами.

Основы иммунизации

Основы иммунизации • Идея использования живых микроорганизмов для создания защитного иммунитета у человека была реализована при создании вакцин против • холеры (Vibrio cholerae), • туберкулёза (Mycobacterium tuberculosis), • брюшного тифа (Salmonella typhi), • жёлтой лихорадки, кори, • эпидемического паротита, • полиомиелита, • краснухи, • ветряной оспы, • аденовирусной и • ротавирусной инфекций.

Основы иммунизации • Все они содержат живые, но ослабленные патогенные микроорганизмы. • Главной целью аттенуации является получение модифицированных микроорганизмов, сохраняющих свойства нативных патогенов и инициирующих развитие иммунного ответа, но не вызывающих заболевания.

Основы иммунизации • Для получения ослабленных штаммов возбудителей применяют метод искусственного мутагенеза с последующим отбором мутантов, направленным на устранение вирулентности. • Однако существует важное обстоятельство, ограничивающее использование живых вакцин — их небезопасность.

Основы иммунизации 1. Использование живых аттенуированных вакцин способно вызвать развитие заболевания в ослабленном организме. Например, у лиц с гипогаммаглобулинемией проведение пероральной иммунизации живым аттеуированным вирусом полиомиелита может привести к развитию заболевания. 2. Не всегда можно отличить эффективно обезвреженные микроорганизмы от патогенных. 3. Существует риск возвращения используемыми штаммами их вирулентности.

Основы иммунизации • Вакцины, содержащие убитые микроорганизмы (возбудители тифа, холеры и столбняка), не способны вызывать клинические симптомы болезни. • Несмотря на инактивацию патогенного микроорганизма или даже его отсутствие, присутствие в составе вакцины его иммуногенных компонентов достаточно для индукции протективного иммунитета.

Основы иммунизации • Так как многие бактерии синтезируют токсины, вызывающие развитие патологических реакций в инфицированном организме, использование вакцин, содержащих обезвреженные токсины, будет способствовать синтезу нейтрализующих антител и препятствовать развитию инфекционного процесса. • Такие вакцины называют токсоидами или анатоксинами.

Основы иммунизации • Слабый ответ иммунной системы на полисахаридные антигены у детей в первые 2— 3 года жизни, обусловленный незрелостью иммунной системы и независимостью иммунного ответа на полисахариды от Т-лимфоцитов, явился предпосылкой для создания конъюгированных вакцин, содержащих комплексы полисахаридов и белков. • Это позволяет усилить иммунный ответ и индуцировать развитие Т- и В-клеточной памяти.

Основы иммунизации • Примерами конъюгированных вакцин являются вакцины против Neisseria meningitidis группы С, некоторых штаммов Strptococcus pneumoniae и Haemophilus influenzae b. • Эффективность конъюгированных вакцин высока. Это подтверждают данные о существенном снижении заболеваемости респираторными инфекциями, вызываемыми Haemophilus influenzae b, у вакцинированных детей.
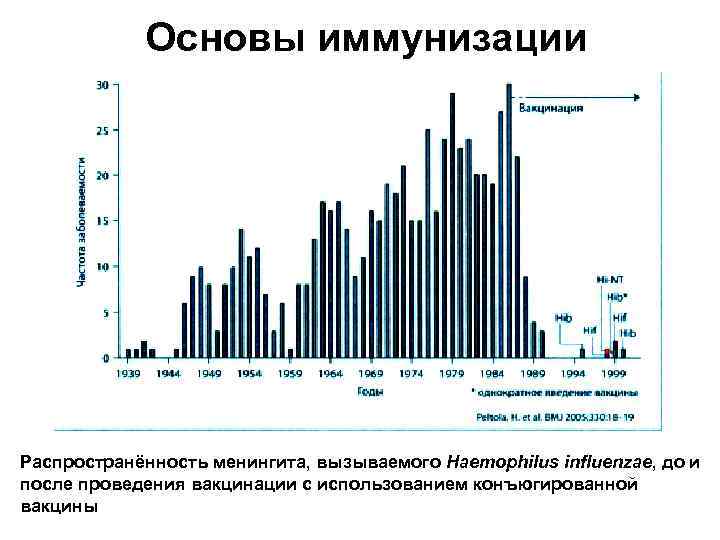
Основы иммунизации Распространённость менингита, вызываемого Haemophilus influenzae, до и после проведения вакцинации с использованием конъюгированной вакцины

Основы иммунизации Адъюванты • Большинство антигенных детерминант, полученных в результате обработки нативного антигена или синтезированных, обладают малой иммуногенностью. • Поэтому для достижения лучших результатов при проведении вакцинации данные антигены вводят в комбинации с веществами, способными усиливать ответ иммунной системы. • Такие вещества называют адъювантами.

Основы иммунизации • Адъюванты широко применяют в клинической и экспериментальной медицине. • В основе действия адъювантов лежит способность к формированию антигенного депо, которое способствует порциальному высвобождению антигена и удлиняет время его контакта с иммунокомпетентными клетками. • Формирование депо обусловлено сорбцией антигена на носителе (квасцах алюминия) или включением антигена в жировую эмульсию (липидные мицеллы).

Основы иммунизации • К наиболее известным адъювантам относят полный и неполный адъюванты Фрейнда, используемые в течение многих лет в экспериментальной медицине. • Адъюванты Фрейнда содержат водножировую эмульсию, вазелиновое масло, ланолин и эмульгатор. • Кроме того, полный адъювант Фрейнда содержит мурамилпептид.

Основы иммунизации • При введении антигена в комплексе с адъювантом происходит стимуляция АПК (дендритных клеток и макрофагов), что приводит к усилению клеточного и гуморального ответа на вводимый антиген. • К сожалению, использование адъюванта Фрейнда ограничено экспериментальными условиями. • Применение данного адъюванта у человека невозможно из-за многочисленных побочных эффектов, обусловленных, в частности, развитием гранулематозного воспаления в селезёнке, печени и коже.

Основы иммунизации • К адъювантам, наиболее широко применяемым у человека, следует отнести алюминиевые квасцы. Например, алюминиевые квасцы присутствуют в противостолбнячной вакцине. • Различные типы адъювантов способны поразному ориентировать развитие ответа иммунной системы на вводимый антиген. • В частности, для достижения Тh 1 опосредованного иммунного ответа антиген целесообразно вводить с адъювантом Фрейнда, в то время как для стимуляции Тh 2 опосредовамного иммунного ответа используют алюминиевые квасцы.
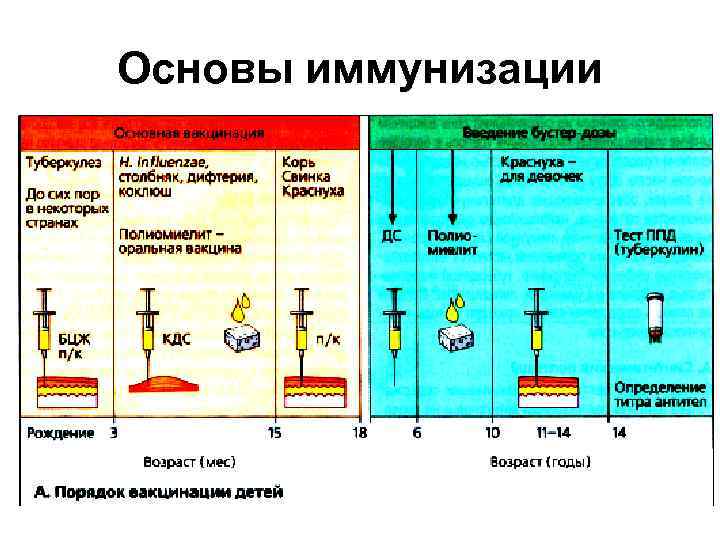
Основы иммунизации
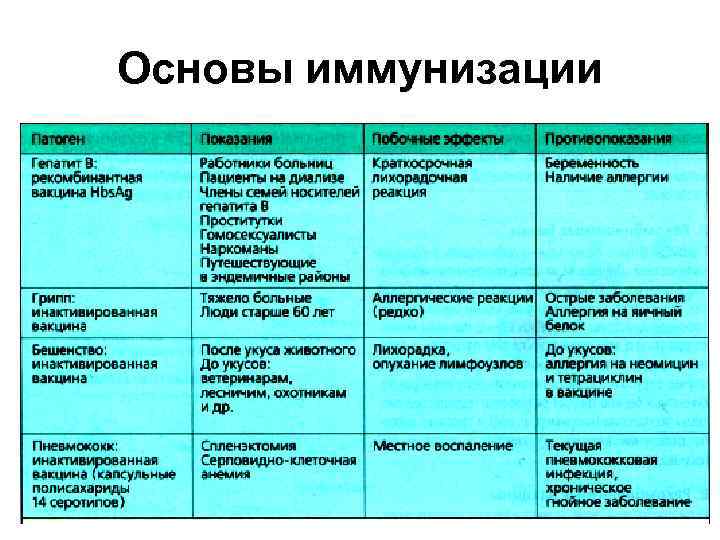
Основы иммунизации

Основы иммунизации

Основы иммунизации Основные принципы профилактической иммунизации • Для профилактики инфекционных заболеваний разработан календарь проведения прививок, готовящих иммунную систему человека к встрече с возбудителями различных инфекционных заболеваний.

Активная иммунизация • Вакцинацию против краснухи проводят женщинам с целью профилактики вредоносного воздействия вируса краснухи на плод в ранний период беременности. Если краснуха развивается в первый триместр беременности, то риск антенатального инфицирования составляет около 80%. • В настоящее время вакцинацию против краснухи проводят всем детям в возрасте 10— 14 лет и серонегативным женщинам, которые имеют риск заражения краснухой, связанный с их профессиональной деятельностью (например, няням, медицинским сёстрам, работающим в детском отделении инфекционного стационара). • Женщины должны предохраняться от беременности в течение 8— 12 недель после вакцинации, поскольку вирус (даже ослабленный) оказывает тератогенное воздействие на плод.

Активная иммунизация • Вакцинапию против туберкулёза проводят всем детям на 3— 7 день жизни, а ревакцинацию — в возрасте 7 и 14 лет в случае получения отрицательной реакции на введение туберкулина. • Однако в настоящее время риск возникновения туберкулёза во многих развитых странах настолько мал, что появилось мнение об отсутствии необходимости введения вакцины БЦЖ без специальных показаний. • Кроме того, при введении вакцины БЦЖ существует риск возникновения БЦЖ-остита, который плохо поддаётся консервативному лечению и оставляет у ребёнка выраженный соматический дефект.

Активная иммунизация • Вакцинацию против дифтерии и столбняка в нашей стране проводят всему детскому населению. Для этого используют адсорбированную коклюшно-дифтерийностолбнячную вакцину (АКДС) и адсорбированную дифтерийно-столбнячную вакцину (АДС). • Для ревакцинации, а также для вакцинации лиц, имеющих противопоказания к введению АКДС и АДС, разрешено использование вакцины АДС-М, содержащей меньшие дозы антигенов.

Активная иммунизация • Пренебрежение правилами вакцинации и большое количество медицинских отводов привели к резкому повышению заболеваемости дифтерией на территории России в 1992— 1994 годах, причём у значительного числа заболевших была диагностирована токсическая форма дифтерии зева. • Это в очередной раз свидетельствует о важности соблюдения всех правил вакцинации.

Активная иммунизация • Пациенты с гипофункцией селезёнки (гипоспленизмом), а также лица с предстоящей спленэктомией входят в группу риска по развитию инфекционных заболеваний, вызываемых пневмококками. • Это обусловлено тем, что именно В-лимфоциты селезёнки вырабатывают Ig. G 2, защищающие организм от пневмококковых антигенов. Поэтому пневмококковая вакцина, используемая в большинстве стран Европы, содержит набор из 23 наиболее часто встречающихся изотипов полисахаридных антигенов. • Введение данной вакцины лицам с гипоспленизмом, а также лицам, которым предстоит спленэктомия, существенным образом (более чем на 60%) снижает вероятность развития инфекционных заболеваний пневмококковой этиологии.

Активная иммунизация • В некоторых странах Европы (например, в Великобритании) проведение вакцинации с использованием пневмококковой вакцины считают целесообразным больным элокачественными лимфопролиферативными заболеваниями (лимфомами), лицам с хронической почечной недостаточностью, ВИЧ-инфицированным лицам, а также пациентам, готовящимся к трансплантации костного мозга. • Из-за недостаточного иммунного ответа на полисахаридные антигены у детей профилактику инфекционных заболеваний пневмококковой этиологии в возрасте 2— 3 лет осуществляют с помощью пневмококковои конъюгированной вакцины, содержащей комплекс белков и полисахаридов.

Активная иммунизация • Проведение вакцинации может сопровождаться развитием побочных эффектов, поэтому для минимизации риска развития осложнений разработаны абсолютные и относительные противопоказания к проведению подобных процедур. • Несмотря на достигнутые успехи в создании вакцин, существует множество опасных и широко распространённых инфекционных заболеваний, для которых вакцины ещё не созданы: ВИЧ-инфекция, малярия, лепра, цитомегаловирусная инфекция и другие.

Активная иммунизация Иммунизация лиц, выезжающих в эндемичные зоны • Выезд в регионы, эндемичные по какомулибо инфекционному заболеванию, сопряжён с риском заражения. • Наряду с основными профилактическими мероприятиями (соблюдение санитарногигиенических норм, химиопрофилактика, использование репеллентов и др. ), для предупреждения ряда инфекционных заболеваний используют вакцинопрофилактику, которую проводят за несколько недель до планируемого посещения эндемичной зоны.

Активная иммунизация • Примером является вакцинопрофилактика • желтой лихорадки, • клещевого энцефалита, • гепатита А, отличающаяся своей безопасностью и высокой (более 86%) иммуногенностью.

Пассивная иммунизация • Временная защита от инфекции может быть достигнута за счёт введения в организм готовых антител (т. е. пассивно). • С этой целью обычно используют препараты человеческого γ-глобулина или высокоочищенный антигенспецифический иммуноглобулин, получаемый от лиц, вакцинированных против конкретного возбудителя несколько недель назад. • Пассивный иммунитет является нестойким и исчезает в течение 6— 8 недель по мере того, как введённые извне антитела выводятся из организма, соединившись с антигеном или в результате нормального метаболизма (период полу-жизни Ig. G составляет 3 -4 недели).

Пассивная иммунизация • Введение препаратов иммуноглобулина человеческого нормального имеет большое значение для лиц с нарушенной иммунореактивностью, особенно лиц с первичными гуморальными иммунодефицитами. • Введение иммуноглобулина человеческого также оправдано лицам, получающим длительное время стероидную терапию, недоношеным детям и детям с выраженной иммуносупрессией с целью краткосрочной профилактики развития ветряной оспы.

Пассивная иммунизация • Введение антигенспецифических нейтрализуюших антител показано в исключительных случаях и проводится по жизненным показаниям. • Несмотря на очевидное преимущество в специфичности, использование моноклональных антител с целью создания пассивного иммунитета пока не нашло широкого применения в практической медицине.

Пассивная иммунизация • Например, применение моноклональных антител к эндотоксину и ФНО-α у больных сепсисом не привело к существенному улучшению клиниколабораторных показателей. • Более того, в группе лиц с септицемией, получавших терапию моноклональными антителами к ФНО- α уровень смертности был достоверно выше, чем в контрольной группе. • Это лишний раз подтверждает точку зрения о том, что несмотря на выраженные провоспалительные свойства ФНО- α, данный цитокин играет важную протективную роль в течении воспалительных реакций.

Создание вакцин нового поколения • Несмотря на значительный прогресс в области профилактики многих инфекционных заболеваний, следует признать, что большинство современных вакцин далеки от совершенства и нуждаются в серьёзной доработке. • Кроме того, для ряда вирусных заболеваний (гепатита С, ВИЧ-инфекции, атипичной пневмонии и др. ) вакцина до сих пор не разработана. • Это является мощным стимулом для создания вакцин нового поколения, эффективных и безопасных.

Вакцины нового поколения • Вакцины, создаваемые на основе полипептидов, - результат специфического расщепления вирусов на отдельные компоненты, обладающие наибольшей иммуногенностью. • Вакцина, имеющая в своём составе лишь незначительную часть вирусного материала, безопасна. Однако иммуногенность такой вакцины относительно невысока. • Известно, что эффективность иммунного ответа зависит от способа подачи чужеродного материала иммунокомпетентным клеткам.

Синтетические пептиды • Синтетические пептиды для вакцинации содержат только эпитолы протективных антигенов и не содержат других частей белка, оказывающих негативное (подавляющее) действие на иммунный ответ, обладающих токсической активностью или способных к перекрестным реакциям с эндогенными пептидами. • Большинство пептидов стимулируют развитие гуморального иммунного ответа, сила которого зависит от соответствующего типа HLA. Оптимальный уровень защиты достигается только у части населения.
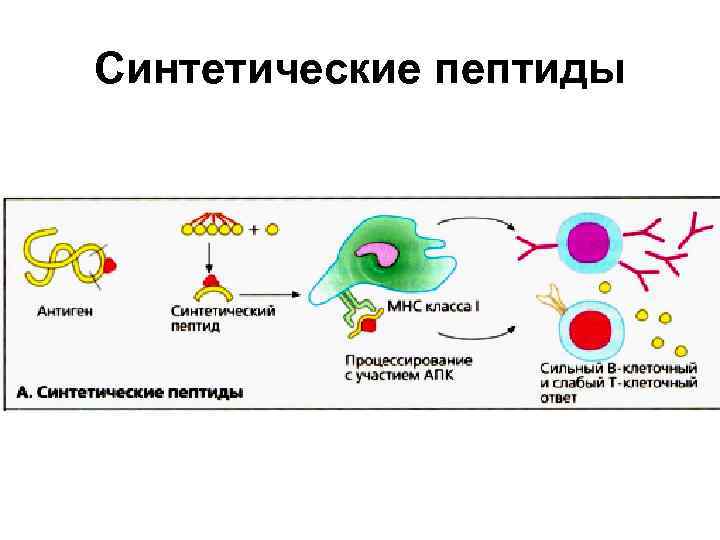
Синтетические пептиды

Рекомбинантные белки • Рекомбинантные белки можно производить в больших количествах. Основным их достоинством является то, что в отличие от классических вакцин они не содержат тех структур патогенов, которые могли бы оказывать побочное действие. • Генноинженерные вакцины можно создавать и в том случае, когда сам патогенный организм трудно или невозможно культивировать (в случае вирусов). • Однако технология получения рекомбинантных белков требует разработки подходящей системы экспрессии (например, Е. соli) и простого способа отделения вакцины от клеток, в которых она произведена.
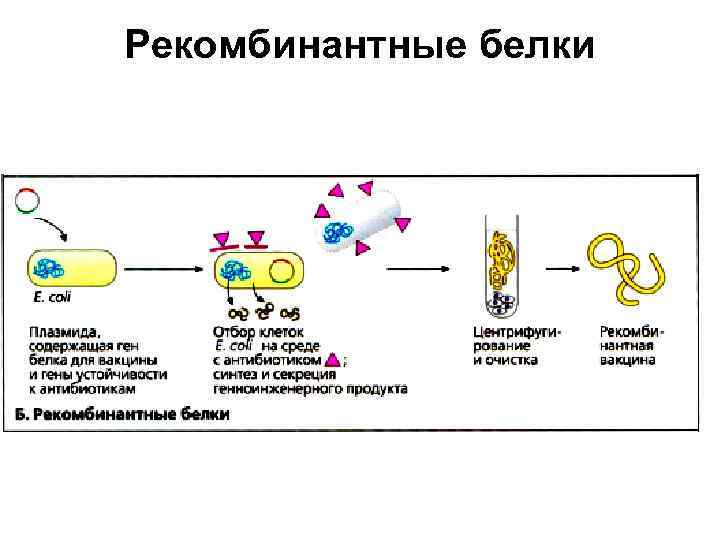
Рекомбинантные белки

Рекомбинантные вакцины • Если рекомбинантный белок не может вызвать адекватного иммунного ответа, особенно Т- клеточного, то возможным выходом из положения является клонирование его гена в подходящем бактериальном носителе (в БЦЖ). • Вместе с антигенами носителя рекомбинантный белок вызовет более сильную защитную иммунную реакцию.
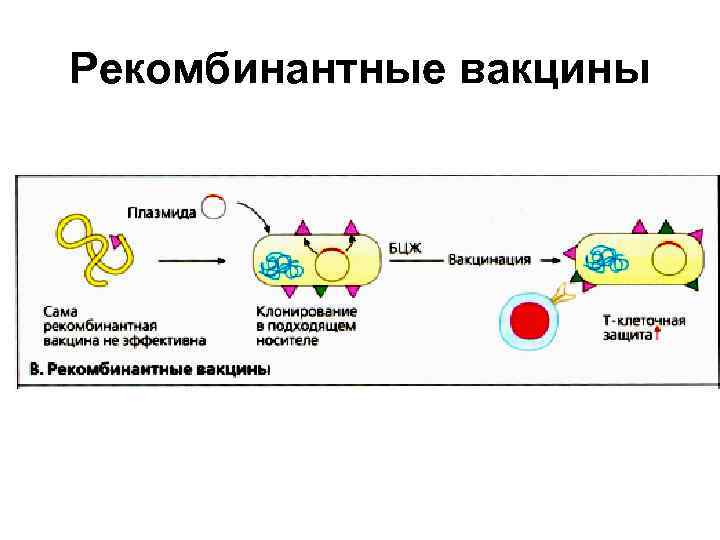
Рекомбинантные вакцины

Делеционные мутанты • Делеция генов, важных для вирулентности или выживаемости патогена в организме хозяина, может лишить патоген болезнетворной активности. • Однако сокращенное время жизни патогена должно быть все же достаточным для того, чтобы вызвать защитную реакцию организма. • -
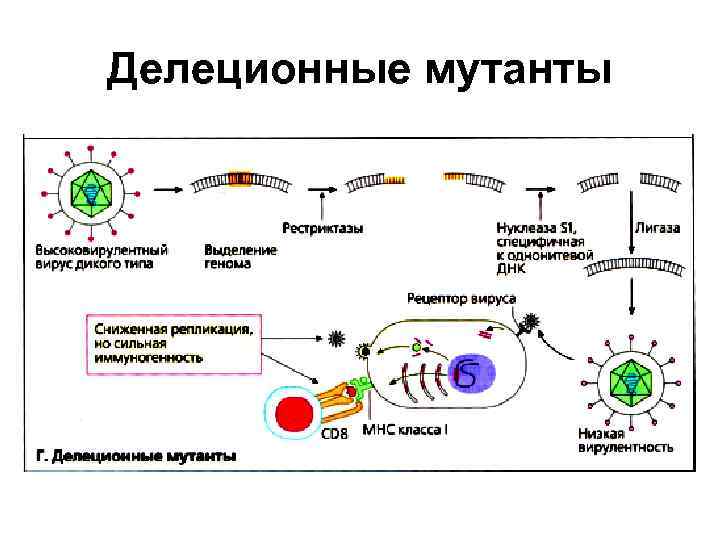
Делеционные мутанты

Очищенная ДНК • Препараты очищенной ДНК, использующиеся для вакцинации, содержат ген, кодирующий антиген патогенного организма, и подходящий промотор. После интеграции в клетку хозяина происходит транскрипция ДНК вакцины, обеспечивающая синтез антигена. Антиген вызывает В-клеточный ответ (при условии, что данный ген содержит последовательность сигнального пептида). • Некоторые антигены могут быть процессированы внутри клетки и представлены на ее поверхности при участии молекул МНС класса 1, что стимулирует Т-клеточный ответ. Тестировение таких вакцин на животных дает обнадеживающие результаты. • Этот метод был не давно предложен для вакцинации против СПИДа. Однако прежде чем такие вакцины можно будет использовать в медицине, следует получить ответы на ряд вопросов. Основной вопрос заключается в дальнейшей судьбе этой ДНК в организме хозяина, а именно, вероятность ее трансформации в вирулентную ДНК, время ее существования в геноме хозяина и способность реплицироваться в организме хозяина.
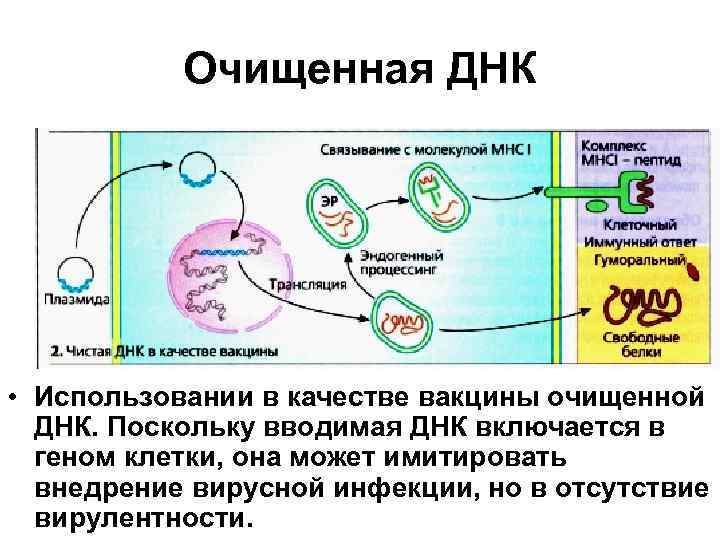
Очищенная ДНК • Использовании в качестве вакцины очищенной ДНК. Поскольку вводимая ДНК включается в геном клетки, она может имитировать внедрение вирусной инфекции, но в отсутствие вирулентности.

Вакцины нового поколения • Наиболее эффективным способом представления чужеродного является его подача на поверхности инфицированных клеток, поэтому для повышения иммуногенности таких вакцин разрабатывают способы внедрения полипептидов в клетку. • Одним из наиболее перспективных подходов к решению данной задачи является конъюгирование полипептидов с мицеллами (например, мицеллами гликозида Quil A), обеспечивающими проникновение антигена внутрь клетки.

Вакцины нового поколения • После идентификации аминокислотной последовательности ДНК (иди РНК), ответственной за синтез иммуногенных вирусных пептидов, существует возможность изолирования генов и их внедрения в плазмидный вектор с помощью соответствующих эндонуклеаз. Наиболее типичным примером рекомбинантной вакцины является вакцина против гепатита В. • Суть создания рекомбинантной вакцины против гепатита В заключается в том, что в генетический материал обычных пекарских дрожжей встраивают ген вируса гепатита В, отвечающий за синтез НВs. Ag. В процессе размножения дрожжей белок-антиген, необходимый для вакцины, растёт «как на дрожжах» .

Вакцины нового поколения • Полученный таким образом антиген экстрагируют из дрожжей, подвергают очистке и смешивают с адъювантом (гидрооксидом алюминия) для усиления эффективности вакцины. • Таким образом, современные рекомбинантные вакцины против гепатита В состоят из одного антигена - НВs. Ag (австралийский антиген). Поскольку антиген расположен на поверхности вируса гепатита В, сформированные вакциной антитела будут атаковать и обезвреживать вирус при его попадании в организм. • Данная вакцина безопасна и эффективна.

Вакцина против СПИДа • Аналогичный подход был использован для создания рекомбинантной вакцины против ВИЧ-1, недавно проходившей клинические испытания — клонировали гены белков gp 120 и gp 160. • К сожалению, данная вакцина оказалась неэффективной, так как антитела, образующиеся к поверхностным белкам ВИЧ-1, не обладают нейтрализующей активностью.

Вакцина против СПИДа Перспективы и препятствия для создания вакцины Клинические испытания некоторых вакцин против ВИЧ-1. • Рекомбинантные субъединичные вакцины. • Вакцина AIDSVAX (Vaxgen Inс. , США), содержащая поверхностный белок вируса (gp 120) - первая вакцина, которая была испытана на людях.

Вакцина против СПИДа • Текущее состояние разработки субъединичных рекомбинантных вакцин: • gp 120 - AIDSVAX производства Vaxgen Inс. , США), - фаза III, • gp 120 - (АLVАС (Авентис Пастер, Франция и Кайрон, США) - фаза II, • р24 - (основной белок оболочки сердцевины вируса) - фаза I.

Вакцина против СПИДа • Живые рекомбинантные вакцины на основе вирусных векторов. • Вакцина на основе вируса птичьей оспы (АLVAC - Авентис Пастер, Франция и Кайрон, США) - II фаза. • Препарат на основе вакцинного вируса натуральной оспы - I фаза.

Вакцина против СПИДа Синтетические пептидные вакцины. • Состоят из небольших, наиболее иммуногенных отрезков белков вируса, являющихся достаточно репрезентативными для формирования иммунного ответа: p 17 (один из белков сердцевины вируса) - I фаза. • Липопептиды - I фаза. • Вакцина, основанная на V 3 (одна из фракций белка gp 120) - I фаза.

Вакцина против СПИДа Основные препятствия на пути создания эффективной вакцины против СПИДа. • Вариабельность вируса иммунодефицита человека. • Слабая нейтрализующая способность большинства антител, вырабатываемых против ВИЧ-1

Вакцины нового поколения • Рекомбинантные вакцины на основе вирусных векторов создают с использованием относительно безвредных вирусов. • Вирусные векторы обеспечивают наиболее эффективную доставку материала в геном клеток. • В качестве векторов используют • альфавирусы: вирус Венесуэльского лошадиного энцефалита, вирус Синдбис и вирус леса Семлики); • аденовирусы (аденовирус-ассоциированный вирус ААV) и • осповирусы (вирус птичьей оспы, вирус куриной оспы, модифицированный вирус натуральной оспы Анкара (modified virus Ankara; МVА).

Вакцины нового поколения • • • К преимуществам таких вакцин относят их относительно низкую себестоимость, простоту введения и стабильность. Однако необходимо учитывать опасность развития побочных эффектов применении вакцин, созданных на базе аттенуированных вирусов.

Вакцины нового поколения • Рекомбинантные вакцины на основе бактериальных векторов создают по аналогичному принципу генетический материал вирусного происхождения встраивают в геном бактерий. • В настоящее время в качестве бактериальных носителей рассматривают представителей родов Salmonella, Shigella, Listeria и др.

Вакцины нового поколения • К наиболее безопасным формам вакцин следует отнести синтетические пептидные вакцины - вакцины, созданные на базе искусственно синтезированных полипептидов. • Пептиды состоят из небольших наиболее иммуногенных отрезков белков вируса, обладающих достаточной репрезентативностью для формирования иммунного ответа. • Основным препятствием для создания таких вакцин является трудность в поиске аминокислотных последовательностей, обеспечивающих иммуногенность патогена.

Вакцины нового поколения • Перспективным направлением в области профилактики инфекционных заболеваний является разработка ДНК-вакцин, основанных на принципе «обнажённой ДНК» . • ДНК-вакцины - очищенные нуклеотидные последовательности ДНК вируса. • Принцип создания таких вакцин заключается в том, что из микроорганизмов получают ДНК, кодирующую протективный антиген, и парентеральным путём вводят её в организм.

Вакцины нового поколения • ДНК проникает в ядро клетки и • обеспечивает экспрессию соответствующего антигена, • который вызывает развитие иммунного ответа. • Вероятно, ДНК может проникать в дендритные клетки, которые напрямую способны активировать Т-хелперы и цитотоксические лимфоциты, обеспечивая формирование гуморального и клеточного иммунитета.

Вакцины нового поколения • ДНК-вакцины для профилактики целого ряда инфекционных заболеваний показали свою эффективность в экспериментальных моделях на животных (вакцина против туберкулёза - на мышах; вакцина против гепатита В- на шимпанзе и т. д. ). • Предстоят клинические испытания нескольких ДНК-вакцин, включая ДНКвакцины для профилактики СПИДа, гриппа, герпеса и Т-клеточной лимфомы.

Вакцины нового поколения • Иммунизация с помощью ДНК-вакцин не сопровождается риском развития основного заболевания. • При применении ДНК-вакцин существует две основные проблемы: • возможное мутагенное действие ДНК, встроенной в геном клеток человека, и • иммунные изменения, которые могут возникнуть при длительной выработке антигена в организме (например, развитие системных аутоиммунных заболеваний вследствие выработки антинуклеарных антител).

Календарь прививок Национальный календарь профилактических прививок в РФ приказ Министерства здравоохранения РФ № 229 от 27. 06. 2001 года. (в ред. Приказов Минздравсоцразвития РФ № 673 от 30. 10. 2007 г)
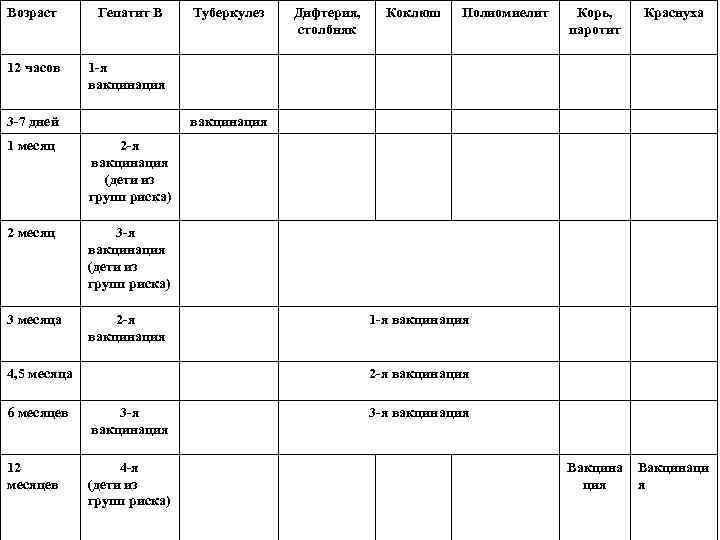
Возраст Гепатит В 12 часов 1 -я вакцинация 3 -7 дней Туберкулез Дифтерия, столбняк Коклюш Полиомиелит Корь, паротит Краснуха Вакцина ция Вакцинаци я вакцинация 1 месяц 2 -я вакцинация (дети из групп риска) 2 месяц 3 -я вакцинация (дети из групп риска) 3 месяца 2 -я вакцинация 4, 5 месяца 1 -я вакцинация 2 -я вакцинация 6 месяцев 3 -я вакцинация 12 месяцев 4 -я (дети из групп риска) 3 -я вакцинация
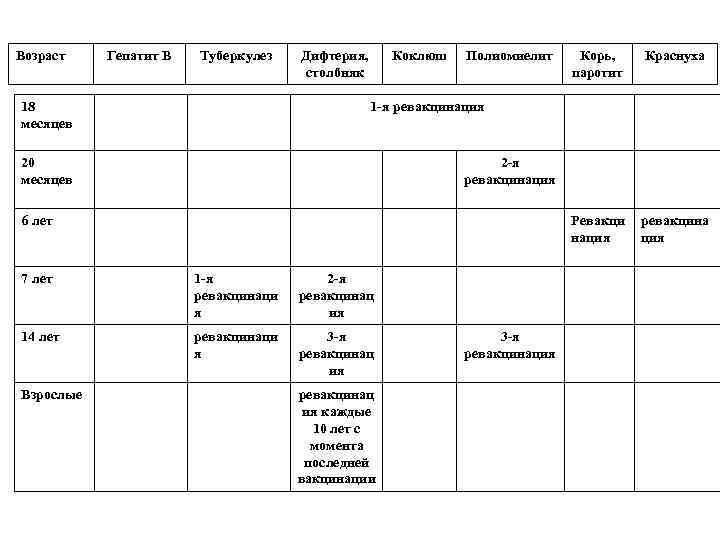
Возраст Гепатит В Туберкулез Коклюш Полиомиелит Краснуха ревакцина ция 1 -я ревакцинация 20 месяцев 2 -я ревакцинация 6 лет 7 лет 1 -я ревакцинаци я 2 -я ревакцинац ия 14 лет ревакцинаци я 3 -я ревакцинац ия Взрослые Корь, паротит Ревакци нация 18 месяцев Дифтерия, столбняк ревакцинац ия каждые 10 лет с момента последней вакцинации 3 -я ревакцинация
Иммунопрофилактика.ppt