2013_Иммунология_ИС_Молекулы ИС.ppt
- Количество слайдов: 114

ИММУНОЛОГИЯ ИММУННАЯ СИСТЕМА (ИС) МОЛЕКУЛЫ ИС Шабан Ж. Г.

ИММУНОЛОГИЯ – наука, изучающая Ø Ø строение, функционирование, эволюцию ИС, способы и механизмы защиты организма от генетически чужеродных веществ с целью сохранения и поддержания гомеостаза, структурной и функциональной целостности организма, его биологической индивидуальности

Задачи иммунологии 1. Исследование структуры молекул, клеток и органов ИС, особенностей функционирования и развития ИС 2. Изучение роли ИС в возникновении и течении заболеваний 3. Разработка методов и средств иммунодиагностики, иммунотерапии и иммунопрофилактики заболеваний

История развития иммунологии Ø возникла в конце 19 в. (1881 г. ) Ø стала самостоятельной наукой в конце 20 в. Этапы развития иммунологии 1. Инфекционный - начало изучения иммунитета к инфекциям • 1796 г. – Дженнер предложил проводить оспопрививание у людей • Пастер – научно обосновал метод Дженнера и сформулировал основной принцип создания живых вакцин (аттенуацию) 2. Клеточно-гуморальный - изучение ИС и механизмов иммунитета • • Мечников – открыл фагоцитоз, разработал теорию клеточного иммунитета Эрлих – разработал теорию гуморального иммунитета 3. Неинфекционный – открытие групп крови и феномена анафилаксии • • • 1901 г. – Ландштейнер открыл изоантигены эритроцитов человека системы ABO 1913 г. – Рише открыл феномен анафилаксии 1940 г. – Ландштейнер и Винер открыли резус-фактор 4. Молекулярно-генетический – изучение структуры Ig, механизмов регуляции функций клеток ИС, генетических основ ИО
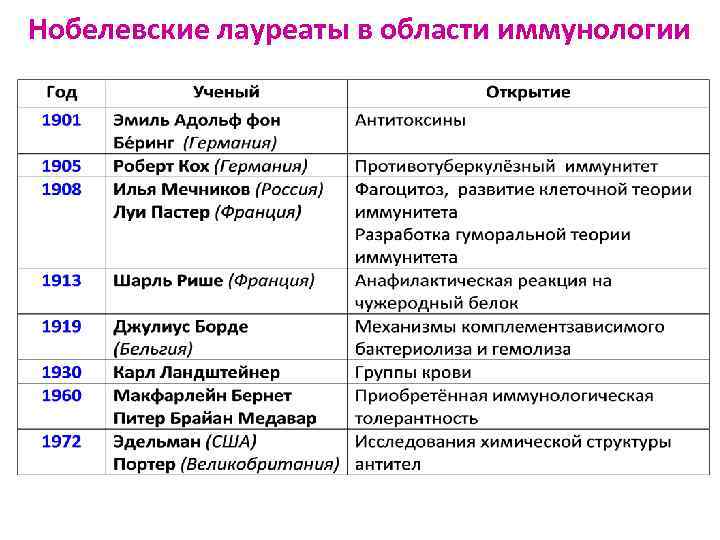
Нобелевские лауреаты в области иммунологии
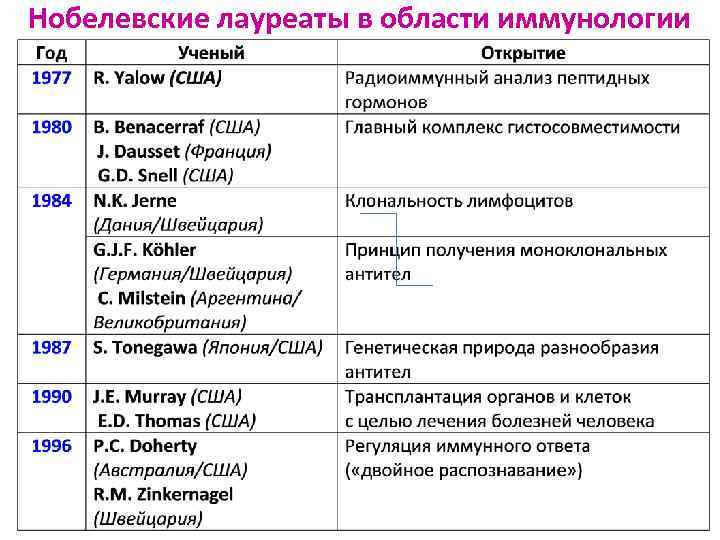
Нобелевские лауреаты в области иммунологии

Методы иммунологии Ø Иммуноморфологический Ø Иммунохимический Ø Иммунобиологические (серологический, аллергологический) Ø Экспериментальный Ø Молекулярно-генетический

Разделы иммунологии Теоретическая (общая, фундаментальная) Ø изучает иммунитет на клеточном (иммуноморфология) и молекулярном (иммунофизиология) уровнях Ø механизмы управления иммунными процессами (иммуногенетика) Ø эволюцию иммунитета (эволюционная иммунология) Прикладная (частная) инфекционная эпидемиологическая иммунопрофилактика клиническая экологическая трансплантационная иммунология репродукции иммунофармакология психоиммунология иммунопатология (аллергология, аутоиммунопатология) Ø онкоиммунология Ø иммунобиотехнология Ø иммуногенотерапия Ø Ø Ø Ø Ø

ИММУННАЯ СИСТЕМА (ИС) – совокупность лимфоидных органов, клеток и молекул, обеспечивающих адаптационные, защитные и репарационные механизмы иммунитета, индивидуальность и целостность организма Функции ИС: Ø Стратегическая - реализация генетической программы индивидуального развития организма от рождения до смерти в условиях чужеродного окружения Ø Тактические: - защита от «чужого» (инфекции, трансплантата) - элиминация модифицированного «своего» (опухолевых, повреждённых, стареющих клеток) - регуляция роста и развития клеток и тканей

Характеристика ИС Ø Представлена лимфоидной тканью Ø Диффузно распределена по организму, некоторые образования находятся в определённых областях Ø Иерархичность (органы, клетки, молекулы в соподчиненном положении) Ø Кооперативность при выполнении функций (ЦНС, ЭС, печень) Ø Интеллектуальность - отличает своё от чужого, распознает образы, надолго запоминает их, быстрее отвечает на их повторное появление Ø Высокая чувствительность Ø Специфичность реагирования Ø Разнообразие реакций и феноменов: - неспецифические механизмы защиты (естественный иммунитет) специфические механизмы защиты (иммунный ответ) иммунологическая память иммунологическая толерантность (неотвечаемость на АГ) иммуноопосредованное повреждение (аллергия, аутоиммунитет)
ИММУННАЯ СИСТЕМА ОРГАНЫ КЛЕТКИ МОЛЕКУЛЫ
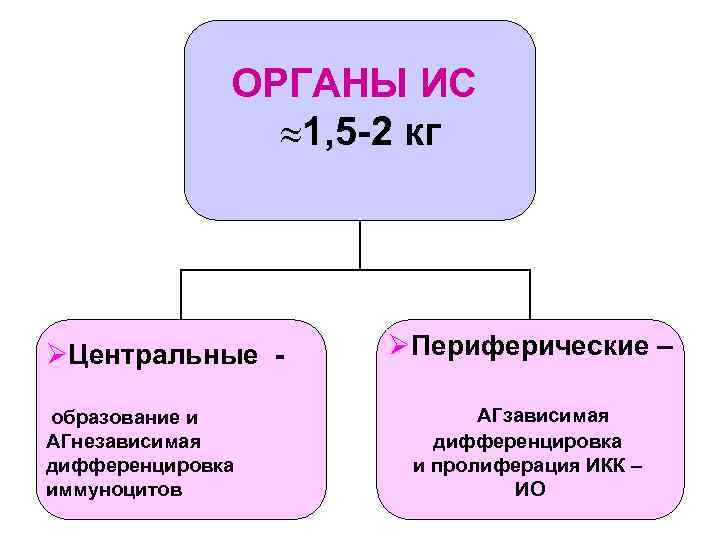
ОРГАНЫ ИС 1, 5 -2 кг ØЦентральные образование и АГнезависимая дифференцировка иммуноцитов ØПериферические – АГзависимая дифференцировка и пролиферация ИКК – ИО
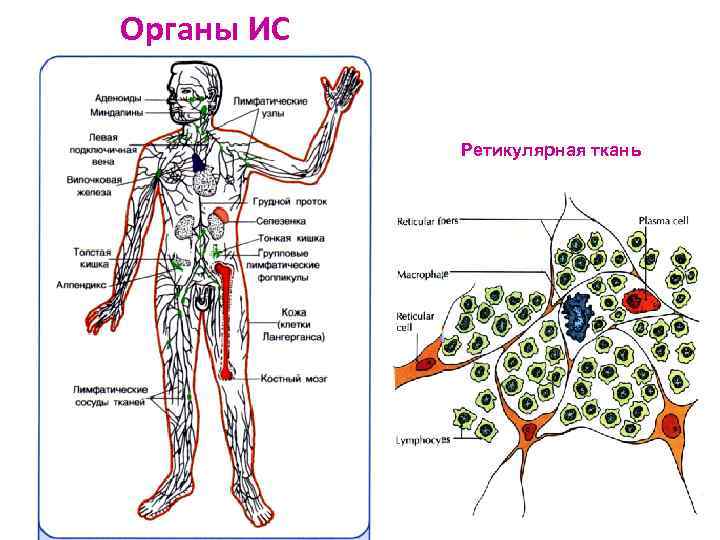
Органы ИС Ретикулярная ткань
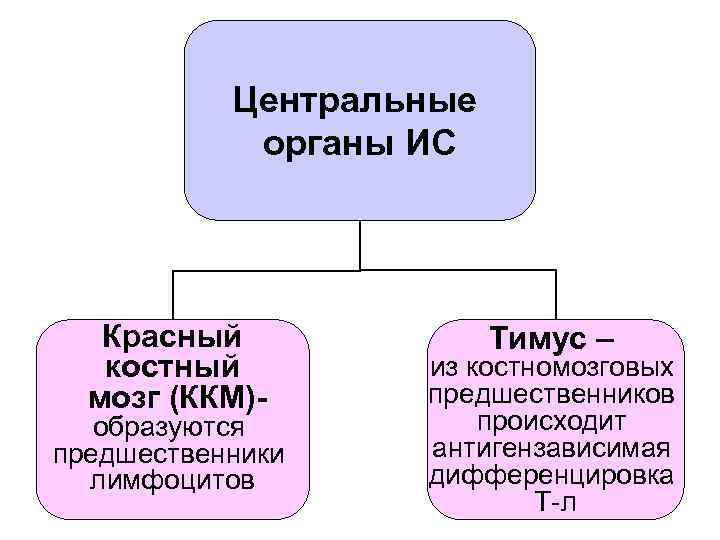
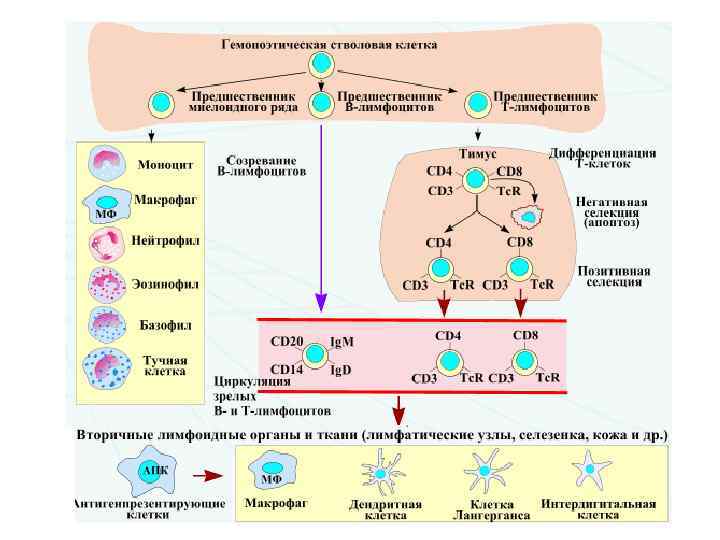
Центральные органы ИС Красный костный мозг (ККМ)- образуются предшественники лимфоцитов Тимус – из костномозговых предшественников происходит антигензависимая дифференцировка Т-л

КРАСНЫЙ КОСТНЫЙ МОЗГ (? аналог фабрициевой сумки птиц) Состоит из ретикулярной стромы и пульпы Строму ККМ образуют: - костные пластинки (трабекулы=Т) - волокна - ретикулярные клетки - эндотелиальные клетки сосудов - жировые клетки (ЖК) - остеобласты и остеокласты К Т Пульпа ККМ - кроветворная ткань, в ней располагаются размножающиеся и дифференцирующиеся элементы эритроидного, миелоидного и мегакариоцитарного ростков В онтогенезе замещается жировой тканью

Функции ККМ Ø Центральный орган кроветворения и лимфопоэза, источник всех клеток ИС (1010 лейкоцитов/день). Предшественница всех клеток ИС – стволовая полипотентная клетка (CD 34+) Ø Осуществляет созревание и дифференцировку: - нейтрофилов, эозинофилов, базофилов - моноцитов - ДК - ЕК - В 2 -л
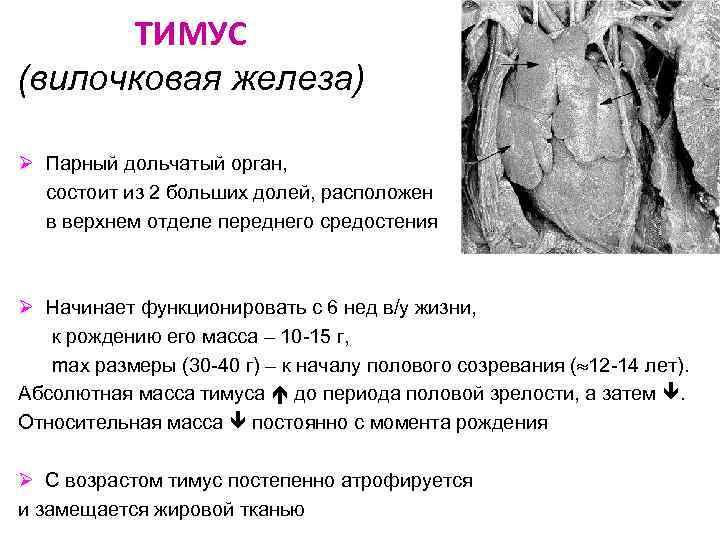
ТИМУС (вилочковая железа) Ø Парный дольчатый орган, состоит из 2 больших долей, расположен в верхнем отделе переднего средостения Ø Начинает функционировать с 6 нед в/у жизни, к рождению его масса – 10 -15 г, max размеры (30 -40 г) – к началу полового созревания ( 12 -14 лет). Абсолютная масса тимуса до периода половой зрелости, а затем . Относительная масса постоянно с момента рождения Ø С возрастом тимус постепенно атрофируется и замещается жировой тканью

Строение тимуса Ø Доли делятся на более мелкие дольки, в каждой - корковая и медуллярная зоны Ø Корковая зона (КЗ) - пролиферация и селекция Т-л Ø Медуллярная зона (МЗ) - внутренний (эпителиальный) слой, сюда из КЗ Лф мигрируют перед выходом в кровь и л/сосуды. На границе зон – заключительные этапы селекции.
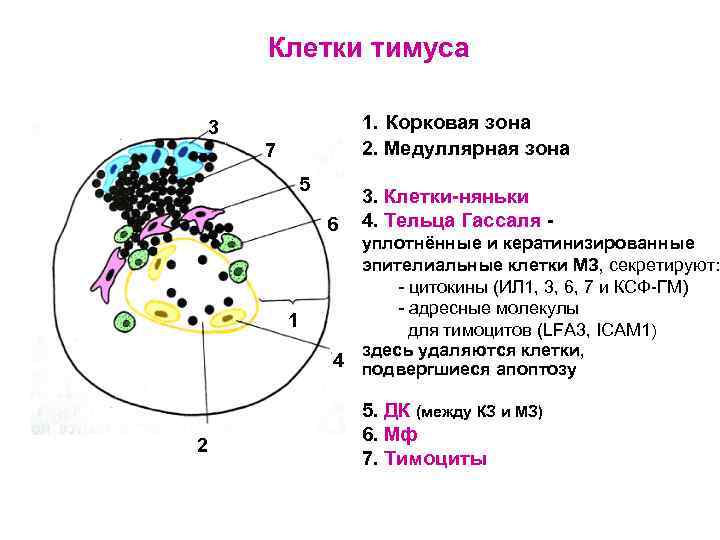
Клетки тимуса 1. Корковая зона 2. Медуллярная зона 3 7 5 6 1 2 3. Клетки-няньки 4. Тельца Гассаля - уплотнённые и кератинизированные эпителиальные клетки МЗ, секретируют: - цитокины (ИЛ 1, 3, 6, 7 и КСФ-ГМ) - адресные молекулы для тимоцитов (LFA 3, ICAM 1) здесь удаляются клетки, 4 подвергшиеся апоптозу 5. ДК (между КЗ и МЗ) 6. Мф 7. Тимоциты
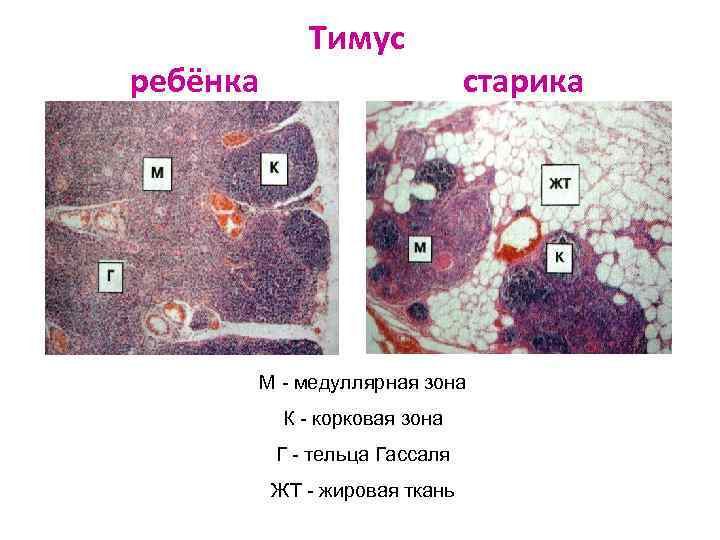
ребёнка Тимус старика М - медуллярная зона К - корковая зона Г - тельца Гассаля ЖТ - жировая ткань

Функции тимуса Ø Т-лимфопоэз - созревание и дифференцировка Т-л (перестройка (реаранжировка) генов TСR, экспрессия рецепторов) под влиянием медиаторов (тимозин, тимопоэтин, тиморин) Ø Селекция Т-л: - отбираются Т-л (СD 4 и СD 8) - апоптоз клеток, специфических к собственным АГ Ø Координация ИС

Периферические органы ИС взаимодействие зрелых неиммунных В- и Т-л с АПК и АГ-зависимая дифференцировка Лф, эффекторные реакции элиминации АГ Лимфоидная ткань: -Миндалин -Диффузные скопления лимфоидной ткани в слизистых оболочках органов ЖКТ, ДС, МПС Селезёнка Л/узлы - Кожи Периферическая кровь
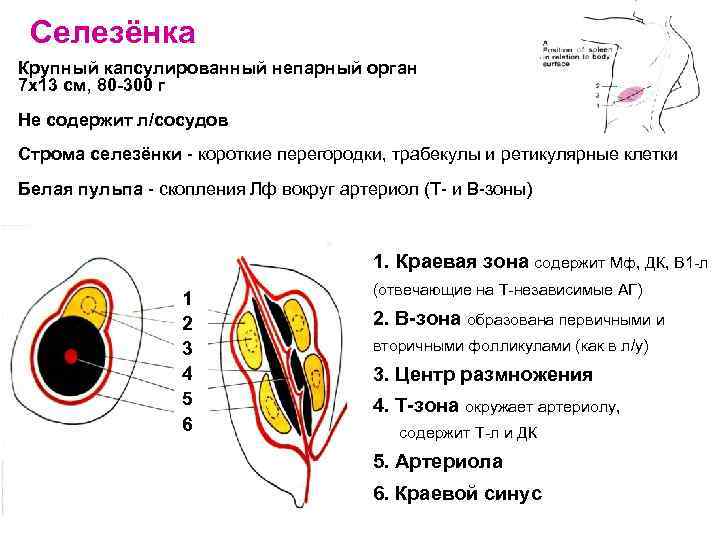
Селезёнка Крупный капсулированный непарный орган 7 х13 см, 80 -300 г Не содержит л/сосудов Строма селезёнки - короткие перегородки, трабекулы и ретикулярные клетки Белая пульпа - скопления Лф вокруг артериол (Т- и В-зоны) 1. Краевая зона содержит Мф, ДК, В 1 -л 1 2 3 4 5 6 (отвечающие на Т-независимые АГ) 2. В-зона образована первичными и вторичными фолликулами (как в л/у) 3. Центр размножения 4. Т-зона окружает артериолу, содержит Т-л и ДК 5. Артериола 6. Краевой синус
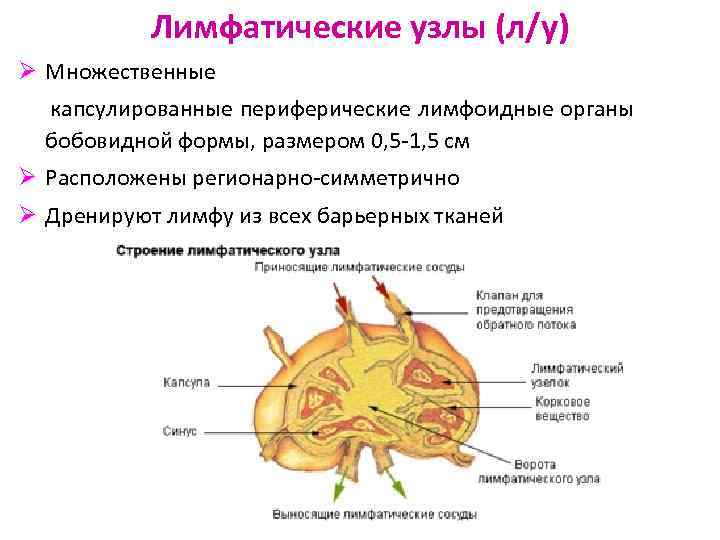
Лимфатические узлы (л/у) Ø Множественные капсулированные периферические лимфоидные органы бобовидной формы, размером 0, 5 -1, 5 см Ø Расположены регионарно-симметрично Ø Дренируют лимфу из всех барьерных тканей
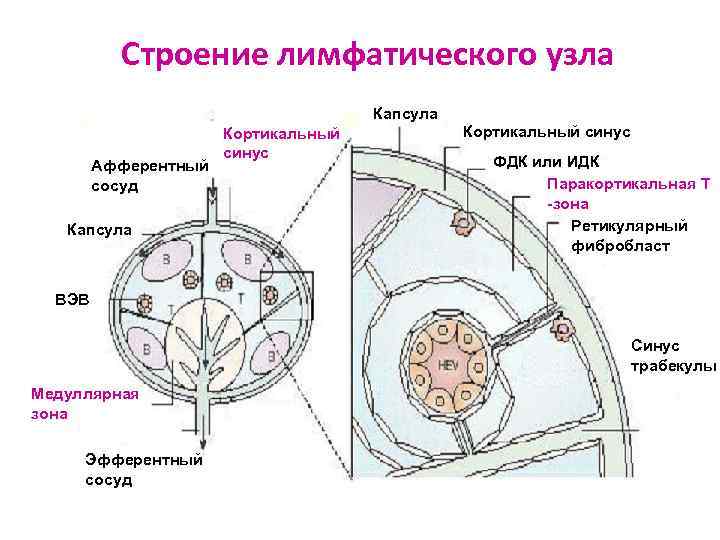
Строение лимфатического узла Капсула Афферентный сосуд Капсула Кортикальный синус ФДК или ИДК Паракортикальная Т -зона Ретикулярный фибробласт ВЭВ Синус трабекулы Медуллярная зона Эфферентный сосуд

Строение лимфатического узла Капсула Афферентный сосуд Капсула Кортикальный синус ФДК или ИДК Паракортикальная Т -зона Ретикулярный фибробласт ВЭВ Синус трабекулы Медуллярная зона Эфферентный сосуд

Строение лимфатического узла Т- и В-зависимые зоны с различным клеточным составом и функциями: Ø Паракортикальная Т-зона - тяжи ткани вокруг ВЭВ граничат с кортикальным синусом, фолликулами и перивенулярными каналами. Здесь ИДК из покровных тканей презентируют АГ Т-л. Ø Кортикальная В-зона разделяется трабекулами на сектора. Функциональная единица В-зоны - фолликул: - первичный фолликул образуется нестимулированными В-л и ФДК крупный герминативный центр - содержит активно делящиеся В-л, ФДК, редкие Т-х. После завершения иммуногенеза ГЦ в размерах. Остаточный фолликул называют вторичным. Ø Медуллярная зона - многочисленные синусы, открывающиеся в эфферентный сосуд. Содержит плазмоциты, Мф и Т-клетки памяти.

Лимфоидная ткань слизистых оболочек: - носоглоточное кольцо Пирогова - ЖКТ (пейеровы бляшки тонкого кишечника, лимфоидные фолликулы аппендикса) - лимфоидная ткань бронхов и бронхиол - лимфоидная ткань МПС - внутриэпителиальные Лф Ø Адрессины обеспечивают хомминг - возвращение Т-л в регионы, где они проходили AГ-зависимую дифференцировку (кожа, респираторная система, ЖКТ, МПС) Ø Стратегию и тип эффекторного ответа определяет тканевое микроокружение

Носоглоточное кольцо Пирогова Ø Миндалины содержат: - В-зоны с первичными и вторичными фолликулами. - Т-зоны, образующиеся вокруг ВЭВ Ø Эпителий в области скопления лимфоидной ткани образует карманы или глубокие щели, облегчая контакт с АГ Ø Вокруг лимфоидных элементов - железистые ткани
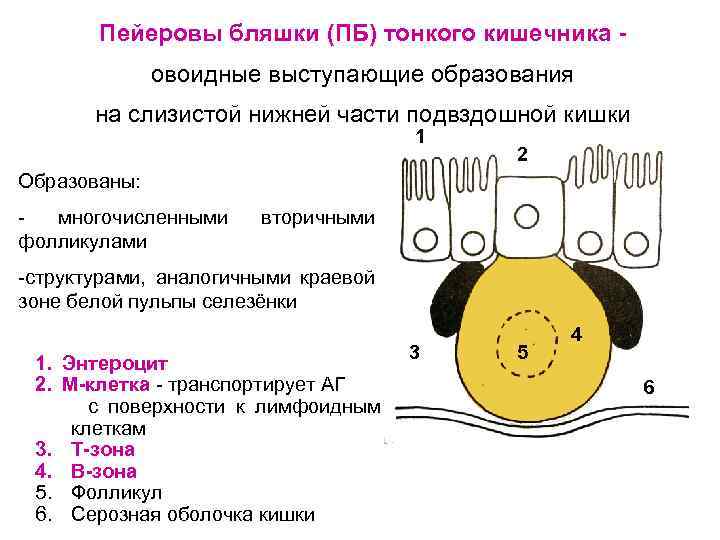
Пейеровы бляшки (ПБ) тонкого кишечника овоидные выступающие образования на слизистой нижней части подвздошной кишки 1 2 Образованы: многочисленными фолликулами вторичными -структурами, аналогичными краевой зоне белой пульпы селезёнки 1. Энтероцит 2. М-клетка - транспортирует АГ с поверхности к лимфоидным клеткам 3. Т-зона 4. В-зона 5. Фолликул 6. Серозная оболочка кишки 3 5 4 6
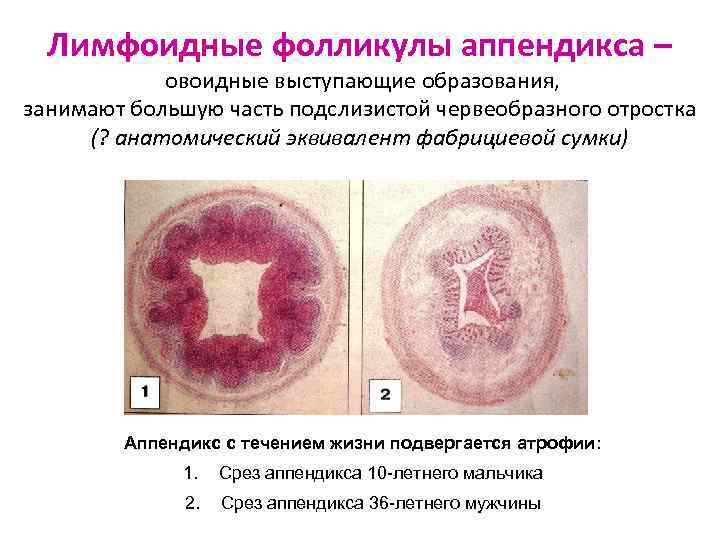
Лимфоидные фолликулы аппендикса – овоидные выступающие образования, занимают большую часть подслизистой червеобразного отростка (? анатомический эквивалент фабрициевой сумки) Аппендикс с течением жизни подвергается атрофии: 1. Срез аппендикса 10 -летнего мальчика 2. Срез аппендикса 36 -летнего мужчины

Лимфоидная ткань, ассоциированная с бронхами (ЛТАБ) Ø Конститутивная ЛТАБ - по ходу бронхов, развивается по АГ-независимому пути Ø Индуцированная ЛТАБ: - развивается при инфекциях респираторного тракта - характеризуется замедленной кинетикой развития - замещает конститутивную ЛТАБ - типичная структура (Т- и В-зоны) - варьирует по выраженности, гиперплазирована при повторных инфекциях заболеваемости

Лимфоидная ткань кожи Ø Эпидермис содержит: - кератиноциты (их функции - барьерная и раннего обнаружения) - небольшое количество CD 8+ Т-л Ø Дерма содержит: - клетки Лангерганса - тучные клетки - небольшое количество Т-клеток памяти, тропных к коже
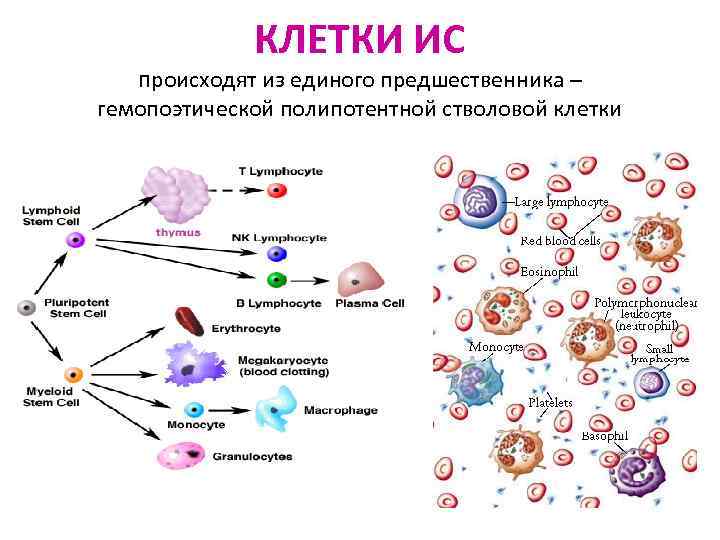
КЛЕТКИ ИС происходят из единого предшественника – гемопоэтической полипотентной стволовой клетки
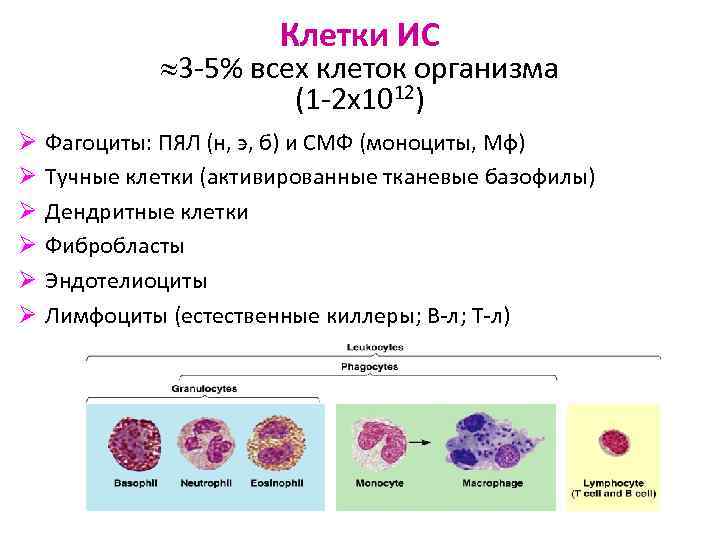
Клетки ИС 3 -5% всех клеток организма (1 -2 х1012) Ø Ø Ø Фагоциты: ПЯЛ (н, э, б) и СМФ (моноциты, Мф) Тучные клетки (активированные тканевые базофилы) Дендритные клетки Фибробласты Эндотелиоциты Лимфоциты (естественные киллеры; В-л; Т-л)

Классификация клеток ИС по функциям Ø ЭФФЕКТОРНЫЕ КЛЕТКИ: - нейтрофилы, эозинофилы, базофилы, тучные клетки, ЕК, Мф - плазматические клетки (дифференцируются из В-л) - цитотоксические Т-клетки CD 8+ (T-к) - эффекторные Т-клетки воспаления CD 4+ (Т-л, ответственные за ГЗТ) Ø АНТИГЕНПРЕЗЕНТИРУЮЩИЕ КЛЕТКИ (АПК): - моноциты, Мф, ДК, В-л, эндотелиоциты, фибробласты, кератиноциты Ø КЛЕТКИ ПАМЯТИ: - Т-клетки памяти CD 8+, Т-клетки памяти CD 4+ - В-клетки памяти, долгоживующие плазматические клетки Ø РЕГУЛЯТОРНЫЕ КЛЕТКИ: - T-индукторы - Тh 1, Тh 2, Тh 3

Особенности ИКК Ø Постоянно рециркулируют по кровотоку, лимфотоку, межтканевым пространствам и секретам Ø Распознают «своё-несвоё» по принципу «лиганд-рецептор» Ø Клональная организация КЛОН - группа Лф, коммитированная к определённому АГ. В организме исходно существуют десятки миллионов клонов Т-л и В-л. После встречи с АГ и в результате ИО коммитированный Лф становится праймированным. Ø Непрерывные реаранжировки в геноме в связи с формированием ИО Ø Запоминают о факте встречи с АГ, при повторной встрече с АГ обеспечивают высокоэффективный ответ на него
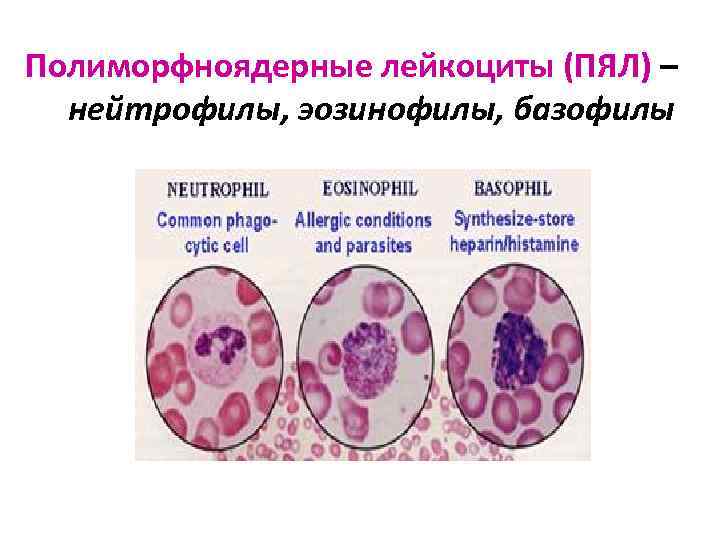
Полиморфноядерные лейкоциты (ПЯЛ) – нейтрофилы, эозинофилы, базофилы
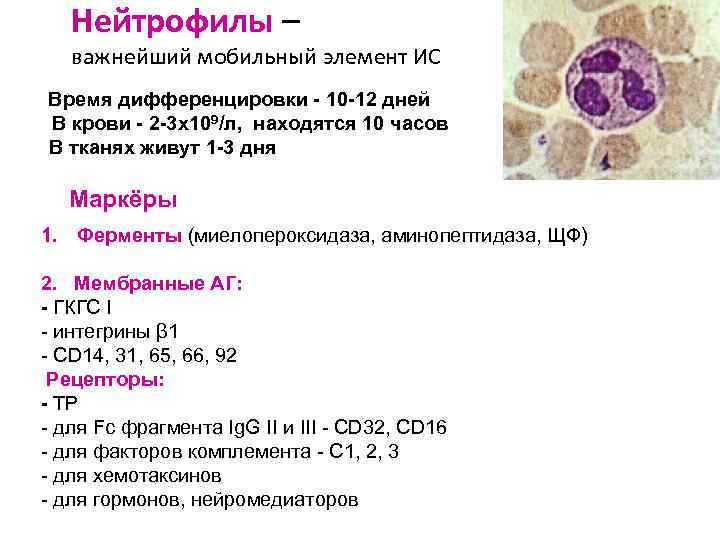
Нейтрофилы – важнейший мобильный элемент ИС Время дифференцировки - 10 -12 дней В крови - 2 -3 х109/л, находятся 10 часов В тканях живут 1 -3 дня Маркёры 1. Ферменты (миелопероксидаза, аминопептидаза, ЩФ) 2. Мембранные АГ: - ГКГС I - интегрины β 1 - CD 14, 31, 65, 66, 92 Рецепторы: - ТР - для Fc фрагмента Ig. G II и III - CD 32, CD 16 - для факторов комплемента - C 1, 2, 3 - для хемотаксинов - для гормонов, нейромедиаторов

Функции нейтрофилов 1. Противомикробная: фагоцитоз 2. Секреторная: - секреция противомикробных веществ - синтез цитокинов и медиаторов (регуляция воспаления) 3. Цитотоксическая: по механизму АЗКЦ 4. Трофическая: - большинство нейтрофилов не покидают ККМ - остальные проникают в ткани и погибают от апоптоза - 1% выходит в ротовую полость ч/з зубо-дёсневые щели
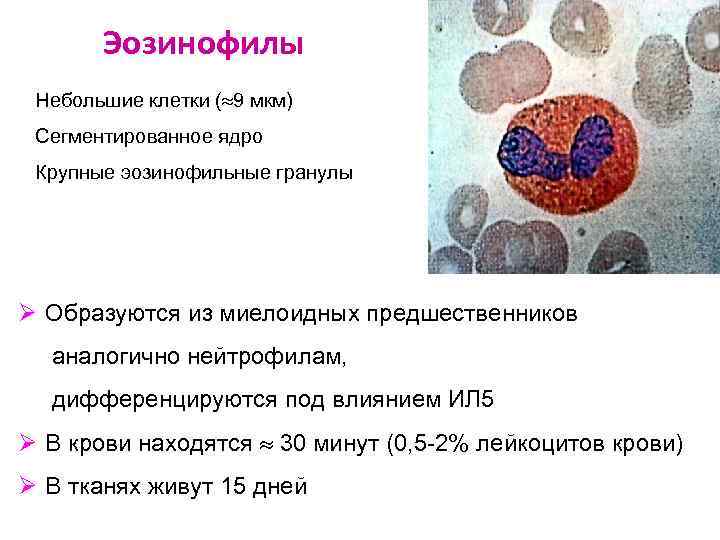
Эозинофилы Небольшие клетки ( 9 мкм) Сегментированное ядро Крупные эозинофильные гранулы Ø Образуются из миелоидных предшественников аналогично нейтрофилам, дифференцируются под влиянием ИЛ 5 Ø В крови находятся 30 минут (0, 5 -2% лейкоцитов крови) Ø В тканях живут 15 дней

Эозинофилы Маркёры: 1. Ферменты: - кислая фосфатаза - арилсульфатаза - эластаза - миелопероксидаза 2. Основной белок 3. Рецепторы: - для Fc фрагментов Ig. G II и Ig. E II (CD 32 и CD 23) - для факторов комплемента - для хемокинов Функции: 1. Внеклеточный цитолиз крупных паразитов, не подлежащих фагоцитозу 2. Регуляция аллергического воспаления 3. Анафилаксия
Базофилы Ø Секретируют биологически активные вещества (гистамин, серотонин и др. ) аллергия (ГНТ медиаторного типа) Ø В тканях превращаются в тучные клетки
Антигенпрезентирующие клетки (АПК)

Функции АПК 1. Обработка АГ: - поглощение АГ АПК - расщепление (процессинг) АГ ферментами в ЦП клетки - связывание образующихся антигенных пептидов с молекулами ГКГС I или II 2. Презентация (представление) АГ Т-х: транспортировка и выход образовавшегося комплекса АГ(пептид)-АГ ГКГС на поверхность мембраны клетки, где АГ (пептид) распознается рецепторами Лф
Моноциты, Мф Моноциты - крупные (15 -25 мкм), ядро неправильной формы Время дифференцировки - 8 -10 дней Находятся в крови 1 -4 дня (2 -8% клеток ПК) мигрируют в ткани Мф Мф крупнее моноцитов, полиморфны, с неправильными очертаниями Всего в организме 1011 В тканях живут 20 дней-7 мес Развитие опосредовано контактными и гуморальными факторами микроокружения: пролиферацию ИЛ 3, ИЛ 6, ГМ-КСФ, М-КСФ пролиферацию TGF

Популяции Мф Ø резидентные – локализуются в определённых тканях: - купферовские клетки печени – 50% популяции всех Мф - альвеолярные Мф - перитонеальные Мф - глиальные клетки ЦНС - мезангиальные клетки почек - остеокласты - Мф соединительной ткани - Мф лимфоидных органов (селезёнки, л/узлов, тимуса, лимфоидных образований слизистых) - дендритные клетки - клетки Лангерганса Ø подвижные – мобилизуются в очаг воспаления

Маркёры Мф 1. Ферменты: - неспецифическая эстераза - β-галактозидаза - 5 -нуклеотидаза - аминопептидаза 2. АГ клеточной поверхности: - ГКГС I и II - интегрины β 1 и β 2 - ICAM 1, 2; CD 31, 45, 40, 86 3. Рецепторы: - для Fc фрагментов Ig. G - CD 64, CD 32, CD 16 - для компонентов комплемента C 1, 2, 3, 4 - для фибрина, гормонов, нейромедиаторов

Свойства Мф Øвысокая подвижность обусловлена - структурой цитоскелета - чувствительностью к хемокинам Øвысокая возбудимость: активируются при различных стимулах, включая прилипание к субстрату Øне имеют собственных рецепторов для распознавания АГ, но фиксация на их поверхности АТ через Fc-рецепторы придает Мф способность к специфическому распознаванию мишеней (АЗКЦ)
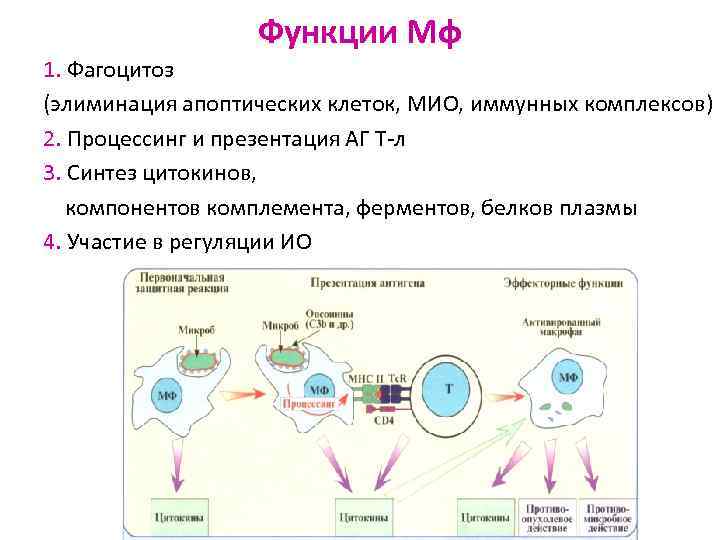
Функции Мф 1. Фагоцитоз (элиминация апоптических клеток, МИО, иммунных комплексов) 2. Процессинг и презентация АГ Т-л 3. Синтез цитокинов, компонентов комплемента, ферментов, белков плазмы 4. Участие в регуляции ИО

Дендритные клетки (ДК) Ø Ветвистые, адгезивные клетки Ø Многочисленные цитоплазматические отростки во много раз площадь мембранной поверхности ДК – зоны взаимодействия с патогенами Ø Диффузно распространены в организме, их много в покровных тканях и лимфоидных органах Ø Продуцируют регуляторные цитокины, определяющие характер и тип ИО (ИЛ 12, INF-α) Ø Основные АПК, более активны, чем Мф в индукции ИО Ø 2 субпопуляции ДК: миелоидные и плазмацитоидные

Миелоидные ДК - костномозгового происхождения; образуются из общего миелоидного гемопоэтического предшественника при действии цитокинов (КСФ-ГМ, ИЛ 4, ФНО ) и при ↑ внутриклеточного ц. АМФ - ДК слизистых связывают, процессируют и презентируют АГ в комплексе с ГКГС II класса Т-л, тем самым инициируя и стимулируя ИО - ДК кожи (клетки Лангерганса) только связывают и процессируют АГ, затем мигрируют в Т-зоны регионарных л/узлов, где превращаются в интердигитальные клетки и с помощью молекул ГКГС презентируют антиген Т-л

Клетки Лангерганса (= белые отростчатые эпидермоциты) Локализация: исчерченный слой эпидермиса Маркёры: Ø АГ ГКГС I и II Ø рецепторы для Fc-фрагмента Ig. G Ø рецепторы для комплемента Ø маркёры незрелых тимоцитов (СD 1 a) и Т-хелперов (СD 4) Ø адгезины Интердигитальные клетки л/узлов Локализация: Т-зоны л/у Маркёры: Ø много АГ ГКГС I Ø нет Fc-рецепторов Ø нет рецепторов для комплемента Функция - презентация АГ: Функции: - не могут связывать и 1. Связывают и обрабатывают процессировать АГ (процессируют) АГ - эффективно презентируют Т-х 2. Не могут презентировать АГ антигенный пептид, (на поверхности нет костимулирующих процессированный на молекул CD 80 и CD 86) предыдущей стадии развития 3. Для презентации АГ мигрируют в активация Т-х и секреция л/узлы и превращаются цитокинов в интердигитальные клетки л/узлов
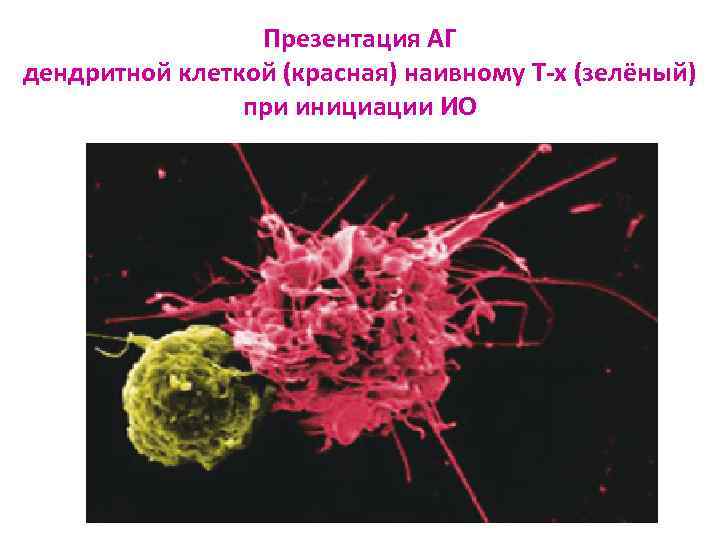
Презентация АГ дендритной клеткой (красная) наивному Т-х (зелёный) при инициации ИО

Плазмацитоидные (фолликулярные) ДК - лимфоидного происхождения - морфологически напоминают плазматические клетки - находятся в первичных и вторичных фолликулах л/у, селезёнки - экспрессируют TР 9 - секретируют в больших количествах интерфероны α и β, а также ИЛ 4 и ИЛ 10, которые переключают дифференцировку Th 0 в Th 2 - не имеют молекул ГКГС II - несут на поверхности комплексы АГ-АТ, презентируют антиген В-л с помощью антительного Fc-рецептора
Естественные (нормальные) киллеры (ЕК, НК, NK) Стадии дифференцировки: • • • стволовая клетка предшественник Лф предшественник тимоцитов предшественник ЕК ЕК ~ 15% лимфоцитов ПК, большие (12 -15 мкм) гранулярные Лф из пула нулевых Лф Накапливаются в тканях: - печень – до 50% всех Лф - лёгкие – 30% - селезёнка – 10%

Маркёры ЕК 1. Маркёры распознавания и киллинга: рецептор лиганд - KIR (CD 158 a-k, z) ГКГС A, B, C - ILT ГКГС G - CD 94 (лектины С-типа) ГКГС Е - NCR, NKG 2 D (CD 159) стрессовые белки 2. Молекулы адгезии - CD 56, CD 57 - интегрины β 1 и β 2 - ICAM 1, CD 44, CD 8, CD 69 Рецепторы: - для Fc фрагмента Ig. G 3 (CD 16) - для цитокинов (стимулируют ЕК - ИЛ 2, ИЛ 18, ИЛ 15, ИЛ 21, INF- угнетает ЕК - ИЛ 3) - для компонентов комплемента - C 3, 4

Цитотоксический механизм ЕК ЕКК выделяют белок перфорин ↓ перфорин связывается с мембраной клетки, формирует в ней трансмембранный канал ↓ ч/з трансмембранный канал в клетку впрыскиваются гранзимы ↓ гранзимы активируют каспазы (сериновые протеазы) в клетке ↓ каспазы активируют эндонуклеазы ↓ - фрагментация ДНК (апоптоз клетки-мишени) - лизис клетки-мишени – прямая клеточно-опосредованная цитотоксичность осуществляется за 1 -2 часа

Функции ЕК обусловлены внеклеточным киллингом клеток, несущих чужеродные антигены 1. Противоопухолевый иммунитет (один ЕК может уничтожить до 40 опухолевых клеток) 2. Противовирусный иммунитет 3. Противогрибковый иммунитет 4. Регуляция ИО
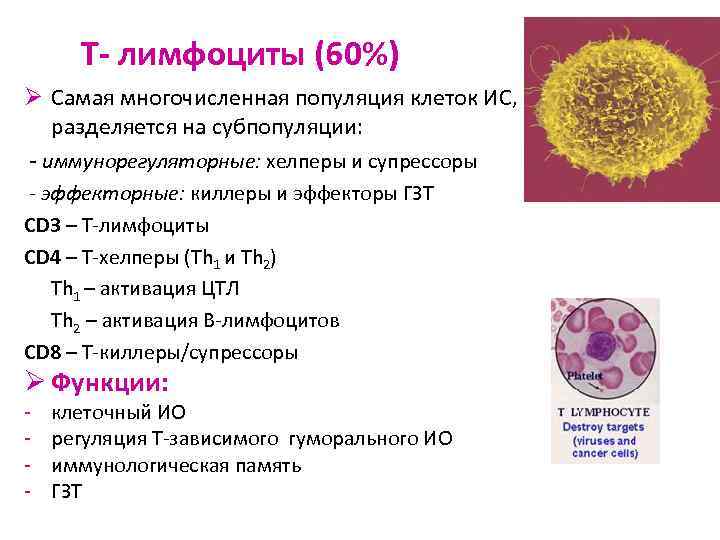
Т- лимфоциты (60%) Ø Самая многочисленная популяция клеток ИС, разделяется на субпопуляции: - иммунорегуляторные: хелперы и супрессоры - эффекторные: киллеры и эффекторы ГЗТ CD 3 – Т-лимфоциты CD 4 – Т-хелперы (Th 1 и Th 2) Th 1 – активация ЦТЛ Th 2 – активация В-лимфоцитов CD 8 – Т-киллеры/супрессоры Ø Функции: - клеточный ИО регуляция Т-зависимого гуморального ИО иммунологическая память ГЗТ
B- лимфоциты (15 -20%) Ø Более гомогенная популяция Ø CD 20 Ø Функции: - гуморальный ИО: имеют АГ-распознающий рецептор - Ig. D, стимулированные В-л (плазмациты) секретируют Ig M, G, A - иммунологическая память - ГНТ
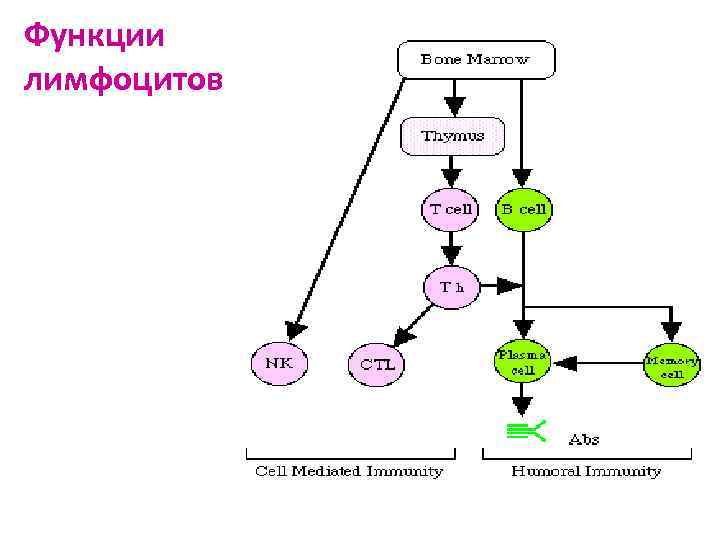
Функции лимфоцитов

Взаимодействия клеток ИС Øс клетками эндотелия (миграция клеток из сосудов в ткани посредством адгезинов) Øс элементами матрикса (миграция в тканях, хемокины) Øнепосредственно между собой (АПК, Т-л, В-л) Øдистантно между собой (посредством цитокинов) Øмежсистемно (нейро-эндокринная регуляция ИС)
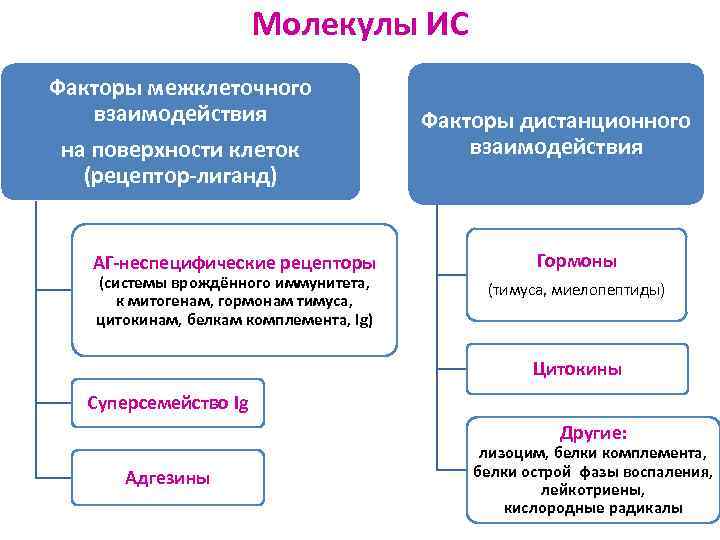
Молекулы ИС Факторы межклеточного взаимодействия на поверхности клеток (рецептор-лиганд) АГ-неспецифические рецепторы (системы врождённого иммунитета, к митогенам, гормонам тимуса, цитокинам, белкам комплемента, Ig) Факторы дистанционного взаимодействия Гормоны (тимуса, миелопептиды) Цитокины Суперсемейство Ig Другие: Адгезины лизоцим, белки комплемента, белки острой фазы воспаления, лейкотриены, кислородные радикалы

Рецепторы системы врождённого иммунитета (связанные с мембраной фагоцитов, TOLL-рецепторы) Ø Рецепторы для распознавания микроорганизмов - результат эволюции, закреплены наследственно Ø Относятся к различным семействам биомолекул Ø Широко специфичны Ø Экспрессированы на эпителиоцитах и всех клетках системы врождённого иммунитета Ø При активации - быстрый эффекторный ответ: - уничтожение, лизис, фагоцитоз - индукция воспаления - организация специфического ИО

TOLL - рецепторы (ТР) Ø трансмембранные гликопротеиды Ø на мембранах клеток обнаружено 11 типов TР Ø на нейтрофилах и Мф значительно экспрессирован ТР 1 Ø реагируют на патогенные МИО Ø специфичны к определённым группам МИО, лиганды к TР – ПГ, тейховые кислоты, ЛПС, полипептиды

Лиганды некоторых TOLL - рецепторов TOLL рецептор TР 2 Лиганды ЛПС, липотейхоевая кислота Пептидогликан Липопептиды микоплазм Клеточная стенка дрожжей (зимозан) TР 3 Двуцепочечная РНК TР 4 ЛПС Липотейхоевая кислота Белок теплового шока TР 5 Флагеллин TР 6 Полипептиды микоплазм, дрожжей (зимозан) TР 9 Бактериальные олигонуклеотиды

Результат активации TOLL - рецепторов При распознавании лиганда в клетке активируются гены, отвечающие за синтез: - противовоспалительных цитокинов - защитных молекул - факторов, блокирующих апоптоз Иммунная клетка активируется и обнаруживает МИО/ повреждение

Суперсемейство иммуноглобулинов Ø Более 70 молекул Ca 2+ - независимых трансмембранных гликопротеинов, сходны с молекулой Ig: имеют хотя бы один консервативный (С) Ig-домен из 70 -100 аминокислот; на внеклеточной стороне имеют Ig-подобные повторы; на цитоплазматической стороне имеют разное строение, включаются в клеточную сигнализацию, связываются с цитоскелетом или секретируются Ø Участвуют в неконтакной межклеточной адгезии: - распознавании - воспалении - миграции лейкоцитов ч/з стенки сосудов
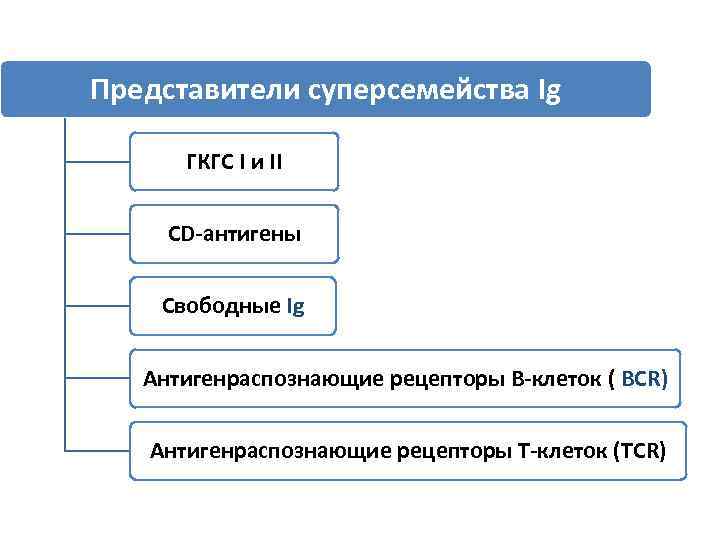
Представители суперсемейства Ig ГКГС I и II CD-антигены Свободные Ig Антигенраспознающие рецепторы В-клеток ( ВCR) Антигенраспознающие рецепторы Т-клеток (TCR)

Главный комплекс гистосовместимости (ГКГС) = МНС (маjor histoсоmpatibility complex) = НLА (human lеucocyte antigens) Система АГ, обеспечивающая: 1) иммунологическую индивидуальность человека и играет определяющую роль в судьбе трансплантата Каждый класс генов имеет несколько локусов, в каждом локусе - много аллельных вариантов строгая индивидуальность набора АГ у каждого человека (возможно > 400 млн наборов вариантов) 2) межклеточные взаимодействия и генетический контроль ИО 3) регулирование эмбриогенеза
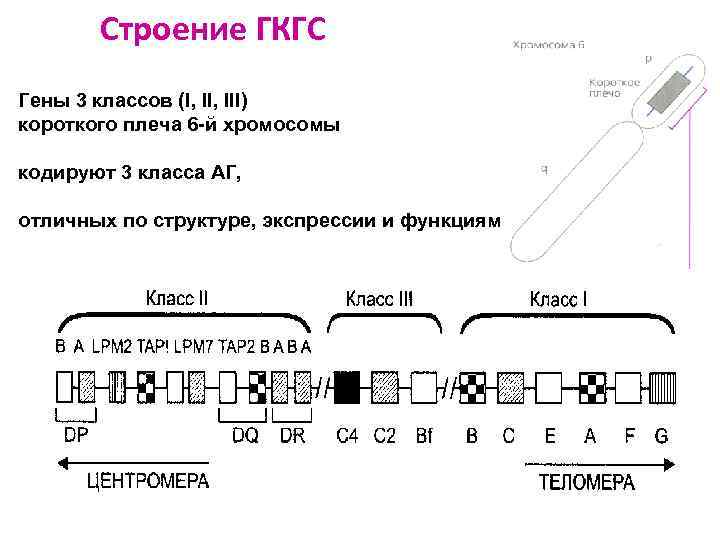
Строение ГКГС Гены 3 классов (I, III) короткого плеча 6 -й хромосомы кодируют 3 класса АГ, отличных по структуре, экспрессии и функциям

Строение молекулы ГКГС I Ø Трансмембранный гликопротеид Ø Одна тяжёлая цепь содержит 3 внеклеточных домена (α 1, α 2, α 3); между α 1 и α 2 доменами - борозда для пептида Ø Тяжёлая цепь нековалентно связана с молекулой β 2 -микроглобулина, он: - узнаёт и связывает пептид - обусловливает транспорт молекул ГКГС I к мембране клетки и их экспрессию Ø Трансмембранный фрагмент Ø Цитоплазматический хвост Мембрана клетки Цитоплазма

Экспрессия и функции молекул ГКГС I Экспрессия: все ядерные клетки Функции: - локусы В, С, А (классические) кодируют трансплантационные АГ - локусы F, G, E кодируют молекулы, участвующие в презентации внутриклеточных АГ CD 8 -лимфоцитам
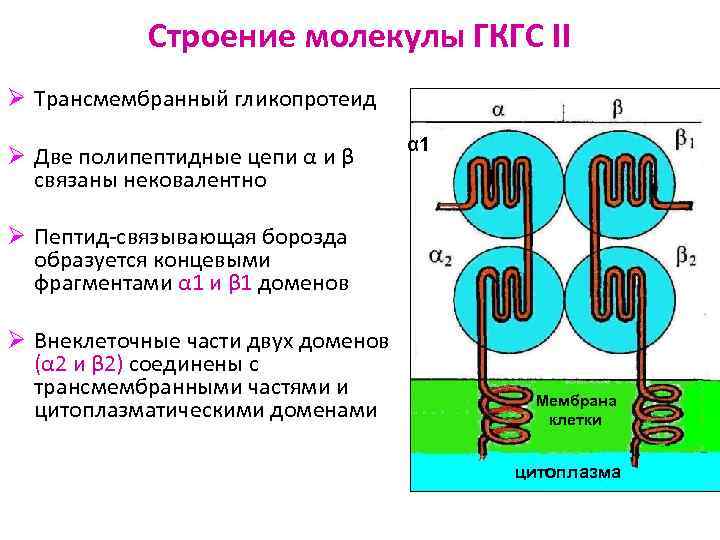
Строение молекулы ГКГС II Ø Трансмембранный гликопротеид Ø Две полипептидные цепи α и β связаны нековалентно α 1 Ø Пептид-связывающая борозда образуется концевыми фрагментами α 1 и β 1 доменов Ø Внеклеточные части двух доменов (α 2 и β 2) соединены с трансмембранными частями и цитоплазматическими доменами Мембрана клетки цитоплазма Цитоплазма

Экспрессия и функции молекул ГКГС I I Экспрессия: ИКК, активированный эпителий и эндотелий Функции: - локусы DR, DP, DQ (классические) кодируют трансплантационные АГ и молекулы, участвующие в презентации внеклеточных АГ CD 4 -лимфоцитам - функция других генов – вспомогательная
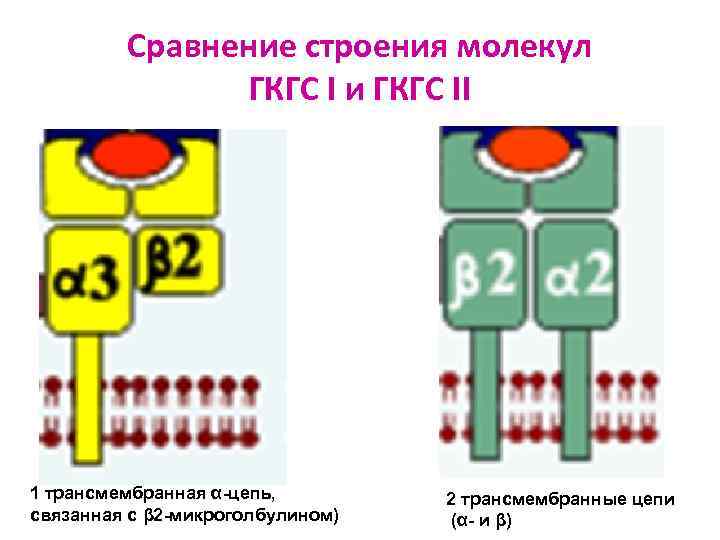
Сравнение строения молекул ГКГС I и ГКГС II 1 трансмембранная α-цепь, связанная с β 2 -микроголбулином) 2 трансмембранные цепи (α- и β)
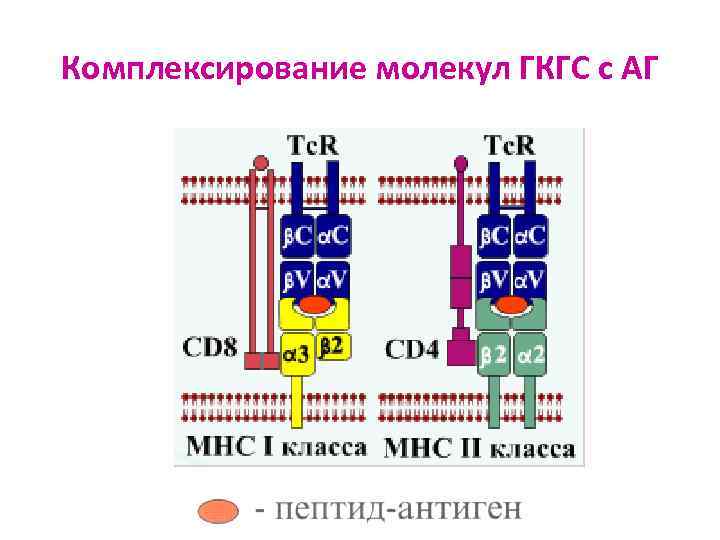
Комплексирование молекул ГКГС с АГ

Строение ГКГС III Расположен между ГКГС I и ГКГС II Включает гены: - кодирующие некоторые белки системы комплемента (С 2, С 4, B) - контролирующие активность ферментов цитохрома (CYP 21) - теплового шока (HSP 70) - ФНО (TNF) АГ ГКГС III не участвуют в презентации АГ

Связь ГКГС с заболеваниями Ø Наличие определённых АГ ГКГС (особенно локусов А, В и DR) обусловливает предрасположенность к аллергии, аутоиммунным заболеваниям, инфекциям: - анкилозирующий спондилоартрит (болезнь Бехтерева) - В 27 - СКВ - B 8 - псориаз - C 6 - врождённые аномалии сердца - A 2 - рассеянный склероз - DR 2

CD-антигены (=CD-молекулы, cluster of differentiation) рецепторы на мембранах клеток ИС Ø Гликопротеины Ø Известно 250 СD антигенов, обозначаемых буквами CD и цифрами (СD 1 и т. д. ) Некоторые CD-антигены - маркёры определённых типов клеток Ø Нoменклатура CD позволяет идентифицировать клетки по происхождению, стадии дифференцировки, функциональному состоянию Ø Проводят сигнал в ЦП клетки, что приводит к ее активации, супрессии или апоптозу Ø Обеспечивают взаимодействие между клетками, с цитокинами, комплементом, молекулами гормонов
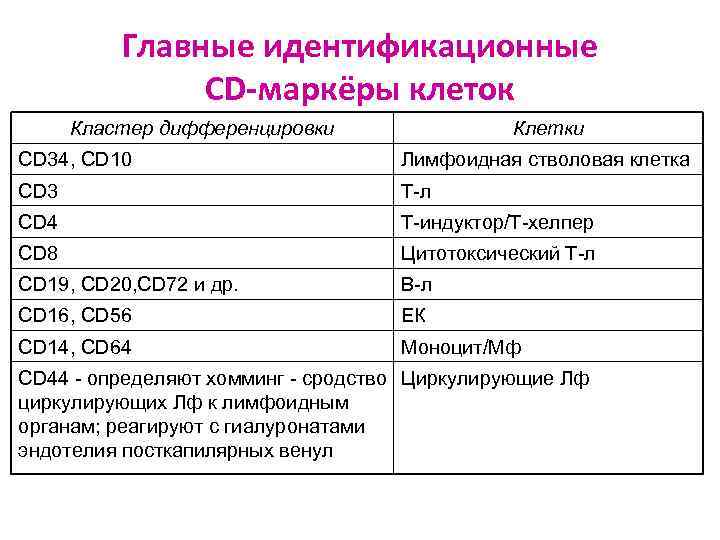
Главные идентификационные CD-маркёры клеток Кластер дифференцировки Клетки CD 34, CD 10 Лимфоидная стволовая клетка CD 3 T-л CD 4 Т-индуктор/Т-хелпер CD 8 Цитотоксический Т-л CD 19, CD 20, CD 72 и др. B-л CD 16, CD 56 ЕК CD 14, CD 64 Моноцит/Мф CD 44 - определяют хомминг - сродство Циркулирующие Лф циркулирующих Лф к лимфоидным органам; реагируют с гиалуронатами эндотелия посткапилярных венул

Адгезины Ø Постоянно экспрессированы на мембранах лейкоцитов, эндотелиоцитов, эпителиоцитов или формируются в процессе ИО Ø Основа реагирования – прилипание за счет сил физико-химических взаимодействий Ø Обеспечивают прямые контакты между клетками ИС и лигандами; молекулы ICAM (intercellular adhesion molecules) ICAM-1, ICAM-2, LFA-3, VCAM-1 Ø Играют ключевую роль в проникновении клеток ИС в ткани

Группы адгезинов Муцины (=васкулярные адрессины) Селектины Интегрины Кадгерины Рецепторы к ФНО и к фактору роста нервов (=молекулы, опосредующие апоптоз)
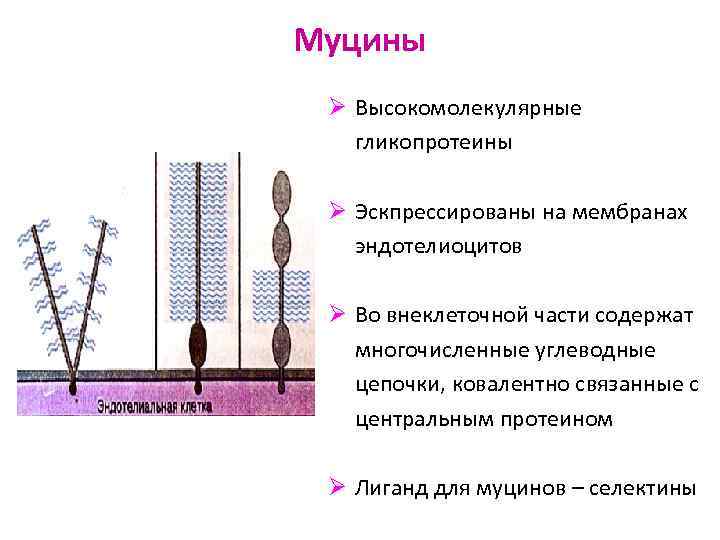
Муцины Ø Высокомолекулярные гликопротеины Ø Эскпрессированы на мембранах эндотелиоцитов Ø Во внеклеточной части содержат многочисленные углеводные цепочки, ковалентно связанные с центральным протеином Ø Лиганд для муцинов – селектины
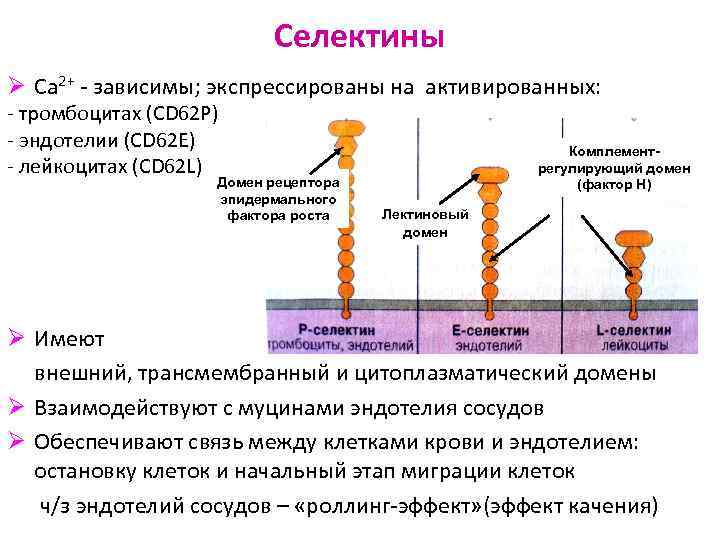
Селектины Ø Ca 2+ - зависимы; экспрессированы на активированных: - тромбоцитах (CD 62 P) - эндотелии (CD 62 E) - лейкоцитах (CD 62 L) Домен рецептора эпидермального фактора роста Комплементрегулирующий домен (фактор Н) Лектиновый домен Ø Имеют внешний, трансмембранный и цитоплазматический домены Ø Взаимодействуют с муцинами эндотелия сосудов Ø Обеспечивают связь между клетками крови и эндотелием: остановку клеток и начальный этап миграции клеток ч/з эндотелий сосудов – «роллинг-эффект» (эффект качения)

Интегрины Ø Ca 2+ или Mg 2+ - зависимы (3 -4 связывающих ионы домена на -цепи); экспрессированы в очень высоких концентрациях: - на мембранах Т-л, моноцитов, Мф, ДК, нейтрофилов - на компонентах внеклеточного матрикса Ø Трансмембранные гетеродимеры – 2 цепи ( и β) связаны с матриксом 14 типов -цепей и 9 типов β-цепей образуют 20 разных гетеродимеров 3 основных семейства (по β-цепям): - β 1 - связь с внеклеточным матриксом (фибронектином, коллагеном) - β 2 - адгезия к эндотелию сосудов или между собой - β 3 - склеивание лейкоцитов и тромбоцитов Ø Имеют внешний, трансмембранный и цитоплазматический домены

Активация интегринов СИГНАЛ ИЗ ВНЕШНЕЙ СРЕДЫ: внешний домен интегрина связывается с лигандом изменение конформации цитоплазматического домена взаимодействие цитоскелета и сигнальных молекул, экспрессия генов МОЛЕКУЛЯРНЫЙ СИГНАЛ ИЗ КЛЕТКИ изменение конформации цитоплазматического домена изменение конформации внеклеточного лигандсвязывающего участка сродства к лиганду
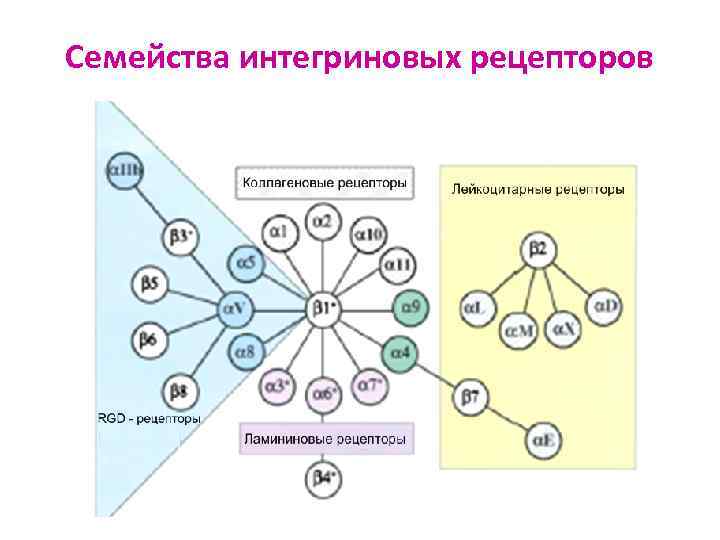
Семейства интегриновых рецепторов

Кадгерины Ø Трансмембранные гликопротеины; на внешней стороне имеют 5 повторов, (3 из них связывают Ca 2+, без Ca 2+ - протеолиз); на цитоплазматической стороне взаимодействуют с белками катенинами и связывают актин Ø Тканеспецифические адгезины, обеспечивают адгезию между клетками одного типа; обуславливают целостность тканей Ø 3 типа: E- кадгерин (эпителий) N- кадгерин (нейрон) P- кадгерины (плацента) Ø На ИКК не обнаружены
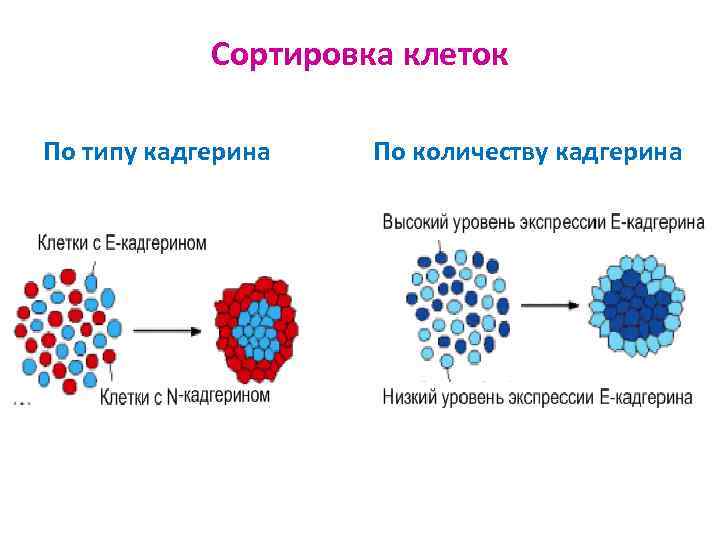
Сортировка клеток По типу кадгерина По количеству кадгерина

ЦИТОКИНЫ Ø Группа низкомолекулярных (5 -50 к. Да) гормоноподобных растворимых биоактивных полипептидов или белков Ø Быстро синтезируются после стимуляции, секретируются активированными клетками ИС (монокины, лимфокины) Ø Большинство цитокинов не синтезируется клетками вне воспалительной реакции и ИО Ø Активны в очень низких концентрациях (10 -11) Ø Регуляторы межклеточных взаимодействий иммунной, кроветворной, нервной и эндокринной систем Ø Обладают эффекторными свойствами – факторы роста, активации, дифференцировки, прролиферации клеток Ø Синтез цитокинов прекращается за счёт различных механизмов ауторегуляции

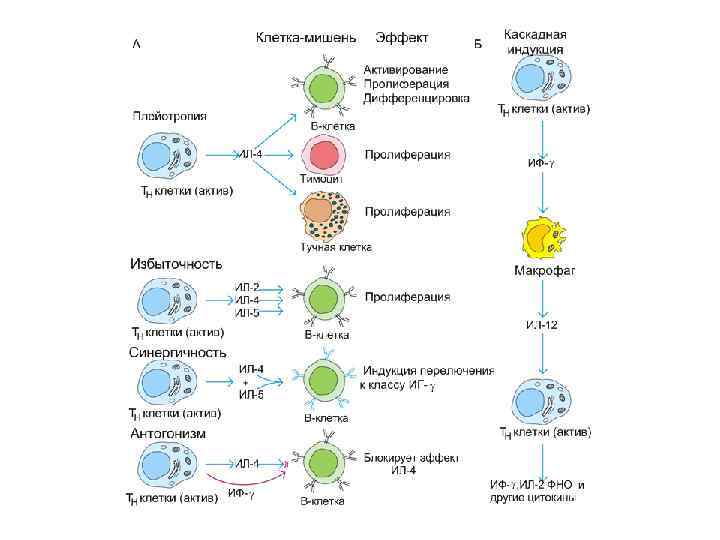
Принципы действия цитокинов Ø Один и тот же цитокин может продуцироваться различными клетками в разных органах Ø Плейотропность биологического действия (=полифункциональная активность): один и тот же цитокин может действовать на многие типы клеток, вызывая различные эффекты в зависимости от вида клеток-мишеней Ø Эстафетный: действие цитокина на клетку индуцирует цитокиновый каскад (синтез ею других цитокинов) Ø Взаимозаменяемость биологического действия (=перекрывающиеся функции): разные цитокины могут вызывать один и тот же биологический эффект или обладать похожей активностью

Механизмы действия цитокинов Ø Интракринный — внутри клетки-продуцента Ø Аутокринный — на клетку, синтезирующую и секретирующую данный цитокин Ø Паракринный — на клетки, расположенные около клеткипродуцента (в очаге воспаления или в лимфоидном органе) Ø Эндокринный — дистантно на клетки любых органов и тканей после попадания цитокина в циркуляцию (напоминает действие гормонов)

Взаимодействие цитокинов с рецепторами клеток (трансмембранными белками) ↓ возникновение сигнала ↓ передача сигнала в ядро ч/з внутриклеточную систему ферментов (киназы) и медиаторов ↓ активация соответствующих генов в ядре ↓ регуляция ИС продуктами генов
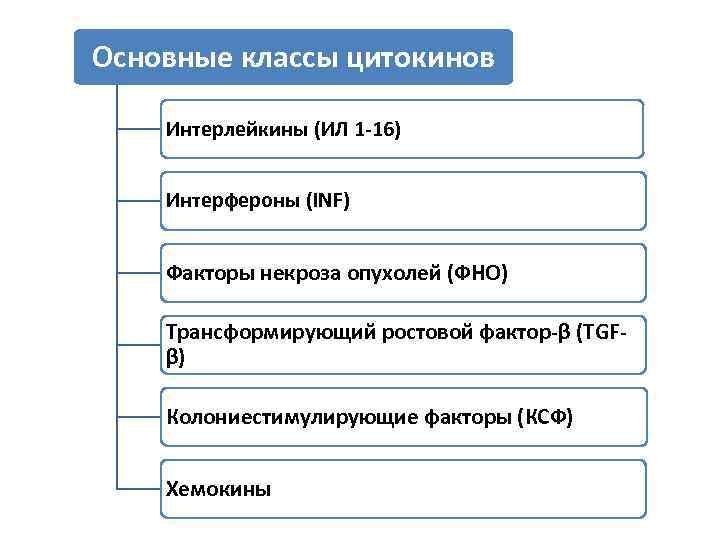
Основные классы цитокинов Интерлейкины (ИЛ 1 -16) Интерфероны (INF) Факторы некроза опухолей (ФНО) Трансформирующий ростовой фактор-β (TGFβ) Колониестимулирующие факторы (КСФ) Хемокины

Свойства цитокинов Ø медиаторы воспаления: ФНО α, INFβ, ИЛ 1, ИЛ 6, ИЛ 12 Ø факторы роста и дифференцировки: ИЛ 3, ИЛ 7, ИЛ 11, КСФ-М, КСМ-ГМ Ø регуляторы: - активации, пролиферации и дифференцировки Лф: ИЛ 4, ИЛ 13, ИЛ 2, TGF-β -иммунного воспаления: INF , ЛТ, ИЛ 5, ИЛ 9, ИЛ 10, ИЛ 12

ИНТЕРЛЕЙКИНЫ Ø более 30 (от ИЛ 1 до ИЛ 30) Ø гликопротеиды Ø продуцируются АГ-стимулированными клетками: Мф, Т-л, нейтрофилами, тучными клетками, базофилами, эндотелиоцитами Ø обеспечивают взаимодействия между клетками ИС

Наиболее изученные ИЛ

Наиболее изученные ИЛ
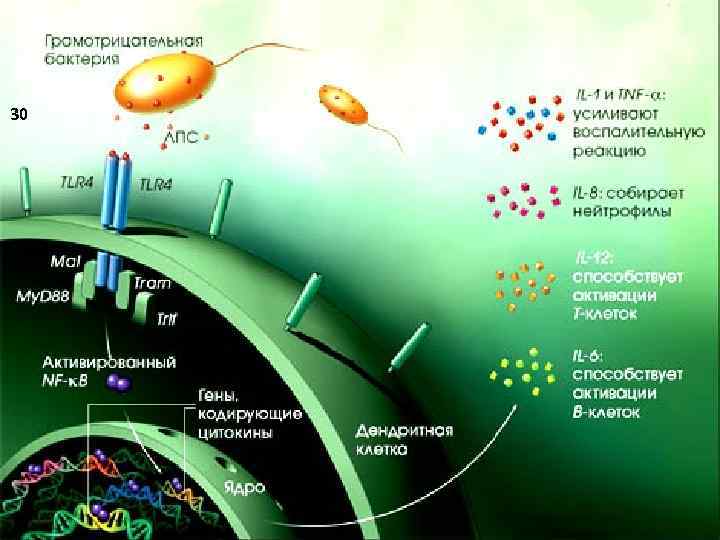
30

ИНТЕРФЕРОНЫ Ø Низкомолекулярные белки Ø Синтезируются: 1) неспецифическими клетками под влиянием: - микроорганизмов (белки, 2 ц. РНК, бактерии и бактериальные продукты) - синтетических полимеров (полианионов) 2) или Т-л, стимулированными АГ Ø Регуляторы межклеточных взаимодействий
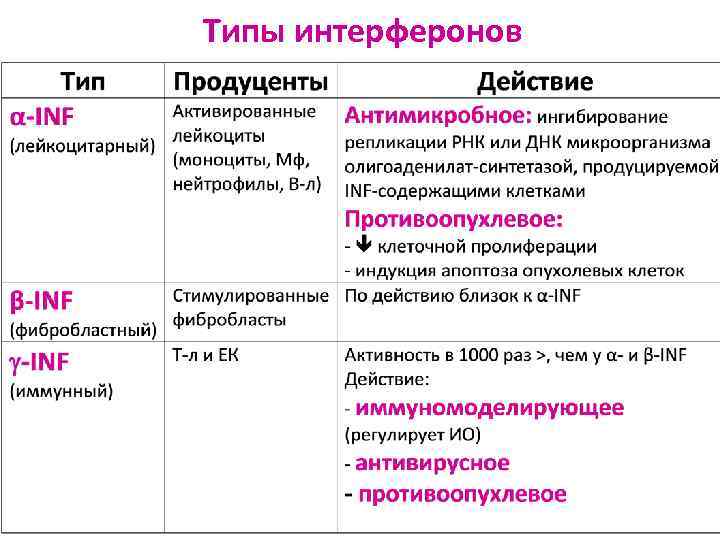
Типы интерферонов

ФАКТОРЫ НЕКРОЗА ОПУХОЛЕЙ (ФНО) – воспалительные цитокины, рецепторы к которым есть на большинстве клеток Ø ФНО-α (кахексин) секретируется моноцитами, Т-л, В-л. Эффекты: - лихорадка и синдром септического шока - повреждение клеток, в т. ч. опухлевых - кахексия (в больших концентрациях) - активация Т-л и В-л - индукция продукции ИЛ 1 и ИЛ 6, экспрессии молекул ГКГС Ø ФНО-β (лимфотоксин) секретируется Т-л и В-л. Эффекты: - индукция апоптоза клеток-мишеней

ТРАНСФОРМИРУЮЩИЙ РОСТОВОЙ ФАКТОР-β (TGF-β) Ø Продуцируется многими типами клеток (В-л, Т-л, моноциты) Ø Иммуносупрессор, ИО, когда теряется его необходимость: рост и активность Т-л, Мф, В-л, нейтрофилов, ЕК

КОЛОНИЕСТИМУЛИРУЮЩИЕ ФАКТОРЫ (КСФ) Ø Продуцируются: - стромальными клетками кроветворных и лимфоидных органов моноцитами Т-л В-л Ø Типы КСФ по специфичности: рост, дифференцировку и активацию: - гранулоцитов (КСФ-Г) - моноцитов (КСФ-М) - гранулоцитов и моноцитов (КСМ-ГМ) Ø Стимулируют образование колоний миелоидных и моноцитарных клеток в ККМ

ХЕМОКИНЫ Ø Низкомолекулярные полипептиды (> 50) Ø Продуценты: - гранулоциты - моноциты - Лф - тромбоциты - фибробласты - эпителиоциты ØИндукторы их синтеза: - цитокины (ИЛ 1, ИЛ 6) - повреждения

Роль хемокинов Ø Участвуют в развитии клеточной фазы воспаления: связываются с элементами межклеточного матрикса, формируя градиент концентрации и обеспечивая направленное движение ИКК по градиенту концентрации Ø Привлекают из крови в очаг повреждения/воспаления определённые ИКК: - которые избирательно экспрессируют рецепторы для хемокинов - обратимо связываются с клеточными рецепторами, вызывают активацию и изменение цитоскелета клеток Ø Роль при аллергии, инфекции, аутоиммунных заболеваниях, опухолевом росте
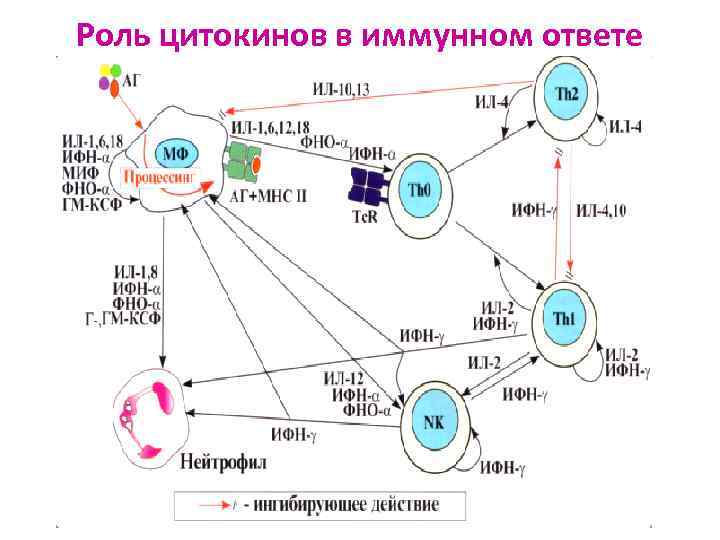
Роль цитокинов в иммунном ответе

Роль молекул ИС в развитии воспаления Ø 1 этап – качение. Под влиянием цитокинов на поверхности эндотелия и лейкоцитов появляются молекулы селектинов. Они тормозят движение лейкоцита, приближают его к эндотелию и он начинает «катиться» по его поверхности. Ø 2 этап – адгезия. По мере приближения к очагу воспаления под влиянием хемокинов лейкоциты прилипают к эндотелию (распластываются). Ø 3 этап – экстравазация. С помощью интегринов лейкоциты проникают между клетками эндотелия и попадают в ткань, где формируется воспалительный очаг.
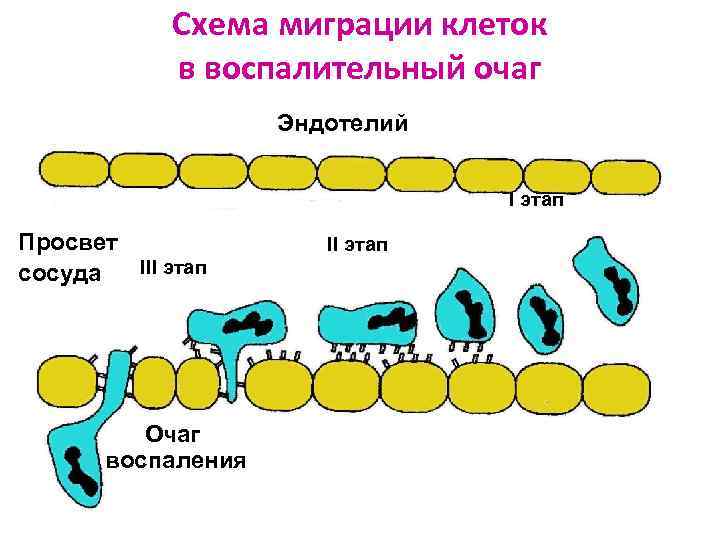
Схема миграции клеток в воспалительный очаг Эндотелий I этап Просвет III этап сосуда Очаг воспаления II этап

2013_Иммунология_ИС_Молекулы ИС.ppt