репродукция и возр особен.ppt
- Количество слайдов: 107

Иммунология беременности • Эмбрион и плод человека получают от отца 50% генетической информации, которая чужеродна для организма матери. Другая половина генетической информации плода является общей для организма плода и матери. Плод всегда является генетически полусовместимым трансплантатом по отношению к организму матери. • Важнейшим фактором защиты плода является иммунологическая толерантность материнского организма к антигенам плода отцовского происхождения.
Плод - всегда генетически полусовместимый трансплантат по отношению к организму матери. Важную роль играет иммунологическая толерантность материнского организма к Аг отца.

Иммунология беременности • Некоторые гормоны, продуцируемые уже на самых ранних сроках беременности (хорионический гонадотропин, плацентарный лактоген, прогестерон и эстрогены), обладают выраженными иммуносупрессивными свойствами. Большую роль в иммунной защите плода играет плацента. • Иммунологические взаимоотношения системы «мать-плод» являются физиологическим процессом, направленным на создание и обеспечение необходимых условий для нормального развития плода. Нарушение этого процесса нередко приводит к развитию патологии беременности (невынашивание, гестозы и др. ).

Эмбрион является потенциальным индуктором для развития выраженного иммунного ответа материнского организма в случае проникновения их в кровеносное русло матери. При попадании лимфоцитов матери в кровоток плода также развивается реакция со стороны эмбриона. В пупочном канатике находятся лимфоциты плода, разрушающие лимфоциты матери.

Роль матки • Матка не является иммунологически привилегированным органом. Об этом свидетельствует: • наличие хорошего кровотока, • большие дренажные способности лимфатической системы и • возможность развития иммунного ответа при попадании в орган патогенного агента.

Роль плаценты • У здоровых женщин репродуктивного возраста в секреторную фазу цикла и на ранних сроках беременности в строме эндометрия встречаются БГЛ или NK (более 75% ИКК, обнаруживаемых в децидуальной оболочке матки во время имплантации). • Фенотип NK децидуальной ткани не экспрессирует молекулу CD 16, а уровень экспрессии CD 64 и CDЗ 2 ничтожно мал. NK -клетки децидуальной оболочки являются активированными, о чём свидетельствует высокий уровень экспрессии молекулы семейства интегринов (VLA-1 или CD 49 а). • Во второй фазе цикла NK-клетки подвергаются пролиферации и дифференцировке и принимают участие в наступлении менструации (при условии отсутствия в матке плодного яйца).

Роль плаценты • Плацента является иммуносорбентом антифетальных антител к HLA (иммуносорбционные свойства плаценты).
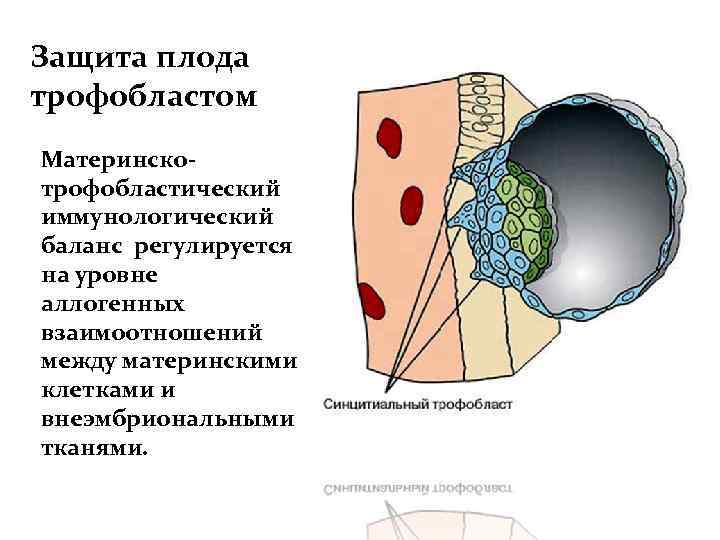
Защита плода трофобластом Материнскотрофобластический иммунологический баланс регулируется на уровне аллогенных взаимоотношений между материнскими клетками и внеэмбриональными тканями.

Особенности трофобласта Присутствуют рецепторы Fc. R к Ig G – участие в переносе материнских иммуноглобулинов в кровоток плода. Клетки трофобласта за счет поверхностных сиаловых кислот несут высокий отрицательный заряд – затруднение контакта с другими клетками, в том числе и с лимфоцитами. В синцитиотрофобласте и ворсинчатом цитотрофобласте почти полностью отсутствуют HLA I локусы А, В и HLA II (локус D), особенно отцовского происхождения.
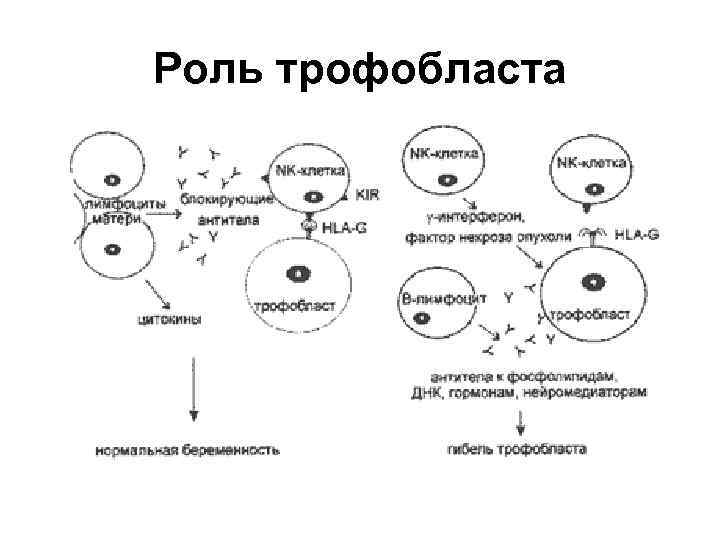
Роль трофобласта

Особенности трофобласта

Особенности трофобласта • HLA-C молекулы характеризуются низким уровнем экспрессии бета-2 -микроглобулина и присутствуют на поверхности клетки только в форме тяжелых цепей. • HLA I (локус G) включает 20 гомологичных генов, псевдогены и генные фрагменты. HLA-G антигены относятся к неклассическим HLA (класса Ib) и экспрессируются лишь на плацентарных тканях зародыша в зоне плодоматеринского взаимодействия. • Экспрессия HLA-G "ассоциирована с беременностью".

Роль плаценты • В процессе внедрения в децидуальную оболочку матки клетки трофобласта секретируют различные типы металлопротеаз, что обеспечивает разрушение матриксных белков эндометрия и проникновение трофобласта в глубжележащие слои. • В ответ на это происходит локальное увеличение синтеза цитокинов (ТФР), а также тканевых ингибиторов металлопротеаз. • К месту имплантации устремляются различные ИКК (NK-клетки, макрофаги и дендритные клетки), синтезирующие громадный спектр цитокинов, стимулируя дальнейшее внедрение трофобласта, или подавляя данный процесс.

Механизмы защиты трофобласта

Роль плаценты • Во время имплантации клеток трофобласта происходит обмен сигналами между ними и ИКК. Рост, пролиферацию клеток трофобласта и процесс их проникновения в эндометрий контролируют NK децидуальной ткани. • NK вырабатывают ТФР-β подавляющий активацию и пролиферацию цитотоксических клеток. • Контакт клеток трофобласта с CD 3 - CD 16 - CD 56+клетками инициирует синтез большого количества ГМ-КСФ и некоторых других факторов роста, что является важным аутокринно-паракрииным механизмом регуляции роста и дифференцировки плаценты. • Лимфоциты децидуальных оболочек выделяют ГМКСФ спонтанно или после стимуляции антигенами отца, представляемыми на клетках трофобласта.

Роль плаценты • Взаимоотношения между CD 3 - CD 16 - CD 56+- клетками и клетками вневорсинного трофобласта способствуют дальнейшему продвижению трофобласта в эндометрий (в зоны спиральных артерий децидуальной оболочки). По мере продвижения они осуществляют ремоделирование данных артерий (перестройка эндотелия и пр. ), что создаёт условия для формирования плаценты и обеспечения адекватного кровоснабжения плода. • Основу иммунологических механизмов невынашивания беременности могут составлять взаимоотношения между клетками трофобласта и киллерами, имеющими фенотип CD 3 - CD 16 - CD 56+. В пользу этой точки зрения свидетельствуют данные о селективном накопленни в эндометрии данного типа клеток у женщин с привычным невынашиванием беременности.

Роль плаценты • В плаценте клетки трофобласта находятся в контакте с материнской кровью. • Клетки вневорсинного трофобласта экспрессируют на своей поверхности молекулы НLA-C, -Е и -G системы МНС 1 класса, защищающие трофобласт от цитотоксического воздействия NК-клеток. • NК-клетки атакуют только те клетки-мишени, которые не экспрессируют аутологичные молекулы МНС 1 класса. Более того, «классические» молекулы МНС 1 класса (НLА-А и НLA-B) на поверхности трофобласта вообще не экспрессируются. • NK-клетки экспрессируют все 3 типа лигандов к вышеназванным молекулам клеток трофобласта. • Результатом подобных лиганд-рецепторных взаимодействий является подавление цитотоксичности в результате активации соответствующих лигандов на поверхности NK (КIR - killing inhibitory receptor).

Роль плаценты • NK располагающиеся в месте имплантации, синтезируют большое количество провоспалительных цитокинов Тh 1 -звена (ИЛ-15 и ИЛ -18), не нарушая обычного течения гестации. • Моноциты, инфильтрирующие эндометрий во время беременности, синтезируют и секретируют ИЛ-12, способствующий ориентации иммунного ответа по Тh 1 - зависимому пути. • Повышение синтеза плацентой провоспалительных цитокинов ФНО-α и ИФН-γ увеличивает частоту прерываний беременности у мышей, а экзогенное введение ИЛ-1 О препятствует этому. • У женщин с привычным невынашиванием беременности имеются лишь косвенные свидетельства наличия Тh 1/Тh 2 дисбаланса в данном процессе.
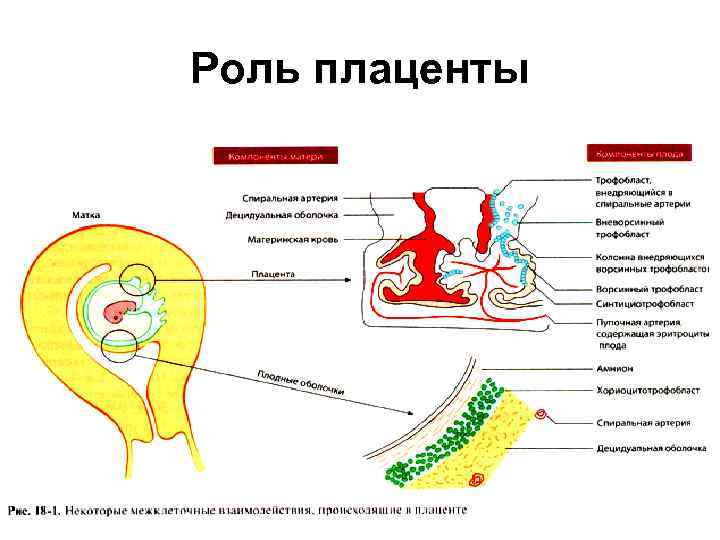
Роль плаценты

Роль плаценты

Прогестерон • Прогестерон в высоких концентрациях миметирует глюкокортикоидные эффекты в силу низкоавидного связывания с рецепторами кортизола. • Обладает противовоспалительными свойствами - Снижает образование кислородных радикалов макрофагами. - Подавляет продукцию ИЛ-1β, ИФ-γ лимфоцитами. - Снижает продукцию ИЛ-8 человеческими эндометриальными клетками. - Ингибирует продукцию ИЛ-6 децидуальными стромальными клетками человека в культуре. - Индуцирует синтез лимфоцитами иммуносупрессивного фактора (предотвращающего аборт). • Прогестерон ингибирует ответ лимфоцитов на митогены и аллоантигены, способен продлевать время выживания трансплантата. • Прогестерон имеет непрямое влияние на активность NК. Прогестерон-индуцированный блокирующий фактор (PIBF) (белок, который опосредует иммунологические эффекты прогестерона), блокирует активность NК in vitro и предотвращает выкидыш.

Эстрогены (эстрадиол, эстрон, эстриол) • Эстрогены тормозят клеточный (Тh 1 -зависимый) и стимулируют гуморальный (Th 2 -зависимый) иммунный ответ. • Уменьшают бласттрансформирующую способность Т-лимфоцитов • Выявляется обратная корреляция между уровнем активности NК и концентрацией эстрадиола в плазме крови при беременности по мере ее прогрессирования. • Избыток эстрогенов снижает устойчивость к опухолям и паразитам. • Назначение эстрогена повышает активность Тхелперов (CD 4 клеток) и супрессирует активность CD 8 клеток. • Эстрадиол ингибирует секрецию ФНО-α, ИЛ-1 и ИЛ 6, cтимулирующих клеточное звено.

Хорионический гонадотропин • ХГ - основной гликопротеиновый гормон, секретируемый плацентой во время беременности. Высокие дозы ХГ (у овариоэктомированных самок животных) вызывают иммуносупрессию. • Угнетает клеточный иммунный ответ. Снижает активность Т-лимфоцитов и ЕКК, • угнетает синтез ИЛ-2. • Снижает фагоцитарную активность моноцитов.

Механизмы блокады отцовских аллоантигенов. • Слой Фибриноидного материала (толщиной 0, 1 -2 мкм), окружающий трофобласт. Состоит из мукополисахаридов (протеогликанов), в составе углеводного компонента которых присутствуют гиалуроновая и сиаловая кислоты. • Фибриноид плаценты - конечный продукт трансформации растворимого в крови фибриногена в нерастворимый фибрин. Слой фибриноида, а также • сиаломуцин и серомукоид частично маскируют антигены плода в трофобласте. Слой фибрина, отличный от фибриноидного слоя; находится между трофобластом и децидуальной тканью, появляется лишь на 10 неделе.

Антитела, иммунные комплексы Адсорбция антител к антигенам плода, играет ведущую роль в защите развивающегося плода против иммунного ответа матери на антигены фетоплацентарного комплекса. В-лимфоциты плаценты синтезируют преимущественно Ig G 1 - фетопротективный. При нормальной беременности превалирует гуморальный иммунитет, хотя продукция Ат варьирует от образования цитотоксических Ат Ig G 2 ( индуцированного клетками Th 1) до образования нецитотоксических Ат - Ig G 1 (индуцированного Th 2). Преобладание Th 1 -клеточного иммунного ответа связано с повышенным риском выкидыша.

Беременность и инфекции • Инфекции, возникающие во время беременности, представляют серьёзную опасность как для матери, так и для плода. • Из бактериальных инфекций при беременности чаще всего встречаются инфекции мочевыводящих путей, в ряде случаев протекающих в виде бессимптомной бактериурии. Чаще всего при посеве обнаруживают E. coli. • К развитию инфекций мочевыводящих путей предрасполагают физиологические изменения во время беременности, обусловленные гормональными влияниями, а также расширение мочеточников и пузырно-мочеточниковый рефлюкс.

Беременность и инфекции • У трети беременных с бессимптомной бактериурией в III триместре беременности развивается пиелонефрит. Беременность предрасполагает к развитию листериоза (возбудитель - Listeria monocytogenes). Заболевание чаще возникает в III триместре и по своей клинической картине напоминает инфекцию мочевыводящих путей. • Для постановки правильного диагноза необходим посев крови, так как результаты посева мочи бывают отрицательными. Бактериальные инфекции околоплодных оболочек (хориоамниониты) несут большую опасность для плода и часто сопровождаются преждевременными родами.

Беременность и инфекции • Заражение плодных оболочек обусловлено полимикробной флорой (E. coli, Gardnerella vaginalis, Мусорlasma spp. , и др. ) и чаще всего происходит восходящим путём при преждевременном излитии околоплодных вод. • Развитие у ребёнка гонококковой инфекции может происходить как в результате его внутриутробного заражения, так и во время родов. Чаще всего гонококковая инфекция у новорождённых проявляется в форме конъюнктивита (бленнорея). • Внутриутробное заражение сифилисом может произойти на любом сроке беременности, однако на сроке до 4 месяцев это случается редко. В отсутствие лечения возможно мёртворождение, а также врождённый сифилис (латентный).

Беременность и инфекции • Особо опасны вирусные инфекции. Некоторые вирусы (цитомегаловирус, вирус простого герпеса, Varicella zoster, вирус краснухи) обладают тератогенным действием. Возможно заражение ребёнка в родах - при прохождении через инфицированные родовые пути. • Особенно тяжёлые последствия для ребёнка возникают при инфицировании организма будущей матери вирусом краснухи (в I триместре беременности). Если мать заболевает краснухой в I триместре беременности, риск поражения плода достигает 80%, при заражении в конце II триместра - 25%. В I триместре беременности (на 4 - 5 неделе) происходит закладка органов и тканей плода. Последствиями внутриутробного инфицирования плода вирусом краснухи могут быть выкидыш или преждевременные роды, а также врождённые пороки сердца, глухота, катаракта и умственная отсталость ребёнка. Врождённую краснуху диагностируют путём определения специфических антител (Ig. M в крови плода). • Инфицирование организма беременной женщины вирусом ветряной оспы может иметь тяжёлые последствия как для неё самой (ветряночная пневмония), так и для плода (пороки развития).

Беременность и инфекции Токсоплазмоз. • Заражение происходит внутриутробно или во время родов. Риск самопроизвольного аборта максимален при заражении матери в I триместре беременности, риск врождённого токсоплазмоза - при заражении в III триместре. Особенностью данной инфекции является её бессимптомное течение. У больного ребёнка симптомы врождённого токсоплазмоза также могут отсутствовать и проявляться только в подростковом возрасте. Чаще всего развивается хориоретинит, встречаются случаи возникновения эпилептических припадков, психомоторной заторможенности и пр. Пороков развития не бывает. • Повышение восприимчивости к инфицированию патогенами типа Listeria, Тохорlasma и др. косвенно свидетельствует о развитии в организме транзиторного Тh 1/Тh 2 дисбаланса в сторону преобладания Тh 2 -опосредованного пути иммунного ответа. Это повышает восприимчивость организма женщины к инфицированию внутриклеточными патогенами. Во время беременности целесообразно проведение оценки иммунного статуса. • Особое значение имеет наличие у беременных антигенспецифичного иммунитета против возбудителей краснухи, кори, ветряной оспы и полиомиелита.
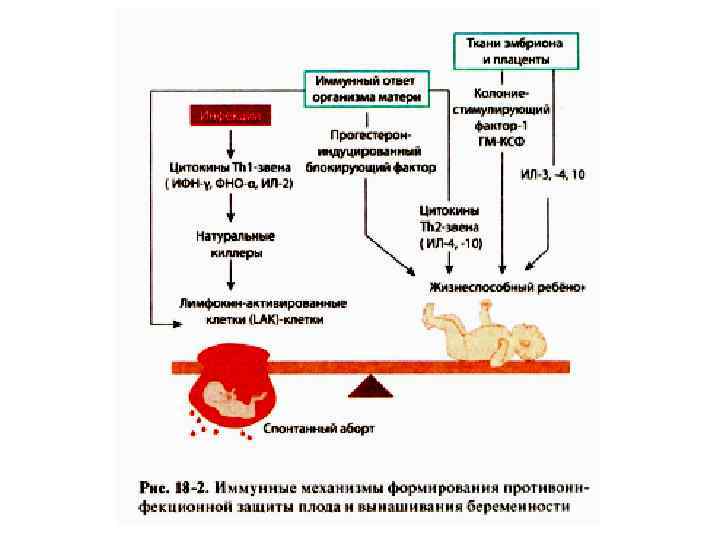

Невынашивание беременности • Примерно в каждом пятом случае беременность заканчивается выкидышем. • Причины невынашивания беременности: • анатомические аномалии, • гормональные нарушения, • генетические дефекты, • инфекции, • аутоиммунные заболевания (СКВ или антифосфолипидный синдром), • патология системы гемостаза. • Роль иммунологических нарушений в невынашивании беременности невелика (не более 10%). Основным является срыв механизмов иммунологической толерантности организма матери по отношению к антигенам плода.

Невынашивание беременности • Серологические исследования, должны быть направлены на диагностику состояний, способных привести к развитию данной патологии. • К ним относят СКВ и антифосфолипидный синдром. • Установлена роль аутоантител в патогенезе невынашивания беременности. К патогенетически значимым аутоантителам относят антитела к кардиолипину и антифосфолипидные антитела. Антифосфолипидные антитела (Ig. G и Ig. M) иногда выявляют в сыворотке у здоровых лиц (2 -7%).

Невынашивание беременности • Выявлена корреляция между титром вышеуказанных аутоантител класса Ig. G в сыворотке и частотой развития самопроизвольных абортов у беременных, болеющих СКВ. • Окончательные иммунопатогенетические механизмы действия антифосфолипидных антител к настоящему времени не изучены. Одним из основных проявлений их действия являются тромбозы. • Поэтому беременным с высоким титром аутоантител показано проведение терапии, направленной на предупреждение развития тромбозов (ацетилсалициловая кислота, гепарин).

Возможные исходы беременности у больных СКВ • Около 70% беременностей с СКВ заканчиваются рождением жизнеспособного плода и не ухудшают прогноз заболевания матери. • К факторам риска неблагоприятного течения и исхода беременности относят высокую активность волчаночного процесса при зачатии и в период гестации, наличие поражения почек, гипертензии и вторичного антифосфолипидного синдрома у беременной. Из иммунологических предикторов осложнений выделяют позитивность по антифосфолипидным антителам. Присутствие Ro/SSA или La/SSB антител, гипокомплементемию. • Внутриутробная гибель плода обычно происходит у беременных с высоким уровнем антифосфолипидных антител.

Возможные исходы беременности у больных СКВ • Кроме преждевременных родов, спонтанных абортов и антенатальной гибели плода неблагоприятным исходом для новорождённого может явиться неонатальная волчанка (1 -2%). • Она обусловлена трансплацентарным переносом материнских Ro/SSA или La/SSB антител.

Возможные исходы беременности у больных СКВ • Культивирование плацентарной ткани с добавлением сыворотки беременных женщин с антифосфолипидным синдромом или СКВ инициирует снижение скорости пролиферации трофобласта и запускает в нём процесс апоптоза. • Проведение адекватной терапии СКВ способствует вынашиванию беременности. • В ряде случаев развитие беременности приводит к изменению течения самого аутоиммунного заболевания у будущей матери. • Описанные выше закономерности можно проследить и при других аутоиммунных заболеваниях соединительной ткани.


Преэклампсия • Развитие преэклампсии характеризуется нарушением плацентарного кровотока и развивающейся гипоксией плода. Нарушение плацентарного кровотока является следствием нарушения процессов и имплантации и ремоделирования сосудов, что приводит к последующей гипоксии плода. • Клинические симптомы преэклампсии (протеинурия, отёки и артериальная гипертензия) обусловлены массивным повреждением эндотелия сосудов матери и развитием системного воспалительного процесса сосудистой стенки. Это происходит в результате высвобождения из ишемизированной плаценты большого количества биологически активных веществ и метаболитов и их последующего поступления в системный кровоток. • К факторам, способным вызвать нарушение васкуляризации плаценты, относят цитокины, продуцируемые самой плацентой, факторы роста и ингибиторы металлопротеаз.

Преэклампсия • Преэклампсия обычно развивается во время первой беременности, повторная беременность сопровождается меньшим риском развития данного состояния. Это обусловлено предварительной сенсибилизацией организма матери к антигенам системы НLA экспрессированным на поверхности клеток трофобласта во время предыдущей беременности. • Во время повторной беременности происходит кооперация уже обученных децидуальных NК-клеток (СDЗ-СD 16 -СD 56+-клеток) с клетками трофобласта, экспрессирующими аналогичные молекулы НLA-C, НLA-E и НLA-G системы МНС I класса. • Это обеспечивает лучшую имплантацию, уменьшает вероятность развития ишемии плаценты и преэклампсии. Подобная закономерность справедлива, если клетки трофобласта во время первой и второй беременности экспрессируют идентичные молекулы НLA-C, НLA-E и НLA-G системы МНС I класса. Это возможно в том случае, если отец первого и второго ребёнка одно и то же лицо.

Аллоиммунизация • Аллоиммунизация (сенсибилизация) организма будущей матери к антигенам плода происходит только в том случае, если фетальные эритроциты попадают с системный кровоток организма матери. Образующиеся в организме матери антитела в дальнейшем проходят через плацентарный барьер и взаимодействуют с эритроцитами плода. Опсонизированные материнскими антителами эритроциты подвергаются фагоцитозу в селезёнке и печени плода, приводя к развитию гемолитической болезни новорождённых. • Наиболее типичной причиной гемолитической болезни новорождённых является резус-конфликт между организмом матери и плодом, причём будущая мать должна быть Rh-негативной, а плод Rh-позитивным.

Аллоиммунизация • Основным Rh-антигеном, определяющим развитие иммунологического конфликта между организмом матери и плодом, является D-антиген. Развитие иммунологического конфликта, основанного на несовместимости Rh-антигенов можно предотвратить путём введения специфического анти- D -иммуноглобулина во время беременности и сразу после её разрешения. • Препарат разрушает фетальные эритроциты в организме матери и препятствует, тем самым, образованию к ним антител. Это, в свою очередь, создаёт предпосылки для нормального течения беременности. • Гемолитическая болезнь новорождённых может являться следствием несовместимости по антигенам группы крови (АВО-несовместимость).
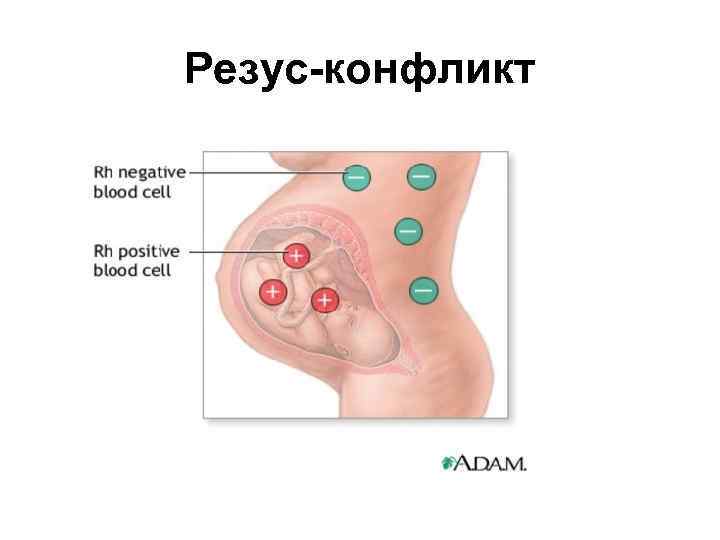
Резус-конфликт

Rh – конфликт

АВО - несовместимость АГ эритроцитов А и В способны также вызвать выраженный иммунный ответ. Факторы, предрасполагающие к развитию АВО несовместимости: Первая беременность (30 % случаев). Иммунизация по системе АВО наиболее часто развивается при первых беременностях, а анти-Dсенсибилизация - при 3 -4 -ой беременности; Rh совместимая беременность (Rh+ группа крови матери и плода); Группа крови I(О).

Аллоиммунизация • Аллоиммунизация фетальными тромбоцитами инициирует образование в организме матери антитромбоцитарных антител, ответственных за развитие аллоиммунной неонатальной тромбоцитопенической пурпуры. • Заболевание встречается редко (1: 1000 новорождённых). Это связано с тем, что основным антигеном, инициирующим образование антитромбоцитарных антител, является антиген НРА-1 а, который экспрессируется на поверхности тромбоцитов у подавляющего числа людей и поэтому не инициирует образование антитромбоцитарных антител.

Аллоиммунизация • Аллоиммунную неонатальную тромбоцитопеническую пурпуру следует отличать от идиопатической тромбоцитопенической пурпуры, при которой в организме матери появляются аутоантитела к собственным тромбоцитам. • В организме матери нередко можно обнаружить антитела к антигенам гистосовместимости плода. Титр антител после первой беременности крайне низок, но может увеличиваться при развитии повторной и последующих беременностей. • Данные аутоантитела относятся к классу G, поэтому могут проходить через плацентарный барьер. Отрицательные последствия для плода в результате действия данных антител не известны.

Органоспецифичные аутоиммунные заболевания при беременности • Развитие органоспецифичных аутоиммунных заболеваний во время беременности может затрагивать как организм матери, так и организм плода. Подобные заболевания могут быть следствием синтеза аутоантител класса G, которые циркулируют в крови и могут преодолевать плацентарный барьер. • Примером такого заболевания является миастения гравис, развивающаяся как у матери, так и у 10% детей, рождённых от страдающих данным заболеванием матерей.

Органоспецифичные аутоиммунные заболевания при беременности

Органоспецифичные аутоиммунные заболевания при беременности • Идиопатическая тромбоцитопеническая пурпура развивается в организме матери вследствие синтеза антител к собственным тромбоцитам. Это достаточно редкое заболевание, которое способно при вести к невынашиванию беременности. • Антитромбоцитарные антитела могут проникать через плацентарный барьер и вызывать неонатальную тромбоцитопению новорождённых (до 50% случаев). • Наличие антител свидетельствует об аутоиммунной идиопатической тромбоцитопении, в то время как обнаружение антител исключительно на поверхности тромбоцитов ребенка - об аллоиммунной неонатальной тромбоцитопении. • Аналогичные механизмы могут обуславливать развитие нейтропении, являющейся следствием выработки антинейтрофильных аутоантител.

Антитела к гормонам • Образующиеся в организме аутоантитела к гормонам, играющим роль в процессах имплантации и вынашивания беременности, могут повлиять на её течение. • С иммунологической точки зрения весьма привлекательным является создание так называемых «контрацептивных вакцин» , способных инициировать в организме будущей матери развитие антител к гормональным факторам, регулирующим процессы имплантации и вынашивания беременности. действительно, если в результате иммунизации к данным гормонам удастся получить нейтрализующие аутоантитела в достаточном титре, перспективы для создания вышеназванных вакцин будут выглядеть вполне реальными.

Антитела к гормонам • В отличие от противоопухолевых вакцин, целью которых является усиление клеточного противоопухолевого иммунитета, в создании контрацептивных вакцин основной целью является стимуляция гуморального звена иммунной системы с целью синтеза нейтрализующих антител. К настоящему времени проходят испытания некоторых контрацептивных вакцин. • Например, положительно завершилась 2 стадия клинических испытаний по оценке эффективности вакцины, направленной на синтез антител к гонадотропному гормону. Проводили испытания (на обезьянах-самцах) вакцины, инициирующей синтез антител к фолликулостимулирующему гормону. Низкая иммуногенность вакцины и её низкая способность вызывать аспермию.


Некоторые случаи бесплодия невыясненного генеза и привычного невынашивания связаны с отсутствием продукции LIF (Leukemia Inhibitory Factor) эндометрием или его количественным дефицитом. Экпрессия Fas-лиганда на трофобластах. При взаимодействии с цитотоксическими лимфоцитами или NK идет запуск программы апоптоза лимфоцита.
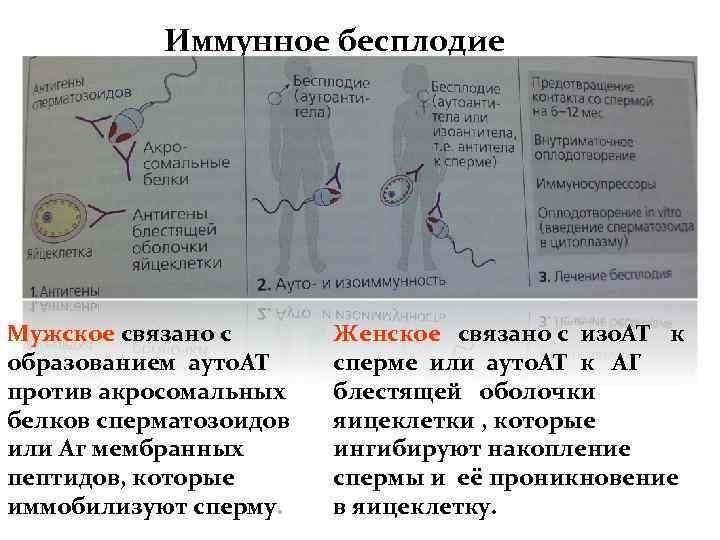
Иммунное бесплодие Мужское связано с образованием ауто. АТ против акросомальных белков сперматозоидов или Аг мембранных пептидов, которые иммобилизуют сперму. Женское связано с изо. АТ к сперме или ауто. АТ к АГ блестящей оболочки яицеклетки , которые ингибируют накопление спермы и её проникновение в яицеклетку.

Причины мужского бесплодия Антитела выявляются у 15 % бесплодных мужчин. Антиспермальные Ig. G, Ig M, Ig А могут нарушать функциональную активность сперматозоидов (обездвиживать или приводить к их гибели), препятствовать проникновению в полость матки. Нарушение механизмов иммуносупрессии; Нарушение гематотестикулярного барьера (семенники – забарьерный орган); Некоторые инфекции – простатит, мембранные бактериальные Аг , действие перекрестно реагирующих Аг.

Антиспермальные антитела • Антиспермальные антитела - антитела к антигенам мембраны сперматозоидов. В настоящее время антиспермальные антитела (чаще всего Ig. G, реже Ig. А или Ig. M) выявляют в сыворотке крови, цервикальной слизи, семенной жидкости, на поверхности сперматозоидов. • Антиспермальные антитела обнаруживают у некоторых здоровых мужчин (не более 10%), у мужчин с бесплодием (до 30%), а также у бесплодных женщин. • В физиологических условиях образованию антиспермальных антител в разных отделах мужской репродуктинной системы препятствуют различные механизмы. К таковым относят:

Антиспермальные антитела • гематотестикулярный барьер (изолирует клетки сперматогенеза от иммунокомпетентных клеток организма); • способность сперматозоидов к мимикрии ( «сбрасывают» с оболочки ранее сорбированные антигены и адсорбируют новые, в том числе и из женского репродуктивного тракта); • иммуносупрессивный фактор спермоплазмы, секретируемый в придаточных железах мужской репродуктивной системы. Сбой механизмов защиты на любом из вышеуказанных уровней приводит к синтезу у мужчины антиспермальных антител.

Антиспермальные антитела • Попадание спермы в женские половые пути может инициировать развитие иммунного ответа и приводить к синтезу антиспермальных антител. В большинстве случаев этого не происходит. Этому также препятствуют различные механизмы: • повышение уровня клеток с супрессорной активностью в период овуляции; • уменьшение концентрации иммуноглобулинов и С 3 компонента системы комплемента; • мимикрия сперматозоидов и иммуносупрессивный фактор спермоплазмы. Вопрос о способности антиспермальных антител влиять на качество эякулята до настоящего времени является предметом дискуссий. Некоторые исследователи считают, что данные антитела вызывают снижение подвижности и жизнеспособности сперматозоидов, нарушая целостность их мембраны.

Антиспермальные антитела • Антиспермальные антитела могут оказывать повреждающее действие на функцию предстательной железы. Тем не менее, обнаружение данных антител у здоровых мужчин ставит под сомнение данную точку зрения. другие исследователи считают, что если антиспермальные антитела и играют какую-либо патологическую роль (приводя к нарушению фертильности), то это происходит исключительно в организме женщины. • Антиспермальные антитела классов Ig. G и Ig. A в цервикальной слизи и других жидкостях женского репродуктивного тракта препятствуют продвижению сперматозоидов и их пенетрации через цервикальную слизь, блокируют рецепторные участки на головке сперматозоида, ответствеиные за связывание с оболочкой яйцеклетки.

Причины женского бесплодия Заболевания половой сферы (активация иммунного ответа на инфицирующие агенты); Увеличение пропорции Т-хелперов (CD 4+) в биоптате эндометрия (в процессе беременности), приводящее к патологическому состоянию эндометрия. Антифосфолипидный синдром (АФС). С бесплодием коррелируют титры антител более 1: 16.
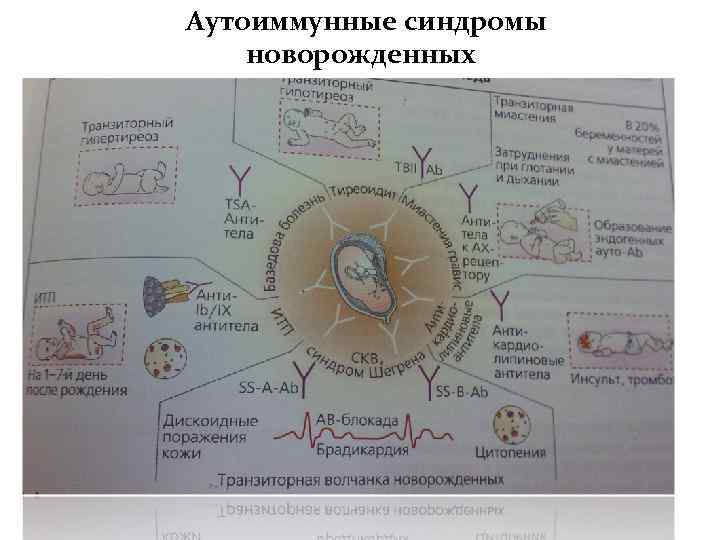
Аутоиммунные синдромы новорожденных

Возрастная иммунология. Особенности функционирования ИС в детском и пожилом возрасте

Иммунологическая реактивность у детей • Процесс закладки иммунной системы • Реализация ее потенциальных возможностей в развертывании специфических реакций • Реализация ее потенциальных возможностей в достижении зрелости

Иммунологическая реактивность у детей • Созревание иммунной реактивности плода • Иммунный статус детей после рождения

Иммунная реактивность плода Закладка тимуса на 2 месяце внутриутробного развития в области 3 -4 жаберного кармана • 6 нед. - имеет эпителиальный характер • 7 -8 нед. – «заселение» лимфоцитоподобными клетками • Конец 3 мес. – формирование тимуса

Иммунная реактивность плода • Лимфатические узлы и другие периферические образования закладываются на 4 месяце. • Окончательное формирование в постнатальном периоде • Лимфоидные фолликулы подвздошной кишки, аппендикса и пейеровых бляшек содержат «клетки предшественники» плазматических клеток. Они дозревают до плазматических клеток синтезирующих Ig. A к 14 -16 неделе.

Иммунная реактивность плода • Стволовые клетки – 3 -8 нед. Эмбриогенеза обнаруживаются в печени, кровяных островках желточного мешка. Позднее продуцируются в костном мозге. • Лимфоциты – 9 нед. в тимусе • 12 -15 нед. в селезенке • 8 -10 нед. в периферической крови • Т- лимфоциты (CD 3+) -10 -11 неделе • В- лимфоциты (CD 19+) – 10 -12 нед. в печени, с 12 нед. в селезенке

Иммунная реактивность плода • • Синтез и секреция иммуноглобулинов : Ig. M – 11 нед (1/10 материнские) Ig. G - 22 нед Система комплемента: 8 нед – С 2 и С 4 – макрофаги; С 5 и С 4 печень, легкие и перитонеальные клетки; С 1 и С 3 – толстый и тонкий кишечник 18 нед – данные компоненты появляются в сыворотке крови плода Неспецифические факторы защиты формируются на ранних стадиях онтогенеза.

Иммунная реактивность плода «Работа» иммунной системы: • 13 нед –способность к отторжению трансплантата • Супрессия функции гуморального иммунного ответа (Ат мало) – хорионический гонадотропин, α -фетопротеин, α-2 -глобулин. • Ограничено взаимодействие ИКК. (ВУИ – преждевременная активация)



Иммунная реактивность плода • • Особенности ИС плода Толерантность собственной ИС Пассивный гуморальный иммунитет (Ig. G матери) Несовершенство системы комплемента (30 -50% от показателей взрослых) Система местного иммунитета в раннем и позднем онтогенезе не развита

Иммунный статус детей после рождения • • • Иммунный статус здорового доношенного ребенка, рожденного здоровой матерью Своеобразный пассивный иммунитет новорожденного (Ig. G матери, недостаток Ig. М – риск развития конфликта по изоантигенам и противоинфекционной защите от ГОБ) Физиологический лейкоцитоз - 12 -15 х109 кл/л Лимфоциты - 35%: Т-лимфоциты – низкий % при высоком абсолютном содержании (ТCD 3+ - 60% (ТCD 4+) и 15% (ТCD 8+) Снижено содержание антителозависимых киллеров Недостаточные функции Т-лимфоцитов (РБТЛ на ФГА в норме или снижена, высокий уровень метаболизма по интенсивности синтеза НК)


Иммунный статус детей после рождения Иммунный статус здорового доношенного ребенка, рожденного здоровой матерью • Увеличение численности В-CD 19+ клеток (рецепторы Ig. М и Ig. Е) • Обнаружены Ig. G и Ig. М; Ig. А и Ig. Е –редко выявляются • Ig. М нарастают к 2 -3 неделе жизни ребенка и снижаются к 1 мес и затем медленно возрастают достигая к 6 -12 мес уровня взрослых • Ig. G возрастают к 7 -8 годам (на искусственном вскармливании быстрее) • Ig. А отсутствуют в 1 -ый месяц жизни ребенка, медленно нарастают и к 1 году составляют 28% уровня взрослых. Нормализация к 8 -15 годам. • Ig. Е отсутствуют у новорожденных, постепенно нарастают и достигают нормы к 11 -12 годам. Ускорение их накопления свидетельствует об аллергизации. • Ig. D не определяются у новорожденных, появляются на 6 неделе жизни ребенка и достигают нормы к 5 -10 -15 годам.

Иммунный статус детей после рождения • Содержание иммуноглобулинов определяется суммой Ат различной специфичности: • Первыми появляются Ат к вирусам и бактериофагам, Н-Аг ГОБ микроорганизмов кожи, позднее – на О-Аг ГОБ. • Большое влияние на синтез Ат оказывает нормальная микрофлора ребенка. • Ат-образование идет по первичному типу, требуется большое количество Аг. Замедлено переключение синтеза с Ig. М на Ig. G (5 -20 д у взрослых и 20 -40 д у детей).

Иммунный статус детей после рождения • • Неспецифические факторы защиты: Хемотаксис и функциональная активность фагоцитов снижены Снижена переваривающая способность гранулоцитов за счет незрелости лизосомальных ферментов Снижены уровни комплемента и пропердина Значительно повышена активность лизоцима и его содержание в слюне (до 200 мкг/мл) выше чем в сыворотке. Наибольшее – 1 год, к 6 годам снижается в 3 раза, к 7 -15 годам возрастает но не достигает первоначальных величин.

Иммунный статус детей после рождения • • • Местный иммунитет Ig. А – защита от инфекций s. Ig. А начинает обнаруживаться на 1 -2 неделе жизни ребенка, в копрофильтрате с 3 недели Пополняется за счет молозива и грудного молока, после 3 -5 дней лактации снижается выработка но постоянно пополняется при увеличении употребления грудного молока Плазматические клетки слизистых синтезируют все классы иммуноглобулинов. (стенка кишечника синтезирует до 3 г иммуноглобулинов в сутки) Местный иммунитет формируется 1 -12 годам жизни ребенка.

Иммунный статус детей после рождения • Местный иммунитет обеспечивается и клеточными факторами: • Альвеолярные макрофаги нарастают через 24 часа после рождения и стабилизируется к 1 мес. • Микробицидные свойства макрофагов и др. фагоцитов отстают в первые недели и месяцы жизни ребенка

Иммунный статус детей после рождения ИС в первые годы жизни динамична • После рождения снижается число лейкоцитов, повышается % содержание лимфоцитов и снижаются гранулоциты (перекрест этих показателей на 5 сутки), аналогичный перекрест снижение Лф и повышение нейтрофилов (в 4 -5 лет) • Медленно повышается содержание Тлимфоцитов • В-лимфоциты снижаются до нормы.

Иммунный статус детей после рождения Особенности ИС новорожденного: • Доминирует материнский пассивный иммунитет • Отмечается синтез собственных Ат

Иммунный статус детей после рождения • В 6 -12 месяцев созревает иммунная реактивность (организм ребенка до 1 года плохо защищен от инфекционных агентов. Недостаток клеточного ответа) • В 1 -3 года включается полноценный Т-клеточный иммунитет (полностью начинает работать иногда только к периоду полового созревания) • К 3 -4 годам созревает плазмоцитарная реакция • Учитывая характер становления ИС необходимо с осторожностью назначать иммунотропные препараты в эти возрастные группы, чтобы не извратить естественный ход развития ИС. • «Медленно стартующие дети» у них в воспалительный процесс могут вовлекаться печень и селезенка и другие органы РЭС

Критические периоды развития ИС • 8 -12 нед внутриутробного развития – стартует дифференцировка органов и клеток ИС • I. Период новорожденности – огромное число Аг поступает после рождения ребенка: супрессорное влияние пассивного материнского иммунитета; функциональный дисбаланс CD 3+ (T) лимфоцитов; супрессорная функция незрелых тимоцитов и CD 8+ клеток • II. 3 -6 месяцев – ослабление пассивного иммунитета; супрессорная направленность сохраняется; первичный иммунный ответ на Аг без формирования иммунологической памяти; такой ответ при вакцинации в этот период

Критические периоды развития ИС • III. 1 -ый год жизни – сохраняется первичный характер иммунного ответа на многие Аг; возможно переключение классов иммуноглобулинов с Ig. М на Ig. G, запаздывает образование субклассов Ig. G 2 и Ig. G 4; супрессорная направленность иммунного ответа сменяется хелперной; система местного иммунитета не развита, дети чувствительны к ОРВИ • IV. 4 -6 годы жизни – средняя концентрация Ig. М и Ig. G соответствует таковой у взрослых; Ig. А не достигает нормы; содержание Ig. Е доходит до максимальных величин; высока частота атопических, паразитарных и иммунокомплексных заболеваний.

Критические периоды развития ИС • V. Подростковый возраст (девочки 12 -13 лет, мальчики 14 -15 лет) – пубертатный скачек роста сочетается с уменьшением массы лимфоидных органов; повышение секреции половых гормонов (андрогенов) ведет к подавлению клеточного звена иммунитета и стимуляции гормональных механизмов.

Особенности ИС у детей • • Т-звено иммунитета При рождении лимфоциты - 3 -9 х109 кл/л (2430%); к 4 -5 суткам 2, 5 -10 х109 кл/л (40 -50%) Высокий метаболизм у новорожденных (увеличен синтез ДНК и РНК) БТЛ выражена хорошо как у доношенных так и у недоношенных Высокий уровень спонтанной трансформации (6 -10% тогда как у взрослых 0, 2%)

Особенности ИС у детей • • В-звено иммунитета Начинает активно функционировать при Аг раздражении Ig. G – при рождении их уровень выше чем у матери, ко 2 -3 -й неделе снижается и достигает максимальной концентрации к 1 -4 мес Ig. М – в минимальных количествах при рождении (<0, 2 г/л), к 1 неделе возрастает Ig. А – отсутствует при рождении или следовые концентрации, возрастает к 1 нед.

Особенности ИС у детей Фагоцитарное звено • Нейтрофилы при рождении 4, 5 -20 х109 кл/л (5070%); к 4 дню снижается до 2, 5 -6 х109 кл/л (3040%), поглотительная активность в норме а переваривающая снижена (незавершенный фагоцитоз), низкий фагоцитарный резерв клеток • Моноциты в течение всего периода новорожденности 0, 6 -2 х109 кл/л (4 -9%), низкая бактерицидная активность и недостаточная миграционная способность

Иммунная реактивность при климаксе • Гиперреактивность иммунных реакций по отношению к компонентам яичников. Снижение функции CD 8 -клеток при умеренной активации В-лимфоцитов за счет гиперпродукции Ig. G. • Изменения иммунного статуса у обоих полов в возрасте до 50 лет проявляются снижением «цензорной функции иммунитета» , увеличение риска развития инфекций, аутоиммунных и онкологических заболеваний.

Иммунная реактивность при старении • Как в России, так и во всем мире проблемы старения становятся все более актуальными и в медицинском, и в социальном аспектах: по данным ВОЗ число лиц пожилого и старческого возраста за последние десятки лет увеличилось в 2 раза. • Связь широкого круга возрастных патологических процессов с дефектами иммунной системы привела к предположению, что старение ее может ограничивать продолжительность жизни. • Вместе с тем одной из основных причин старения считают нарушения в функционировании иммунной системы как в целом, так и в отдельных ее звеньях. • С нарушениями работы именно иммунной системы ассоциируются многие заболевания пожилого и старческого возраста, к которым прежде всего относятся аутоиммунные заболевания, опухоли, болезни суставов, почек, амилоидоз, патология сердечно-сосудистой системы, инфекционные заболевания.

Иммунная реактивность при старении • С нарушениями работы иммунной системы ассоциируются многие заболевания пожилого и старческого возраста, к которым прежде всего относятся • аутоиммунные заболевания, • опухоли, • болезни суставов, • почек, • амилоидоз, • патология сердечно-сосудистой системы, • инфекционные заболевания • Дегенерация и гибель клеток – нервной ткани (старческое слабоумие, болезнь Паркинсона).

Иммунная реактивность при старении • Накоплены данные об участии генов системы гистосовместимости в регуляции иммунореактивности и об их связи с патологией. Набор антигенов каждой особи строго индивидуален, фенотип человека определяет особенности функционирования многих органов и систем, и в целом общеповеденческую реакцию при взаимодействии с окружающей средой. • Выявлена связь комплекса гистосовместимости с чувствительностью к вирусным инфекциям, опухолям и аутоиммуным заболеваниям.

Иммунная реактивность при старении • Интерес представляет связь комплекса гистосовместимости HLA c рядом патологических состояний, из которых можно выделить следующие группы: • артропатии, связанные с HLA-В 27 (анкилозирующий спондиллит, реактивный артрит и острый передний увеит); • иммунопатии, связанные с HLA-В 8 и DR 3 (ювенильный диабет, миастения гравис, целиакия, гипертиформный дерматит, аддисонова болезнь, тиреотоксикоз); • заболевания, связанные с фенотипом HLA-В 7, DR 2 (множественный склероз, недостаточность С 4 компонента комплемента).

Иммунная реактивность при старении • На возрастные ослабления функций иммунной системы влияют как экзогенные, так и эндогенные факторы: изменение клеточного окружения (нарушения нейрогуморального равновесия), изменения самих клеток иммунной системы. • Многими исследователями старость рассматривается как Т-иммунодефицит, при этом отмечается достаточно высокий уровень иммунологической резистентности, т. е. можно говорить о сбалансированном Т-иммунодефиците. • Результаты исследований свидетельствуют о том, что характерные для старения изменения в популяции Т-клеток обусловлены возрастной инволюцией тимуса.

Иммунная реактивность при старении • • Доказательством служат следующие факты: ослабление Т-зависимых иммунных функций совпадает с началом инволюции тимуса. С этим ослаблением связано повышение восприимчивости к некоторым инфекциям и склонность к аутоиммунным реакциям; иммунодефицит и аутоиммунитет у мышей, тимэктомированных при рождении, удается предотвратить путем пересадки им сингенного тимуса от молодых животных; больные с первичным иммунодефицитом чаще страдают аутоиммунными заболеваниями, у них чаще возникают злокачественные новообразования; способность тимуса влиять на дифференцировку и созревание Т-клеток с возрастом уменьшается

Иммунная реактивность при старении • Уменьшение количества Т-лимфоцитов, но увеличивается количество молчащих, невостребованных клеток, что связано со снижением активности рецепторного аппарата клетки. • Старение характеризуется более выраженным снижением уровня популяции ТCD 8+клеток и менее выраженным - Т-хелперов (CD 4+ клеток). • Наблюдается дефицит Т-клеток памяти. Снижение активности Т-клеток при старении, по-видимому, является следствием генетически запрограммированной инволюции функции тимуса. • Инволюция тимуса, начинающаяся при половом созревании, это главное возрастное изменение иммунной системы. Инволюция состоит в прогрессивном истощении лимфоидного пула клеток в зонах коры и кистозных изменениях эпителиальных клеток.

Иммунная реактивность при старении • Выход дифференцированных Т-клеток снижается с увеличением возраста. • Прогрессивно снижается синтез и секреция полипептидных гормонов тимуса, таких как тимозин, тимопоэтин и тимулин. Во всех случаях снижение эндокринной активности тимуса играет патогенную роль в возрастных дисфункциях иммунной системы, поскольку заместительная гормонотерапия способна восстановить различные иммунные функции в старости. • По мере возрастной инволюции тимус утрачивает свою способность трансформировать клетки предшественники в зрелые Т-лимфоциты. Возможно, что и снижение активности разных субпопуляций Тлимфоцитов находится под генетическим контролем. • Запрограммированная инволюция функции тимуса играет существенную роль в патогенезе старения.

Иммунная реактивность при старении • Способность к пролиферации Т-клеток от старых индивидуумов снижена, происходит как снижение числа клеток, отвечающих на стимуляцию, так и преждевременное истощение мощности клона отвечающих клеток. • C увеличением возраста прогрессивно снижается концентрация глюкокортикоидных рецепторов в селезенке. Это изменение связано с модификацией лимфоидных клеток, несущих различные плотности рецепторов, или с естественной неспособностью стареющих клеток поддерживать адекватный обмен рецепторных молекул.

Иммунная реактивность при старении • По мере старения обнаруживаются также изменения рецепторов гормонов относительно низкой молекулярной массы, расположенных в мембранах лимфоидных клеток, хотя это больше связано с нарушением сигнальных проводящих систем. Было показано, что количество рецепторных молекул с возрастом снижается, в то время как их аффинные свойства не меняются. • Возможно, что в стареющей популяции с измененной функцией иммунной системы присутствие в пище иммуномодуляторов усиливает дисфункцию иммунной системы, делая стариков более подверженными болезням, связанным с возрастом.

Иммунная реактивность при старении • Инволюционные процессы в тимусе захватывают и В-клеточное звено - как путем взаимодействия клеток в иммунном ответе, так и путем влияния на формирование В-клеток из их предшественников в костном мозге. • В-клеточный иммунодефицит зависит от внутренних дефектов самих В-клеток. • Возрастные изменения гуморального иммунитета выявляются труднее. • Старение ассоциируется с присутствием различных антител, особенно антител против ядерных антигенов. • Старение действует на скорость продукции антител с помощью активированных В-клеток

Иммунная реактивность при старении • Происходит снижение экспрессии антигенов гистосовместимости на Т-лимфоцитах, что способствует снижению распознавания аллоантигенов и дальнейшей передачи информации, необходимой для элиминации антигена и антителопродукции. • Снижается способность Т-клеток продуцировать интерлейкин-2, • Нарушается активность реакции на митогены. • Уменьшение плотности распределения специфических рецепторов на поверхности Т-клеток. • Снижается способность организма распознавать и давать ответ на малые антигены, каковыми являются аллоантигены "малых" эритроцитарных систем и ряда других клеток крови. Это связано суменьшением титра естественных изогемагглютининов.

Иммунная реактивность при старении • Все изложенное объясняет причины некоторой арективности организма в пожилом возрасте в ответ на гемотрансфузионную терапию и вместе с тем требует более углубленных исследований при подборе доноров в случае необходимости интенсивной гемотрансфузионной терапии. • С возрастом развивается дисбаланс иммуноглобулинов. Однозначным при старении является снижение в крови концентрации Ig. M, т. е. снижен первичный гуморальный ответ. • Содержание Ig. G и Ig. A имеет тенденцию к увеличению. При наличии инфекционного процесса особенно возрастает концентрация Ig. A. • Дисбаланс иммуноглобулинов указывает на снижение противомикробной защиты, с этим связано повышение восприимчивости к инфекциям у людей пожилого и старческого возраста.

Иммунная реактивность при старении • Имеются сведения о снижении концентрации лизоцима, активности β-лизина и содержания С 3 -компонента комплемента у пожилых лиц. • Изменения в макрофагальной системе при старении связаны со снижением миграционной способности клеток, с уменьшением числа активных клеток, со снижением интенсивности поглощения и разрушения захваченного материала, т. е. снижением поглотительной и переваривающей способности макрофагов. • Характерно снижение противовирусной и противоопухолевой защиты, что связано с дисбалансом естественных киллеров (ЕК-клетки). Функциональная же их активность после 70 лет, как правило, снижается. Лишь у долгожителей отмечается вновь возрастание активности ЕК-клеток, берущих на себя реакции клеточного иммунитета.

Иммунная реактивность при старении • Изменение спектра вырабатываемых цитокинов, • нарушение созревания иммунного ответа, • снижение аффинности антител, • увеличение перекрестной реактивности, в том числе к собственным антигенам, что ведет к учащению явлений аутоиммунизации в старших возрастных группах.

Иммунная реактивность при старении • Существует теория о том, что старение есть аутоиммунный процесс. • Одной из существенных причин увеличения частоты случаев аутоиммунной патологии в старости, повидимому, является функциональное ослабление иммунологического надзора, с одной стороны, и накопление мутантных клеток, несущих чуждые организму антигены, - с другой, что приводит к гиперпродукции аутоантител. • Предполагается, что этот феномен является либо компенсаторной реакцией (увеличение выведения продуктов распада), либо нарушением контрольных механизмов иммунной системы в пожилом и старческом возрастах. При этом отмечена более высокая смертность в группе носителей аутоантител широкой специфичности.

Иммунная реактивность при старении • Естественное старение - это процесс развития сбалансированного иммунодефицита, увядание всех звеньев иммунной системы. • Болезни в старости усугубляют характерный для пожилых иммунодефицит. • В связи с этим излечение многочисленных старческих недугов, практическое продление жизни человека тесно связано с необходимостью детальной оценки генетического и иммунного статуса больного, поиском и использованием на этой основе эффективной терапии, включающей адекватные средства иммунокоррекции. • Отсрочить начало старения, смягчить проявления болезней пожилого возраста вполне возможно, препятствуя ослаблению нормальных функций иммунитета.
репродукция и возр особен.ppt