Иммунный ответ Антигены В-лимфоциты ГИО Антитела















































2013_ГИО.ppt
- Количество слайдов: 100
 Иммунный ответ Антигены В-лимфоциты ГИО Антитела ШАБАН Ж. Г.
Иммунный ответ Антигены В-лимфоциты ГИО Антитела ШАБАН Ж. Г.
 Иммунитет по возникновению Врождённый Приобретённый
Иммунитет по возникновению Врождённый Приобретённый
 Приобретённый иммунитет обеспечивают Клеточные Гуморальные факторы защиты: - В-л -Т-хелперы - цитотоксические Т-л (ЦТЛ) - АТ (Ig) - иммунный фагоцитоз
Приобретённый иммунитет обеспечивают Клеточные Гуморальные факторы защиты: - В-л -Т-хелперы - цитотоксические Т-л (ЦТЛ) - АТ (Ig) - иммунный фагоцитоз
 Проявления приобретённого иммунитета Антителообразование Иммунный фагоцитоз Киллерная функция Лф Аллергические реакции (ГНТ, ГЗТ) Иммунологическая память Иммунологическая толерантность
Проявления приобретённого иммунитета Антителообразование Иммунный фагоцитоз Киллерная функция Лф Аллергические реакции (ГНТ, ГЗТ) Иммунологическая память Иммунологическая толерантность
 Иммунный ответ (ИО)- сложная многокомпонентная кооперативная реакция организма, индуцированная АГ и направленная на: 1) элиминацию (удаление) АГ 2) формирование иммунологической памяти
Иммунный ответ (ИО)- сложная многокомпонентная кооперативная реакция организма, индуцированная АГ и направленная на: 1) элиминацию (удаление) АГ 2) формирование иммунологической памяти
 На развитие ИО влияют АГ: Условия Свойства Место попадания Состояние внешней Доза ИС среды Кратность попадания (воздействуют и на организм, и на АГ)
На развитие ИО влияют АГ: Условия Свойства Место попадания Состояние внешней Доза ИС среды Кратность попадания (воздействуют и на организм, и на АГ)
 Антигены (АГ) - ü химические вещества (белки, ПС, ЛПС) ü свободные или входящие в состав клеток ü способны индуцировать ИО, в результате которого появляются АТ (ГИО) или сенсибилизированные Лф (КИО)
Антигены (АГ) - ü химические вещества (белки, ПС, ЛПС) ü свободные или входящие в состав клеток ü способны индуцировать ИО, в результате которого появляются АТ (ГИО) или сенсибилизированные Лф (КИО)
 Свойства АГ 1. Иммуногенность – способность индуцировать специфический ИО, в результате которого продуцируются АТ или иммунные Лф На иммуногенность АГ влияют: - чужеродность АГ - химический состав: иммуногенны белки и липопротеины - молекулярная масса или размер молекулы: чем > размер молекулы и её масса, тем иммуногенные свойства 2. Способность специфически взаимодействовать с АТ или клетками, которые образовались на введение этого АГ
Свойства АГ 1. Иммуногенность – способность индуцировать специфический ИО, в результате которого продуцируются АТ или иммунные Лф На иммуногенность АГ влияют: - чужеродность АГ - химический состав: иммуногенны белки и липопротеины - молекулярная масса или размер молекулы: чем > размер молекулы и её масса, тем иммуногенные свойства 2. Способность специфически взаимодействовать с АТ или клетками, которые образовались на введение этого АГ
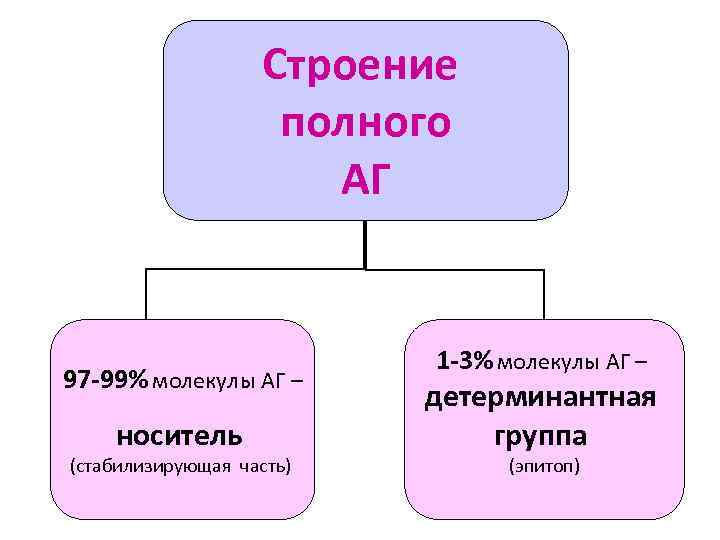
 Строение полного АГ 1 -3% молекулы АГ – 97 -99% молекулы АГ – детерминантная носитель группа (стабилизирующая часть) (эпитоп)
Строение полного АГ 1 -3% молекулы АГ – 97 -99% молекулы АГ – детерминантная носитель группа (стабилизирующая часть) (эпитоп)
 Носитель - обеспечивает иммуногенность АГ Химическая природа: - макромолекулы (белки, нуклеопротеиды, ПС, ЛПС) - клетки (любые) - корпускулярные частицы (в искусственных условиях) Свойства: - высокая молекулярная масса - сложное строение - высокая метаболическая активность Функция: индукция ИО
Носитель - обеспечивает иммуногенность АГ Химическая природа: - макромолекулы (белки, нуклеопротеиды, ПС, ЛПС) - клетки (любые) - корпускулярные частицы (в искусственных условиях) Свойства: - высокая молекулярная масса - сложное строение - высокая метаболическая активность Функция: индукция ИО
 Эпитоп АГ - обусловливает специфичность ИО, комплементарен активному центру АТ или ТКР Химическая природа: любое вещество (олигосахарид, олигопептид, аминогруппа) Свойства: - малая молекулярная масса - жёсткая структура - низкая метаболическая активность - чужеродность для организма Функция: специфичность ИО АГ содержит несколько различных или повторяющихся эпитопов. Один эпитоп или несколько – детерминантная группа. Моновалентный АГ состоит из однородных детерминантных групп, поливалентный АГ - из неоднородных.
Эпитоп АГ - обусловливает специфичность ИО, комплементарен активному центру АТ или ТКР Химическая природа: любое вещество (олигосахарид, олигопептид, аминогруппа) Свойства: - малая молекулярная масса - жёсткая структура - низкая метаболическая активность - чужеродность для организма Функция: специфичность ИО АГ содержит несколько различных или повторяющихся эпитопов. Один эпитоп или несколько – детерминантная группа. Моновалентный АГ состоит из однородных детерминантных групп, поливалентный АГ - из неоднородных.
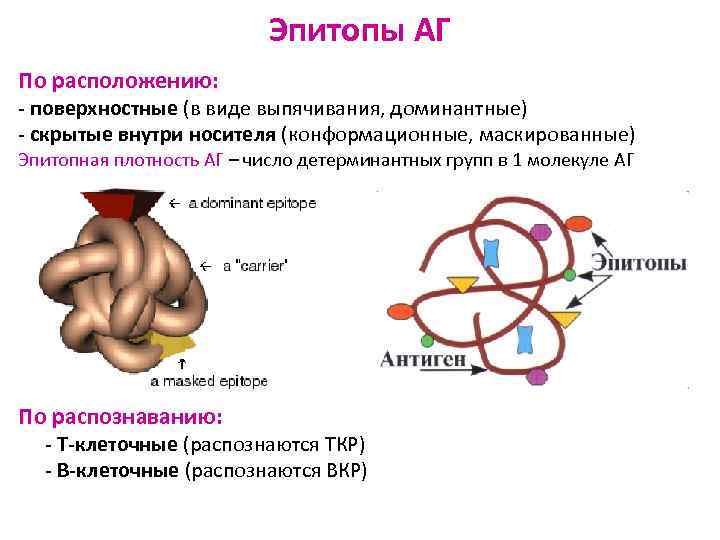
 Эпитопы АГ По расположению: - поверхностные (в виде выпячивания, доминантные) - скрытые внутри носителя (конформационные, маскированные) Эпитопная плотность АГ – число детерминантных групп в 1 молекуле АГ По распознаванию: - Т-клеточные (распознаются ТКР) - В-клеточные (распознаются ВКР)
Эпитопы АГ По расположению: - поверхностные (в виде выпячивания, доминантные) - скрытые внутри носителя (конформационные, маскированные) Эпитопная плотность АГ – число детерминантных групп в 1 молекуле АГ По распознаванию: - Т-клеточные (распознаются ТКР) - В-клеточные (распознаются ВКР)
 Классификации АГ
Классификации АГ
 АГ по функциональной активности Полные (носитель и эпитоп) Неполные (эпитоп)
АГ по функциональной активности Полные (носитель и эпитоп) Неполные (эпитоп)
 Полный АГ: - содержит носитель и эпитоп - обладает антигенностью и иммуногенностью Неполный АГ (=гаптен): - содержит только эпитоп - обладает только антигенностью - не способен индуцировать ИО - может стать полным АГ, если свяжется с носителем
Полный АГ: - содержит носитель и эпитоп - обладает антигенностью и иммуногенностью Неполный АГ (=гаптен): - содержит только эпитоп - обладает только антигенностью - не способен индуцировать ИО - может стать полным АГ, если свяжется с носителем
 АГ по иммуногенности Сильные Слабые Супер. АГ
АГ по иммуногенности Сильные Слабые Супер. АГ
 Адъюванты – вещества, иммуногенность слабых АГ: Неорганические молекулы (Al(OH)3) Бактериальные и растительные ПС и ЛПС Некоторые микробные клетки (вакцина БЦЖ) Минеральные масла Синтетические адъюванты Механизмы действия адъювантов: ü Резкое молекулярной массы АГ ü Для гаптенов адъюванты играют роль носителя ü Медленное высвобождение АГ и > длительное антигенное воздействие ( «депо» АГ) ü Способность вызывать пролиферацию лимфоидной ткани
Адъюванты – вещества, иммуногенность слабых АГ: Неорганические молекулы (Al(OH)3) Бактериальные и растительные ПС и ЛПС Некоторые микробные клетки (вакцина БЦЖ) Минеральные масла Синтетические адъюванты Механизмы действия адъювантов: ü Резкое молекулярной массы АГ ü Для гаптенов адъюванты играют роль носителя ü Медленное высвобождение АГ и > длительное антигенное воздействие ( «депо» АГ) ü Способность вызывать пролиферацию лимфоидной ткани
 Супер. АГ ü АГ МИО, взаимодействующие с молекулами ГКГС II АПК и ТКР Т-л, вне АГ-связывающей щели, т. е. не в активных центрах ü Присоединяются сбоку молекул ГКГС II и ТКР ü Блокируют возможный специфичный ИО, вызывают поликлональную активацию Лф, выброс цитокинов, затем - гибель Т-л
Супер. АГ ü АГ МИО, взаимодействующие с молекулами ГКГС II АПК и ТКР Т-л, вне АГ-связывающей щели, т. е. не в активных центрах ü Присоединяются сбоку молекул ГКГС II и ТКР ü Блокируют возможный специфичный ИО, вызывают поликлональную активацию Лф, выброс цитокинов, затем - гибель Т-л
 Взаимодействие супер. АГ с АПК и Т-л
Взаимодействие супер. АГ с АПК и Т-л
 АГ по степени чужеродности для организма Аутоа. АГ – собственные молекулы организма, на которые отреагировала ИС. Как правило, такая реакция приводит к иммунопатологическим состояниям Аллогенные (гомо. АГ, изо. АГ) – АГ других особей вида Сингенные – от однояйцевых близнецов или клонированных особей Ксеногенные (гетерогенные) – АГ разных видов (для человека – АГ бактерий, растений, вирусов, животных) Комплексные АГ – собственные клетки или молекулы и простые химические вещества
АГ по степени чужеродности для организма Аутоа. АГ – собственные молекулы организма, на которые отреагировала ИС. Как правило, такая реакция приводит к иммунопатологическим состояниям Аллогенные (гомо. АГ, изо. АГ) – АГ других особей вида Сингенные – от однояйцевых близнецов или клонированных особей Ксеногенные (гетерогенные) – АГ разных видов (для человека – АГ бактерий, растений, вирусов, животных) Комплексные АГ – собственные клетки или молекулы и простые химические вещества
 Ауто. АГ ü Поздние белки (молоко, сперма) ü Эмбриональные белки (при онкозаболеваниях, лучевой болезни) ü АГ органов, отделенных ГЭБ (щитовидная железа, стекловидное тело, хрусталик, яичко) ü Собственные ткани, измененные под влиянием внешних факторов (ожог, обморожение, гипоксия, ишемия)
Ауто. АГ ü Поздние белки (молоко, сперма) ü Эмбриональные белки (при онкозаболеваниях, лучевой болезни) ü АГ органов, отделенных ГЭБ (щитовидная железа, стекловидное тело, хрусталик, яичко) ü Собственные ткани, измененные под влиянием внешних факторов (ожог, обморожение, гипоксия, ишемия)
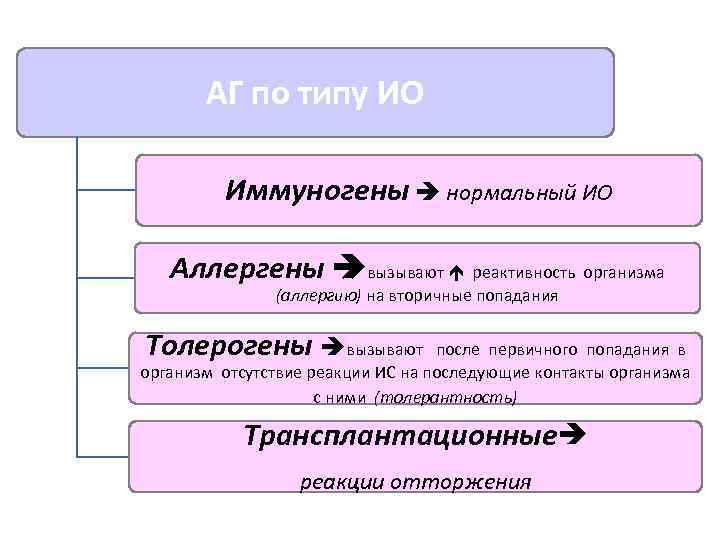
 АГ по типу ИО Иммуногены нормальный ИО Аллергены вызывают реактивность организма (аллергию) на вторичные попадания Толерогены вызывают после первичного попадания в организм отсутствие реакции ИС на последующие контакты организма с ними (толерантность) Трансплантационные реакции отторжения
АГ по типу ИО Иммуногены нормальный ИО Аллергены вызывают реактивность организма (аллергию) на вторичные попадания Толерогены вызывают после первичного попадания в организм отсутствие реакции ИС на последующие контакты организма с ними (толерантность) Трансплантационные реакции отторжения
 АГ по связи ИО с тимусом Т-зависимые Т-независимые
АГ по связи ИО с тимусом Т-зависимые Т-независимые
 АГ по способу попадания в организм Экзогенные (из внешней среды) Эндогенные (из своего организма)
АГ по способу попадания в организм Экзогенные (из внешней среды) Эндогенные (из своего организма)
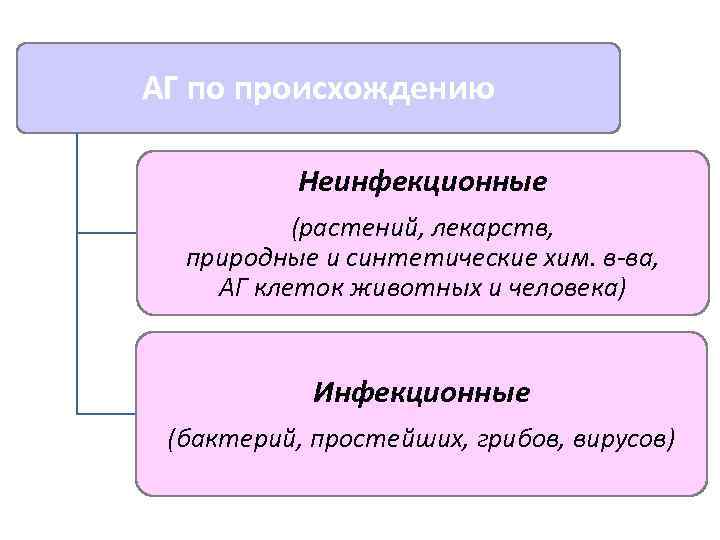
 АГ по происхождению Неинфекционные (растений, лекарств, природные и синтетические хим. в-ва, АГ клеток животных и человека) Инфекционные (бактерий, простейших, грибов, вирусов)
АГ по происхождению Неинфекционные (растений, лекарств, природные и синтетические хим. в-ва, АГ клеток животных и человека) Инфекционные (бактерий, простейших, грибов, вирусов)
 Инфекционные АГ– вещества, обладающие свойствами АГ, входят в состав МИО или выделяются МИО во внешнюю среду Количество АГ зависит от сложности строения МИО: üу простых вирусов полиомиелита – 2 üу сложных вирусов герпеса – 10 üу бактерий – десятки üу грибов – сотни
Инфекционные АГ– вещества, обладающие свойствами АГ, входят в состав МИО или выделяются МИО во внешнюю среду Количество АГ зависит от сложности строения МИО: üу простых вирусов полиомиелита – 2 üу сложных вирусов герпеса – 10 üу бактерий – десятки üу грибов – сотни
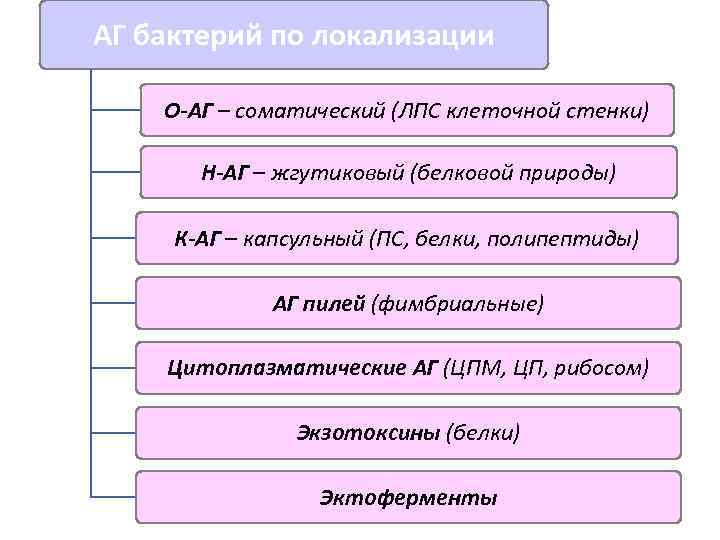
 АГ бактерий по локализации О-АГ – соматический (ЛПС клеточной стенки) Н-АГ – жгутиковый (белковой природы) К-АГ – капсульный (ПС, белки, полипептиды) АГ пилей (фимбриальные) Цитоплазматические АГ (ЦПМ, ЦП, рибосом) Экзотоксины (белки) Эктоферменты
АГ бактерий по локализации О-АГ – соматический (ЛПС клеточной стенки) Н-АГ – жгутиковый (белковой природы) К-АГ – капсульный (ПС, белки, полипептиды) АГ пилей (фимбриальные) Цитоплазматические АГ (ЦПМ, ЦП, рибосом) Экзотоксины (белки) Эктоферменты
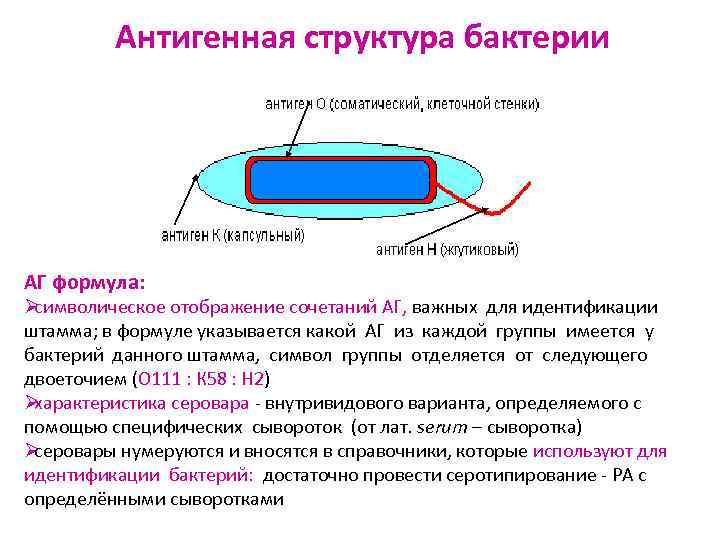
 Антигенная структура бактерии АГ формула: Øсимволическое отображение сочетаний АГ, важных для идентификации штамма; в формуле указывается какой АГ из каждой группы имеется у бактерий данного штамма, символ группы отделяется от следующего двоеточием (О 111 : К 58 : Н 2) Øхарактеристика серовара - внутривидового варианта, определяемого с помощью специфических сывороток (от лат. serum – сыворотка) Øсеровары нумеруются и вносятся в справочники, которые используют для идентификации бактерий: достаточно провести серотипирование - РА с определёнными сыворотками
Антигенная структура бактерии АГ формула: Øсимволическое отображение сочетаний АГ, важных для идентификации штамма; в формуле указывается какой АГ из каждой группы имеется у бактерий данного штамма, символ группы отделяется от следующего двоеточием (О 111 : К 58 : Н 2) Øхарактеристика серовара - внутривидового варианта, определяемого с помощью специфических сывороток (от лат. serum – сыворотка) Øсеровары нумеруются и вносятся в справочники, которые используют для идентификации бактерий: достаточно провести серотипирование - РА с определёнными сыворотками
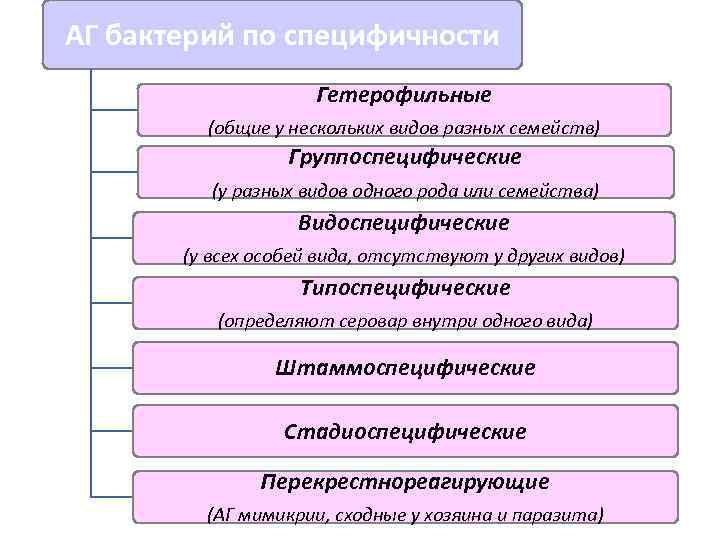
 АГ бактерий по специфичности Гетерофильные (общие у нескольких видов разных семейств) Группоспецифические (у разных видов одного рода или семейства) Видоспецифические (у всех особей вида, отсутствуют у других видов) Типоспецифические (определяют серовар внутри одного вида) Штаммоспецифические Стадиоспецифические Перекрестнореагирующие (АГ мимикрии, сходные у хозяина и паразита)
АГ бактерий по специфичности Гетерофильные (общие у нескольких видов разных семейств) Группоспецифические (у разных видов одного рода или семейства) Видоспецифические (у всех особей вида, отсутствуют у других видов) Типоспецифические (определяют серовар внутри одного вида) Штаммоспецифические Стадиоспецифические Перекрестнореагирующие (АГ мимикрии, сходные у хозяина и паразита)
 Протективные АГ МИО ü Эпитопы экзогенных АГ, АТ против которых обладают наиболее выраженными защитными свойствами, что предохраняет организм от реинфекции ü Используются для получения вакцин
Протективные АГ МИО ü Эпитопы экзогенных АГ, АТ против которых обладают наиболее выраженными защитными свойствами, что предохраняет организм от реинфекции ü Используются для получения вакцин
 2 фактор ИО - состояние ИС ИО определяется кооперативной реакцией клеток: - АПК (Мф, ДК) - В-л - Т-л - фибробластов ИО развивается в периферических лимфоидных органах: - в селезенке - при проникновении АГ в кровь - в регионарных л/у – ч/з кожу - в лимфоидных образованиях слизистых оболочек – при попадании АГ в дыхательные пути или ЖКТ
2 фактор ИО - состояние ИС ИО определяется кооперативной реакцией клеток: - АПК (Мф, ДК) - В-л - Т-л - фибробластов ИО развивается в периферических лимфоидных органах: - в селезенке - при проникновении АГ в кровь - в регионарных л/у – ч/з кожу - в лимфоидных образованиях слизистых оболочек – при попадании АГ в дыхательные пути или ЖКТ
 Иммунный ответ Гуморальный Клеточный (ГИО) (КИО)
Иммунный ответ Гуморальный Клеточный (ГИО) (КИО)
 ГИО – комплексная кооперативная многокомпонентная реакция организма, которая индуцируется АГ и реализуется В-л: ü В процессе эволюции появился позже КИО ü Контролируется ККМ ü Развивается на различные АГ: - растворимые (ПС, ЛПС, белки) - внеклеточных паразитов - экзотоксины Суть ГИО: 1) активация В-л, их дифференцировка в плазматические клетки, которые синтезируют специфические АТ к АГ, вызвавшему ИО 2) образование иммунных комплексов (АГ-АТ) и элиминация АГ
ГИО – комплексная кооперативная многокомпонентная реакция организма, которая индуцируется АГ и реализуется В-л: ü В процессе эволюции появился позже КИО ü Контролируется ККМ ü Развивается на различные АГ: - растворимые (ПС, ЛПС, белки) - внеклеточных паразитов - экзотоксины Суть ГИО: 1) активация В-л, их дифференцировка в плазматические клетки, которые синтезируют специфические АТ к АГ, вызвавшему ИО 2) образование иммунных комплексов (АГ-АТ) и элиминация АГ
 В-система иммунитета ü В-л происходят из гемопоэтической стволовой клетки, дифференцируются в эмбриональной печени, затем в ККМ. У птиц В-л созревают в фабрициевой сумке (bursa) – отсюда название «В-л» . ü Ежедневно образуется около 2, 5 млрд пре-В-л. Большая их часть погибает в результате негативной селекции и апоптоза. Остальные дифференцируются в зрелые В-л (5 х107 в день). ü Популяция периферических В-л обновляется каждые 5 -6 дней. Часть В-л сохраняются месяцы-годы (В-л памяти).
В-система иммунитета ü В-л происходят из гемопоэтической стволовой клетки, дифференцируются в эмбриональной печени, затем в ККМ. У птиц В-л созревают в фабрициевой сумке (bursa) – отсюда название «В-л» . ü Ежедневно образуется около 2, 5 млрд пре-В-л. Большая их часть погибает в результате негативной селекции и апоптоза. Остальные дифференцируются в зрелые В-л (5 х107 в день). ü Популяция периферических В-л обновляется каждые 5 -6 дней. Часть В-л сохраняются месяцы-годы (В-л памяти).
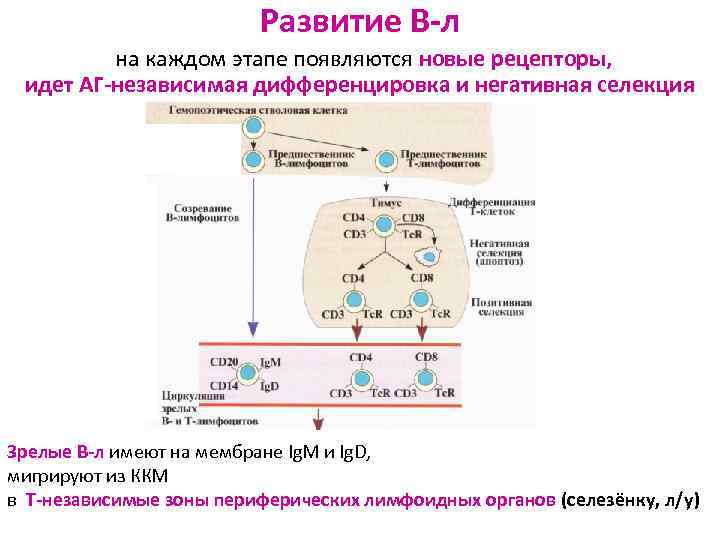
 Развитие В-л на каждом этапе появляются новые рецепторы, идет АГ-независимая дифференцировка и негативная селекция Зрелые В-л имеют на мембране Ig. M и Ig. D, мигрируют из ККМ в Т-независимые зоны периферических лимфоидных органов (селезёнку, л/у)
Развитие В-л на каждом этапе появляются новые рецепторы, идет АГ-независимая дифференцировка и негативная селекция Зрелые В-л имеют на мембране Ig. M и Ig. D, мигрируют из ККМ в Т-независимые зоны периферических лимфоидных органов (селезёнку, л/у)
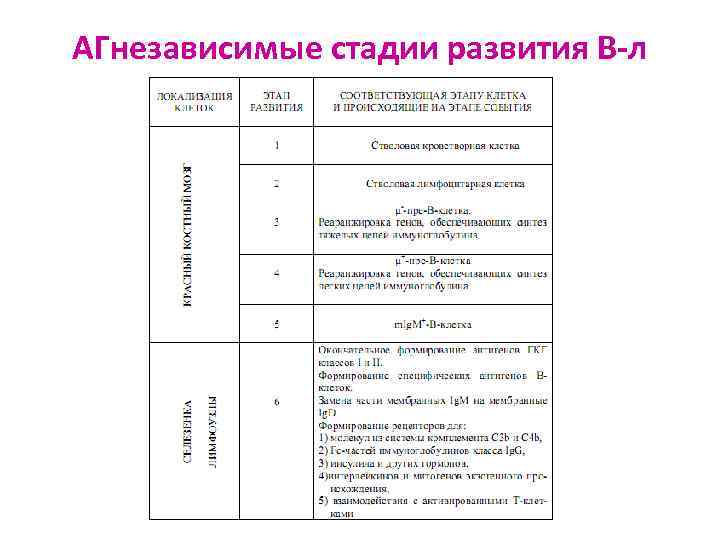
 Этапы развития В-л ü СКК имеет рецепторы для стромальных клеток (VLA 4 и B-CAM) ü пре-В-л: а) ранний - перестраивает D-J гены H-цепи б) поздний: - экспрессирует CD 117 (KIT-рецептор) для фактора роста CКК - перестраивает V-DJ гены H-цепи - экспрессирует рецептор к ИЛ 7 - синтезирует пре-ВКР в) большой - имеет пре-ВКР, состоящий из настоящей H-цепи и суррогатных L-цепей (V-пре-пептид и λ 5 -пептид) г) малый - в ЦП только готовая μ-цепь; перестраивает гены L-цепи ü незрелый В-л имеет BКР (Ig. M) ü зрелый В-л имеет BКР (Ig. M и Ig. D)
Этапы развития В-л ü СКК имеет рецепторы для стромальных клеток (VLA 4 и B-CAM) ü пре-В-л: а) ранний - перестраивает D-J гены H-цепи б) поздний: - экспрессирует CD 117 (KIT-рецептор) для фактора роста CКК - перестраивает V-DJ гены H-цепи - экспрессирует рецептор к ИЛ 7 - синтезирует пре-ВКР в) большой - имеет пре-ВКР, состоящий из настоящей H-цепи и суррогатных L-цепей (V-пре-пептид и λ 5 -пептид) г) малый - в ЦП только готовая μ-цепь; перестраивает гены L-цепи ü незрелый В-л имеет BКР (Ig. M) ü зрелый В-л имеет BКР (Ig. M и Ig. D)
 АГнезависимые стадии развития В-л
АГнезависимые стадии развития В-л
 Субпопуляции В-л üВ-1 - клетки врождённого иммунитета, особенности: 1) на поверхности В 1 -л присутствует только для них характерная молекула CD 5 2) разнообразие В 1 -л по специфичности их АГраспознающих рецепторов (ВКР) значительно , чем у В 2 -л 3) синтезируют естественные (нормальные АТ) – Ig. М и Ig. A: - АТ к ПС УП бактерий - изогемагглютинины групп крови (АВО) 4) после выхода из серозных полостей в кровоток во время миграции по организму оседают преимущественно в миндалинах, брюшной и плевральной полостях, сальнике; в л/узлах их количество не 35 % от всех В-л üВ-2 (17 -30% В-л от общего числа Лф ПК человека) – распознают АГ ПК синтез и секреция специфических АТ
Субпопуляции В-л üВ-1 - клетки врождённого иммунитета, особенности: 1) на поверхности В 1 -л присутствует только для них характерная молекула CD 5 2) разнообразие В 1 -л по специфичности их АГраспознающих рецепторов (ВКР) значительно , чем у В 2 -л 3) синтезируют естественные (нормальные АТ) – Ig. М и Ig. A: - АТ к ПС УП бактерий - изогемагглютинины групп крови (АВО) 4) после выхода из серозных полостей в кровоток во время миграции по организму оседают преимущественно в миндалинах, брюшной и плевральной полостях, сальнике; в л/узлах их количество не 35 % от всех В-л üВ-2 (17 -30% В-л от общего числа Лф ПК человека) – распознают АГ ПК синтез и секреция специфических АТ
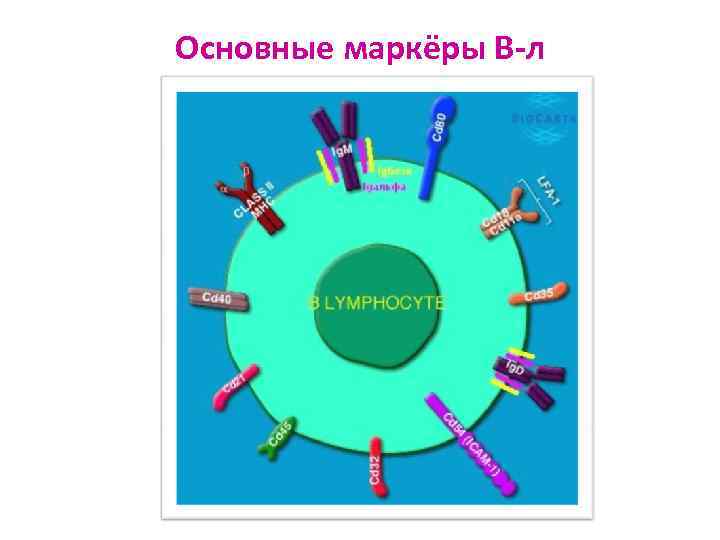
 Поверхностные маркёры В-л 1. Молекулы, вовлеченные в распознавание АГ и сигнальные процессы: а) BКР: поверхностные Ig (собственно BКР) CD 79 α- и β- (проводят в клетку сигнал о распознавании АГ) б) Ко-рецепторы: CD 21 – CRII (для С 3 d) CD 19 CD 81 (TAPA) в) Регулятор активности BКР: CD 45 г) Переключатель изотипа: CD 40
Поверхностные маркёры В-л 1. Молекулы, вовлеченные в распознавание АГ и сигнальные процессы: а) BКР: поверхностные Ig (собственно BКР) CD 79 α- и β- (проводят в клетку сигнал о распознавании АГ) б) Ко-рецепторы: CD 21 – CRII (для С 3 d) CD 19 CD 81 (TAPA) в) Регулятор активности BКР: CD 45 г) Переключатель изотипа: CD 40
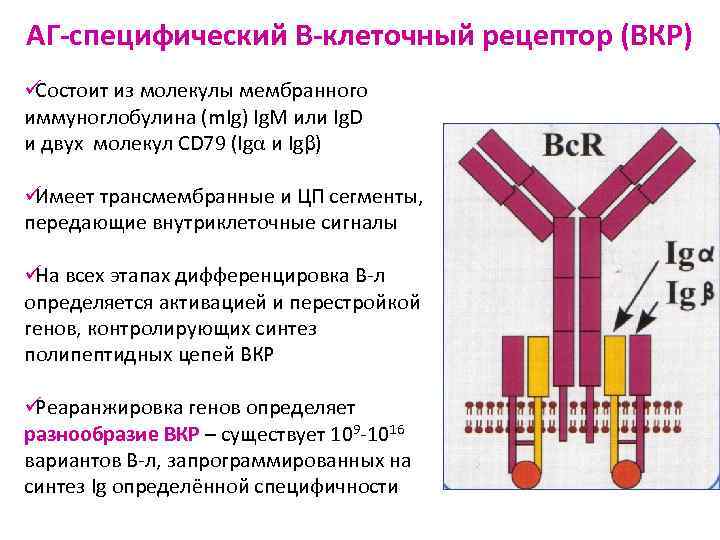
 АГ-специфический В-клеточный рецептор (ВКР) üСостоит из молекулы мембранного иммуноглобулина (m. Ig) Ig. М или Ig. D и двух молекул CD 79 (Igα и Igβ) üИмеет трансмембранные и ЦП сегменты, передающие внутриклеточные сигналы ü всех этапах дифференцировка В-л На определяется активацией и перестройкой генов, контролирующих синтез полипептидных цепей ВКР üРеаранжировка генов определяет разнообразие ВКР – существует 109 -1016 вариантов В-л, запрограммированных на синтез Ig определённой специфичности
АГ-специфический В-клеточный рецептор (ВКР) üСостоит из молекулы мембранного иммуноглобулина (m. Ig) Ig. М или Ig. D и двух молекул CD 79 (Igα и Igβ) üИмеет трансмембранные и ЦП сегменты, передающие внутриклеточные сигналы ü всех этапах дифференцировка В-л На определяется активацией и перестройкой генов, контролирующих синтез полипептидных цепей ВКР üРеаранжировка генов определяет разнообразие ВКР – существует 109 -1016 вариантов В-л, запрограммированных на синтез Ig определённой специфичности
 2. Молекулы контактного межклеточного взаимодействия и презентации а) Адгезия: CD 72 (взаимодействует с CD 5) CD 54 (ICAM 1) (взаимодействует с LFA 1(CD 11 a/CD 18) CD 58(LFA 3) (взаимодействует с CD 2) б) Ко-стимуляция В-л: CD 40 (взаимодействует с CD 154 (CD 40 L)) в) Ко-стимуляция Т-л: CD 80, CD 86 (взаимодействует с CD 28, CTLA) г) Рестрикция: молекулы ГКГС II (взаимодействует с CD 4)
2. Молекулы контактного межклеточного взаимодействия и презентации а) Адгезия: CD 72 (взаимодействует с CD 5) CD 54 (ICAM 1) (взаимодействует с LFA 1(CD 11 a/CD 18) CD 58(LFA 3) (взаимодействует с CD 2) б) Ко-стимуляция В-л: CD 40 (взаимодействует с CD 154 (CD 40 L)) в) Ко-стимуляция Т-л: CD 80, CD 86 (взаимодействует с CD 28, CTLA) г) Рестрикция: молекулы ГКГС II (взаимодействует с CD 4)
 3. Молекулы дистантного взаимодействия – рецепторы для цитокинов: а) рецептор для ИЛ 2 – CD 25, CD 122, CD 132 б) рецептор для ИЛ 4 – CD 124, CD 132 в) рецептор для ИЛ 5 – CD 125, CD 131 г) рецептор для ИЛ 6 – CD 126, CD 130 д) рецептор для INF- – CD 119 е) рецептор для ИЛ 1 – CD 121 ж) рецептор для ФНО-α – CD 120
3. Молекулы дистантного взаимодействия – рецепторы для цитокинов: а) рецептор для ИЛ 2 – CD 25, CD 122, CD 132 б) рецептор для ИЛ 4 – CD 124, CD 132 в) рецептор для ИЛ 5 – CD 125, CD 131 г) рецептор для ИЛ 6 – CD 126, CD 130 д) рецептор для INF- – CD 119 е) рецептор для ИЛ 1 – CD 121 ж) рецептор для ФНО-α – CD 120
 4. Маркёры активации: а) CD 25 и другие высокоаффинные рецепторы к цитокинам б) CD 69 – передача сигнала о пролиферации в) CD 71 – рецептор для трансферрина г) CD 23 – низкоаффинный рецептор для Fc-фрагмента Ig. EII типа, необходим для клеточного деления д) Гиперэкспрессия молекул ГКГС II е) CD 30 – передача сигнала о пролиферации/апоптозе (лиганд-CD 153)
4. Маркёры активации: а) CD 25 и другие высокоаффинные рецепторы к цитокинам б) CD 69 – передача сигнала о пролиферации в) CD 71 – рецептор для трансферрина г) CD 23 – низкоаффинный рецептор для Fc-фрагмента Ig. EII типа, необходим для клеточного деления д) Гиперэкспрессия молекул ГКГС II е) CD 30 – передача сигнала о пролиферации/апоптозе (лиганд-CD 153)
 5. Другие важные молекулы: CD 32 – рецептор к Fc -фрагменту Ig. G II типа – при связывании передает отрицательный сигнал ( активацию) CD 5 – молекула из семейства скавенжер-подобных рецепторов; ассоциирована с ВКР, помогает распознавать/активирует В 1 -л CD 49 – опосредует взаимодействие с внеклеточным матриксом CD 24 – участвует в костимуляции и активации В-л CD 35 – рецептор для комплемента 1 типа (С 3 b)
5. Другие важные молекулы: CD 32 – рецептор к Fc -фрагменту Ig. G II типа – при связывании передает отрицательный сигнал ( активацию) CD 5 – молекула из семейства скавенжер-подобных рецепторов; ассоциирована с ВКР, помогает распознавать/активирует В 1 -л CD 49 – опосредует взаимодействие с внеклеточным матриксом CD 24 – участвует в костимуляции и активации В-л CD 35 – рецептор для комплемента 1 типа (С 3 b)
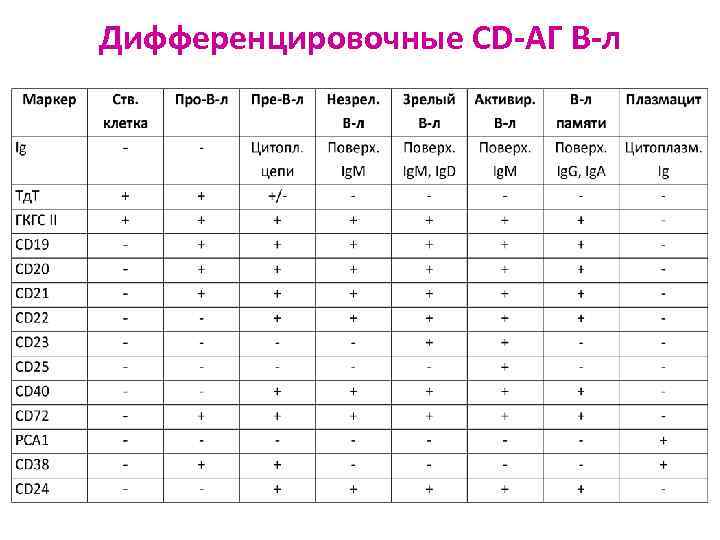
 Дифференцировочные CD-АГ В-л
Дифференцировочные CD-АГ В-л
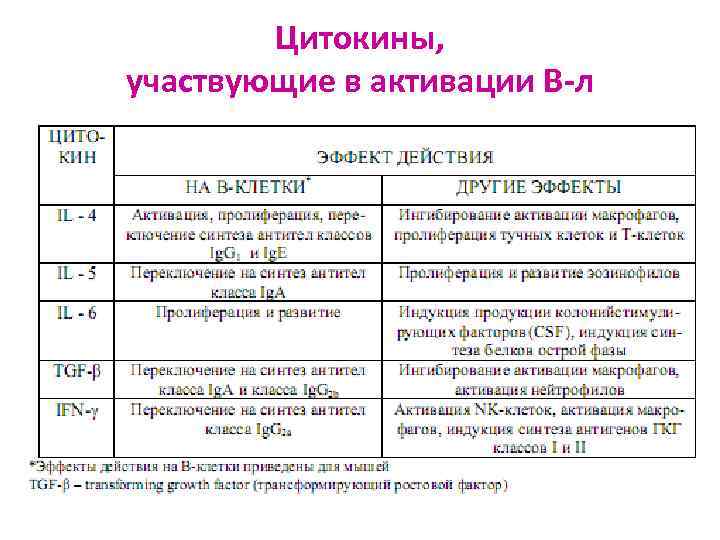
 Цитокины, участвующие в активации В-л
Цитокины, участвующие в активации В-л
 Основные маркёры В-л
Основные маркёры В-л
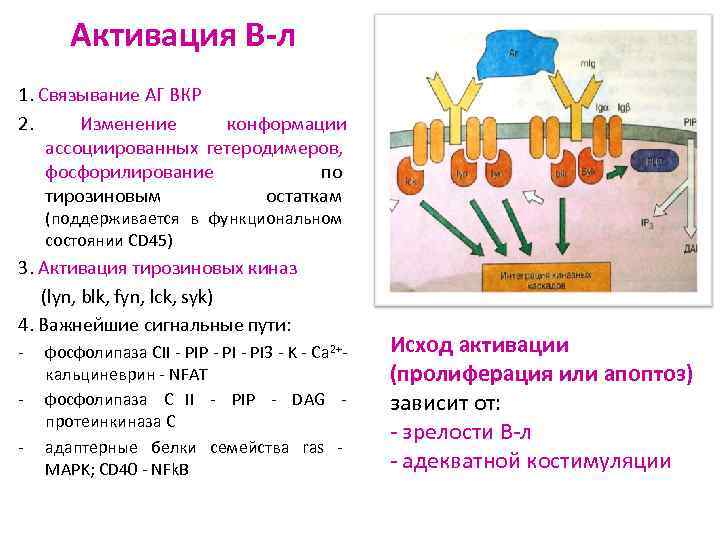
 Активация В-л 1. Связывание АГ BКР 2. Изменение конформации ассоциированных гетеродимеров, фосфорилирование по тирозиновым остаткам (поддерживается в функциональном состоянии CD 45) 3. Активация тирозиновых киназ (lyn, blk, fyn, lck, syk) 4. Важнейшие сигнальные пути: - фосфолипаза СII - PIP - PI 3 - K - Ca 2+- Исход активации кальциневрин - NFAT (пролиферация или апоптоз) - фосфолипаза С II - PIP - DAG - зависит от: протеинкиназа С - зрелости В-л - адаптерные белки семейства ras - MAPK; CD 40 - NFk. B - адекватной костимуляции
Активация В-л 1. Связывание АГ BКР 2. Изменение конформации ассоциированных гетеродимеров, фосфорилирование по тирозиновым остаткам (поддерживается в функциональном состоянии CD 45) 3. Активация тирозиновых киназ (lyn, blk, fyn, lck, syk) 4. Важнейшие сигнальные пути: - фосфолипаза СII - PIP - PI 3 - K - Ca 2+- Исход активации кальциневрин - NFAT (пролиферация или апоптоз) - фосфолипаза С II - PIP - DAG - зависит от: протеинкиназа С - зрелости В-л - адаптерные белки семейства ras - MAPK; CD 40 - NFk. B - адекватной костимуляции
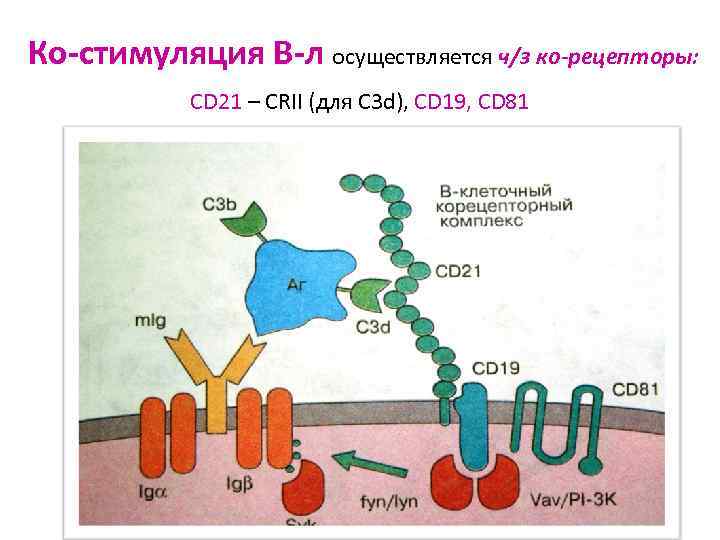
 Ко-стимуляция В-л осуществляется ч/з ко-рецепторы: CD 21 – CRII (для С 3 d), CD 19, CD 81
Ко-стимуляция В-л осуществляется ч/з ко-рецепторы: CD 21 – CRII (для С 3 d), CD 19, CD 81
 Динамика развития ГИО 1. Распознавание, процессинг и презентация АГ в комплексе с АГ ГКГС АПК 2. Индуктивная стадия: а) передача информации на соответствующий клон В-л: - непосредственно (при ответе на ТНЗ АГ) - или (при ответе на ТЗ АГ) при участии CD 4+ Т-л б) активация В-л одним из путей в зависимости от типа АГ (ТЗ АГ и ТНЗ АГ): - Т-независимая активация - выработка АТ без участия Т-л - Т-зависимая активация - ИО осуществляется при обязательном участии Т-л в) пролиферация В-л и дифференцировка в плазмациты и В-л памяти 3. Эффекторная стадия - синтез АТ и элиминация АГ: - образование ИК - комплементзависимый лизис - фагоцитоз
Динамика развития ГИО 1. Распознавание, процессинг и презентация АГ в комплексе с АГ ГКГС АПК 2. Индуктивная стадия: а) передача информации на соответствующий клон В-л: - непосредственно (при ответе на ТНЗ АГ) - или (при ответе на ТЗ АГ) при участии CD 4+ Т-л б) активация В-л одним из путей в зависимости от типа АГ (ТЗ АГ и ТНЗ АГ): - Т-независимая активация - выработка АТ без участия Т-л - Т-зависимая активация - ИО осуществляется при обязательном участии Т-л в) пролиферация В-л и дифференцировка в плазмациты и В-л памяти 3. Эффекторная стадия - синтез АТ и элиминация АГ: - образование ИК - комплементзависимый лизис - фагоцитоз
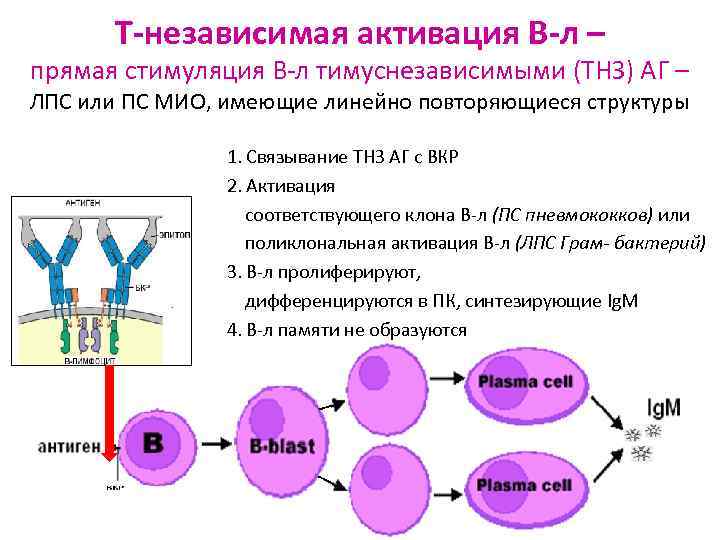
 Т-независимая активация В-л – прямая стимуляция В-л тимуснезависимыми (ТНЗ) АГ – ЛПС или ПС МИО, имеющие линейно повторяющиеся структуры 1. Связывание ТНЗ АГ с ВКР 2. Активация соответствующего клона В-л (ПС пневмококков) или поликлональная активация В-л (ЛПС Грам- бактерий) 3. В-л пролиферируют, дифференцируются в ПК, синтезирующие Ig. M 4. В-л памяти не образуются
Т-независимая активация В-л – прямая стимуляция В-л тимуснезависимыми (ТНЗ) АГ – ЛПС или ПС МИО, имеющие линейно повторяющиеся структуры 1. Связывание ТНЗ АГ с ВКР 2. Активация соответствующего клона В-л (ПС пневмококков) или поликлональная активация В-л (ЛПС Грам- бактерий) 3. В-л пролиферируют, дифференцируются в ПК, синтезирующие Ig. M 4. В-л памяти не образуются
 Распознавание АГ В-л
Распознавание АГ В-л
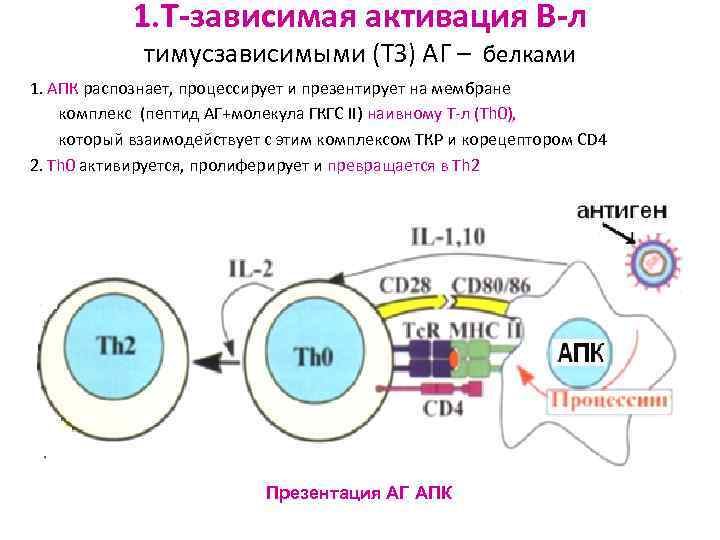
 1. Т-зависимая активация В-л тимусзависимыми (ТЗ) АГ – белками 1. АПК распознает, процессирует и презентирует на мембране комплекс (пептид АГ+молекула ГКГС II) наивному Т-л (Тh 0), который взаимодействует с этим комплексом ТКР и корецептором СD 4 2. Тh 0 активируется, пролиферирует и превращается в Тh 2 Презентация АГ АПК
1. Т-зависимая активация В-л тимусзависимыми (ТЗ) АГ – белками 1. АПК распознает, процессирует и презентирует на мембране комплекс (пептид АГ+молекула ГКГС II) наивному Т-л (Тh 0), который взаимодействует с этим комплексом ТКР и корецептором СD 4 2. Тh 0 активируется, пролиферирует и превращается в Тh 2 Презентация АГ АПК
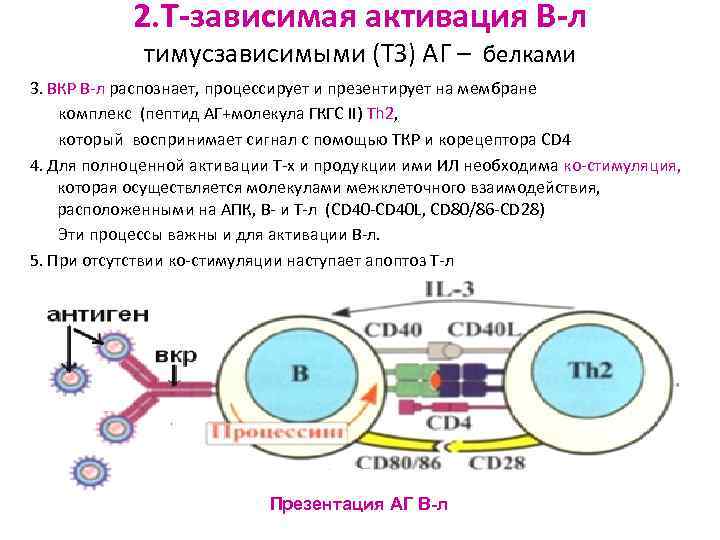
 2. Т-зависимая активация В-л тимусзависимыми (ТЗ) АГ – белками 3. ВКР В-л распознает, процессирует и презентирует на мембране комплекс (пептид АГ+молекула ГКГС II) Тh 2, который воспринимает сигнал с помощью ТКР и корецептора СD 4 4. Для полноценной активации Т-х и продукции ими ИЛ необходима ко-стимуляция, которая осуществляется молекулами межклеточного взаимодействия, расположенными на АПК, В- и Т-л (CD 40 -CD 40 L, CD 80/86 -CD 28) Эти процессы важны и для активации В-л. 5. При отсутствии ко-стимуляции наступает апоптоз Т-л Презентация АГ В-л
2. Т-зависимая активация В-л тимусзависимыми (ТЗ) АГ – белками 3. ВКР В-л распознает, процессирует и презентирует на мембране комплекс (пептид АГ+молекула ГКГС II) Тh 2, который воспринимает сигнал с помощью ТКР и корецептора СD 4 4. Для полноценной активации Т-х и продукции ими ИЛ необходима ко-стимуляция, которая осуществляется молекулами межклеточного взаимодействия, расположенными на АПК, В- и Т-л (CD 40 -CD 40 L, CD 80/86 -CD 28) Эти процессы важны и для активации В-л. 5. При отсутствии ко-стимуляции наступает апоптоз Т-л Презентация АГ В-л
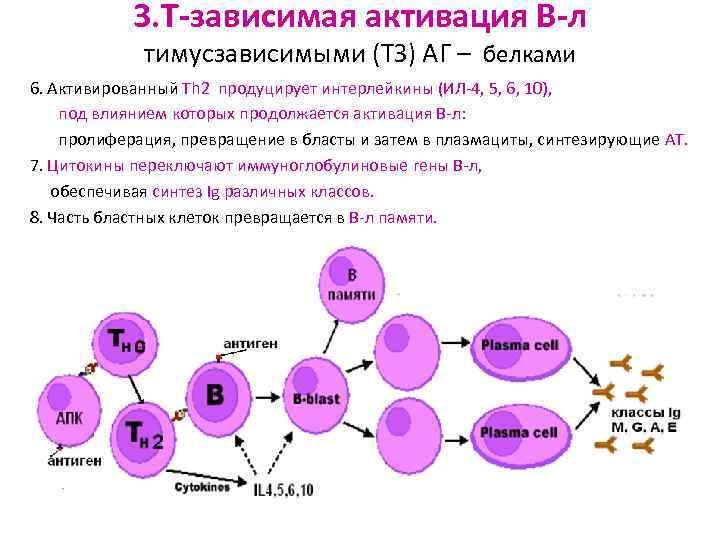
 3. Т-зависимая активация В-л тимусзависимыми (ТЗ) АГ – белками 6. Активированный Тh 2 продуцирует интерлейкины (ИЛ-4, 5, 6, 10), под влиянием которых продолжается активация В-л: пролиферация, превращение в бласты и затем в плазмациты, синтезирующие АТ. 7. Цитокины переключают иммуноглобулиновые гены В-л, обеспечивая синтез Ig различных классов. 8. Часть бластных клеток превращается в В-л памяти.
3. Т-зависимая активация В-л тимусзависимыми (ТЗ) АГ – белками 6. Активированный Тh 2 продуцирует интерлейкины (ИЛ-4, 5, 6, 10), под влиянием которых продолжается активация В-л: пролиферация, превращение в бласты и затем в плазмациты, синтезирующие АТ. 7. Цитокины переключают иммуноглобулиновые гены В-л, обеспечивая синтез Ig различных классов. 8. Часть бластных клеток превращается в В-л памяти.
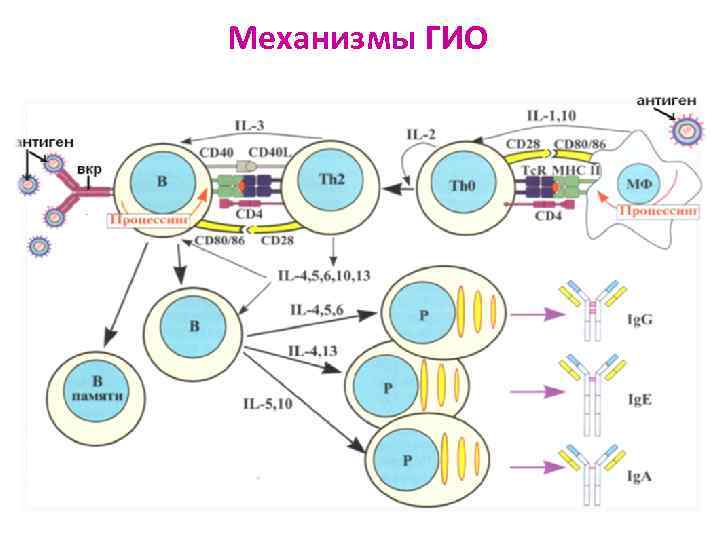
 Механизмы ГИО
Механизмы ГИО
 Плазматические клетки (плазмоциты, = ПК) Ø Большая часть возникающих при делении клеток переходит к продукции и секреции молекул Ig Ø При этом часть клеток успевает пройти генетические перестройки, приводящие к смене класса (изотипа) продуцируемого Ig с Ig. M (или Ig. D) на Ig. A, Ig. G или Ig. E Ø Действие конкретных цитокинов стимулирует переключение продукции АТ с Ig. D: INFγ на Ig. G 1 или Ig. G 3 ИЛ 4 – на Ig. G 4 или Ig. E ИЛ 5 – на Ig. A Ø Представители этого субклона переходят в кровоток (поэтому получили название ПК или плазмоциты) и продуцируют АТ в огромных количествах по заданной генетической программе
Плазматические клетки (плазмоциты, = ПК) Ø Большая часть возникающих при делении клеток переходит к продукции и секреции молекул Ig Ø При этом часть клеток успевает пройти генетические перестройки, приводящие к смене класса (изотипа) продуцируемого Ig с Ig. M (или Ig. D) на Ig. A, Ig. G или Ig. E Ø Действие конкретных цитокинов стимулирует переключение продукции АТ с Ig. D: INFγ на Ig. G 1 или Ig. G 3 ИЛ 4 – на Ig. G 4 или Ig. E ИЛ 5 – на Ig. A Ø Представители этого субклона переходят в кровоток (поэтому получили название ПК или плазмоциты) и продуцируют АТ в огромных количествах по заданной генетической программе
 Особенности ПК – следствие переключения всего метаболизма клетки на единственную задачу – образование и секрецию Ig Ø Крупнее обычных В-л Ø Ядро плотное и по размеру Ø Количество рибосом и элементов комплекса Гольджи сильно Ø Не могут делиться, срок их жизни до нескольких дней Ø Погибают в результате апоптоза, что связывают с невозможностью их перестройки с режима максимальной секреции белка на обычный клеточный метаболизм • Несмотря на быструю гибель ПК, их количество в организме в период выраженного ИО поддерживается на значительном уровне несколько недель • Это объясняется тем, что в каждом клоне небольшое количество активированных В-л сохраняет пролиферативную способность около месяца, давая новые клетки, большая часть которых превращается в ПК • Благодаря таким субклонам существенно уровень ИО и Т АТ данной специфичности
Особенности ПК – следствие переключения всего метаболизма клетки на единственную задачу – образование и секрецию Ig Ø Крупнее обычных В-л Ø Ядро плотное и по размеру Ø Количество рибосом и элементов комплекса Гольджи сильно Ø Не могут делиться, срок их жизни до нескольких дней Ø Погибают в результате апоптоза, что связывают с невозможностью их перестройки с режима максимальной секреции белка на обычный клеточный метаболизм • Несмотря на быструю гибель ПК, их количество в организме в период выраженного ИО поддерживается на значительном уровне несколько недель • Это объясняется тем, что в каждом клоне небольшое количество активированных В-л сохраняет пролиферативную способность около месяца, давая новые клетки, большая часть которых превращается в ПК • Благодаря таким субклонам существенно уровень ИО и Т АТ данной специфичности
 В-л памяти - небольшая популяция клеток, образуются в процессе ПГИО из активированных В-л Ø Возникают в зародышевых центрах вторичных лимфоидных фолликулов под влиянием ФДК Ø Не продуцируют АТ Ø Не делятся Ø Долгоживущие: переживают в состоянии функционального покоя годы-десятилетия после элиминации АГ из организма Ø Несут «память» об АГ в виде АГ-специфических ВКР (Ig. G (преимущественно) и Ig. A в отличие от обычных В-л, экспрессирующих Ig. M и Ig. D)
В-л памяти - небольшая популяция клеток, образуются в процессе ПГИО из активированных В-л Ø Возникают в зародышевых центрах вторичных лимфоидных фолликулов под влиянием ФДК Ø Не продуцируют АТ Ø Не делятся Ø Долгоживущие: переживают в состоянии функционального покоя годы-десятилетия после элиминации АГ из организма Ø Несут «память» об АГ в виде АГ-специфических ВКР (Ig. G (преимущественно) и Ig. A в отличие от обычных В-л, экспрессирующих Ig. M и Ig. D)
 Роль В-л памяти Ø Мигрируют по организму по повторяющейся схеме «кровоток – вторичные лимфоидные органы – кровоток» Ø При попадании в организм АГ, идентичного вызвавшему образование В-л памяти, быстро активируется и даёт начало клону Атпродуцирующих клеток Ø Высокая аффинность и плотность АГ-специфических ВКР (в 100 раз >, чем на нестимулированных АГ В-л) обеспечивает при вторичной стимуляции тем же АГ быструю пролиферацию В-л памяти и превращение в ПК, секретирующие АТ нужный для защиты уровень ИО будет достигнут за очень короткий срок (ВГИО)
Роль В-л памяти Ø Мигрируют по организму по повторяющейся схеме «кровоток – вторичные лимфоидные органы – кровоток» Ø При попадании в организм АГ, идентичного вызвавшему образование В-л памяти, быстро активируется и даёт начало клону Атпродуцирующих клеток Ø Высокая аффинность и плотность АГ-специфических ВКР (в 100 раз >, чем на нестимулированных АГ В-л) обеспечивает при вторичной стимуляции тем же АГ быструю пролиферацию В-л памяти и превращение в ПК, секретирующие АТ нужный для защиты уровень ИО будет достигнут за очень короткий срок (ВГИО)
 ГИО Первичный Вторичный
ГИО Первичный Вторичный
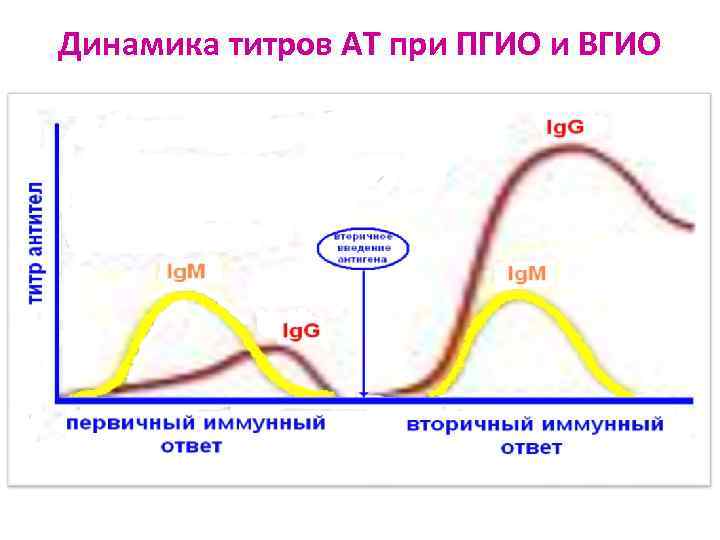
 Первичный ГИО ü Развивается на первое попадание АГ в организм после латентного периода (2 -3 сут). Определённое время уходит на процессинг АГ, перемещения клеток, установление межклеточных контактов, образование клонов Т-х, а затем клонов В-л. ü Когда клоны уже образованы, за счет множества ПК происходит быстрое (логарифмическое) количества АТ, которое продолжается 2 -7 сут. Первыми (ч/з 2 -3 сут) синтезируются Ig. M , затем - Ig. G (пик - 10 -14 сут, при максимальном Т АТ они составляют > 99%). Реализующаяся в ходе ПИО смена классов образующихся АТ объясняется структурой и свойствами Ig. M – пентамеры, имеют 10 АГсвязывающих участков, но заметно уступают Ig. G в способности проходить ч/з стенки капилляров и распространяться по организму. Поэтому в первые часы (сутки) ПИО, когда надо максимально прочно связать незнакомый организму АГ и ограничить его распространение, Ig. M наиболее подходящие. Но в то же время организму приходится необходимо обеспечить защиту всего организма от возможного нового проникновения этого АГ. Для решения этой задачи и образуются в гораздо больших количествах высоко мобильные Ig. G. ü Параллельно отмечается небольшое уровня Ig. A, Ig. E, Ig. D ü Затем количество АТ постепенно и через 2 -3 мес АТ, специфичных к конкретному АГ, практически не остаётся (низкие Т Ig. G могут сохраняться в течение жизни). ü После ПИО остаются В-л памяти
Первичный ГИО ü Развивается на первое попадание АГ в организм после латентного периода (2 -3 сут). Определённое время уходит на процессинг АГ, перемещения клеток, установление межклеточных контактов, образование клонов Т-х, а затем клонов В-л. ü Когда клоны уже образованы, за счет множества ПК происходит быстрое (логарифмическое) количества АТ, которое продолжается 2 -7 сут. Первыми (ч/з 2 -3 сут) синтезируются Ig. M , затем - Ig. G (пик - 10 -14 сут, при максимальном Т АТ они составляют > 99%). Реализующаяся в ходе ПИО смена классов образующихся АТ объясняется структурой и свойствами Ig. M – пентамеры, имеют 10 АГсвязывающих участков, но заметно уступают Ig. G в способности проходить ч/з стенки капилляров и распространяться по организму. Поэтому в первые часы (сутки) ПИО, когда надо максимально прочно связать незнакомый организму АГ и ограничить его распространение, Ig. M наиболее подходящие. Но в то же время организму приходится необходимо обеспечить защиту всего организма от возможного нового проникновения этого АГ. Для решения этой задачи и образуются в гораздо больших количествах высоко мобильные Ig. G. ü Параллельно отмечается небольшое уровня Ig. A, Ig. E, Ig. D ü Затем количество АТ постепенно и через 2 -3 мес АТ, специфичных к конкретному АГ, практически не остаётся (низкие Т Ig. G могут сохраняться в течение жизни). ü После ПИО остаются В-л памяти
 Вторичный ГИО ü За счёт В-л памяти стимуляция синтеза АТ наступает быстро (ч/з 1 -3 сут) ü Т АТ быстро (логарифмически) , сразу синтезируются высокоаффинные Ig. G, их Т достигает максимума на 3– 5 сут. Максимальный Т АТ во много раз >, чем при ПИО. АГ клеткам памяти могут представлять не только Мф, но и другие клетки, что делает ВИО ещё более быстрым. Т происходит в течение большего времени ü На слизистых оболочках значительно уровень s. Ig. A ü Уровень Ig. M существенно не меняется из-за отсутствия В-л памяти с рецептором Ig. M ü Время затухания ВИО значительно >, чем ПИО ü С точки зрения защиты от АГ (возбудителя заболевания) ВИО > эффективен, чем ПИО. Во многих случаях инфекционный процесс останавливается на стадии инкубационного периода и не доходит до стадии проявления симптомов заболевания ü Каждый вновь образовавшийся клон В-л, даёт новые клетки памяти, продлевая уже имеющийся активный иммунитет. Поэтому эффективно защищая себя при второй (третьей и т. д. ) встрече с уже известным АГ, организм обеспечивает себе защиту от возможной последующей встречи с ним. Поэтому по отношению к наиболее распространённым АГ активная защита может поддерживаться в течение всей жизни
Вторичный ГИО ü За счёт В-л памяти стимуляция синтеза АТ наступает быстро (ч/з 1 -3 сут) ü Т АТ быстро (логарифмически) , сразу синтезируются высокоаффинные Ig. G, их Т достигает максимума на 3– 5 сут. Максимальный Т АТ во много раз >, чем при ПИО. АГ клеткам памяти могут представлять не только Мф, но и другие клетки, что делает ВИО ещё более быстрым. Т происходит в течение большего времени ü На слизистых оболочках значительно уровень s. Ig. A ü Уровень Ig. M существенно не меняется из-за отсутствия В-л памяти с рецептором Ig. M ü Время затухания ВИО значительно >, чем ПИО ü С точки зрения защиты от АГ (возбудителя заболевания) ВИО > эффективен, чем ПИО. Во многих случаях инфекционный процесс останавливается на стадии инкубационного периода и не доходит до стадии проявления симптомов заболевания ü Каждый вновь образовавшийся клон В-л, даёт новые клетки памяти, продлевая уже имеющийся активный иммунитет. Поэтому эффективно защищая себя при второй (третьей и т. д. ) встрече с уже известным АГ, организм обеспечивает себе защиту от возможной последующей встречи с ним. Поэтому по отношению к наиболее распространённым АГ активная защита может поддерживаться в течение всей жизни
 Динамика титров АТ при ПГИО и ВГИО
Динамика титров АТ при ПГИО и ВГИО
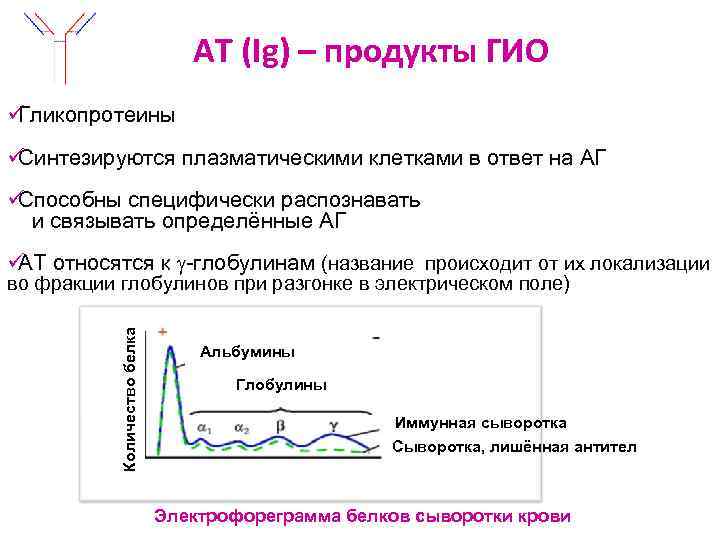
 АТ (Ig) – продукты ГИО üГликопротеины üСинтезируются плазматическими клетками в ответ на АГ üСпособны специфически распознавать и связывать определённые АГ ü относятся к -глобулинам (название происходит от их локализации АТ во фракции глобулинов при разгонке в электрическом поле) Количество белка Альбумины Глобулины Иммунная сыворотка Сыворотка, лишённая антител Электрофореграмма белков сыворотки крови
АТ (Ig) – продукты ГИО üГликопротеины üСинтезируются плазматическими клетками в ответ на АГ üСпособны специфически распознавать и связывать определённые АГ ü относятся к -глобулинам (название происходит от их локализации АТ во фракции глобулинов при разгонке в электрическом поле) Количество белка Альбумины Глобулины Иммунная сыворотка Сыворотка, лишённая антител Электрофореграмма белков сыворотки крови
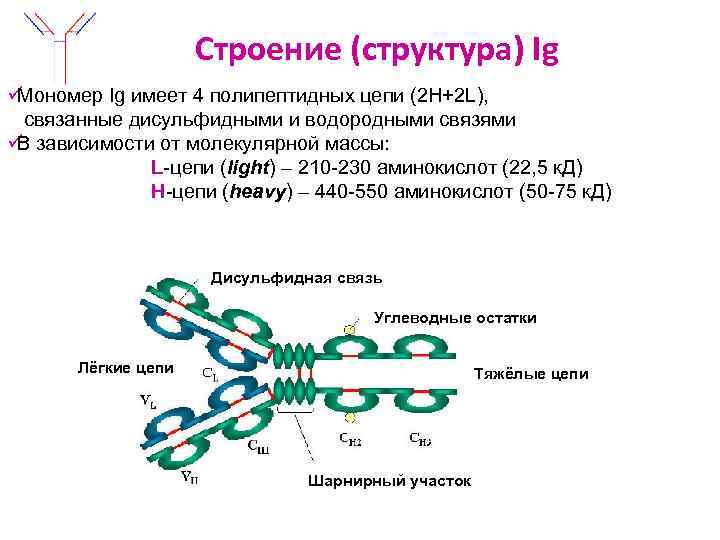
 Строение (структура) Ig üМономер Ig имеет 4 полипептидных цепи (2 Н+2 L), связанные дисульфидными и водородными связями ü зависимости от молекулярной массы: В L-цепи (light) – 210 -230 аминокислот (22, 5 к. Д) H-цепи (heavy) – 440 -550 аминокислот (50 -75 к. Д) Дисульфидная связь Углеводные остатки Лёгкие цепи Тяжёлые цепи Шарнирный участок
Строение (структура) Ig üМономер Ig имеет 4 полипептидных цепи (2 Н+2 L), связанные дисульфидными и водородными связями ü зависимости от молекулярной массы: В L-цепи (light) – 210 -230 аминокислот (22, 5 к. Д) H-цепи (heavy) – 440 -550 аминокислот (50 -75 к. Д) Дисульфидная связь Углеводные остатки Лёгкие цепи Тяжёлые цепи Шарнирный участок
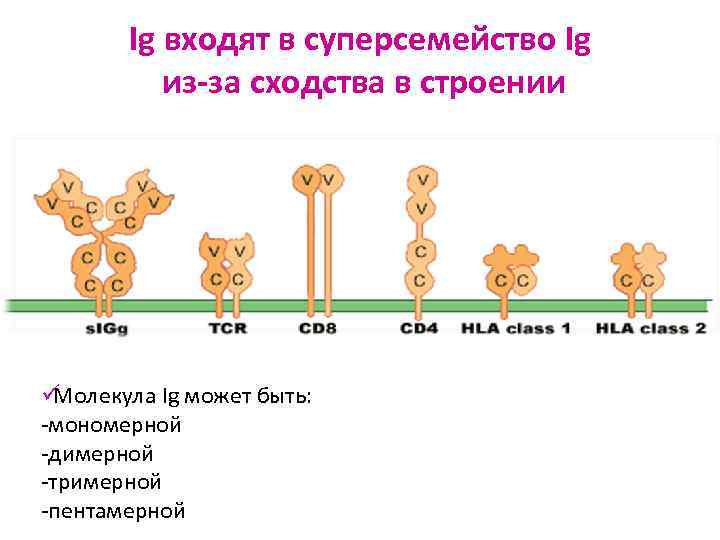
 Ig входят в суперсемейство Ig из-за сходства в строении ü Молекула Ig может быть: -мономерной -димерной -тримерной -пентамерной
Ig входят в суперсемейство Ig из-за сходства в строении ü Молекула Ig может быть: -мономерной -димерной -тримерной -пентамерной
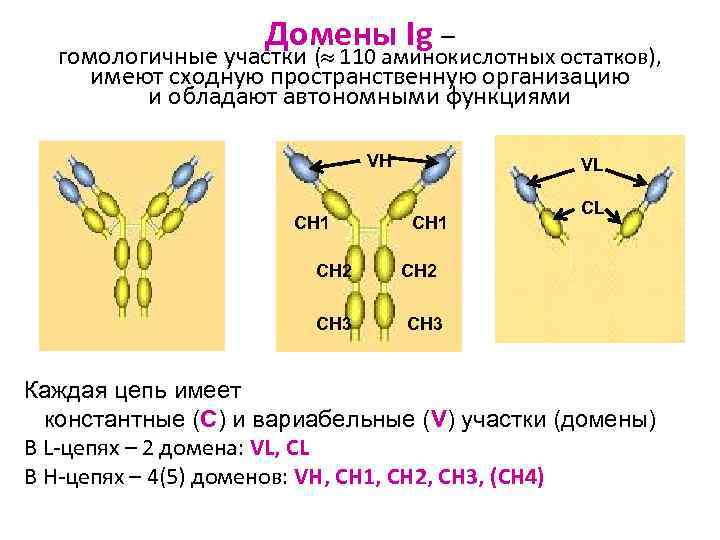
 Домены Ig – гомологичные участки ( 110 аминокислотных остатков), имеют сходную пространственную организацию и обладают автономными функциями VH VL CL CH 1 CH 2 CH 3 Каждая цепь имеет константные (С) и вариабельные (V) участки (домены) В L-цепях – 2 домена: VL, CL В H-цепях – 4(5) доменов: VH, CH 1, CH 2, CH 3, (CH 4)
Домены Ig – гомологичные участки ( 110 аминокислотных остатков), имеют сходную пространственную организацию и обладают автономными функциями VH VL CL CH 1 CH 2 CH 3 Каждая цепь имеет константные (С) и вариабельные (V) участки (домены) В L-цепях – 2 домена: VL, CL В H-цепях – 4(5) доменов: VH, CH 1, CH 2, CH 3, (CH 4)
 Типы лёгких (L) цепей Ig ü κ (каппа) - 2/3 молекул Ig ü λ (лямбда) - 1/3 молекул Ig ØВходят в состав Ig независимо от класса Ø одной молекуле Ig не могут присутствовать L-цепи обоих типов В Ø Цепи κ и λ: - отличаются аминокислотными последовательностями - Функционально идентичны
Типы лёгких (L) цепей Ig ü κ (каппа) - 2/3 молекул Ig ü λ (лямбда) - 1/3 молекул Ig ØВходят в состав Ig независимо от класса Ø одной молекуле Ig не могут присутствовать L-цепи обоих типов В Ø Цепи κ и λ: - отличаются аминокислотными последовательностями - Функционально идентичны
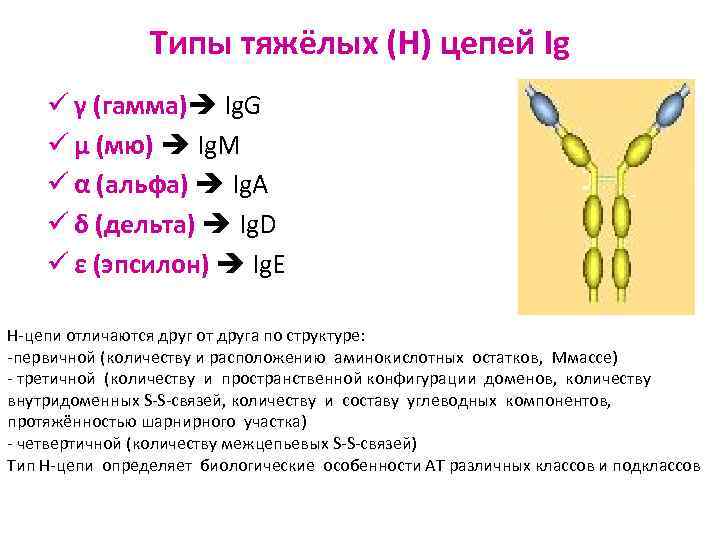
 Типы тяжёлых (H) цепей Ig ü γ (гамма) Ig. G ü μ (мю) Ig. М ü α (альфа) Ig. А ü δ (дельта) Ig. D ü ε (эпсилон) Ig. Е H-цепи отличаются друг от друга по структуре: -первичной (количеству и расположению аминокислотных остатков, Mмассе) - третичной (количеству и пространственной конфигурации доменов, количеству внутридоменных S-S-связей, количеству и составу углеводных компонентов, протяжённостью шарнирного участка) - четвертичной (количеству межцепьевых S-S-связей) Тип H-цепи определяет биологические особенности АТ различных классов и подклассов
Типы тяжёлых (H) цепей Ig ü γ (гамма) Ig. G ü μ (мю) Ig. М ü α (альфа) Ig. А ü δ (дельта) Ig. D ü ε (эпсилон) Ig. Е H-цепи отличаются друг от друга по структуре: -первичной (количеству и расположению аминокислотных остатков, Mмассе) - третичной (количеству и пространственной конфигурации доменов, количеству внутридоменных S-S-связей, количеству и составу углеводных компонентов, протяжённостью шарнирного участка) - четвертичной (количеству межцепьевых S-S-связей) Тип H-цепи определяет биологические особенности АТ различных классов и подклассов
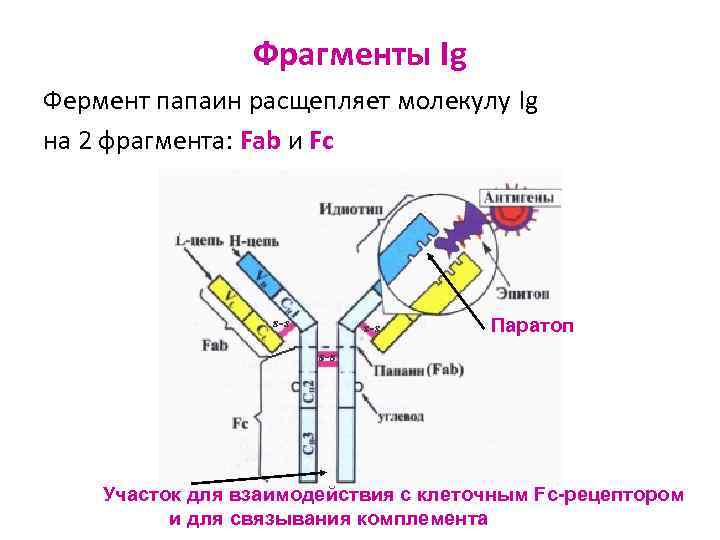
 Фрагменты Ig Фермент папаин расщепляет молекулу Ig на 2 фрагмента: Fab и Fc Паратоп Участок для взаимодействия с клеточным Fc-рецептором и для связывания комплемента
Фрагменты Ig Фермент папаин расщепляет молекулу Ig на 2 фрагмента: Fab и Fc Паратоп Участок для взаимодействия с клеточным Fc-рецептором и для связывания комплемента
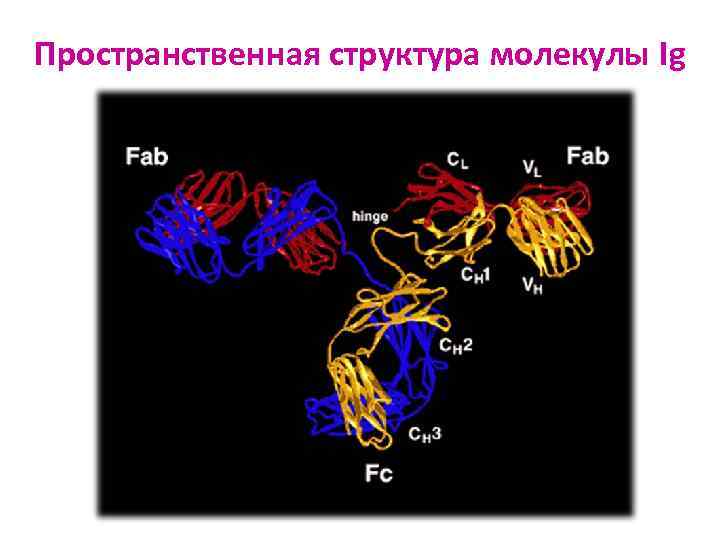
 Пространственная структура молекулы Ig
Пространственная структура молекулы Ig
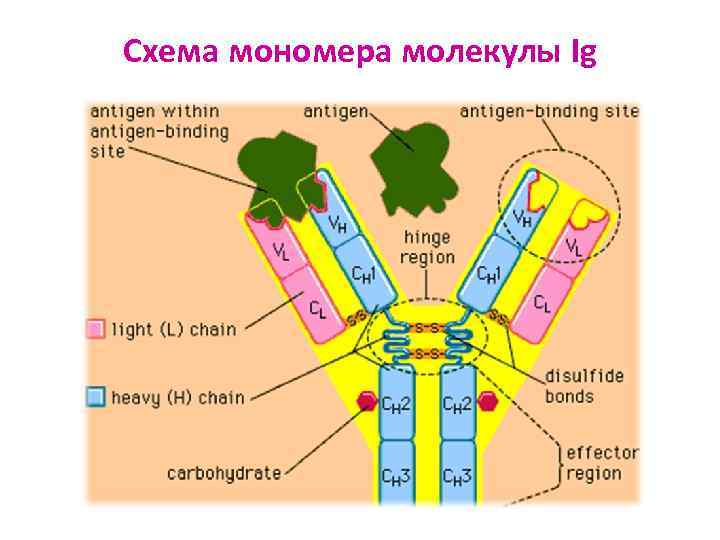
 Схема мономера молекулы Ig
Схема мономера молекулы Ig
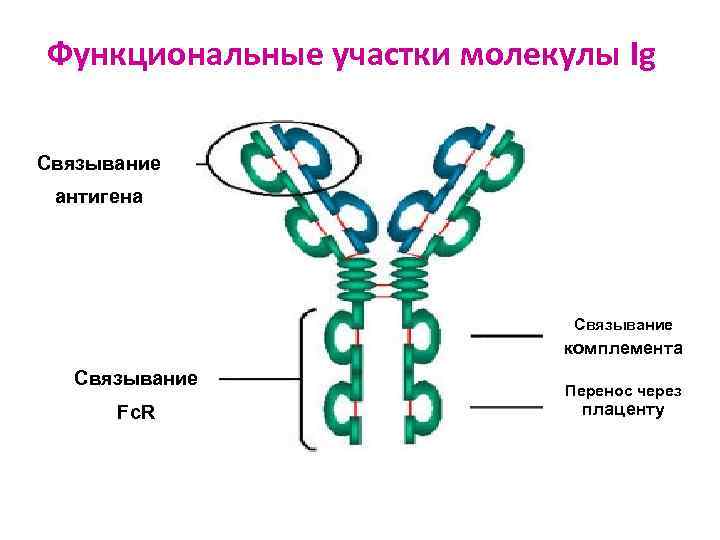
 Функциональные участки молекулы Ig Связывание антигена Связывание комплемента Связывание Перенос через Fc. R плаценту
Функциональные участки молекулы Ig Связывание антигена Связывание комплемента Связывание Перенос через Fc. R плаценту
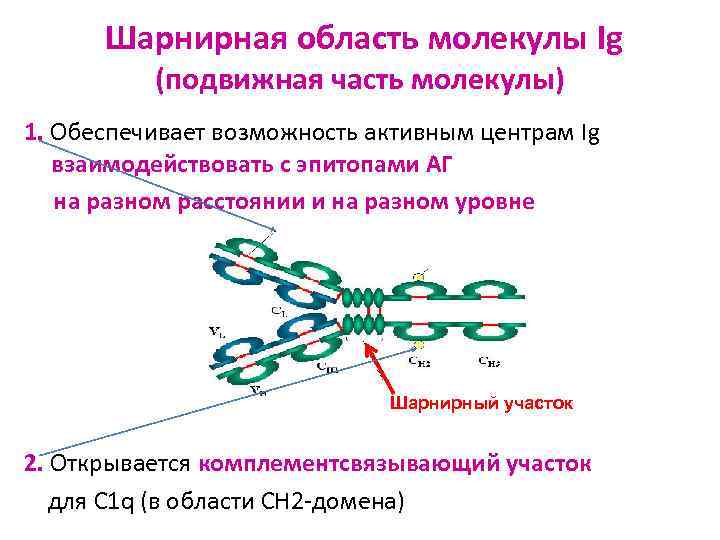
 Шарнирная область молекулы Ig (подвижная часть молекулы) 1. Обеспечивает возможность активным центрам Ig взаимодействовать с эпитопами АГ на разном расстоянии и на разном уровне Шарнирный участок 2. Открывается комплементсвязывающий участок для C 1 q (в области CH 2 -домена)
Шарнирная область молекулы Ig (подвижная часть молекулы) 1. Обеспечивает возможность активным центрам Ig взаимодействовать с эпитопами АГ на разном расстоянии и на разном уровне Шарнирный участок 2. Открывается комплементсвязывающий участок для C 1 q (в области CH 2 -домена)
 Fab-фрагмент Ig – fragment antigen binding ü Связывает эпитопы АГ ü АГ-связывающий участок Fab-фрагмента Ig образован гипервариабельными (часты замены аминокислот) участками в V-доменах Н- и L-цепей (в каждой цепи – по 3 гипервариабельных участка) ü Это активный центр молекулы Ig, паратоп АТ, CDR (complementarity determining region = область, определяющая комплементарность к антигенным эпитопам) – полость (длина 6 нм, ширина 1 -1, 7 нм, глубина 0, 6 -0, 7 нм), в которую входит эпитоп АГ
Fab-фрагмент Ig – fragment antigen binding ü Связывает эпитопы АГ ü АГ-связывающий участок Fab-фрагмента Ig образован гипервариабельными (часты замены аминокислот) участками в V-доменах Н- и L-цепей (в каждой цепи – по 3 гипервариабельных участка) ü Это активный центр молекулы Ig, паратоп АТ, CDR (complementarity determining region = область, определяющая комплементарность к антигенным эпитопам) – полость (длина 6 нм, ширина 1 -1, 7 нм, глубина 0, 6 -0, 7 нм), в которую входит эпитоп АГ
 Fс-фрагмент Ig (сristallisable - кристаллизабельный) 1. Взаимодействует с Fc-рецепторами клеток: ü моноцитов и Мф ü нейтрофилов, эозинофилов, базофилов, тучных клеток ü ЕК ü ДК ü клеток эндотелия ü В- и Т-л 2. Обеспечивает транспорт Ig. G ч/з плаценту путём рецепторного эндоцитоза 3. Связывает комплемент (Ig. G и Ig. M)
Fс-фрагмент Ig (сristallisable - кристаллизабельный) 1. Взаимодействует с Fc-рецепторами клеток: ü моноцитов и Мф ü нейтрофилов, эозинофилов, базофилов, тучных клеток ü ЕК ü ДК ü клеток эндотелия ü В- и Т-л 2. Обеспечивает транспорт Ig. G ч/з плаценту путём рецепторного эндоцитоза 3. Связывает комплемент (Ig. G и Ig. M)
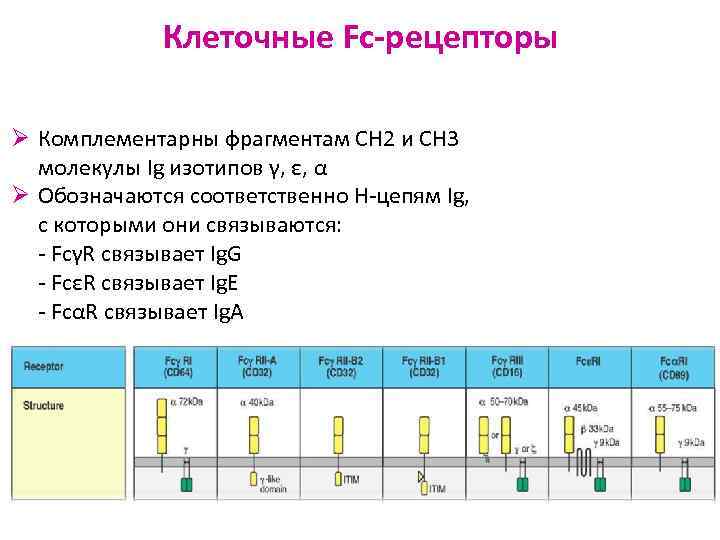
 Клеточные Fc-рецепторы Ø Комплементарны фрагментам СН 2 и СН 3 молекулы Ig изотипов γ, ε, α Ø Обозначаются соответственно Н-цепям Ig, с которыми они связываются: - FcγR связывает Ig. G - FcεR связывает Ig. E - FcαR связывает Ig. A
Клеточные Fc-рецепторы Ø Комплементарны фрагментам СН 2 и СН 3 молекулы Ig изотипов γ, ε, α Ø Обозначаются соответственно Н-цепям Ig, с которыми они связываются: - FcγR связывает Ig. G - FcεR связывает Ig. E - FcαR связывает Ig. A
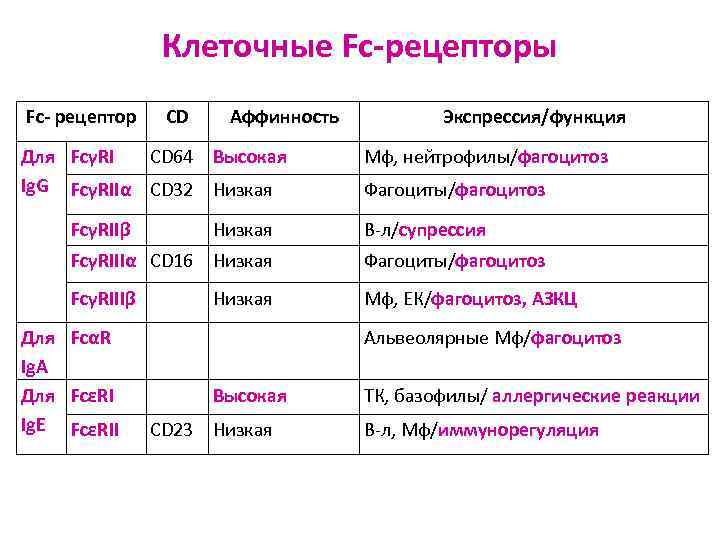
 Клеточные Fc-рецепторы Fc- рецептор CD Аффинность Экспрессия/функция Для FcγRI CD 64 Высокая Мф, нейтрофилы/фагоцитоз Ig. G FcγRIIα CD 32 Низкая Фагоциты/фагоцитоз FcγRIIβ Низкая В-л/супрессия FcγRIIIα CD 16 Низкая Фагоциты/фагоцитоз FcγRIIIβ Низкая Мф, ЕК/фагоцитоз, АЗКЦ Для FcαR Альвеолярные Мф/фагоцитоз Ig. A Для FcεRI Высокая ТК, базофилы/ аллергические реакции Ig. E FcεRII CD 23 Низкая В-л, Мф/иммунорегуляция
Клеточные Fc-рецепторы Fc- рецептор CD Аффинность Экспрессия/функция Для FcγRI CD 64 Высокая Мф, нейтрофилы/фагоцитоз Ig. G FcγRIIα CD 32 Низкая Фагоциты/фагоцитоз FcγRIIβ Низкая В-л/супрессия FcγRIIIα CD 16 Низкая Фагоциты/фагоцитоз FcγRIIIβ Низкая Мф, ЕК/фагоцитоз, АЗКЦ Для FcαR Альвеолярные Мф/фагоцитоз Ig. A Для FcεRI Высокая ТК, базофилы/ аллергические реакции Ig. E FcεRII CD 23 Низкая В-л, Мф/иммунорегуляция
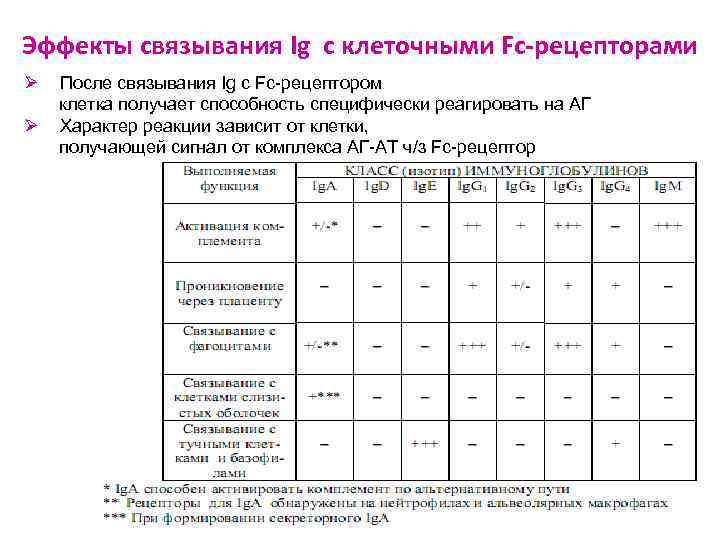
 Эффекты связывания Ig с клеточными Fс-рецепторами Ø После связывания Ig с Fc-рецептором клетка получает способность специфически реагировать на АГ Ø Характер реакции зависит от клетки, получающей сигнал от комплекса АГ-АТ ч/з Fc-рецептор
Эффекты связывания Ig с клеточными Fс-рецепторами Ø После связывания Ig с Fc-рецептором клетка получает способность специфически реагировать на АГ Ø Характер реакции зависит от клетки, получающей сигнал от комплекса АГ-АТ ч/з Fc-рецептор
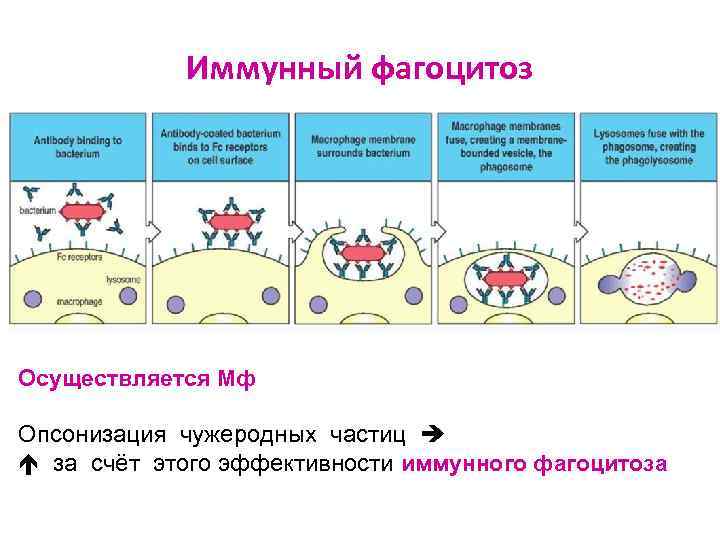
 Иммунный фагоцитоз Осуществляется Мф Опсонизация чужеродных частиц за счёт этого эффективности иммунного фагоцитоза
Иммунный фагоцитоз Осуществляется Мф Опсонизация чужеродных частиц за счёт этого эффективности иммунного фагоцитоза
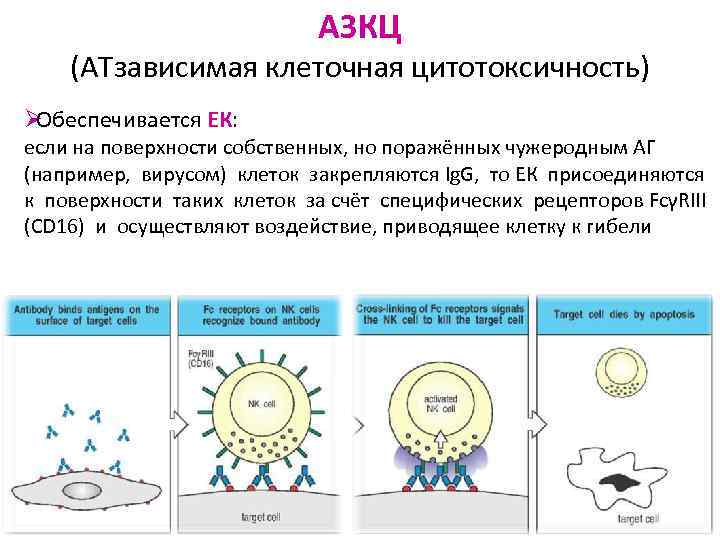
 АЗКЦ (АТзависимая клеточная цитотоксичность) ØОбеспечивается ЕК: если на поверхности собственных, но поражённых чужеродным АГ (например, вирусом) клеток закрепляются Ig. G, то ЕК присоединяются к поверхности таких клеток за счёт специфических рецепторов FcγRIII (CD 16) и осуществляют воздействие, приводящее клетку к гибели
АЗКЦ (АТзависимая клеточная цитотоксичность) ØОбеспечивается ЕК: если на поверхности собственных, но поражённых чужеродным АГ (например, вирусом) клеток закрепляются Ig. G, то ЕК присоединяются к поверхности таких клеток за счёт специфических рецепторов FcγRIII (CD 16) и осуществляют воздействие, приводящее клетку к гибели
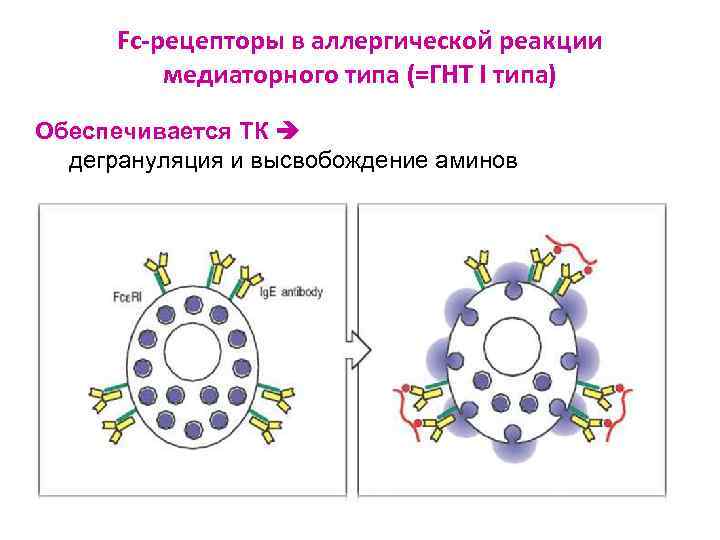
 Fc-рецепторы в аллергической реакции медиаторного типа (=ГНТ I типа) Обеспечивается ТК дегрануляция и высвобождение аминов
Fc-рецепторы в аллергической реакции медиаторного типа (=ГНТ I типа) Обеспечивается ТК дегрануляция и высвобождение аминов
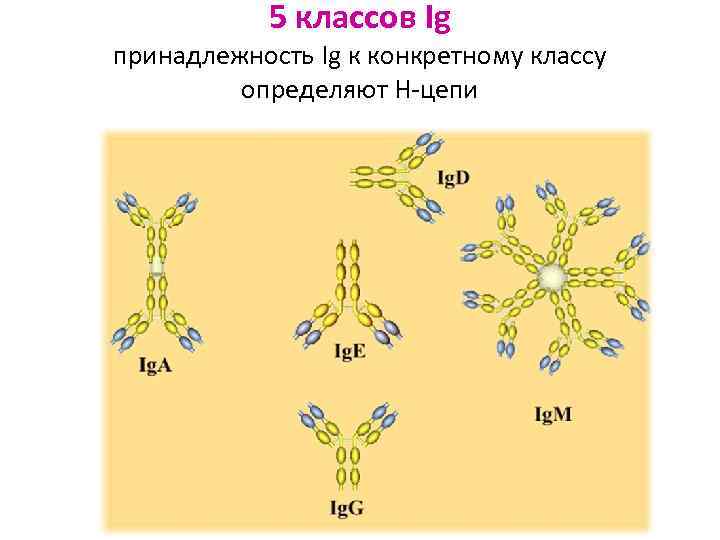
 5 классов Ig принадлежность Ig к конкретному классу определяют H-цепи
5 классов Ig принадлежность Ig к конкретному классу определяют H-цепи
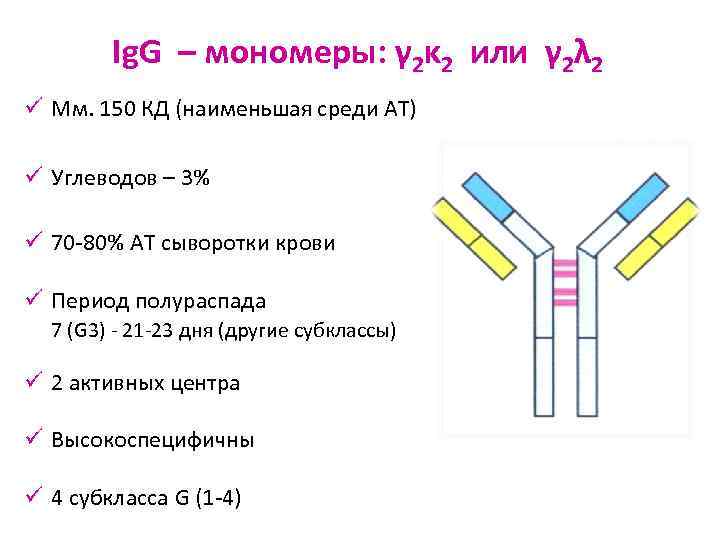
 Ig. G – мономеры: γ 2κ 2 или γ 2λ 2 ü Мм. 150 КД (наименьшая среди АТ) ü Углеводов – 3% ü 70 -80% АТ сыворотки крови ü Период полураспада 7 (G 3) - 21 -23 дня (другие субклассы) ü 2 активных центра ü Высокоспецифичны ü 4 субкласса G (1 -4)
Ig. G – мономеры: γ 2κ 2 или γ 2λ 2 ü Мм. 150 КД (наименьшая среди АТ) ü Углеводов – 3% ü 70 -80% АТ сыворотки крови ü Период полураспада 7 (G 3) - 21 -23 дня (другие субклассы) ü 2 активных центра ü Высокоспецифичны ü 4 субкласса G (1 -4)
 Функции Ig. G Ø Основные молекулы, обеспечивающие ГИ: - при развитии ПИО к 10 суткам почти полностью заменяют появляющиеся первыми Ig. М - ВИО практически сразу начинается с их продукции Ø Опсонины: - Fab-фрагментами присоединяются к фагоцитируемому объекту - на поверхности фагоцитов много рецепторов к H-цепям типа γ Fс-фрагмент Ig. G связывается с Мф, нейтрофилами Ø Связывание с ЕК (Fс-фрагмент) АЗКЦ Ø КП активации комплемента (Fс-фрагмент) комплементзависимая цитотоксичность Ø Нейтрализация токсинов и вирусов Ø Участие в реакции агглютинации Ø Преодолевают барьеры между кровью и тканями, передаются траснплацентарно, обеспечивает защиту новорожденного в первые месяцы жизни (естественный пассивный иммунитет)
Функции Ig. G Ø Основные молекулы, обеспечивающие ГИ: - при развитии ПИО к 10 суткам почти полностью заменяют появляющиеся первыми Ig. М - ВИО практически сразу начинается с их продукции Ø Опсонины: - Fab-фрагментами присоединяются к фагоцитируемому объекту - на поверхности фагоцитов много рецепторов к H-цепям типа γ Fс-фрагмент Ig. G связывается с Мф, нейтрофилами Ø Связывание с ЕК (Fс-фрагмент) АЗКЦ Ø КП активации комплемента (Fс-фрагмент) комплементзависимая цитотоксичность Ø Нейтрализация токсинов и вирусов Ø Участие в реакции агглютинации Ø Преодолевают барьеры между кровью и тканями, передаются траснплацентарно, обеспечивает защиту новорожденного в первые месяцы жизни (естественный пассивный иммунитет)
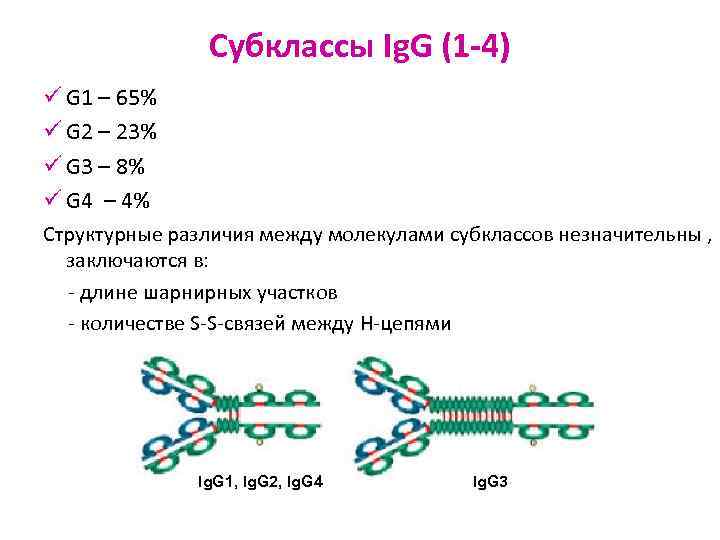
 Субклассы Ig. G (1 -4) ü G 1 – 65% ü G 2 – 23% ü G 3 – 8% ü G 4 – 4% Структурные различия между молекулами субклассов незначительны , заключаются в: - длине шарнирных участков - количестве S-S-связей между H-цепями Ig. G 1, Ig. G 2, Ig. G 4 Ig. G 3
Субклассы Ig. G (1 -4) ü G 1 – 65% ü G 2 – 23% ü G 3 – 8% ü G 4 – 4% Структурные различия между молекулами субклассов незначительны , заключаются в: - длине шарнирных участков - количестве S-S-связей между H-цепями Ig. G 1, Ig. G 2, Ig. G 4 Ig. G 3
 Функциональные особенности субклассов Ig. G Ø Ig. G 2 обладает наименьшим сродством к Fcγ-рецепторам на поверхности клеток хуже остальных Ig. G проходит ч/з плаценту и фагоцитоз Ø Ig. G 3 и Ig. G 1 - наилучшие опсонины и активаторы комплемента Ø Ig. G 4: - не способны активировать комплемент, - обладают сродством к рецепторам на поверхности ТК и базофилов, это свойство Ig. G 4 сближает их с Ig. Е и делает причастными к развитию ГНТ
Функциональные особенности субклассов Ig. G Ø Ig. G 2 обладает наименьшим сродством к Fcγ-рецепторам на поверхности клеток хуже остальных Ig. G проходит ч/з плаценту и фагоцитоз Ø Ig. G 3 и Ig. G 1 - наилучшие опсонины и активаторы комплемента Ø Ig. G 4: - не способны активировать комплемент, - обладают сродством к рецепторам на поверхности ТК и базофилов, это свойство Ig. G 4 сближает их с Ig. Е и делает причастными к развитию ГНТ
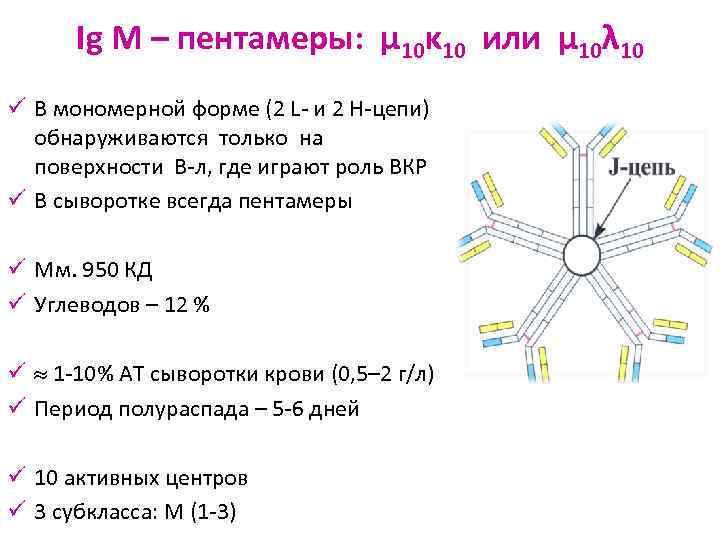
 Ig M – пентамеры: μ 10κ 10 или μ 10λ 10 ü В мономерной форме (2 L- и 2 H-цепи) обнаруживаются только на поверхности В-л, где играют роль BКР ü В сыворотке всегда пентамеры ü Мм. 950 КД ü Углеводов – 12 % ü 1 -10% АТ сыворотки крови (0, 5– 2 г/л) ü Период полураспада – 5 -6 дней ü 10 активных центров ü 3 субкласса: М (1 -3)
Ig M – пентамеры: μ 10κ 10 или μ 10λ 10 ü В мономерной форме (2 L- и 2 H-цепи) обнаруживаются только на поверхности В-л, где играют роль BКР ü В сыворотке всегда пентамеры ü Мм. 950 КД ü Углеводов – 12 % ü 1 -10% АТ сыворотки крови (0, 5– 2 г/л) ü Период полураспада – 5 -6 дней ü 10 активных центров ü 3 субкласса: М (1 -3)
 Функции Ig. M ü Образуются только на первых этапах ПИО ü Поверхностный рецептор В-л (мономерные формы) ü Первыми появляются при первичном попадании АГ ü Основной класс АТ, синтезируемых у новорожденных и младенцев ü КП активации комплемента (Fс-фрагмент) комплементзависимая цитотоксичность ü Пентамеры Ig. М имеют 10 АГсвязывающих участков прочнее связывают АГ с несколькими повторяющимися АГ детерминантами достаточно 1 молекулы пентамера Ig. М для участия в РА, РП, РСК ü Благодаря наличию j-цепи Ig. М (как и Ig. А) попадают в секреты слизистых ü Недостаточно мобильны: имея большую Ммассу и сложную пространственную конфигурацию, медленнее диффундируют и хуже, чем мономеры, преодолевают барьеры между кровью и тканями
Функции Ig. M ü Образуются только на первых этапах ПИО ü Поверхностный рецептор В-л (мономерные формы) ü Первыми появляются при первичном попадании АГ ü Основной класс АТ, синтезируемых у новорожденных и младенцев ü КП активации комплемента (Fс-фрагмент) комплементзависимая цитотоксичность ü Пентамеры Ig. М имеют 10 АГсвязывающих участков прочнее связывают АГ с несколькими повторяющимися АГ детерминантами достаточно 1 молекулы пентамера Ig. М для участия в РА, РП, РСК ü Благодаря наличию j-цепи Ig. М (как и Ig. А) попадают в секреты слизистых ü Недостаточно мобильны: имея большую Ммассу и сложную пространственную конфигурацию, медленнее диффундируют и хуже, чем мономеры, преодолевают барьеры между кровью и тканями
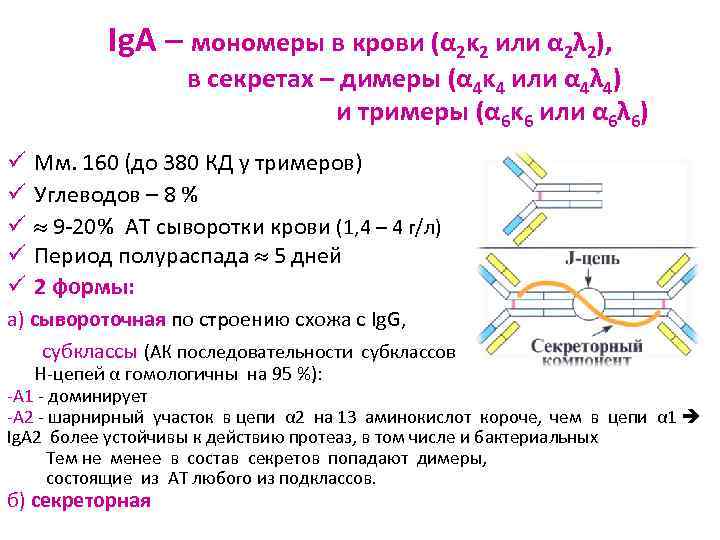
 Ig. A – мономеры в крови (α 2κ 2 или α 2λ 2), в секретах – димеры (α 4κ 4 или α 4λ 4) и тримеры (α 6κ 6 или α 6λ 6) ü Мм. 160 (до 380 КД у тримеров) ü Углеводов – 8 % ü 9 -20% АТ сыворотки крови (1, 4 – 4 г/л) ü Период полураспада 5 дней ü 2 формы: а) сывороточная по строению схожа с Ig. G, субклассы (АК последовательности субклассов H-цепей α гомологичны на 95 %): -А 1 - доминирует -А 2 - шарнирный участок в цепи α 2 на 13 аминокислот короче, чем в цепи α 1 Ig. А 2 более устойчивы к действию протеаз, в том числе и бактериальных Тем не менее в состав секретов попадают димеры, состоящие из АТ любого из подклассов. б) секреторная
Ig. A – мономеры в крови (α 2κ 2 или α 2λ 2), в секретах – димеры (α 4κ 4 или α 4λ 4) и тримеры (α 6κ 6 или α 6λ 6) ü Мм. 160 (до 380 КД у тримеров) ü Углеводов – 8 % ü 9 -20% АТ сыворотки крови (1, 4 – 4 г/л) ü Период полураспада 5 дней ü 2 формы: а) сывороточная по строению схожа с Ig. G, субклассы (АК последовательности субклассов H-цепей α гомологичны на 95 %): -А 1 - доминирует -А 2 - шарнирный участок в цепи α 2 на 13 аминокислот короче, чем в цепи α 1 Ig. А 2 более устойчивы к действию протеаз, в том числе и бактериальных Тем не менее в состав секретов попадают димеры, состоящие из АТ любого из подклассов. б) секреторная
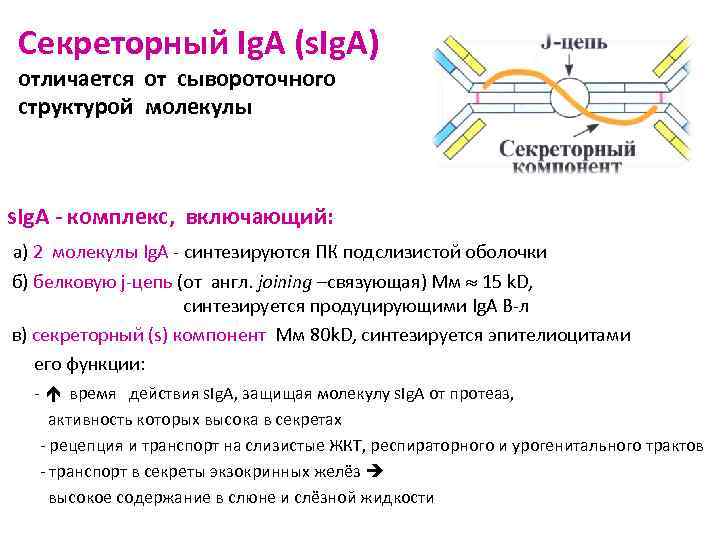
 Секреторный Ig. A (s. Ig. A) отличается от сывороточного структурой молекулы s. Ig. A - комплекс, включающий: а) 2 молекулы Ig. A - синтезируются ПК подслизистой оболочки б) белковую j-цепь (от англ. joining –связующая) Мм 15 k. D, синтезируется продуцирующими Ig. A В-л в) секреторный (s) компонент Мм 80 k. D, синтезируется эпителиоцитами его функции: - время действия s. Ig. A, защищая молекулу s. Ig. A от протеаз, активность которых высока в секретах - рецепция и транспорт на слизистые ЖКТ, респираторного и урогенитального трактов - транспорт в секреты экзокринных желёз высокое содержание в слюне и слёзной жидкости
Секреторный Ig. A (s. Ig. A) отличается от сывороточного структурой молекулы s. Ig. A - комплекс, включающий: а) 2 молекулы Ig. A - синтезируются ПК подслизистой оболочки б) белковую j-цепь (от англ. joining –связующая) Мм 15 k. D, синтезируется продуцирующими Ig. A В-л в) секреторный (s) компонент Мм 80 k. D, синтезируется эпителиоцитами его функции: - время действия s. Ig. A, защищая молекулу s. Ig. A от протеаз, активность которых высока в секретах - рецепция и транспорт на слизистые ЖКТ, респираторного и урогенитального трактов - транспорт в секреты экзокринных желёз высокое содержание в слюне и слёзной жидкости
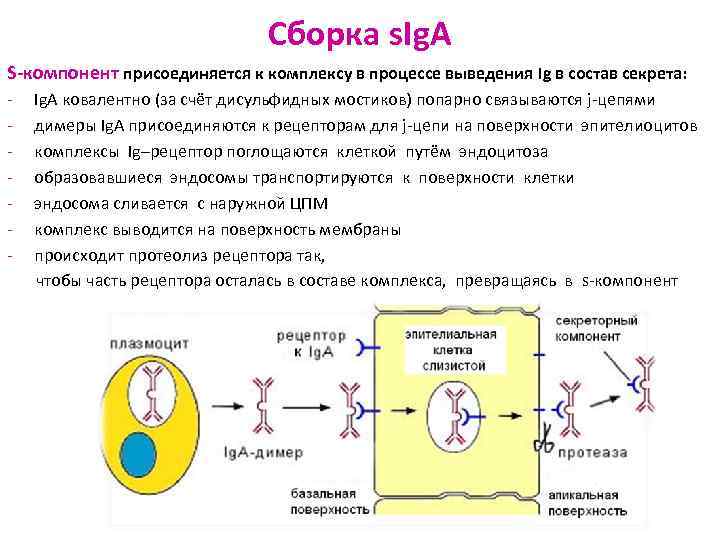
 Сборка s. Ig. A S-компонент присоединяется к комплексу в процессе выведения Ig в состав секрета: - Ig. A ковалентно (за счёт дисульфидных мостиков) попарно связываются j-цепями - димеры Ig. A присоединяются к рецепторам для j-цепи на поверхности эпителиоцитов - комплексы Ig–рецептор поглощаются клеткой путём эндоцитоза - образовавшиеся эндосомы транспортируются к поверхности клетки - эндосома сливается с наружной ЦПМ - комплекс выводится на поверхность мембраны - происходит протеолиз рецептора так, чтобы часть рецептора осталась в составе комплекса, превращаясь в s-компонент
Сборка s. Ig. A S-компонент присоединяется к комплексу в процессе выведения Ig в состав секрета: - Ig. A ковалентно (за счёт дисульфидных мостиков) попарно связываются j-цепями - димеры Ig. A присоединяются к рецепторам для j-цепи на поверхности эпителиоцитов - комплексы Ig–рецептор поглощаются клеткой путём эндоцитоза - образовавшиеся эндосомы транспортируются к поверхности клетки - эндосома сливается с наружной ЦПМ - комплекс выводится на поверхность мембраны - происходит протеолиз рецептора так, чтобы часть рецептора осталась в составе комплекса, превращаясь в s-компонент
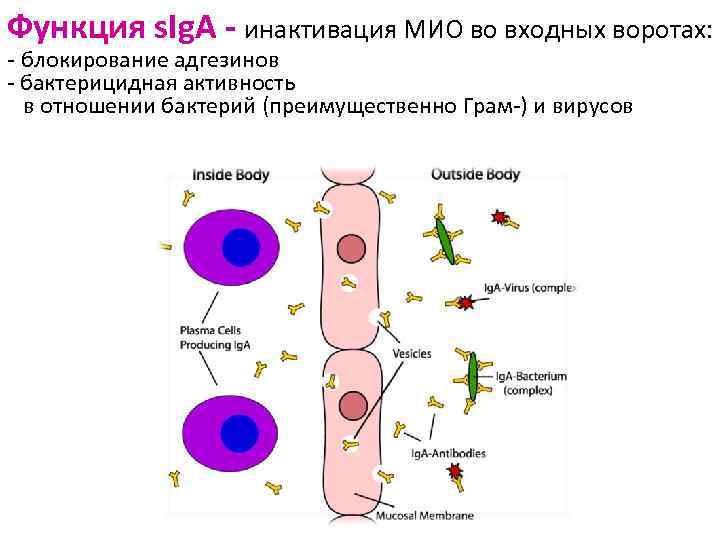
 Функция s. Ig. A - инактивация МИО во входных воротах: - блокирование адгезинов - бактерицидная активность в отношении бактерий (преимущественно Грам-) и вирусов
Функция s. Ig. A - инактивация МИО во входных воротах: - блокирование адгезинов - бактерицидная активность в отношении бактерий (преимущественно Грам-) и вирусов
 Ig. E – мономеры: ε 2κ 2 или ε 2λ 2 ü Мм. 185 КД ü Углеводов – 12 % ü Наименьшее количество АТ сыворотки крови: 0, 003% (0, 014 -0, 45 г/л) ü Период полураспада – 2, 5 дня (фиксированный в тканях – 28 дней) ü 2 активных центра, 4 С-домена в H-цепях ü Не имеют шарнирного участка, его роль выполняет весь домен СН 2 ü Функции: - защита против вирусов, бактерий, гельминтов - цитофильны по отношению к базофилам и ТК; Fc-фрагменты Ig. E связываются с Fc- рецептором ТК и базофилов, при вторичных попаданиях АГ закрепляются на поверхности этих клеток, вызывают их дегрануляцию и выброс медиаторов воспаления; т. о. Ig. E м. б. причиной развития нежелательного для человека ИО на некоторые АГ – одной из форм ГНТ
Ig. E – мономеры: ε 2κ 2 или ε 2λ 2 ü Мм. 185 КД ü Углеводов – 12 % ü Наименьшее количество АТ сыворотки крови: 0, 003% (0, 014 -0, 45 г/л) ü Период полураспада – 2, 5 дня (фиксированный в тканях – 28 дней) ü 2 активных центра, 4 С-домена в H-цепях ü Не имеют шарнирного участка, его роль выполняет весь домен СН 2 ü Функции: - защита против вирусов, бактерий, гельминтов - цитофильны по отношению к базофилам и ТК; Fc-фрагменты Ig. E связываются с Fc- рецептором ТК и базофилов, при вторичных попаданиях АГ закрепляются на поверхности этих клеток, вызывают их дегрануляцию и выброс медиаторов воспаления; т. о. Ig. E м. б. причиной развития нежелательного для человека ИО на некоторые АГ – одной из форм ГНТ
 Ig. D – мономеры: δ 2κ 2 или δ 2λ 2 ü Мм. 185 КД ü Углеводов – 13 % ü Их продуцируется в организме 1 %, на поверхности В-л играют роль ВКР рецептора В-л ü В сыворотку попадают вследствие разрушения В-л, в сыворотке крови присутствуют в следовых количествах: 0, 2% АТ сыворотки крови (0 -0, 4 г/л) ü Период полураспада – 2, 5 -2, 8 дня: высоко чувствительны к протеазам сыворотки крови, быстро катаболизируются ü 2 активных центра Якорный участок
Ig. D – мономеры: δ 2κ 2 или δ 2λ 2 ü Мм. 185 КД ü Углеводов – 13 % ü Их продуцируется в организме 1 %, на поверхности В-л играют роль ВКР рецептора В-л ü В сыворотку попадают вследствие разрушения В-л, в сыворотке крови присутствуют в следовых количествах: 0, 2% АТ сыворотки крови (0 -0, 4 г/л) ü Период полураспада – 2, 5 -2, 8 дня: высоко чувствительны к протеазам сыворотки крови, быстро катаболизируются ü 2 активных центра Якорный участок
 Генетическое разнообразие АТ Популяция В-л представлена множеством клонов, каждый клон синтезирует АТ определенной специфичности разнообразие АТ , которое обусловлено: ü большим количеством генов, кодирующих цепи Ig ü случайным выбором одного из генов каждой группы ü реаранжировкой (перестройкой) генов Ig ü генетическими D-J и V-D-J рекомбинациями ü ошибками рекомбинации ü мутациями в ходе ИО и в процессе пролиферации клеток (протекают с высокой частотой, индивидуальны) ü различными комбинациями Н- и L-цепей
Генетическое разнообразие АТ Популяция В-л представлена множеством клонов, каждый клон синтезирует АТ определенной специфичности разнообразие АТ , которое обусловлено: ü большим количеством генов, кодирующих цепи Ig ü случайным выбором одного из генов каждой группы ü реаранжировкой (перестройкой) генов Ig ü генетическими D-J и V-D-J рекомбинациями ü ошибками рекомбинации ü мутациями в ходе ИО и в процессе пролиферации клеток (протекают с высокой частотой, индивидуальны) ü различными комбинациями Н- и L-цепей
 Гены Ig ü Имеют фрагментарную организацию, их сегменты находятся на расстоянии друг от друга ü Любые клетки содержат весь набор генов, но только у В-л эти гены реально работают ü L- и H-цепи кодируются разными генами и разным их количеством ü Гены расположены в разных хромосомах, V и С домены кодируются отдельно ü При дифференцировке В-л происходит реаранжировка (перестройка) генов – их перенос и объединение
Гены Ig ü Имеют фрагментарную организацию, их сегменты находятся на расстоянии друг от друга ü Любые клетки содержат весь набор генов, но только у В-л эти гены реально работают ü L- и H-цепи кодируются разными генами и разным их количеством ü Гены расположены в разных хромосомах, V и С домены кодируются отдельно ü При дифференцировке В-л происходит реаранжировка (перестройка) генов – их перенос и объединение
 L-цепи кодируются 3 группами генов: V, J, C Гены κ-цепи - во 2 -й хромосоме: – 250 V-генов – 5 J-генов (joining – соединение) – 1 С-ген Число возможных вариантов κ-цепи: 250 х5 х1 = 1225 Гены λ -цепи – в 22 -й хромосоме: – 100 V-генов – 6 J-генов – 1 С-ген Число возможных вариантов λ-цепи: 100 х6 х1 = 600
L-цепи кодируются 3 группами генов: V, J, C Гены κ-цепи - во 2 -й хромосоме: – 250 V-генов – 5 J-генов (joining – соединение) – 1 С-ген Число возможных вариантов κ-цепи: 250 х5 х1 = 1225 Гены λ -цепи – в 22 -й хромосоме: – 100 V-генов – 6 J-генов – 1 С-ген Число возможных вариантов λ-цепи: 100 х6 х1 = 600
 Н-цепи кодируются 4 группами генов V, D, J, C 14 хромосомы: üОтличия от кластеров генов для L-цепей заключаются: - в наличии дополнительных D-генов - большей протяжённости участков, соответствующих С-генам ü V-домены кодируются 3 группами генов (V, D, J): – 200 V-генов, – 50 D-генов (от англ. diversity –различность) – 5 J-генов ü С-домены кодируются группой генов С: – 5 С-генов (по типу Н-цепей) Число возможных вариантов Н-цепей: 200 х50 х5 х5=250000
Н-цепи кодируются 4 группами генов V, D, J, C 14 хромосомы: üОтличия от кластеров генов для L-цепей заключаются: - в наличии дополнительных D-генов - большей протяжённости участков, соответствующих С-генам ü V-домены кодируются 3 группами генов (V, D, J): – 200 V-генов, – 50 D-генов (от англ. diversity –различность) – 5 J-генов ü С-домены кодируются группой генов С: – 5 С-генов (по типу Н-цепей) Число возможных вариантов Н-цепей: 200 х50 х5 х5=250000

