Immunitet-_Noyabrsk.ppt
- Количество слайдов: 106
 Иммунитет. Факторы и механизмы иммунной защиты. Кафедра КЛД Тюм. ГМА Д. м. н. Ананьева О. В.
Иммунитет. Факторы и механизмы иммунной защиты. Кафедра КЛД Тюм. ГМА Д. м. н. Ананьева О. В.
 Иммунитет (лат. immunitas – освобождение, избавление от чего-либо) – это функция иммунной системы, направленная на сохранение генетического или антигенного гомеостаза организма и которая осуществляется лимфоцитами.
Иммунитет (лат. immunitas – освобождение, избавление от чего-либо) – это функция иммунной системы, направленная на сохранение генетического или антигенного гомеостаза организма и которая осуществляется лимфоцитами.

 Классификация В зависимости от происхождения механизмов, формирующих невосприимчивость организма к патогенным агентам: ¢ Наследственный иммунитет (син. врожденный, видовой, естественный, конституцианальный) присущ тому или иному виду животных или человеку и передается из поколения в поколение по наследству. Приобретенный (адаптивный) иммунитет может развиться в результате перенесенной инфекции или иммунизации. Он также строго специфичен, но по наследству не передается.
Классификация В зависимости от происхождения механизмов, формирующих невосприимчивость организма к патогенным агентам: ¢ Наследственный иммунитет (син. врожденный, видовой, естественный, конституцианальный) присущ тому или иному виду животных или человеку и передается из поколения в поколение по наследству. Приобретенный (адаптивный) иммунитет может развиться в результате перенесенной инфекции или иммунизации. Он также строго специфичен, но по наследству не передается.
 Активно приобретенный иммунитет возникает в результате перенесенной инфекции или после вакцинации живыми или убитыми вакцинами – искусственно приобретенный. Активно приобретенный иммунитет может держаться годами (грипп – 1 -2 года), десятилетиями (сибирская язва, риккетсиозы) или пожизненно (полиомиелит, корь, коклюш).
Активно приобретенный иммунитет возникает в результате перенесенной инфекции или после вакцинации живыми или убитыми вакцинами – искусственно приобретенный. Активно приобретенный иммунитет может держаться годами (грипп – 1 -2 года), десятилетиями (сибирская язва, риккетсиозы) или пожизненно (полиомиелит, корь, коклюш).
 Пассивно приобретенный иммунитет возникает у плода вследствии того, что он получает антитела от матери через плаценту, он создается также путем введения в организм иммуноглобулинов, полученных от активно иммунизированных людей и животных.
Пассивно приобретенный иммунитет возникает у плода вследствии того, что он получает антитела от матери через плаценту, он создается также путем введения в организм иммуноглобулинов, полученных от активно иммунизированных людей и животных.
 Приобретенный (адаптивный) иммунитет В зависимости от исхода инфекционного процесса: ¢ Стерильный иммунитет сопровождается полным освобождением от инфекционного агента. ¢ Нестерильный или инфекционный иммунитет обусловлен наличием инфекционного агента в организме и продолжается до тех пор, пока микробы остаются в организме (например, иммунитет при туберкулезе).
Приобретенный (адаптивный) иммунитет В зависимости от исхода инфекционного процесса: ¢ Стерильный иммунитет сопровождается полным освобождением от инфекционного агента. ¢ Нестерильный или инфекционный иммунитет обусловлен наличием инфекционного агента в организме и продолжается до тех пор, пока микробы остаются в организме (например, иммунитет при туберкулезе).
 По направленности: ¢ ¢ ¢ Противоопухолевый Трансплантационный Аутоиммунный Антимикробный Противовирусный Противогрибковый
По направленности: ¢ ¢ ¢ Противоопухолевый Трансплантационный Аутоиммунный Антимикробный Противовирусный Противогрибковый
 На основании того, что иммунная система обеспечивает развитие двух принципиально различных по механизму форм реакций, выделяют гуморальный (обусловлен антителами) и клеточный иммунитет (обусловлен CD 4+ и CD 8+ Tлимфоцитами), между которыми существует тесная взаимосвязь.
На основании того, что иммунная система обеспечивает развитие двух принципиально различных по механизму форм реакций, выделяют гуморальный (обусловлен антителами) и клеточный иммунитет (обусловлен CD 4+ и CD 8+ Tлимфоцитами), между которыми существует тесная взаимосвязь.
 Факторы естественной резистентности
Факторы естественной резистентности
 Естественная резистентность ¢ – совокупность генетически детерминированных неспецифичеких защитных механизмов, обусловливающих невосприимчивость к инфекциям. Это комплекс тканевых, клеточных и гуморальных факторов защиты организма от возбудителей инфекций, действия которых не характеризуется антигенной специфичностью.
Естественная резистентность ¢ – совокупность генетически детерминированных неспецифичеких защитных механизмов, обусловливающих невосприимчивость к инфекциям. Это комплекс тканевых, клеточных и гуморальных факторов защиты организма от возбудителей инфекций, действия которых не характеризуется антигенной специфичностью.
 Механизмы естественной резистентности и приобретенного иммунитета тесно переплетаются: их взаимодействие осуществляется на всех этапах проникновения, существования в организме и элиминации «чужого» .
Механизмы естественной резистентности и приобретенного иммунитета тесно переплетаются: их взаимодействие осуществляется на всех этапах проникновения, существования в организме и элиминации «чужого» .
 Факторы естественной резистентности: Естественные барьеры: кожа, слизистые - поверхности, которые первыми вступают в контакт с возбудителями инфекций. Клеточные факторы: ¢ Система фагоцитов, включающая нейтрофилы и макрофаги. ¢ Система естественных киллеров. Гуморальные факторы: ¢ Система комплемента. ¢ Цитокины. ¢ Бактерицидные гуморальные факторы. ¢
Факторы естественной резистентности: Естественные барьеры: кожа, слизистые - поверхности, которые первыми вступают в контакт с возбудителями инфекций. Клеточные факторы: ¢ Система фагоцитов, включающая нейтрофилы и макрофаги. ¢ Система естественных киллеров. Гуморальные факторы: ¢ Система комплемента. ¢ Цитокины. ¢ Бактерицидные гуморальные факторы. ¢
 Система фагоцитов ¢ микрофаги - полиморфноядерные нейтрофилы - короткоживущие, эффекторные клетки ¢ макрофаги – клетки, образующиеся из моноцитов, мигрирующие во все ткани организма. Существуют там в виде зрелых тканевых макрофагов (клетки Лангерганса кожи, Купферовы клетки печени, альвеолярные макрофаги легких, клетки микроглии нервной ткани, остеокласты, гистиоциты соединительной ткани, мезенгиальные макрофаги почек, синовиальные А-клетки ) и образуют систему мононуклеарных фагоцитов.
Система фагоцитов ¢ микрофаги - полиморфноядерные нейтрофилы - короткоживущие, эффекторные клетки ¢ макрофаги – клетки, образующиеся из моноцитов, мигрирующие во все ткани организма. Существуют там в виде зрелых тканевых макрофагов (клетки Лангерганса кожи, Купферовы клетки печени, альвеолярные макрофаги легких, клетки микроглии нервной ткани, остеокласты, гистиоциты соединительной ткани, мезенгиальные макрофаги почек, синовиальные А-клетки ) и образуют систему мононуклеарных фагоцитов.
 Функция фагоцитов - фагоцитоз ¢ Явление фагоцитоза было открыто И. И. Мечниковым еще в 1882 году. ¢В настоящее время это один из наиболее изученных процессов, обеспечивающих неспецифическую защиту организма
Функция фагоцитов - фагоцитоз ¢ Явление фагоцитоза было открыто И. И. Мечниковым еще в 1882 году. ¢В настоящее время это один из наиболее изученных процессов, обеспечивающих неспецифическую защиту организма
 Этапы фагоцитоза Активация фагоцита ¢ Хемотаксис – направленное движение фагоцита к месту проникновения патогена ¢ Адгезия - прикрепление к объекту фагоцитоза ¢ Поглощение объекта – образование фагосомы и фаголизосомы ¢ Киллинг (внутриклеточное уничтожение) и переваривание, процессинг (переработка) объекта фагоцитоза для представления его иммунокомпетентным клеткам ¢
Этапы фагоцитоза Активация фагоцита ¢ Хемотаксис – направленное движение фагоцита к месту проникновения патогена ¢ Адгезия - прикрепление к объекту фагоцитоза ¢ Поглощение объекта – образование фагосомы и фаголизосомы ¢ Киллинг (внутриклеточное уничтожение) и переваривание, процессинг (переработка) объекта фагоцитоза для представления его иммунокомпетентным клеткам ¢
 Опсонины ( от лат. opsonin ¢ -усиливющий) – белки, обволакивающие микробы, корпускулярные антигены и усиливающие их фагоцитоз. Роль опсонинов выполняют Ig. G 1, Ig. G 3, частично Ig. A, белки острой фазы, фибронектин, ЛПСсвязывающий белок, компоненты комплемента (С 3 b, С 4 b), сурфактантные протеины легких и т. д.
Опсонины ( от лат. opsonin ¢ -усиливющий) – белки, обволакивающие микробы, корпускулярные антигены и усиливающие их фагоцитоз. Роль опсонинов выполняют Ig. G 1, Ig. G 3, частично Ig. A, белки острой фазы, фибронектин, ЛПСсвязывающий белок, компоненты комплемента (С 3 b, С 4 b), сурфактантные протеины легких и т. д.

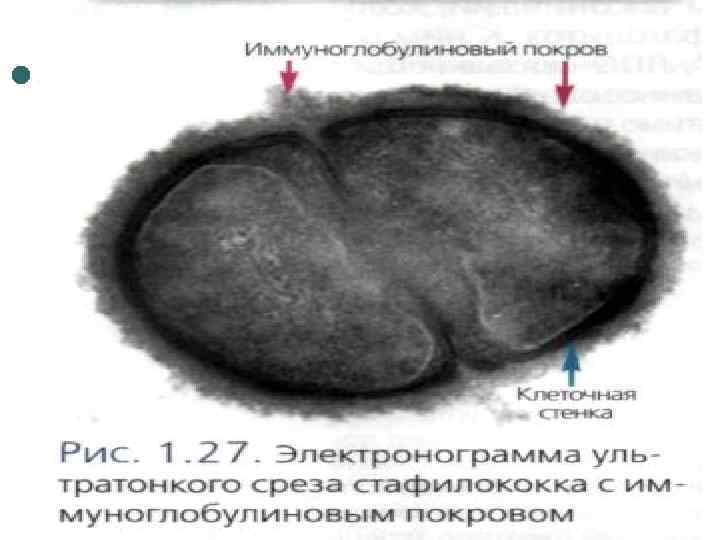
 Уничтожение патогенов происходит с помощью: ¢ закисления среды в фаголизосоме (p. H 3, 5 -4, 0); ¢ активных форм кислорода (супероксидный анион-радикал, синглетный кислород, перекись водорода, гидроксильный радикал, гипохлорит); ¢ окиси азота; ¢ литических ферментов (лизоцим, кислые гидролазы); ¢ антимикробных пептидов (дефенсины и катионные белки).
Уничтожение патогенов происходит с помощью: ¢ закисления среды в фаголизосоме (p. H 3, 5 -4, 0); ¢ активных форм кислорода (супероксидный анион-радикал, синглетный кислород, перекись водорода, гидроксильный радикал, гипохлорит); ¢ окиси азота; ¢ литических ферментов (лизоцим, кислые гидролазы); ¢ антимикробных пептидов (дефенсины и катионные белки).
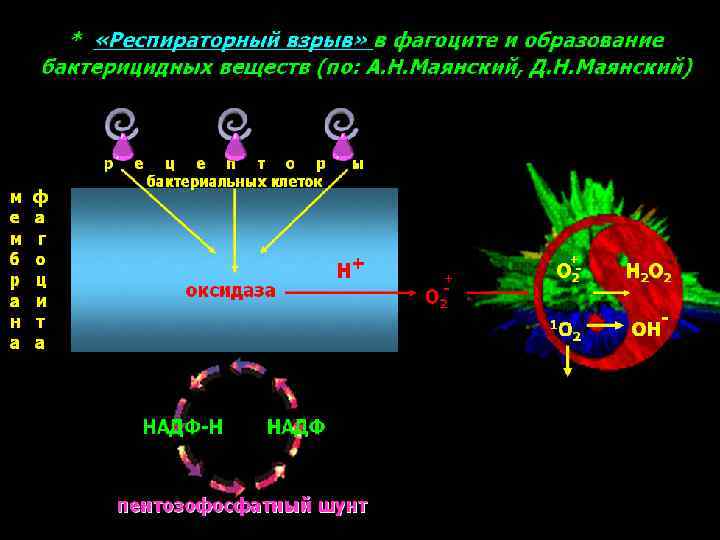
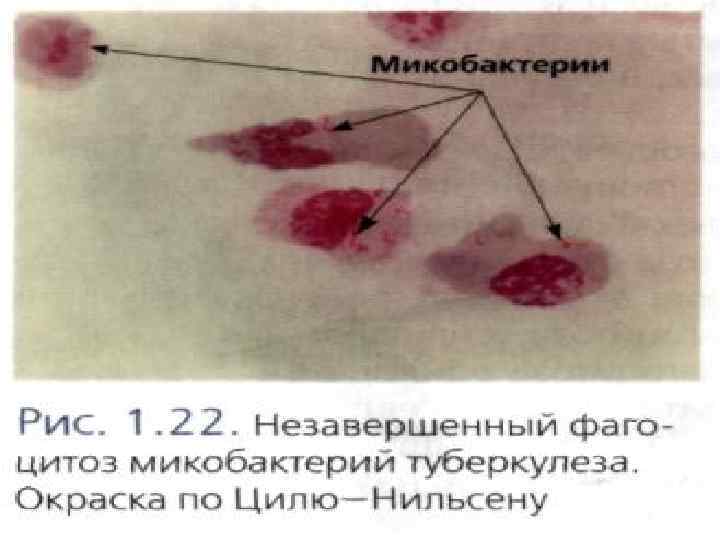
 Фагоцитоз может быть завершенным, в результате разрушения захваченного микроба, и незавершенным, при котором микробы не погибают, сохраняя способность к размножению.
Фагоцитоз может быть завершенным, в результате разрушения захваченного микроба, и незавершенным, при котором микробы не погибают, сохраняя способность к размножению.
 Выживанию микробов способствуют следующие механизмы: подавление слияния лизосом с фагосомой, содержащей микробы (при туберкулезе, лейшманиозе и токсоплазмозе); ¢ устойчивость к лизосомальным ферментам (гонококки); ¢ выход микробов из фагосом и персистенция их в цитоплазме клеток (листерии, риккетсии). ¢
Выживанию микробов способствуют следующие механизмы: подавление слияния лизосом с фагосомой, содержащей микробы (при туберкулезе, лейшманиозе и токсоплазмозе); ¢ устойчивость к лизосомальным ферментам (гонококки); ¢ выход микробов из фагосом и персистенция их в цитоплазме клеток (листерии, риккетсии). ¢
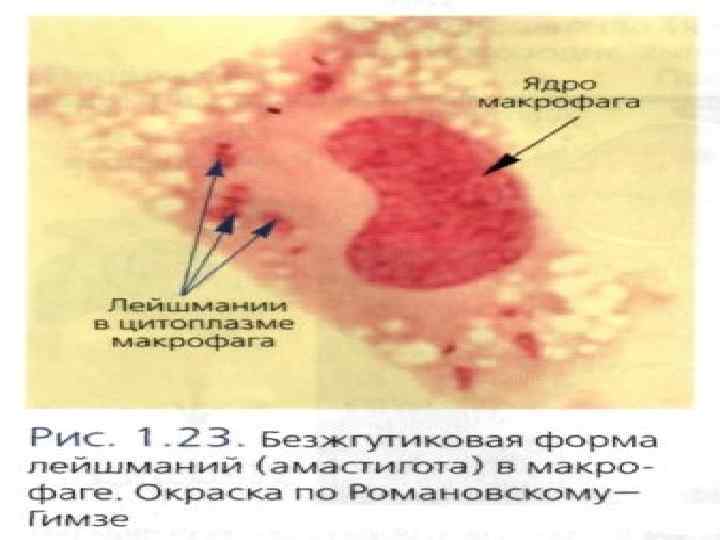
 Центральная роль в иммунитете принадлежит макрофагу Основные функции макрофага: ¢ фагоцитоз, ¢ презентация антигена Т- лимфоцитам, ¢ секреция цитокинов, ¢ повреждение клеток- мишеней (спонтанная и антителозависимая цитотоксичность, иммунный фагоцитоз)
Центральная роль в иммунитете принадлежит макрофагу Основные функции макрофага: ¢ фагоцитоз, ¢ презентация антигена Т- лимфоцитам, ¢ секреция цитокинов, ¢ повреждение клеток- мишеней (спонтанная и антителозависимая цитотоксичность, иммунный фагоцитоз)
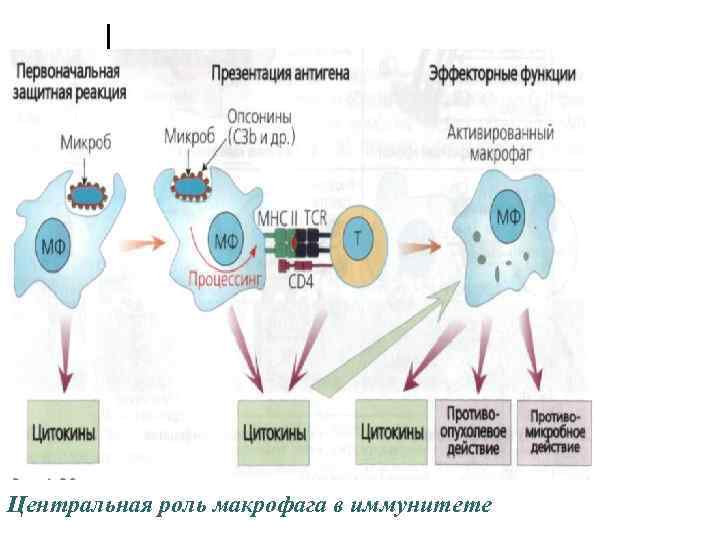 Центральная роль макрофага в иммунитете
Центральная роль макрофага в иммунитете
 Естественные киллеры (NKклетки, от англ. Natural killers или естественные киллеры). Это лимфоциты, лишенные антигенраспознающих рецепторов, в кооперации с цитокинами проявляют неспецифическую цитотоксичность против инфицированных вирусом клеток, стареющих и опухолевых клеток, а также против тканей трансплантата. Они участвуют в противовирусном, противопаразитарном, противоопухолевом и трансплантационном иммунитете, осуществляя контроль экспрессии молекул МНС I класса.
Естественные киллеры (NKклетки, от англ. Natural killers или естественные киллеры). Это лимфоциты, лишенные антигенраспознающих рецепторов, в кооперации с цитокинами проявляют неспецифическую цитотоксичность против инфицированных вирусом клеток, стареющих и опухолевых клеток, а также против тканей трансплантата. Они участвуют в противовирусном, противопаразитарном, противоопухолевом и трансплантационном иммунитете, осуществляя контроль экспрессии молекул МНС I класса.
 Доля их в крови составляет около 10 -19% от общего числа лимфоцитов, находятся преимущественно в печени и селезенке. Морфологически они идентифицируются как большие гранулярные лимфоциты. Типичными маркерами NK-клетки являются молекула адгезии CD 56 и рецептор для Fс-фагмента Ig. G- СD 16.
Доля их в крови составляет около 10 -19% от общего числа лимфоцитов, находятся преимущественно в печени и селезенке. Морфологически они идентифицируются как большие гранулярные лимфоциты. Типичными маркерами NK-клетки являются молекула адгезии CD 56 и рецептор для Fс-фагмента Ig. G- СD 16.
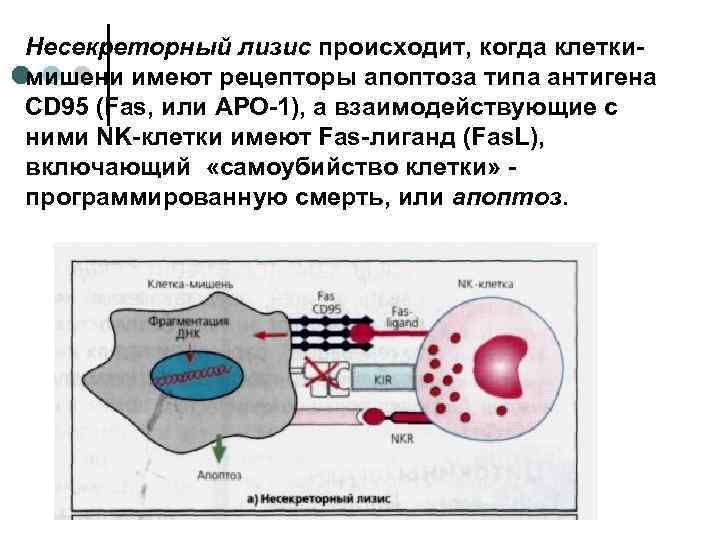 Несекреторный лизис происходит, когда клеткимишени имеют рецепторы апоптоза типа антигена СD 95 (Fas, или АPO-1), а взаимодействующие с ними NK-клетки имеют Fas-лиганд (Fas. L), включающий «самоубийство клетки» программированную смерть, или апоптоз.
Несекреторный лизис происходит, когда клеткимишени имеют рецепторы апоптоза типа антигена СD 95 (Fas, или АPO-1), а взаимодействующие с ними NK-клетки имеют Fas-лиганд (Fas. L), включающий «самоубийство клетки» программированную смерть, или апоптоз.
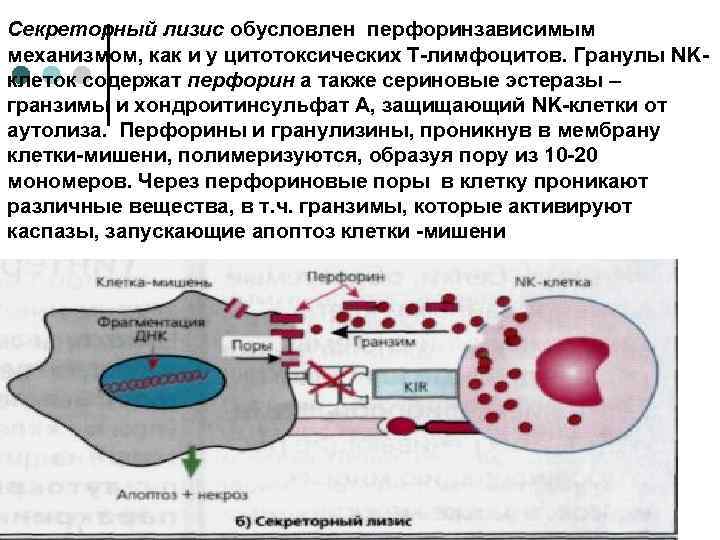 Секреторный лизис обусловлен перфоринзависимым механизмом, как и у цитотоксических Т-лимфоцитов. Гранулы ΝΚклеток содержат перфорин а также сериновые эстеразы – гранзимы и хондроитинсульфат А, защищающий NK-клетки от аутолиза. Перфорины и гранулизины, проникнув в мембрану клетки-мишени, полимеризуются, образуя пору из 10 -20 мономеров. Через перфориновые поры в клетку проникают различные вещества, в т. ч. гранзимы, которые активируют каспазы, запускающие апоптоз клетки -мишени
Секреторный лизис обусловлен перфоринзависимым механизмом, как и у цитотоксических Т-лимфоцитов. Гранулы ΝΚклеток содержат перфорин а также сериновые эстеразы – гранзимы и хондроитинсульфат А, защищающий NK-клетки от аутолиза. Перфорины и гранулизины, проникнув в мембрану клетки-мишени, полимеризуются, образуя пору из 10 -20 мономеров. Через перфориновые поры в клетку проникают различные вещества, в т. ч. гранзимы, которые активируют каспазы, запускающие апоптоз клетки -мишени
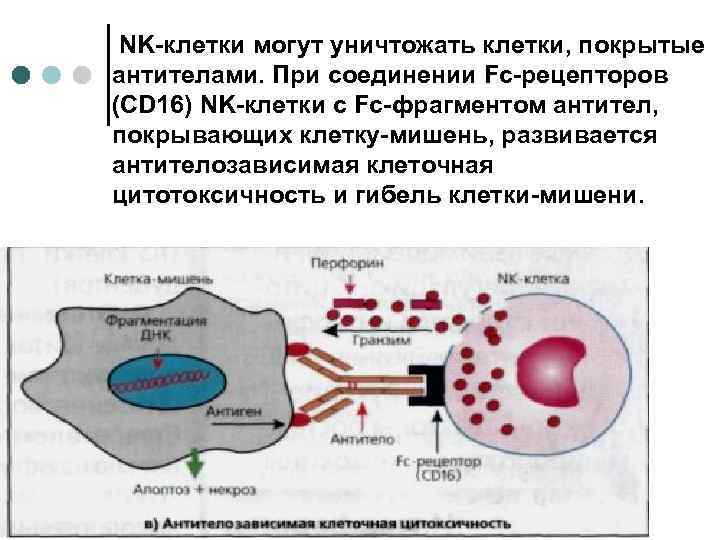 ΝΚ-клетки могут уничтожать клетки, покрытые антителами. При соединении Fс-рецепторов (СD 16) NK-клетки с Fс-фрагментом антител, покрывающих клетку-мишень, развивается антителозависимая клеточная цитотоксичность и гибель клетки-мишени.
ΝΚ-клетки могут уничтожать клетки, покрытые антителами. При соединении Fс-рецепторов (СD 16) NK-клетки с Fс-фрагментом антител, покрывающих клетку-мишень, развивается антителозависимая клеточная цитотоксичность и гибель клетки-мишени.
 Система комплемента – это совокупность более 25 белков сыворотки крови, из которых 9 – комплементарные белки (компоненты С 1 -С 9), а остальные – факторы (В, D, P, H и др. ). Большинство из них являются высокоактивными протеазами, циркулируют в крови в неактивном состоянии. Активация системы (бактериями, иммунными комплексами и т. д. ) идет по типу ферментативно- каскадной реакции с образованием растворимых и нерастворимых фрагментов и комплексов с различной биологической функцией (активаторы, ингибиторы и медиаторы различных процессов). При активации происходит расщепление молекул компонентов на фрагменты а (меньший, как правило, активный) и b (больший)
Система комплемента – это совокупность более 25 белков сыворотки крови, из которых 9 – комплементарные белки (компоненты С 1 -С 9), а остальные – факторы (В, D, P, H и др. ). Большинство из них являются высокоактивными протеазами, циркулируют в крови в неактивном состоянии. Активация системы (бактериями, иммунными комплексами и т. д. ) идет по типу ферментативно- каскадной реакции с образованием растворимых и нерастворимых фрагментов и комплексов с различной биологической функцией (активаторы, ингибиторы и медиаторы различных процессов). При активации происходит расщепление молекул компонентов на фрагменты а (меньший, как правило, активный) и b (больший)
 Комплемент играет важную роль в защите от чужеродного: он разрушает бактериальные и инфицированные вирусами собственные клетки, участвует в регуляции воспалительных и иммунных реакций. Некоторые фрагменты компонентов комплемента, например C 3 b, являются опсонинами. Опсонизированные клетки быстрее фагоцитируются, поскольку фагоциты активно связываются с этими клетками через соответствующие рецепторы.
Комплемент играет важную роль в защите от чужеродного: он разрушает бактериальные и инфицированные вирусами собственные клетки, участвует в регуляции воспалительных и иммунных реакций. Некоторые фрагменты компонентов комплемента, например C 3 b, являются опсонинами. Опсонизированные клетки быстрее фагоцитируются, поскольку фагоциты активно связываются с этими клетками через соответствующие рецепторы.
 Центральное положение в системе комплемента занимает белок С 3. При отсутствии активаторов происходит его медленный распад на С 3 а + С 3 b. При появлении какого-либо активатора распад С 3 происходит значительно быстрее, благодаря запуску систем активации комплемента по альтернативному или классическому путям.
Центральное положение в системе комплемента занимает белок С 3. При отсутствии активаторов происходит его медленный распад на С 3 а + С 3 b. При появлении какого-либо активатора распад С 3 происходит значительно быстрее, благодаря запуску систем активации комплемента по альтернативному или классическому путям.
 Классический путь активации: процесс инициирует присоединение компонента C 1 к комплексу АГ–АТ. Альтернативный путь: сигналом к активации является прямая (без участия АТ) активация компонента С 3 липополисахаридами мембраны микроба.
Классический путь активации: процесс инициирует присоединение компонента C 1 к комплексу АГ–АТ. Альтернативный путь: сигналом к активации является прямая (без участия АТ) активация компонента С 3 липополисахаридами мембраны микроба.
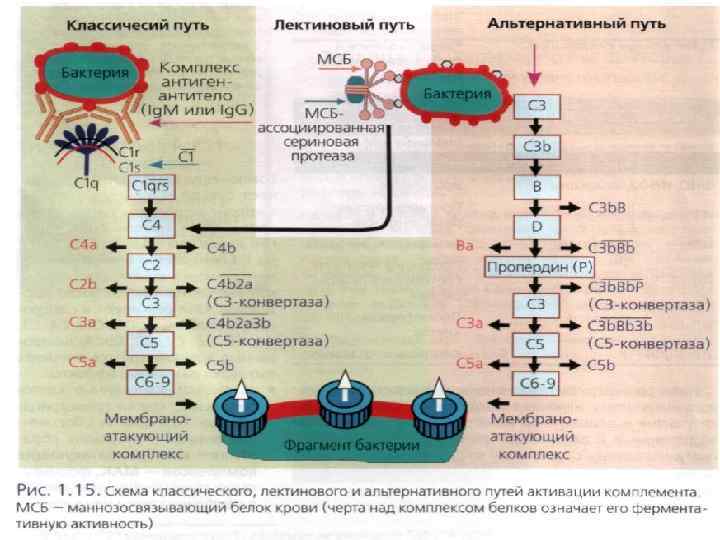
 Как классический, так и альтернативный путь в конечном итоге приводят к активации компонента C 5, а затем компонентов C 6, C 7, C 8 и C 9. Завершает процесс образование так называемого мембраноатакующего комплекса (С 5–С 9), связывание которого с мембраной клетки-мишени приводит к нарушению её целостности и в конечной итоге к гибели клетки (осмотический лизис).
Как классический, так и альтернативный путь в конечном итоге приводят к активации компонента C 5, а затем компонентов C 6, C 7, C 8 и C 9. Завершает процесс образование так называемого мембраноатакующего комплекса (С 5–С 9), связывание которого с мембраной клетки-мишени приводит к нарушению её целостности и в конечной итоге к гибели клетки (осмотический лизис).
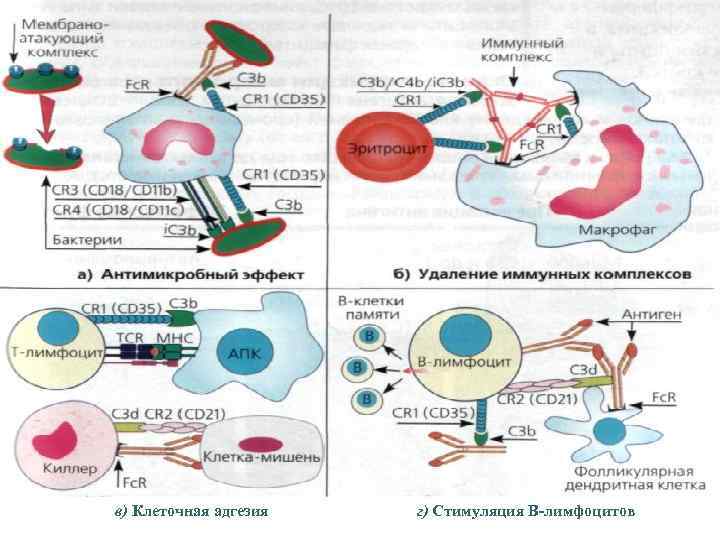 в) Клеточная адгезия г) Стимуляция В-лимфоцитов
в) Клеточная адгезия г) Стимуляция В-лимфоцитов
 Цитокины (от греч. cyto-клетка, kinos – движение) - - белки, образуемые активированными клетками иммунной системы, реже другими клетками (эпителием, фибробластами и др. ), обеспечивающие рост и пролиферацию многих клеток, а также межклеточные взаимодействия и иммунорегуляцию. К цитокинам относятся интерлейкины, интерфероны, ФНО, колониестимулирующие факторы, факторы роста, нейропоэтины, хемокины.
Цитокины (от греч. cyto-клетка, kinos – движение) - - белки, образуемые активированными клетками иммунной системы, реже другими клетками (эпителием, фибробластами и др. ), обеспечивающие рост и пролиферацию многих клеток, а также межклеточные взаимодействия и иммунорегуляцию. К цитокинам относятся интерлейкины, интерфероны, ФНО, колониестимулирующие факторы, факторы роста, нейропоэтины, хемокины.
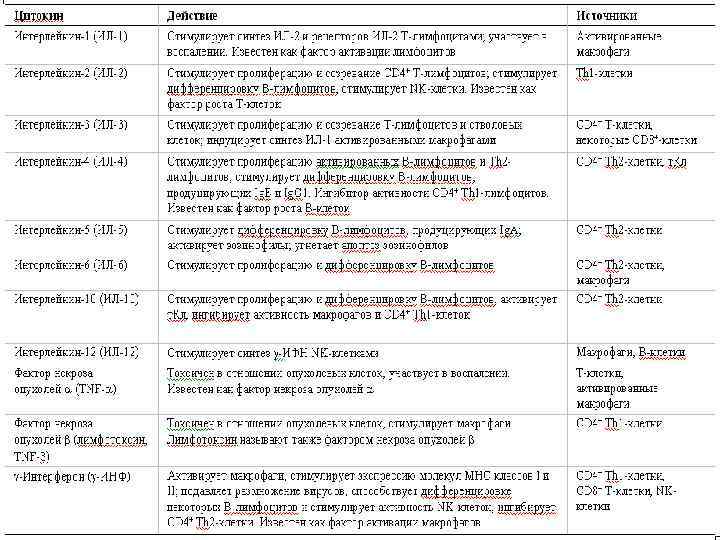
 Структура иммунной системы
Структура иммунной системы
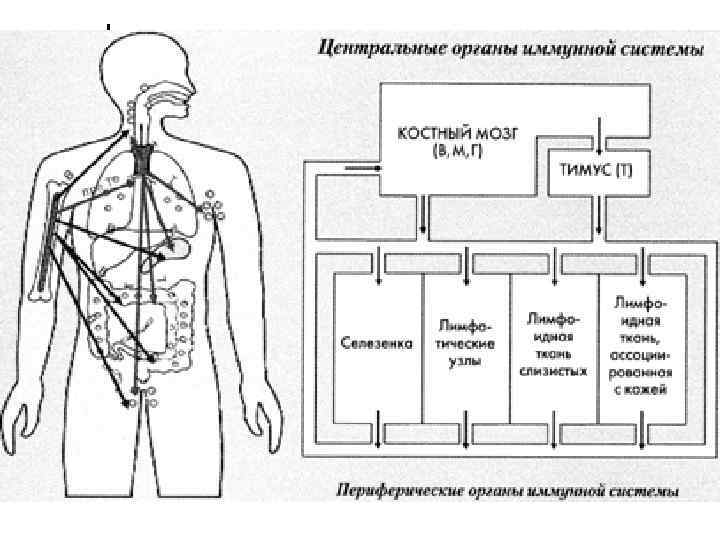
 Красный костный мозг. Его главная функция – продукция иммунокомпетентных клеток из полипотентной стволовой клетки. Лимфоидные клетки составляют примерно 6 -8% клеток костного мозга. В костном мозге могут протекать разнообразные иммунные реакции. Например, цитотоксические реакции (панмиелофтиз, агранулоцитоз) могут быть связаны с агрессией цитотоксических клеток против стволовых клеток, клеток-предшественников и более зрелых клеток.
Красный костный мозг. Его главная функция – продукция иммунокомпетентных клеток из полипотентной стволовой клетки. Лимфоидные клетки составляют примерно 6 -8% клеток костного мозга. В костном мозге могут протекать разнообразные иммунные реакции. Например, цитотоксические реакции (панмиелофтиз, агранулоцитоз) могут быть связаны с агрессией цитотоксических клеток против стволовых клеток, клеток-предшественников и более зрелых клеток.
 Вилочковая железа (тимус) Является местом созревания и дифференцировки Т-лимфоцитов (их общий маркер – CD 3+), затем заселяющих периферические органы иммунной системы. В ней происходит селекция Т-лимфоцитов, имеющих рецепторы к собственным тканям. Основная масса (95%) лимфоцитов в тимусе разрушается и только 5% поступает в кровь. Гибель клеток в тимусе усиливается при стрессе, гипертермии, длительном голодании и т. д. Чем более длительно функционирует тимус, тем дольше живет организм.
Вилочковая железа (тимус) Является местом созревания и дифференцировки Т-лимфоцитов (их общий маркер – CD 3+), затем заселяющих периферические органы иммунной системы. В ней происходит селекция Т-лимфоцитов, имеющих рецепторы к собственным тканям. Основная масса (95%) лимфоцитов в тимусе разрушается и только 5% поступает в кровь. Гибель клеток в тимусе усиливается при стрессе, гипертермии, длительном голодании и т. д. Чем более длительно функционирует тимус, тем дольше живет организм.
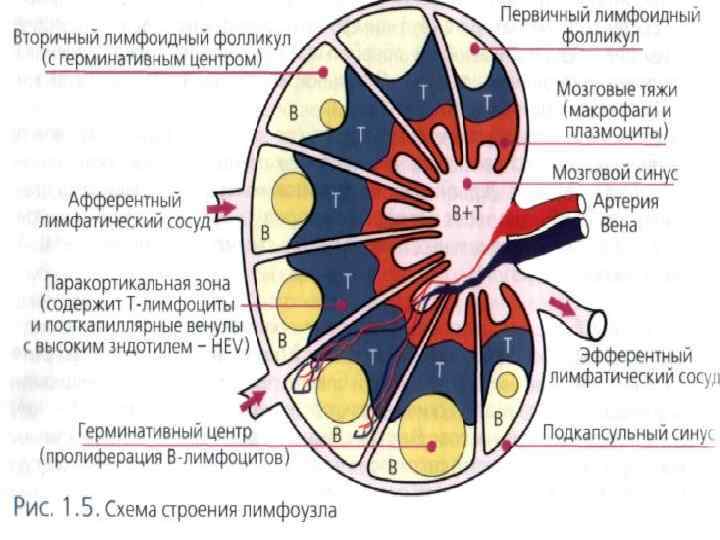
 Лимфатические узлы выполняют неспецифическую барьерную функцию – элиминацию микробов из лимфы, они являются местом развития клеточного и гуморального иммунного ответа. Строма лимфоузла образована рыхлой соединительной тканью, в его паренхиме различают корковое и мозговое вещество. Корковое вещество – В-зависимая зона – содержит лимфатические фолликулы, состоящие в основном из В-лимфоцитов. В паракортикальной – Т-зависимой – зоне расположены преимущественно Т-лимфоциты.
Лимфатические узлы выполняют неспецифическую барьерную функцию – элиминацию микробов из лимфы, они являются местом развития клеточного и гуморального иммунного ответа. Строма лимфоузла образована рыхлой соединительной тканью, в его паренхиме различают корковое и мозговое вещество. Корковое вещество – В-зависимая зона – содержит лимфатические фолликулы, состоящие в основном из В-лимфоцитов. В паракортикальной – Т-зависимой – зоне расположены преимущественно Т-лимфоциты.
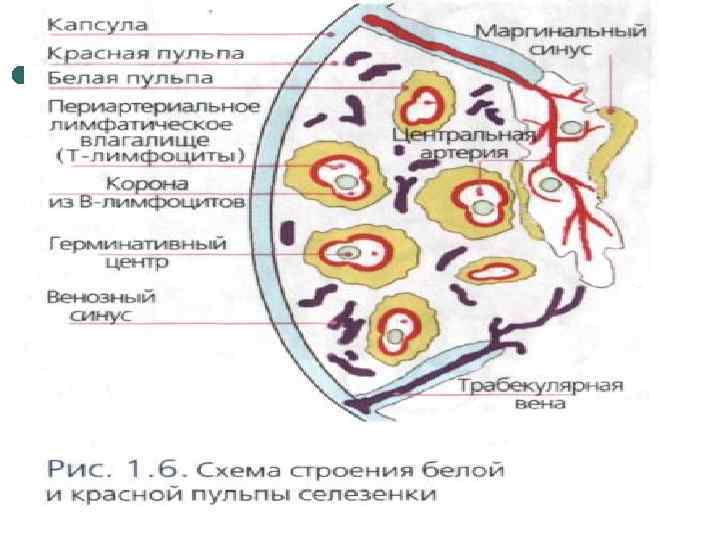
 Селезенка является фильтрующим органом для крови, в ней осуществляется детоксикация, удаление старых и поврежденных эритроцитов, тромбоцитов и других клеток, проводится дифференцировка лимфоцитов, образуется тафтсин (тетрапептид, который может повышать миграцию, фагоцитарную активность и продолжительность жизни макрофагов и нейтрофилов, увеличивает цитотоксическое действие Т-лимфоцитов, стимулирует синтез антител). Лимфоидная ткань селезенки представлена островками белой пульпы, которые подобно лимфоузлам имеют фолликулярное строение и разделены на В- и Т-зависимые зоны.
Селезенка является фильтрующим органом для крови, в ней осуществляется детоксикация, удаление старых и поврежденных эритроцитов, тромбоцитов и других клеток, проводится дифференцировка лимфоцитов, образуется тафтсин (тетрапептид, который может повышать миграцию, фагоцитарную активность и продолжительность жизни макрофагов и нейтрофилов, увеличивает цитотоксическое действие Т-лимфоцитов, стимулирует синтез антител). Лимфоидная ткань селезенки представлена островками белой пульпы, которые подобно лимфоузлам имеют фолликулярное строение и разделены на В- и Т-зависимые зоны.
 Лимфатические фолликулы ЖКТ и дыхательных путей – это миндалины, собственно лимфатичесие фолликулы и пейеровы бляшки. Они также разделены на В- и Т-зависимые зоны
Лимфатические фолликулы ЖКТ и дыхательных путей – это миндалины, собственно лимфатичесие фолликулы и пейеровы бляшки. Они также разделены на В- и Т-зависимые зоны
 Небные миндалины осуществляют защиту верхних дыхательных путей от инфекции. Тимус взаимосвязан с миндалинами. Тимэктомия ведет к гипертрофии миндалин, тонзилэктомия – к атрофии тимуса, а также к более частому поражению нижних дыхательных путей, к нарастанию аллергических заболеваний.
Небные миндалины осуществляют защиту верхних дыхательных путей от инфекции. Тимус взаимосвязан с миндалинами. Тимэктомия ведет к гипертрофии миндалин, тонзилэктомия – к атрофии тимуса, а также к более частому поражению нижних дыхательных путей, к нарастанию аллергических заболеваний.
 Пейеровы бляшки кишечника имеют огромное значение как в формировании иммунного ответа, так и в созревании Т- и В-лимфоцитов. Неадекватная антигенная стимуляция пейеровых бляшек кишечника может приводить к их атрофии, нарушению созревания Т-лимфоцитов и к аллергическим заболеваниям.
Пейеровы бляшки кишечника имеют огромное значение как в формировании иммунного ответа, так и в созревании Т- и В-лимфоцитов. Неадекватная антигенная стимуляция пейеровых бляшек кишечника может приводить к их атрофии, нарушению созревания Т-лимфоцитов и к аллергическим заболеваниям.
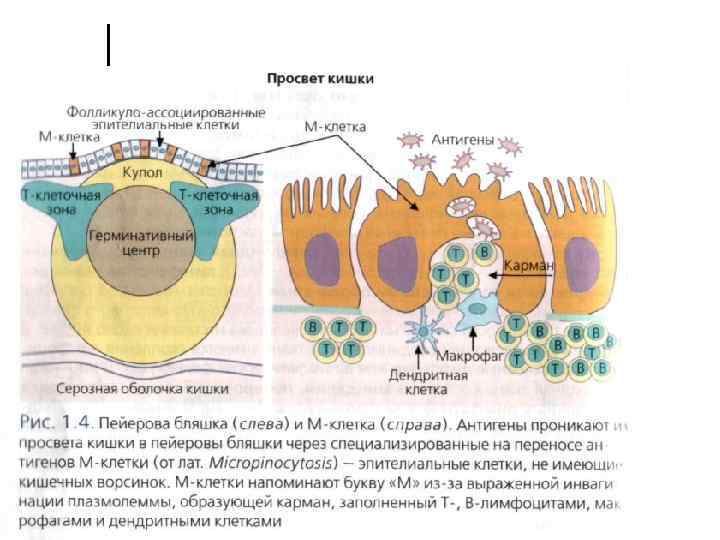
 Иммунокомпетентные клетки ¢ Т-лимфоциты (CD 3+)– наиболее многочисленная популяция иммунокомпетентных клеток (до 80% лимфоцитов), участвуют в реакциях клеточного иммунитета: аллергических реакциях замедленного типа, реакции отторжения трансплантата и других, обеспечивают противоопухолевый иммунитет.
Иммунокомпетентные клетки ¢ Т-лимфоциты (CD 3+)– наиболее многочисленная популяция иммунокомпетентных клеток (до 80% лимфоцитов), участвуют в реакциях клеточного иммунитета: аллергических реакциях замедленного типа, реакции отторжения трансплантата и других, обеспечивают противоопухолевый иммунитет.
 Иммунокомпетентные клетки 1. CD 3+CD 4+ - Т-хелперы – клетки, генетически запрограммированные «помогать» , т. е. индуцировать размножение и (или) дифференцировку клеток других типов. Их до 70%. Существует 2 вида Т-хелперов: ¢ Th 1, активирующие клеточный иммунитет, ¢ Th 2, активирующие гуморальный иммунитет. ¢
Иммунокомпетентные клетки 1. CD 3+CD 4+ - Т-хелперы – клетки, генетически запрограммированные «помогать» , т. е. индуцировать размножение и (или) дифференцировку клеток других типов. Их до 70%. Существует 2 вида Т-хелперов: ¢ Th 1, активирующие клеточный иммунитет, ¢ Th 2, активирующие гуморальный иммунитет. ¢
 Иммунокомпетентные клетки ¢ 2. CD 3+CD 8+ (20 -30%) – Тсупрессоры и цитотоксические Т-лимфоциты (эффекторные клетки, секретирующие цитотоксические лимфокины, клетки-убийцы).
Иммунокомпетентные клетки ¢ 2. CD 3+CD 8+ (20 -30%) – Тсупрессоры и цитотоксические Т-лимфоциты (эффекторные клетки, секретирующие цитотоксические лимфокины, клетки-убийцы).
 Иммунокомпетентные клетки В-лимфоциты (СD 19 или СD 20) отвечают за развитие гуморального иммунитета. ¢ Раннее, антигеннезависимое, созревание и дифференцировка Влимфоцитов происходит в костном мозге. ¢ В кровь, в циркуляцию, попадают зрелые, но «наивные, девственные» В-лимфоциты. ¢
Иммунокомпетентные клетки В-лимфоциты (СD 19 или СD 20) отвечают за развитие гуморального иммунитета. ¢ Раннее, антигеннезависимое, созревание и дифференцировка Влимфоцитов происходит в костном мозге. ¢ В кровь, в циркуляцию, попадают зрелые, но «наивные, девственные» В-лимфоциты. ¢
 Антигензависимая дифференцировка Влимфоцитов является вторым этапом их развития. Этот этап дифференцировки характерен только для тех клонов Влимфоцитов, которые имеют антигенраспознающие рецепторы, специфичные (комплементарные) для данного вида антигена, его детерминант, и осуществляется при участии макрофагов (АП-клетки) и Т-лимфоцитов. В-лимфоцит трансформируется в активно пролиферирующие бласты (реакция бластной трансформации – РБТЛ), на завершающем этапе превращаясь в зрелые плазматические клетки, синтезирующие молекулы антител.
Антигензависимая дифференцировка Влимфоцитов является вторым этапом их развития. Этот этап дифференцировки характерен только для тех клонов Влимфоцитов, которые имеют антигенраспознающие рецепторы, специфичные (комплементарные) для данного вида антигена, его детерминант, и осуществляется при участии макрофагов (АП-клетки) и Т-лимфоцитов. В-лимфоцит трансформируется в активно пролиферирующие бласты (реакция бластной трансформации – РБТЛ), на завершающем этапе превращаясь в зрелые плазматические клетки, синтезирующие молекулы антител.
 Плазматические клетки (СD 21 -22 , СD 25, СD 38) способны синтезировать и секретировать несколько тысяч иммуноглобулинов в секунду, продолжительность жизни этих клеток составляет в среднем 2 -3 дня (до 7 дней).
Плазматические клетки (СD 21 -22 , СD 25, СD 38) способны синтезировать и секретировать несколько тысяч иммуноглобулинов в секунду, продолжительность жизни этих клеток составляет в среднем 2 -3 дня (до 7 дней).
 После антигенной стимуляции часть клона активированных Влимфоцитов вновь превращается в малые лимфоциты. Это долгоживущие клетки. При повторной стимуляции антигеном они активируются гораздо легче, чем исходные В-клетки, и обеспечивают быстрый синтез большого количества антител. Из-за этого свойства их назвали В-клетками памяти (имеют на поверхности CD 27).
После антигенной стимуляции часть клона активированных Влимфоцитов вновь превращается в малые лимфоциты. Это долгоживущие клетки. При повторной стимуляции антигеном они активируются гораздо легче, чем исходные В-клетки, и обеспечивают быстрый синтез большого количества антител. Из-за этого свойства их назвали В-клетками памяти (имеют на поверхности CD 27).
 Иммуноглобулины. ¢ Антитела – это иммуноглобулины, представляющие собой молекулы белка, которые образуются при взаимодействии В-лимфоцитов с антигеном и специфически с ним реагируют. По своей природе иммуноглобулины – это белки гаммаглобулиновой фракции.
Иммуноглобулины. ¢ Антитела – это иммуноглобулины, представляющие собой молекулы белка, которые образуются при взаимодействии В-лимфоцитов с антигеном и специфически с ним реагируют. По своей природе иммуноглобулины – это белки гаммаглобулиновой фракции.
 Иммуноглобулины. ¢ Любая молекула иммуноглобулина (Ig) имеет Y-образную форму и состоит из 2 тяжелых (Н) и 2 легких (L) цепей, связанных между собой дисульфидными мостиками. Каждая молекула антитела имеет 2 одинаковых антигенсвязывающих фрагмента Fab (англ. fragment antigen binding) и один Fc-фрагмент (англ. fragment crystallizable), с помощью которого антитела комплементарно связываются с Fc-рецептором клеточной мембраны.
Иммуноглобулины. ¢ Любая молекула иммуноглобулина (Ig) имеет Y-образную форму и состоит из 2 тяжелых (Н) и 2 легких (L) цепей, связанных между собой дисульфидными мостиками. Каждая молекула антитела имеет 2 одинаковых антигенсвязывающих фрагмента Fab (англ. fragment antigen binding) и один Fc-фрагмент (англ. fragment crystallizable), с помощью которого антитела комплементарно связываются с Fc-рецептором клеточной мембраны.
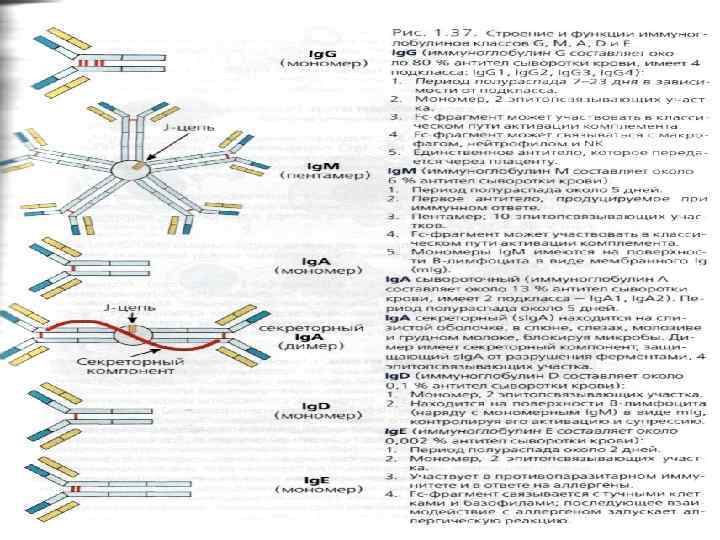
 Существует 5 классов иммуноглобулинов – Ig. A, Ig. G, Ig. M, Ig. D и Ig. E – соответственно 5 типам константных областей тяжелых цепей. Легкие цепи могут быть лишь двух типов – к (каппа) и л (ламбда). Каждая молекула иммуноглобулина состоит из тяжелых цепей одного типа, соединенных с легкими цепями также только одного типа. Иммуноглобулины одного класса могут содержать как к-, так и л-цепи.
Существует 5 классов иммуноглобулинов – Ig. A, Ig. G, Ig. M, Ig. D и Ig. E – соответственно 5 типам константных областей тяжелых цепей. Легкие цепи могут быть лишь двух типов – к (каппа) и л (ламбда). Каждая молекула иммуноглобулина состоит из тяжелых цепей одного типа, соединенных с легкими цепями также только одного типа. Иммуноглобулины одного класса могут содержать как к-, так и л-цепи.
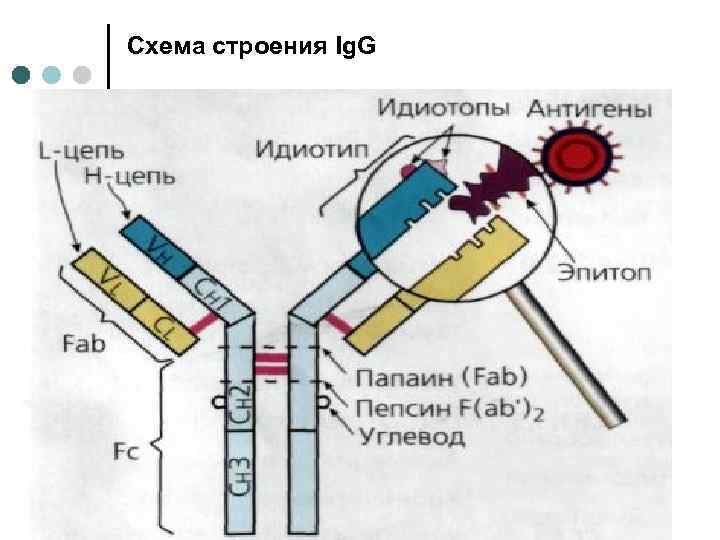 Схема строения Ig. G
Схема строения Ig. G
 Классы Ig разделяются на подклассы. Мономерные Ig, например Ig. G, состоит из одной молекулы, полимерные - Ig. M и Ig. A - из нескольких Так, пентамер Ig. M состоит из 10 м-цепей и 10 к- или л-цепей. Помимо легких и тяжелых цепей молекулы полимерных иммуноглобулинов включают J-цепь, а молекулы Ig. A - секреторный компонент.
Классы Ig разделяются на подклассы. Мономерные Ig, например Ig. G, состоит из одной молекулы, полимерные - Ig. M и Ig. A - из нескольких Так, пентамер Ig. M состоит из 10 м-цепей и 10 к- или л-цепей. Помимо легких и тяжелых цепей молекулы полимерных иммуноглобулинов включают J-цепь, а молекулы Ig. A - секреторный компонент.
 Биологические свойства антител: ¢ ¢ ¢ Специфичность – способность Ig реагировать только с определенным антигеном, что обусловлено наличием у них антидетерминант, контактирующих с соответствующими детерминантами антигена. Валентность – количество антидетерминант в молекуле антитела. Чаще всего они бивалентны. Аффинность, аффинитет – прочность соединения в реакции между детерминантами (эпитопом) антигена и антидетерминантами (паратопом) антитела. Авидность характеризует прочность связи антигена с антителом. Гетерогенность – неоднордность.
Биологические свойства антител: ¢ ¢ ¢ Специфичность – способность Ig реагировать только с определенным антигеном, что обусловлено наличием у них антидетерминант, контактирующих с соответствующими детерминантами антигена. Валентность – количество антидетерминант в молекуле антитела. Чаще всего они бивалентны. Аффинность, аффинитет – прочность соединения в реакции между детерминантами (эпитопом) антигена и антидетерминантами (паратопом) антитела. Авидность характеризует прочность связи антигена с антителом. Гетерогенность – неоднордность.
 Антигены иммунной системы – химические вещества, свободные или встроенные в мембрану клетки, способные индуцировать иммунный ответ. Мембранные антигены делятся на дифференцировочные (С D -антигены), антигены главного комплекса гистосовместимости (ГКГС или МНС – major histocompatibility complex), детерминантные.
Антигены иммунной системы – химические вещества, свободные или встроенные в мембрану клетки, способные индуцировать иммунный ответ. Мембранные антигены делятся на дифференцировочные (С D -антигены), антигены главного комплекса гистосовместимости (ГКГС или МНС – major histocompatibility complex), детерминантные.
 Главный комплекс гистосовместимости - это группа генов и кодируемых ими антигенов клеточной поверхности, которые играют важнейшую роль в распознавании чужеродного и развитии иммунного ответа. Главный комплекс гистосовместимости (МНС) человека получил название HLA (human leukocyte antigen). Антигены HLA подразделяются на антигены классов I и II.
Главный комплекс гистосовместимости - это группа генов и кодируемых ими антигенов клеточной поверхности, которые играют важнейшую роль в распознавании чужеродного и развитии иммунного ответа. Главный комплекс гистосовместимости (МНС) человека получил название HLA (human leukocyte antigen). Антигены HLA подразделяются на антигены классов I и II.
 Антигены HLA класса I необходимы для распознавания трансформированных клеток цитотоксическими Т-лимфоцитами. Функция антигенов HLA класса II обеспечение взаимодействия между Тлимфоцитами и макрофагами в процессе иммунного ответа. Т-хелперы распознают чужеродный антиген лишь после его переработки макрофагами, соединения с антигенами HLA класса II и появления этого комплекса на поверхности макрофага.
Антигены HLA класса I необходимы для распознавания трансформированных клеток цитотоксическими Т-лимфоцитами. Функция антигенов HLA класса II обеспечение взаимодействия между Тлимфоцитами и макрофагами в процессе иммунного ответа. Т-хелперы распознают чужеродный антиген лишь после его переработки макрофагами, соединения с антигенами HLA класса II и появления этого комплекса на поверхности макрофага.
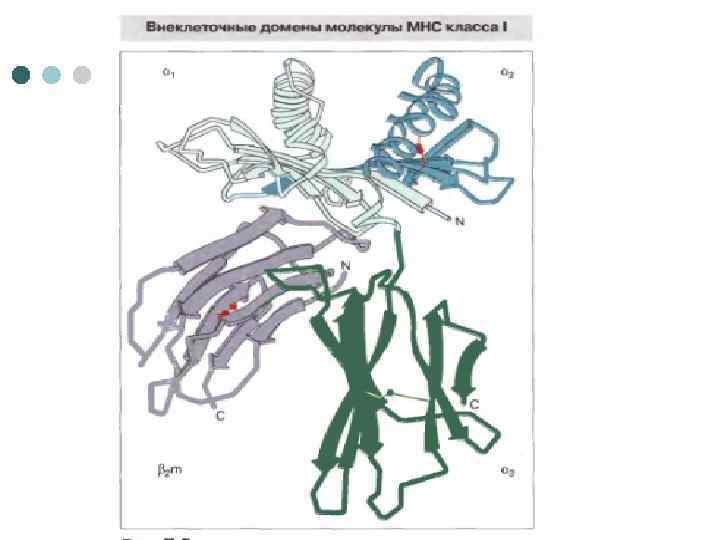
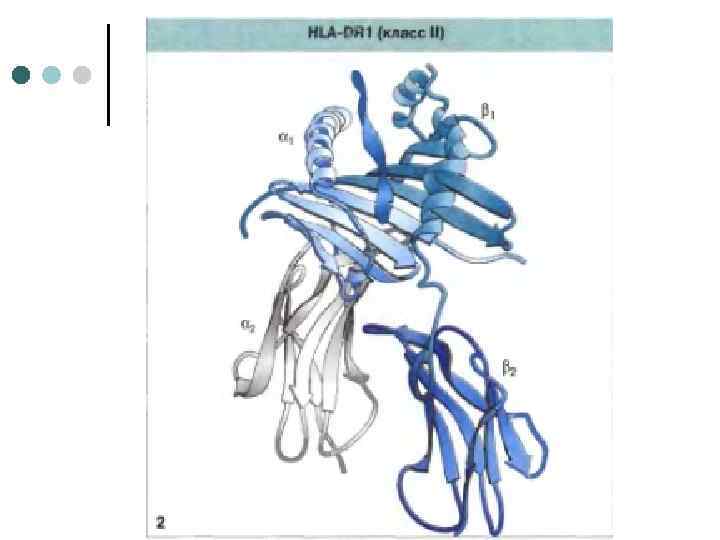
 Способность Т-лимфоцитов распознавать чужеродные антигены только в комплексе с антигенами HLA называют ограничением по HLA. Определение антигенов HLA классов I и II имеет большое значение в клинической иммунологии и используется, например, при подборе пар донор – реципиент перед трансплантацией органов.
Способность Т-лимфоцитов распознавать чужеродные антигены только в комплексе с антигенами HLA называют ограничением по HLA. Определение антигенов HLA классов I и II имеет большое значение в клинической иммунологии и используется, например, при подборе пар донор – реципиент перед трансплантацией органов.
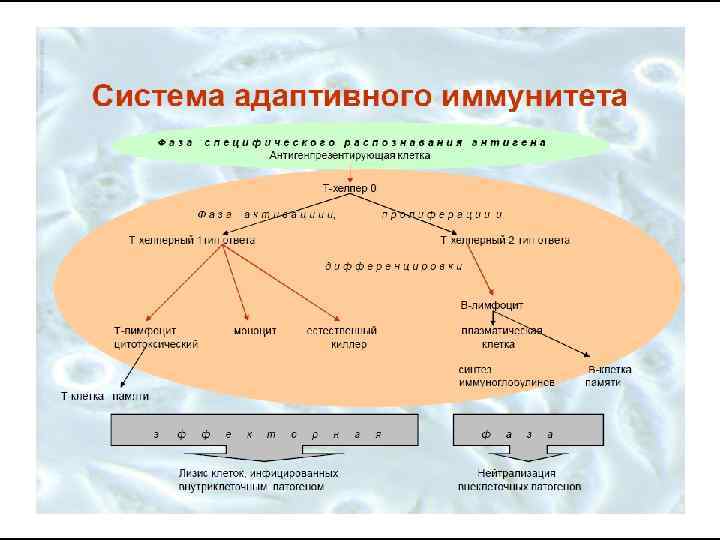
 Механизмы иммунитета Иммунный ответ происходит в результате взаимодействия дендритных клеток, макрофагов, цитокинов, Т- и В-лимфоцитов (клетки взаимодействуют при межклеточном контакте мембранами с помощью молекул межклеточной адгезии и с помощью цитокинов). Он включает 3 фазы: 1. распознавание антигена, ¢ 2. активация, пролиферация и дифференцировка клеток. ¢ 3. эффекторная фаза ¢
Механизмы иммунитета Иммунный ответ происходит в результате взаимодействия дендритных клеток, макрофагов, цитокинов, Т- и В-лимфоцитов (клетки взаимодействуют при межклеточном контакте мембранами с помощью молекул межклеточной адгезии и с помощью цитокинов). Он включает 3 фазы: 1. распознавание антигена, ¢ 2. активация, пролиферация и дифференцировка клеток. ¢ 3. эффекторная фаза ¢

 Гуморальный иммунный ответ (антителообразовние Основой гуморального (от лат. humor – жидкость) иммунного ответа является активация В- лимфоцитов и их дифференцировка в антителообразующие плазматические клетки – плазмоциты. ¢ В–лимфоцит играет роль антигенраспознающей, антигенпрезентирующей клетки и антиелообразующей клетки. ¢
Гуморальный иммунный ответ (антителообразовние Основой гуморального (от лат. humor – жидкость) иммунного ответа является активация В- лимфоцитов и их дифференцировка в антителообразующие плазматические клетки – плазмоциты. ¢ В–лимфоцит играет роль антигенраспознающей, антигенпрезентирующей клетки и антиелообразующей клетки. ¢
 Гуморальный иммунный ответ (антителообразовние ¢ Иммуноглобулиновый рецептор Влимфоцитов (ВСR) распознает антиген, и клетка поглощает его. После процессинга (расщепления поглощенного антигена до низкомолекулярных пептидов и встраивания их в HLA II класса) Влимфоциты представляют образовавшийся комплекс Тh 2 -хелперам, которые взаимодействуют с ним рецептором ТСR и корецептором СD 4. Происходит активация и пролиферация В-лимфоцитов. Размножаясь в геометрической прогрессии (7 -9 делений), В-клетка формирует клон плазматических клеток.
Гуморальный иммунный ответ (антителообразовние ¢ Иммуноглобулиновый рецептор Влимфоцитов (ВСR) распознает антиген, и клетка поглощает его. После процессинга (расщепления поглощенного антигена до низкомолекулярных пептидов и встраивания их в HLA II класса) Влимфоциты представляют образовавшийся комплекс Тh 2 -хелперам, которые взаимодействуют с ним рецептором ТСR и корецептором СD 4. Происходит активация и пролиферация В-лимфоцитов. Размножаясь в геометрической прогрессии (7 -9 делений), В-клетка формирует клон плазматических клеток.
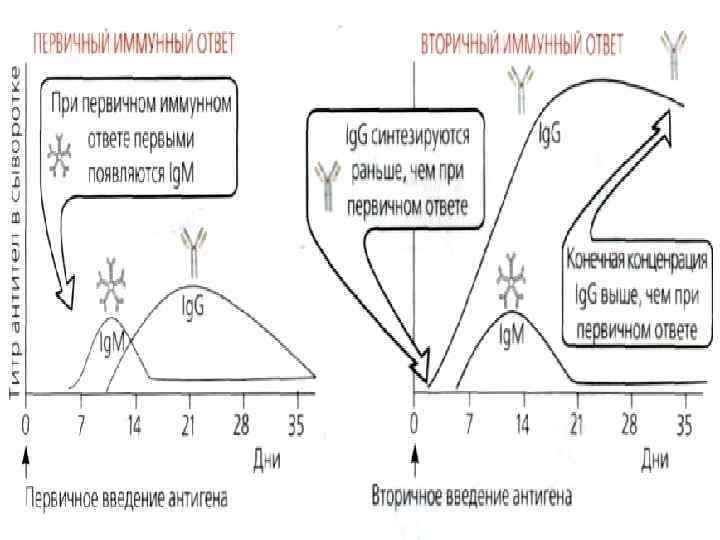
 Гуморальный иммунный ответ (антителообразовние Начинается активный синтез иммуноглобулинов. Плазматические клетки в основном все уходят в к. м. , и там продуцируют до 30 000 молекул Ig в мин. ¢ Первые АТ появляются в крови на 5 -е сутки (от момента проникновения патогена) класса Ig. M (можно диагностировать о фазу инфекции) ¢ Max. синтез Ig. M – на 14 день ¢ К концу месяца – уровень ↓ до нормы ¢
Гуморальный иммунный ответ (антителообразовние Начинается активный синтез иммуноглобулинов. Плазматические клетки в основном все уходят в к. м. , и там продуцируют до 30 000 молекул Ig в мин. ¢ Первые АТ появляются в крови на 5 -е сутки (от момента проникновения патогена) класса Ig. M (можно диагностировать о фазу инфекции) ¢ Max. синтез Ig. M – на 14 день ¢ К концу месяца – уровень ↓ до нормы ¢
 Гуморальный иммунный ответ (антителообразовние Когда Тh 2 -хелперы начинают секретировать ИЛ-6, происходит переключение иммуноглобулиновых генов В-лимфоцитов на синтез Ig. G (на 7 -е сутки). ¢ По соотношению Ig. M и Ig. G можно определить стадию болези: Острая - + Ig. M Подострая - +Ig. M и Ig. G Затяжное, хрон. течение, ремиссия - +Ig. G ¢ Max. синтез Ig. G – на 30 день ¢ Срок жизни – до 60 дней ¢
Гуморальный иммунный ответ (антителообразовние Когда Тh 2 -хелперы начинают секретировать ИЛ-6, происходит переключение иммуноглобулиновых генов В-лимфоцитов на синтез Ig. G (на 7 -е сутки). ¢ По соотношению Ig. M и Ig. G можно определить стадию болези: Острая - + Ig. M Подострая - +Ig. M и Ig. G Затяжное, хрон. течение, ремиссия - +Ig. G ¢ Max. синтез Ig. G – на 30 день ¢ Срок жизни – до 60 дней ¢
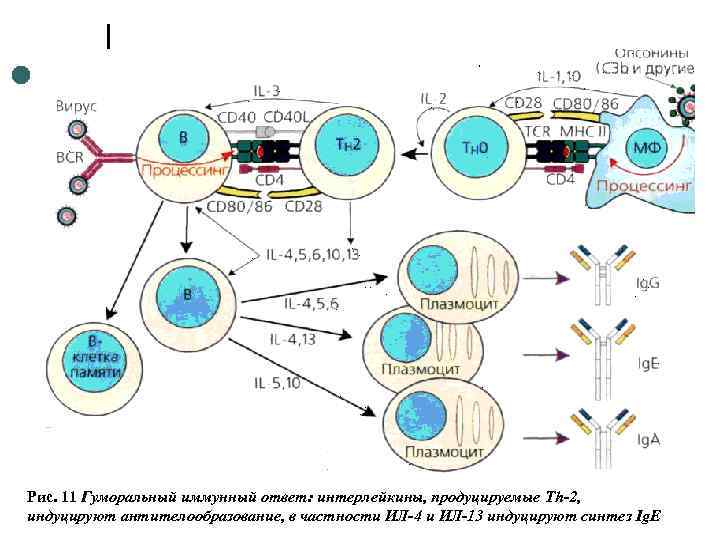 Рис. 11 Гуморальный иммунный ответ: интерлейкины, продуцируемые Th-2, индуцируют антителообразование, в частности ИЛ-4 и ИЛ-13 индуцируют синтез Ig. E
Рис. 11 Гуморальный иммунный ответ: интерлейкины, продуцируемые Th-2, индуцируют антителообразование, в частности ИЛ-4 и ИЛ-13 индуцируют синтез Ig. E
 Гуморальный иммунный ответ (антителообразовние Клетки памяти формируются после 30 дня заболевания. ¢ У взрослых ~ 85% лимфоцитов – клетки памяти. ¢ Клеток памяти нет до встречи с антигеном. ¢ Формирование клеток памяти – главное в иммунном ответе. ¢
Гуморальный иммунный ответ (антителообразовние Клетки памяти формируются после 30 дня заболевания. ¢ У взрослых ~ 85% лимфоцитов – клетки памяти. ¢ Клеток памяти нет до встречи с антигеном. ¢ Формирование клеток памяти – главное в иммунном ответе. ¢
 Клеточный иммунный ответ. ¢ Участвуют популяции Тh 1 -хелперов CD 4+ и цитотоксических Т-лимфоцитов CD 8+ (ЦТЛ). АПК (макрофаги и дендритные клетки) после процессинга поглощенного антигена представляют ЦТЛ микробные пептиды в комплексе с МНС І класса. ЦТЛ с помощью антигенраспознающего рецептора (ТСR) и его корецептора CD 8 распознают соответственно микробный пептид и МНС І класса (двойное распознавание).
Клеточный иммунный ответ. ¢ Участвуют популяции Тh 1 -хелперов CD 4+ и цитотоксических Т-лимфоцитов CD 8+ (ЦТЛ). АПК (макрофаги и дендритные клетки) после процессинга поглощенного антигена представляют ЦТЛ микробные пептиды в комплексе с МНС І класса. ЦТЛ с помощью антигенраспознающего рецептора (ТСR) и его корецептора CD 8 распознают соответственно микробный пептид и МНС І класса (двойное распознавание).
 Клеточный иммунный ответ. ¢ Активированные дифференцированные ЦТЛ вызывают гибель клеток-мишеней с участием перфорина, гранзимов, гранулизинов, Fas -рецепторов и ФНО.
Клеточный иммунный ответ. ¢ Активированные дифференцированные ЦТЛ вызывают гибель клеток-мишеней с участием перфорина, гранзимов, гранулизинов, Fas -рецепторов и ФНО.
 Клеточный иммунный ответ. ¢ Разновидностью клеточного иммунного ответа является гиперчувствительность замедленного типа с участием Тh 1 хелперов CD 4+ и активированных макрофагов. Тh 1 -хелперы CD 4+ распознают на поверхности длительно инфицированных макрофагов микробные пептиды в комплексе с МНС II класса и выделяют IF-y. Происходит активация макрофагов и гибель внутриклеточных микробов.
Клеточный иммунный ответ. ¢ Разновидностью клеточного иммунного ответа является гиперчувствительность замедленного типа с участием Тh 1 хелперов CD 4+ и активированных макрофагов. Тh 1 -хелперы CD 4+ распознают на поверхности длительно инфицированных макрофагов микробные пептиды в комплексе с МНС II класса и выделяют IF-y. Происходит активация макрофагов и гибель внутриклеточных микробов.
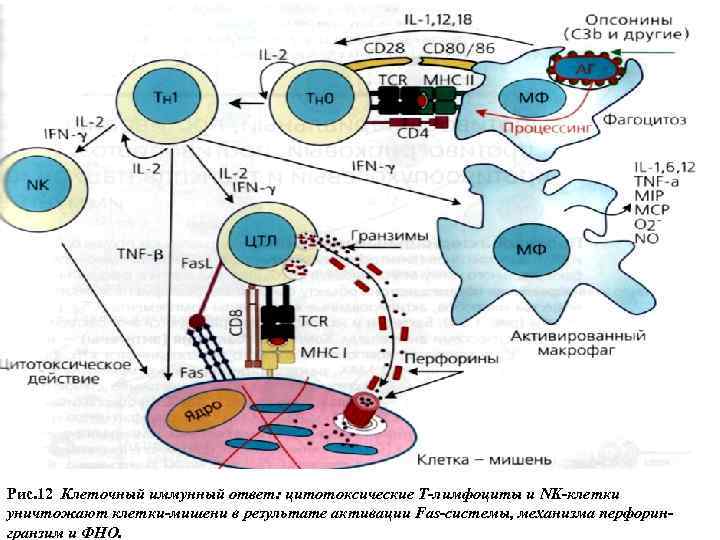 Рис. 12 Клеточный иммунный ответ: цитотоксические Т-лимфоциты и NK-клетки уничтожают клетки-мишени в результате активации Fas-системы, механизма перфорингранзим и ФНО.
Рис. 12 Клеточный иммунный ответ: цитотоксические Т-лимфоциты и NK-клетки уничтожают клетки-мишени в результате активации Fas-системы, механизма перфорингранзим и ФНО.
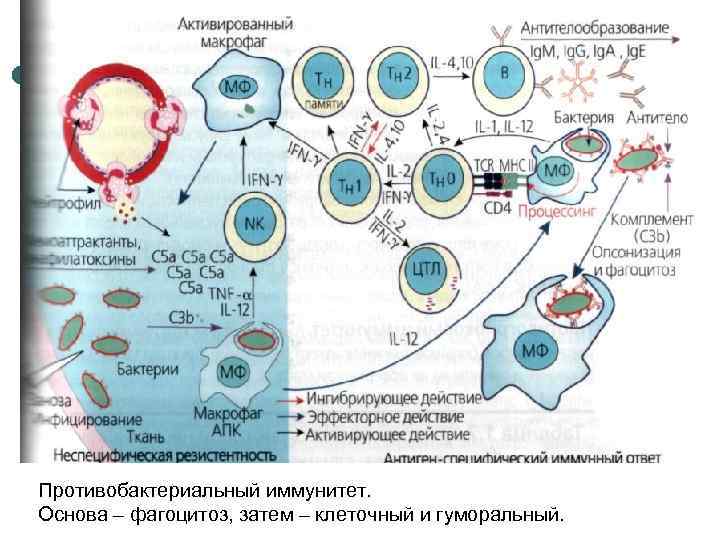 Противобактериальный иммунитет. Основа – фагоцитоз, затем – клеточный и гуморальный.
Противобактериальный иммунитет. Основа – фагоцитоз, затем – клеточный и гуморальный.
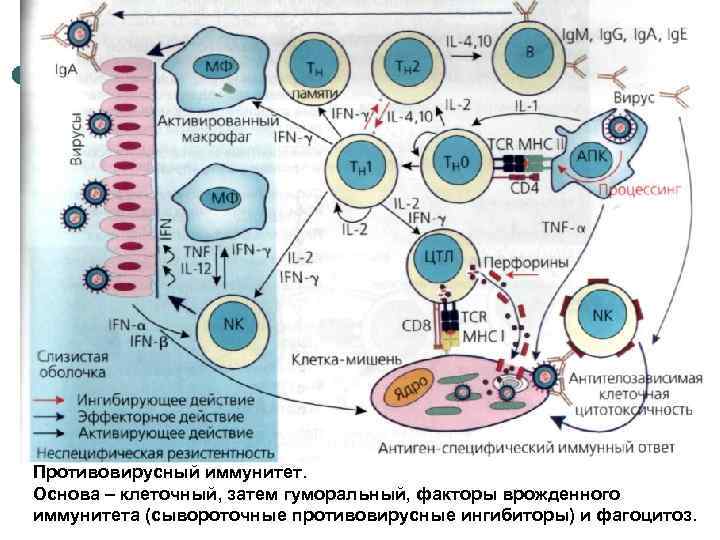 ¢ Противовирусный иммунитет. Основа – клеточный, затем гуморальный, факторы врожденного иммунитета (сывороточные противовирусные ингибиторы) и фагоцитоз.
¢ Противовирусный иммунитет. Основа – клеточный, затем гуморальный, факторы врожденного иммунитета (сывороточные противовирусные ингибиторы) и фагоцитоз.
 Противогрибковый иммунитет Основой противогрибкового иммунитета является клеточный иммунитет: фагоцитоз эпителиоидная гранулематозная реакция ГЗТ Аллергия Ig. E-антитела против антигенов грибов ГЗТ и ГНТ. Антитела (Ig. M, Ig. G) при микозах выявляются в низких титрах. Факторы противогрибковой неспецифической резистентности кожи, слизистых оболочек рта и слюны
Противогрибковый иммунитет Основой противогрибкового иммунитета является клеточный иммунитет: фагоцитоз эпителиоидная гранулематозная реакция ГЗТ Аллергия Ig. E-антитела против антигенов грибов ГЗТ и ГНТ. Антитела (Ig. M, Ig. G) при микозах выявляются в низких титрах. Факторы противогрибковой неспецифической резистентности кожи, слизистых оболочек рта и слюны
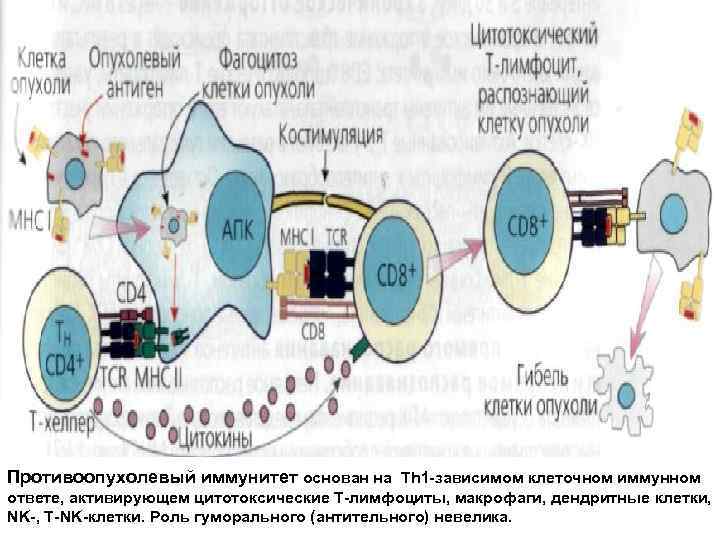 Противоопухолевый иммунитет основан на Тh 1 -зависимом клеточном иммунном ответе, активирующем цитотоксические Т-лимфоциты, макрофаги, дендритные клетки, NK-, T-NK-клетки. Роль гуморального (антительного) невелика.
Противоопухолевый иммунитет основан на Тh 1 -зависимом клеточном иммунном ответе, активирующем цитотоксические Т-лимфоциты, макрофаги, дендритные клетки, NK-, T-NK-клетки. Роль гуморального (антительного) невелика.
 Противоопухолевый иммунитет ¢ ¢ ¢ Антигены опухоли слабо иммуногенны. Антитела, соединяясь с антигенными детерминантами на опухолевых клетках, экранируют их от цитопатогенного действия иммунных лимфоцитов. Механизм презентации антигена часто нарушается, нет достаточного уровня ФНО, интерферонов, ИЛ -2 и др. цитокинов. Опухоли запускают феномен «ускользания» от иммунитета. Уменьшение экспрессии МНС на опухолевых клетках ведет к отмене распознавания опухоли. Неспецифические факторы, повреждающие опухолевые клетки: 1) NK-клетки, система мононуклеарных фагоцитов, противоопухолевая активность которых усиливается под действием ИЛ-2 и ИФН-α, -β; 2) цитокины (ИФН-α, -β, ФНО-α и ИЛ-2).
Противоопухолевый иммунитет ¢ ¢ ¢ Антигены опухоли слабо иммуногенны. Антитела, соединяясь с антигенными детерминантами на опухолевых клетках, экранируют их от цитопатогенного действия иммунных лимфоцитов. Механизм презентации антигена часто нарушается, нет достаточного уровня ФНО, интерферонов, ИЛ -2 и др. цитокинов. Опухоли запускают феномен «ускользания» от иммунитета. Уменьшение экспрессии МНС на опухолевых клетках ведет к отмене распознавания опухоли. Неспецифические факторы, повреждающие опухолевые клетки: 1) NK-клетки, система мононуклеарных фагоцитов, противоопухолевая активность которых усиливается под действием ИЛ-2 и ИФН-α, -β; 2) цитокины (ИФН-α, -β, ФНО-α и ИЛ-2).
 Лабораторные показатели для оценки иммунного статуса ¢ Иммунный статус – состояние иммунной системы человека, оцениваемое комплексом качественных и количественных клинико-лабораторных показателей. Гематологические показатели: ¢ 1. Количество лейкоцитов, эритроцитов, тромбоцитов, гемоглобина в эритроците и в эритроцитах; цветовой показатель. ¢ 2. Процентное содержание нейтрофилов, лимфоцитов, моноцитов, эозинофилов, базофилов. ¢ 3. Показатели СОЭ. ¢
Лабораторные показатели для оценки иммунного статуса ¢ Иммунный статус – состояние иммунной системы человека, оцениваемое комплексом качественных и количественных клинико-лабораторных показателей. Гематологические показатели: ¢ 1. Количество лейкоцитов, эритроцитов, тромбоцитов, гемоглобина в эритроците и в эритроцитах; цветовой показатель. ¢ 2. Процентное содержание нейтрофилов, лимфоцитов, моноцитов, эозинофилов, базофилов. ¢ 3. Показатели СОЭ. ¢
 Оценка Т-клеточной системы иммунитета (клеточного иммунитета): ¢ ¢ ¢ ¢ ¢ 1. Определение общего числа лимфоцитов. 2. Определение числа зрелых Т-лимфоцитов (CD 3+) и их субпопуляций – хелперов (CD 4+) и цитотоксических Тлимфоцитов (CD 8+). 3. Определение соотношения CD 4+CD 8+ (иммунорегуляторный индекс). 4. Определение реакции Т-лимфоцитов на активацию фитогемагглютинином (Т-митоген) в реакции бластной трансформации (РБТЛ). 5. Постановка кожных проб ГЗТ. 6. Дополнительные уточняющие методы: • определение маркера ранней активации CD 25 (рецептор для ИЛ-2) и HLA-DR на Т-лимфоцитах; • исследование продукции цитокинов (ИФН-γ, ИЛ-2, -4, -6, ФНО); определение пролиферативного ответа на специфический антиген в РБТЛ; • определение готовности Т-лимфоцитов к апоптозу (определение апоптозного антигена Fas – CD 95).
Оценка Т-клеточной системы иммунитета (клеточного иммунитета): ¢ ¢ ¢ ¢ ¢ 1. Определение общего числа лимфоцитов. 2. Определение числа зрелых Т-лимфоцитов (CD 3+) и их субпопуляций – хелперов (CD 4+) и цитотоксических Тлимфоцитов (CD 8+). 3. Определение соотношения CD 4+CD 8+ (иммунорегуляторный индекс). 4. Определение реакции Т-лимфоцитов на активацию фитогемагглютинином (Т-митоген) в реакции бластной трансформации (РБТЛ). 5. Постановка кожных проб ГЗТ. 6. Дополнительные уточняющие методы: • определение маркера ранней активации CD 25 (рецептор для ИЛ-2) и HLA-DR на Т-лимфоцитах; • исследование продукции цитокинов (ИФН-γ, ИЛ-2, -4, -6, ФНО); определение пролиферативного ответа на специфический антиген в РБТЛ; • определение готовности Т-лимфоцитов к апоптозу (определение апоптозного антигена Fas – CD 95).
 Оценка В-клеточной системы иммунитета (гуморального иммунитета): ¢ ¢ ¢ ¢ 1. Определения числа В-лимфоцитов (CD 19+ или CD 20+). 2. Определение количества неспецифических иммуноглобулинов (Іg. A, Ig. M, Ig. G, Ig. E). 3. Определение циркулирующих в крови иммунных комплексов. 4. Определение функциональной активности лимфоцитов с помощью РБТЛ на В-клеточный митоген. 5. Дополнительные уточняющие методы: • определение количества специфических иммуноглобулинов (Іg. A, Ig. M, Ig. G, Ig. E); • определение продукции ИЛ-6; • определение секреторного Іg. A.
Оценка В-клеточной системы иммунитета (гуморального иммунитета): ¢ ¢ ¢ ¢ 1. Определения числа В-лимфоцитов (CD 19+ или CD 20+). 2. Определение количества неспецифических иммуноглобулинов (Іg. A, Ig. M, Ig. G, Ig. E). 3. Определение циркулирующих в крови иммунных комплексов. 4. Определение функциональной активности лимфоцитов с помощью РБТЛ на В-клеточный митоген. 5. Дополнительные уточняющие методы: • определение количества специфических иммуноглобулинов (Іg. A, Ig. M, Ig. G, Ig. E); • определение продукции ИЛ-6; • определение секреторного Іg. A.
 Показатели системы комплемента: Определение компонентов комплемента (С 1 q, С 1, С 3, С 4, С 5 и др. ) в сыворотке крови. Система фагоцитов (нейтрофилов): 1. Определение числа нейтрофилов. 2. Определение индекса фагоцитоза (процент клеток, участвующий в фагоцитозе) и фагоцитарного числа (число микробов или др. частиц, захваченных одной клеткой). Определение индекса завершенности фагоцитоза. 3. Определение бактерицидности фагоцитов (по НСТтесту и др. ). 4. Дополнительные уточняющие методы: • определение активности хемотаксиса фагоцитов; • определение способности нейтрофилов к адгезии к пластику и наличия клеток с адгезивными молекулами CD 11 CD 18.
Показатели системы комплемента: Определение компонентов комплемента (С 1 q, С 1, С 3, С 4, С 5 и др. ) в сыворотке крови. Система фагоцитов (нейтрофилов): 1. Определение числа нейтрофилов. 2. Определение индекса фагоцитоза (процент клеток, участвующий в фагоцитозе) и фагоцитарного числа (число микробов или др. частиц, захваченных одной клеткой). Определение индекса завершенности фагоцитоза. 3. Определение бактерицидности фагоцитов (по НСТтесту и др. ). 4. Дополнительные уточняющие методы: • определение активности хемотаксиса фагоцитов; • определение способности нейтрофилов к адгезии к пластику и наличия клеток с адгезивными молекулами CD 11 CD 18.
 Оценка функциональной активности лимфоцитов: (пролиферативный ответ на Т- и В-митогены, цитотоксическая активность NK-клеток. Оценка цитокинового профиля: Определение ИЛ-1, -2, -4, -6 и др. Оценка интерферонового профиля: Определение ИФН-α и ИФН-γ.
Оценка функциональной активности лимфоцитов: (пролиферативный ответ на Т- и В-митогены, цитотоксическая активность NK-клеток. Оценка цитокинового профиля: Определение ИЛ-1, -2, -4, -6 и др. Оценка интерферонового профиля: Определение ИФН-α и ИФН-γ.
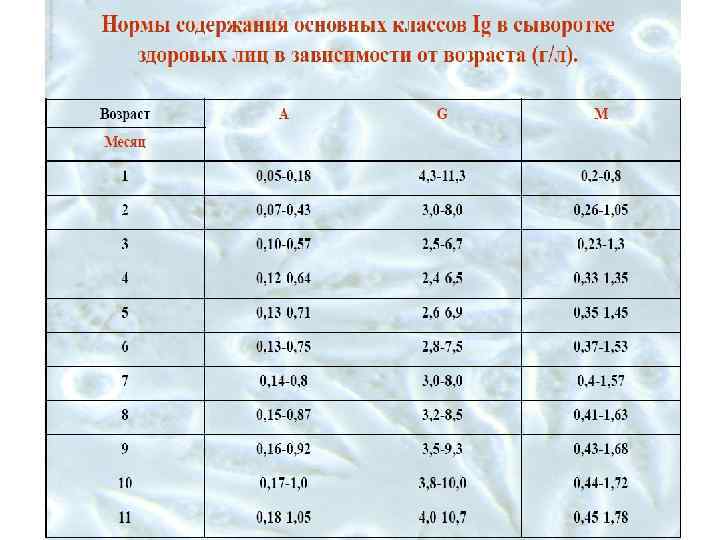
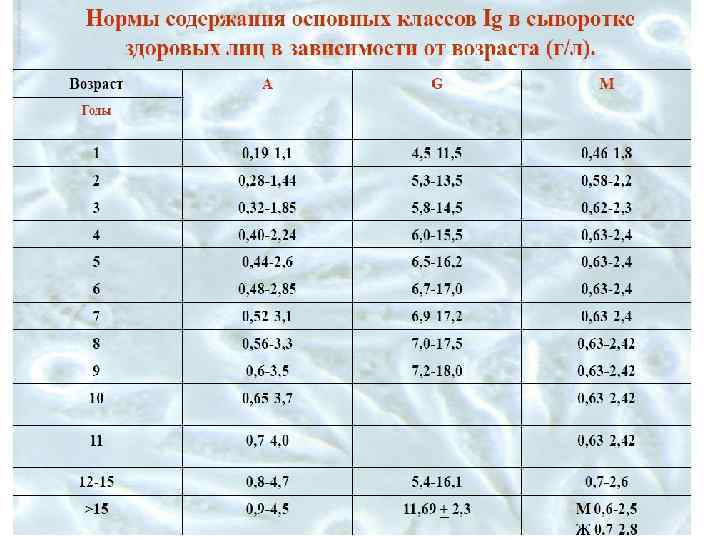
 Нормативные значения некоторых лабораторных показателей иммунного статуса человека в различные возрастные периоды (Проф. Н. М. Калинина, г. С-Петербург Всероссийский центр экстренной и радиационной медицины)
Нормативные значения некоторых лабораторных показателей иммунного статуса человека в различные возрастные периоды (Проф. Н. М. Калинина, г. С-Петербург Всероссийский центр экстренной и радиационной медицины)




 Спасибо за внимание
Спасибо за внимание


