III_гр_обзор_и_химия_бора.ppt
- Количество слайдов: 11
 III Группа ПС ( «короткий» вариант ПС) Главная подгруппа: бор, алюминий и элементы подгруппы галлия Побочная подгруппа: подгруппа Sc + лантаноиды + актиниды Особенности группы в целом: p d (f) f f f - самая элементоемкая группа (37 B элементов); - самая «аномальная группа» ; «аномальные» элементы: B, Ga, Tl – Al Sc в главной подгруппе, Sc, Ce, Tb, Eu, Yb – в побочной. Ga (Элементы, у которых заполнение Y электрона впервые происходит на In новые оболочки: B, Sc, Ce) La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Следствие «аномальностей» : Lu аналогии – особенно в главной Tl Ac Th Pa U Np Pu Am подгруппе проследить более сложно, Cm Bk Cf Es Fm Md No чем в других подгруппах; Lr
III Группа ПС ( «короткий» вариант ПС) Главная подгруппа: бор, алюминий и элементы подгруппы галлия Побочная подгруппа: подгруппа Sc + лантаноиды + актиниды Особенности группы в целом: p d (f) f f f - самая элементоемкая группа (37 B элементов); - самая «аномальная группа» ; «аномальные» элементы: B, Ga, Tl – Al Sc в главной подгруппе, Sc, Ce, Tb, Eu, Yb – в побочной. Ga (Элементы, у которых заполнение Y электрона впервые происходит на In новые оболочки: B, Sc, Ce) La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Следствие «аномальностей» : Lu аналогии – особенно в главной Tl Ac Th Pa U Np Pu Am подгруппе проследить более сложно, Cm Bk Cf Es Fm Md No чем в других подгруппах; Lr
 III Группа ПС ( «короткий» вариант ПС) Главная подгруппа: бор, алюминий и элементы подгруппы галлия Побочная подгруппа: подгруппа Sc + лантаноиды + актиниды p d (f) f f f Особенности группы в целом (продолжение): B - разница между элементами III главной и III побочной подгрупп Al минимальна в ПС (в максимальной Sc степени окисления +3 элементы Ga подгруппы скандия приобретают Y структуру sp элементов (s 2 p 6), а элементы подгруппы галлия – In La Ce Pr Nd Pm Sm Eu структуру d– элементов d 10, т. е. Gd Tb Dy Ho Er Tm Yb главная и побочные подгруппы как Lu бы меняются местами). Tl Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr
III Группа ПС ( «короткий» вариант ПС) Главная подгруппа: бор, алюминий и элементы подгруппы галлия Побочная подгруппа: подгруппа Sc + лантаноиды + актиниды p d (f) f f f Особенности группы в целом (продолжение): B - разница между элементами III главной и III побочной подгрупп Al минимальна в ПС (в максимальной Sc степени окисления +3 элементы Ga подгруппы скандия приобретают Y структуру sp элементов (s 2 p 6), а элементы подгруппы галлия – In La Ce Pr Nd Pm Sm Eu структуру d– элементов d 10, т. е. Gd Tb Dy Ho Er Tm Yb главная и побочные подгруппы как Lu бы меняются местами). Tl Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr
 Особенности химии бора и его соединений: - для впервые появившегося на p- орбитали электрона потенциал ионизации очень велик (по этой причине преобладающими становятся неметаллические свойства); - появляется диагональная аналогия с кремнием; - реализуются соединения с дефицитом электронов (например, диборан B 2 H 6 и другие бораны), которые не трактуются в МВС; - изоэлектронная углероду пара B-N может давать огромное многообразие «псевдоорганических» соединений и, возможно, быть альтернативой известной нам углеродной жизни.
Особенности химии бора и его соединений: - для впервые появившегося на p- орбитали электрона потенциал ионизации очень велик (по этой причине преобладающими становятся неметаллические свойства); - появляется диагональная аналогия с кремнием; - реализуются соединения с дефицитом электронов (например, диборан B 2 H 6 и другие бораны), которые не трактуются в МВС; - изоэлектронная углероду пара B-N может давать огромное многообразие «псевдоорганических» соединений и, возможно, быть альтернативой известной нам углеродной жизни.
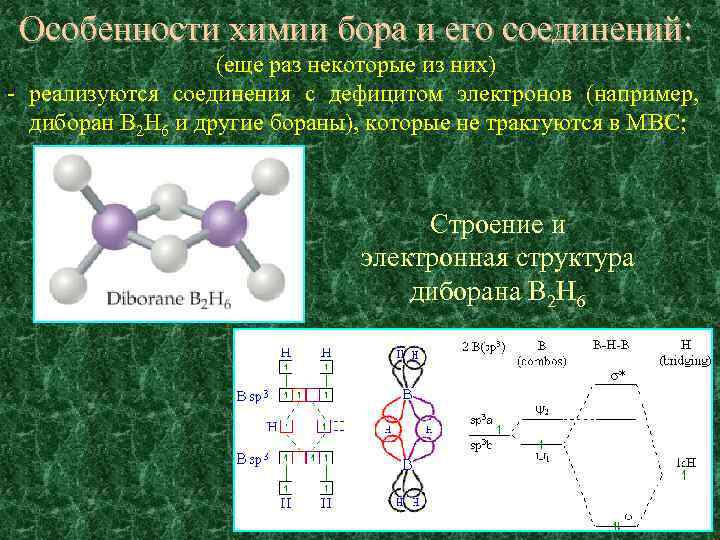 Особенности химии бора и его соединений: (еще раз некоторые из них) - реализуются соединения с дефицитом электронов (например, диборан B 2 H 6 и другие бораны), которые не трактуются в МВС; Строение и электронная структура диборана B 2 H 6
Особенности химии бора и его соединений: (еще раз некоторые из них) - реализуются соединения с дефицитом электронов (например, диборан B 2 H 6 и другие бораны), которые не трактуются в МВС; Строение и электронная структура диборана B 2 H 6
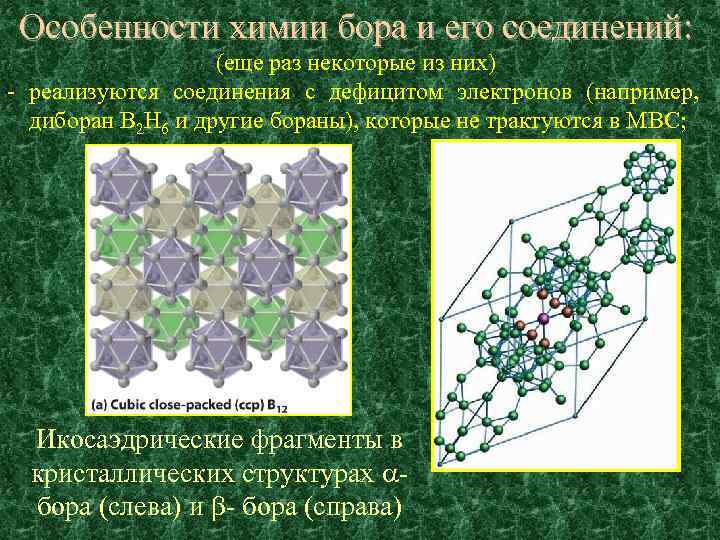 Особенности химии бора и его соединений: (еще раз некоторые из них) - реализуются соединения с дефицитом электронов (например, диборан B 2 H 6 и другие бораны), которые не трактуются в МВС; Икосаэдрические фрагменты в кристаллических структурах бора (слева) и - бора (справа)
Особенности химии бора и его соединений: (еще раз некоторые из них) - реализуются соединения с дефицитом электронов (например, диборан B 2 H 6 и другие бораны), которые не трактуются в МВС; Икосаэдрические фрагменты в кристаллических структурах бора (слева) и - бора (справа)
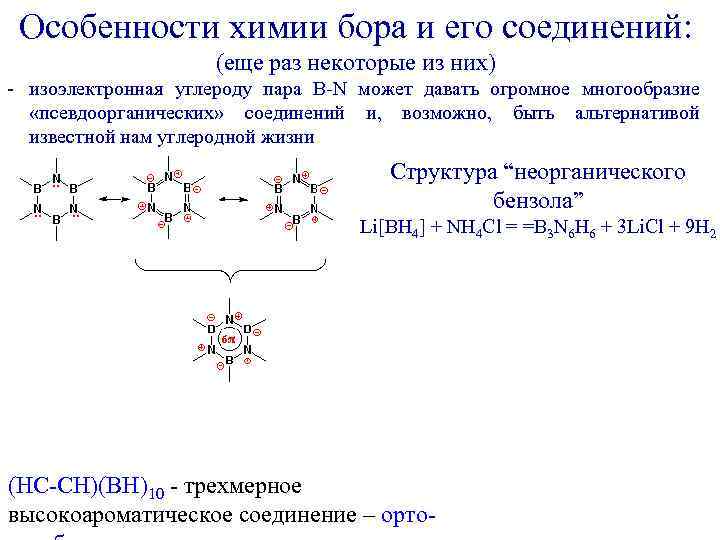 Особенности химии бора и его соединений: (еще раз некоторые из них) - изоэлектронная углероду пара B-N может давать огромное многообразие «псевдоорганических» соединений и, возможно, быть альтернативой известной нам углеродной жизни. Структура “неорганического бензола” Li[BH 4] + NH 4 Cl = =B 3 N 6 H 6 + 3 Li. Cl + 9 H 2 (HC-CH)(BH)10 - трехмерное высокоароматическое соединение – орто-
Особенности химии бора и его соединений: (еще раз некоторые из них) - изоэлектронная углероду пара B-N может давать огромное многообразие «псевдоорганических» соединений и, возможно, быть альтернативой известной нам углеродной жизни. Структура “неорганического бензола” Li[BH 4] + NH 4 Cl = =B 3 N 6 H 6 + 3 Li. Cl + 9 H 2 (HC-CH)(BH)10 - трехмерное высокоароматическое соединение – орто-
 Свойства бора (продолжение) 1. Единственный неметалл в 13 группе 2. Очень высокие т. пл. (2573 о. С) и т. кип. (3660 о. С) 3. = 2. 35 г/см 3 – черный, кристаллический бор; = 1. 73 г/см 3 – коричневый, аморфный бор 4. Кристаллический бор очень твердый (9. 5 по шкале Мооса) 5. Кристаллический бор – полупроводник, Еg = 1. 55 э. В 6. Бор имеет 2 стабильных изотопа 10 В, 11 В 10 В + 1 n = 4 He + 7 Li – замедление нейтронов 7. Бор – восстановитель, Е 0(Н 3 ВО 3/В) = -0. 87 В
Свойства бора (продолжение) 1. Единственный неметалл в 13 группе 2. Очень высокие т. пл. (2573 о. С) и т. кип. (3660 о. С) 3. = 2. 35 г/см 3 – черный, кристаллический бор; = 1. 73 г/см 3 – коричневый, аморфный бор 4. Кристаллический бор очень твердый (9. 5 по шкале Мооса) 5. Кристаллический бор – полупроводник, Еg = 1. 55 э. В 6. Бор имеет 2 стабильных изотопа 10 В, 11 В 10 В + 1 n = 4 He + 7 Li – замедление нейтронов 7. Бор – восстановитель, Е 0(Н 3 ВО 3/В) = -0. 87 В
 Химические свойства бора 1. Бор химически инертен. Не реагирует с водой, кислотами и щелочами при н. у. 2. При нагревании реагирует с неметаллами 4 B + 3 O 2 = 2 B 2 O 3 700 o. C 2 B + 3 Cl 2 = 2 BCl 3 800 o. C 2 B + N 2 = 2 BN 900 o. C 3. При Т>1000 о. С реагирует со многими металлами и оксидами 2 B + Al = Al. B 2 10 B + 2 P 2 O 5 = P 4 + 5 B 2 O 3 2 B + 3 H 2 O = 3 H 2 + B 2 O 3 4. Окисляется кислотами-окислителями и в щелочных расплавах B + 3 HNO 3 конц = H 3 BO 3 + 3 NO 2 ∼ 100 o. C 2 B + KCl. O 3 + 2 KOH = 2 KBO 2 + KCl + H 2 O
Химические свойства бора 1. Бор химически инертен. Не реагирует с водой, кислотами и щелочами при н. у. 2. При нагревании реагирует с неметаллами 4 B + 3 O 2 = 2 B 2 O 3 700 o. C 2 B + 3 Cl 2 = 2 BCl 3 800 o. C 2 B + N 2 = 2 BN 900 o. C 3. При Т>1000 о. С реагирует со многими металлами и оксидами 2 B + Al = Al. B 2 10 B + 2 P 2 O 5 = P 4 + 5 B 2 O 3 2 B + 3 H 2 O = 3 H 2 + B 2 O 3 4. Окисляется кислотами-окислителями и в щелочных расплавах B + 3 HNO 3 конц = H 3 BO 3 + 3 NO 2 ∼ 100 o. C 2 B + KCl. O 3 + 2 KOH = 2 KBO 2 + KCl + H 2 O
 Прочие особенности химии бора и его соединений: соединений • Преобладание кислотных свойств над основными для оксида и гидроксида бора: B 2 O 3 + 2 Na. OH(расплав) = Na. BO 2 + H 2 O B 2 O 3 + 3 H 2 O 2 B(OH)3 ; при нагревании борная кислота ( B(OH)3 H 3 BO 3 ) разлагается; B(OH)3 + H 2 O H[B(OH)4] H+ + [B(OH)4] (сильно смещено влево!); • B(OH)3 – амфолит с преобладанием кислотных свойств: 4 H 3 BO 3 + 2 Na. OH = Na 2 B 4 O 7 + 7 H 2 O. Но: 2 B(OH)3 + 3 H 2 SO 4 (б/в) = B 2(SO 4)3 + 3 H 2 O • Склонность бора к формированию ковалентности, равной 4 (одна из связей сформирована по д/а механизму): Li. H + B 2 H 6 = 2 Li[BH 4] • Склонность к образованию сложных эфиров со спиртами: В(OH)3 + 3 CH 3 OH B(OCH 3)3 + 3 H 2 O
Прочие особенности химии бора и его соединений: соединений • Преобладание кислотных свойств над основными для оксида и гидроксида бора: B 2 O 3 + 2 Na. OH(расплав) = Na. BO 2 + H 2 O B 2 O 3 + 3 H 2 O 2 B(OH)3 ; при нагревании борная кислота ( B(OH)3 H 3 BO 3 ) разлагается; B(OH)3 + H 2 O H[B(OH)4] H+ + [B(OH)4] (сильно смещено влево!); • B(OH)3 – амфолит с преобладанием кислотных свойств: 4 H 3 BO 3 + 2 Na. OH = Na 2 B 4 O 7 + 7 H 2 O. Но: 2 B(OH)3 + 3 H 2 SO 4 (б/в) = B 2(SO 4)3 + 3 H 2 O • Склонность бора к формированию ковалентности, равной 4 (одна из связей сформирована по д/а механизму): Li. H + B 2 H 6 = 2 Li[BH 4] • Склонность к образованию сложных эфиров со спиртами: В(OH)3 + 3 CH 3 OH B(OCH 3)3 + 3 H 2 O
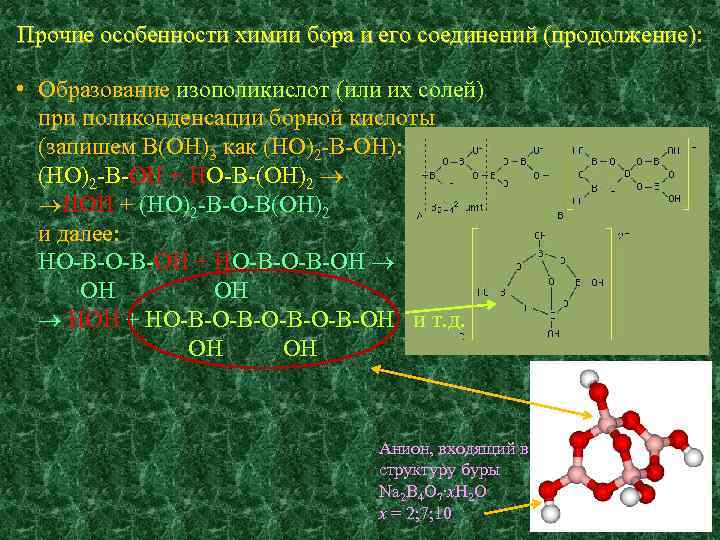 Прочие особенности химии бора и его соединений (продолжение): (продолжение) • Образование изополикислот (или их солей) при поликонденсации борной кислоты (запишем B(OH)3 как (HO)2 -B-OH): (HO)2 -B-OH + HO-B-(OH)2 HOH + (HO)2 -B-O-B(OH)2 и далее: HO-B-OH + HO-B-OH OH OH HOH + HO-B-O-B-OH и т. д. OH OH Анион, входящий в структуру буры Na 2 B 4 O 7∙x. H 2 O x = 2; 7; 10
Прочие особенности химии бора и его соединений (продолжение): (продолжение) • Образование изополикислот (или их солей) при поликонденсации борной кислоты (запишем B(OH)3 как (HO)2 -B-OH): (HO)2 -B-OH + HO-B-(OH)2 HOH + (HO)2 -B-O-B(OH)2 и далее: HO-B-OH + HO-B-OH OH OH HOH + HO-B-O-B-OH и т. д. OH OH Анион, входящий в структуру буры Na 2 B 4 O 7∙x. H 2 O x = 2; 7; 10
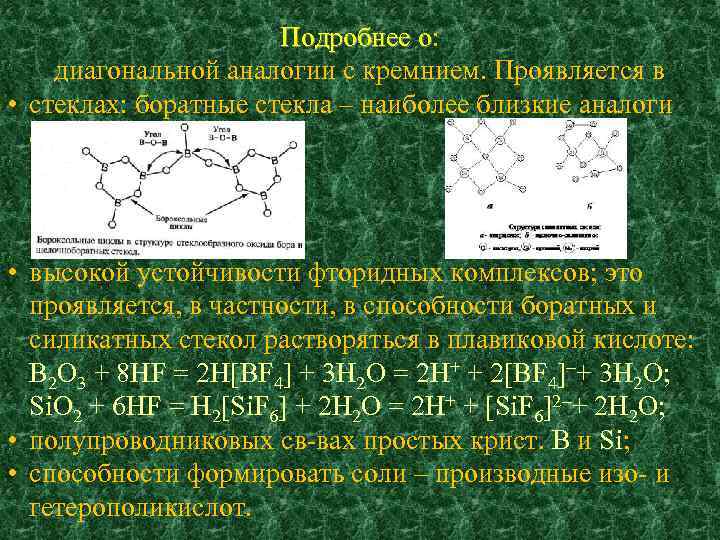 Подробнее о: о диагональной аналогии с кремнием. Проявляется в • стеклах: боратные стекла – наиболее близкие аналоги силикатных стекол; • высокой устойчивости фторидных комплексов; это проявляется, в частности, в способности боратных и силикатных стекол растворяться в плавиковой кислоте: B 2 O 3 + 8 HF = 2 H[BF 4] + 3 H 2 O = 2 H+ + 2[BF 4] + 3 H 2 O; Si. O 2 + 6 HF = H 2[Si. F 6] + 2 H 2 O = 2 H+ + [Si. F 6]2 + 2 H 2 O; • полупроводниковых св-вах простых крист. B и Si; • способности формировать соли – производные изо- и гетерополикислот.
Подробнее о: о диагональной аналогии с кремнием. Проявляется в • стеклах: боратные стекла – наиболее близкие аналоги силикатных стекол; • высокой устойчивости фторидных комплексов; это проявляется, в частности, в способности боратных и силикатных стекол растворяться в плавиковой кислоте: B 2 O 3 + 8 HF = 2 H[BF 4] + 3 H 2 O = 2 H+ + 2[BF 4] + 3 H 2 O; Si. O 2 + 6 HF = H 2[Si. F 6] + 2 H 2 O = 2 H+ + [Si. F 6]2 + 2 H 2 O; • полупроводниковых св-вах простых крист. B и Si; • способности формировать соли – производные изо- и гетерополикислот.


