II закон термодинамики Формулировка условий самопроизвольности протекания процессов







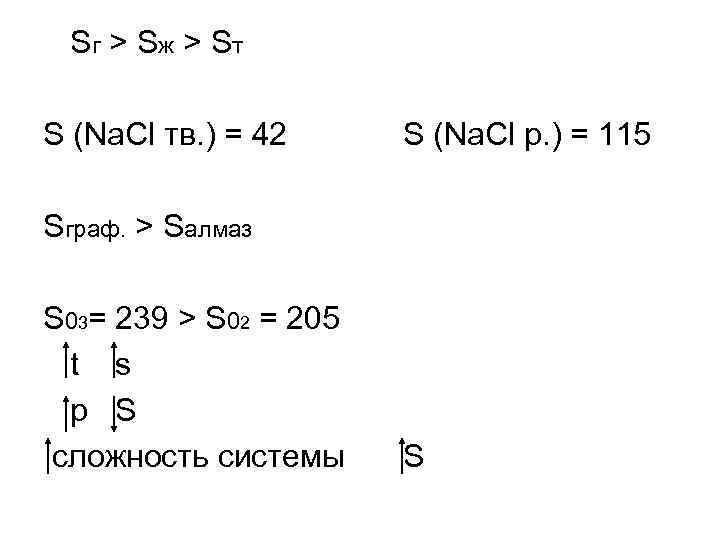




















II закон термодинамики.ppt
- Количество слайдов: 31
 II закон термодинамики Формулировка условий самопроизвольности протекания процессов
II закон термодинамики Формулировка условий самопроизвольности протекания процессов
 Самопроизвольные процессы совершаются без затрат работы извне. Самопроизвольная система Переходит в более устойчивое состояние.
Самопроизвольные процессы совершаются без затрат работы извне. Самопроизвольная система Переходит в более устойчивое состояние.
 В изолированных системах Самопроизвольно идут процессы с увеличением энтропии S>0 Энтропия (S)- т/д функция, мера неупорядоченности системы
В изолированных системах Самопроизвольно идут процессы с увеличением энтропии S>0 Энтропия (S)- т/д функция, мера неупорядоченности системы
 Клаузиус (1865) Энтропия-часть энергии системы, которая рассеивается в виде теплоты и не может превратиться в полезную работу. S=Q/T Q-тепло, полученное системой Дж/моль*к T-температура системы S энергия на полезную работу
Клаузиус (1865) Энтропия-часть энергии системы, которая рассеивается в виде теплоты и не может превратиться в полезную работу. S=Q/T Q-тепло, полученное системой Дж/моль*к T-температура системы S энергия на полезную работу
 Больцман: • «любая система стремится самопроизвольно перейти в наиболее вероятное состояние хаоса, беспорядка с max энтропией. S=K*Log. W W-т/д вероятность KБ= R/Na=1, 38*10 -23
Больцман: • «любая система стремится самопроизвольно перейти в наиболее вероятное состояние хаоса, беспорядка с max энтропией. S=K*Log. W W-т/д вероятность KБ= R/Na=1, 38*10 -23
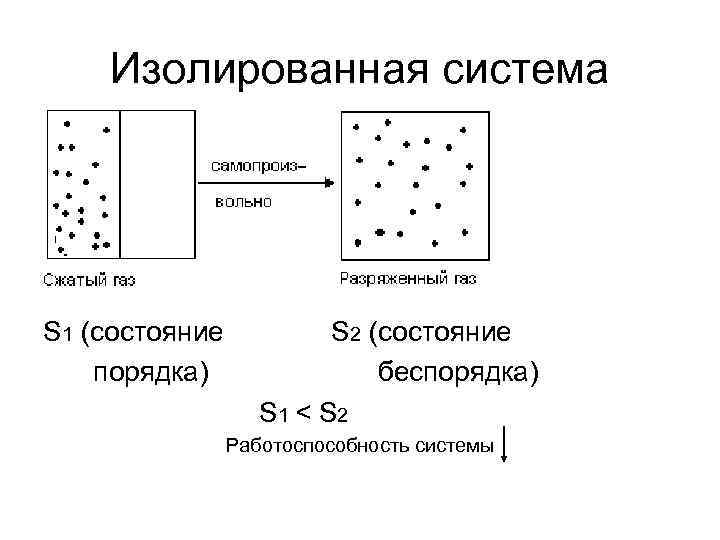
 Изолированная система S 1 (состояние S 2 (состояние порядка) беспорядка) S 1 < S 2 Работоспособность системы
Изолированная система S 1 (состояние S 2 (состояние порядка) беспорядка) S 1 < S 2 Работоспособность системы
 Энтропия- функция состояния. Изменение энтропии в ходе процесса – по 1 му следствию из за кона Гесса: S 0 p= S 0 прод. - S 0 реаг. (Дж/моль*к) S 0 - стандартная энтропия Рассчитывают при 298 К, 101, 3 к. Па (1 атм)
Энтропия- функция состояния. Изменение энтропии в ходе процесса – по 1 му следствию из за кона Гесса: S 0 p= S 0 прод. - S 0 реаг. (Дж/моль*к) S 0 - стандартная энтропия Рассчитывают при 298 К, 101, 3 к. Па (1 атм)
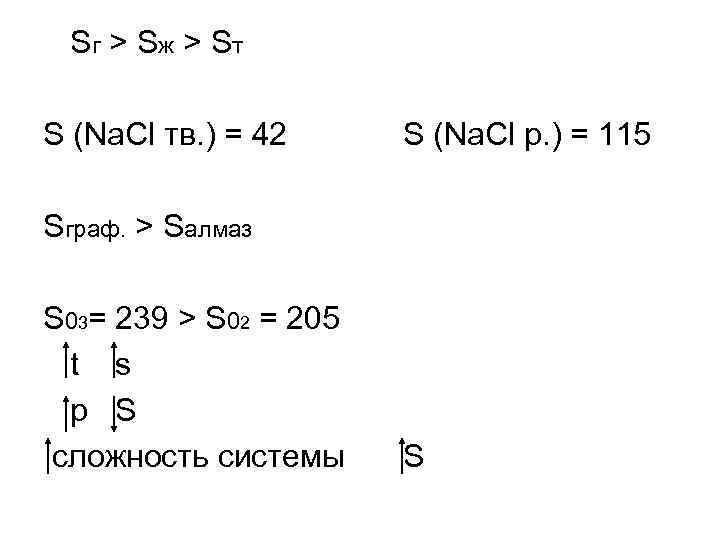 Sг > S ж > S т S (Na. Cl тв. ) = 42 S (Na. Cl p. ) = 115 Sграф. > Sалмаз S 03= 239 > S 02 = 205 t s p S сложность системы S
Sг > S ж > S т S (Na. Cl тв. ) = 42 S (Na. Cl p. ) = 115 Sграф. > Sалмаз S 03= 239 > S 02 = 205 t s p S сложность системы S
 In vivo S при эмбриогенезе, регенерации тканей, росте раковых клеток, при старении. Smax - смерть Smin в 25 -32 года
In vivo S при эмбриогенезе, регенерации тканей, росте раковых клеток, при старении. Smax - смерть Smin в 25 -32 года
 Энтропийный фактор- учитывает стремление к максимуму энтропии. Энтальпийный фактор- учитывает стремление к достижению минимума энергии.
Энтропийный фактор- учитывает стремление к максимуму энтропии. Энтальпийный фактор- учитывает стремление к достижению минимума энергии.
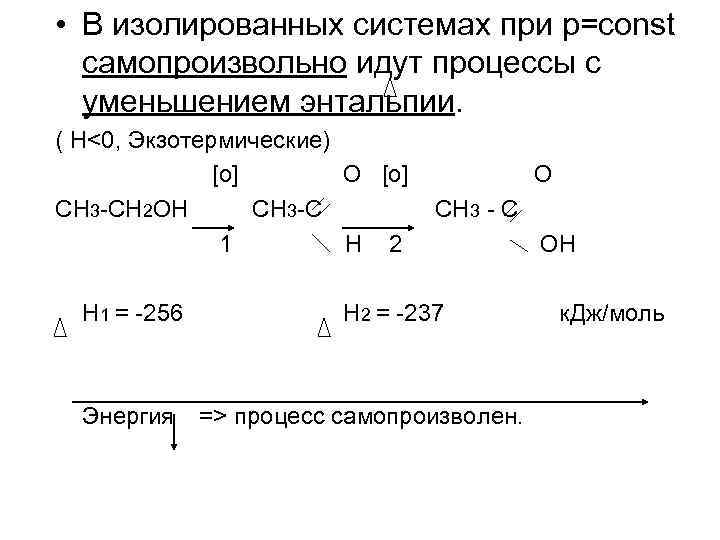
 • В изолированных системах при p=const самопроизвольно идут процессы с уменьшением энтальпии. ( H<0, Экзотермические) [o] O [o] O CH 3 -CH 2 OH CH 3 -C CH 3 - C 1 H 2 OH H 1 = -256 H 2 = -237 к. Дж/моль Энергия => процесс самопроизволен.
• В изолированных системах при p=const самопроизвольно идут процессы с уменьшением энтальпии. ( H<0, Экзотермические) [o] O [o] O CH 3 -CH 2 OH CH 3 -C CH 3 - C 1 H 2 OH H 1 = -256 H 2 = -237 к. Дж/моль Энергия => процесс самопроизволен.
 Свободная энергия Гиббса (G)- обобщенная т/д функция состояния системы, учитывающая энергетику и неупорядоченность системы при изобарно – изотермических условиях. Энергия Гиббса- та часть энергии системы, которая идёт на совершение полезной работы. G = H - TS
Свободная энергия Гиббса (G)- обобщенная т/д функция состояния системы, учитывающая энергетику и неупорядоченность системы при изобарно – изотермических условиях. Энергия Гиббса- та часть энергии системы, которая идёт на совершение полезной работы. G = H - TS
 Совершение работы => убыль свободной энергии Гиббса. A= - G G сгорание глюкозы in vivo = -2880 к. Дж/моль Þ -кровообращение -дыхание -секреция соков -передача нервных импульсов
Совершение работы => убыль свободной энергии Гиббса. A= - G G сгорание глюкозы in vivo = -2880 к. Дж/моль Þ -кровообращение -дыхание -секреция соков -передача нервных импульсов
 Энергия Гиббса Главный критерий самопроизвольных процессов, т. к. характеризует работоспособность системы. 2 закон термодинамики «При р, Т = const в системе самопроизвольно идут процессы с уменьшением энергии Гиббса, т. с. G<0 G= H–T S G - полезная работа H – энергетическое состояние, изменение энтальпии S – мера неупорядоченности
Энергия Гиббса Главный критерий самопроизвольных процессов, т. к. характеризует работоспособность системы. 2 закон термодинамики «При р, Т = const в системе самопроизвольно идут процессы с уменьшением энергии Гиббса, т. с. G<0 G= H–T S G - полезная работа H – энергетическое состояние, изменение энтальпии S – мера неупорядоченности
 Три способа расчета G 1. по 2 закону т/д G= H–T S Возможны самопроиз- H S вольные процессы -экзо + G<0 при любой Т -экзо - G<0 при низкой Т +эндо + G<0 при высокой Т +эндо - G>0 при не возможно при любой Т
Три способа расчета G 1. по 2 закону т/д G= H–T S Возможны самопроиз- H S вольные процессы -экзо + G<0 при любой Т -экзо - G<0 при низкой Т +эндо + G<0 при высокой Т +эндо - G>0 при не возможно при любой Т
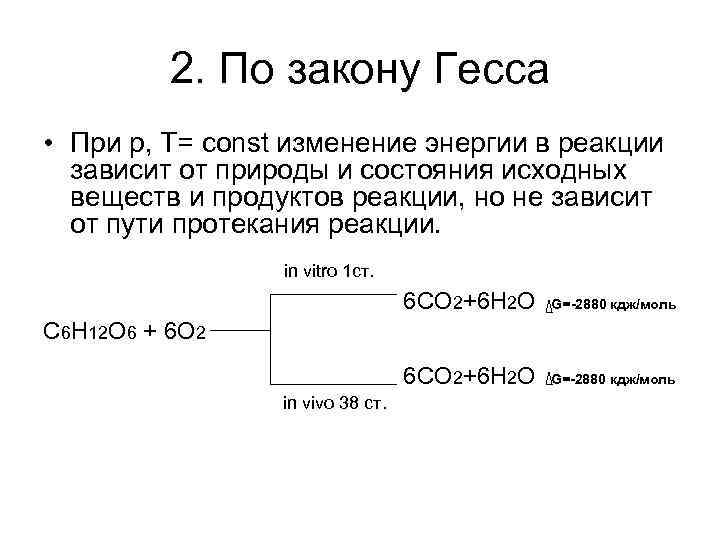
 2. По закону Гесса • При р, Т= const изменение энергии в реакции зависит от природы и состояния исходных веществ и продуктов реакции, но не зависит от пути протекания реакции. in vitro 1 ст. 6 CO 2+6 H 2 O G=-2880 кдж/моль C 6 H 12 O 6 + 6 O 2 6 CO 2+6 H 2 O G=-2880 кдж/моль in vivo 38 ст.
2. По закону Гесса • При р, Т= const изменение энергии в реакции зависит от природы и состояния исходных веществ и продуктов реакции, но не зависит от пути протекания реакции. in vitro 1 ст. 6 CO 2+6 H 2 O G=-2880 кдж/моль C 6 H 12 O 6 + 6 O 2 6 CO 2+6 H 2 O G=-2880 кдж/моль in vivo 38 ст.
 3. По 1 му следствию закона Гесса Изменение энергии Гиббса в химической реакции равно разности между суммой стандартных энергий Гиббса образования продуктов реакции и суммой стандартных энергий Гиббса образования исходных веществ (с учётом коэффициентов) Gр = G 0 обр. прод. - G 0 обр. исх. в-ва к. Дж/моль G 0 обр. -стандартные энергии Гиббса образованная 1 моль вещества при 298 к и 101, 3 к. Па. G 0 обр. прост. в-ва=0
3. По 1 му следствию закона Гесса Изменение энергии Гиббса в химической реакции равно разности между суммой стандартных энергий Гиббса образования продуктов реакции и суммой стандартных энергий Гиббса образования исходных веществ (с учётом коэффициентов) Gр = G 0 обр. прод. - G 0 обр. исх. в-ва к. Дж/моль G 0 обр. -стандартные энергии Гиббса образованная 1 моль вещества при 298 к и 101, 3 к. Па. G 0 обр. прост. в-ва=0
 Биоэнергетика- наука о превращении, сохранении, использовании энергии в организме. Источник Е: энергия химических связей в компонентах пищи (белках, жирах, углеводах). Окисление пищи => энергия => работа внутри и вне организма.
Биоэнергетика- наука о превращении, сохранении, использовании энергии в организме. Источник Е: энергия химических связей в компонентах пищи (белках, жирах, углеводах). Окисление пищи => энергия => работа внутри и вне организма.
 Особенности живых систем: 1. G 01~const => Gmin => 70 -80 лет жизни. 2. S~const (~ 60% энергии сгорание пищи запасается в виде АТФ). 3. Возможны процессы с G>0, S<0 (биосинтез) за счёт сопряжения с процессами G<0
Особенности живых систем: 1. G 01~const => Gmin => 70 -80 лет жизни. 2. S~const (~ 60% энергии сгорание пищи запасается в виде АТФ). 3. Возможны процессы с G>0, S<0 (биосинтез) за счёт сопряжения с процессами G<0
 • Биохимические реакции в уменьшением энергии Гиббса ( G<0)- экзэргонические самопроизвольные. Биологические реакции с увеличением энергии Гиббса ( G>0)- эндэрганические, не возможны без внешнего подвода энергии. Фотосинтез в растениях под воздействием солнечной энергии. свет 6 CO 2+6 H 2 O C 6 H 12 O 6+6 O 2 Gр=2870 к. Дж/моль
• Биохимические реакции в уменьшением энергии Гиббса ( G<0)- экзэргонические самопроизвольные. Биологические реакции с увеличением энергии Гиббса ( G>0)- эндэрганические, не возможны без внешнего подвода энергии. Фотосинтез в растениях под воздействием солнечной энергии. свет 6 CO 2+6 H 2 O C 6 H 12 O 6+6 O 2 Gр=2870 к. Дж/моль
 Прототрофные клетки (растительные)- Источник энергии солнечный свет. Гетеротрофные клетки (животные)- получают энергию за счёт окисления пищи. 40% этой энергии => в хим. энергию связей в АТФ. O О О Аденозин P O ~ Р ОН ОН ОН Макроэргические связи- при их гидролизе выделяется значительное количество энергии.
Прототрофные клетки (растительные)- Источник энергии солнечный свет. Гетеротрофные клетки (животные)- получают энергию за счёт окисления пищи. 40% этой энергии => в хим. энергию связей в АТФ. O О О Аденозин P O ~ Р ОН ОН ОН Макроэргические связи- при их гидролизе выделяется значительное количество энергии.
 АТФ + H 2 O АДФ + Ф ∆G 01 p =-30, 5 к. Дж/моль АТФ + 2 H 2 O АМФ + Ф ∆G 01 p =-61, 0 к. Дж/моль АТФ- промежуточный продукт, обеспечивающий организм энергии, необходимой для протекания жизненно важных эндэргонических процессов: -синтез метаболитов (химическая работа) -сокращение мышц (механическая работа) -перенос веществ через мембраны против градиента концентрации (активный транспорт) Передача информации (передача нервных импульсов)
АТФ + H 2 O АДФ + Ф ∆G 01 p =-30, 5 к. Дж/моль АТФ + 2 H 2 O АМФ + Ф ∆G 01 p =-61, 0 к. Дж/моль АТФ- промежуточный продукт, обеспечивающий организм энергии, необходимой для протекания жизненно важных эндэргонических процессов: -синтез метаболитов (химическая работа) -сокращение мышц (механическая работа) -перенос веществ через мембраны против градиента концентрации (активный транспорт) Передача информации (передача нервных импульсов)
 In vivo эндэргонические процессы ∆G>0 сопряжены с экзэргоническими (∆G<0) Пример 1. а)синтез сахарозы, эндэргоническая реакция. АТФ + H 2 O АДФ + Ф ∆G 01 р = -30, 5 к. Дж/моль < 0 Гл + Фр + АТФ Сах + АДФ + Ф ∆G 01 р = -20, 9 к. Дж/моль < 0 Пример 2. а) синтез дипептида Ала + Гли ала-гли + H 2 O ∆G 01 р > 0, эндэрг. б) АТФ + H 2 O АДФ + Ф ∆G 01 р < 0, экзэрг. Сопряжение реакции идут ∆G<0, сопр. р-я возможна в тандеме.
In vivo эндэргонические процессы ∆G>0 сопряжены с экзэргоническими (∆G<0) Пример 1. а)синтез сахарозы, эндэргоническая реакция. АТФ + H 2 O АДФ + Ф ∆G 01 р = -30, 5 к. Дж/моль < 0 Гл + Фр + АТФ Сах + АДФ + Ф ∆G 01 р = -20, 9 к. Дж/моль < 0 Пример 2. а) синтез дипептида Ала + Гли ала-гли + H 2 O ∆G 01 р > 0, эндэрг. б) АТФ + H 2 O АДФ + Ф ∆G 01 р < 0, экзэрг. Сопряжение реакции идут ∆G<0, сопр. р-я возможна в тандеме.
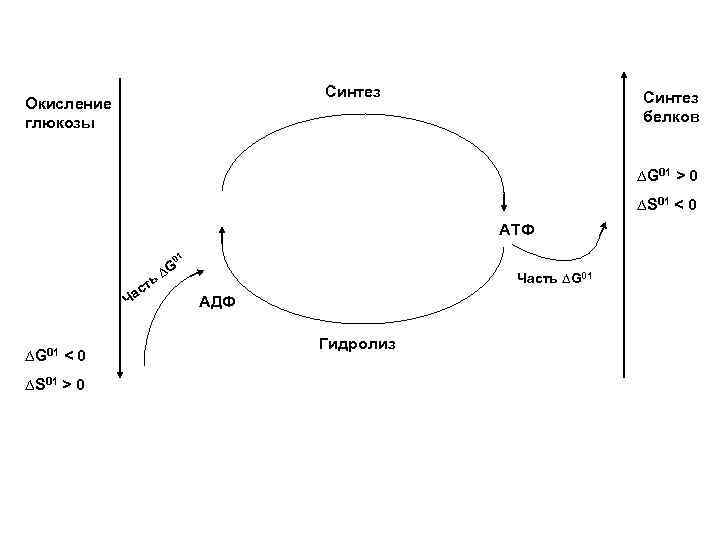
 Синтез Окисление глюкозы белков ∆G 01 > 0 ∆S 01 < 0 АТФ 01 ∆G Часть ∆G 01 ь ст Ча АДФ Гидролиз ∆G 01 < 0 ∆S 01 > 0
Синтез Окисление глюкозы белков ∆G 01 > 0 ∆S 01 < 0 АТФ 01 ∆G Часть ∆G 01 ь ст Ча АДФ Гидролиз ∆G 01 < 0 ∆S 01 > 0
 Эффективные фосфорилированные макроэргические соединения Название ∆G 01 гидролиза Креатинфосфат - 43, 1 3 -фосфоглицерилфосфат - 49, 4 фосфоенол пируват - 61, 9 С помощью этих веществ синтез АТФ из АДФ
Эффективные фосфорилированные макроэргические соединения Название ∆G 01 гидролиза Креатинфосфат - 43, 1 3 -фосфоглицерилфосфат - 49, 4 фосфоенол пируват - 61, 9 С помощью этих веществ синтез АТФ из АДФ
 Химическое равновесие 1. Равенство скоростей прямой и обратной реакции Vпр. = Vобр. 2. Энергитическая выгодность (G=min) 3. Отсутствие изменений величин параметров и функций состояния системы (∆С=0 ∆H=0 ∆S=0 ∆G=0) Большинство биохимических реакций обратимы: НВ + O 2 НВо 2; CO 2 + H 2 O H 2 CO 3; гидролиз
Химическое равновесие 1. Равенство скоростей прямой и обратной реакции Vпр. = Vобр. 2. Энергитическая выгодность (G=min) 3. Отсутствие изменений величин параметров и функций состояния системы (∆С=0 ∆H=0 ∆S=0 ∆G=0) Большинство биохимических реакций обратимы: НВ + O 2 НВо 2; CO 2 + H 2 O H 2 CO 3; гидролиз
 ĸ 1 а. А + в. В с. С + d. D ĸ 2 реагенты продукты Vпр = К 1 [А]а [В]в Vобр = К 2 [С]c [D]d равновесие: Vпр = Vобр К 1 [А]а [В]в = K 2 [С]с [D]d Кравн. = К 1 = [С]с [D]d К 2 [А]а [В]в
ĸ 1 а. А + в. В с. С + d. D ĸ 2 реагенты продукты Vпр = К 1 [А]а [В]в Vобр = К 2 [С]c [D]d равновесие: Vпр = Vобр К 1 [А]а [В]в = K 2 [С]с [D]d Кравн. = К 1 = [С]с [D]d К 2 [А]а [В]в
 ∆ G= - RT ln Kравн. = 1 ∆ G=0 равновесие Kравн. > 1 (K 1 > K 2) самопроизвольна прямая реакция Kравн. < 1 (K 1 < K 2) самопроизвольна обратная реакция Нв + O 2 Hв. O 2 Кравн. = 1300 при 37 C ; 1 атм. Кравн. синтеза дипептидов = 0, 001 => самопроизвольно не идёт.
∆ G= - RT ln Kравн. = 1 ∆ G=0 равновесие Kравн. > 1 (K 1 > K 2) самопроизвольна прямая реакция Kравн. < 1 (K 1 < K 2) самопроизвольна обратная реакция Нв + O 2 Hв. O 2 Кравн. = 1300 при 37 C ; 1 атм. Кравн. синтеза дипептидов = 0, 001 => самопроизвольно не идёт.
 Принцип Ле Шателье: «Если на систему, находящуюся в равновесии, произвести внешнее воздействие (изменить р, Т, С), то равновесие сместится в сторону реакции, компенсирующей воздействие» . Hв + O 2 Hво 2 В легких Ро 2 В тканях Ро 2
Принцип Ле Шателье: «Если на систему, находящуюся в равновесии, произвести внешнее воздействие (изменить р, Т, С), то равновесие сместится в сторону реакции, компенсирующей воздействие» . Hв + O 2 Hво 2 В легких Ро 2 В тканях Ро 2
 Живая система при воздействии на неё перестраивается так, чтобы уменьшить воздействие (для поддержания стационарного состояния). Отравление рвота Вирус t Усталость сон
Живая система при воздействии на неё перестраивается так, чтобы уменьшить воздействие (для поддержания стационарного состояния). Отравление рвота Вирус t Усталость сон
 Общие законы химической термодинамики дают врачу ключ к пониманию энергетической стороны биохимических реакций в организме и возможность регулировать эти процессы путём профилактических и лечебных мероприятий.
Общие законы химической термодинамики дают врачу ключ к пониманию энергетической стороны биохимических реакций в организме и возможность регулировать эти процессы путём профилактических и лечебных мероприятий.

