10 IIB группа.ppt
- Количество слайдов: 50

II группа периодической системы IIB-группа

Особенности 2 • Характеризуются полностью укомплектованными (n-1)d 10 слоями. Поэтому d-электроны здесь в принципе не являются валентными, возможности к взаимодействию обусловлены ns 2 электронами. Типичная ст. ок. +2. • Наличие заполненного d-подуровня усиливает ковалентный характер связи при движении вниз по группе. Особенно это характерно для Нg, ее галогениды – типичные ковалентные соединения. При движении вниз по группе возрастают атомные и ионные радиусы, особенно значительно при переходе от Zn к Сd

Особенности • По химическим свойствам Cd ближе к Zn – высокая химическая активность, степень окисления +2 • Hg – химически инертна, эффект «инертной» 6 s 2 -электронной пары; ион Hg 2+ – сильный окислитель. Для нее типично образование линейных биядерных (Hg 22+) кластеров, в которых ковалентные связи Hg–Hg формируются при участии spгибридных орбиталей атомов ртути 3

Особенности • Ковалентность связи в соединениях с неметаллами возрастает в ряду Zn 2+ Cd 2+ Hg 2+ по мере понижения энергии и увеличения размера валентных d-орбиталей • В водных растворах для Zn и Cd характерны к. ч. 4 и 6, для Cd – больше 6. Для Hg – к. ч. 4, иногда даже 2 и 3 4

Нахождение в природе • Высокое сродство к S, преимущественно в виде сульфидов • Zn – 7, 6 10– 3 масс. %, Cd – на 3 порядка ниже, чем Zn, но в 2 раза превышает содержание Hg. Hg – 8, 0 10– 6 масс. % Cd 5 48

Получение 700 3 O 2 °C • • 2 Zn. S + 2 Zn. O + 2 SO 2 затем обработка серной кислотой, Zn выделяют электролизом Также: 1000 Zn. O + C°C Zn + CO Так кадмий – редкий и рассеянный элемент, источник – цинковые руды Hg – образует минералы: киноварь Hg. S 600 + O 2 °C t °C Hg + SO 2 4 Hg. S + 4 Ca. O 4 Hg + Ca. SO 4 + Ca. S t °C Hg. S + Fe Fe. S + Hg 6

Физические свойства • Zn и Cd – ГЦК-структура. Полностью заполненные d-орбитали не способны вносить ковалентный вклад в металлическую связь, поэтому она обеспечивается только внешними электронами и ослаблена. Следовательно, небольшая энергия кристаллической решетки, низкая температура плавления (понижается вниз по группе) 7

Физические свойства • Необычайно низкая температура плавления Hg объясняется наличием 6 s 2 инертной электронной пары и ее неспособностью участвовать в формировании металлической связи. Следовательно, исключительно высокое сопротивление среди металлов 8

Физические свойства • Hg кристаллизуется при – 39 С, образуя ромбоэдрические кристаллы, при – 194 С образуется тетрагональная модификация с ОЦК-структурой 9

Химические свойства • В ряду напряжения Zn и Сd стоят до водорода, ртуть – после, соответственно активность металлов убывает вниз по группе • Zn на воздухе покрывается тонким слоем Zn. O, Cd и Hg – устойчивы, в реакцию с О 2 с образованием Me. O они вступают при 350 С • При повышенной температуре Zn и Cd реагируют с Hal, S, P. Hg образует Hg. Hal 2 и Hg. S уже при комнатной температуре, с P – не взаимодействует 10

Химические свойства • Металлы IIВ группы напрямую не реагируют с H 2, гидриды – косвенным путем: Li. H + Zn. Br 2 = Zn. H 2 + 2 Li. Br Cd. I 2 + 2 Li. Al. H 4 = Cd. H 2 + 2 Al. H 3 + 2 Li. H • Zn образует также комплексные гидриды: Li. Zn. H 3, Li 2 Zn. H 4, Li 3 Zn. H 5 • Cd. H 2 и Hg. H 2 чрезвычайно неустойчивы • Взаимодействие с кислотами – неокислителями: Cd + H 2 SO 4(20%) = Cd. SO 4 + H 2 11

Химические свойства • При температуре красного каления: 800 H 2 O°C Zn + Zn. O + H 2 • С кислотами – окислителями состав продуктов определяется концентрацией раствора 12

Химические свойства • Нg стоит в ряду напряжений правее водорода и не восстанавливает H+. С серной кислотой реагирует при нагревании: 800 2 H 2 SO 4(конц) °C Hg + Hg. SO 4 + SO 2 + 2 H 2 O Hg + 4 HNO 3(конц) = Hg(NO 3)2 + 2 NO 2 + H 2 O 6 Hg(губ) + 8 HNO 3(30%) = 3 Hg 2(NO 3)2 + 2 NO + 4 H 2 O Hg + HCl + HNO 3 Hg. Cl 2 сулема 13

Химические свойства • С растворами щелочей – только Zn: Zn + 2 Na. OH + 2 H 2 O = Na 2[Zn(OH)4] + H 2 • В щелочной среде Zn – очень сильный восстановитель: 4 Zn + Na. NO 3 + 7 Na. OH + 6 H 2 O = 4 Na 2[Zn(OH)4] + NH 3 • В растворах аммиака: Zn + 4 NH 3 H 2 O = [Zn(NH 3)4](OH)2 + H 2 + 2 H 2 O 14

Оксиды, пероксиды и гидроксиды

Оксиды • Оксиды известны лишь состава Me. O. Zn. O образуется при прокаливании Zn на воздухе и при термическом разложении его солей. При нагревании желтеет – образование нестехиометрической фазы Zn. O 1 -x • При прокаливании Cd. O также окраска становится более интенсивной. • Zn. O – решетка типа вюрцита, Cd. O – типа Na. Cl, Hg. O – зигзагообразные цепи Hg–O··· 16

Получение оксидов 300 Zn. CO 3 °C 180 Cd(OH)2 °C Zn. O + CO 2 Cd. O + H 2 O 2 Hg + O 2 = 2 Hg. O Hg. Cl 2 + 2 Na. OH = Hg. O↓ + 2 Na. Cl + H 2 O • Hg. O термически неустойчив, разлагается выше 400 ºС 17
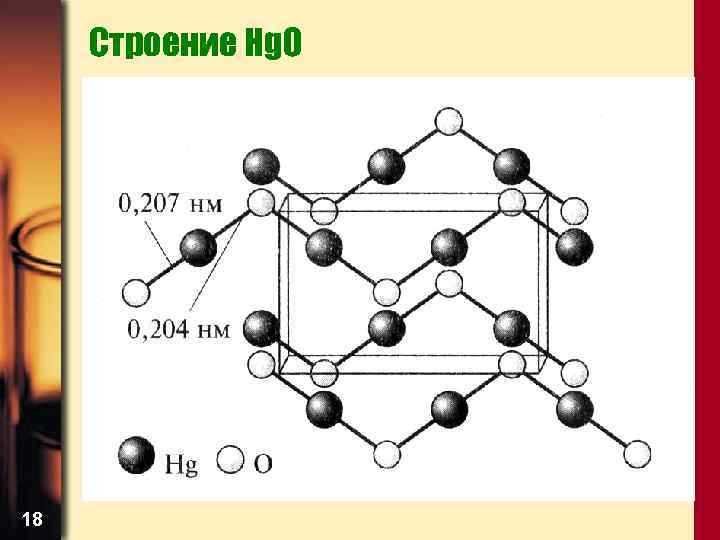
Строение Hg. O 18

Оксиды • Hg. O – красная и желтая модификации, они отличаются лишь размером частиц, известна еще красная ромбоэдрическая форма • Оксиды Zn, Cd, Hg практически нерастворимы в H 2 O и не взаимодействуют с ней, реагируют с кислотами: Hg. O + 2 HCl = Hg. Cl 2 + H 2 O 19
![Оксиды • Zn. O амфотерен, легко растворяется в растворах щелочей: [Zn(OH)3]– и [Zn(OH)4]2 – Оксиды • Zn. O амфотерен, легко растворяется в растворах щелочей: [Zn(OH)3]– и [Zn(OH)4]2 –](https://present5.com/presentation/3/14884915_68582546.pdf-img/14884915_68582546.pdf-20.jpg)
Оксиды • Zn. O амфотерен, легко растворяется в растворах щелочей: [Zn(OH)3]– и [Zn(OH)4]2 – • Оксид Сd – гидроксокомплексы лишь в очень крепких щелочных растворах [Cd(OH)4]2– • Hg. O c растворами щелочей не взаимодействует • Таким образом, основные свойства усиливаются вниз по группе 20

Пероксиды • Меркураты Me 2 IHg. O 2 получают нагреванием Hg. O с пероксидами и надпероксидами щелочных металлов. Цинкаты и кадматы – сплавлением оксидов и карбонатов: Na 2 Me. O 2, Na 2 Me 2 O 3, Na 6 Me. O 4 • Пероксиды образуются при действии H 2 O 2 на соли металлов IIВ группы, при нагревании или при ударе разлагаются со взрывом • Состав Me. O 2 21

Оксиды • Окислительные свойства оксидов усиливаются вниз по группе: Hg. O выше 400 ºС разлагается даже без участия восстановителя • В кислородных соединениях Zn и Cd проявляют степень окисления +2, для ртути известны катионы Hg 22+, Hg 32+, Hg 42+, входящие в состав солей 22
![Гидроксиды • В водных растворах солей Zn и Сd преобладают [M(H 2 O)6]2+. Слабокислая Гидроксиды • В водных растворах солей Zn и Сd преобладают [M(H 2 O)6]2+. Слабокислая](https://present5.com/presentation/3/14884915_68582546.pdf-img/14884915_68582546.pdf-23.jpg)
Гидроксиды • В водных растворах солей Zn и Сd преобладают [M(H 2 O)6]2+. Слабокислая среда возникает вследствие гидролиза: [M(H 2 O)6]2+ [M(H 2 O)5(OH)]+ + H+ Me. SO 4 + 2 Na. OH = Me(OH)2↓ + Na 2 SO 4 (Me = Zn, Cd) • Процесс проходит через стадию образования основных солей. В избытке щелочи: Zn(OH)2 + Na. OH + H 2 O = Na[Zn(OH)3(H 2 O)] • Cd(OH)2 – лишь в очень концентрированных растворах 23
![Гидроксиды • Соединения ртути в водных растворах сильно гидролизованы: [Hg(H 2 O)6]2+ [Hg(H 2 Гидроксиды • Соединения ртути в водных растворах сильно гидролизованы: [Hg(H 2 O)6]2+ [Hg(H 2](https://present5.com/presentation/3/14884915_68582546.pdf-img/14884915_68582546.pdf-24.jpg)
Гидроксиды • Соединения ртути в водных растворах сильно гидролизованы: [Hg(H 2 O)6]2+ [Hg(H 2 O)5(OH)]+ + H+ • Гидроксид ртути (II) не известен, гидролиз солей сопровождается образованием полиядерных гидроксо- и оксикатионов: [Hg 2(OH)(H 2 O)2]3+, [Hg 3 O(H 2 O)3]4+, [Hg 4 O(OH)(H 2 O)3]5+. Конечный продукт гидролиза – Hg. O 24

Гидроксиды • Ст. ок. +1 для Hg представлена соединениями, содержащими кластерные группировки, наиболее стабильны биядерные Hg 22+. Их образование обусловлено высокой устойчивостью 6 s 2 e-пары и стремлением атома Hg сохранить эту пару хотя бы в виде ковалентной связи, принадлежащей одновременно обоим атомам: Hg 22+ + 2 OH– = Hg↓ + Hg. O↓ + H 2 O • Ион диртути (I) в форме аквакомплекса [H 2 O–Hg–Hg–OH 2]2+ только при стандартных условиях устойчив к диспропорционированию 25

Соли и комплексы

Соединения Hg(I) • Соли Hg(I) устойчивы лишь с анионами кислородсодержащих кислот, хлоридам и бромидам • Hg 2(NO 3)2(H 2 O)2 кристаллизуется из растворов, полученных взаимодействием избытка Hg с разбавленной HNO 3 – на холоду, медленно. При высокой температуре разлагается на Hg. O, NO 2 и H 2 O Hg(NO 3)2 + 4 HNO 3(конц) = 2 Hg(NO 3)2 + 2 NO 2↑ + 2 H 2 O • Существуют также Hg 2 CO 3 (Hg 2(NO 3)2 + Na 2 CO 3) и Hg 2 Cr. O 4 (Na 2 Cr. O 4 + Hg 2(NO 3)2) 27

Соединения Hg(I) • Комплексы Hg(I) получены лишь с азотдонорными лигандами типа пиридина • Существуют соединения ртути с катионами Hgn 2+ c дробными степенями окисления: 3 Hg + 3 As. F 5 = Hg 3(As. F 6)2 + As. F 3 4 Hg + 3 As. F 5 = Hg 4(As. F 6)2 + As. F 3 28
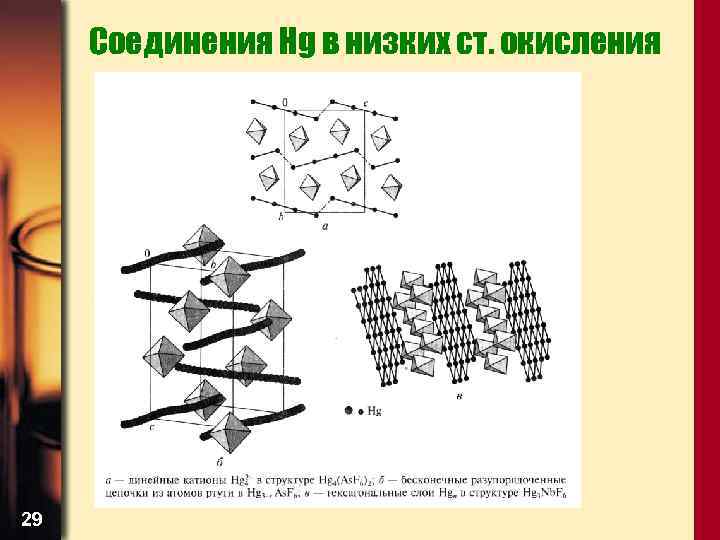
Соединения Hg в низких ст. окисления 29

Степень окисления +1 • Для Zn и Сd эта степень окисления не характерна, однако есть сведения, например, о Cd 2(Al. Cl 4)2 30

Степень окисления +2 • Соединения в степени окисления +2 характерны для всех элементов IIB группы. Эта степень окисления соответствует конфигурации d 10 • Соли Zn и Cd c анионами кислородсодержащих кислот, как правило, изоморфны солям Mg, но менее устойчивы. • Малорастворимы сульфиды, фосфаты, карбонаты, оксалаты, силикаты и сульфиты. Безводные карбонаты, сульфаты, нитраты термически разлагаются до оксидов 31

Степень окисления +2 • Zn. SO 4· 7 H 2 O – цинковый купорос, выделяется из растворов, полученных взаимодействием Zn + SO 4 • Сплавление: 500 Zn. O + Na 2 S 2 O 7°C Na 2[Zn(SO 4)2] • При растворении карбонатов или гидроксидов в HNO 3 – Zn(NO 3)2· 6 H 2 O; Cd(NO 3)2· 4 H 2 O 32

Степень окисления +2 • Соединения Zn(II) в гораздо большей степени ковалентны, чем Cd(II) из-за меньшего ионного радиуса Zn 2+ при одном и том же типе оболочки. Поэтому комплексные соединения Zn более устойчивы, чем Cd Zn(OH)2 + 4 NH 3 = [Zn(NH 3)4](OH)2 Ку = 5, 6· 1012 Сd(OH)2 + 6 NH 3 = [Cd(NH 3)6](OH)2 Ку = 3, 6· 104 • При кипячении и разбавлении водой разрушается лишь кадмиевый комплекс и выпадает Cd(OH)2 33

Степень окисления +2 • Zn и Cd, подобно Mg, образуют двойные соли типа шёнитов: Me 2 ISO 4·Zn. SO 4· 6 H 2 O • Соли Hg(II) в водных растворах сильно гидролизованы: [Hg(H 2 O)6]2+ [Hg(H 2 O)5(OH)]+ + H+ • Гидролиз сопровождается образованием полиядерных гидроксо- и оксокатионов 34

Соединения ртути (II) • Известны соли ртути (II) с сильными кислородсодержащими кислотами, например, Hg(NO 3)2·H 2 O получается растворением Hg в избытке концентрированной HNO 3 • Аналогично получают Hg. SO 4 • Соли слабых кислот – Н 2 СО 3, Н 2 Si. О 3, Н 2 SО 3 – малоустойчивы или неизвестны. Более, чем сульфит, устойчива комплексная соль Na 2[Hg(SO 3)2] • Известны фосфаты: Hg(PO 4)2, Hg. HPO 4, Hg 2 P 2 O 7 35

Соединения ртути (II) • Соединения Hg(II) проявляют окислительные свойства: Hg. SO 4 + 2 Fe. SO 4 = Fe 2(SO 4)3 + Hg↓ Hg(NO 3)2 + Cu = Cu(NO 3)2 + Hg↓ Hg(NO 3)2 + Hg = Hg 2(NO 3)2 36
![Комплексообразование NH 4+ Hg. Cl 2 + 2 NH 3 [Hg(NH 3)2]Cl 2↓ • Комплексообразование NH 4+ Hg. Cl 2 + 2 NH 3 [Hg(NH 3)2]Cl 2↓ •](https://present5.com/presentation/3/14884915_68582546.pdf-img/14884915_68582546.pdf-37.jpg)
Комплексообразование NH 4+ Hg. Cl 2 + 2 NH 3 [Hg(NH 3)2]Cl 2↓ • В отсутствие ионов NH 4+: Hg. Cl 2 + 2 NH 3 → [Hg. NH 2]Cl↓ + NH 4 Cl Hg. Cl 2 + NH 3 + Hg. O → [Hg. NH]Cl 2↓+ H 2 O Hg 2+ + C 6 H 6 ↔ [Hg. C 6 H 6]2+ • Вообще имеется большое число ртутьорганических соединений 37

Галогениды и галогенидные комплексы • Для всех 3 -х металлов известен полный набор дигалогенидов, низшие – только для Hg • При переходе от Zn к Cd степень ионности связи Me–Hal возрастает, что приводит к росту Тпл и Ткип, увеличению устойчивости к гидролизу • Галогениды Hg все, за исключением фторида, ковалентны (инертность 6 s 2 пары, эффективное перекрывание 5 dорбиталей Hg с валентными МО лигандов) 38

Галогениды и галогенидные комплексы 39 • Ковалентность связи Me–Hal возрастает также с ростом атомного номера Hal по мере уменьшения его электроотрицательности и в этом же ряду – усиление -взаимодействия металллиганд – что приводит к резкому возрастанию устойчивости галогенидных комплексов при переходе от фторидов к иодидам • Хлориды, бромиды и иодиды Zn и Cd очень хорошо растворимы в H 2 O, безводные – гигроскопичны, кристаллизуются из водных растворов в виде кристаллогидратов
![Галогениды и галогенидные комплексы • В разбавленных растворах наряду с [Zn(H 2 O)6]2+ присутствуют Галогениды и галогенидные комплексы • В разбавленных растворах наряду с [Zn(H 2 O)6]2+ присутствуют](https://present5.com/presentation/3/14884915_68582546.pdf-img/14884915_68582546.pdf-40.jpg)
Галогениды и галогенидные комплексы • В разбавленных растворах наряду с [Zn(H 2 O)6]2+ присутствуют [Zn. Cl 4]2–, [Zn. Cl 3(H 2 O)]–, [Zn. Cl 2(H 2 O)4]. Для кадмия известны и Cd 2 OCl 2, Cd(OH)Cl, Cd(OH)3 Cl. Образует и автокомплекс: 2 Cd. I 2 + 6 H 2 O [Cd(H 2 O)6]2+ + [Cd. I 4]2– • Галогениды Zn и Cd легко образуют комплексы, к. ч. в основном 4: K[Zn. Cl 3(H 2 O)], K 2[Zn. Cl 4], но бывает и 6: K 4[Cd. Cl 6] t °C Hg. SO 4 + 2 Na. Cl Hg. Cl 2 + Na 2 SO 4 (в присутствии Mn. O 2) 40 сулема, бесцветный

Галогениды и галогенидные комплексы • Бромид и иодид ртути слабо диссоциированы в водных растворах: Hg. I 2 + 2 I– = [Hg. I 4]2– – устойчив, не разрушается при добавлении щелочи • Для некоторых солей переходных металлов характерен полиморфизм, сопровождающийся изменением окраски 41
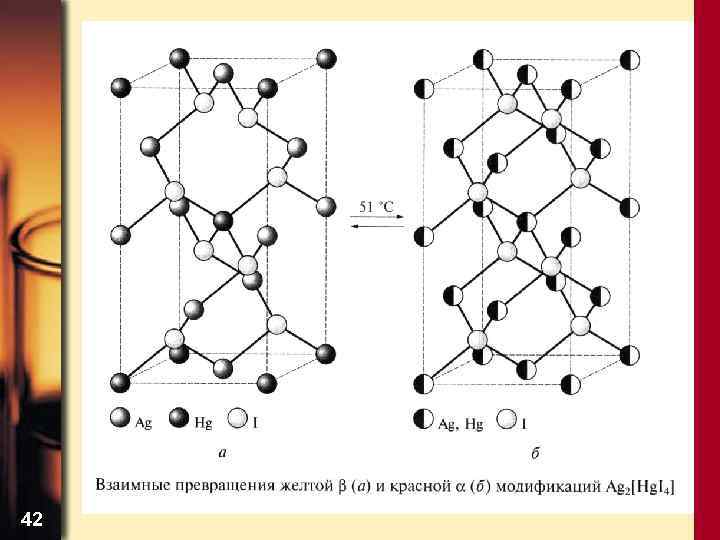
42

Галогениды и галогенидные комплексы • В твердых галогенидах (кроме фторидов) содержатся тетраэдры [Hg. X 4], во фторидах – октаэдры [Hg. F 6] Hg 2 X 2 Hg. X 2 + Hg • Склонность к диспропорционированию возрастает вниз по группе • Иодид при комнатной температуре: Hg 2 I 2 + 2 KI = K 2[Hg. I 4] + Hg 43

Галогениды и галогенидные комплексы • Все галогениды имеют молекулярное строение и состоят из линейных молекул Hg. X 2 со связью Hg–Hg. каломель, белый Hg. Cl 2 + Hg = Hg 2 Cl 2 t °C Hg 2 Cl 2 + KCl K[Hg. Cl 3] + Hg • Каломель легко окисляется: Hg 2 Cl 2 + Cl 2 = 2 Hg. Cl 2 • и восстанавливается: Hg 2 Cl 2 + Sn. Cl 2 + 2 HCl = Hg + H 2[Sn. Cl 6] • При действии аммиака чернеет: Hg 2 Cl 2 + 2 NH 3 = [Hg. NH 2]Cl + Hg + NH 4 Cl 44

Сульфиды • Известны лишь Me. S, все они нерастворимы в H 2 O, поэтому осаждаются из водных растворов сероводородом или сульфидами, могут быть получены прямым синтезом из простых веществ • Устойчивость к действию кислот возрастает вниз по группе: Zn. S легко реагирует с разбавленными кислотами, Cd. S – в концентрированной HCl, а Hg. S – в царской водке 45

Сульфиды • Zn. S(крист): t, P 3 Zn. O + 4 S + NH 3 + H 2 O 3 Zn. S + (NH 4)2 SO 4 • Cd. S: t 2 Cd. O + 3 S °C 2 Cd. S + SO 2 • Это кристаллический, аморфный – из водных растворов • При осаждении сероводородом: 3 Hg. Cl 2 + 2 H 2 S = Hg 3 S 2 Cl 2 + 4 HCl Hg 3 S 2 Cl 2 + H 2 S = 3 Hg. S + 2 HCl метакиноварь черный 46

Сульфиды • После обработки полисульфидами щелочных металлов или возгонки – красная модификация Hg. S, киноварь. Она необычайно инертна к кислотам и щелочам, растворяется лишь в царской водке • Черная модификация – структурный тип сфалерита, каркас из тетраэдров [Hg. S 4], соединенных вершинами 47

Киноварь 48

Сульфиды • Киноварь построена из спиралевидных цепей –Hg–S– , в которых атомы серы из соседних цепей дополняют координацию атомов Hg до искаженной октаэдрической • Сульфиды Zn, Cd, Hg при сплавлении с сульфидами щелочных металлов образуют тиосоли 49
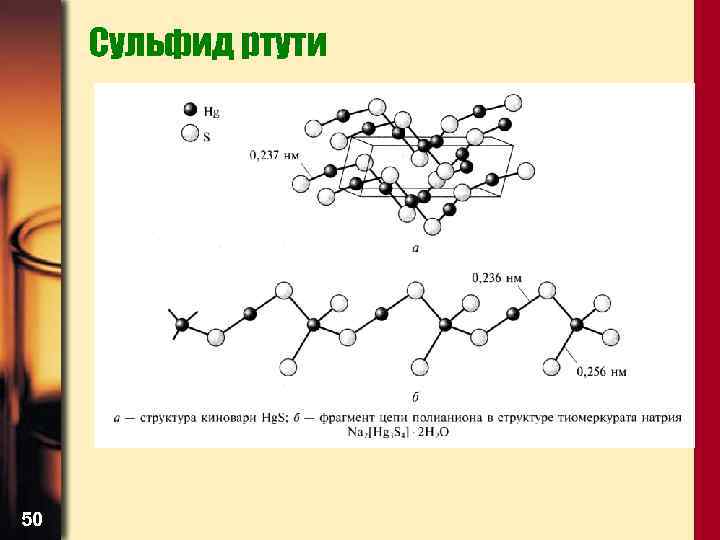
Сульфид ртути 50
10 IIB группа.ppt