 И ОН МА К Е ЗА СТ ВА Й СИ ЕЕ КИ Я ЕЛ ЕС КА НД ИЧ ЧЕС Е ОД ДИ В М И О Р ТО Е И Н П ЕР Е П ЕМ Я 3 Л КЦИ ЭЕ Л
И ОН МА К Е ЗА СТ ВА Й СИ ЕЕ КИ Я ЕЛ ЕС КА НД ИЧ ЧЕС Е ОД ДИ В М И О Р ТО Е И Н П ЕР Е П ЕМ Я 3 Л КЦИ ЭЕ Л
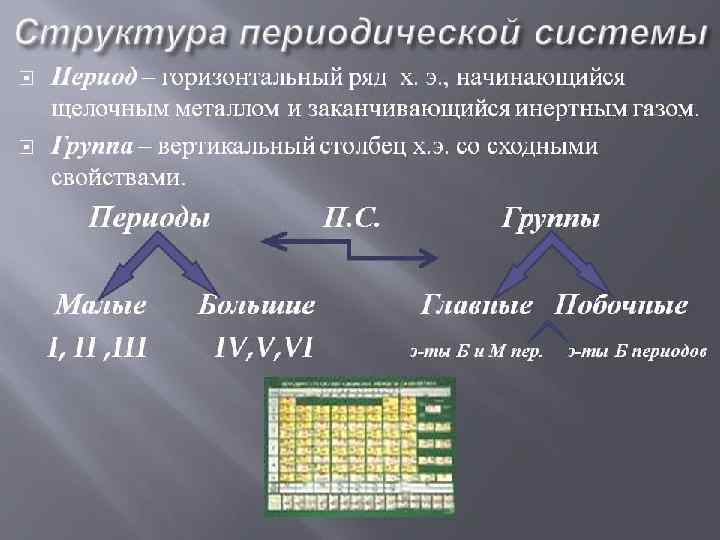
 ПЕРИОДИЧЕСКИЙ ЗАКОН Химический элемент – вид атомов с определенным зарядом ядра. ПЕРИОДИЧЕСКИЙ ЗАКОН: Свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от зарядов атомных ядер. Это связано с повторением электронной конфигурации внешнего электронного слоя в элементах периода, а также с увеличением числа электронных слоев в каждым новым периодом. Номер периода = число энергетических уровней Номер группы = число электронов на внешнем энергетическом уровне 2
ПЕРИОДИЧЕСКИЙ ЗАКОН Химический элемент – вид атомов с определенным зарядом ядра. ПЕРИОДИЧЕСКИЙ ЗАКОН: Свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от зарядов атомных ядер. Это связано с повторением электронной конфигурации внешнего электронного слоя в элементах периода, а также с увеличением числа электронных слоев в каждым новым периодом. Номер периода = число энергетических уровней Номер группы = число электронов на внешнем энергетическом уровне 2
 3
3
 4
4
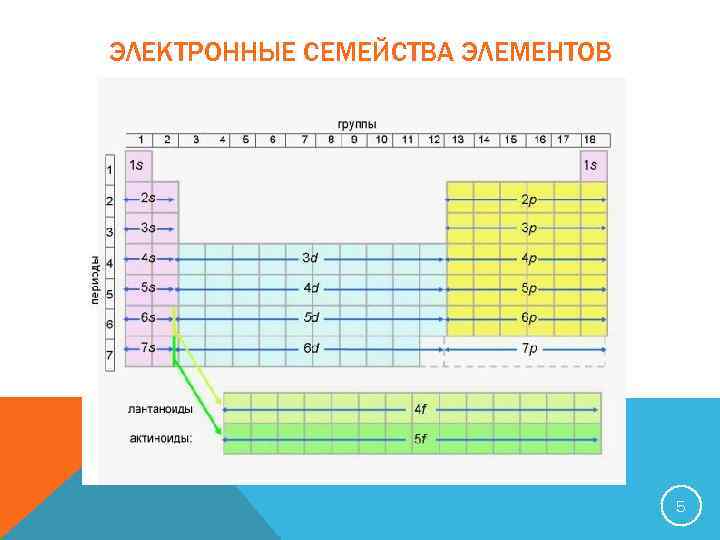 ЭЛЕКТРОННЫЕ СЕМЕЙСТВА ЭЛЕМЕНТОВ 5
ЭЛЕКТРОННЫЕ СЕМЕЙСТВА ЭЛЕМЕНТОВ 5
 МЕТАЛЛЫ И НЕМЕТАЛЛЫ 6
МЕТАЛЛЫ И НЕМЕТАЛЛЫ 6
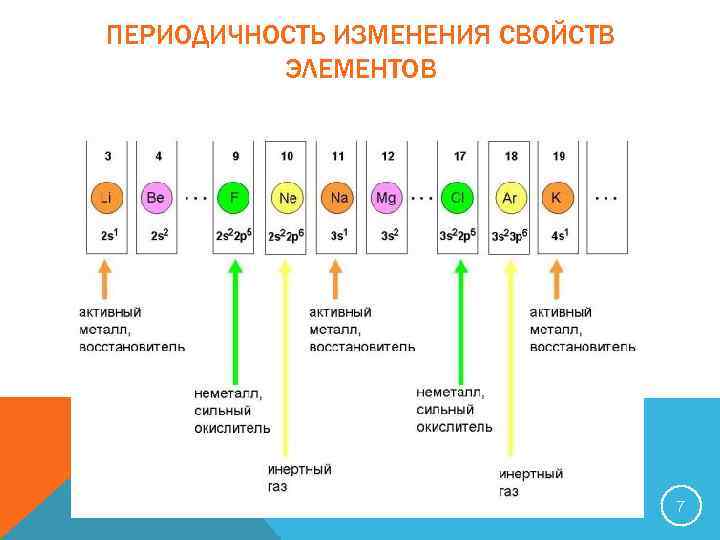 ПЕРИОДИЧНОСТЬ ИЗМЕНЕНИЯ СВОЙСТВ ЭЛЕМЕНТОВ 7
ПЕРИОДИЧНОСТЬ ИЗМЕНЕНИЯ СВОЙСТВ ЭЛЕМЕНТОВ 7
 ИЗМЕНЕНИЕ РАДИУСОВ АТОМОВ 8
ИЗМЕНЕНИЕ РАДИУСОВ АТОМОВ 8
 9
9
 10
10
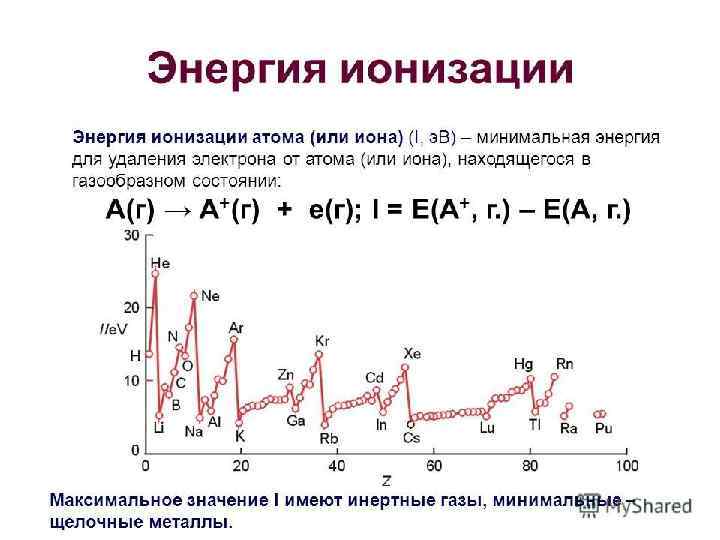 11
11
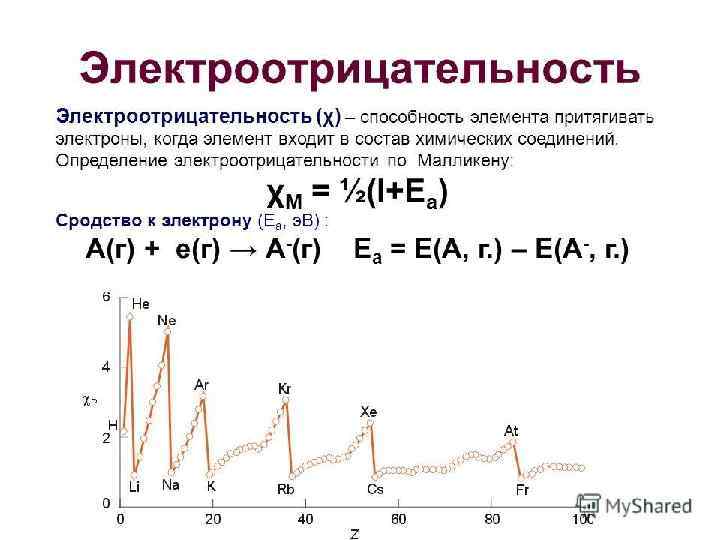 12
12
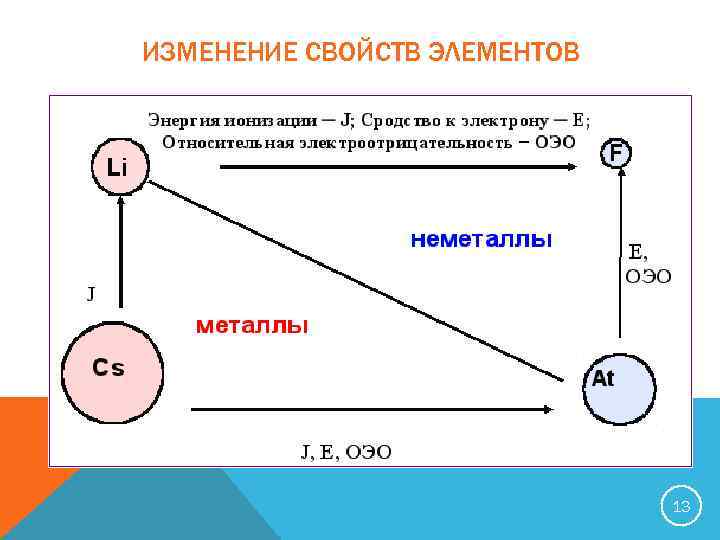 ИЗМЕНЕНИЕ СВОЙСТВ ЭЛЕМЕНТОВ 13
ИЗМЕНЕНИЕ СВОЙСТВ ЭЛЕМЕНТОВ 13
 ИЗМЕНЕНИЕ СВОЙСТВ ЭЛЕМЕНТОВ 14
ИЗМЕНЕНИЕ СВОЙСТВ ЭЛЕМЕНТОВ 14
 ИЗМЕНЕНИЕ СВОЙСТВ ЭЛЕМЕНТОВ 15
ИЗМЕНЕНИЕ СВОЙСТВ ЭЛЕМЕНТОВ 15
 ДИАГОНАЛЬНАЯ ПЕРИОДИЧНОСТЬ 16
ДИАГОНАЛЬНАЯ ПЕРИОДИЧНОСТЬ 16
 СВОЙСТВА ОКСИДОВ ЭЛЕМЕНТОВ 17
СВОЙСТВА ОКСИДОВ ЭЛЕМЕНТОВ 17
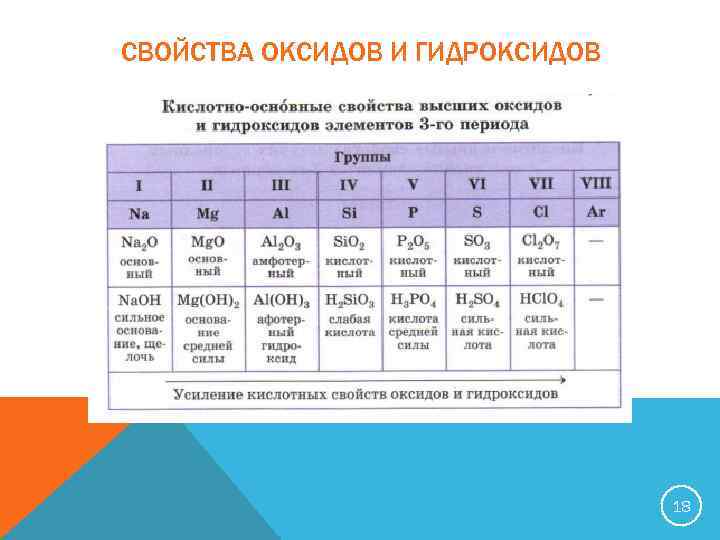 СВОЙСТВА ОКСИДОВ И ГИДРОКСИДОВ 18
СВОЙСТВА ОКСИДОВ И ГИДРОКСИДОВ 18
 19
19
 ЛЕТУЧИЕ ВОДОРОДНЫЕ СОЕДИЕНИЯ 20
ЛЕТУЧИЕ ВОДОРОДНЫЕ СОЕДИЕНИЯ 20
 ЛЕТУЧИЕ ВОДОРОДНЫЕ СОЕДИЕНИЯ 21
ЛЕТУЧИЕ ВОДОРОДНЫЕ СОЕДИЕНИЯ 21
 ПОДВЕДЕМ ИТОГИ Слева направо и снизу вверх увеличиваются: F o Число валентных электронов (и высшая валентность) o Энергия ионизации o Сродство к электрону o Электроотрицательность o Неметаллические свойства o Окислительная способность o Кислотные свойства оксидов o Кислотные свойства гидроксидов 22
ПОДВЕДЕМ ИТОГИ Слева направо и снизу вверх увеличиваются: F o Число валентных электронов (и высшая валентность) o Энергия ионизации o Сродство к электрону o Электроотрицательность o Неметаллические свойства o Окислительная способность o Кислотные свойства оксидов o Кислотные свойства гидроксидов 22
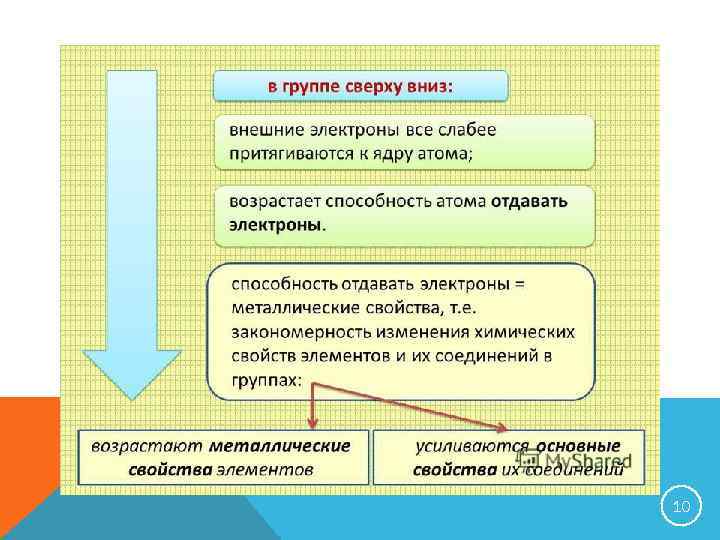
 ПОДВЕДЕМ ИТОГИ Справа налево и сверху вниз увеличиваются: o Радиус атома o Металлические свойства o Восстановительная способность o Основные свойства оксидов o Основные свойства гидроксидов Слева направо и сверху вниз увеличиваются: o Кислотные свойства летучих водородных соединений 23
ПОДВЕДЕМ ИТОГИ Справа налево и сверху вниз увеличиваются: o Радиус атома o Металлические свойства o Восстановительная способность o Основные свойства оксидов o Основные свойства гидроксидов Слева направо и сверху вниз увеличиваются: o Кислотные свойства летучих водородных соединений 23
 А! К ТИ К РЬ Е А РА П ЕП Т 24
А! К ТИ К РЬ Е А РА П ЕП Т 24