Лекция по химии от 13.09.ppt
- Количество слайдов: 101
 I и II начала термодинамики Основные понятия химической термодинамики
I и II начала термодинамики Основные понятия химической термодинамики
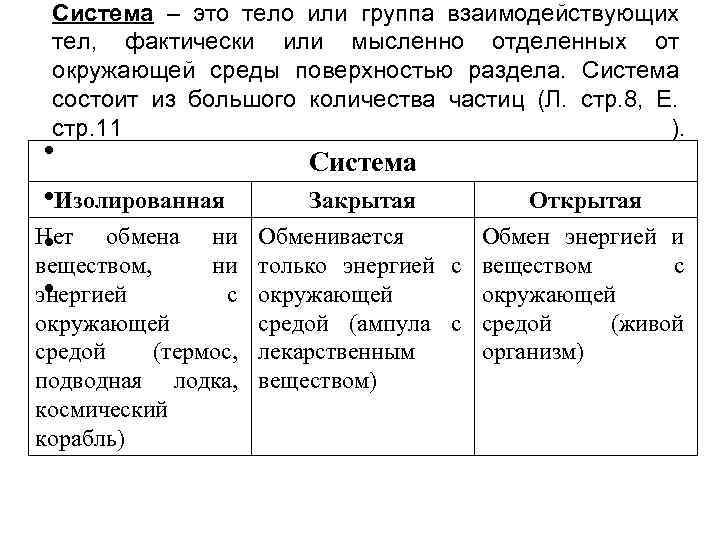 Система – это тело или группа взаимодействующих тел, фактически или мысленно отделенных от окружающей среды поверхностью раздела. Система состоит из большого количества частиц (Л. стр. 8, Е. стр. 11 ). • • Изолированная Нет обмена ни • веществом, ни • энергией с Система Закрытая Открытая Обменивается Обмен энергией и только энергией с веществом с окружающей средой (ампула с средой (живой средой (термос, лекарственным организм) подводная лодка, веществом) космический корабль)
Система – это тело или группа взаимодействующих тел, фактически или мысленно отделенных от окружающей среды поверхностью раздела. Система состоит из большого количества частиц (Л. стр. 8, Е. стр. 11 ). • • Изолированная Нет обмена ни • веществом, ни • энергией с Система Закрытая Открытая Обменивается Обмен энергией и только энергией с веществом с окружающей средой (ампула с средой (живой средой (термос, лекарственным организм) подводная лодка, веществом) космический корабль)
 Совокупность физических и химических величин, характеризующих состояние системы, называются параметрами. Параметры Экстенсивные Пропорциональны числу частиц в системе (масса, объем, энергия) Интенсивные Величина не зависит от числа частиц в системе (температура, давление, концентрация и т. д. )
Совокупность физических и химических величин, характеризующих состояние системы, называются параметрами. Параметры Экстенсивные Пропорциональны числу частиц в системе (масса, объем, энергия) Интенсивные Величина не зависит от числа частиц в системе (температура, давление, концентрация и т. д. )
 • Процесс – переход системы из одного состояния в другое, характеризуется изменением хотя бы одного параметра. • • В термодинамике принято изменение параметра ( ) рассчитывать как разность: • • = конечное значение параметра – начальное значение параметра
• Процесс – переход системы из одного состояния в другое, характеризуется изменением хотя бы одного параметра. • • В термодинамике принято изменение параметра ( ) рассчитывать как разность: • • = конечное значение параметра – начальное значение параметра
 • Функции состояния - свойства, величины которых при переходе системы из одного состояния в другое зависят только от начального и конечного состояния системы и не зависят от пути перехода (давление, объем, температура и т. д. ). • Материя содержит энергию в виде кинетической и потенциальной энергии ее частиц, сумма которых – внутренняя энергия - функция состояния, экстенсивный параметр: • U = Eпот + Екин, измеряется в Дж или к. Дж • U происходит в результате взаимодействия системы с окружающей средой в двух формах работы (А) и теплоты (Q). A и Q в общем случае не функции состояния.
• Функции состояния - свойства, величины которых при переходе системы из одного состояния в другое зависят только от начального и конечного состояния системы и не зависят от пути перехода (давление, объем, температура и т. д. ). • Материя содержит энергию в виде кинетической и потенциальной энергии ее частиц, сумма которых – внутренняя энергия - функция состояния, экстенсивный параметр: • U = Eпот + Екин, измеряется в Дж или к. Дж • U происходит в результате взаимодействия системы с окружающей средой в двух формах работы (А) и теплоты (Q). A и Q в общем случае не функции состояния.
 I закон (первое начало) термодинамики, закон сохранения и превращения энергии • Формулировки I начала для различного вида систем: 1. В изолированной системе внутренняя энергия постоянна, т. е. U=0 2. Если к закрытой системе подвести теплоту Q, то эта энергия расходуется на увеличение внутренней энергии системы и на совершение системой работы против внешних сил окружающей среды: Q = U + А или Q = d. U + A
I закон (первое начало) термодинамики, закон сохранения и превращения энергии • Формулировки I начала для различного вида систем: 1. В изолированной системе внутренняя энергия постоянна, т. е. U=0 2. Если к закрытой системе подвести теплоту Q, то эта энергия расходуется на увеличение внутренней энергии системы и на совершение системой работы против внешних сил окружающей среды: Q = U + А или Q = d. U + A
 • Для изобарно-изотермических условий А=р V, тогда: • Qр= U+р V = (Uкон-Uнач )+(р. Vкон -р. Vнач)= • = (Uкон +р. Vкон) - (Uнач+p. V нач), • но U и V – функции состояния, тогда новая функция состояния – энтальпия: • H U + p. V и Qp = Нкон - Ннач = Н
• Для изобарно-изотермических условий А=р V, тогда: • Qр= U+р V = (Uкон-Uнач )+(р. Vкон -р. Vнач)= • = (Uкон +р. Vкон) - (Uнач+p. V нач), • но U и V – функции состояния, тогда новая функция состояния – энтальпия: • H U + p. V и Qp = Нкон - Ннач = Н
 Измерение тепловых эффектов калориметрия • Н – экстенсивный параметр, зависит от количества вещества, Т, р, поэтому стандартные условия: • 1. Количество химически чистого вещества 1 моль. • 2. В растворе С=1 моль/л (1 моль/кг растворителя). • 3. р =1 атм или 101325 Па. • 4. Т = 298 К. • 5. Наиболее устойчивая форма вещества.
Измерение тепловых эффектов калориметрия • Н – экстенсивный параметр, зависит от количества вещества, Т, р, поэтому стандартные условия: • 1. Количество химически чистого вещества 1 моль. • 2. В растворе С=1 моль/л (1 моль/кг растворителя). • 3. р =1 атм или 101325 Па. • 4. Т = 298 К. • 5. Наиболее устойчивая форма вещества.
 Термохимические уравнения • С 2 Н 2(г) + 2, 5 О 2(г) = 2 СО 2(г) + Н 2 О(ж) • Н 0298 = -1256 к. Дж/моль • • Н 0 - эндотермические процессы Н 0 - экзотермические процессы • Стандартные энтальпии образования • Обозначение и размерность - Н 0298 (вещество, агрегатное состояние) Дж/моль
Термохимические уравнения • С 2 Н 2(г) + 2, 5 О 2(г) = 2 СО 2(г) + Н 2 О(ж) • Н 0298 = -1256 к. Дж/моль • • Н 0 - эндотермические процессы Н 0 - экзотермические процессы • Стандартные энтальпии образования • Обозначение и размерность - Н 0298 (вещество, агрегатное состояние) Дж/моль
 Для простых веществ Н 0298 приняты равными 0. • Н 0298 (О 2, газ ) = 0 , но • Н 0298 (О 3, газ ) = 142, 4 к. Дж/моль • • Н 0298(Сграфит) = 0, но • Н 0 298(Салмаз) = 1, 83 к. Дж/моль
Для простых веществ Н 0298 приняты равными 0. • Н 0298 (О 2, газ ) = 0 , но • Н 0298 (О 3, газ ) = 142, 4 к. Дж/моль • • Н 0298(Сграфит) = 0, но • Н 0 298(Салмаз) = 1, 83 к. Дж/моль
 Для сложного вещества Н 0298(С 2 Н 5 ОН, ж) = -277 к. Дж/моль это стандартная энтальпия реакции образования 1 моль вещества из простых веществ 2 С(графит)+ 3 Н 2(газ) + 0, 5 О 2(газ) = С 2 Н 5 ОН(ж) Величины Н 0298 - справочные данные
Для сложного вещества Н 0298(С 2 Н 5 ОН, ж) = -277 к. Дж/моль это стандартная энтальпия реакции образования 1 моль вещества из простых веществ 2 С(графит)+ 3 Н 2(газ) + 0, 5 О 2(газ) = С 2 Н 5 ОН(ж) Величины Н 0298 - справочные данные
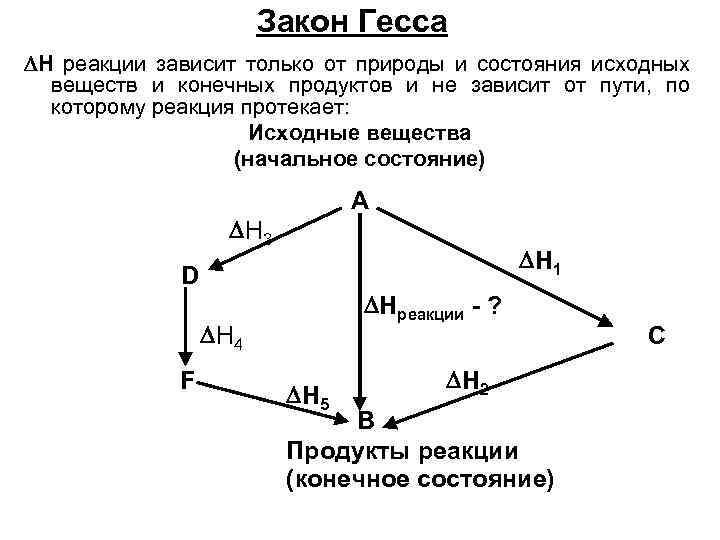 Закон Гесса Н реакции зависит только от природы и состояния исходных веществ и конечных продуктов и не зависит от пути, по которому реакция протекает: Исходные вещества (начальное состояние) А H 3 H 1 D H 4 F Hреакции - ? C H 5 H 2 В Продукты реакции (конечное состояние)
Закон Гесса Н реакции зависит только от природы и состояния исходных веществ и конечных продуктов и не зависит от пути, по которому реакция протекает: Исходные вещества (начальное состояние) А H 3 H 1 D H 4 F Hреакции - ? C H 5 H 2 В Продукты реакции (конечное состояние)
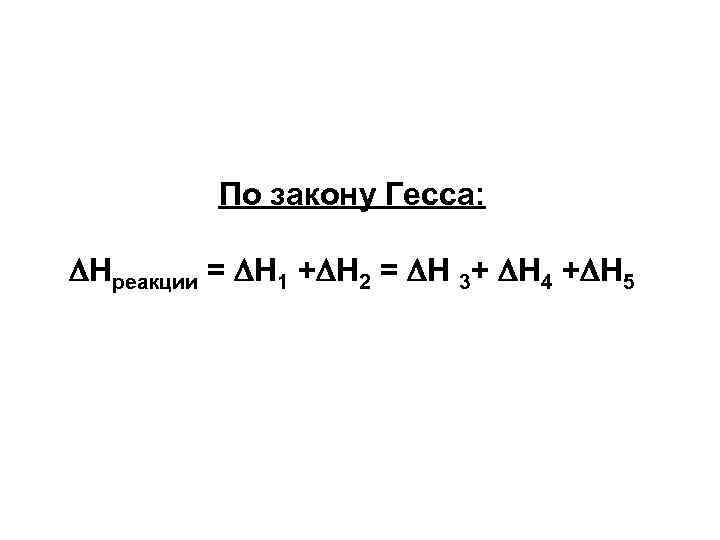 По закону Гесса: Нреакции = Н 1 + Н 2 = Н 3+ Н 4 + Н 5
По закону Гесса: Нреакции = Н 1 + Н 2 = Н 3+ Н 4 + Н 5
 I следствие • • • Hреакции = i Hпродукты - i Hисходные вещества Пример: • 2 NH 3(г) + СО 2(г) = СО(NH 2)2(тв) + Н 2 О(г) Н 0298 -45, 8 -393, 8 -333 242 к. Дж/моль Н 0298 реакции= (-333 - 242) - -(2 х45. 8)-393, 8 = • -89, 6 к. Дж/моль
I следствие • • • Hреакции = i Hпродукты - i Hисходные вещества Пример: • 2 NH 3(г) + СО 2(г) = СО(NH 2)2(тв) + Н 2 О(г) Н 0298 -45, 8 -393, 8 -333 242 к. Дж/моль Н 0298 реакции= (-333 - 242) - -(2 х45. 8)-393, 8 = • -89, 6 к. Дж/моль
 II следствие Hреакции = i Hсгорания исходных веществ - i Hсгорания продуктов Пример расчета теплового эффекта с использованием Н 0 сгорания: С 6 Н 6(ж) 3 С 2 Н 2(г), Hреакции - H 0 реакции = Н 0 сгорания(С 6 Н 6(ж)) - 3 Н 0 сгорания(С 2 Н 2(г)) = -3268 – (-3 х 1300) = 632 к. Дж /моль Н 0 сгорания соответствует сгоранию 1 моль вещества в атмосфере О 2 при 101. 3 к. Па с образованием высших оксидов (Л. стр. 20) Калорийность – энергия, выделяемая при полном окислении (сгорании) 1 г питательных веществ. 1 калория = 4, 18 Дж Жиры (9 -9, 5 ккал/г), белки, углеводы (4 -4, 1 ккал/г)
II следствие Hреакции = i Hсгорания исходных веществ - i Hсгорания продуктов Пример расчета теплового эффекта с использованием Н 0 сгорания: С 6 Н 6(ж) 3 С 2 Н 2(г), Hреакции - H 0 реакции = Н 0 сгорания(С 6 Н 6(ж)) - 3 Н 0 сгорания(С 2 Н 2(г)) = -3268 – (-3 х 1300) = 632 к. Дж /моль Н 0 сгорания соответствует сгоранию 1 моль вещества в атмосфере О 2 при 101. 3 к. Па с образованием высших оксидов (Л. стр. 20) Калорийность – энергия, выделяемая при полном окислении (сгорании) 1 г питательных веществ. 1 калория = 4, 18 Дж Жиры (9 -9, 5 ккал/г), белки, углеводы (4 -4, 1 ккал/г)
 II начало термодинамики
II начало термодинамики
 Статистическое толкование энтропии. • Энтропия – мера неупорядоченности расположения частиц в системе.
Статистическое толкование энтропии. • Энтропия – мера неупорядоченности расположения частиц в системе.
 • S(газ) S(ж) S(тв) • Пример качественной оценки S • Для реакции 2 NO(г) + O 2(г) = 2 NO 2(г) S 0 можно установить качественно, не производя вычислений. • Т 1 Т 2 S 1 S 2 • р1 р2 S 1 S 2 • S – экстенсивный параметр. Для сложной системы • S S 1 + S 2 + S 3
• S(газ) S(ж) S(тв) • Пример качественной оценки S • Для реакции 2 NO(г) + O 2(г) = 2 NO 2(г) S 0 можно установить качественно, не производя вычислений. • Т 1 Т 2 S 1 S 2 • р1 р2 S 1 S 2 • S – экстенсивный параметр. Для сложной системы • S S 1 + S 2 + S 3
 • • S 0(идеальный кристалл) = 0, поэтому S 2980(простое вещ-во) 0 (справочные данные). S 0298 реакции= i. S 0298 продукты- i. S 0298 исх. в-ва где I – стехиометрические коэффициенты в уравнении химической реакции.
• • S 0(идеальный кристалл) = 0, поэтому S 2980(простое вещ-во) 0 (справочные данные). S 0298 реакции= i. S 0298 продукты- i. S 0298 исх. в-ва где I – стехиометрические коэффициенты в уравнении химической реакции.
 Формулировки II начала термодинамики 1. В изолированной системе самопроизвольно совершаются только такие процессы, при которых S возрастает, т. е. S 0. 2. Для закрытых систем необходимо учитывать 2 фактора, определяющих направление самопроизвольно протекающих процессов. Энтальпийный – стремление системы к минимуму энергии за счет экзотермической реакции, энтропийный – к увеличению неупорядоченности в расположении частиц за счет теплового движения , поэтому новая функция состояния G H - TS, где G -энергия Гиббса.
Формулировки II начала термодинамики 1. В изолированной системе самопроизвольно совершаются только такие процессы, при которых S возрастает, т. е. S 0. 2. Для закрытых систем необходимо учитывать 2 фактора, определяющих направление самопроизвольно протекающих процессов. Энтальпийный – стремление системы к минимуму энергии за счет экзотермической реакции, энтропийный – к увеличению неупорядоченности в расположении частиц за счет теплового движения , поэтому новая функция состояния G H - TS, где G -энергия Гиббса.
 • Для изобарно-изотермических условий G – функция состояния, учитывающая энергетику и неупорядоченность системы. • G 0298 ре-ции= i G 0298 продукты- i G 0298 исх. в-ва • где G 0 веществ –справочные данные • или для нестандартных условий • G = H - T S
• Для изобарно-изотермических условий G – функция состояния, учитывающая энергетику и неупорядоченность системы. • G 0298 ре-ции= i G 0298 продукты- i G 0298 исх. в-ва • где G 0 веществ –справочные данные • или для нестандартных условий • G = H - T S
 В системе при постоянных р и Т самопроизвольно совершаются только такие процессы, в которых уменьшается энергия Гиббса, т. е. G 0 (экзэргонические). Эндэргонические процессы имеют G 0
В системе при постоянных р и Т самопроизвольно совершаются только такие процессы, в которых уменьшается энергия Гиббса, т. е. G 0 (экзэргонические). Эндэргонические процессы имеют G 0
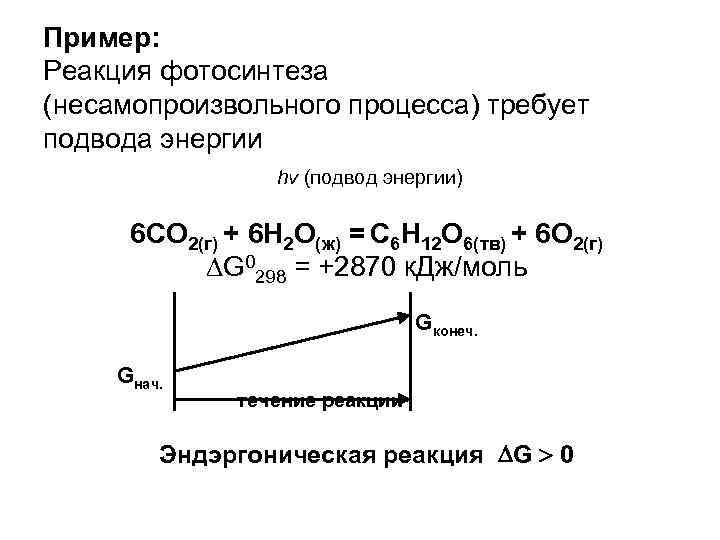 Пример: Реакция фотосинтеза (несамопроизвольного процесса) требует подвода энергии hv (подвод энергии) 6 СО 2(г) + 6 Н 2 О(ж) = C 6 Н 12 О 6(тв) + 6 О 2(г) G 0298 = +2870 к. Дж/моль Gнач. Gконеч. течение реакции Эндэргоническая реакция G 0
Пример: Реакция фотосинтеза (несамопроизвольного процесса) требует подвода энергии hv (подвод энергии) 6 СО 2(г) + 6 Н 2 О(ж) = C 6 Н 12 О 6(тв) + 6 О 2(г) G 0298 = +2870 к. Дж/моль Gнач. Gконеч. течение реакции Эндэргоническая реакция G 0
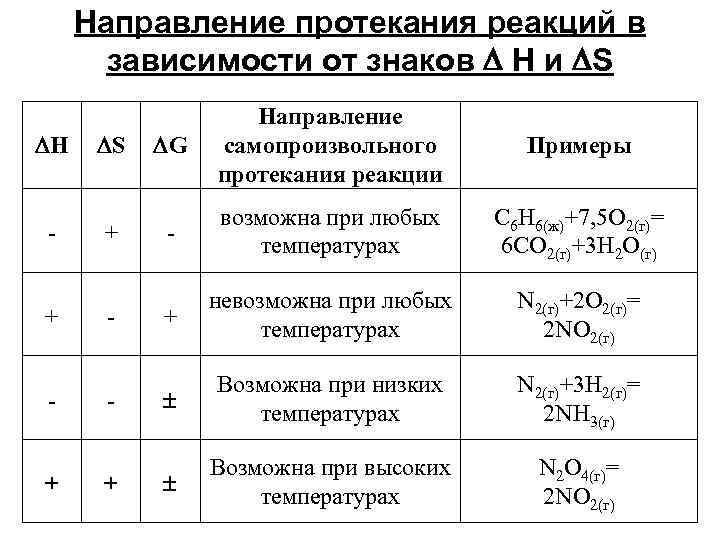 Направление протекания реакций в зависимости от знаков H и S H S G Направление самопроизвольного протекания реакции Примеры С 6 Н 6(ж)+7, 5 О 2(г)= 6 СО 2(г)+3 Н 2 О(г) - + - возможна при любых температурах + - + невозможна при любых температурах N 2(г)+2 O 2(г)= 2 NO 2(г) Возможна при низких температурах N 2(г)+3 Н 2(г)= 2 NН 3(г) Возможна при высоких температурах N 2 О 4(г)= 2 NO 2(г) + +
Направление протекания реакций в зависимости от знаков H и S H S G Направление самопроизвольного протекания реакции Примеры С 6 Н 6(ж)+7, 5 О 2(г)= 6 СО 2(г)+3 Н 2 О(г) - + - возможна при любых температурах + - + невозможна при любых температурах N 2(г)+2 O 2(г)= 2 NO 2(г) Возможна при низких температурах N 2(г)+3 Н 2(г)= 2 NН 3(г) Возможна при высоких температурах N 2 О 4(г)= 2 NO 2(г) + +
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 28
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 28
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 29
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 29
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 32
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 32
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 33
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 33
 Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 34
Х и м и ч е с к о е р а в н о в е с и е и б и о т е р м о д и н а м и к а 34
 Теория электролитической диссоциации (С. Аррениус, 1888– 1889) q Электролиты – вещества, при растворении подвергающиеся ионизации (диссоциации) и сообщающие раствору способность проводить электрический ток. 35
Теория электролитической диссоциации (С. Аррениус, 1888– 1889) q Электролиты – вещества, при растворении подвергающиеся ионизации (диссоциации) и сообщающие раствору способность проводить электрический ток. 35
 Электролиты Сильные (α > 0. 3 или 30%) Слабые (α < 0. 03 или 3%) 1. Кислоты: HCl; HBr; HI; HNO 3; H 2 SO 4; 2. Щелочи: Li. OH; Na. OH; KOH; Cs. OH; Ca(OH)2; Ba(OH)2; Sr(OH)2. 3. Соли 1. Кислоты: HF; HCN; H 2 SO 3; H 2 CO 3; H 2 Si. O 3; H 3 PO 4; CH 3 COOH; HCOOH; HNO 2. 2. Основания и амфотерные гидроксиды: NH 3; Fe(OH)2; Cu(OH)2; Zn(OH)2; Al(OH)3; Fe(OH)3. 1. 2. 3. 4. 1. HF H+ + F– 2. H 3 PO 4 H+ + H 2 PO 4– H+ + HPO 42– H+ + PO 43– 1 >> 2 >> 3 3. NH 3 + H 2 O NH 4+ + OH– HCl H+ + Cl– H 2 SO 4 2 H+ + SO 42– Ca(OH)2 Ca 2+ + 2 OH– Al 2(SO 4)3 2 Al 3+ + 3 SO 42– Диссоциируют необратимо, полностью 1 2 3 Диссоциируют обратимо, неполностью, ступенчато Неэлектролиты – этанол, глицерин, глюкоза, сахароза, фруктоза 36
Электролиты Сильные (α > 0. 3 или 30%) Слабые (α < 0. 03 или 3%) 1. Кислоты: HCl; HBr; HI; HNO 3; H 2 SO 4; 2. Щелочи: Li. OH; Na. OH; KOH; Cs. OH; Ca(OH)2; Ba(OH)2; Sr(OH)2. 3. Соли 1. Кислоты: HF; HCN; H 2 SO 3; H 2 CO 3; H 2 Si. O 3; H 3 PO 4; CH 3 COOH; HCOOH; HNO 2. 2. Основания и амфотерные гидроксиды: NH 3; Fe(OH)2; Cu(OH)2; Zn(OH)2; Al(OH)3; Fe(OH)3. 1. 2. 3. 4. 1. HF H+ + F– 2. H 3 PO 4 H+ + H 2 PO 4– H+ + HPO 42– H+ + PO 43– 1 >> 2 >> 3 3. NH 3 + H 2 O NH 4+ + OH– HCl H+ + Cl– H 2 SO 4 2 H+ + SO 42– Ca(OH)2 Ca 2+ + 2 OH– Al 2(SO 4)3 2 Al 3+ + 3 SO 42– Диссоциируют необратимо, полностью 1 2 3 Диссоциируют обратимо, неполностью, ступенчато Неэлектролиты – этанол, глицерин, глюкоза, сахароза, фруктоза 36
 Ионизация (диссоциация) воды a (acid); w (water) 37
Ионизация (диссоциация) воды a (acid); w (water) 37
![Водородный показатель Кислотность (С. Сёренсен, 1909) p. H =– lg[H+] p. H < 7 Водородный показатель Кислотность (С. Сёренсен, 1909) p. H =– lg[H+] p. H < 7](https://present5.com/presentation/3/10904782_219858417.pdf-img/10904782_219858417.pdf-38.jpg) Водородный показатель Кислотность (С. Сёренсен, 1909) p. H =– lg[H+] p. H < 7 – среда кислая, p. H = 7 – нейтральная, p. H > 7 – щелочная p. OH =– lgc(OH–) p. H + p. OH = 14; p. H = 14 – p. OH; p. OH = 14 – p. H 38
Водородный показатель Кислотность (С. Сёренсен, 1909) p. H =– lg[H+] p. H < 7 – среда кислая, p. H = 7 – нейтральная, p. H > 7 – щелочная p. OH =– lgc(OH–) p. H + p. OH = 14; p. H = 14 – p. OH; p. OH = 14 – p. H 38
 Расчет р. Н в растворах сильных электролитов 1. Сильные кислоты НХ (HCl, HNO 3) p. H = – lgc(H+) = – lgc(HX) (1. 3) 39
Расчет р. Н в растворах сильных электролитов 1. Сильные кислоты НХ (HCl, HNO 3) p. H = – lgc(H+) = – lgc(HX) (1. 3) 39
 Пример. Рассчитать р. Н в 0. 1 М растворе HCl. p. H = – lgc(H+) = – lgc(HCl) = – lg 10– 1 = 1. 0 Среда кислая 40
Пример. Рассчитать р. Н в 0. 1 М растворе HCl. p. H = – lgc(H+) = – lgc(HCl) = – lg 10– 1 = 1. 0 Среда кислая 40
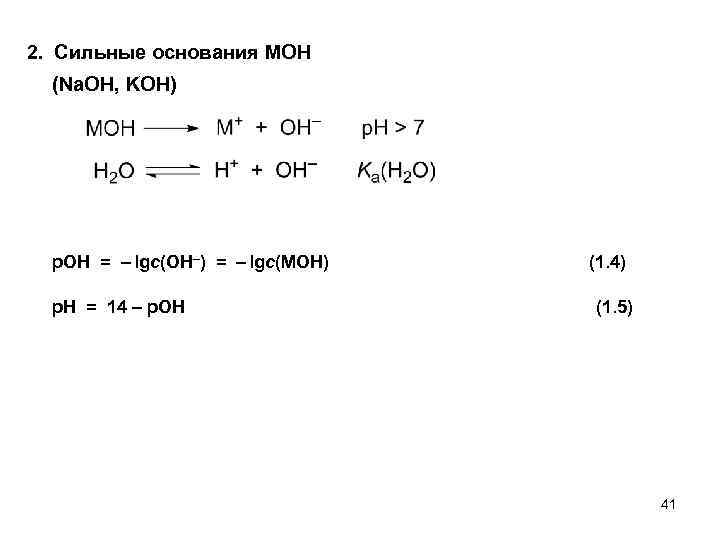 2. Сильные основания MOH (Na. OH, KOH) p. OH = – lgc(OH–) = – lgc(MOH) (1. 4) p. H = 14 – p. OH (1. 5) 41
2. Сильные основания MOH (Na. OH, KOH) p. OH = – lgc(OH–) = – lgc(MOH) (1. 4) p. H = 14 – p. OH (1. 5) 41
 Пример. Рассчитать р. Н в 0. 001 М растворе Na. OH p. OH = – lgc(OH–) = – lgc(MOH) = – lg 10– 3 = 3 p. H = 14 – 3 = 11 Среда щелочная 42
Пример. Рассчитать р. Н в 0. 001 М растворе Na. OH p. OH = – lgc(OH–) = – lgc(MOH) = – lg 10– 3 = 3 p. H = 14 – 3 = 11 Среда щелочная 42
 3. Растворы солей сильных кислот и сильных оснований MX (Na. Cl, KBr) p. H = 7 Среда нейтральная 43
3. Растворы солей сильных кислот и сильных оснований MX (Na. Cl, KBr) p. H = 7 Среда нейтральная 43
 Слабые электролиты (в растворе присутствуют и молекулы и ионы) q Степень диссоциации ( ) – доля молекул электролита, распавшихся на ионы (в долях единицы или в процентах). v Не может служить однозначной количественной характеристикой вещества — зависит от концентрации. Степень диссоциации слабого электролита возрастает с разбавлением раствора 44
Слабые электролиты (в растворе присутствуют и молекулы и ионы) q Степень диссоциации ( ) – доля молекул электролита, распавшихся на ионы (в долях единицы или в процентах). v Не может служить однозначной количественной характеристикой вещества — зависит от концентрации. Степень диссоциации слабого электролита возрастает с разбавлением раствора 44
 Константа диссоциации (КД) • На основании закона действующих масс (зависит только от природы вещества и температуры) 45
Константа диссоциации (КД) • На основании закона действующих масс (зависит только от природы вещества и температуры) 45
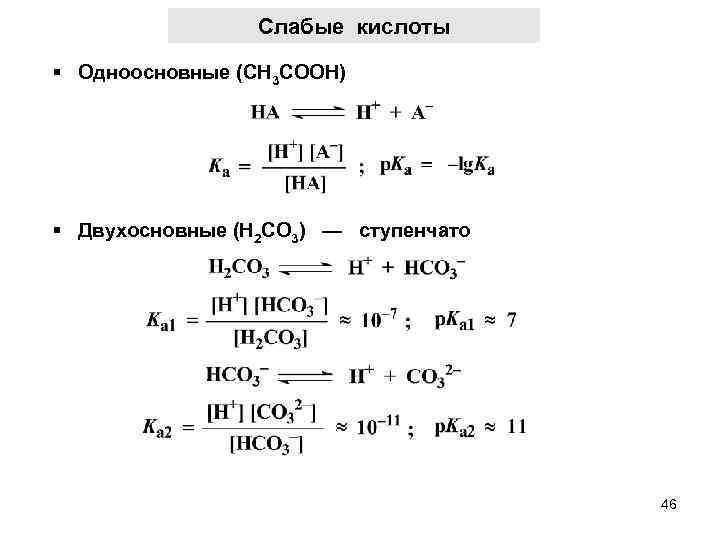 Слабые кислоты § Одноосновные (СН 3 СООН) § Двухосновные (Н 2 СО 3) — ступенчато 46
Слабые кислоты § Одноосновные (СН 3 СООН) § Двухосновные (Н 2 СО 3) — ступенчато 46
 Кислотность и основность «Классическая» теория (С. Аррениус, 1880) q Кислота – донор протона; основание – донор гидроксид-иона. Протолитическая (протонная) теория кислот и оснований (И. Брёнстед, Т. Лоури, 1923) q Кислота – молекула или ион, способные служить донором протона. q Основание – молекула или ион, способные присоединить протон, т. е. акцептор протона. перенос протона § Сопряженные кислотно-основные пары кислота основание + Н+ + сопряженное основание сопряженная кислота 47
Кислотность и основность «Классическая» теория (С. Аррениус, 1880) q Кислота – донор протона; основание – донор гидроксид-иона. Протолитическая (протонная) теория кислот и оснований (И. Брёнстед, Т. Лоури, 1923) q Кислота – молекула или ион, способные служить донором протона. q Основание – молекула или ион, способные присоединить протон, т. е. акцептор протона. перенос протона § Сопряженные кислотно-основные пары кислота основание + Н+ + сопряженное основание сопряженная кислота 47
 Кислоты и основания Кислота CH 3 COOH Основание H+ + CH 3 COO– H 2 O H 3 O + H+ + H 2 O NH 4+ H+ + NH 3 HS– +H H+ + OH– H+ + S 2– 3 NCH 2 COOH +H 3 NCH 2 COO – H+ + +H 3 NCH 2 COO– H+ + H 2 NCH 2 COO– q Амфолиты – вещества, способные как отдавать, так и присоединять протон, т. е. реагировать и как кислоты и как основания ( H 2 O, +H 3 NCH 2 COO–, HCO 3–, HPO 42– ). 48
Кислоты и основания Кислота CH 3 COOH Основание H+ + CH 3 COO– H 2 O H 3 O + H+ + H 2 O NH 4+ H+ + NH 3 HS– +H H+ + OH– H+ + S 2– 3 NCH 2 COOH +H 3 NCH 2 COO – H+ + +H 3 NCH 2 COO– H+ + H 2 NCH 2 COO– q Амфолиты – вещества, способные как отдавать, так и присоединять протон, т. е. реагировать и как кислоты и как основания ( H 2 O, +H 3 NCH 2 COO–, HCO 3–, HPO 42– ). 48
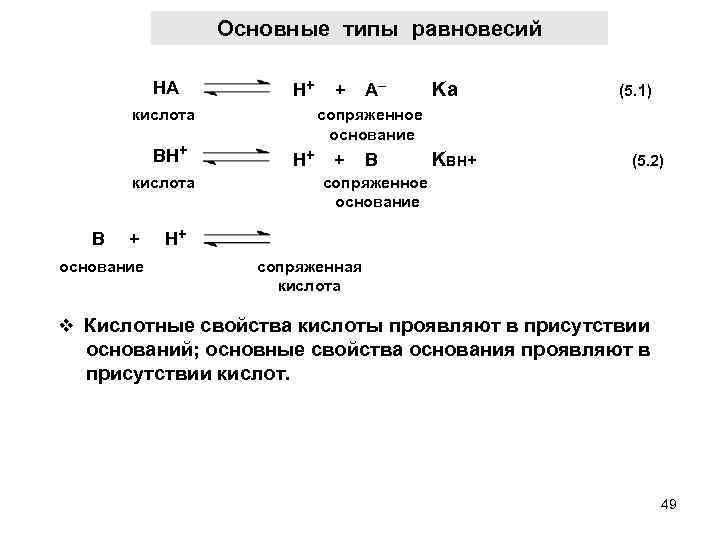 Основные типы равновесий НА кислота BH+ кислота H+ + А– Ka (5. 1) сопряженное основание H+ + B KBH+ (5. 2) сопряженное основание B + H+ основание сопряженная кислота v Кислотные свойства кислоты проявляют в присутствии оснований; основные свойства основания проявляют в присутствии кислот. 49
Основные типы равновесий НА кислота BH+ кислота H+ + А– Ka (5. 1) сопряженное основание H+ + B KBH+ (5. 2) сопряженное основание B + H+ основание сопряженная кислота v Кислотные свойства кислоты проявляют в присутствии оснований; основные свойства основания проявляют в присутствии кислот. 49
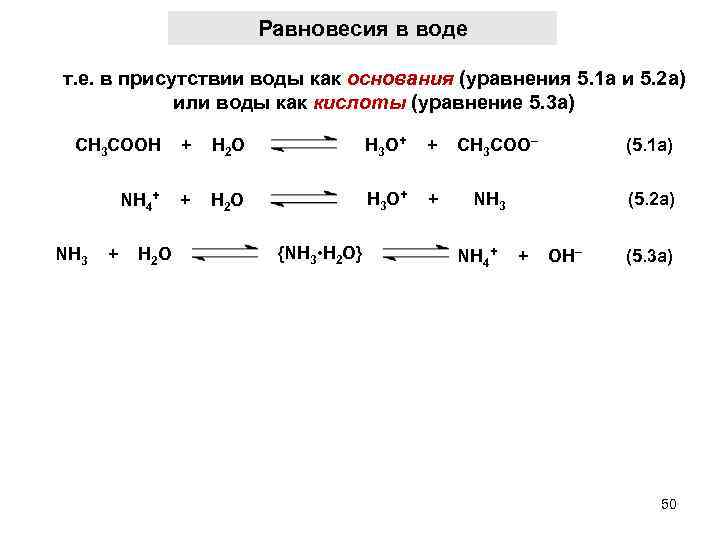 Равновесия в воде т. е. в присутствии воды как основания (уравнения 5. 1 а и 5. 2 а) или воды как кислоты (уравнение 5. 3 а) СH 3 COOH + H 2 O NH 4+ + H 2 O NH 3 + H 2 O H 3 O+ + CH 3 COO– (5. 1 a) H 3 O+ + NH 3 (5. 2 a) {NH 3 • H 2 O} NH 4+ + OH– (5. 3 a) 50
Равновесия в воде т. е. в присутствии воды как основания (уравнения 5. 1 а и 5. 2 а) или воды как кислоты (уравнение 5. 3 а) СH 3 COOH + H 2 O NH 4+ + H 2 O NH 3 + H 2 O H 3 O+ + CH 3 COO– (5. 1 a) H 3 O+ + NH 3 (5. 2 a) {NH 3 • H 2 O} NH 4+ + OH– (5. 3 a) 50
 Расчет р. Н в растворах слабых кислот и оснований Слабые кислоты v Трудно отдают протон, превращаясь в сопряженные основания, активно принимающие протон; – это делает ионизацию слабых кислот обратимым процессом. • Одноосновные слабые кислоты (тип СН 3 СООН) H 2 O H+ + OH– НА + H 2 O НА (K H 2 O) H 3 O+ + А– H+ + А– или в упрощенном виде (p. H < 7) (константа ионизации кислоты) p. H = ½(p. Ka – lgc. HA) (5. 4) 51
Расчет р. Н в растворах слабых кислот и оснований Слабые кислоты v Трудно отдают протон, превращаясь в сопряженные основания, активно принимающие протон; – это делает ионизацию слабых кислот обратимым процессом. • Одноосновные слабые кислоты (тип СН 3 СООН) H 2 O H+ + OH– НА + H 2 O НА (K H 2 O) H 3 O+ + А– H+ + А– или в упрощенном виде (p. H < 7) (константа ионизации кислоты) p. H = ½(p. Ka – lgc. HA) (5. 4) 51
 Пример. Рассчитать р. Н в 0. 1 М растворе CH 3 COOH (p. Ka = 4. 76). H 3 O+ + CH 3 COO– CH 3 COOH + H 2 O CH 3 COOH H+ + CH 3 COO– H 2 O H+ + OH– (K (p. H < 7) H 2 O) p. H = ½(p. Ka – lgc. HA) = ½(4. 76 – lg 10– 1) = ½(4. 76 + 1) = 2. 88 Среда кислая 52
Пример. Рассчитать р. Н в 0. 1 М растворе CH 3 COOH (p. Ka = 4. 76). H 3 O+ + CH 3 COO– CH 3 COOH + H 2 O CH 3 COOH H+ + CH 3 COO– H 2 O H+ + OH– (K (p. H < 7) H 2 O) p. H = ½(p. Ka – lgc. HA) = ½(4. 76 – lg 10– 1) = ½(4. 76 + 1) = 2. 88 Среда кислая 52
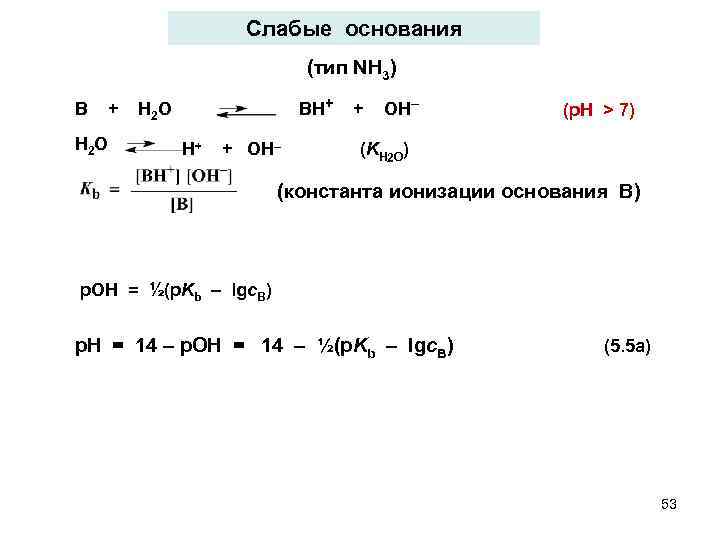 Слабые основания (тип NН 3) BH+ + OH– B + H 2 O H+ + OH– (K (p. H > 7) H 2 O) (константа ионизации основания B) p. OH = ½(p. Kb – lgc. B) p. H = 14 – p. OH = 14 – ½(p. Kb – lgc. B) (5. 5 a) 53
Слабые основания (тип NН 3) BH+ + OH– B + H 2 O H+ + OH– (K (p. H > 7) H 2 O) (константа ионизации основания B) p. OH = ½(p. Kb – lgc. B) p. H = 14 – p. OH = 14 – ½(p. Kb – lgc. B) (5. 5 a) 53
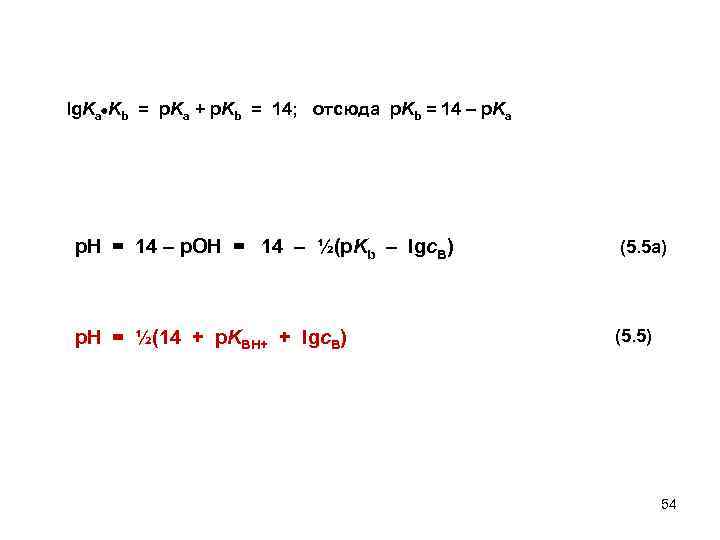 lg. Ka Kb = p. Ka + p. Kb = 14; отсюда p. Kb = 14 – p. Ka p. H = 14 – p. OH = 14 – ½(p. Kb – lgc. B) (5. 5 a) p. H = ½(14 + p. KBH+ + lgc. B) (5. 5) 54
lg. Ka Kb = p. Ka + p. Kb = 14; отсюда p. Kb = 14 – p. Ka p. H = 14 – p. OH = 14 – ½(p. Kb – lgc. B) (5. 5 a) p. H = ½(14 + p. KBH+ + lgc. B) (5. 5) 54
 Пример. Рассчитать р. Н в 0. 01 М растворе аммиака (p. KBH+ = 9. 2). NH 3 + H 2 O H+ + OH– NH 4+ + OH– (K (p. H > 7) H 2 O) p. H = ½(14 + p. KBH+ + lgc. B) = ½(14 + 9. 2 + lg 10– 2) = = ½(14 + 9. 2 – 2) = 10. 6 Среда основная 55
Пример. Рассчитать р. Н в 0. 01 М растворе аммиака (p. KBH+ = 9. 2). NH 3 + H 2 O H+ + OH– NH 4+ + OH– (K (p. H > 7) H 2 O) p. H = ½(14 + p. KBH+ + lgc. B) = ½(14 + 9. 2 + lg 10– 2) = = ½(14 + 9. 2 – 2) = 10. 6 Среда основная 55
 Расчет р. Н в растворах гидролизующихся солей § Соль сильной кислоты и слабого основания BHX (тип NН 4 Сl) BHX BН+ + H 2 O BH+ { CH 3 COOH BH+ + X– H 3 O+ + B H+ + B (p. H < 7) H+ + CH 3 COO– } p. H = ½(p. KBH+ – lgcсоли) (5. 4 a) Гидролиз по катиону 56
Расчет р. Н в растворах гидролизующихся солей § Соль сильной кислоты и слабого основания BHX (тип NН 4 Сl) BHX BН+ + H 2 O BH+ { CH 3 COOH BH+ + X– H 3 O+ + B H+ + B (p. H < 7) H+ + CH 3 COO– } p. H = ½(p. KBH+ – lgcсоли) (5. 4 a) Гидролиз по катиону 56
 Пример. Рассчитать р. Н в 1 М растворе NH 4 Cl (p. KBH+ = 9. 2). NH 4 Cl NН 4+ + H 2 O NH 4+ + Cl– NH 3 + H 3 O+ (p. H < 7) p. H = ½(p. KBH+ – lgcсоли) = ½(9. 2 – lg 1) = ½(9. 2 – 0) = 4. 6 Среда кислая 57
Пример. Рассчитать р. Н в 1 М растворе NH 4 Cl (p. KBH+ = 9. 2). NH 4 Cl NН 4+ + H 2 O NH 4+ + Cl– NH 3 + H 3 O+ (p. H < 7) p. H = ½(p. KBH+ – lgcсоли) = ½(9. 2 – lg 1) = ½(9. 2 – 0) = 4. 6 Среда кислая 57
 • Соль слабой кислоты и сильного основания MA (тип СН 3 СООNa) MA M+ + A– A – + H 2 O { NH 3 + H 2 O HA + OH– (p. H > 7) NH 4+ + OH– } p. H = ½(14 + p. Ka + lgcсоли) (5. 5 b) Гидролиз по аниону 58
• Соль слабой кислоты и сильного основания MA (тип СН 3 СООNa) MA M+ + A– A – + H 2 O { NH 3 + H 2 O HA + OH– (p. H > 7) NH 4+ + OH– } p. H = ½(14 + p. Ka + lgcсоли) (5. 5 b) Гидролиз по аниону 58
 Пример. Рассчитать р. Н в 1 М растворе CH 3 COONa (p. Ka = 4. 76). CH 3 COONa CH 3 COO– + H 2 O Na+ + CH 3 COO– CH 3 COOH + OH– (p. H > 7) p. H = ½(14 + p. Ka + lgcсоли) = ½(14 + 4. 76 + lg 1) = = ½(14 + 4. 76 + 0) = 9. 38 Среда основная 59
Пример. Рассчитать р. Н в 1 М растворе CH 3 COONa (p. Ka = 4. 76). CH 3 COONa CH 3 COO– + H 2 O Na+ + CH 3 COO– CH 3 COOH + OH– (p. H > 7) p. H = ½(14 + p. Ka + lgcсоли) = ½(14 + 4. 76 + lg 1) = = ½(14 + 4. 76 + 0) = 9. 38 Среда основная 59
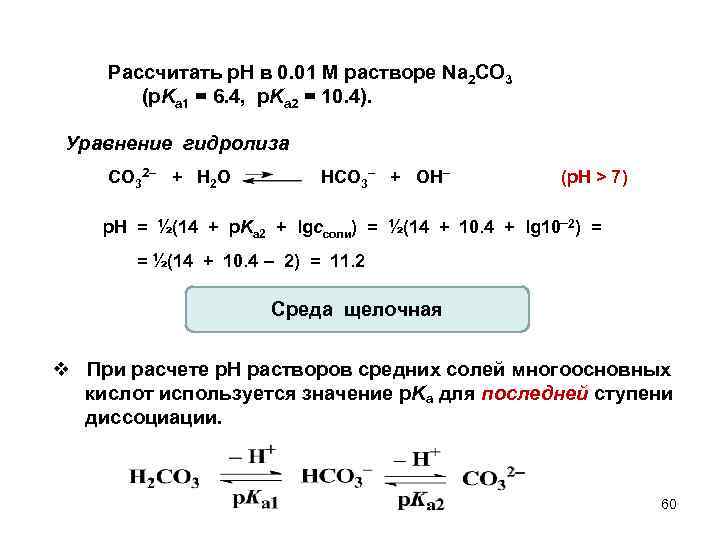 Рассчитать р. Н в 0. 01 М растворе Na 2 CO 3 (p. Ka 1 = 6. 4, p. Ka 2 = 10. 4). Уравнение гидролиза CO 32– + H 2 O HCO 3– + OH– (p. H > 7) p. H = ½(14 + p. Ka 2 + lgcсоли) = ½(14 + 10. 4 + lg 10 2) = = ½(14 + 10. 4 – 2) = 11. 2 Среда щелочная v При расчете р. Н растворов средних солей многоосновных кислот используется значение p. Ka для последней ступени диссоциации. 60
Рассчитать р. Н в 0. 01 М растворе Na 2 CO 3 (p. Ka 1 = 6. 4, p. Ka 2 = 10. 4). Уравнение гидролиза CO 32– + H 2 O HCO 3– + OH– (p. H > 7) p. H = ½(14 + p. Ka 2 + lgcсоли) = ½(14 + 10. 4 + lg 10 2) = = ½(14 + 10. 4 – 2) = 11. 2 Среда щелочная v При расчете р. Н растворов средних солей многоосновных кислот используется значение p. Ka для последней ступени диссоциации. 60
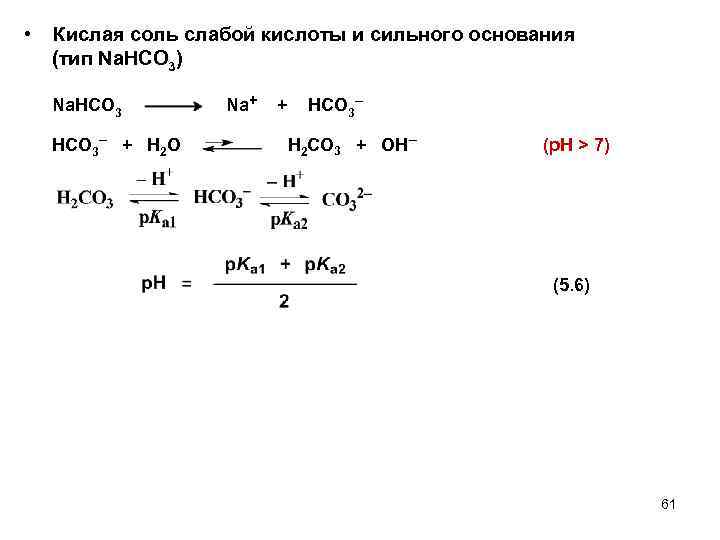 • Кислая соль слабой кислоты и сильного основания (тип Na. НCO 3) Na. HCO 3– + H 2 O Na+ + HCO 3– H 2 CO 3 + OH– (p. H > 7) (5. 6) 61
• Кислая соль слабой кислоты и сильного основания (тип Na. НCO 3) Na. HCO 3– + H 2 O Na+ + HCO 3– H 2 CO 3 + OH– (p. H > 7) (5. 6) 61
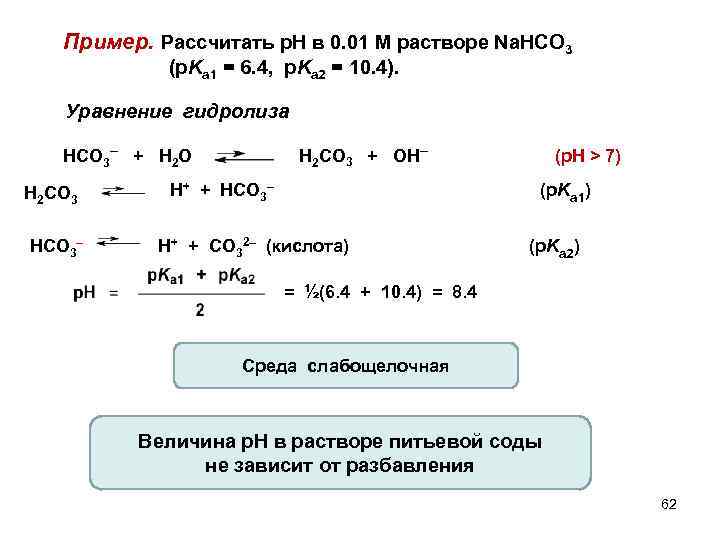 Пример. Рассчитать р. Н в 0. 01 М растворе Na. HCO 3 (p. Ka 1 = 6. 4, p. Ka 2 = 10. 4). Уравнение гидролиза H 2 CO 3 + OH– HCO 3– + H 2 O H 2 CO 3 HCO 3– H+ + HCO 3– (p. H > 7) (p. Ka 1) H+ + CO 32– (кислота) (p. Ka 2) = ½(6. 4 + 10. 4) = 8. 4 Среда слабощелочная Величина р. Н в растворе питьевой соды не зависит от разбавления 62
Пример. Рассчитать р. Н в 0. 01 М растворе Na. HCO 3 (p. Ka 1 = 6. 4, p. Ka 2 = 10. 4). Уравнение гидролиза H 2 CO 3 + OH– HCO 3– + H 2 O H 2 CO 3 HCO 3– H+ + HCO 3– (p. H > 7) (p. Ka 1) H+ + CO 32– (кислота) (p. Ka 2) = ½(6. 4 + 10. 4) = 8. 4 Среда слабощелочная Величина р. Н в растворе питьевой соды не зависит от разбавления 62
 § Кислотно-основные буферные системы и растворы 63
§ Кислотно-основные буферные системы и растворы 63
 Кислотно-основные буферные системы и растворы ● Кислотно-основные буферные системы ○ Буферные растворы ● Количественные закономерности буферного действия ○ Уравнение Гендерсона-Хассельбаха ● Буферная емкость ● Буферные системы организма человека 64
Кислотно-основные буферные системы и растворы ● Кислотно-основные буферные системы ○ Буферные растворы ● Количественные закономерности буферного действия ○ Уравнение Гендерсона-Хассельбаха ● Буферная емкость ● Буферные системы организма человека 64
 Кислотно-основные (протолитические) буферные системы q Протолитические буферные системы – системы, поддерживающие постоянство р. Н при добавлении небольших количеств кислот или оснований, а также при разбавлении. Играют исключительную роль в процессах жизнедеятельности (большинство биологических жидкостей – буферные растворы) – поддерживают р. Н биологических жидкостей, тканей и органов (кислотно-щелочной, т. е. протолитический гомеостаз); Кариесрезистентность зубов связана с р. Н слюны: высокий уровень кариесрезистентности – 7. 4, средний – 7. 25, низкий – 7. 2. Существенное деминерализирующее действие при р. Н 6. Смещение р. Н в щелочную область – возрастает минерализующий эффект (зубные камни) Десневая жидкость р. Н 8. 5 (входящий в нее фермент эластаза действует наиболее активно именно при этом р. Н) 65
Кислотно-основные (протолитические) буферные системы q Протолитические буферные системы – системы, поддерживающие постоянство р. Н при добавлении небольших количеств кислот или оснований, а также при разбавлении. Играют исключительную роль в процессах жизнедеятельности (большинство биологических жидкостей – буферные растворы) – поддерживают р. Н биологических жидкостей, тканей и органов (кислотно-щелочной, т. е. протолитический гомеостаз); Кариесрезистентность зубов связана с р. Н слюны: высокий уровень кариесрезистентности – 7. 4, средний – 7. 25, низкий – 7. 2. Существенное деминерализирующее действие при р. Н 6. Смещение р. Н в щелочную область – возрастает минерализующий эффект (зубные камни) Десневая жидкость р. Н 8. 5 (входящий в нее фермент эластаза действует наиболее активно именно при этом р. Н) 65
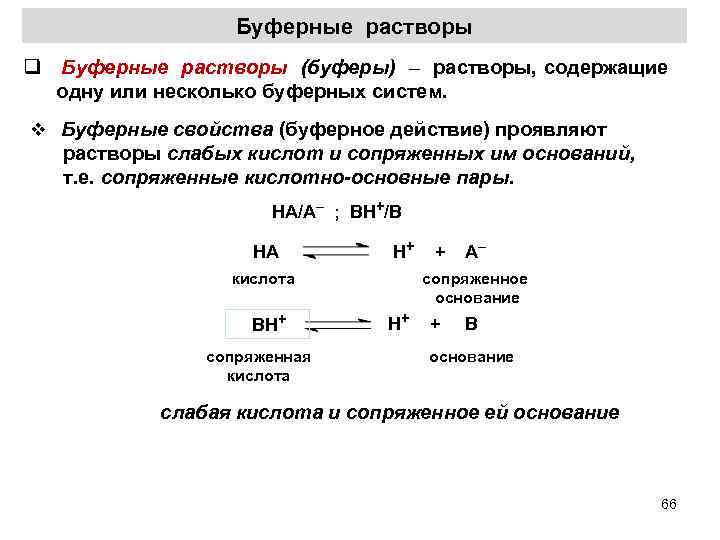 Буферные растворы q Буферные растворы (буферы) – растворы, содержащие одну или несколько буферных систем. v Буферные свойства (буферное действие) проявляют растворы слабых кислот и сопряженных им оснований, т. е. сопряженные кислотно-основные пары. HA/A– ; BH+/B НА кислота H+ + А– сопряженное основание H+ + B BH+ сопряженная кислота основание слабая кислота и сопряженное ей основание 66
Буферные растворы q Буферные растворы (буферы) – растворы, содержащие одну или несколько буферных систем. v Буферные свойства (буферное действие) проявляют растворы слабых кислот и сопряженных им оснований, т. е. сопряженные кислотно-основные пары. HA/A– ; BH+/B НА кислота H+ + А– сопряженное основание H+ + B BH+ сопряженная кислота основание слабая кислота и сопряженное ей основание 66
 Схема (механизм) буферного действия 67
Схема (механизм) буферного действия 67
 Количественные закономерности буферного действия Уравнение Гендерсона-Хассельбаха Интервал буферного действия (p. Ka 1) 68
Количественные закономерности буферного действия Уравнение Гендерсона-Хассельбаха Интервал буферного действия (p. Ka 1) 68
 Уравнение Гендерсона-Хассельбаха 69
Уравнение Гендерсона-Хассельбаха 69
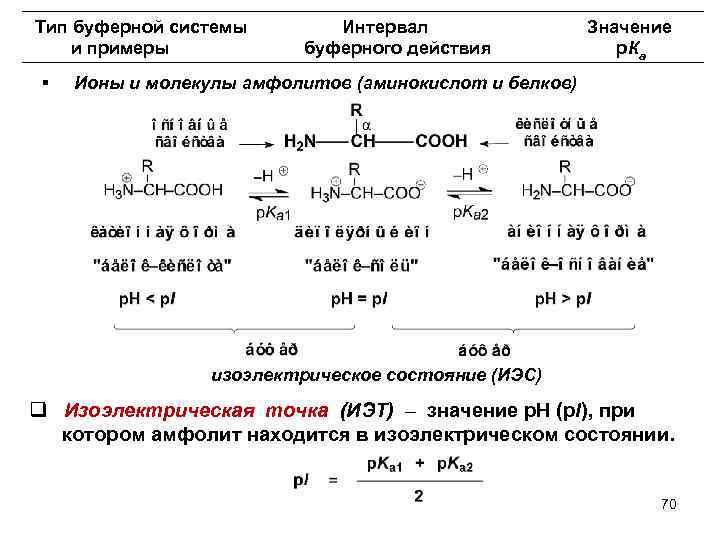 Тип буферной системы Интервал Значение и примеры буферного действия р. Ка § Ионы и молекулы амфолитов (аминокислот и белков) изоэлектрическое состояние (ИЭС) q Изоэлектрическая точка (ИЭТ) – значение р. Н (p. I), при котором амфолит находится в изоэлектрическом состоянии. 70
Тип буферной системы Интервал Значение и примеры буферного действия р. Ка § Ионы и молекулы амфолитов (аминокислот и белков) изоэлектрическое состояние (ИЭС) q Изоэлектрическая точка (ИЭТ) – значение р. Н (p. I), при котором амфолит находится в изоэлектрическом состоянии. 70
 Пример. Рассчитать р. Н раствора, содержащего 1 моль СН 3 СОOH (p. Ka = 4. 76) и 1 моль СН 3 СОONa. o Каково будет значение р. Н после добавления 0. 1 моля HCl к 1 л этого раствора. H+ + CH 3 COO– 0. 1 CH 3 COOH – 0. 1 моль p. H 0. 1; [H+] возрастает в 1. 22 раза Для сравнения: при добавлении 0. 1 моля HCl к 1 л Н 2 О p. H 6. 0; т. е. [H+] возрастает в 106 раз 71
Пример. Рассчитать р. Н раствора, содержащего 1 моль СН 3 СОOH (p. Ka = 4. 76) и 1 моль СН 3 СОONa. o Каково будет значение р. Н после добавления 0. 1 моля HCl к 1 л этого раствора. H+ + CH 3 COO– 0. 1 CH 3 COOH – 0. 1 моль p. H 0. 1; [H+] возрастает в 1. 22 раза Для сравнения: при добавлении 0. 1 моля HCl к 1 л Н 2 О p. H 6. 0; т. е. [H+] возрастает в 106 раз 71
 3) Определение соотношения компонентов буферного раствора Уравнение Гендерсона-Хассельбаха Пример. Рассчитать соотношение концентраций СН 3 СООН (р. Ка 4. 8) и СН 3 СООNa в буферном растворе со значением р. Н = 5. 8. из уравнения Гендерсона-Хассельбаха следует т. е. соотношение концентраций соли и кислоты равно 10 : 1 72
3) Определение соотношения компонентов буферного раствора Уравнение Гендерсона-Хассельбаха Пример. Рассчитать соотношение концентраций СН 3 СООН (р. Ка 4. 8) и СН 3 СООNa в буферном растворе со значением р. Н = 5. 8. из уравнения Гендерсона-Хассельбаха следует т. е. соотношение концентраций соли и кислоты равно 10 : 1 72
 Буферная емкость — величина, характеризующая способность буферного раствора противодействовать изменению р. Н среды при добавлении кислот или щелочей; — количество кислоты или щелочи, при добавлении которого к 1 л буферного раствора его р. Н изменяется на 1. Зависит: 1) от концентрации компонентов буфера; 2) от соотношения компонентов (т. е. от р. Н). v Буферная емкость не постоянна в интервале буферного действия. v Интервал буферного действия: р. Н = p. Ka 1. v р. Н = p. Ka + lg 10/1; р. Н = p. Ka + lg 1/10 v Bmax при р. Н = p. Ka; при этом Вк = Вщ 73
Буферная емкость — величина, характеризующая способность буферного раствора противодействовать изменению р. Н среды при добавлении кислот или щелочей; — количество кислоты или щелочи, при добавлении которого к 1 л буферного раствора его р. Н изменяется на 1. Зависит: 1) от концентрации компонентов буфера; 2) от соотношения компонентов (т. е. от р. Н). v Буферная емкость не постоянна в интервале буферного действия. v Интервал буферного действия: р. Н = p. Ka 1. v р. Н = p. Ka + lg 10/1; р. Н = p. Ka + lg 1/10 v Bmax при р. Н = p. Ka; при этом Вк = Вщ 73
 Буферные системы организма человека • • • Буферные системы в стоматологии Буферными свойствами обладают слюна и эмаль зуба. Ca 10(OH)2(PO 4)6 + 14 H+ → 10 Ca 2+ + H 2 PO 4− + 2 H 2 O Реакции между поверхностью зуба и средой ротовой полости: Ca 10(OH)2(PO 4)6 + 2 H+ → Ca 9 H 2(OH)2(PO 4)6 + Ca 2+ Способ профилактики кариеса – увеличение буферной емкости слюны добавлением в пищу специальных фосфат-карбонатных смесей для предотвращения снижения р. Н 74
Буферные системы организма человека • • • Буферные системы в стоматологии Буферными свойствами обладают слюна и эмаль зуба. Ca 10(OH)2(PO 4)6 + 14 H+ → 10 Ca 2+ + H 2 PO 4− + 2 H 2 O Реакции между поверхностью зуба и средой ротовой полости: Ca 10(OH)2(PO 4)6 + 2 H+ → Ca 9 H 2(OH)2(PO 4)6 + Ca 2+ Способ профилактики кариеса – увеличение буферной емкости слюны добавлением в пищу специальных фосфат-карбонатных смесей для предотвращения снижения р. Н 74
 Буферные системы организма человека гидрокарбонатная, гидрофосфатная, белковая, гемоглобиновая (А. С. Ленский, 1989, 155 160; В. И. Слесарев, 2000, 197 207; А. С. Ленский, И. Ю. Белавин, С. Ю. Быликин, 2008, 316 321) Буферные системы крови Плазма крови Эритроциты гидрокарбонатная, гидрофосфатная, белковая гидрокарбонатная, гемоглобиновая, гидрофосфатная v Плазма крови: р. Н = 7. 40 0. 05; a(H+) = 3. 7 • 10– 8 – 4. 0 • 10– 8 моль/л. v Артериальная кровь: р. Н = 7. 38 – 7. 42. v Венозная кровь: р. Н = 7. 36 – 7. 40. v Внутриклеточные жидкости: р. Н = 6. 8 – 7. 8. 75
Буферные системы организма человека гидрокарбонатная, гидрофосфатная, белковая, гемоглобиновая (А. С. Ленский, 1989, 155 160; В. И. Слесарев, 2000, 197 207; А. С. Ленский, И. Ю. Белавин, С. Ю. Быликин, 2008, 316 321) Буферные системы крови Плазма крови Эритроциты гидрокарбонатная, гидрофосфатная, белковая гидрокарбонатная, гемоглобиновая, гидрофосфатная v Плазма крови: р. Н = 7. 40 0. 05; a(H+) = 3. 7 • 10– 8 – 4. 0 • 10– 8 моль/л. v Артериальная кровь: р. Н = 7. 38 – 7. 42. v Венозная кровь: р. Н = 7. 36 – 7. 40. v Внутриклеточные жидкости: р. Н = 6. 8 – 7. 8. 75
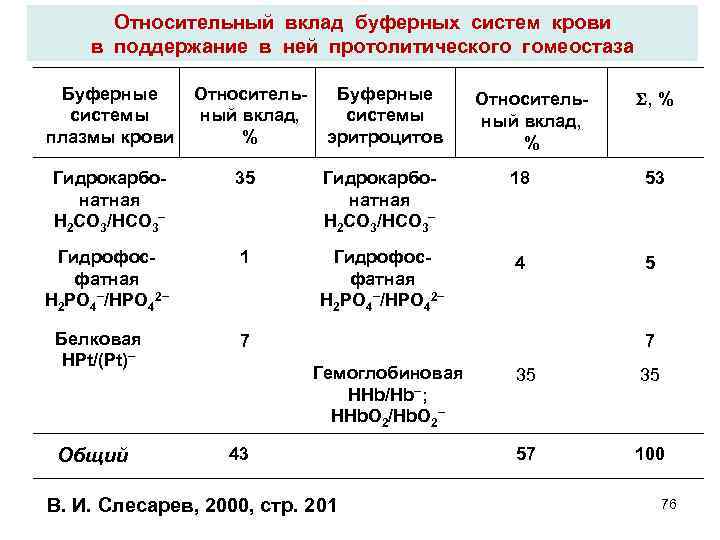 Относительный вклад буферных систем крови в поддержание в ней протолитического гомеостаза Буферные системы плазмы крови Относительный вклад, % Буферные системы эритроцитов Относительный вклад, % , % Гидрокарбонатная H 2 CO 3/HCO 3– 35 Гидрокарбонатная H 2 CO 3/HCO 3– 18 53 Гидрофосфатная H 2 PO 4–/HPO 42– 1 Гидрофосфатная H 2 PO 4–/HPO 42– 4 5 Белковая HPt/(Pt)– Общий 7 7 Гемоглобиновая HHb/Hb–; HHb. O 2/Hb. O 2– 43 В. И. Слесарев, 2000, стр. 201 35 35 57 100 76
Относительный вклад буферных систем крови в поддержание в ней протолитического гомеостаза Буферные системы плазмы крови Относительный вклад, % Буферные системы эритроцитов Относительный вклад, % , % Гидрокарбонатная H 2 CO 3/HCO 3– 35 Гидрокарбонатная H 2 CO 3/HCO 3– 18 53 Гидрофосфатная H 2 PO 4–/HPO 42– 1 Гидрофосфатная H 2 PO 4–/HPO 42– 4 5 Белковая HPt/(Pt)– Общий 7 7 Гемоглобиновая HHb/Hb–; HHb. O 2/Hb. O 2– 43 В. И. Слесарев, 2000, стр. 201 35 35 57 100 76
 • Гидрокарбонатная буферная система (H 2 CO 3/HCO 3–) Вк(эритр) < Вк(плазмы крови) • Гидрофосфатная буферная система (Н 2 РО 4– / НРО 42–) фосфатов больше внутри клетки v По сравнению с гидрокарбонатной гидрофосфатная система более «консервативна» – избыточные продукты нейтрализации выводятся через почки (2– 3 суток). 77
• Гидрокарбонатная буферная система (H 2 CO 3/HCO 3–) Вк(эритр) < Вк(плазмы крови) • Гидрофосфатная буферная система (Н 2 РО 4– / НРО 42–) фосфатов больше внутри клетки v По сравнению с гидрокарбонатной гидрофосфатная система более «консервативна» – избыточные продукты нейтрализации выводятся через почки (2– 3 суток). 77
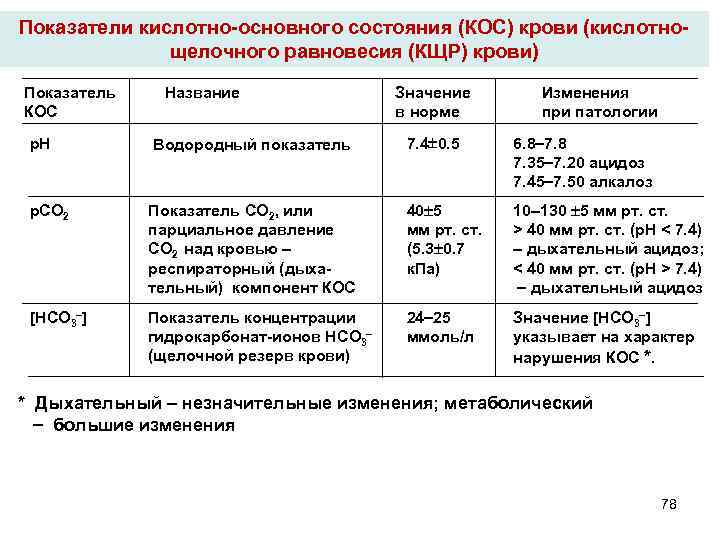 Показатели кислотно-основного состояния (КОС) крови (кислотнощелочного равновесия (КЩР) крови) Показатель КОС Название Значение в норме Изменения при патологии р. Н Водородный показатель 7. 4 0. 5 6. 8 7. 35 7. 20 ацидоз 7. 45 7. 50 алкалоз р. СО 2 Показатель СО 2, или парциальное давление СО 2 над кровью респираторный (дыхательный) компонент КОС 40 5 мм рт. ст. (5. 3 0. 7 к. Па) 10 130 5 мм рт. ст. > 40 мм рт. ст. (р. Н < 7. 4) дыхательный ацидоз; < 40 мм рт. ст. (р. Н > 7. 4) дыхательный ацидоз [HCO 3 ] Показатель концентрации гидрокарбонат-ионов HCO 3 (щелочной резерв крови) 24 25 ммоль/л Значение [HCO 3 ] указывает на характер нарушения КОС *. * Дыхательный незначительные изменения; метаболический большие изменения 78
Показатели кислотно-основного состояния (КОС) крови (кислотнощелочного равновесия (КЩР) крови) Показатель КОС Название Значение в норме Изменения при патологии р. Н Водородный показатель 7. 4 0. 5 6. 8 7. 35 7. 20 ацидоз 7. 45 7. 50 алкалоз р. СО 2 Показатель СО 2, или парциальное давление СО 2 над кровью респираторный (дыхательный) компонент КОС 40 5 мм рт. ст. (5. 3 0. 7 к. Па) 10 130 5 мм рт. ст. > 40 мм рт. ст. (р. Н < 7. 4) дыхательный ацидоз; < 40 мм рт. ст. (р. Н > 7. 4) дыхательный ацидоз [HCO 3 ] Показатель концентрации гидрокарбонат-ионов HCO 3 (щелочной резерв крови) 24 25 ммоль/л Значение [HCO 3 ] указывает на характер нарушения КОС *. * Дыхательный незначительные изменения; метаболический большие изменения 78
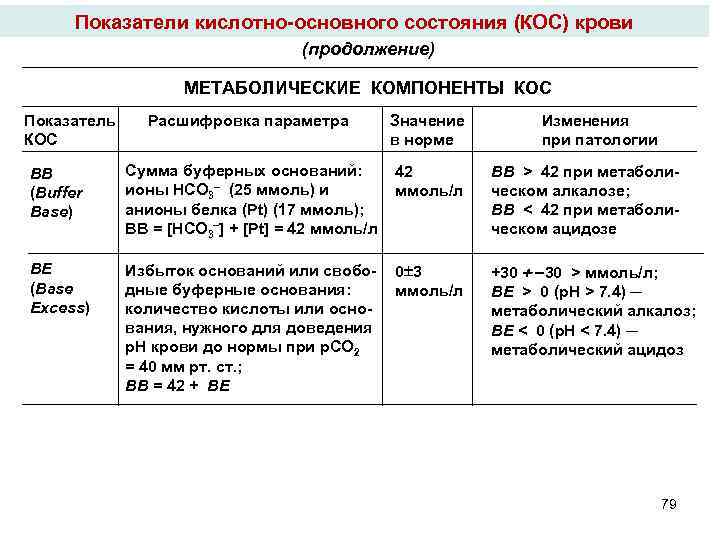 Показатели кислотно-основного состояния (КОС) крови (продолжение) МЕТАБОЛИЧЕСКИЕ КОМПОНЕНТЫ КОС Показатель КОС Расшифровка параметра Значение в норме Изменения при патологии BB (Buffer Base) Сумма буферных оснований: 42 (25 ммоль) и ионы HCO 3 ммоль/л анионы белка (Pt) (17 ммоль); BB = [HCO 3 ] + [Pt] = 42 ммоль/л BB > 42 при метаболическом алкалозе; BB < 42 при метаболическом ацидозе BE (Base Excess) Избыток оснований или свободные буферные основания: количество кислоты или основания, нужного для доведения р. Н крови до нормы при р. CO 2 = 40 мм рт. ст. ; BB = 42 + BE +30 30 > ммоль/л; BE > 0 (р. Н > 7. 4) ─ метаболический алкалоз; BE < 0 (р. Н < 7. 4) ─ метаболический ацидоз 0 3 ммоль/л 79
Показатели кислотно-основного состояния (КОС) крови (продолжение) МЕТАБОЛИЧЕСКИЕ КОМПОНЕНТЫ КОС Показатель КОС Расшифровка параметра Значение в норме Изменения при патологии BB (Buffer Base) Сумма буферных оснований: 42 (25 ммоль) и ионы HCO 3 ммоль/л анионы белка (Pt) (17 ммоль); BB = [HCO 3 ] + [Pt] = 42 ммоль/л BB > 42 при метаболическом алкалозе; BB < 42 при метаболическом ацидозе BE (Base Excess) Избыток оснований или свободные буферные основания: количество кислоты или основания, нужного для доведения р. Н крови до нормы при р. CO 2 = 40 мм рт. ст. ; BB = 42 + BE +30 30 > ммоль/л; BE > 0 (р. Н > 7. 4) ─ метаболический алкалоз; BE < 0 (р. Н < 7. 4) ─ метаболический ацидоз 0 3 ммоль/л 79
 Комплексные (координационные) соединения • — устойчивые химические соединения сложного состава, в которых имеется хотя бы одна связь, возникшая по донорно-акцепторному механизму. • — один из атомов имеет валентность, превышающую его степень окисления • Cu(OH)2 + 4 NH 3 H 2 O [Cu(NH 3)4](OH)2 + 4 H 2 O • Ag. Cl + 2 NH 3 H 2 O [Ag(NH 3)2]Cl + 2 H O
Комплексные (координационные) соединения • — устойчивые химические соединения сложного состава, в которых имеется хотя бы одна связь, возникшая по донорно-акцепторному механизму. • — один из атомов имеет валентность, превышающую его степень окисления • Cu(OH)2 + 4 NH 3 H 2 O [Cu(NH 3)4](OH)2 + 4 H 2 O • Ag. Cl + 2 NH 3 H 2 O [Ag(NH 3)2]Cl + 2 H O
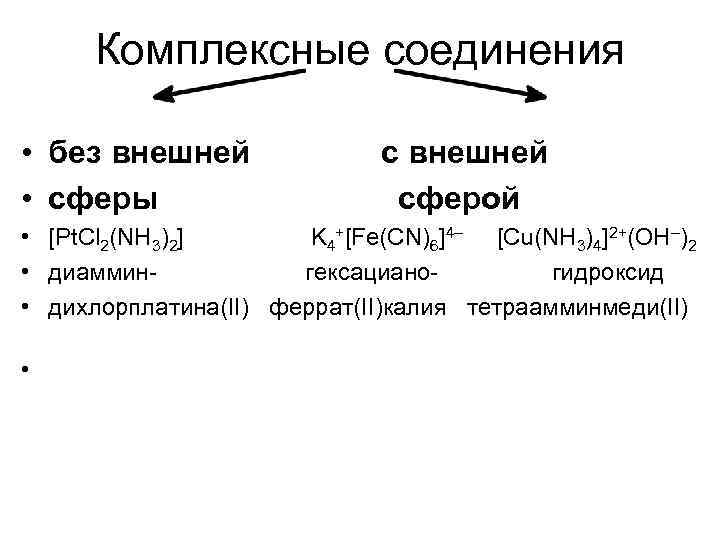 Комплексные соединения • без внешней с внешней • сферы сферой • [Pt. Cl 2(NH 3)2] K 4+[Fe(CN)6]4– [Cu(NH 3)4]2+(OH–)2 • диаммин- гексациано- гидроксид • дихлорплатина(II) феррат(II)калия тетраамминмеди(II) •
Комплексные соединения • без внешней с внешней • сферы сферой • [Pt. Cl 2(NH 3)2] K 4+[Fe(CN)6]4– [Cu(NH 3)4]2+(OH–)2 • диаммин- гексациано- гидроксид • дихлорплатина(II) феррат(II)калия тетраамминмеди(II) •
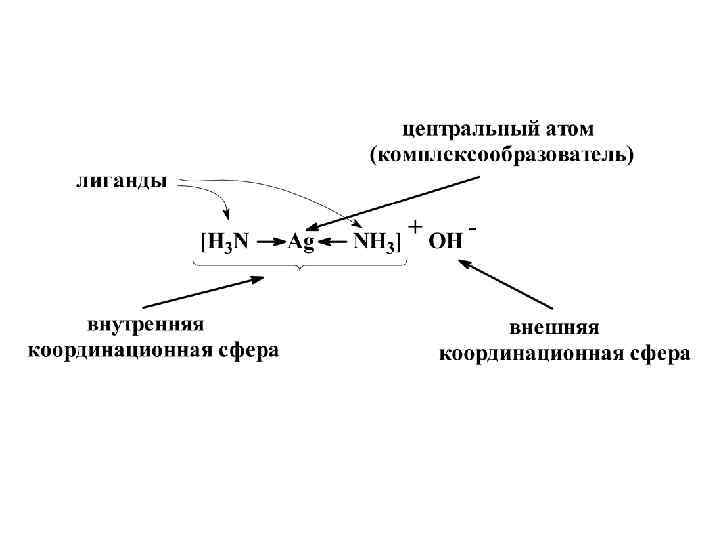
 • Центральный атом (комплексообразователь) - атом или ион, который является акцептором электронных пар, предоставляя свободные атомные орбитали для образования связи • — координационное число; • — степень окисления
• Центральный атом (комплексообразователь) - атом или ион, который является акцептором электронных пар, предоставляя свободные атомные орбитали для образования связи • — координационное число; • — степень окисления
 • Координационное число — число атомов, непосредственно присоединенных к центральному атому (2, 4, 5, 6 и т. д. ) • Степень окисления — заряд, которым обладал бы атом элемента в химическом соединении, если электроны в каждой связи этого атома сместить к более электроотрицательному атому Fe. Cl 2 - (хлорид железа(II) - (Fe+2, Cl-1) Fe. Cl 3 - (хлорид железа(III) - (Fe+3, Cl-1) NH 4+ - (аммоний-ион) - (N-3, H+1) K 3[Fe(CN)6] – (гексацианоферрат (III) калия) – (K+, Fe+3, CN-) K 4[Fe(CN)6] – (гексацианоферрат (II) калия) – (K+, Fe+2, CN-)
• Координационное число — число атомов, непосредственно присоединенных к центральному атому (2, 4, 5, 6 и т. д. ) • Степень окисления — заряд, которым обладал бы атом элемента в химическом соединении, если электроны в каждой связи этого атома сместить к более электроотрицательному атому Fe. Cl 2 - (хлорид железа(II) - (Fe+2, Cl-1) Fe. Cl 3 - (хлорид железа(III) - (Fe+3, Cl-1) NH 4+ - (аммоний-ион) - (N-3, H+1) K 3[Fe(CN)6] – (гексацианоферрат (III) калия) – (K+, Fe+3, CN-) K 4[Fe(CN)6] – (гексацианоферрат (II) калия) – (K+, Fe+2, CN-)
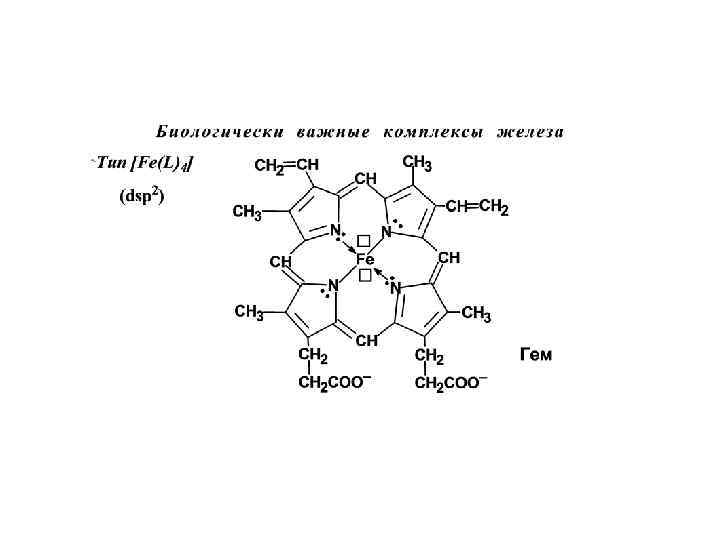
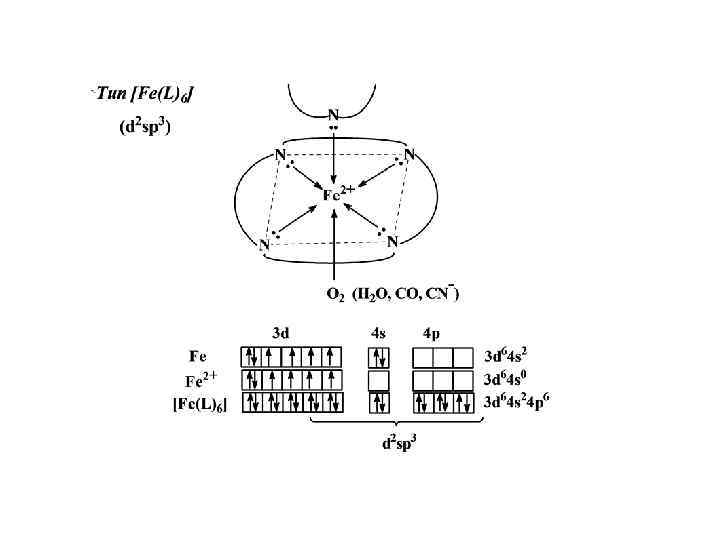
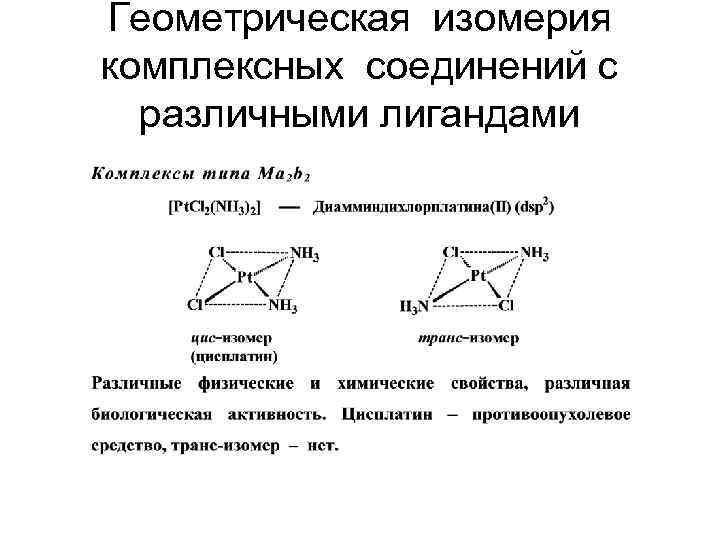 Геометрическая изомерия комплексных соединений с различными лигандами
Геометрическая изомерия комплексных соединений с различными лигандами
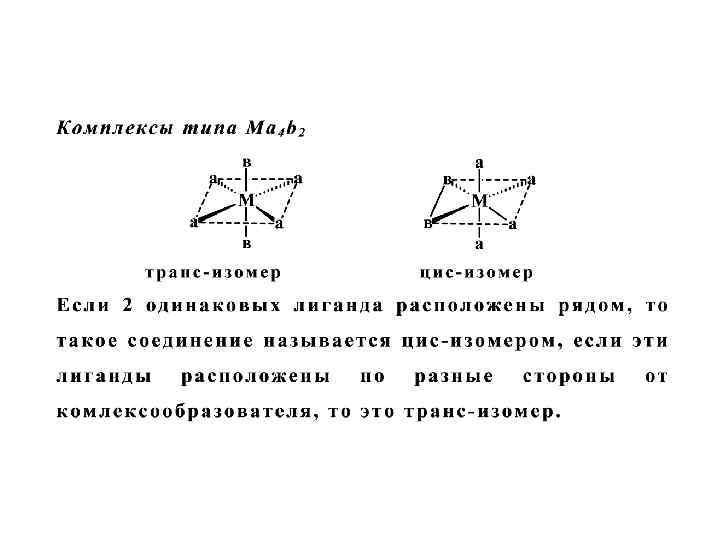
 РАВНОВЕСИЯ В РАСТВОРАХ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
РАВНОВЕСИЯ В РАСТВОРАХ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ


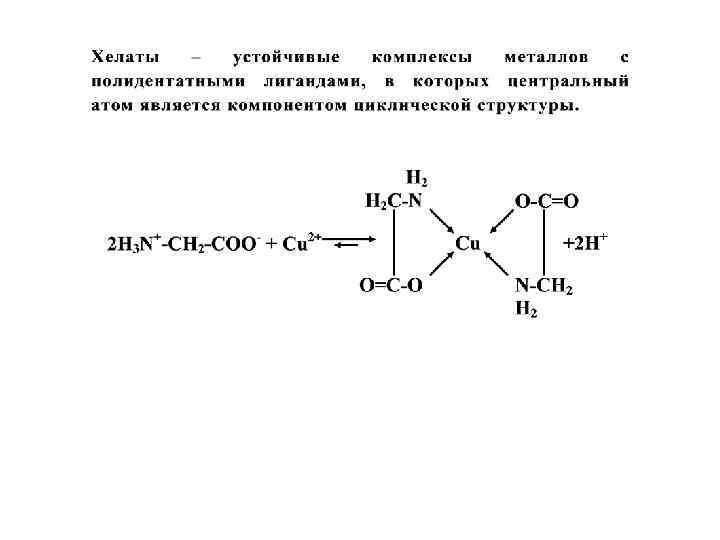
 РАВНОВЕСИЕ ТВЕРДОЕ ТЕЛО — РАСТВОР (гетерогенное)
РАВНОВЕСИЕ ТВЕРДОЕ ТЕЛО — РАСТВОР (гетерогенное)





 • Гетерогенные равновесия в биологических системах В организме наиболее важные гетерогенные процессы протекают при образовании костной ткани, а также при образовании различных камней при почечнокаменной и желчнокаменной болезни. • Процесс образования кости происходит в клетках костной ткани остеобластах при р. Н 8, 3 на белке коллагене, который способствует формированию правильно организованных ядер кристаллизации.
• Гетерогенные равновесия в биологических системах В организме наиболее важные гетерогенные процессы протекают при образовании костной ткани, а также при образовании различных камней при почечнокаменной и желчнокаменной болезни. • Процесс образования кости происходит в клетках костной ткани остеобластах при р. Н 8, 3 на белке коллагене, который способствует формированию правильно организованных ядер кристаллизации.

 Ca/P = 1. 67
Ca/P = 1. 67


