Фазовые переходы.pptx
- Количество слайдов: 21

http: //earthchronicles. ru/Publications/ 92/9/4158835518_8 b 97 f 1036 2_o. jpg

Как известно липиды при комнатной температуре могут находиться в двух состояниях твердом и жидком. СОСТОЯНИЕ БИСЛОЯ Усреднённая площадь липида Усреднённая длина липида ТВЁРДОКРИСТАЛЛИЧЕСКОЕ ЖИДКОКРИСТАЛЛИЧЕСКОЕ 0, 46 -0, 48 нм 2 4, 7 нм 0, 60 -0, 80 нм 2 3, 9 нм http: //upload. wikimedia. org/wikipedia/commons/thumb/2/ 2 e/Lipid_unsaturation_effect. svg/320 px. Lipid_unsaturation_effect. svg. png
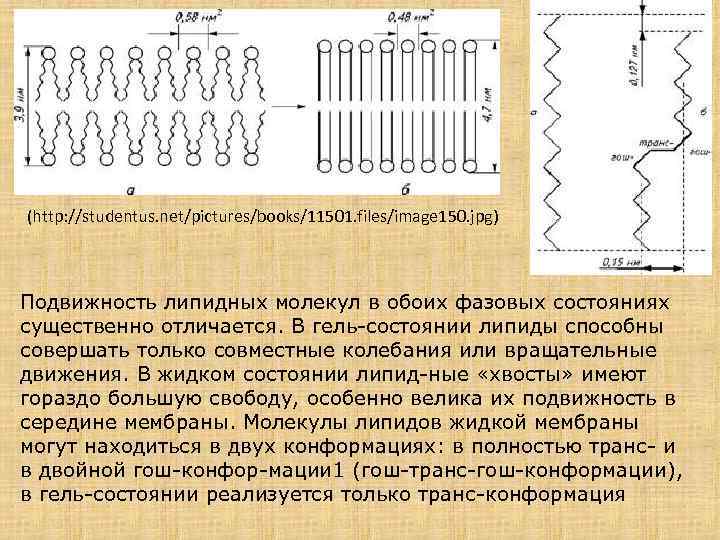
(http: //studentus. net/pictures/books/11501. files/image 150. jpg) Подвижность липидных молекул в обоих фазовых состояниях существенно отличается. В гель-состоянии липиды способны совершать только совместные колебания или вращательные движения. В жидком состоянии липид-ные «хвосты» имеют гораздо большую свободу, особенно велика их подвижность в середине мембраны. Молекулы липидов жидкой мембраны могут находиться в двух конформациях: в полностью транс- и в двойной гош-конфор-мации 1 (гош-транс-гош-конформации), в гель-состоянии реализуется только транс-конформация
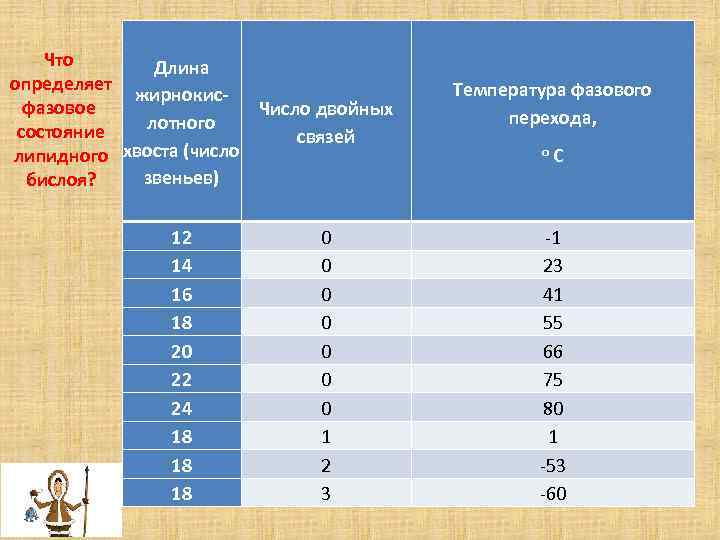
Что Длина определяет жирнокисфазовое Число двойных лотного состояние связей липидного хвоста (число звеньев) бислоя? 12 14 16 18 20 22 24 18 18 18 0 0 0 0 1 2 3 Температура фазового перехода, о С -1 23 41 55 66 75 80 1 -53 -60

Профиль подвижности звеньев жирнокислотных цепей в мембране Интересное применение нашел метод изучения ЯМР в области поглощения дейтерия. Поскольку ядра дейтерия в два раза тяжелее ядер обычного водорода, поглощение этих атомов лежит при совершенно разных частотах при одном и том же поле. Были проведены опыты по избирательному дейтерированию метиленовых групп в определенных местах углеводородной цепи жирных кислот, входящих в состав фосфолипидов мембран. Уширение Влияние расстояние углеродного атома полос поглощения оказалось разным, в от поверхности на его молекулярную подвижность в биологических зависимости от положения мембранах по данным ЯМР. S метиленовой группы в цепи. Это параметр упорядоченности вращения говорит о различии в подвижности сегмента. Кривые получены при разных соответствующих групп. температурах. Текучесть мембраны ограничена внутренней гидрофобной фазой
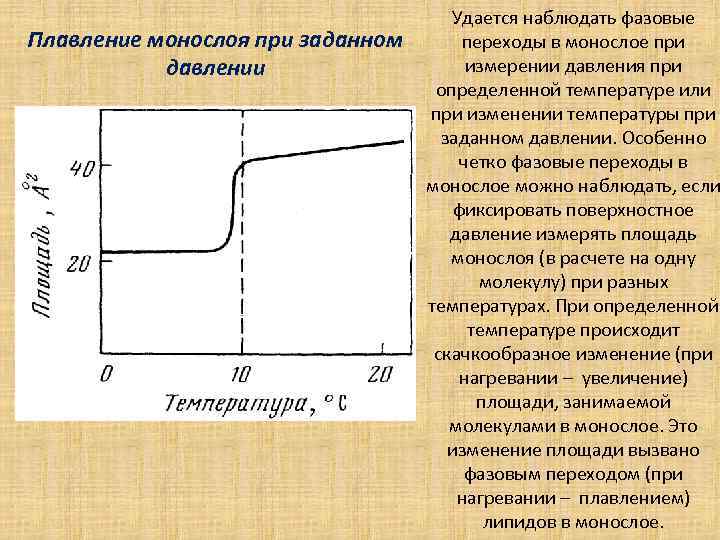
Плавление монослоя при заданном давлении Удается наблюдать фазовые переходы в монослое при измерении давления при определенной температуре или при изменении температуры при заданном давлении. Особенно четко фазовые переходы в монослое можно наблюдать, если фиксировать поверхностное давление измерять площадь монослоя (в расчете на одну молекулу) при разных температурах. При определенной температуре происходит скачкообразное изменение (при нагревании – увеличение) площади, занимаемой молекулами в монослое. Это изменение площади вызвано фазовым переходом (при нагревании – плавлением) липидов в монослое.
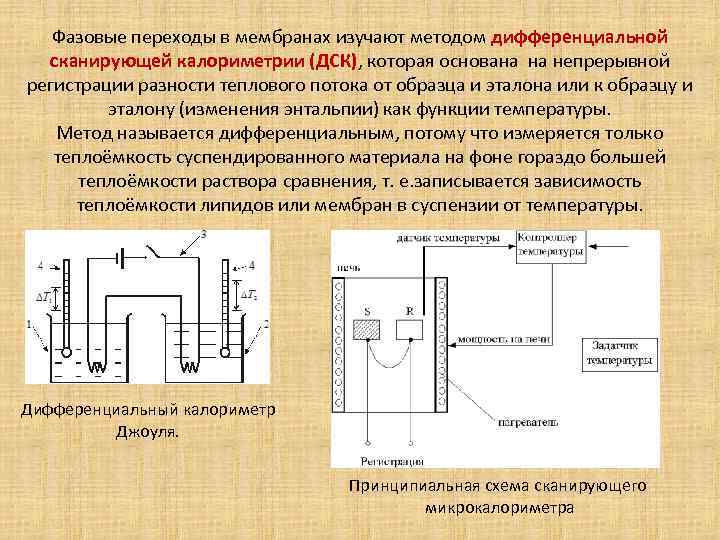
Фазовые переходы в мембранах изучают методом дифференциальной сканирующей калориметрии (ДСК), которая основана на непрерывной регистрации разности теплового потока от образца и эталона или к образцу и эталону (изменения энтальпии) как функции температуры. Метод называется дифференциальным, потому что измеряется только теплоёмкость суспендированного материала на фоне гораздо большей теплоёмкости раствора сравнения, т. е. записывается зависимость теплоёмкости липидов или мембран в суспензии от температуры. Дифференциальный калориметр Джоуля. Принципиальная схема сканирующего микрокалориметра
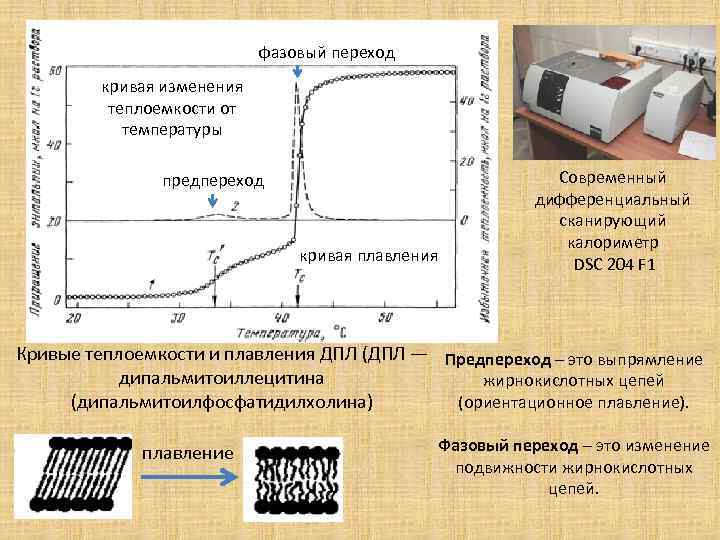
фазовый переход кривая изменения теплоемкости от температуры предпереход кривая плавления Современный дифференциальный сканирующий калориметр DSC 204 F 1 Кривые теплоемкости и плавления ДПЛ (ДПЛ — Предпереход – это выпрямление дипальмитоиллецитина жирнокислотных цепей (дипальмитоилфосфатидилхолина) (ориентационное плавление). плавление Фазовый переход – это изменение подвижности жирнокислотных цепей.
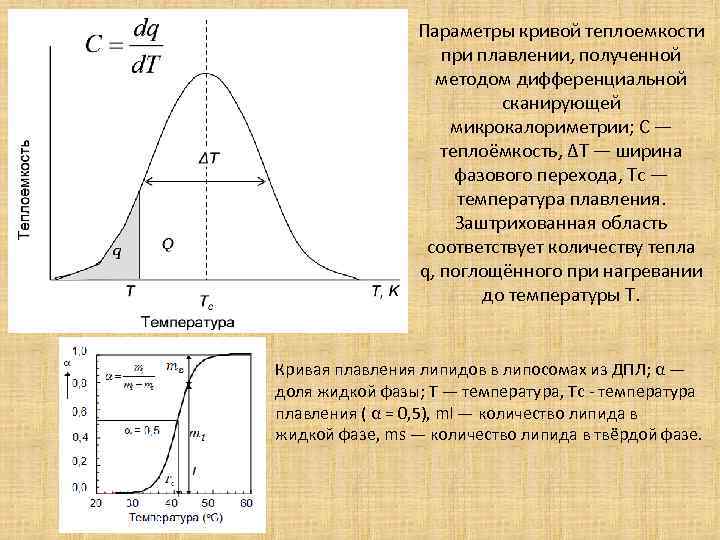
Параметры кривой теплоемкости при плавлении, полученной методом дифференциальной сканирующей микрокалориметрии; С — теплоёмкость, ΔT — ширина фазового перехода, Tc — температура плавления. Заштрихованная область соответствует количеству тепла q, поглощённого при нагревании до температуры T. Кривая плавления липидов в липосомах из ДПЛ; α — доля жидкой фазы; T — температура, Tc - температура плавления ( α = 0, 5), ml — количество липида в жидкой фазе, ms — количество липида в твёрдой фазе.
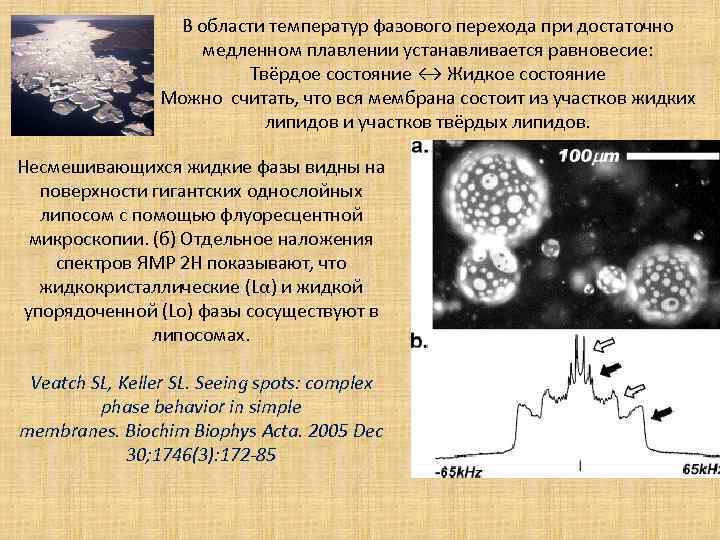
В области температур фазового перехода при достаточно медленном плавлении устанавливается равновесие: Твёрдое состояние ↔ Жидкое состояние Можно считать, что вся мембрана состоит из участков жидких липидов и участков твёрдых липидов. Несмешивающихся жидкие фазы видны на поверхности гигантских однослойных липосом с помощью флуоресцентной микроскопии. (б) Отдельное наложения спектров ЯМР 2 H показывают, что жидкокристаллические (Lα) и жидкой упорядоченной (Lo) фазы сосуществуют в липосомах. Veatch SL, Keller SL. Seeing spots: complex phase behavior in simple membranes. Biochim Biophys Acta. 2005 Dec 30; 1746(3): 172 -85
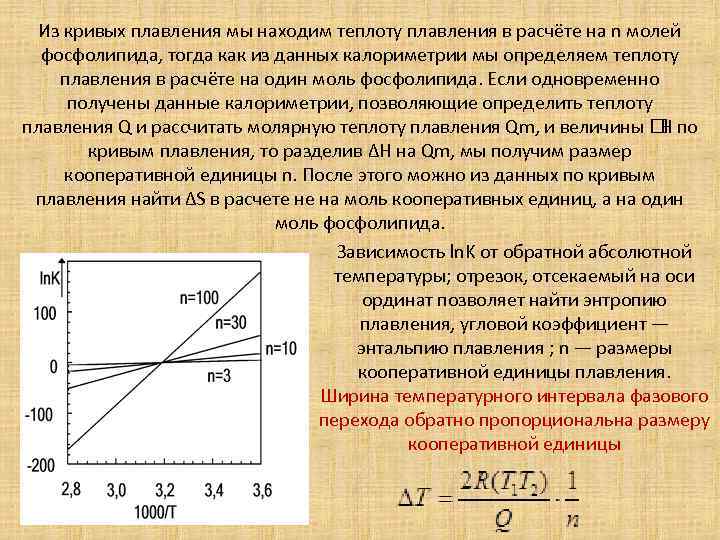
Из кривых плавления мы находим теплоту плавления в расчёте на n молей фосфолипида, тогда как из данных калориметрии мы определяем теплоту плавления в расчёте на один моль фосфолипида. Если одновременно получены данные калориметрии, позволяющие определить теплоту плавления Q и рассчитать молярную теплоту плавления Qm, и величины по H кривым плавления, то разделив ΔH на Qm, мы получим размер кооперативной единицы n. После этого можно из данных по кривым плавления найти ΔS в расчете не на моль кооперативных единиц, а на один моль фосфолипида. Зависимость ln. K от обратной абсолютной температуры; отрезок, отсекаемый на оси ординат позволяет найти энтропию плавления, угловой коэффициент — энтальпию плавления ; n — размеры кооперативной единицы плавления. Ширина температурного интервала фазового перехода обратно пропорциональна размеру кооперативной единицы
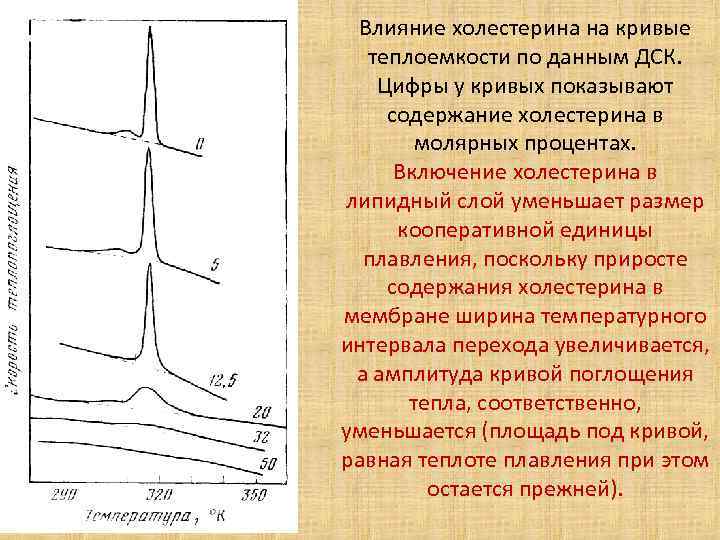
Влияние холестерина на кривые теплоемкости по данным ДСК. Цифры у кривых показывают содержание холестерина в молярных процентах. Включение холестерина в липидный слой уменьшает размер кооперативной единицы плавления, поскольку приросте содержания холестерина в мембране ширина температурного интервала перехода увеличивается, а амплитуда кривой поглощения тепла, соответственно, уменьшается (площадь под кривой, равная теплоте плавления при этом остается прежней).

Холестерин обладает пластифицирующим действием на липидный бислой: 1) Нарушает кооперативный характер фазовых переходов; 2) Твёрдые мембраны холестерин разжижает; 3) Жидкие становятся более вязкими.
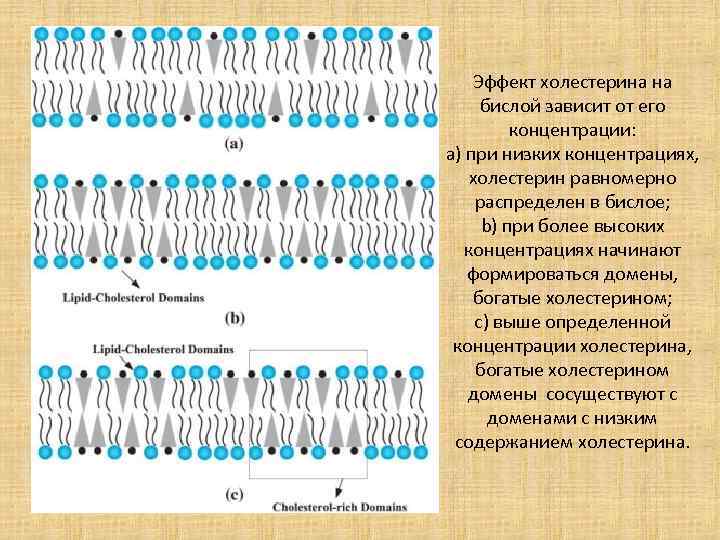
Эффект холестерина на бислой зависит от его концентрации: а) при низких концентрациях, холестерин равномерно распределен в бислое; b) при более высоких концентрациях начинают формироваться домены, богатые холестерином; с) выше определенной концентрации холестерина, богатые холестерином домены сосуществуют с доменами с низким содержанием холестерина.

Antonov VF, Petrov VV, Molnar AA, Predvoditelev DA, Ivanov AS. The appearance of single-ion channels in unmodified lipid bilayer membranes at the phase transition temperature. Nature. 1980 Feb 7; 283(5747): 585 -6. В 1980 г. В. Ф. Антонов с Валерий Федорович Антонов, доктор соавторами показал, что в точке биологических наук, профессор, зав. кафедрой медицинской и фазового перехода липидная биологической физики Московской мембрана теряет свои медицинской академии им. И. М. барьерные функции. Сеченова. Область научных интересов биофизика мембран. Автор более 200 Работа была выполнена на каф. научных статей, двух монографий, а биофизики МБФ 2 -го МОЛГМИ им. Н. И. также учебных программ и учебных Пирогова пособий по биофизике для студентов медицинских специальностей.
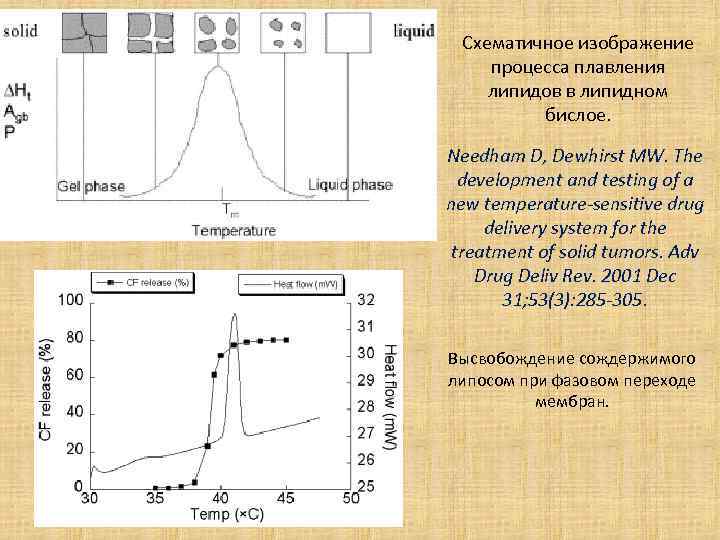
Схематичное изображение процесса плавления липидов в липидном бислое. Needham D, Dewhirst MW. The development and testing of a new temperature-sensitive drug delivery system for the treatment of solid tumors. Adv Drug Deliv Rev. 2001 Dec 31; 53(3): 285 -305. Высвобождение сождержимого липосом при фазовом переходе мембран.

Схема строения рогового слоя (верхняя часть рисунка) и мембраны ламеллярных слоёв (нижняя часть рисунка) Если температура фазового перехода (плавления) фосфолипидов лежит в области температур близких к 0 о С, то у длинноцепочечных сфинголипидов мембран рогового слоя она лежит в диапазоне 65 -70 о С и при нагревании выше 70 о С электрическое сопротивление мембран резко снижается, становясь таким, как в локальных областях транспорта при электропорации. С точки зрения потери барьерных свойств мембран в точке фазового перехода становится понятным, почему мембраны рогового слоя состоят из «тугоплавких» церамидов. Если бы они состояли из фосфолипидов, то взяв в руки льдышку, локально охлаждающую кожу до температур близких к нулевой, мембраны рогового слоя потеряли бы свои барьерные свойства при фазовом переходе, который у фосфолипидов близок к температурам около нуля.

Живые организмы, обитающие в разных климатических условиях, имеют различное соотношение насыщенных и ненасыщенных связей в молекулах липидов, что обеспечивает им приспособление к холоду или жаре в зависимости от среды их обитания. Более того, это соотношение меняется для разных участков тела одного и того же организма. Например, температура ноги возле копыта полярного оленя может составлять -20 °С, а температура ноги возле туловища достигает +30 °С. Однако клеточные мембраны не претерпевают фазовый переход за счет того, что мембраны клеток возле копыта содержат больше ненасыщенных липидов, а возле туловища — больше насыщенных.

В крупных городах участились случаи заболеваний туберкулезом среди высокообеспеченных женщин. Разбираясь в причинах этого явления, диетологи выяснили, что это явление наблюдалось у тех, кто исключил из своей диеты сливочное масло, заменив его исключительно оливковым. К сожалению, эти женщины не учли того факта, что насыщенные жирные кислоты, которыми богато сливочное масло, являются необходимыми компонентами легочного сурфактанта – тонкой пленки, которая выстилает альвеолы изнутри и контактирует с воздухом. Значение сурфактанта состоит в том, что, уменьшая поверхностное натяжение, он предотвращает слипание альвеол во время выдоха. Кроме того, он обладает бактерицидным действием и не дает возможности микроорганизмам проникать из воздуха через стенку альвеолы. Если не хватает насыщенных жирных кислот, то функциональная активность сурфактанта снижена, и бактерии из воздуха легко проникают в легкие.
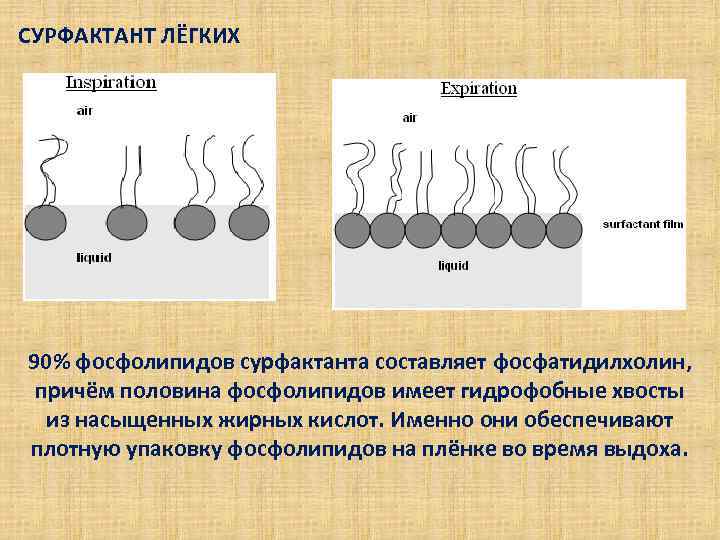
СУРФАКТАНТ ЛЁГКИХ 90% фосфолипидов сурфактанта составляет фосфатидилхолин, причём половина фосфолипидов имеет гидрофобные хвосты из насыщенных жирных кислот. Именно они обеспечивают плотную упаковку фосфолипидов на плёнке во время выдоха.
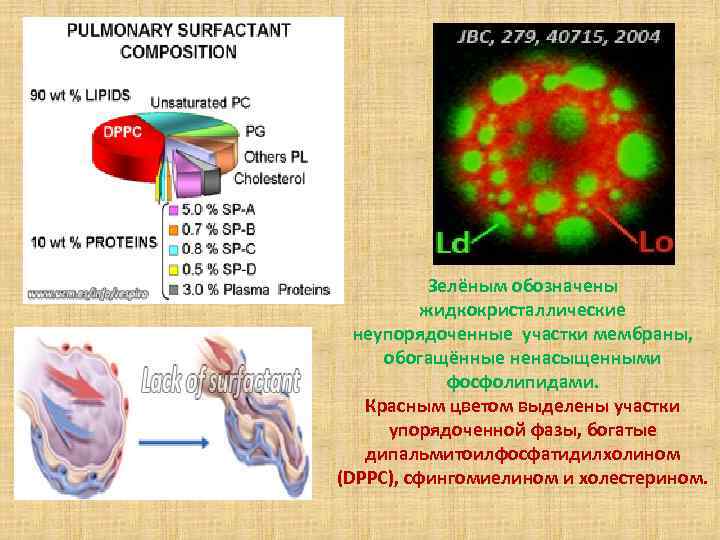
Зелёным обозначены жидкокристаллические неупорядоченные участки мембраны, обогащённые ненасыщенными фосфолипидами. Красным цветом выделены участки упорядоченной фазы, богатые дипальмитоилфосфатидилхолином (DPPC), сфингомиелином и холестерином.
Фазовые переходы.pptx