презентация. химия.pptx
- Количество слайдов: 15
 H 2 O Вода (оксид водорода) — химическое вещество в виде прозрачной жидкости, не имеющей цвета (в малом объёме), запаха и вкуса (при нормальных условиях). Химическая формула: Н 2 O. В твёрдом состоянии называется льдом или снегом, а в газообразном — водяным паром. Около 71 % поверхности Земли покрыто водой (океаны, моря, озёра, реки, лёд). Является хорошим сильнополярным растворителем. В природных условиях всегда содержит растворённые вещества (соли, газы). Вода имеет ключевое значение в создании и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и погоды.
H 2 O Вода (оксид водорода) — химическое вещество в виде прозрачной жидкости, не имеющей цвета (в малом объёме), запаха и вкуса (при нормальных условиях). Химическая формула: Н 2 O. В твёрдом состоянии называется льдом или снегом, а в газообразном — водяным паром. Около 71 % поверхности Земли покрыто водой (океаны, моря, озёра, реки, лёд). Является хорошим сильнополярным растворителем. В природных условиях всегда содержит растворённые вещества (соли, газы). Вода имеет ключевое значение в создании и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и погоды.
 Вода на Земле может существовать в трёх основных состояниях — жидком, газообразном и твёрдом и приобретать различные формы, которые могут одновременно соседствовать друг с другом.
Вода на Земле может существовать в трёх основных состояниях — жидком, газообразном и твёрдом и приобретать различные формы, которые могут одновременно соседствовать друг с другом.
 По особенностям происхождения, состава или применения, выделяют, в числе прочего: Мягкая вода и жёсткая вода — по содержанию катионов кальция и магния По изотопам молекулы: Лёгкая вода (по составу почти соответствует обычной) Тяжёлая вода (дейтериевая) Сверхтяжёлая вода (тритиевая) Талая вода Пресная вода Дождевая вода Морская вода Подземные воды Минеральная вода Солоноватая вода Питьевая вода, Водопроводная вода Дистиллированная вода и деионизированная вода Сточные воды Ливневая вода или поверхностные воды Мёртвая вода и Живая вода — виды воды из сказок (со сказочными свойствами) Святая вода — особый вид воды согласно религиозным учениям Поливода Структурированная вода — термин, применяемый в различных неакадемических теориях.
По особенностям происхождения, состава или применения, выделяют, в числе прочего: Мягкая вода и жёсткая вода — по содержанию катионов кальция и магния По изотопам молекулы: Лёгкая вода (по составу почти соответствует обычной) Тяжёлая вода (дейтериевая) Сверхтяжёлая вода (тритиевая) Талая вода Пресная вода Дождевая вода Морская вода Подземные воды Минеральная вода Солоноватая вода Питьевая вода, Водопроводная вода Дистиллированная вода и деионизированная вода Сточные воды Ливневая вода или поверхностные воды Мёртвая вода и Живая вода — виды воды из сказок (со сказочными свойствами) Святая вода — особый вид воды согласно религиозным учениям Поливода Структурированная вода — термин, применяемый в различных неакадемических теориях.
 Химические названия воды С формальной точки зрения вода имеет несколько различных корректных химических названий: Оксид водорода Гидроксид водорода Монооксид дигидрогена Гидроксильная кислота англ. hydroxic acid Оксидан Дигидромонооксид
Химические названия воды С формальной точки зрения вода имеет несколько различных корректных химических названий: Оксид водорода Гидроксид водорода Монооксид дигидрогена Гидроксильная кислота англ. hydroxic acid Оксидан Дигидромонооксид
 Оксид углерода Оксид углерода(IV) (углекислый газ, диоксид углерода, двуокись углерода, угольный ангидрид) — CO 2, бесцветный газ, без запаха, со слегка кисловатым вкусом. Плотность при нормальных условиях 1, 97 кг/м³. При атмосферном давлении диоксид углерода не существует в жидком состоянии, переходя непосредственно из твёрдого состояния в газообразное. Твёрдый диоксид углерода называют сухим льдом. При повышенном давлении и обычных температурах углекислый газ переходит в жидкость, что используется для его хранения. В природе. Один из распространенных оксидов – диоксид углерода CO 2 – содержится в составе вулканических газов.
Оксид углерода Оксид углерода(IV) (углекислый газ, диоксид углерода, двуокись углерода, угольный ангидрид) — CO 2, бесцветный газ, без запаха, со слегка кисловатым вкусом. Плотность при нормальных условиях 1, 97 кг/м³. При атмосферном давлении диоксид углерода не существует в жидком состоянии, переходя непосредственно из твёрдого состояния в газообразное. Твёрдый диоксид углерода называют сухим льдом. При повышенном давлении и обычных температурах углекислый газ переходит в жидкость, что используется для его хранения. В природе. Один из распространенных оксидов – диоксид углерода CO 2 – содержится в составе вулканических газов.
 Углекислый газ легко пропускает ультрафиолетовые лучи и лучи видимой части спектра, которые поступают на Землю от Солнца и обогревают её. В то же время он поглощает испускаемые Землёй инфракрасные лучи и является одним из парниковых газов, вследствие чего принимает участие в процессе глобального потепления. Постоянный рост уровня содержания этого газа в атмосфере наблюдается с начала индустриальной эпохи. Монооксид углерода в атмосфере Земли
Углекислый газ легко пропускает ультрафиолетовые лучи и лучи видимой части спектра, которые поступают на Землю от Солнца и обогревают её. В то же время он поглощает испускаемые Землёй инфракрасные лучи и является одним из парниковых газов, вследствие чего принимает участие в процессе глобального потепления. Постоянный рост уровня содержания этого газа в атмосфере наблюдается с начала индустриальной эпохи. Монооксид углерода в атмосфере Земли
 Химические свойства По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует угольную кислоту. Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов. Вступает в реакции электрофильного замещения (например, с фенолом ) и нуклеофильного присоединения (например, с магнийорганическими соединениями).
Химические свойства По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует угольную кислоту. Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов. Вступает в реакции электрофильного замещения (например, с фенолом ) и нуклеофильного присоединения (например, с магнийорганическими соединениями).
 Биологические свойства Диоксид углерода играет одну из главных ролей в живой природе, участвуя во многих процессах метаболизма живой клетки. Диоксид углерода получается в результате множества окислительных реакций у животных, и выделяется в атмосферу с дыханием. Углекислый газ атмосферы — основной источник углерода для растений. Однако, ошибкой будет утверждение, что животные только выделяют углекислый газ, а растения — только поглощают его. Растения поглощают углекислый газ в процессе фотосинтеза, а без освещения они тоже его выделяют. Диоксид углерода не токсичен, но не поддерживает дыхание. Большая концентрация в воздухе вызывает удушье (см. Гиперкапния). Недостаток углекислого газа тоже опасен (см. Гипокапния) Углекислый газ в организмах животных имеет и физиологическое значение, например, участвует в регуляции сосудистого тонуса
Биологические свойства Диоксид углерода играет одну из главных ролей в живой природе, участвуя во многих процессах метаболизма живой клетки. Диоксид углерода получается в результате множества окислительных реакций у животных, и выделяется в атмосферу с дыханием. Углекислый газ атмосферы — основной источник углерода для растений. Однако, ошибкой будет утверждение, что животные только выделяют углекислый газ, а растения — только поглощают его. Растения поглощают углекислый газ в процессе фотосинтеза, а без освещения они тоже его выделяют. Диоксид углерода не токсичен, но не поддерживает дыхание. Большая концентрация в воздухе вызывает удушье (см. Гиперкапния). Недостаток углекислого газа тоже опасен (см. Гипокапния) Углекислый газ в организмах животных имеет и физиологическое значение, например, участвует в регуляции сосудистого тонуса
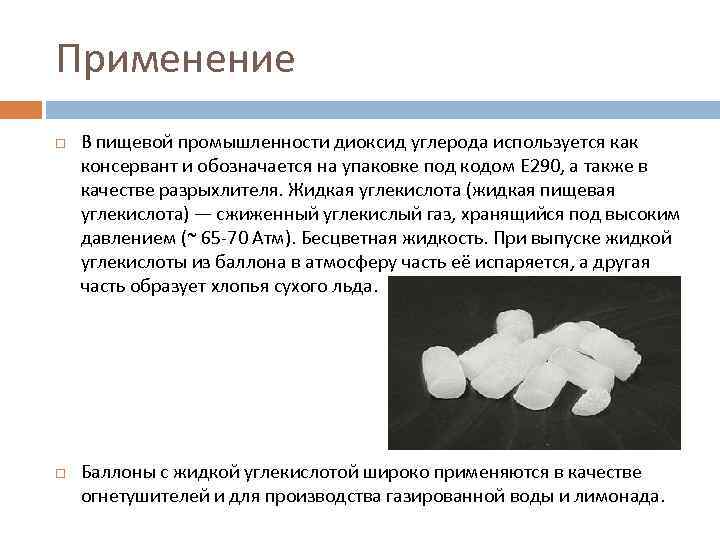 Применение В пищевой промышленности диоксид углерода используется как консервант и обозначается на упаковке под кодом Е 290, а также в качестве разрыхлителя. Жидкая углекислота (жидкая пищевая углекислота) — сжиженный углекислый газ, хранящийся под высоким давлением (~ 65 -70 Атм). Бесцветная жидкость. При выпуске жидкой углекислоты из баллона в атмосферу часть её испаряется, а другая часть образует хлопья сухого льда. Баллоны с жидкой углекислотой широко применяются в качестве огнетушителей и для производства газированной воды и лимонада.
Применение В пищевой промышленности диоксид углерода используется как консервант и обозначается на упаковке под кодом Е 290, а также в качестве разрыхлителя. Жидкая углекислота (жидкая пищевая углекислота) — сжиженный углекислый газ, хранящийся под высоким давлением (~ 65 -70 Атм). Бесцветная жидкость. При выпуске жидкой углекислоты из баллона в атмосферу часть её испаряется, а другая часть образует хлопья сухого льда. Баллоны с жидкой углекислотой широко применяются в качестве огнетушителей и для производства газированной воды и лимонада.
 Методы регистраций Измерение парциального давления углекислого газа требуется в технологических процессах, в медицинских применениях — анализ дыхательных смесей при искусственной вентиляции лёгких и в замкнутых системах жизнеобеспечения. Анализ концентрации CO 2 в атмосфере используется для экологических и научных исследований, для изучения парникового эффекта.
Методы регистраций Измерение парциального давления углекислого газа требуется в технологических процессах, в медицинских применениях — анализ дыхательных смесей при искусственной вентиляции лёгких и в замкнутых системах жизнеобеспечения. Анализ концентрации CO 2 в атмосфере используется для экологических и научных исследований, для изучения парникового эффекта.
 Оксид кремния Кремний - второй по распространенности (после кислорода) элемент земной коры. В верхних осадочных слоях он содержится в виде глин, кварца и других соединений и составляет 27, 6% состава земной коры. В чистом виде кремний в природе не встречается. Наиболее распространен оксид кремния и силикаты. Первый встречается в виде минерала кварца (кремнезем, кремень). В природе из этого соединения сложены целые горы. Попадаются очень крупные, до 40 т кристаллы кварца. Обычный песок состоит из мелкого кварца с различными примесями. Песок - оксид кремния(IV)
Оксид кремния Кремний - второй по распространенности (после кислорода) элемент земной коры. В верхних осадочных слоях он содержится в виде глин, кварца и других соединений и составляет 27, 6% состава земной коры. В чистом виде кремний в природе не встречается. Наиболее распространен оксид кремния и силикаты. Первый встречается в виде минерала кварца (кремнезем, кремень). В природе из этого соединения сложены целые горы. Попадаются очень крупные, до 40 т кристаллы кварца. Обычный песок состоит из мелкого кварца с различными примесями. Песок - оксид кремния(IV)
 Чистый оксид кремния (IV) находится в природе в виде горного хрусталя, кристаллы которого достигают иногда больших размеров. Самый крупный кристалл, найденный в Казахстане, весил 70 т. Горный хрусталь - совершенно прозрачные кристаллы кварца. В зависимости от примесей он может приобретать различную окраску. Так, оксиды марганца и железа дают фиолетовый оттенок. Это аметист. Желтоватый хрусталь - цитрин, дымчатый - раухтопаз. В нем могут находится и различные включения. Кошачий глаз включает в себя волокнистые материалы, «стрелы Амура» - включения оксида титана. Горный хрусталь - это бесцветный прозрачный кварц, оксид кремния.
Чистый оксид кремния (IV) находится в природе в виде горного хрусталя, кристаллы которого достигают иногда больших размеров. Самый крупный кристалл, найденный в Казахстане, весил 70 т. Горный хрусталь - совершенно прозрачные кристаллы кварца. В зависимости от примесей он может приобретать различную окраску. Так, оксиды марганца и железа дают фиолетовый оттенок. Это аметист. Желтоватый хрусталь - цитрин, дымчатый - раухтопаз. В нем могут находится и различные включения. Кошачий глаз включает в себя волокнистые материалы, «стрелы Амура» - включения оксида титана. Горный хрусталь - это бесцветный прозрачный кварц, оксид кремния.
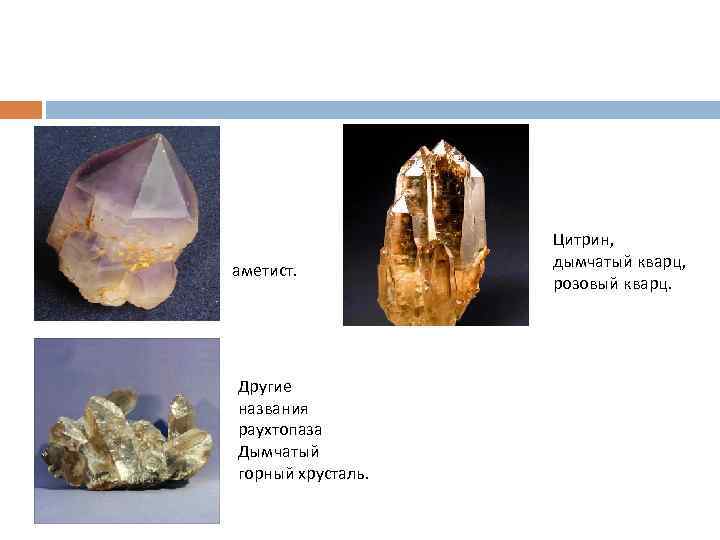 аметист. Другие названия раухтопаза Дымчатый горный хрусталь. Цитрин, дымчатый кварц, розовый кварц.
аметист. Другие названия раухтопаза Дымчатый горный хрусталь. Цитрин, дымчатый кварц, розовый кварц.
 Анализ лунного грунта показал присутствие оксида кремния (IV) в количестве более 40%. В составе каменных метеоритов содержание кремния достигает 20%. Оксид кремния - кремень - сыграл важную роль в истории развития человечества. Именно с кремневых наконечников копий, ножей и топориков начинается истории большинства народов. Позже кремень стал источником огня - путешественники никуда не отправлялись без огнива. А глиняные дома, посуда, предметы быта! Трудно сказать, как бы развивался мир без стекла. В наши дни все более необходим становится чистый кремний, как полупроводник. Так называемые «девять девяток чистоты» - 99, 9999999% чистого кремния - первое требование к полупроводнику. Ни один из современных компьютеров не существовал бы без кремния. Тоже можно сказать и о ряде других технических средств. Велико значение различных веществ, основой которых являются соединения кремния. Это бетон, керамики, стекло.
Анализ лунного грунта показал присутствие оксида кремния (IV) в количестве более 40%. В составе каменных метеоритов содержание кремния достигает 20%. Оксид кремния - кремень - сыграл важную роль в истории развития человечества. Именно с кремневых наконечников копий, ножей и топориков начинается истории большинства народов. Позже кремень стал источником огня - путешественники никуда не отправлялись без огнива. А глиняные дома, посуда, предметы быта! Трудно сказать, как бы развивался мир без стекла. В наши дни все более необходим становится чистый кремний, как полупроводник. Так называемые «девять девяток чистоты» - 99, 9999999% чистого кремния - первое требование к полупроводнику. Ни один из современных компьютеров не существовал бы без кремния. Тоже можно сказать и о ряде других технических средств. Велико значение различных веществ, основой которых являются соединения кремния. Это бетон, керамики, стекло.
 Применение Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках. Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87 % массы литосферы. Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E 551, препятствующего слёживанию и комкованию, парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство Фармакопей), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента. Искусственно полученные плёнки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов. Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов. Кремнезёмная нить также используется в нагревательных элементах электронных сигарет, так как хорошо впитывает жидкость и не разрушается под нагревом спирали.
Применение Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках. Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87 % массы литосферы. Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E 551, препятствующего слёживанию и комкованию, парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство Фармакопей), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента. Искусственно полученные плёнки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов. Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов. Кремнезёмная нить также используется в нагревательных элементах электронных сигарет, так как хорошо впитывает жидкость и не разрушается под нагревом спирали.


