Антибиотики 2.ppt
- Количество слайдов: 123


Группа антибактериальных препаратов является самой большой по числу ЛС, которые разделены на подгруппы по химическому строению: Бета-лактамы (имеют в своей структуре беталактамное кольцо), макролиды (имеют макроциклические лактонное кольцо), аминогликозиды (аминосахара, соединенные гликозидной связью с агликоновым фрагментом) и т. п. На химическое строение указывают названия других групп (тетрациклины, диаминопиримидины, хиноксалины, оксазолидиноны и др. ). Группа "другие лекарственные средства" состоит из отдельных препаратов разного химического строения.

АКТУАЛЬНОСТЬ ü Более половины всех используемых в настоящее время в мире антибиотиков составляют беталактамы. лактамы ü Бета-лактамы - основа современной химиотерапии, т. к. занимают ведущее или важное место в лечении большинства инфекций. ü Их объединяют в одну группу, т. к. важнейшая часть их молекулы, от которой зависит антимикробная активность, реакционно-способное четырехчленное бета-лактамное кольцо (циклический амид).
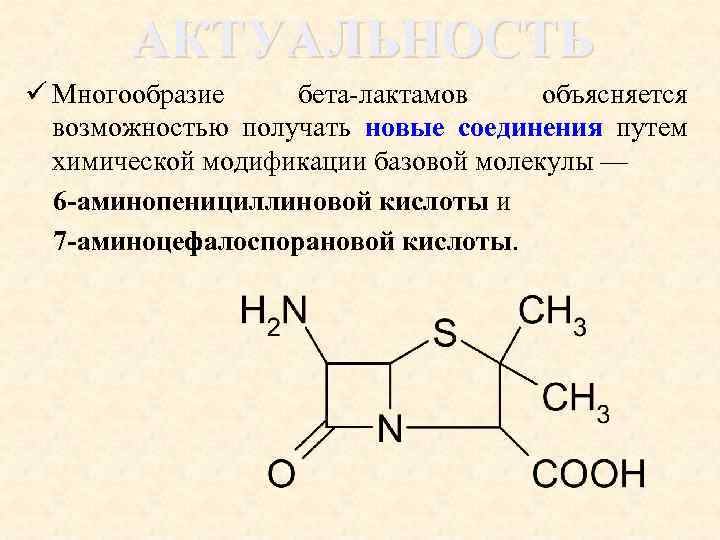
АКТУАЛЬНОСТЬ ü Многообразие бета-лактамов объясняется возможностью получать новые соединения путем химической модификации базовой молекулы — 6 -аминопенициллиновой кислоты и 7 -аминоцефалоспорановой кислоты.

1) 2) 3) 4) 5) 6) 7) 8) 9) 10) Пенициллины (пенамы); Цефалоспорины (цефемы); Монобактамы; Карбапенемы (тиенамицин); Цефамицины; Оксацефемы; Пенемы; Клавуланаты; Нокардицины; Комбинированные средства. 5

БЕТА-ЛАКТАМЫ 1 • ПЕНИЦИЛЛИНЫ 2 • ЦЕФАЛОСПОРИНЫ 3 • МОНОБАКТАМЫ 4 • КАРБАПЕНЕМЫ 6

7

ЛАКТАМЫ - это циклические амиды, образующиеся при перегруппировке оксимов циклических кетонов, что сопровождается расширением цикла (аминокислоты с удаленными функциональными группами). 8

Бета-лактамы – это четырехчленные циклические амиды или оксопроизводные азотсодержащих гетероциклов. Бета-лактамное кольцо 9

Бета-лактамное кольцо получило свое название в виду того, что при его образовании происходит замыкание связи между углеродом арбоксильной к группы аминокислоты и азотом аминогруппы, находящейся при бетауглеродном атоме. 10

11

ПОЛУЧЕНИЕ БЕТА-ЛАКТАМОВ 12

Поиск и получение новых бета-лактамных антибиотиков осуществляется путем направленной модификации беталактамов, связанной с введением заместителей, изменяющих определенные свойства природного или синтетического аналога. ПОЛУЧЕНИЕ ПОЛУСИНТЕТИЧЕСКИХ СРЕДСТВ 13

14
В результате жизнедеятельности плесневых грибов образуются различные пенициллины (G, F, К, X, V). Наиболее активным и устойчивым во внешней среде является бензилпенициллин (пенициллин G — в лактамном кольце содержится бензильная группа). 15

Антимикробная активность Бета-лактамов 16

ШИРОКИЙ СПЕКТР АНТИМИКРОБНОЙ АКТИВНОСТИ 17

Грамположительные микроорганизмы

Грамположительные микроорганизмы Большинство бета-лактамов высоко активны в отношении грамположительных микроорганизмов. Единственное исключение – группа монобактамов. 19

Грамположительные Streptococcus spp микроорганизмы Streptococcus spp. высоко чувствительны к бета-лактамам. Наиболее активны природные пенициллины, что делает их ЛС выбора при лечении стрептококковых инфекций. Сравнительно мало активны оксациллин и карбоксипенициллины. Активность других представителей полусинтетических пенициллинов и цефалоспоринов различается, но нет оснований считать эти различия клинически значимыми.

Грамположительные Streptococcus spp микроорганизмы Не обнаружено ни одного штамма Str. pyogenes, устойчивого к пенициллину и к другим беталактамам. Резистентность других стрептококков часто подвержена значительным колебаниям. Во всех случаях она связана с модификацией ПСБ; продукции бета-лактамаз у стрептококков не выявлено. 21

Грамположительные Streptococcus spp микроорганизмы Отмечается тенденция к повышению частоты устойчивости к пенициллину среди стрептококков групп В и viridans, но такие штаммы остаются весьма редкими. 22

Грамположительные микроорганизмы Pn Наибольшее практическое значение имеют пенициллинрезистентные пневмококки В отдельных регионах Испании, Франции, Венгрии частота устойчивости достигает 60%. В РФ распространение устойчивости пневмококков к пенициллину невелико (около 10%). Кроме того, умеренная устойчивость пневмококков к пенициллину не сопровождается клиническим неуспехом при лечении бета-лактамами.

Грамположительные микроорганизмы Str. pn. Предсказать чувствительность или устойчивость пенициллинрезистентных пневмококков к другим бета-лактамам достаточно сложно: часто активность сохраняют цефалоспорины III поколения, практически всегда активны цефалоспорины IV поколения и карбапенемы. Полусинтетические пенициллины и цефалоспорины I-II поколения чаще всего неактивны.

Грамположительные микроорганизмы Поскольку резистентность у стрептококков / пневмококков не связана с продукцией беталактамаз, ингибиторзащищенные беталактамы не имеют преимуществ. 25

Грамположительные Enterococcus spp. микроорганизмы Enterococcus spp. значительно менее чувствительны к бета-лактамам, чем другие Гр(+) микроорганизмы, что связано с пониженной аффинностью ПСБ к этим антибиотикам. Энтерококкам свойственны выраженные межвидовые различия в чувствительности к бета-лактамам, наибольшую чувствительность имеет Е. faecalis. Природно устойчивы к бета-лактамам Е. faecium и другие виды энтерококков — они синтезируют большое количество ПСБ пятого типа с низкой аффинностью к этим антибиотикам. 26

Грамположительные Enterococcus spp. микроорганизмы Из всех бета-лактамов клинически значимой антиэнтерококковой активностью (в отношении Е. faecalis) обладают природные пенициллины, амино-, уреидопенициллины и карбапенемы. ЛС выбора для лечения энтерококковых (Е. faecalis) инфекций являются аминопенициллины. Цефалоспорины реальной активностью не обладают. У бета-лактамов отмечается бактериостатическая активность лишь в отношении Е. faecalis, а бактерицидное действие проявляется только при комбинации с аминогликозидами. 27

Грамположительные микроорганизмы Staphylococcus spp. (S. aureus и коагулазонегативные стафилококки) от природы высоко чувствительны к бета-лактамам, наименьшие значения МПК имеют природные пенициллины и аминопенициллины. В ряду цефалоспоринов от I к III поколению наблюдается некоторое снижение активности, хотя реального клинического значения это не имеет. Исключением являются пероральные цефалоспорины III поколения — цефиксим и цефтибутен, — практически лишенные антистафилококковой активности. 28

Грамположительные микроорганизмы Staphylococcus spp. Стафилококки оказались первыми микроорганизмами, чья приобретенная резистентность привела к резкому снижению эффективности терапии. Менее чем через 10 лет после внедрения в клиническую практику бензилпенициллина частота резистентности к этому антибиотику в отдельных стационарах достигала 50%, а в настоящее время практически повсеместно, в том числе и в России, устойчивость даже внебольничных штаммов превышает 80%. 29

Грамположительные Staphylococcus spp. микроорганизмы Резистентность Устойчивость связана с продукцией плазмидных бета-лактамаз. Пути преодоления резистентности: ü Создание полусинтетических изоксозолинпенициллинов (метициллина, оксациллина), ü а также цефалоспориновых антибиотиков, устойчивых к ферментативному гидролизу. 30

Грамположительные микроорганизмы Staphylococcus spp. Разрушаются St бета-лактамазами: ü Аминопенициллины, ü Карбоксипенициллины, ü Уреидопенициллины, ü Природные пенициллины, ü Иногда наблюдается частичный гидролиз цефалоспоринов I поколения. Стафилококковые бета-лактамазы эффективно подавляются ингибиторами, что обеспечивает высокую активность защищенных пенициллинов.

Грамположительные микроорганизмы Staphylococcus spp. В 1961 г. появились первые сообщения о г. выделении метициллинрезистентных стафилококков (MRSA). стафилококков MRSA Резистентность оказалась связанной с появлением нового ПСБ (ПСБ 2 и ПСБ 2 а), отсутствующего у чувствительных штаммов и обладающего пониженной аффинностью ко всем бета-лактамам.

Грамположительные микроорганизмы Staphylococcus spp. Поскольку для установления метициллинрезистентности обычно используют оксациллин (он более стабилен при хранении), появился равнозначный термин "оксациллинрезистентность". оксациллинрезистентность

Грамположительные микроорганизмы Staphylococcus spp. При исследованиях in vitro в отношении некоторых штаммов MRSA цефалоспорины и карбапенемы цефалоспорины карбапенемы иногда проявляют достаточно высокую активность. Формально по величине МПК или диаметру зоны ингибирования роста такие штаммы следует считать чувствительными. Тем не менее клинические исследования показали, что при метициллинрезистентности эффективность всех бета-лактамов существенно снижается независимо от их активности in vitro.

Грамположительные микроорганизмы Staphylococcus spp. Следовательно, при определении устойчивости к оксациллину у стафилококков ни один беталактамный антибиотик (независимо от активности in vitro) не может быть рекомендован для лечения.

Грамположительные микроорганизмы Staphylococcus spp. Оценка чувствительности к оксациллину остается ключевой в планировании терапии стафилококковых инфекций. При инфекциях, вызванных штаммами, чувствительными к оксациллину, оксациллин является ЛС выбора. Практически равную эффективность будут проявлять защищенные пенициллины, цефалоспорины (цефалоспорины III и IV поколений несколько более высокую эффективность, чем ЛС III поколения) и карбапенемы. При выявлении оксациллинрезистентных штаммов применение любых бета-лактамов должно быть исключено.

Грамотрицательные микроорганизмы

Грамотрицательные микроорганизмы Грамотрицательные кокки Ø Neisseria meningitides, Ø N. gonorrhoeae, Ø Moxarella (Branhamella) catarrhalis 38

Neisseria meningitides, N. gonorrhoeae, Moxarella (Branhamella) catarrhalis имеют высокую природную чувствительность к бета-лактамам. Их внешняя мембрана проницаема не только для цефалоспоринов и полусинтетических пенициллинов, но и для природных пенициллинов (по этому признаку указанные микроорганизмы отличаются от других грамотрицательных). 39

Не действуют на: ü Облигатные и факультативные внутриклеточные микроорганизмы (риккетсии, хламидии, легионеллы, бруцеллы и др. ). Клиническая неэффективность при инфекциях, вызываемых этими микроорганизмами, связана с ограниченной способностью бета-лактамов проникать внутрь клетки макроорганизма, прежде всего внутрь фагоцитов, где локализуется возбудитель. 40

Не действуют на: ü Также устойчивы ко всем бета-лактамам метициллинрезистентные стафилококки. ü Кроме того, природной устойчивостью к беталактамам обладают микоплазмы. 41
ФАРМАКОЛОГИЯ ПЕНИЦИЛЛИНОВ 42

1 Классификация пенициллинов 43

I. Природные (биосинтетические): Короткого действия: ь Бензилпенициллина натриевая соль (пенициллин); ь Бензилпенициллина калиевая соль; ь Феноксиметилпенициллин; Длительного действия: ь Бензилпенициллинпрокаин (бензилпенициллина новокаиновая соль); ь Бензатин бензилпенициллин (бициллин-1, бициллин-5); 44

II. Полусинтетические: Ø Изоксазоилпенициллины (антистафилококковые, резистентные к беталактамазам, пенициллиназоустойчивые): оксациллин, нафциллин, клоксациллин, диклоксациллин; Ø Аминопенициллины (широкого спектра действия): ампициллин, амоксициллин; 45

Ш Карбоксипенициллины: карбенициллин, карфециллин, тикарциллин; Ш Уреидопенициллины: азлоциллин, мезлоциллин, пиперациллин; Антисинегнойные пенициллины 46

Ш Ингибиторозащищенные: «АУГМЕНТИН» • Амоксициллин / клавуланат «АМОКСИКЛАВ» • Амоксициллин / клавуланат «УНАЗИН» • Ампициллин / сульбактам «ТАЗОЦИН» • Пиперациллин / тазобактам «СУЛЬПЕРАЗОН» • Цефоперазон / сульбактам 47

Ш Комбинированные: Ампициллин / оксациллин. 48

Биосинтетические пенициллины Биосинтетические (природные) пенициллины получают из культуральной среды, на которой произрастают определенные штаммы плесневых грибов (Penicillium), являющиеся продуцентами пенициллина. 49

Полусинтетические пенициллины создаются путем ферментативного гидролиза плесневых грибов с последующей химической модификацией 6 -аминопенициллановой кислоты, являющейся структурной основой природных пенициллинов. 50

Действуют пенициллины бактерицидно, бактерицидно оказывая влияние только на делящиеся микроорганизмы Антибактериальное действие связано с нарушением синтеза клеточной стенки бактерий – препятствуют образованию пептидных связей (мишень действия – фермент транспептидаза). транспептидаза Для бактерий характерно необычайно высокое внутреннее давление, поэтому ослабление клеточной стенки приводит к ее разрыву и, соответственно, гибели микроорганизмов. 51

Бактерицидное действие На делящиеся микроорганизмы Мишень действия – транспептидаза

Пенициллин - природное вещество, продуцируемое разными видами плесневого гриба пенициллиума (Penicillium chrysogenum, notatum), а также стрептомицетами. В результате жизнедеятельности этих грибов образуются различные виды пенициллина. В производственных условиях бензилпенициллин получают на жидких питательных средах – в ферментаторах. 53

БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ Активность препаратов пенициллина определяют биологическим путем по антибактериальному действию на определенный штамм золотистого стафилококка. За одну единицу действия (1 ЕД) принимают ЕД активность 0, 5988 мкг химически чистой кристаллической натриевой соли бензилпенициллина. 54

2 ХИМИЧЕСКОЕ СТРОЕНИЕ ПЕНИЦИЛЛИНОВ
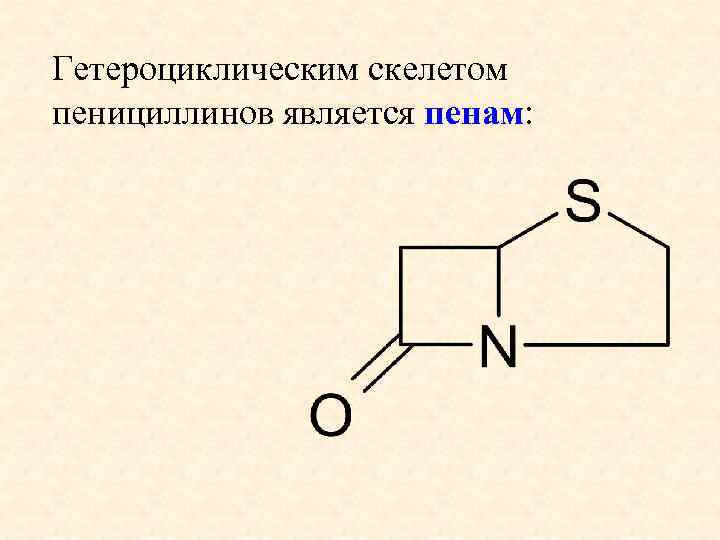
Гетероциклическим скелетом пенициллинов является пенам:
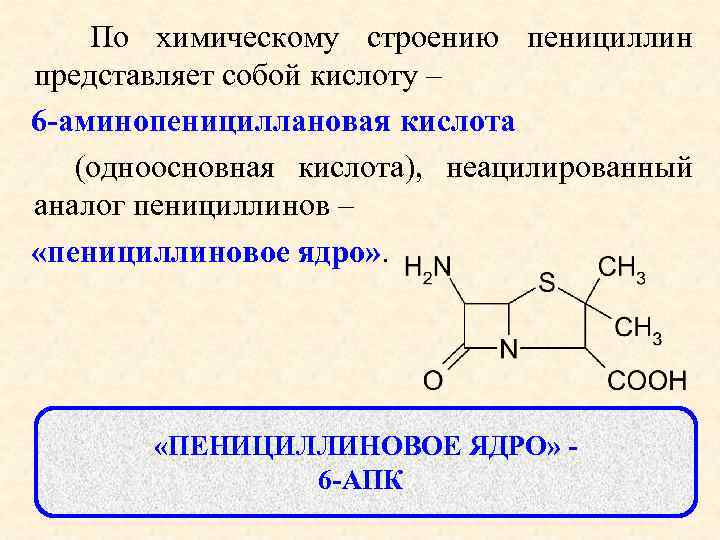
По химическому строению пенициллин представляет собой кислоту – 6 -аминопенициллановая кислота (одноосновная кислота), неацилированный аналог пенициллинов – «пенициллиновое ядро» . «ПЕНИЦИЛЛИНОВОЕ ЯДРО» 6 -АПК « 57
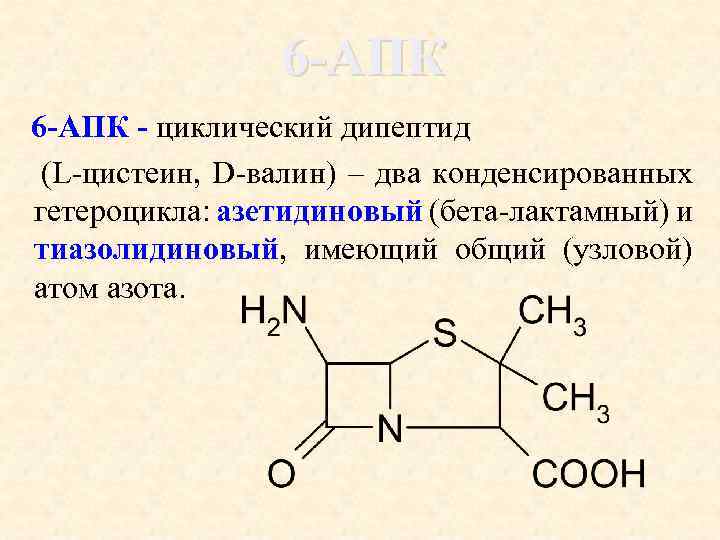
6 -АПК - циклический дипептид (L-цистеин, D-валин) – два конденсированных гетероцикла: азетидиновый (бета-лактамный) и тиазолидиновый, имеющий общий (узловой) атом азота.

3 МЕХАНИЗМ ДЕЙСТВИЯ ПЕНИЦИЛЛИНОВ 59

Пенициллины (и все другие бета-лактамы) обладают бактерицидным эффектом в отношении микроорганизмов, находящихся в фазе роста. Бета-лактамные антибиотики – полярные гидрофильные соединения, проникающие в клетки бактерий через пориновые каналы внешней мембраны. 60

Пориновые каналы Основной компонент внешней мембраны у грамотрицательных микроорганизмов – липополисахаридный слой, практически непроницаемый для экзогенных гидрофильных веществ (моно- и дисахаридов, аминокислот, коротких пептидов), транспорт их внутрь бактериальной клетки осуществляется через пориновые каналы. Пориновые каналы представляют собой воронкообразные белковые структуры (пориновые белки), встроенные в липополисахаридный слой.

Инактивация антибиотиков в периплазматическом пространстве клеточной стенки грамотрицательной бактерии. 1. Тример поринового белка. 2. Наружная клеточная оболочка. 3. Периплазматическое пространство. 4. Внутренняя мембрана. 5. Цитоплазма. 62

Мишень действия пенициллинов – пенициллиносвязывающие белки (ПСБ) бактерий, выполняющие роль ферментов (транспептидаз, карбоксипептидаз и эндопептидаз) на завершающем этапе синтеза пептидогликана – биополимера, являющегося основным компонентом клеточной стенки бактерий – образовании пептидогликановых цепей внутренней мембраны бактериальной клетки. Благодаря способности связываться с пенициллином, ферменты получили название пенициллинсвязывающие белки (ПСБ) 63
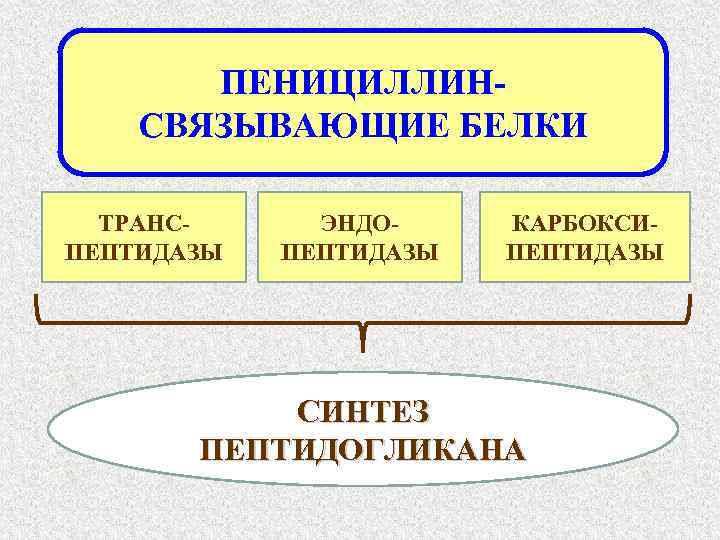
ПЕНИЦИЛЛИНСВЯЗЫВАЮЩИЕ БЕЛКИ ТРАНСПЕПТИДАЗЫ ЭНДОПЕПТИДАЗЫ КАРБОКСИПЕПТИДАЗЫ СИНТЕЗ ПЕПТИДОГЛИКАНА
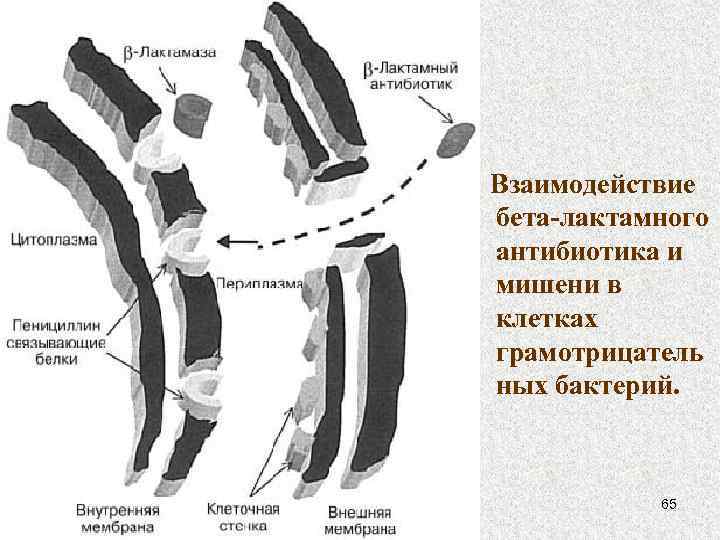
Взаимодействие бета-лактамного антибиотика и мишени в клетках грамотрицатель ных бактерий. 65

ПЕПТИДОГЛИКАН ü Обязательный компонент наружной мембраны прокариотических микроорганизмов (кроме микоплазм); ü Биологический полимер, состоящий из параллельных полисахаридных цепей; ü Пептидогликановый каркас приобретает жесткость при образовании между полисахаридными цепями поперечных сшивок. ü Поперечные сшивки образуются через аминокислотные мостики, замыкание сшивок осуществляют ферменты карбокси- и транспептидазы (ПСБ). 66

Поскольку пептидогликан и ПСБ отсутствуют у млекопитающих, специфическая токсичность в отношении макроорганизма для β-лактамов нехарактерна. БЕТА-ЛАКТАМЫ: низкая токсичность
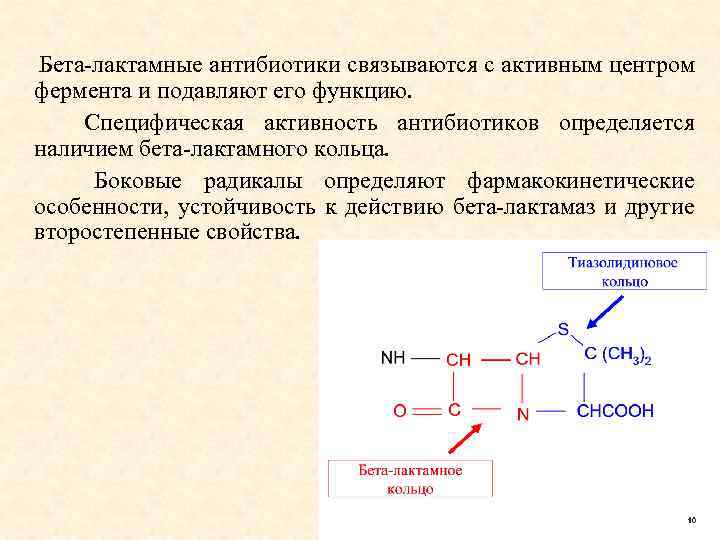
Бета-лактамные антибиотики связываются с активным центром фермента и подавляют его функцию. Специфическая активность антибиотиков определяется наличием бета-лактамного кольца. Боковые радикалы определяют фармакокинетические особенности, устойчивость к действию бета-лактамаз и другие второстепенные свойства. 68
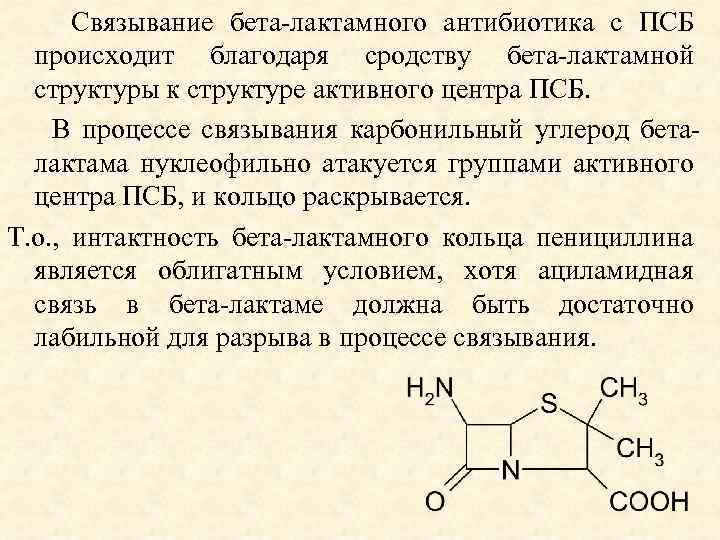
Связывание бета-лактамного антибиотика с ПСБ происходит благодаря сродству бета-лактамной структуры к структуре активного центра ПСБ. В процессе связывания карбонильный углерод беталактама нуклеофильно атакуется группами активного центра ПСБ, и кольцо раскрывается. Т. о. , интактность бета-лактамного кольца пенициллина является облигатным условием, хотя ациламидная связь в бета-лактаме должна быть достаточно лабильной для разрыва в процессе связывания.

Бактерицидная активность пенициллинов обусловлена: ü торможением синтеза ригидного слоя клеточной стенки; ü связыванием со специфическими рецепторами (ПСБ) ЦПМ; ü активацией аутолитических ферментов клеточной стенки. Все это справедливо лишь при условии роста микроорганизма (во время синтеза ригидной оболочки). 70

4 БЕТА-ЛАКТАМАЗЫ

Бета-лактамазы ü Причина приобретенной устойчивости (беталактамазный механизм резистентности микроорганизмов является наиболее действенным и распространенным); ü Расположены на наружной поверхности ЦПМ и/или в периплазматическом пространстве); ü Разрушают бета-лактамы до биологически неактивной пенициллановой кислоты (лишают способности выступать антибиотик в качестве ацилирующих агентов); ü Ингибиторы (клавуланат, сульбактам, тазобактам) необратимо подавляют активность бета-лактамаз. 72

Бета-лактамазы По локализации кодирующих их генов в микробной клетке • Хромосомные • Плазмидные По субстратной специфичности • Пенициллиназы, • Цефалоспориназы, • Бета-лактамазы широкого и расширенного спектра действия 73
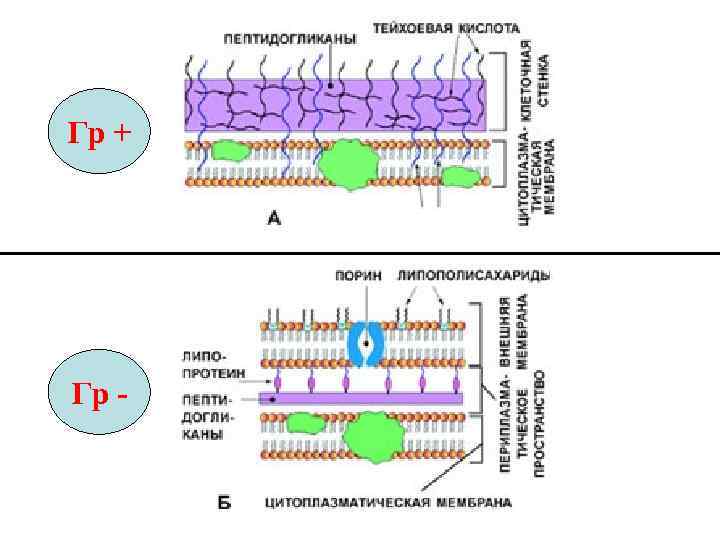
Гр + Гр -
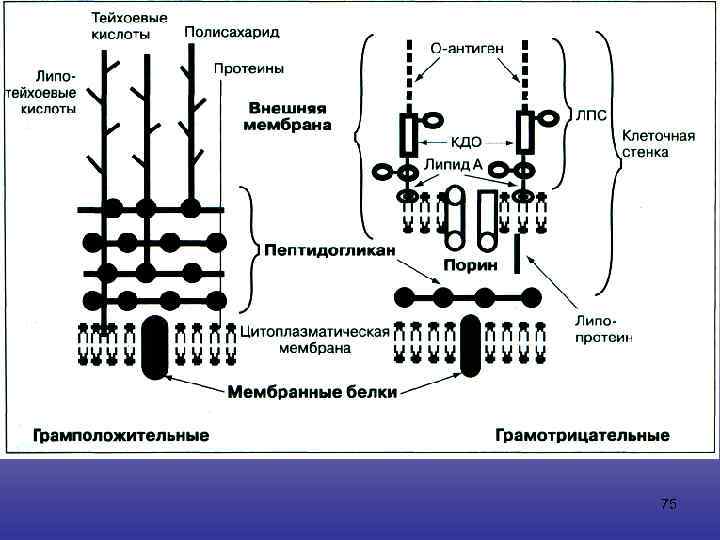
75

ЛОКАЛИЗАЦИЯ БЕТА-ЛАКТАМАЗ Грамположительные • Свободно диффундируют в окружающую бактерии среду Грамотрицательные • В периплазматичес ком пространстве 76

Бета-лактамазы расширенного спектра действия: Бактериальные ферменты, вырабатываемые микроорганизмами семейства Enterobacteriaceae (в основном K. pneumoniae, E. coli, реже другими энтеробактериями), способные инактивировать бета-лактамные антибиотики различных классов, включая пенициллины и цефалоспороины I-IV поколений, кроме цефамицинов (цефокситин, цефотетан) и карбапенемов. 77

Бета-лактамазы широкого спектра действия: Бактериальные ферменты, вырабатываемые в основном представителями семейства Enterobacteriaceae и некоторыми неферментирующими бактериями, способные инактивировать пенициллины, включая аминопенициллины, антисинегнойные пенициллины (карбенициллин, пиперациллин и др. ), цефалоспорины I и отчасти II (цефаклор) поколений. 78

Бета-лактамазы К практически важным свойствам бета-лактамаз относятся: ü Субстратный профиль (способность к преимущественному гидролизу тех или иных бета-лактамов, например пенициллинов или цефалоспоринов или тех и других в равной степени). ü Локализация кодирующих генов (плазмидная или хромосомная). Эта характеристика определяет эпидемиологию резистентности. При плазмидной локализации генов происходит быстрое внутри- и межвидовое распространение резистентности, при хромосомной наблюдают распространение резистентного клона. ü Тип экспрессии (конститутивный или индуцибельный). При конститутивном типе микроорганизмы синтезируют беталактамазы с постоянной скоростью, при индуцибельном количество синтезируемого фермента резко возрастает после контакта с антибиотиком (индукции). 79

6 80

Тазобактам Сульбактам Клавуланат 81
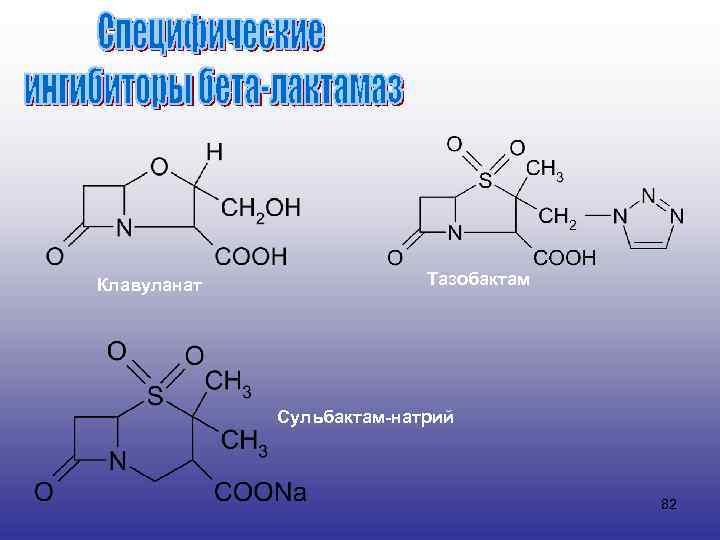
Клавуланат Тазобактам Сульбактам-натрий 82

Данные вещества, подобно бета-лактамным антибиотикам, содержат лактамное кольцо. Они «захватываются» бета-лактамазами, вследствие чего происходит необратимое ингибирование этих ферментов и при сочетании их с антибиотиками последние имеют возможность полностью проявлять свое антимикробное действие; их активность и спектр антибактериального эффекта даже несколько увеличиваются. 83

Сами ингибиторы бета-лактамаз обладают слабой антибактериальной активностью. Наиболее эффективным неконкурентным ингибитором беталактамаз различной этиологии является клавулановая кислота, получаемая биосинтетически. Будучи малоактивным антибиотиком, она находит широкое применение для борьбы с бета-лактамазной резистентностью микроорганизмов. Гетероциклический скелет клавулановой кислоты – клавам 84

7 Химический аспект механизма действия бета-лактамов 85
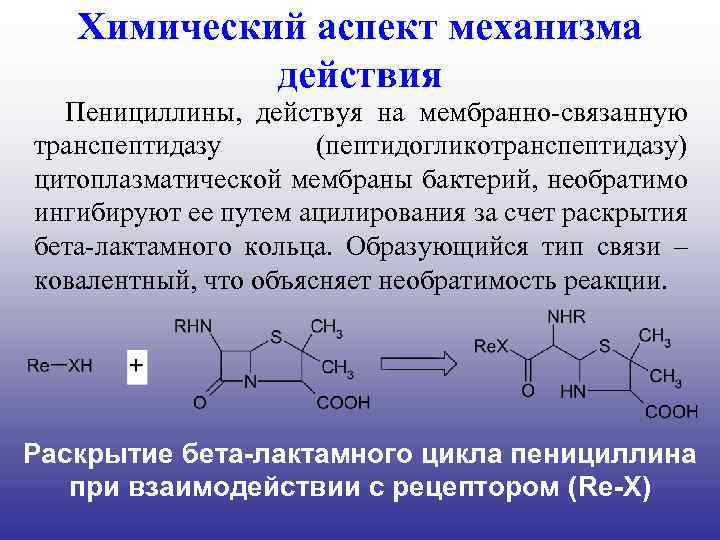
Химический аспект механизма действия Пенициллины, действуя на мембранно-связанную транспептидазу (пептидогликотранспептидазу) цитоплазматической мембраны бактерий, необратимо ингибируют ее путем ацилирования за счет раскрытия бета-лактамного кольца. Образующийся тип связи – ковалентный, что объясняет необратимость реакции. Раскрытие бета-лактамного цикла пенициллина при взаимодействии с рецептором (Re-X)
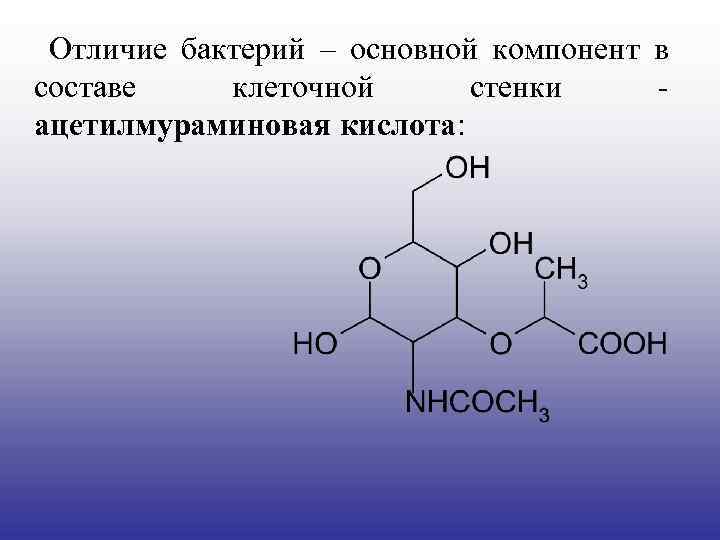
Отличие бактерий – основной компонент в составе клеточной стенки - ацетилмураминовая кислота:

Ацетилмураминовая кислота связывается с полипептидами на участках типа –CO-NHCH(CH 3)-CO-NH-CH(COR)-CH 2 -CO-NHCH[(CH 2)4 NH 2]-CO-. Действие пенициллинов основано на блокаде включения образующихся ацетилмураминовых полипептидов в клеточную стенку. Пенициллин действует на мембранносвязанную транспептидазу ЦПМ, взаимодействуя сначала с D-аланил-Dаланиновой группировкой мономера, полимеризация которого и создает клеточную 88 оболочку.

Этот мономер – пептидогликан состоит из описанного выше муропептида, связанного с углеводными компонентами. Создание полимера протекает ферментативно, опознавательным сигналом для фермента служит фрагмент D-аланина и фермент ацилируется сначала пептидогликанами. Фермент + R-D-Ala → R-D-Ala-Фермент + D-Ala Ингибирование именно этого процесса летально для микроорганизмов, а пенициллины выступают в качестве ацилирующих агентов по отношению к транспептидазной части фермента, причем ацилирование происходит за счет легко раскрывающегося бета-лактамного цикла. 89

Т. о. , пенициллины являются антагонистами D-аланил-D-аланинов, причем необратимость их взаимодействия с транспептидазой обусловлена образованием прочной ковалентной связи. 90

Р Е З Ю М Е

Ø Клеточная стенка у бактерий имеет жесткую структуру, она придает микроорганизмам форму и обеспечивает их защиту от разрушения. Ø Основа клеточной стенки - гетерополимер — пептидогликан, состоящий из полисахаридов и полипептидов. Его сетчатая структура с поперечными сшивками придает клеточной стенке прочность. Ø В состав полисахаридов входят такие аминосахара как N-ацетилглюкозамин, а также N-ацетилмурамовая кислота, имеющаяся только у бактерий. Ø С аминосахарами связаны короткие пептидные цепи, включающие некоторые L- и D-аминокислоты. Ø У грамположительных бактерий клеточная стенка содержит 50– 100 слоев пептидогликана, у грамотрицательных — 1– 2 слоя. 92

Ø В процессе биосинтеза пептидогликана участвуют около 30 бактериальных ферментов, этот процесс состоит из 3 этапов. Ø Пенициллины нарушают поздние этапы синтеза клеточной стенки, препятствуя образованию пептидных связей за счет ингибирования фермента транспептидазы. Ø Транспептидаза — один из пенициллинсвязывающих белков, с которыми взаимодействуют бета-лактамные антибиотики. Ø К ПСБ — ферментам, принимающим участие на конечных стадиях формирования клеточной стенки бактерий, помимо транспептидаз, относятся карбоксипептидазы и эндопептидазы. Они есть у всех бактерий (например, у Staphylococcus aureus их 4, у Escherichia coli — 7). Ø Пенициллины связываются с ПСБ с разной скоростью с образованием ковалентной связи. При этом происходит инактивация пенициллинсвязывающих белков, прочность клеточной стенки бактерий нарушается и клетки подвергаются лизису. 93

Нерастущие, «покоящиеся» клетки не затрагиваются пенициллинами. С нарушением синтеза клеточной оболочки под действием пенициллина связано образование у бактерий так называемых Lформ. 94

8 ЧАСТНАЯ ФАРМАКОЛОГИЯ ПЕНИЦИЛЛИНОВ

96

БИОСИНТЕТИЧЕСКИЕ ПЕНИЦИЛЛИНЫ ü К природным пенициллинам относится только бензилпенициллин. ü Однако, исходя из спектра активности, пролонгированные производные (бензилпенициллин прокаин, бензатин бензилпенициллин) и пероральные (феноксиметилпенициллин) также можно отнести к этой группе. ü Все они разрушаются β-лактамазами, поэтому их нельзя использовать для терапии стафилококковых инфекций, так как в большинстве случаев стафилококки вырабатывают βлактамазы. 97

БЕНЗИЛПЕНИЦИЛЛИНА НАТРИЕВАЯ СОЛЬ 98

q Benzylpenicillinum-natrium (TN), q Пенициллин G, q Пенициллин (INN). Формы выпуска: Порошок для приготовления инъекционных растворов во флаконах по 250000, 500000, 1000000, 5000000, 10000000 ЕД. Теоретически активность натриевой соли равна 1670 ЕД в 1 мг, практически препарат выпускается активностью не менее 1600 ЕД в 1 мг. Аптечный отпуск: по рецепту врача 99

ДОСТОИНСТВА Ø Мощное бактерицидное действие в отношении ряда клинически значимых возбудителей (стрептококки, менингококки и др. ); Ø Широкий спектр антибактериальной активности; Ø Низкая токсичность; Ø Низкая стоимость. 100

НЕДОСТАТКИ Ø Приобретенная резистентность стафилококков, пневмококков, гонококков, бактероидов. Ø Высокая аллергенность, перекрестная со всеми пенициллинами, некоторыми цефалоспоринами. 101

Раствор препарата для внутримышечного введения готовят непосредственно перед введением (ex tempore), добавляя к содержимому флакона 1 -3 мл воды для инъекций или стерильного раствора натрия хлорида изотонического 0, 9%, или 0, 5% раствора новокаина. Rp. : Benzylpenicillini-natrii 1 000 EД D. t. D. № 10 S. : содержимое флакона развести 3 мл 0, 5% раствора новокаина, вводить вну тримышечно 6 раз в день. 102
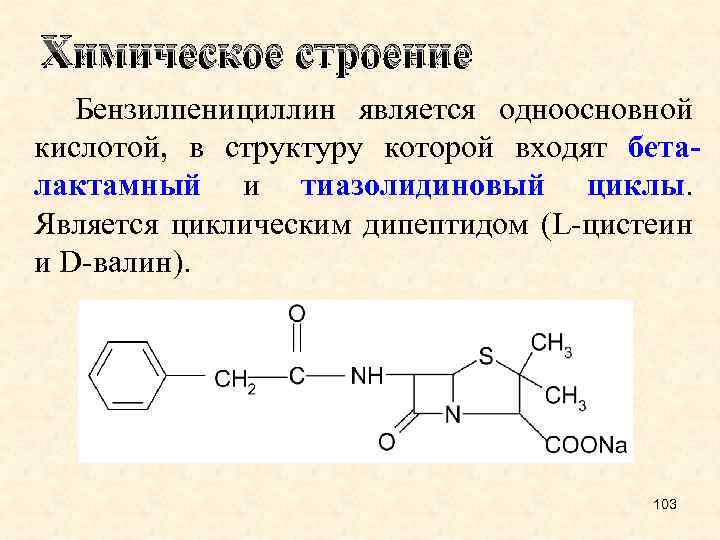
Химическое строение Бензилпенициллин является одноосновной кислотой, в структуру которой входят беталактамный и тиазолидиновый циклы. Является циклическим дипептидом (L-цистеин и D-валин). 103

Спектр антибактериальной активности Грам (+) кокки ü Стрептококки (особенно βГСА), включая пневмококки; ü Энтерококки (устойчивы к низким концентрациям); ü Стафилококки, однако большинство штаммов (S. aureus, S. epidermidis) устойчивы, так как вырабатывают β-лактамазы. 104

Спектр антибактериальной активности Грам (+) палочки ü Листерии, ü Возбудители дифтерии, ü Сибирской язвы. 105

Спектр антибактериальной активности Грам (-) кокки ü Менингококки; ü Гонококки (в устойчивы). большинстве случаев 106

Спектр антибактериальной активности Спирохеты ü Бледная трепонема, ü Лептоспиры, ü Боррелии. 107

Спектр антибактериальной активности Анаэробы ü Спорообразующие - клостридии; ü Неспорообразующие - пептококк, пептострептококки, фузобактерии (основной представитель неспорообразующих анаэробов кишечника В. fragilis устойчив); ü Актиномицеты. 108

Спектр антибактериальной активности НЕ ДЕЙСТВУЕТ ü Большинство грамотрицательных бактерий, ü Вирусы, ü Простейшие. ü Грибы; ü Штаммы стафилококков, продуцирующие лактамазы; ü Бактерии кишечной группы; бета- ü Синегнойную палочку. 109

НЕ ДЕЙСТВУЕТ Группа микроорганизмов, которая исключена из спектра активности - облигатные и факультативные внутриклеточные микроорганизмы (риккетсии, хламидии, легионеллы, бруцеллы и др. ). Клиническая неэффективность (или низкая эффективность) при инфекциях, вызываемых этими микроорганизмами, связана с ограниченной способностью бета-лактамов проникать внутрь клетки макроорганизма, прежде всего внутрь фагоцитов, где локализуется возбудитель. Также устойчивы ко всем беталактамам метициллинрезистентные стафилококки. Кроме того, природной устойчивостью к бета-лактамам обладают микоплазмы. 110

Резистентность Приобретенная резистентность к бензилпенициллину чаще всего встречается среди стафилококков. Она связана с продукцией бета-лактамаз (частота распространения 60 -80%) или наличием дополнительного пенициллиносвязывающего белка. В последние годы отмечается рост устойчивости гонококков. 111

ФАРМАКОКИНЕТИКА ь Плохо абсорбируется в ЖКТ. ь Разрушается в кислой среде желудка пенициллиназой, продуцируемой микрофлорой кишечника, поэтому применяется только парентерально. ь При внутримышечном введении быстро и хорошо всасывается в кровь и хорошо проникает в ткани и жидкие среды организма. Сmax = 30 -60 мин. ь В цереброспинальую жидкость проникает в незначительных количествах, однако при воспалении мозговых оболочек его концентрация в ликворе повышается. 112

ФАРМАКОКИНЕТИКА ь При подкожных инъекциях скорость абсорбции непостоянна, Сmax в среднем через 60 мин. Через 3 -4 часа после подкожной или внутримышечной инъекции в плазме крови обнаруживаются следовые концентрации антибиотика, поэтому для поддержания терапевтических концентраций препарата в крови необходимо производить инъекции каждые 3 -4 часа. ь При внутривенном введении концентрация препарата в крови быстро снижается. ь Элиминация преимущественно ренальная в неизмененном виде. Т 1/2 - 0, 5 час. 113

П О К А З А Н И Я Str, Pn, Hn ü Инфекции, вызванные βГСА: ангина, тонзиллофарингит, рожа, скарлатина, острая ревматическая лихорадка; ü Внебольничная пневмококковая пневмония; ü Менингококковые инфекции (менингит, менингококцемия); ü Бактериальный эндокардит - обязательно в сочетании с гентамицином или стрептомицином; ü Сифилис; ü Лептоспироз; 114

П О К А З А Н И Я Str, Pn, Hn ü Клещевой боррелиоз (болезнь Лайма); ü Сибирская язва; ü Анаэробные инфекции: клостридиальные - газовая гангрена, столбняк; неклостридиальные (вызванные неспорообразующими анаэробами) при локализации процесса выше диафрагмы. ü Актиномикоз; ü Раневые инфекции, гнойные инфекции кожи и мягких тканей, гнойный плеврит; 115

П р и м е н и е Бензилпенициллина натриевую соль вводят в виде растворов подкожно, внутримышечно, подкожно внутримышечно при необходимости – внутривенно или в внутривенно полости (плевральную, брюшную и т. д. ). полости При легочной патологии используется также ингаляционно, при заболеваниях глаз – в виде ингаляционно глазных капель и субконъюнктивально. глазных капель субконъюнктивально Из всех препаратов бензилпенициллина только натриевую соль можно вводить эндолюмбально. Другие препараты эндолюмбально пенициллина так не используются. 116

Внутримышечное введение бензилпенициллина является наиболее распространенным. Для внутримышечного введения препарат готовят ex tempore, добавляя к содержимому флакона 1 -3 мл стерильной воды для инъекций, изотонического раствора натрия хлорида или 0, 5% раствора новокаина. Добавление последнего обеспечивает пролонгацию эффекта. Растворы бензилпенициллина в растворе новокаина иногда становятся мутными ввиду образования новокаиновой соли бензилпенициллина. Однако это не является препятствием для внутримышечного введения. Внутривенно (болюсно или капельно) вводится при тяжелом течении заболевания (менингит, сепсис и др. ). 117

Взрослым вводится по 2 000 -12 000 ЕД в сутки (в 4 -6 приемов); при менингите, эндокардите и газовой гангрене – внутривенно 18 000 -24 000 ЕД в сутки (в 6 приемов). Растворы используются сразу после приготовления, добавление других препаратов к ним недопустимо. Эндолюмбальное введение бензилпенициллина натриевой соли проводится при гнойных заболеваниях головного и спинного мозга, мозговых оболочек. Назначается по 5 000 - 10 000 ЕД. Препарат разводится в стерильной воде для инъекций или в изотоническом растворе натрия хлорида из расчета 1000 ЕД/мл. Перед инъекцией из спинномозгового канала извлекают 5 -10 мл (в зависимости от уровня внутричерепного давления) ликвора и добавляют его к раствору препарата в равном соотношении. Вводят медленно (1 мл/мин) обычно 1 раз в сутки в течение 2 -3 дней, после чего переходят на внутримышечное введение. 118

Реестр побочных эффектов • Головная боль, повышение температуры тела, экзантема, боли в суставах, эозинофилия, ангионевротический отек, анафилактический шок. • При ингаляционном введении фарингиты и ларингиты аллергического характера, приступы бронхиальной астмы. • Использование препарата в очень больших дозах, особенно при эндолюмбальном введении, может сопровождаться нейротоксическими явлениями: тошнота, рвота, повышение рефлекторной возбудимости, симптомы менингизма, судороги, кома. • При наличии выраженных аллергических реакций назначаются адреналин, глюкокортикостероиды, антигистаминные средства, кальция хлорид. Возможно введение пенициллиназы (1 000 ЕД). 119

Пенициллины и другие бета-лактамные антибиотики вызывают лекарственную аллергию чаще других лекарственных средств. Распространенность аллергии к пенициллинам составляет, по разным данным, от 0, 75 до 8%, анафилактические реакции на эти препараты отмечаются лишь в 0, 01% случаев. Чаще всего аллергия к пенициллинам встречается в возрасте 20 -49 лет. 120

Лекарственные взаимодействия ü Синергизм при сочетании с аминогликозидами, но их нельзя смешивать в одном шприце, так как при этом отмечается инактивация аминогликозидов. ü Используются комбинации с макролидами при пневмонии, с хлорамфениколом при менингите. ü Нельзя сочетать с сульфаниламидами. 121

ü Бактерицидные антибиотики (в т. ч. цефалоспорины, ванкомицин, рифампицин, аминогликозиды) оказывают синергидное действие; ü бактериостатические (в т. ч. макролиды, хлорамфеникол, линкозамиды, тетрациклины) - антагонистическое. 122

• Повышает эффективность непрямых антикоагулянтов (подавляя кишечную микрофлору, снижает протромбиновый индекс); снижает эффективность пероральных контрацептивов, ЛС, в процессе метаболизма которых образуется ПАБК, этинилэстрадиола - риск развития кровотечений "прорыва". Диуретики, аллопуринол, блокаторы канальцевой секреции, фенилбутазон, НПВП, снижая канальцевую секрецию, повышают концентрацию бензилпенициллина. Аллопуринол повышает риск развития аллергических реакций (кожной сыпи). 123
Антибиотики 2.ppt