dlya_MMCh_S_V_Ts-11_gravimetria.pptx
- Количество слайдов: 8
 Гравиметрия Гравиметрический (весовой) метод анализа основан на измерении массы определяемого компонента после его выделения в виде гравиметрической формы. 1. Метод осаждения. В нем определяемый компонент вступает в химическую реакцию с реагентом-осадителем, образуя малорастворимое соединение. После проведения ряда аналитических операций твердый осадок известного состава взвешивают и проводят необходимые вычис ления. 2. Методы отгонки могут быть прямые и косвенные. В методе прямой отгонки определяемый компонент выделяют из пробы в виде газообразного продукта, улавливают и затем определяют его массу. В методах косвенной отгонки массу газообразного продукта определяют по разности масс анализируемого компонента до и после термической обработки. 3. В термогравиметрическом анализе фиксируют изменение массы вещества в процессе нагревания, что позволяет судить о про исходящих превращениях и установить состав образующихся промежуточных продуктов. 4. Электрогравиметрический анализ основан на электролитическом выделении металлов и взвешивании полученного на электроде осадка. Основным физическим условием электpoлитичecкoгo разделения металлов является определенное напряжение, при котором осаждаются одни и не выделяются другие металлы.
Гравиметрия Гравиметрический (весовой) метод анализа основан на измерении массы определяемого компонента после его выделения в виде гравиметрической формы. 1. Метод осаждения. В нем определяемый компонент вступает в химическую реакцию с реагентом-осадителем, образуя малорастворимое соединение. После проведения ряда аналитических операций твердый осадок известного состава взвешивают и проводят необходимые вычис ления. 2. Методы отгонки могут быть прямые и косвенные. В методе прямой отгонки определяемый компонент выделяют из пробы в виде газообразного продукта, улавливают и затем определяют его массу. В методах косвенной отгонки массу газообразного продукта определяют по разности масс анализируемого компонента до и после термической обработки. 3. В термогравиметрическом анализе фиксируют изменение массы вещества в процессе нагревания, что позволяет судить о про исходящих превращениях и установить состав образующихся промежуточных продуктов. 4. Электрогравиметрический анализ основан на электролитическом выделении металлов и взвешивании полученного на электроде осадка. Основным физическим условием электpoлитичecкoгo разделения металлов является определенное напряжение, при котором осаждаются одни и не выделяются другие металлы.
 Метод осаждения Осадитель - это реагент, содержащий в своем составе катион или анион, образующий с определяемым ионом малорастворимое соединение. Последовательность аналитических операций в гравиметрическом методе осаждения 1. Расчет массы навески анализируемого вещества и ее взвешивание 2. Растворение навески 3. Создание условий осаждения 4. Осаждение (получение осаж денной формы) 5. Отделение осадка фильтрова нием 6. Промывание осадка 7. Получение гравиметриче ской формы (высушивание, прокаливание до постоян ной массы) 8. Взвешивание гравиметриче ской формы 9. Расчет результатов анализа
Метод осаждения Осадитель - это реагент, содержащий в своем составе катион или анион, образующий с определяемым ионом малорастворимое соединение. Последовательность аналитических операций в гравиметрическом методе осаждения 1. Расчет массы навески анализируемого вещества и ее взвешивание 2. Растворение навески 3. Создание условий осаждения 4. Осаждение (получение осаж денной формы) 5. Отделение осадка фильтрова нием 6. Промывание осадка 7. Получение гравиметриче ской формы (высушивание, прокаливание до постоян ной массы) 8. Взвешивание гравиметриче ской формы 9. Расчет результатов анализа
 Насыщенный раствор, в котором малорастворимое вещество при дан ных условиях достигло максимальной концентрации и больше не растворяется. Осадок данного вещества находится в равновесном состоянии с веществом в растворе. Равновесие малорастворимого соединения Ktm. Ann с его насыщенным раствором Ktm. Ann = m. Ktn+ + n. Anm Количественно можно охарактеризовать константой равновесия (частный случай константы диссоциации) Подстановка А. вместо концентраций в уравнения, определяющие условия фазовых, химических или электрохимических равновесий для идеальных растворов, делает эти уравнения применимыми к реальным растворам. Активность индивидуального твердого соединения постоянна, поэтому Полученная таким образом константа равновесия называется произведением растворимости (произведением активностей).
Насыщенный раствор, в котором малорастворимое вещество при дан ных условиях достигло максимальной концентрации и больше не растворяется. Осадок данного вещества находится в равновесном состоянии с веществом в растворе. Равновесие малорастворимого соединения Ktm. Ann с его насыщенным раствором Ktm. Ann = m. Ktn+ + n. Anm Количественно можно охарактеризовать константой равновесия (частный случай константы диссоциации) Подстановка А. вместо концентраций в уравнения, определяющие условия фазовых, химических или электрохимических равновесий для идеальных растворов, делает эти уравнения применимыми к реальным растворам. Активность индивидуального твердого соединения постоянна, поэтому Полученная таким образом константа равновесия называется произведением растворимости (произведением активностей).
 Произведение растворимости малорастворимого соединения связано с его растворимостью (S) соотношением Растворимость – это способность в ва образовывать с др. в вом (или в вами) гомогенные смеси с дисперсным распределением компонентов. Механизм образования осадка Образование осадка происходит в том случае, когда возникает местное (относительное) пересыщение раствора, ко торое рассчитывают по формуле: (Q - S) /S, где Q концентрация растворенного вещества в какой либо момент време ни, моль/см 3; S растворимость вещества в момент равновесия, моль/см 3 Для получения осадка, которые можно легко отфильтровать и промыть, необходимо проводить осаждение из разбавленных растворов медленным прибавлением осадителя и при нагрева нии (табл. 1).
Произведение растворимости малорастворимого соединения связано с его растворимостью (S) соотношением Растворимость – это способность в ва образовывать с др. в вом (или в вами) гомогенные смеси с дисперсным распределением компонентов. Механизм образования осадка Образование осадка происходит в том случае, когда возникает местное (относительное) пересыщение раствора, ко торое рассчитывают по формуле: (Q - S) /S, где Q концентрация растворенного вещества в какой либо момент време ни, моль/см 3; S растворимость вещества в момент равновесия, моль/см 3 Для получения осадка, которые можно легко отфильтровать и промыть, необходимо проводить осаждение из разбавленных растворов медленным прибавлением осадителя и при нагрева нии (табл. 1).
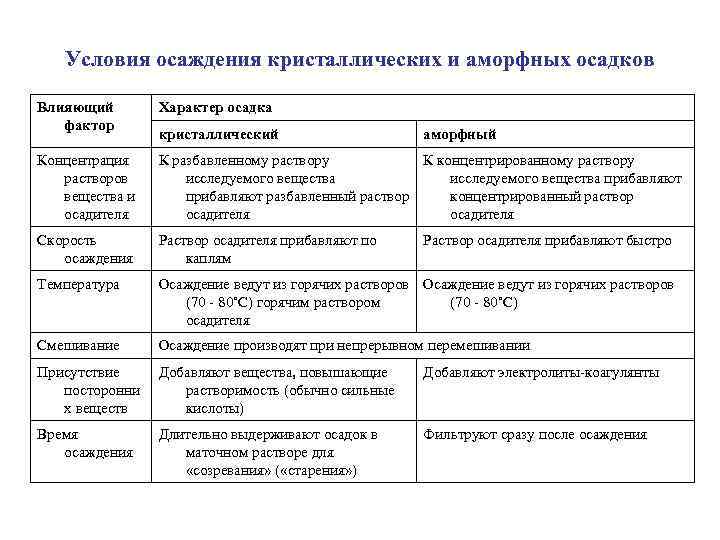 Условия осаждения кристаллических и аморфных осадков Влияющий фактор Характер осадка Концентрация растворов вещества и осадителя К разбавленному раствору К концентрированному раствору исследуемого вещества прибавляют разбавленный раствор концентрированный раствор осадителя Скорость осаждения Раствор осадителя прибавляют по каплям Температура Осаждение ведут из горячих растворов (70 80˚С) горячим раствором (70 80˚С) осадителя Смешивание Осаждение производят при непрерывном перемешивании Присутствие посторонни х веществ Добавляют вещества, повышающие растворимость (обычно сильные кислоты) Добавляют электролиты коагулянты Время осаждения Длительно выдерживают осадок в маточном растворе для «созревания» ( «старения» ) Фильтруют сразу после осаждения кристаллический аморфный Раствор осадителя прибавляют быстро
Условия осаждения кристаллических и аморфных осадков Влияющий фактор Характер осадка Концентрация растворов вещества и осадителя К разбавленному раствору К концентрированному раствору исследуемого вещества прибавляют разбавленный раствор концентрированный раствор осадителя Скорость осаждения Раствор осадителя прибавляют по каплям Температура Осаждение ведут из горячих растворов (70 80˚С) горячим раствором (70 80˚С) осадителя Смешивание Осаждение производят при непрерывном перемешивании Присутствие посторонни х веществ Добавляют вещества, повышающие растворимость (обычно сильные кислоты) Добавляют электролиты коагулянты Время осаждения Длительно выдерживают осадок в маточном растворе для «созревания» ( «старения» ) Фильтруют сразу после осаждения кристаллический аморфный Раствор осадителя прибавляют быстро
 Осажденная и гравиметрическая форма и требования к ним Осажденной формой называют соединение, в виде которого определяемый компонент осаждается из раствора. Гравиметрической (весовой) формой называют соединение, которое взве шивают. S 042 - + Ва 2+ ↔ Ba. S 04↓ → Ba. S 04 ↓ определяемый осадитель осажденная гравиметрическая ион форма Fe 3+ + 3 OH‾ ↔ Fe(OH)3↓ → Fe 2 O 3↓ определяемый осадитель осажденная гравиметрическая ион форма Из приведенных примеров видно, что не всегда гравиметрическая форма совпадает с осажденной формой вещества.
Осажденная и гравиметрическая форма и требования к ним Осажденной формой называют соединение, в виде которого определяемый компонент осаждается из раствора. Гравиметрической (весовой) формой называют соединение, которое взве шивают. S 042 - + Ва 2+ ↔ Ba. S 04↓ → Ba. S 04 ↓ определяемый осадитель осажденная гравиметрическая ион форма Fe 3+ + 3 OH‾ ↔ Fe(OH)3↓ → Fe 2 O 3↓ определяемый осадитель осажденная гравиметрическая ион форма Из приведенных примеров видно, что не всегда гравиметрическая форма совпадает с осажденной формой вещества.
 Вычисление результатов в гравиметрическом методе Массовая процентная доля w, % определяемого компонента в навеске: где mн масса навески анализируемого вещества; mгр. ф масса гравиметрической формы анализируемого вещества. F гравиметрический фактор (фактор пересчета, аналитический мно житель) рассчитывают как отношение молекулярной массы определяемого компонента к молекулярной массе гравиметрической формы с учетом стехио метрических коэффициентов.
Вычисление результатов в гравиметрическом методе Массовая процентная доля w, % определяемого компонента в навеске: где mн масса навески анализируемого вещества; mгр. ф масса гравиметрической формы анализируемого вещества. F гравиметрический фактор (фактор пересчета, аналитический мно житель) рассчитывают как отношение молекулярной массы определяемого компонента к молекулярной массе гравиметрической формы с учетом стехио метрических коэффициентов.
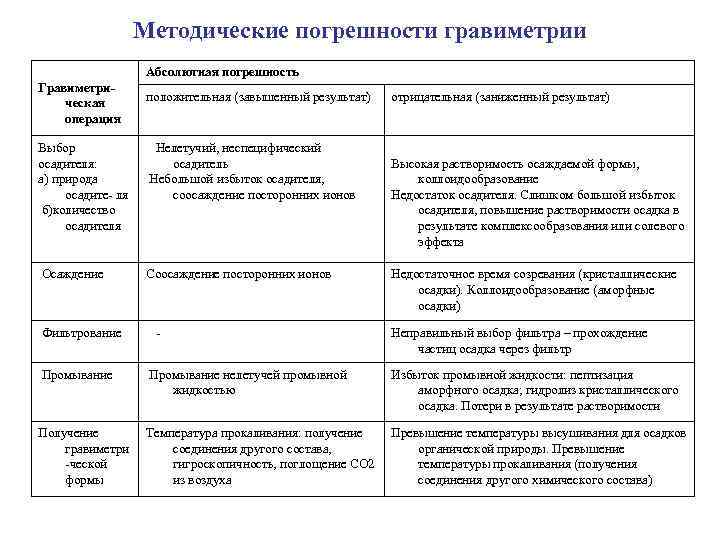 Методические погрешности гравиметрии Гравиметрическая операция Абсолютная погрешность положительная (завышенный результат) отрицательная (заниженный результат) Выбор осадителя: а) природа осадите ля б)количество осадителя Нелетучий, неспецифический осадитель Небольшой избыток осадителя, соосаждение посторонних ионов Высокая растворимость осаждаемой формы, коллоидообразование Недостаток осадителя. Слишком большой избыток осадителя, повышение растворимости осадка в результате комплексообразования или солевого эффекта Осаждение Соосаждение посторонних ионов Недостаточное время созревания (кристаллические осадки). Коллоидообразование (аморфные осадки) Фильтрование Неправильный выбор фильтра – прохождение частиц осадка через фильтр Промывание нелетучей промывной жидкостью Избыток промывной жидкости: пептизация аморфного осадка; гидролиз кристаллического осадка. Потери в результате растворимости Получение гравиметри ческой формы Температура прокаливания: получение Превышение температуры высушивания для осадков соединения другого состава, органической природы. Превышение гигроскопичность, поглощение СО 2 температуры прокаливания (получения из воздуха соединения другого химического состава)
Методические погрешности гравиметрии Гравиметрическая операция Абсолютная погрешность положительная (завышенный результат) отрицательная (заниженный результат) Выбор осадителя: а) природа осадите ля б)количество осадителя Нелетучий, неспецифический осадитель Небольшой избыток осадителя, соосаждение посторонних ионов Высокая растворимость осаждаемой формы, коллоидообразование Недостаток осадителя. Слишком большой избыток осадителя, повышение растворимости осадка в результате комплексообразования или солевого эффекта Осаждение Соосаждение посторонних ионов Недостаточное время созревания (кристаллические осадки). Коллоидообразование (аморфные осадки) Фильтрование Неправильный выбор фильтра – прохождение частиц осадка через фильтр Промывание нелетучей промывной жидкостью Избыток промывной жидкости: пептизация аморфного осадка; гидролиз кристаллического осадка. Потери в результате растворимости Получение гравиметри ческой формы Температура прокаливания: получение Превышение температуры высушивания для осадков соединения другого состава, органической природы. Превышение гигроскопичность, поглощение СО 2 температуры прокаливания (получения из воздуха соединения другого химического состава)


