ГОУ ВПО «Сибирский государственный медицинский университет»


ГОУ ВПО «Сибирский государственный медицинский университет» Полиморфные модификации лекарственных веществ их физико – химические свойства и анализ. Лекция по фармацевтической химии для студентов 4 курса фармацевтического факультета Сиб. ГМУ (2010 -2011 уч. гг. )

Тема лекции: Полиморфные модификации лекарственных веществ, их физико – химические свойства и анализ. Вопросы: 1. Общая характеристика 2. Типы полиморфизма 3. Физико – химические свойства полиморфных модификаций 4. Методы обнаружение полиморфных модификаций 5. Получение полиморфных модификаций веществ 6. Относительная стабильность полиморфных модификаций и ее влияние на биодоступность лекарственного вещества 7. Влияние полиморфизма и псевдополиморфизма на фармакотехнологические и биофармацевтические свойства лекарственных веществ.

Общая характеристика Термином «полиморфизм» принято определять способность вещества существовать в нескольких кристаллических формах с различными физико- химическими свойствами, но имеющих одинаковый химический состав. Такие формы называются полиморфными модификациями, каждая из них устойчива в определенной области температур, давления и других внешних условий. Впервые явление полиморфизма было открыто в 1788 г. немецким химиком М. Г. Клапротом на примере 2 минералов – кальцита и арагонита, имеющих одинаковый химический состав , но различающихся формой кристаллов. Термин «полиморфизм» (от греч. Polymorphos – многообразие) был предложен в 90 -х годах XIX века французским академиком Ж. Б. Дюма. Первыми органическими веществами, для которых были обнаружены и изучены несколько кристаллических форм с различными температурами плавления, были бензамид, изонитрофенол и бензофенон, а термин «полиморфизм» в ряду органических соединений впервые был применен для случая двух модификаций 2, 4 -динитрохлорбензола.

В 1942 г. было известно более 1200 органических полиморфных соединений, а в последние годы их насчитывается уже несколько десятков тысяч веществ. Исследование полиморфизма биологически активных органических соединений и, прежде всего лекарственных веществ, началось в конце 30 -х годов прошлого столетия. В 1937 г. был обнаружен полиморфизм сульфаниламида, в 1941 г. выделены и изучены рентгенографически его полиморфные модификации. Первый обзор о фармацевтическом применении полиморфизма был опубликован в 1969 г. В 80 -е годы в отдельную область выделилось термодинамическое направление в изучении полиморфизма. В настоящее время полиморфизм выявлен у более, чем 70 % лекарственных веществ практически всех фармакологических групп и по мнению американского химика У. Мак-Кроуна «каждое соединение имеет различные полиморфные модификации, и число модификаций, выделяемых для данного соединения, зависит от времени, средств и усилий исследователя» . Академик В. И. Вернадский назвал полиморфизм «общим свойством материи» .

В настоящее время компьютерные программы позволяют для некоторых органических соединений, исходя из их состава и на основании расчета энергии решетки молекулярных кристаллов, рассчитывать вероятные для них полиморфные модификации. В США тесты на полиморфизм в требованиях FDА для аналитического контроля новых ЛС утвержден набор методик, выявления полиморфизма и его изучение. Полиморфизм оказался чрезвычайно важным фактором, определяющим лечебный эффект фармацевтических субстанций и лекарственных форм, существенно влияющим на их параметры и биологическую активность.

Полиморфные изменения лекарственных веществ могут явиться причиной быстрой инактивации препаратов, изменения физических показателей готовых лекарств, химической несовместимости ингредиентов в одной и той же лекарственной форме. Полиморфные модификации ряда широко применяемых лекарственных веществ заметно различаются по химической стабильности, гигроскопичности, прессуемости. В зависимости от типа связей в кристалле, окружающих условий, химической структуры они могут переходить в свои менее активные, стабильные аналоги. Полиморфные превращения наиболее характерны для лекарственных и вспомогательных веществ в суспензиях, мазях, суппозиториях, гранулах, таблетках, капсулах, спансулах, аэрозолях с твердой дисперсной фазой.

Типы полиморфизма Кристаллы одного вещества могут иметь различное число, размеры и форму граней. Их развитие относительно друга может происходить по-разному. Это приводит к различию внешней формы кристаллов (габитуса ). Твердые вещества с близким габитусом называются изоморфными. Многие вещества способны существовать в более чем одной кристаллической форме, каждая из которых называется полиморфной модификацией, а само явление - полиморфизмом. Но изменение габитуса может иметь место и там, где нет полиморфизма: в процессе кристаллизации растворитель внедряется в кристаллическую решетку вещества, вызывая ее изменение. Точки плавления и растворимость сольватов и несольватированных форм вещества могут значительно различаться. Подобное явление называется псевдополиморфизмом.

Структурная классификация типов полиморфизма (по Г. Б. Бокий) основывается на следующих признаках: Различие координационного числа; Различие типа плотнейшей упаковки; Изменение мотива расположения катионов; Различие в повороте некоторых структурных групп в процессе полиморфного превращения; Вращение молекул или радикалов в кристаллической решетке (конформация)

Причиной полиморфизма может быть не только расположение молекул в решетке, но и их конформация, а иногда – оба фактора. В связи с этим предложено разделить все случаи полиморфизма органических веществ на 4 типа: 1. В двух полиморфных модификациях молекулы имеют практически одинаковое строение и уложены одинаковым образом; 2. Молекулы с одинаковым строением уложены по – разному; 3. Строение молекул несколько отличается, но сохраняется их укладка; 4. Молекулы с разным строением уложены различным образом.

Физико – химические свойства полиморфных модификаций Физико-химические свойства формируются на этапе кристаллизации из растворов или расплавов. Наиболее чувствительны к полиморфизму: размер кристаллитов, плотность, растворимость, температура плавления, удельная теплоемкость, электропроводимость, угол смачивания, показатель преломления, коэффициент рассеяния света, степень деполяризации света, ИК-спектры, КР-спектры, термограммы, рентгеновские дифрактограммы.

Методы обнаружения полиморфных модификаций Для обнаружения и изучения полиморфных модификаций используют следующие методы: микроскопия (включая электронную), ИК- и мессбауэровская спектроскопия, ЭПР, рентгенофазовый метод, ДСК, термооптический и термогравиметрический анализы. Для растворов используют молекулярное светорассеяние, дилатометрию, кондуктометрию, определение константы ионизации, ПМР, С 13 -ЯМР, биологические методы. Для идентификации и характеристики полиморфных модификаций ЛВ согласно руководству Международной конференции по гармонизации ( IC Н Q 6 A) рекомендованы следующие методы: дифракция рентгеновских лучей – для прямого определения кристаллической структуры ЛВ; спектральные методы - для характеристики модификаций ЛВ на основе внутримолекулярных взаимодействий; термоаналитические методы – для количественной характеристики фазовых переходов, десольватации ЛВ; оптическая и сканирующая электоронная микроскопия – для исследования морфологии кристаллов ЛВ.

Микроскопия, в том числе электронная; ИК – спектроскопия; Мёссбауэровская спектроскопия; Электронно – парамагнитный резонанс; Рентгенофазовый метод; Дифференциальная сканирующая калориметрия; Термооптический анализ; Термогравиметрический анализ (изучение псевдополиморфизма)

Микрокристаллоскопический анализ Основан на обнаружении веществ по форме, величине и окраске их кристаллов. В большинстве случаев для идентификации химических соединений с помощью микрокристаллоскопического метода определяют форму или окраску не самих исследуемых веществ, а кристаллических продуктов , которые образуются при взаимодействии этих соединений с соответствующими реактивами. Форму и окраску кристаллов определяют с помощью микроскопа. Достоинства метода: Ø требуются малые количества исследуемых веществ; Ø метод может быть использован для обнаружения взрывчатых и ядовитых веществ, работа с большими количествами которых небезопасна; Ø исключаются такие громоздкие операции, как фильтрование, выпаривание, прокаливание и т. д.

Недостатки метода: Ø при выполнении микрокристаллоскопических реакций в ряде случаев довольно трудно получить кристаллы строго определенной формы, которая зависит от многих факторов (концентрации исследуемого вещества, объема и концентрации реактива, наличия примесей, природы растворителя, условий кристаллизации, скорости образования кристаллов, испарения жидкостей на предметном стекле, р. Н среды, температуры, положения кристаллов во время роста и др. ); Ø Ограниченное число форм кристаллов, образующихся при микрокристаллоскопических реакциях, и большое число веществ, которые можно определять с помощью этих реакций, приводят к тому, что одну и ту же форму могут иметь кристаллы нескольких веществ; Ø Отсутствие научно обоснованной номенклатуры форм кристаллов, образующихся при микрокристаллоскопических реакциях, препятствует широкому применению этого метода в анализе.

ИК – спектроскопия Инфракрасная спектроскопия (ИКС) — раздел спектроскопии, охватывающий длинноволновую область спектра (>730 нм за красной границей видимого света). Инфракрасные спектры возникают в результате колебательного (отчасти вращательного) движения молекул, а именно — в результате переходов между колебательными уровнями основного электронного состояния молекул. По числу и положению пиков в ИК спектрах поглощения можно судить о природе вещества (качественный анализ), а по интенсивности полос поглощения — о количестве вещества (количественный анализ). Основные приборы — различного типа инфракрасные спектрометры.

Одной из областей применения ИК-спектроскопии является исследование химического состава и контроля качества полиморфных модификаций и готовых лекарственных форм, позволяющий решать следующие задачи: Ø определение подлинности полиморфных модификаций по стандартным спектрам Фармакопеи; Ø качественный и количественный анализ исходных веществ и продуктов синтеза; Ø идентификация и контроль качества сырья; Ø контроль качества готовых лекарственных форм.

Мёссбауэровская спектроскопия (гамма – резонансная спектроскопия) основана на явлении излучения и резонансного поглощения ɣ-квантов ядрами атомов в твердых телах без потери части энергии на отдачу ядра. При этом внутренняя энергия решетки твердого тела не изменяется (не происходит возбуждения фононов- колебательных квантов). Это явление названо эффектом Мёссбауэра. Схематическое изображение процессов излучения и резонансного поглощения ɣ-квантов.

Электронный – парамагнитный резонанс Электронный парамагнитный резонанс (ЭПР), резонансное поглощение электромагнитной энергии в сантиметровом или миллиметровом диапазоне длин волн веществами, содержащими парамагнитные частицы. ЭПР — один из методов радиоспектроскопии. Парамагнитными частицами могут быть атомы и молекулы, как правило, с нечётным числом электронов (например, атомы азота и водорода, молекулы NO); радикалы свободные (например, CH 3); ионы с частично заполненными внутренними электронными оболочками (например, ноны переходных элементов); центры окраски в кристаллах; примесные атомы (например, доноры в полупроводниках). ЭПР наблюдается в диапазоне СВЧ.

Для измерения поглощения используют радиоспектрометры (спектрометры ЭПР), в которых при постоянной частоте и медленном изменении внешнего магнитного поля регистрируется изменение поглощаемой в образце мощности.

Рентгенофазовый анализ Основной задачей рентгенофазового анализа (РФА) является идентификация различных фаз в их смеси на основе анализа дифракционной картины, даваемой исследуемым образцом. Определение вещества в смеси проводится по набору его межплоскостных расстояний и относительным интенсивностям соответствующих линий на рентгенограмме. Когерентно рассеянные рентгеновские лучи интерферируют между собой, при этом дифракционной решеткой для рентгеновского излучения служит кристаллическая решетка, поскольку межплоскостные расстояния в кристалле сравнимы с длиной волны излучения. Целью рентгенофазового анализа является идентификация вещества в смеси по набору его межплоскостных расстояний (d) и относительным интенсивностям (I) соответствующих линий на рентгенограмме. Для этого, согласно закону Брегга — Вульфа, необходимо определение углов отражения θ.

Дифференциальная сканирующая калориметрия Дифференциальная сканирующая калориметрия – метод, основанный на измерении разницы тепловых потоков, идущих от исследуемого образца и образца сравнения при контролируемой (обычно, линейно меняющейся) температуре. Количественное измерение величины тепловых потоков, возникающих при одновременном программированном нагреве образца и эталона позволяет изучать процессы, связанные с химическими и фазовыми переходами в системе, производить высокоточное определение зависимости теплоемкости от температуры или времени при изотермическом анализе.

Применение ДСК: ü плавление-кристаллизация ü полиморфизм ü фазовые диаграммы ü переходы в жидких кристаллах ü чистота материалов ü кристалличность полукристаллических материалов ü соотношение твердое тело-жидкость ü фазовые переходы в твердом теле ü переходы стеклования ü удельная теплоемкость ü структурообразующие реакции ü окислительная стабильность ü начало разложения ü совместимость

Возможности ДСК: ü Определение температуры начала, максимума, перегиба, конца теплового эффекта ü Автоматический поиск пика ü Тепловые эффекты переходов: определение площади пика (энтальпии) с выбранной базовой линией и парциальной площади пика ü Определение параметров процесса кристаллизации ü Комплексный анализ переходов стеклования/расстекловывания ü Автоматическая коррекция базовой линии ü Определение удельной теплоемкости.

Термогравиметрический анализ Термогравиметрия или термогравиметрический анализ (ТГ) — метод термического анализа, при котором регистрируется изменение массы образца в зависимости от температуры. Этот метод анализа основывается на высокоточных измерениях трех параметров: массы, температуры и изменения температуры. Поскольку многие ТГ-кривые выглядят сходно, может потребоваться их дополнительная обработка, прежде чем они могут быть правильно интерпретированы. Производная ТГ -кривой позволяет установить точку, в которой изменение массы происходит наиболее быстро.
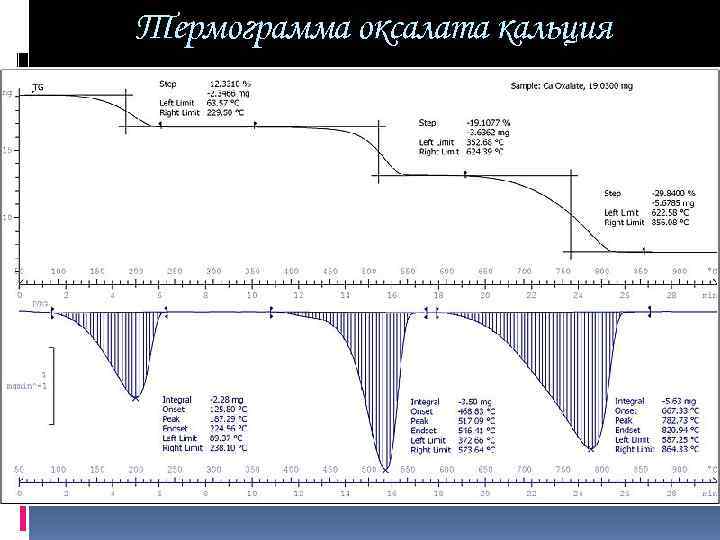
Термограмма оксалата кальция

Получение полиморфных модификаций При разработке технологии производства фармацевтической субстанции обязательным является установление взаимосвязи между кристаллической формой ЛВ и условиями его получения. Это связано с двумя обстоятельствами: 1) Незначительные изменения условий могут привести к получению вещества с различным соотношением полиморфных модификаций или новых полиморфных модификаций. 2) Это необходимо для разработки технологии целенаправленного получения конкретных метастабильных полиморфных модификаций ЛВ, которые обладают более высокой биологической активностью по сравнению со стабильными модификациями. Наиболее распространенными технологическими операциями получения кристаллических веществ являются: Измельчение твердых продуктов в различных устройствах кристаллизация химические методы (методы равновесной и неравновесной кристаллизации)

Наиболее эффективным и универсальным методом получения кристаллических модификаций ЛВ является кристаллизация из растворов и расплавов. Кристаллизационные методы получения полиморфных модификаций и сольватов ЛВ можно разделить на равновесные и неравновесные. Метод равновесной кристаллизации из раствора основан на изотермическом и изоконцентрационном медленном испарении растворителя из раствора, находящегося в равновесии с кристаллами данной полиморфной модификации. Неравновесные методы кристаллизации основаны на относительно быстрой кристаллизации из расплава, замены растворителя, распылительной и сублимационной сушке.

Метод дегидратации основан на дегидратации кристаллогидратов ЛВ путем плавления и последующей кристаллизации из расплава. Метод десольватации основан на десольватации сольватов ЛВ таким же путем, как в методе дегидратации. Важными параметрами, которые влияют на процесс кристаллизации полиморфных модификаций ЛВ является температура, давление, степень пересыщения, природа растворителя, состав раствора, р. Н, скорость перемешивания. Температура и давление играют решающее значение для выбора условий получения определенной полиморфной модификации ЛВ, поскольку определяют условие их стабильности, метод стабильности, растворимость. При получении полиморфных модификаций с перспективными терапевтическими параметрами предпочтения отдают тем методам, которые обеспечивают лучшую растворимость и способность фармацевтических субстанций к всасыванию, превращению и взаимодействию в организме, придают им специфическую адсорбцию в некоторых органах и тканях, а также определенную скорость и степень эллиминации из организма.

Относительная стабильность полиморфных модификаций и ее влияние на биодоступность лекарственного вещества Полиморфизм обусловлен различием в расположении молекул в кристаллической структуре, поэтому полиморфные модификации одного вещества характеризуются различным запасом свободной энергии. В заданных условиях полиморфная форма, имеющая наименьшую свободную энергию, является наиболее стабильной, вследствие чего другие формы будут трансформироваться в нее. Переход одной полиморфной модификации в другую обязательно сопровождается тепловым эффектом и скачкообразным изменением свойств. Различают монотропные и энантиотропные превращения, из которых первые необратимы. Для вторых возможны взаимные переходы с изменением температуры, давления, влажности и др.

При кристаллизации твердого вещества из раствора или расплава первой образуется наименее устойчивая фаза, которая по величине свободной энергии наиболее близка к раствору (правило В. Освальда). Именно по этому метастабильные модификации обладают меньшим внутренним сцеплением молекул, что выражается в их повышенной растворимости. Растворимость ЛВ в воде является наиболее важным его физическим свойством и растворение играет роль лимитирующей стадии и абсорбции ЛВ из желудочно- кишечного тракта. Вот почему именно метастабильные формы вызывают особый интерес при создании фармацевтической субстанции.

Имеется разнообразный арсенал методов и средств, с помощью которых можно затормозить переход метастабильных кристаллических модификаций в стабильные. Повышают устойчивость метастабильных полиморфных форм некоторые вспомогательные вещества (метилцеллюлоза, поливинилпирролидон и др. ) Если для превращения одной полиморфной формы в другую требуется малое количество энергии , то в условиях in vivo эти формы легко переходят друг в друга. Поэтому, если вместо одной полиморфной модификации ЛВ применяется другая, его биодоступность не претерпевает существенных изменений.

Влияние полиморфизма и псевдополиморфизма на фармакотехнологические и биофармацевтические свойства лекарственных веществ. Физико-химические свойства кристаллических веществ в конечном итоге обуславливают: прессуемость, сыпучесть, гигроскопичность, химическую стабильность, биодоступность лекарственных веществ. Например, кубические кристаллы парацетамола прессуются лучше, чем игольчатые, что объясняется их легкой перегруппировкой, возникновение лучшего контакта и более прочных связей. Различие в гигроскопичности может быть продемонстрировано на примере леокаина и дикаина, для которых потеря в массе при высушивании составляет до 3, 5% и до 0, 5% соответственно. Различие в биодоступности обуславливает биофармацевтическую неэквивалентность химически идентичных лекарственных веществ, с которой связана терапевтическая неэквивалентность. В группе снотворных лекарственных веществ (барбитуратов) также выявлена неэквивалентность как физико-химических, так и биофармацевтических. Например, обнаружено, влияние кристаллического строения бензонала на характер судорог и продолжительность снотворного эффекта.

Многочисленные примеры влияния псевдополиморфизма на биодоступность лекарственных веществ, например, безводная форма ампициллина при 37 о. С на 20% более растворима в воде, чем его тригидрат. Поэтому время, необходимое для растворения 50% безводного ампициллина значительно меньше. Применяя ту или иную полиморфную форму лекарственного вещества, можно влиять не только на уровень его абсорбции и фармакотерапевти- ческую активность, но и изменять время действия лекарственного вещества. Изменяя фармакокинетику лекарственного вещества, полиморфизм может оказывать влияние на его токсичность. Так, токсичность дикаина в 3 раза превышает токсичность его полиморфной формы. Таким образом, полиморфизм имеет исключительное значение для клинической практики с точки зрения повышения эффективности препаратов, нивелирования их побочных действий, а также сокращения экономических затрат. Выбор на основе биофармацевтических исследований наиболее активных полиморфных модификаций ЛВ позволяет снизить дозы применяемых препаратов.
Презентация Полиморфизм.pptx
- Количество слайдов: 33

