Презентация МЕТАЛЛЫ.ppt
- Количество слайдов: 12
 ГОУ СПО (ССУЗ) «Темниковское медицинское училище» ПРЕЗЕНТАЦИЯ Подготовила: преподаватель химии Сергеева Любовь Юрьевна Темников – 2010 г.
ГОУ СПО (ССУЗ) «Темниковское медицинское училище» ПРЕЗЕНТАЦИЯ Подготовила: преподаватель химии Сергеева Любовь Юрьевна Темников – 2010 г.
 История открытия металлов • Каменный век • Медный век (IV – III тысячелетия до н. э. ) • Бронзовый век (конец IV – начало I тысячелетия до н. э. ) • Железный век (I тысячелетие до н. э. )
История открытия металлов • Каменный век • Медный век (IV – III тысячелетия до н. э. ) • Бронзовый век (конец IV – начало I тысячелетия до н. э. ) • Железный век (I тысячелетие до н. э. )
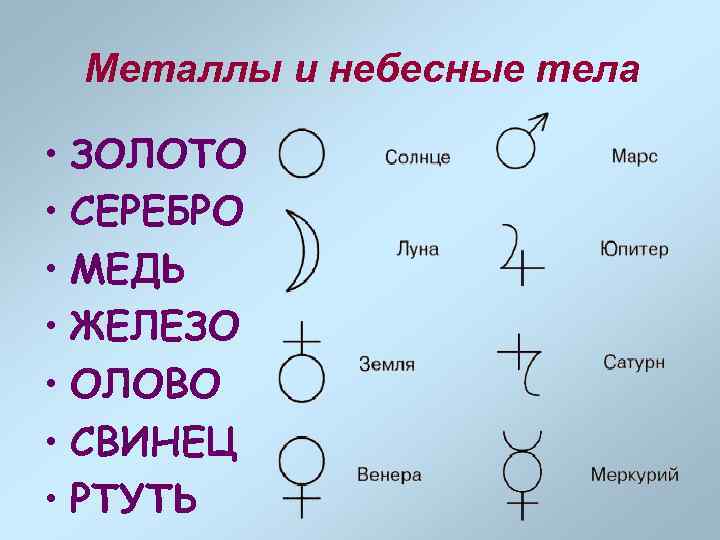 Металлы и небесные тела • ЗОЛОТО • СЕРЕБРО • МЕДЬ • ЖЕЛЕЗО • ОЛОВО • СВИНЕЦ • РТУТЬ
Металлы и небесные тела • ЗОЛОТО • СЕРЕБРО • МЕДЬ • ЖЕЛЕЗО • ОЛОВО • СВИНЕЦ • РТУТЬ
 ФИЗИЧЕСКИЕ СВОЙСВА МЕТАЛЛОВ электропроводность металлический блеск теплопроводность Ме температура кипения твердость температура плавления плотность
ФИЗИЧЕСКИЕ СВОЙСВА МЕТАЛЛОВ электропроводность металлический блеск теплопроводность Ме температура кипения твердость температура плавления плотность
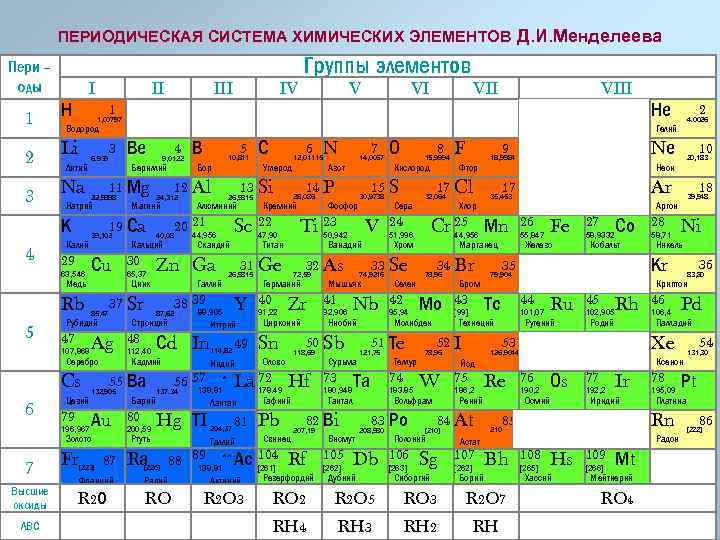 ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. Менделеева Пери – оды 1 I Н Na Литий 6. 939 3 11 Мg 22, 9898 Калий 29 39, 102 Сu Медь Rb 47 85, 47 Цезий 79 196, 967 65, 37 Ag 112, 40 55 Ва 88, 905 Аu Барий 80 200, 59 [226] 114, 82 * 138, 81 Hg ТI Rа Иттрий 49 Индий Ртуть 87 Y Кремний Таллий Zr Цирконий Sn V Мышьяк 41 92, 906 Nb VII Сурьма 73 180, 948 Та VIII Не 2 4. 0026 Свинец Rf [262] 42 95, 94 34 Br 78, 96 Мо Теллур 83 Ро Db Дубний [263] Бром [99] 52 I 26 55, 847 Со Кобальт 186, 2 101, 07 Ru Рутений Re 84 At [210] 45 102, 905 Rh Родий [262] Франций Радий Актиний Резерфордий Борий R 2 О RO R 2 O 3 RO 2 R 2 O 5 RO 3 R 2 O 7 RH 4 RH 3 RH 2 RH 36 83, 80 46 106, 4 Pd Палладий 76 190, 2 Оs 77 192, 2 Ir Иридий 78 195, 09 54 Радон 108 [265] Hs Хассий 109 [266] Мt Мейтнерий RO 4 131, 30 Рt Платина Rn 85 Bh Никель Ксенон Астат 107 Ni Xe Осмий 210 58, 71 Криптон 126, 9044 75 28 Кr 44 Рений Сиборгий 58, 9332 35 Йод Sg 27 53 78, 96 W Fe 79, 904 Тс 43 18 39, 948 Аргон Железо Технеций Полоний 106 Ar 17 Хлор 10 20, 183 Неон 35, 453 Марганец Вольфрам Висмут 105 Селен 183. 85 208, 980 Фтор 44, 956 51, 996 Nе 9 18, 9984 Cr 25 Мn 24 74 Тантал 207, 19 Сера 32, 064 Молибден 121, 75 F 17 Cl 51 Тe 82 Вi Pb Кислород 33 Se 74, 9216 50 Sb Гафний 8 15, 9994 Хром Ниобий 118, 69 Олово 88 89 ** Ас 104 138, 81 [261] Фосфор 32 As 72, 59 О 15 S 30, 9738 Ванадий 178. 49 81 Азот 50, 942 La 72 Hf Лантан 204, 37 91, 22 7 14, 0067 Ti 23 Германий 40 N 14 P 28, 086 31 Ge 38 39 12, 01115 Титан 26, 9815 Галлий 56 57 Углерод 47, 90 Скандий 137. 34 6 Sc 22 44, 956 Сd In С 13 Si 26, 9815 Алюминий Кадмий 132, 905 [223] Бор Zn Ga 87, 62 48 5 10, 811 20 21 Стронций Золото Fr 40, 08 Кальций 30 В 12 Al 24, 312 Магний 37 Sr Серебро Cs 4 9, 0122 Цинк Рубидий 107, 868 ЛВС Ве 19 Сa 63, 546 Высшие оксиды VI Гелий Бериллий Натрий К 7 V Водород 3 6 IV 1 Li 5 III 1, 00797 2 4 II Группы элементов 86 [222]
ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. Менделеева Пери – оды 1 I Н Na Литий 6. 939 3 11 Мg 22, 9898 Калий 29 39, 102 Сu Медь Rb 47 85, 47 Цезий 79 196, 967 65, 37 Ag 112, 40 55 Ва 88, 905 Аu Барий 80 200, 59 [226] 114, 82 * 138, 81 Hg ТI Rа Иттрий 49 Индий Ртуть 87 Y Кремний Таллий Zr Цирконий Sn V Мышьяк 41 92, 906 Nb VII Сурьма 73 180, 948 Та VIII Не 2 4. 0026 Свинец Rf [262] 42 95, 94 34 Br 78, 96 Мо Теллур 83 Ро Db Дубний [263] Бром [99] 52 I 26 55, 847 Со Кобальт 186, 2 101, 07 Ru Рутений Re 84 At [210] 45 102, 905 Rh Родий [262] Франций Радий Актиний Резерфордий Борий R 2 О RO R 2 O 3 RO 2 R 2 O 5 RO 3 R 2 O 7 RH 4 RH 3 RH 2 RH 36 83, 80 46 106, 4 Pd Палладий 76 190, 2 Оs 77 192, 2 Ir Иридий 78 195, 09 54 Радон 108 [265] Hs Хассий 109 [266] Мt Мейтнерий RO 4 131, 30 Рt Платина Rn 85 Bh Никель Ксенон Астат 107 Ni Xe Осмий 210 58, 71 Криптон 126, 9044 75 28 Кr 44 Рений Сиборгий 58, 9332 35 Йод Sg 27 53 78, 96 W Fe 79, 904 Тс 43 18 39, 948 Аргон Железо Технеций Полоний 106 Ar 17 Хлор 10 20, 183 Неон 35, 453 Марганец Вольфрам Висмут 105 Селен 183. 85 208, 980 Фтор 44, 956 51, 996 Nе 9 18, 9984 Cr 25 Мn 24 74 Тантал 207, 19 Сера 32, 064 Молибден 121, 75 F 17 Cl 51 Тe 82 Вi Pb Кислород 33 Se 74, 9216 50 Sb Гафний 8 15, 9994 Хром Ниобий 118, 69 Олово 88 89 ** Ас 104 138, 81 [261] Фосфор 32 As 72, 59 О 15 S 30, 9738 Ванадий 178. 49 81 Азот 50, 942 La 72 Hf Лантан 204, 37 91, 22 7 14, 0067 Ti 23 Германий 40 N 14 P 28, 086 31 Ge 38 39 12, 01115 Титан 26, 9815 Галлий 56 57 Углерод 47, 90 Скандий 137. 34 6 Sc 22 44, 956 Сd In С 13 Si 26, 9815 Алюминий Кадмий 132, 905 [223] Бор Zn Ga 87, 62 48 5 10, 811 20 21 Стронций Золото Fr 40, 08 Кальций 30 В 12 Al 24, 312 Магний 37 Sr Серебро Cs 4 9, 0122 Цинк Рубидий 107, 868 ЛВС Ве 19 Сa 63, 546 Высшие оксиды VI Гелий Бериллий Натрий К 7 V Водород 3 6 IV 1 Li 5 III 1, 00797 2 4 II Группы элементов 86 [222]
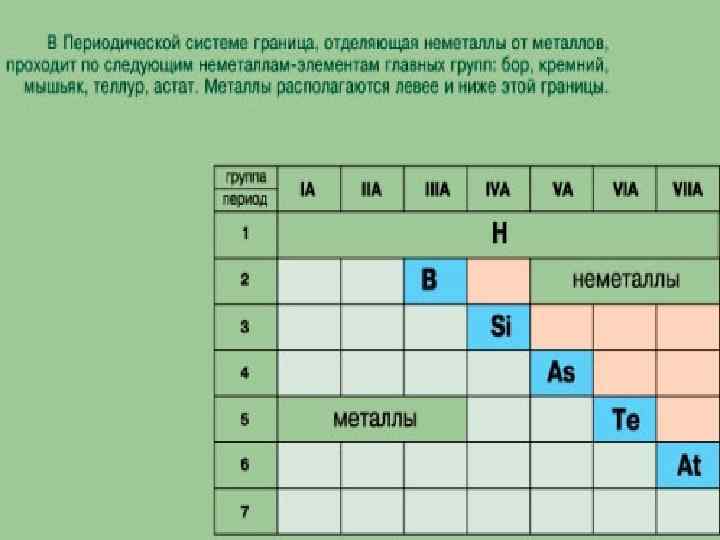
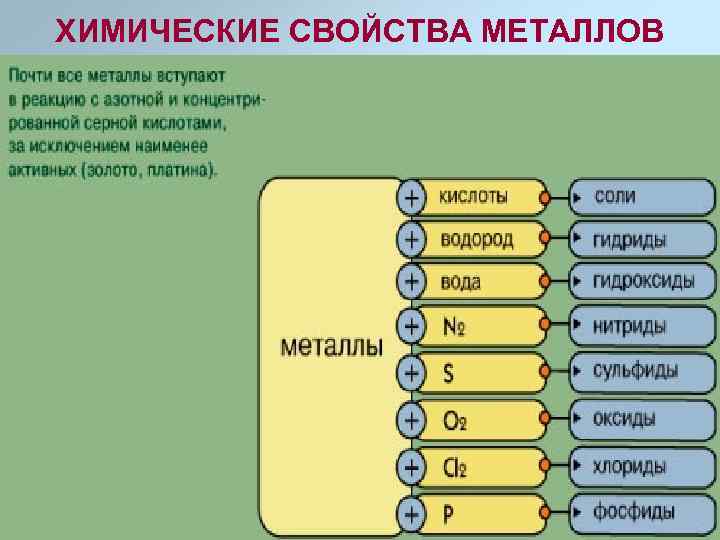 ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ

 СОЕДИНЕНИЯ Na и K в природе Na. Cl каменная соль Na 2 SO 4*10 H 2 O глауберова соль Na 2 CO 3, Na. HCO 3 сода Na, K Na. Cl*KCl сильвинит KCl*Mg Cl 2*6 H 2 O карналлит
СОЕДИНЕНИЯ Na и K в природе Na. Cl каменная соль Na 2 SO 4*10 H 2 O глауберова соль Na 2 CO 3, Na. HCO 3 сода Na, K Na. Cl*KCl сильвинит KCl*Mg Cl 2*6 H 2 O карналлит
 СОЕДИНЕНИЯ Са и Mg в природе Ca. CO 3 Ca. SO 4*2 H 2 мел, мрамор, известняк гипс Ca 3 (PO 4)2 Са, Mg фосфорит 2 Mg. O*4 Si. O 2* H 2 O тальк Ca. CO 3*Mg CO 3 доломит Mg. CO 3 магнезит Ca. O* Mg. O*4 Si. O 2 асбест
СОЕДИНЕНИЯ Са и Mg в природе Ca. CO 3 Ca. SO 4*2 H 2 мел, мрамор, известняк гипс Ca 3 (PO 4)2 Са, Mg фосфорит 2 Mg. O*4 Si. O 2* H 2 O тальк Ca. CO 3*Mg CO 3 доломит Mg. CO 3 магнезит Ca. O* Mg. O*4 Si. O 2 асбест
 СОЕДИНЕНИЯ Al в природе Al 2 O 3*n H 2 O Na 3 Al. F 6 боксит криолит Al Al 2 O 3 корунд, рубин, сапфир К Al(SO 4)2 алюмокалиевые квасцы
СОЕДИНЕНИЯ Al в природе Al 2 O 3*n H 2 O Na 3 Al. F 6 боксит криолит Al Al 2 O 3 корунд, рубин, сапфир К Al(SO 4)2 алюмокалиевые квасцы
 Темы самостоятельных исследований: • История древних цивилизаций – история металлов и их сплавов. • Семь «доисторических металлов» , • «Металл – всех недр владыка» . • Использование металлов в искусстве. • Использование физических свойств металлов в быту и технике. • «Болезни» металлов и как их лечить. • Роль металлов в организме человека. • Свинцовое загрязнение. • Серебряная вода.
Темы самостоятельных исследований: • История древних цивилизаций – история металлов и их сплавов. • Семь «доисторических металлов» , • «Металл – всех недр владыка» . • Использование металлов в искусстве. • Использование физических свойств металлов в быту и технике. • «Болезни» металлов и как их лечить. • Роль металлов в организме человека. • Свинцовое загрязнение. • Серебряная вода.


