ПРИНЦИПЫ МОЛЕКУЛЯРНОЙ ОНКОЛОГИИ vers.4.pptx
- Количество слайдов: 59

Государственное бюджетное образовательное учреждение высшего профессионального образования «Российский национальный исследовательский медицинский университет имени Н. И. Пирогова» Министерства здравоохранения Российской Федерации Кафедра онкологии и лучевой терапии лечебного факультета ОСНОВЫ МОЛЕКУЛЯРНОЙ ОНКОЛОГИИ лекция 29. 08. 2013

Молекулярная онкология • Это междисциплинарная область онкологии, которая объединяет молекулярную биологию злокачественных новообразований, медицинскую химию и онкологию. • Она изучает злокачественные новообразования на молекулярном уровне. • Практическое значение молекулярной онкологии включает: – Поиск новых механизмов роста и прогрессии злокачественных новообразований, включая валидацию новых мишеней для таргетной терапии – Разработка новых препаратов для мишень-направленной терапии злокачественных новообразований (таргетной терапии) – Молекулярное стадирование опухолей и прогнозирование течения болезни и эффективности противоопухолевой терапии – Использование таргетной терапии в клинической онкологии 29. 08. 2013

Молекулярная биология рака 29. 08. 2013

Основные молекулярные механизмы возникновения, роста и прогрессии злокачественных новообразований (Weinberg, 2005) • независимость от ростовых сигналов • нечувствительность к сигналам, блокирующим деление • уклонение от программированной клеточной гибели (апоптоза) • возможность неограниченного деления • адекватный ангиогенез • способность к тканевой инвазии и метастазированию. 29. 08. 2013

Независимость от ростовых сигналов • Гиперактивность рецепторов факторов роста (EGFR, PDGFR, и другие) и их сигнальных путей позволяют опухолевой клетке постоянно получать сигнал для стимуляции деления 29. 08. 2013

Программированная клеточная гибель (апоптоз) • Ингибирование апоптоза ассоциировано с химирезистентностью к противоопухолевой терапии 29. 08. 2013
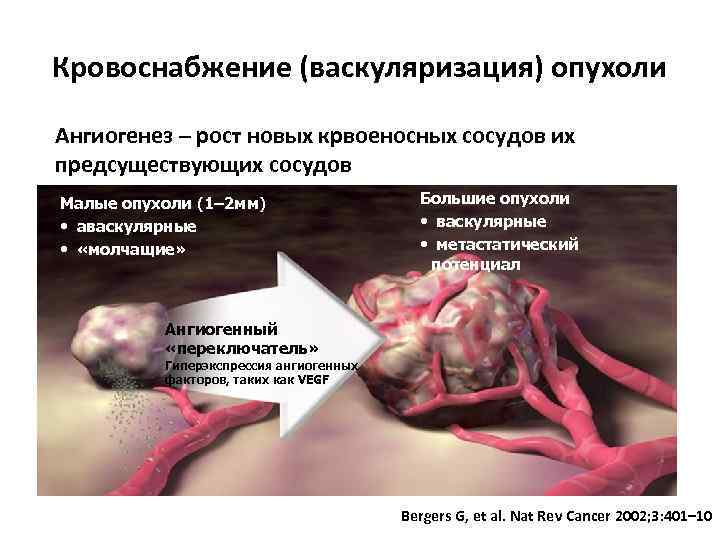
Кровоснабжение (васкуляризация) опухоли Ангиогенез – рост новых крвоеносных сосудов их предсуществующих сосудов Малые опухоли (1– 2 мм) • аваскулярные • «молчащие» Большие опухоли • васкулярные • метастатический потенциал Ангиогенный «переключатель» Гиперэкспрессия ангиогенных факторов, таких как VEGF Bergers G, et al. Nat Rev Cancer 2002; 3: 401– 10
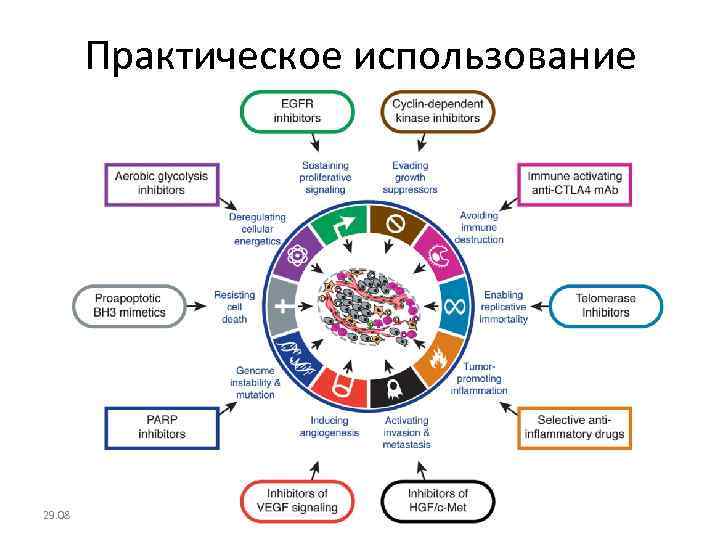
Практическое использование 29. 08. 2013

Молекулярно-биологические маркеры злокачественных новообразований 29. 08. 2013

Молекулярно-биологические маркеры (биомаркеры) • Молекулярно-биологические маркеры опухолей – это определенные хромосомные и генные мутации, а также экспрессия различных молекул клеточного и иного происхождения, подвергающихся качественным и(или) количественным специфическим изменениям, и участвующих в развитии и прогрессии злокачественных заболеваний.

Биомаркеры – это молекулы, которые участвуют в патологических клеточных процессах, определяющих способность клетки к злокачественному росту • независимость от ростовых сигналов • нечувствительность к сигналам, блокирующим деление • уклонение от программированной клеточной гибели (апоптоза) • возможность неограниченного деления • адекватный ангиогенез • способность к тканевой инвазии и метастазированию.

Молекулярно-биологические опухолевые маркеры для прогноза и лечения больных злокачественными новообразованиями • Предсказание безрецидивной и общей выживаемости больных • Предсказание лечебного эффекта традиционной химиотерапии и выбор рационального лечения. • Специфические молекулярно-биологические мишени для направленной (таргетной) терапии

Биомаркеры могут быть измерены на различном молекулярном уровне: • • • ДНК РНК Белок Клетка Ткань

ДНК биомаркеры • • Мутации различных генов (B-RAF, EGFR) Делеции в генах Амплификация генов (HER 2) Метилирование генов (AGT) 29. 08. 2013

РНК биомаркеры • м. РНК • микро. РНК (предотвращают трансляцию генов в белки) 29. 08. 2013

Белковые биомаркеры • Гиперэкспрессия белка (HER 2, Ki-67) • Отсутствие экспрессии белка • Качественные нарушения в экспрессии белка (NFk. B) 29. 08. 2013

Детекция биомаркеров • «Циркулирующие» биомаркеры определяют в крови больных • «Наследственные» биомаркеры определяют на нормальных клетках • Биомаркеры опухолевых клеток определяют на опухолевых клетках 29. 08. 2013

Типы биомаркеров • Прогностические – предсказывают появление метастазов и безрецидивную и общую выживаемость больных после удаления первичной опухоли в отсутствии дополнительного противоопухолевого лечения • Предсказывающие - предсказывают чувствительность или резистентность опухоли к определенной противоопухолевой терапии – Биомаркер является непосредственно мишенью для противоопухолевого препарата (РЭ/РП и эндокринотерапия; HER 2/neu и Герцептин) – Биомаркер является критическим индикатором сигнального пути или процесса, вовлеченного в активность препарата (н-р, мутации гена K-Ras и анти-EGFR терапия) 29. 08. 2013
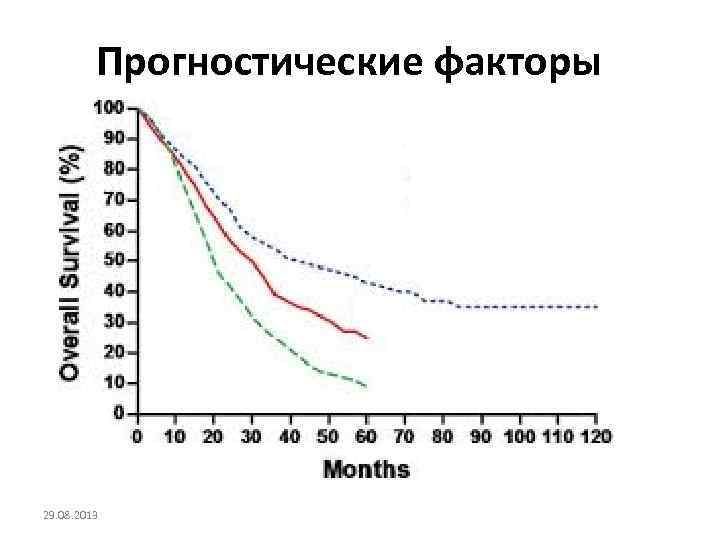
Прогностические факторы 29. 08. 2013

Практическое использование опухолевых биомаркеров • Риск развития злокачественных новообразований • Скрининг • Дифференциальный диагноз • Прогноз • Предсказание эффективности • Мониторинг 29. 08. 2013

Прогностические факторы при РМЖ – Исследования для клинического использования • ЭР, ПР, Ki 67, HER 2 • Генетические тесты – Mammaprint/Oncotype Dx – BRCA 1/2 – Как использовать полученные данные? – Взаимодействие «патоморфолог-онколог» • Многофакторный подход к диагностике

Развитие молекулярной диагностики рака молочной железы Определение рецепторов эстрогенов и прогестерона (80 -е годы) Определение рецепторов HER 2/neu (90 -е годы) Определение субтипа РМЖ (5 маркеров) (2005 год) Генетическая характеристика рака молочной железы (70 или 21 ген)
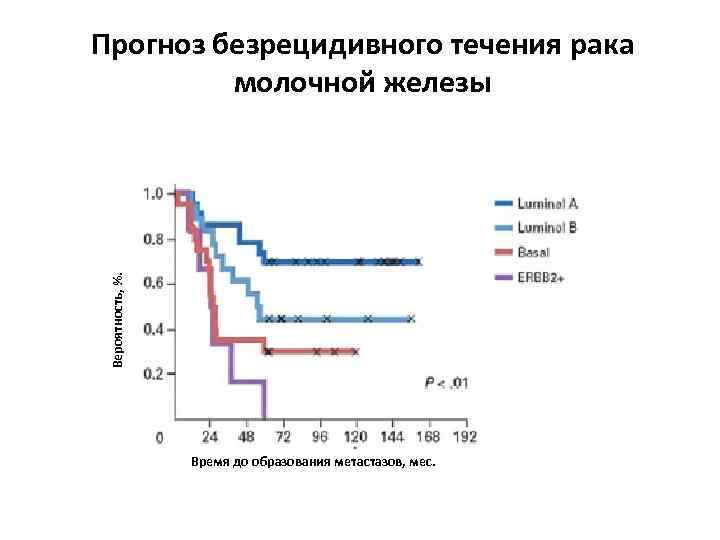
Вероятность, %. Прогноз безрецидивного течения рака молочной железы Время до образования метастазов, мес.

Генные чипы для прогнозирования рака молочной железы • Onco. Type DX при лечении рака молочной железы - тест для тестирования более 70 биомаркеров для определения метастазирования и ответа на химиотерапию • Mammaprint при лечении рака молочной железы - nест для тестирования 21 биомаркеров для определения метастазирования и ответа на химиотерапию

Молекулярно-биологические маркеры при колоректальном раке • Маркеры, связанные с факторами роста: • Мутации в гене EGFR • Мутации в гене K-Ras • PTEN • Маркеры, связанные с резистентностью к фторпиримидинам: • Тимидилат синтетаза • Тимидин фосфорилаза • Дигидропиримидин дегидрогеназа • Маркеры ангиогенеза: • VEGF • Количество микрососудов в опухоли

Выбор рационального противоопухолевого химиотерапевтического лечения 29. 08. 2013
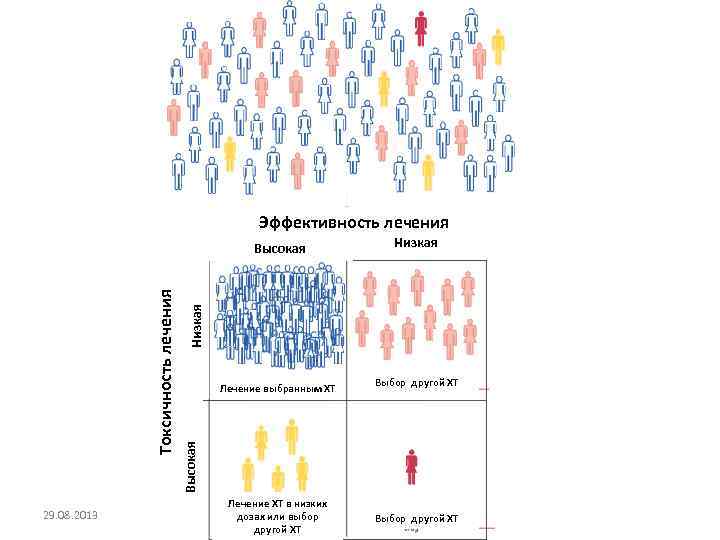
Эффективность лечения 29. 08. 2013 Низкая Лечение выбранным ХТ Выбор другой ХТ Высокая Токсичность лечения Высокая Лечение ХТ в низких дозах или выбор другой ХТ Выбор другой ХТ

Маркеры, предсказывающие резистентность к 5 -фторурацилу • Тимидилат синтетаза • Тимидин фосфорилаза • ДПД

Тимидилат синтетаза • Фермент участвует в синтезе ДНК. • Тимидилат синтетаза является мишенью для 5 фторурацила, который связываясь с ней ингибирует деление клеток. • Экспрессия ТС в опухолевой ткани связана с: – С высокой пролиферативной активностью опухоли, – Наличием метастазов в лимфоузлах, – Укорочением безрецидивной и общей выживаемости больных, – Резистентностью к 5 -фторурацилу.

Тимидин фосфорилаза • Тромбоцитарный фактор роста эндотелия сосудов (PD-ECGF), • Стимулирует неоангиогенез в опухоли и ингибирует апоптоз в опухолевых клетках • Присутствие тимидин фосфорилазы в опухоли коррелирует с: • Быстрым ростом опухоли • Высоким инвазивным потенциалом, • Плохим прогнозом
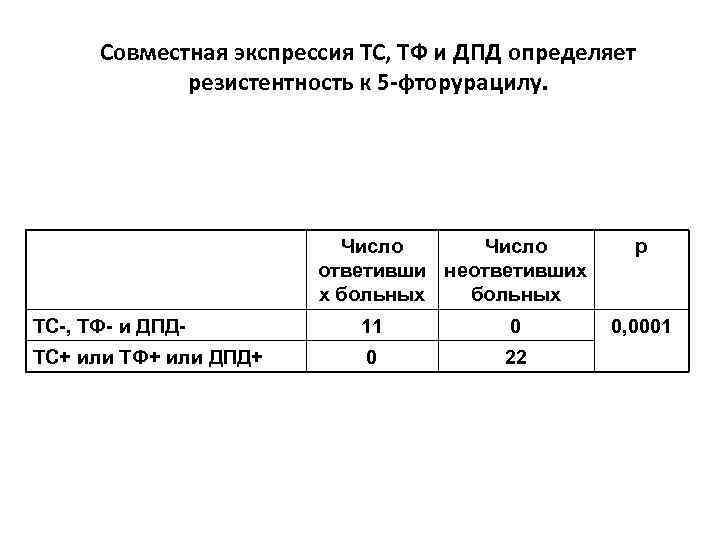
Совместная экспрессия ТС, ТФ и ДПД определяет резистентность к 5 -фторурацилу. Число ответивши неответивших х больных ТС-, ТФ- и ДПД- 11 0 ТС+ или ТФ+ или ДПД+ 0 22 р 0, 0001

Маркеры, предсказывающие резистентность к платина-содержащим препаратам • • • ERCC-1 XRCC-1 Глютатион трансфераза пи Xeroderma Pigmentosum group D (XPD) EGFR
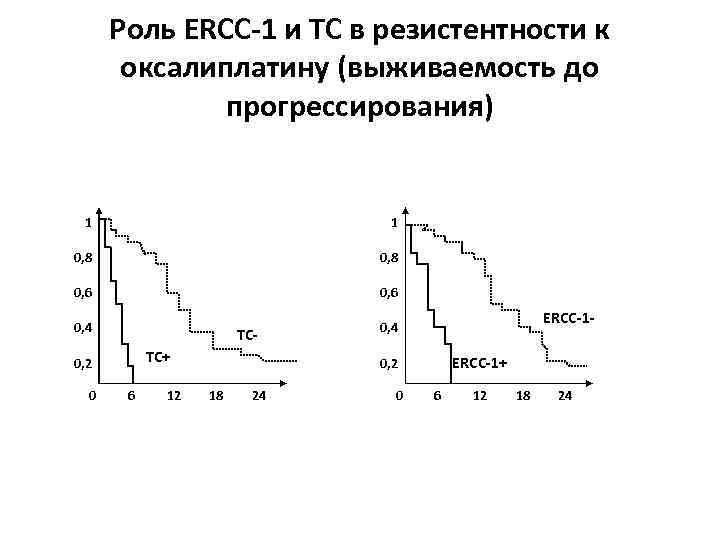
Роль ERCC-1 и ТС в резистентности к оксалиплатину (выживаемость до прогрессирования) 1 1 0, 8 0, 6 0, 4 ТСТС+ 0, 2 0 6 12 ERCC-1+ 0, 2 18 24 0 6 12 18 24

Другие иммуногистохимические маркеры химиорезистентности Маркер Опухоли Высокая экспрессия ассоциирована АГТ (AGT, MGMT) Меланома, глиомы Резистентность к нитрозомочевинам, темозоломиду Tubulin beta НМРЛ, РМЖ Резистентность к таксанам Topoisomerase 2 a РМЖ, саркомы Чувствительностььк доксорубицину, этопозиду Topoisomerase 1 РМЖ, РТК Чувствительность к ингибиторам топоизомеразы 1 (иринотекан, топотекан) RRM 1 НМРЛ Резистентность к гемцитабину 29. 08. 2013

Фармакогеномика и маркеры предсказания токсичности химиотерапии

• Фармакогеномика изучает наследственные, герминальные мутации (SNP) в генах, ответственных за метаболизм препаратов или действующих как прямая или непрямая мишень для препаратов. • Эти гены могут играть важную роль в оценке эффективности и токсичности определенных противоопухолевых препаратов 29. 08. 2013

ДПД синдром (клинические проявления) • наследственный аутосомно-рецессивный синдром, который может быть связан с развитием потенциально летальных осложнений терапии 5 -ФУ • неожиданно тяжелые явления токсичности: – гематологической (лейкопения, включая фибрильная нейтопения, анемия, тромбоцитопения) – гастроинтестинальной (мукозиты, стоматиты, диарея, тошнота и рвота) – реже встречается кожная токсичность (синдром «руки-ноги» , потеря волос и сухость кожи) • Встречается у 5 -15% больных, получающих 5 -ФУ или его аналоги (Капецитабин) 29. 08. 2013
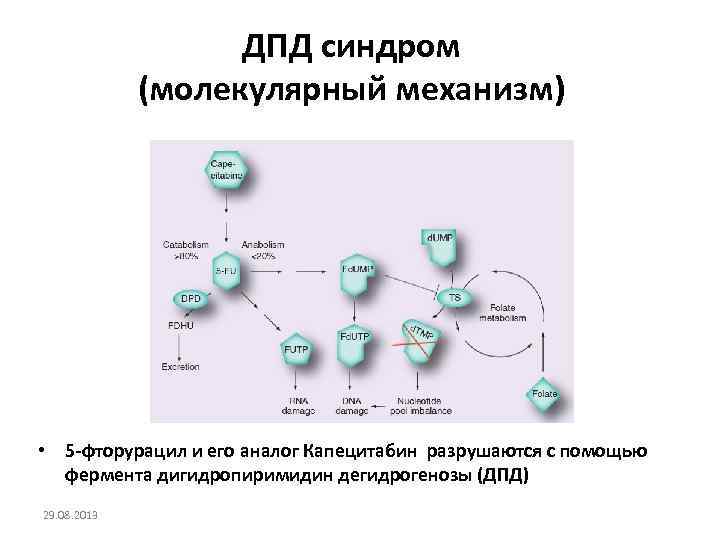
ДПД синдром (молекулярный механизм) • 5 -фторурацил и его аналог Капецитабин разрушаются с помощью фермента дигидропиримидин дегидрогенозы (ДПД) 29. 08. 2013

ДПД синдром (генетика) • Ген ДПД (DPD, DPYD) локализуется на хромосоме 1 p 22. Это сравнительно большой ген (843 kb), включающий 23 экзона. • Пациенты, гомозиготные по селективным неактивным аллелям гена ДПД, не способны выводить эти агенты и даже введение очень малых доз препаратов ассоциировано с тяжелой и даже смертельной токсичностью. • Исследования показывают, что не менее 3 -5% популяции имеют низкую активность фермента ДПД или его полное отсутствие. Среди больных с высокой токсичностью 5 -ФУ 70 -80% больных имеют низкую активность фермента ДПД или его полное отсутствие. • На сегодняшний день выявлено более 20 различных SNP гена ДПД, ассоциированные с тяжелой токсичностью. • К сожалению, доступные и точные тесты для этого наследственного синдромы широко не распространены. 29. 08. 2013
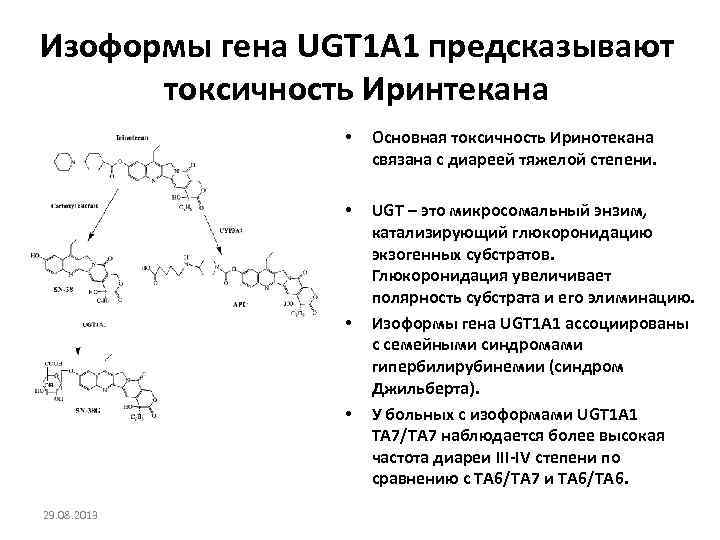
Изоформы гена UGT 1 A 1 предсказывают токсичность Иринтекана • Основная токсичность Иринотекана связана с диареей тяжелой степени. • UGT – это микросомальный энзим, катализирующий глюкоронидацию экзогенных субстратов. Глюкоронидация увеличивает полярность субстрата и его элиминацию. Изоформы гена UGT 1 A 1 ассоциированы с семейными синдромами гипербилирубинемии (синдром Джильберта). У больных с изоформами UGT 1 A 1 TA 7/TA 7 наблюдается более высокая частота диареи III-IV степени по сравнению с ТА 6/ТА 7 и ТА 6/ТА 6. • • 29. 08. 2013

Таргетная терапия 29. 08. 2013

• Таргетные препараты – это мишеньнаправленные противоопухолевые препараты, блокирующие определенные рецепторы и сигнальные белки на опухолевых клетках. • Или это новый класс лекарственных средств, имеющих целенаправленное действие строго на определённый сигнальный путь или рецептор поверхности клетки, участвующий в развитии и росте опухоли. 29. 08. 2013

Типы таргетных препаратов • Гуманизированные моноклональные антитела (Герцептин, Авастин и другие) • Малые синтетические молекулы (Гливек, Сутент, Сунитиниб, Зелбораф и другие) • Иммуноконьюгаты (Кадсула) 29. 08. 2013

Рецепторы факторов роста как мишени для направленной терапии • Рецепторы эпидермального фактора роста – EGFR – HER 2 • Другие рецепторы роста: C-Kit, PDGFR • Нижележащие сигнальные молекулы: B-RAF • Рецепторы и лиганд сосудистого фактора роста – VEGFR 2
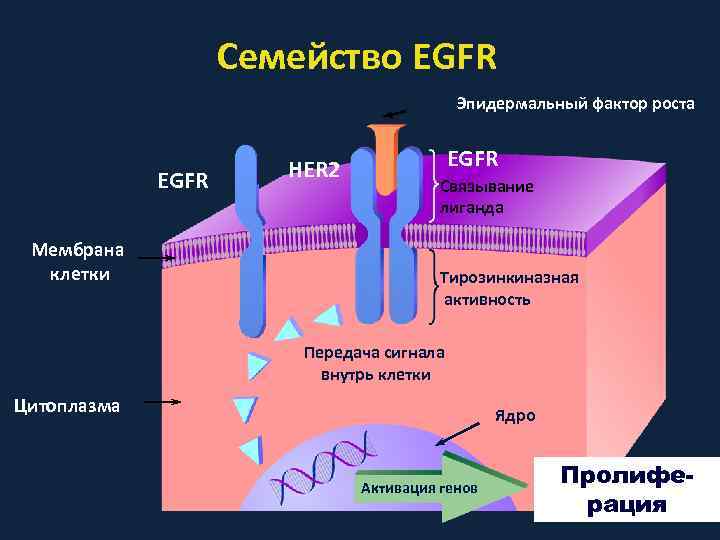
Семейство EGFR Эпидермальный фактор роста EGFR Мембрана клетки HER 2 EGFR Связывание лиганда Тирозинкиназная активность Передача сигнала внутрь клетки Цитоплазма Ядро Активация генов Пролиферация

Ингибиторы EGFR • Цетуксимаб (С 225) представляет собой рекомбинантое химерное моноклональное антитело, обладающее высокой специфичностью к внеклеточному домену EGFR и, соответственно, способное конкурировать с естественными лигандами (EGF; TGF-a) за связывание с рецептором. • Иресса – малая синтетическая молекула, блокирующая активность EGFR рецептора. • Лапатиниб (Тайверб) - новый двойной, селективный ингибитор внутриклеточной тирозинкиназы, связывающийся с EGFR и HER 2 рецепторами. 29. 08. 2013

Ингибиторы HER 2 рецепторов • Герцептин (Трастузумаб) - рекомбинантное гуманизированное моноклональное антитело, которое блокирует активацию рецептора HER 2/neu • Кадсула (Трастузумаб-DM 1) – комплекс антитела против рецптора HER 2 с цитотоксическим агентом DM 1, влияющим на микротрубочки (иммуно-коньюгат). Разрешен FDA (США) и в Европе в феврале 2013 года • Перьета (Пертузумаб) - рекомбинантное гуманизированное моноклональное антитело к экстрацеллюлярному домену HER 2. Ингибитор димеризации рецепторов EGF. Разрешен FDA (США) и в Европе в июне 2012 года 29. 08. 2013
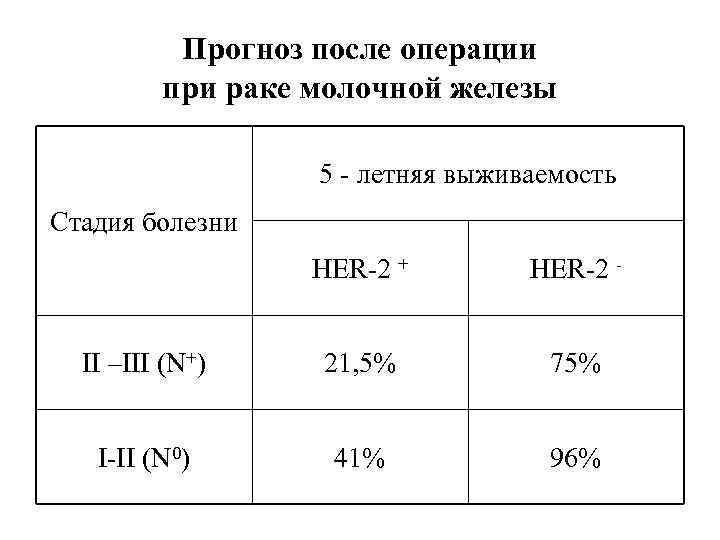
Прогноз после операции при раке молочной железы 5 - летняя выживаемость Стадия болезни HER-2 + HER-2 - II –III (N+) 21, 5% 75% I-II (N 0) 41% 96%

Гиперэкспрессия HER-2+ при раке молочной железы • Уменьшение безрецидивной и общей выживаемости • Уменьшение эффективности химиотерапии и эндокринотерапии • Ухудшение прогноза даже при ранних стадиях
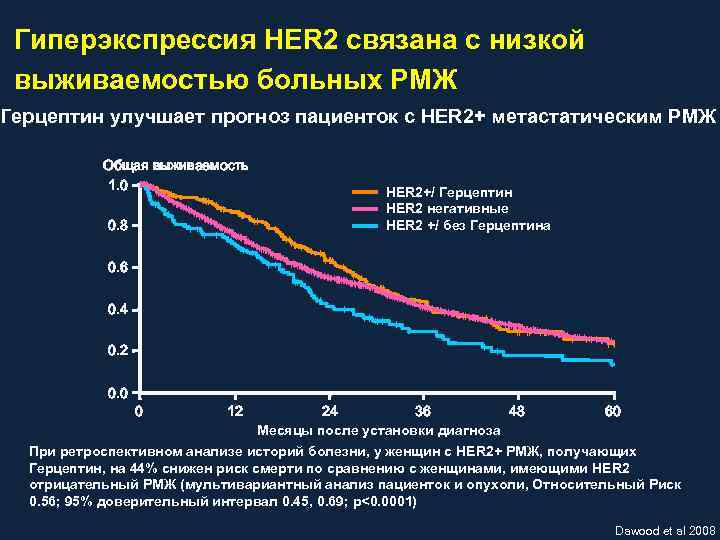
Гиперэкспрессия HER 2 связана с низкой выживаемостью больных РМЖ Герцептин улучшает прогноз пациенток с HER 2+ метастатическим РМЖ Общая выживаемость 1. 0 0. 8 HER 2+/ Герцептин HER 2 негативные HER 2 +/ без Герцептина 0. 6 0. 4 0. 2 0. 0 0 12 24 36 48 60 Месяцы после установки диагноза При ретроспективном анализе историй болезни, у женщин с HER 2+ РМЖ, получающих Герцептин, на 44% снижен риск смерти по сравнению с женщинами, имеющими HER 2 отрицательный РМЖ (мультивариантный анализ пациенток и опухоли, Относительный Риск 0. 56; 95% доверительный интервал 0. 45, 0. 69; p<0. 0001) Dawood et al 2008

Авастин (Bevacizumab) моноклональные гуманизированные антитела против VEGF

Потенциальные эффекты ингибирования VEGF • Блокирование роста новых опухолевых микрососудов – блокирование роста первичного очага и метастазов • Регрессия опухолевой кровеносной сети и «нормализация» проницаемости сосудов и внтуриопухолевого давления – улучшение доставки других противоопухолевых агентов • Регрессия сосудов – возможность перевода опухолей в «покоящиеся» Jain RK. Nat Med 2001; 7: 987 -9 Willett CG, et al. Nat Med 2004; 10: 145 -7
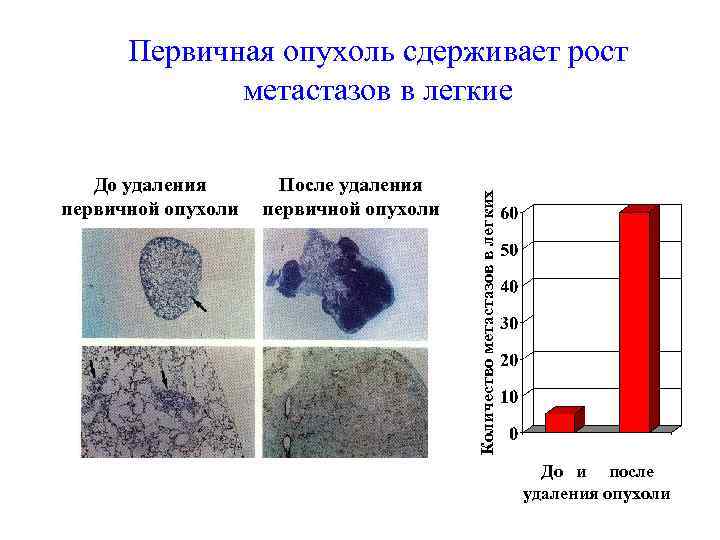
До удаления первичной опухоли После удаления первичной опухоли Количество метастазов в легких Первичная опухоль сдерживает рост метастазов в легкие До и после удаления опухоли
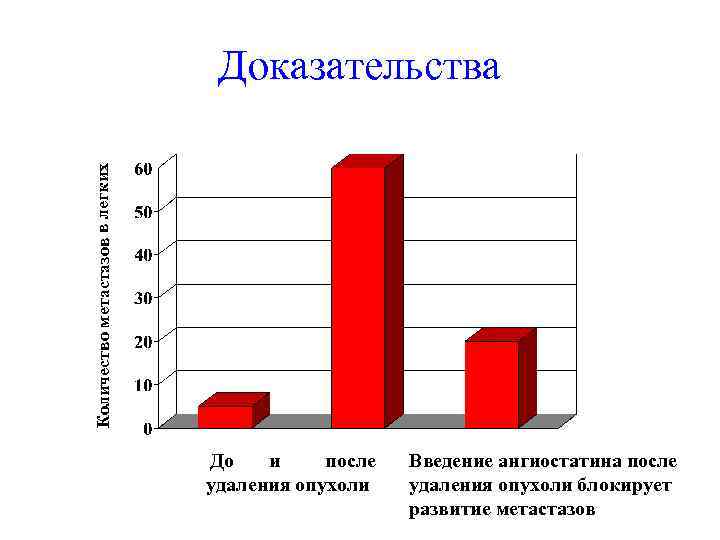
Количество метастазов в легких Доказательства До и после удаления опухоли Введение ангиостатина после удаления опухоли блокирует развитие метастазов
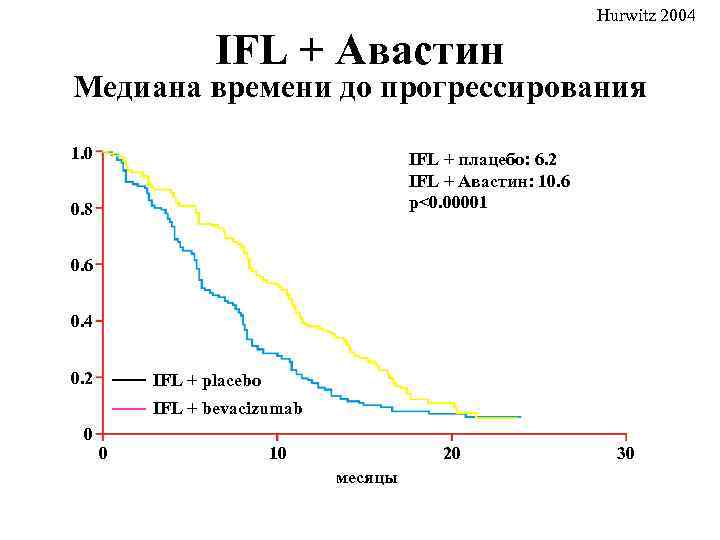
IFL + Авастин Hurwitz 2004 Медиана времени до прогрессирования 1. 0 IFL + плацебо: 6. 2 IFL + Авастин: 10. 6 p<0. 00001 0. 8 0. 6 0. 4 0. 2 IFL + placebo IFL + bevacizumab 0 0 10 20 месяцы 30
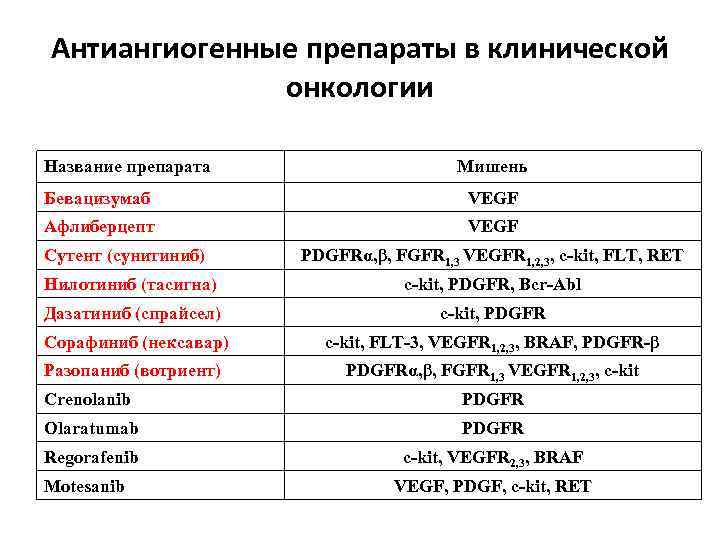
Антиангиогенные препараты в клинической онкологии Название препарата Мишень Бевацизумаб VEGF Афлиберцепт VEGF Сутент (сунитиниб) PDGFRα, β, FGFR 1, 3 VEGFR 1, 2, 3, c-kit, FLT, RET Нилотиниб (тасигна) c-kit, PDGFR, Bcr-Abl Дазатиниб (спрайсел) c-kit, PDGFR Сорафиниб (нексавар) c-kit, FLT-3, VEGFR 1, 2, 3, BRAF, PDGFR-β Разопаниб (вотриент) PDGFRα, β, FGFR 1, 3 VEGFR 1, 2, 3, c-kit Crenolanib PDGFR Olaratumab PDGFR Regorafenib c-kit, VEGFR 2, 3, BRAF Motesanib VEGF, PDGF, c-kit, RET

Ингибиторы B-RAF для лечения меланомы • Активирующие мутации в гене B-RAF V 600 встречаются в 40 -60% случаев и ассоциированы с плохим прогнозом течения болезни и химиорезистентностью • Вемурафениб (PLX 4032, Зелбораф) - ингибитор BRAF сигнального пути 29. 08. 2013

Следует ли продолжать лечение таргетными препаратами прогрессировании (со сменой режима химиотерапии)? Частота лечебного эффекта Изменение режима химиотерапии Трастузумаб продолжен Трастузумаб отменен 48% 27%

Всегда ли нужно определять мишень до назначения таргетных препаратов? Экспрессия мишени Ответ мишени Общая эффективность 100 больных 90% 80% 72% 100 больных 50% 80% 40% 100 больных 25% 80% 20% 100 больных 10% 8% • Ингибиторы HER 2, блокаторы B-RAF – тестируется в обязательном порядке • Ингибиторы ангиогенеза – наличие мишени не предсказывает эффективность лечения 29. 08. 2013
ПРИНЦИПЫ МОЛЕКУЛЯРНОЙ ОНКОЛОГИИ vers.4.pptx