9_ Галогены.ppt
- Количество слайдов: 25

ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ СРЕДНЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «КРАСНОЯРСКИЙ МЕДИКО-ФАРМАЦЕВТИЧЕСКИЙ КОЛЛЕДЖ» МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ Лекция № 9 Галогены Преподаватель Ростовцева Л. В. , 2011 г.

План: 1. Общая характеристика элементов VII А группы периодической системы Д. И. Менделеева. 2. Распространение в природе и физические свойства галогенов 3. Хлор, способы получения, химические свойства. 4. Кислородные соединения хлора. 5. Галогеноводороды. Качественные реакции на хлорид, бромид и иодид-ионы.

1. Общая характеристика элементов VII А группы периодической системы Д. И. Менделеева. Элементы 7 А группы (галогены) фтор 9 F хлор 17 Cl бром 35 Br йод 53 I астат 85 At

Строение электронной оболочки ↑↓ пs 2 ↑↓ ↑↓ ↑ … пs 2 np 5 Распределение электронов внешнего энергетического уровня в основном состоянии np 5 Галогены относятся к p- элементам. Кроме фтора, у атомов всех галогенов возможно возбужденное состоянии поэтому галогены в соединениях могут проявлять валентность I, III, V, VII.
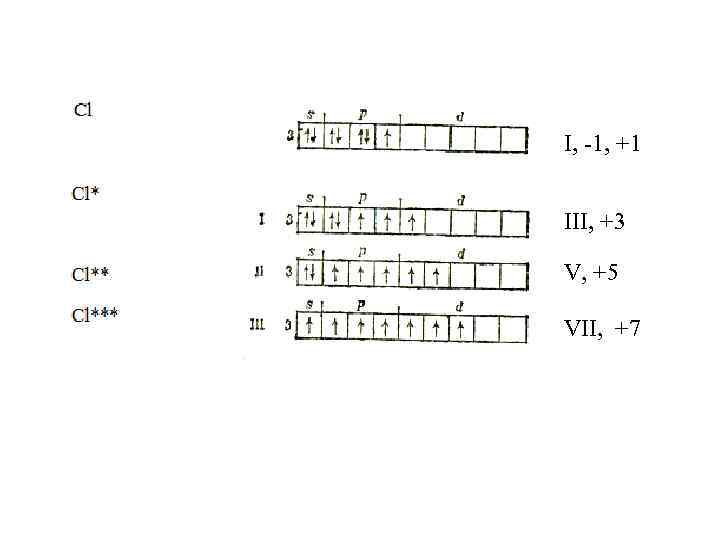
I, -1, +1 III, +3 V, +5 VII, +7

В соединениях с водородом и металлами галогены проявляют характерную степень HCl- окисления -1 Ca. Br 2 - Во всех кислородсодержащих соединениях галогены, кроме фтора, проявляют положительные степени окисления +1, +3, +5, +7 HCl+1 O HCl+3 O 2 HCl+5 O 3 HCl+7 O 4

фтор 9 F радиус атома ↑ хлор 17 Cl неметаллические свойства ↓ бром 35 Br электроотрицательность ↓ йод 53 I окислительные свойства ↓ астат 85 At восстановительные свойства ↑

Ионы галогенов (кроме F-) способны отдавать электроны и поэтому являются восстановителями Восстановительная способность галогенид-ионов увеличивается в ряду: Cl- → Br - → I-

В свободном состоянии галогены существуют в виде двух атомных молекул, атомы галогенов связаны друг с другом ковалентной неполярной связью.

2. Распространение в природе и физические свойства галогенов Важнейшие природные соединения галогенов флюорит Ca. F 2 криолит Nаз [Аl. F 6] фторапатит Са 5(РО 4)3 F каменная соль (галит) Na. Cl сильвинит KCl ∙ Na. Cl Много хлора (в виде различных хлоридов) содержится в морской воде. Основными природными источникам брома и йода являются вода озер и морская вода. Соединения йода имеются также в буровых водах, сопутствующих нефти.

Физические свойства галогенов Ядовиты, с резким запахом фтор F 2 – бледно-желтый газ, хлор Cl 2 - зелено-желтый газ, легко сжижающийся бром Br 2 – тяжелая красно-бурая жидкость йод I 2 - серо-фиолетовые кристаллы с металлическим блеском

Растворимость галогенов в воде в подгруппе сверху вниз уменьшается. хлор бром

3. Хлор, способы получения, химические свойства. Получение хлора 1. Электролиз водного раствора или расплава хлорида натрия 2 Na. Cl (электрический ток) → 2 Na + Cl 2 2. В лаборатории 4 НСl + Мn. О 2 = Мn. C 12+ Cl 2 + 2 Н 2 О 16 HCI + 2 KMn. O 4 = 2 КСl + 2 Mn. Cl 2 + 5 Cl 2 + 8 Н 2 О 2 CI- - 2 е = Cl 20 2 Mn. O 4 – + 8 Н+ + 5 е = Mn 2+ + 4 Н 2 О 5 10 5 2 10 CI- + 2 Mn. O 4 – + 16 Н+ = 5 Cl 20 + 2 Mn 2+ + 8 Н 2 О

Химические свойства хлора 1. Взаимодействие с металлами 2 Na + Cl 2 = 2 Na. Cl 2. Взаимодействие с неметаллами (водородом, фосфором, серой и др. ) свет Н 2 + Cl 2 = 2 HCl Механизм реакции цепной, свободнорадикальный Cl 2 → 2 Cl. + Н 2 = НСl + H. Н. + Cl 2 = НСI + Cl.

3. Взаимодействие с водой Cl 2 + H 2 O = НСl + НCl. O 4. Взаимодействие со щелочами (ОВР диспропорционирования) Cl 20 + 2 КОН = КСl- + КСl+1 O + Н 2 О гипохлорит калия при нагревании (до 100 0 С) 3 Сl 2 + 6 КОН = 5 КСl + КСl. O 3 + 3 Н 2 О хлорат калия 2 Сl 2 + 2 Са(ОН)2 = Са. Сl 2 + Са(Сl. O)2 + 2 Н 2 О «хлорная известь»

5. Окислительные свойства Свободные галогены - сильные окислители Окислительная способность галогенов снижается в ряду F 2 - С 12 - Вr 2 - I 2 2 КВr + Сl 2 = Br 2 + 2 KCl 2 КI + Сl 2 = I 2 + 2 KCl Br 2+ 5 Cl 2 + 12 KOH = 2 KBr. O 3 + 10 KCl + 6 H 2 O Br 2 0+ 12 OH- - 10 е = 2 Br. O 3 - + 6 H 2 O Cl 20 + 2 е = 2 Cl- 10 1 2 5 Br 2 0+ 12 OH- + 5 Cl 2 = 2 Br. O 3 - + 6 H 2 O + 10 Cl-
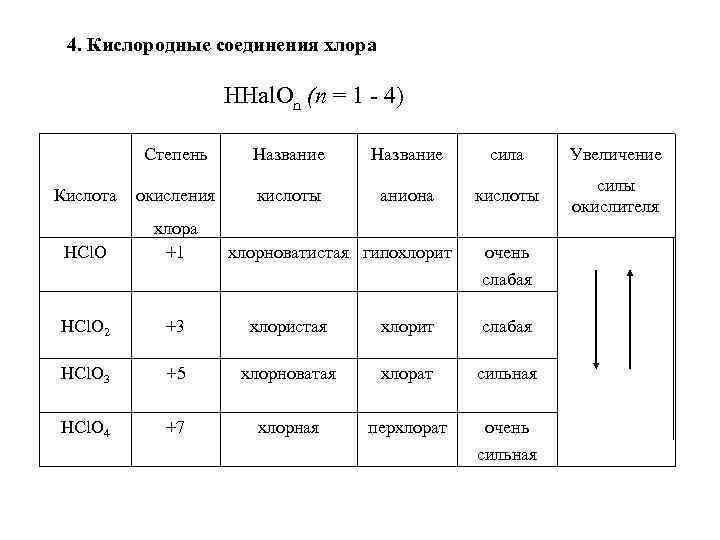
4. Кислородные соединения хлора ННаl. On (п = 1 - 4) Степень Название сила Увеличение Кислота окисления кислоты аниона кислоты силы окислителя НCl. O хлора +1 HCl. O 2 +3 хлористая хлорит слабая HCl. O 3 +5 хлорноватая хлорат сильная HCl. O 4 +7 хлорная перхлорат очень сильная хлорноватистая гипохлорит очень слабая
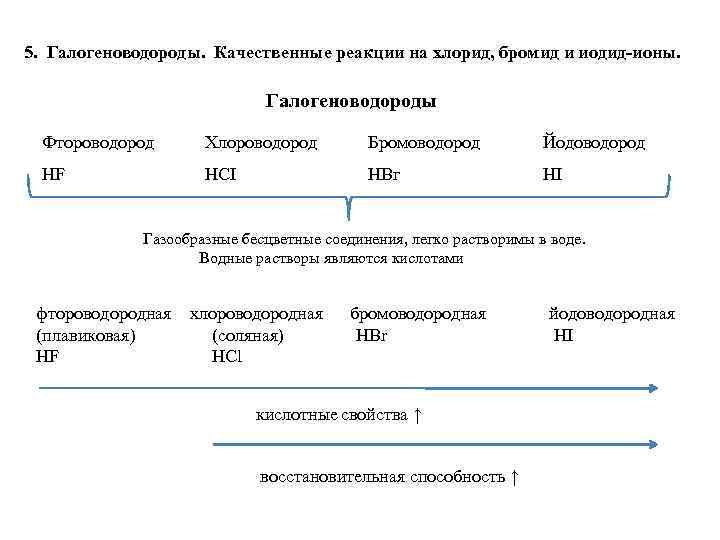
5. Галогеноводороды. Качественные реакции на хлорид, бромид и иодид-ионы. Галогеноводороды Фтороводород Хлороводород Бромоводород Йодоводород HF HCI НВг HI Газообразные бесцветные соединения, легко растворимы в воде. Водные растворы являются кислотами фтороводородная (плавиковая) HF хлороводородная (соляная) HCl бромоводородная HBr кислотные свойства ↑ восстановительная способность ↑ йодоводородная HI

Получение галогеноводородов 1. Фтороводород HF получают по реакции между фторидом кальция и концентрированной серной кислотой: Ca. F 2+ H 2 SO 4 = Ca. SO 4 + 2 HF Фтороводород и соответствующая кислота – очень едкие вещества их нельзя хранить в стеклянных сосудах так как HF взаимодействует с оксидом кремния (IV), который входит в состав стекла: 4 HF+ Si. O 2 == Si. F 4 + 2 H 2 O

2. Основной метод получения хлороводорода HCI в промышленности Н 2 + Cl 2 = 2 HCl В лаборатории Na. Cl тв + H 2 SO 4 конц= Na. HSO 4 + НСl 3. Бромоводород НВr и йодоводород HI получают в промышленности из простых веществ в присутствии катализаторов

Хлороводородная (соляная) кислота Химические свойства Mg + 2 НСl = Mg. Cl 2+ H 2 Na 2 O + 2 НСl = 2 Na. Cl + H 2 O Сu(ОН)2 + 2 НСl = Сu. Сl 2 + 2 H 2 O Pb(NO 3)2 + 2 НСl = Pb. Cl 2+ 2 НNО 3

Газообразные НCI, НВг, HI, а также соответствующие кислоты и их соли проявляют свойства восстановителей. Восстановительная способность усиливается от HCI к HI. HF и фториды восстановительных свойств не проявляют. Mn. O 2 + 4 HCl = Mn. Cl 2 + 2 H 2 O 2 KMn. O 4 + 10 KI + 8 H 2 SO 4 = 2 Mn. SO 4 + 6 K 2 SO 4 + 5 I 2 + 8 H 2 O

Качественные реакции на галогенид – ионы Ag+ + Cl- =Ag. Cl↓ белый творожистый Ag+ + Br- = Ag. Br↓ светло-желтый Ag+ + I- = Ag. I↓ желтый

Контрольные вопросы для закрепления: 1. Каково строение внешнего электронного слоя галогенов? К какому электронному семейству они принадлежат? 2. Почему фтор проявляет во всех соединениях постоянную валентность? 3. Какой галогенид-ион является самым сильным восстановителем?

Рекомендуемая литература Обязательная Пустовалова Л. М. , Никанорова И. Е. Неорганическая химия. Ростов-на-Дону. Феникс. 2005. – 352 с. гл. 2. 1 с. 182 -197 Дополнительная Ахметов Н. С. Общая и неорганическая химия. М. : Высшая школа, 2009. - 368 с. Глинка Н. Л. Общая химия. Кно. Рус, 2009. -436 с. Ерохин Ю. М. Химия. Учебник для студ. Сред проф. образ. -М. : Академия, 2006. - 384 с.
9_ Галогены.ppt