Обмен белков -5.ppt
- Количество слайдов: 154


Главные научные открытия в области обмена белков принадлежат Российским ученым

Академик Опарин Александр Иванович (Лауреат Ленинской премии 1974 г. ; Премии им. А. Н. Баха, Награжден Золотой медалью им. М. В. Ломоносова

Академик Баев Александрович. (Лауреат Государственной премии 1969 г)

Академик Спирин Александр Сергеевич (лауреат Ленинской премии 1976 г. Награжден медалью им. Ганса Кребса федерации Европейского биохимического общества)

Роль белков в организме • • Структурная Каталитическая Транспортная Регуляторная Защитная Гомеостатическая Депонирующая Функциональная

Динамика обновления белков За сутки распадается белков ~ 400 г Из них распадается полностью до СО 2; NН 3 и Н 2 О ~ 100 г В сутки синтезируется белков ~ 400 г Суточная потребность в белках ~ 100 г Период полуобновления белков ~ 80 дней
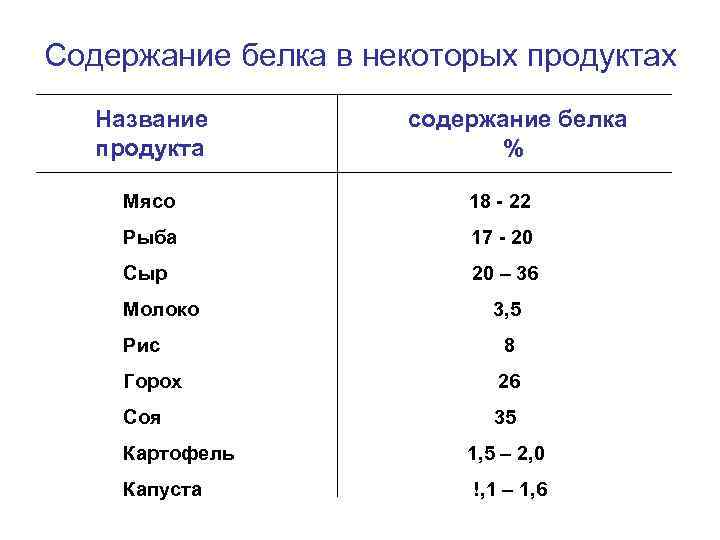
Содержание белка в некоторых продуктах Название продукта содержание белка % Мясо 18 - 22 Рыба 17 - 20 Сыр 20 – 36 Молоко 3, 5 Рис 8 Горох 26 Соя 35 Картофель Капуста 1, 5 – 2, 0 !, 1 – 1, 6

Биологическая ценность аминокислот заменимые незаменимые пируват -----------→ аланин треонин глицерин- -----------→ серин метионин серин -------------→ глицин валин аланин------------→ цистеин лейцин щук --------→ аспарагиновая к-та изолейцин оксоглутаровая → глутаминовая к-та лизин глутаминовая к-та -----→ пролин фенилаланин глутаминовая к-та ----→ гистидин триптофан фенилаланин -------→ тирозин аргинин

примеры продуктов, содержащие неполноценные белки название продукта 1. белки растительных продуктов 2. белки кукурузы 3. белки соевых бобов отсутствующая аминокислота несбалансированный аминокислотный состав лизин триптофан

Переваривание белков в желудочнокишечном тракте
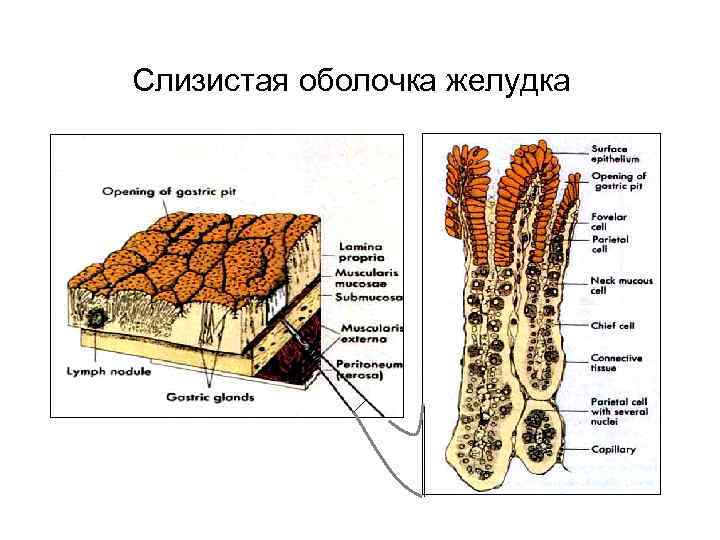
Слизистая оболочка желудка
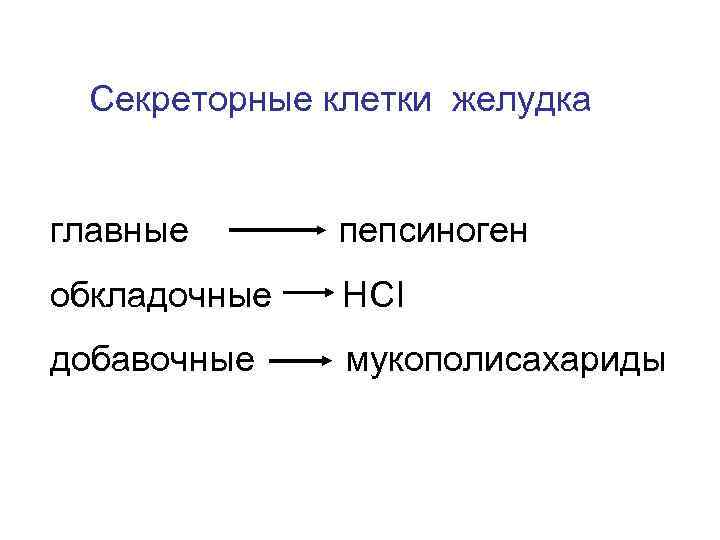
Секреторные клетки желудка главные пепсиноген обкладочные НCI добавочные мукополисахариды
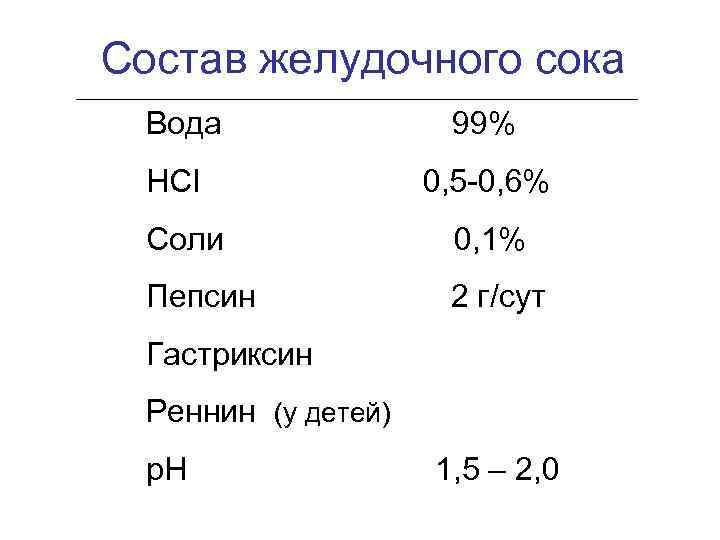
Состав желудочного сока Вода НСI 99% 0, 5 -0, 6% Соли 0, 1% Пепсин 2 г/сут Гастриксин Реннин (у детей) р. Н 1, 5 – 2, 0

Роль НСI в переваривании белков 1. Создает оптимум р. Н для активности пепсина; 2. 2. Обладает бактерицидным действием; 3. Разрушая водородные связи в молекуле белка, способствует его разрыхлению и улучшению взаимодействия пепсина с пептидными связями белка; 4. 4. В пилорическом отделе желудка НСI стимулирует образование местных гормонов – секретина и панкреозимина, которые, в свою очередь, стимулируют секрецию сока поджелудочной железы.
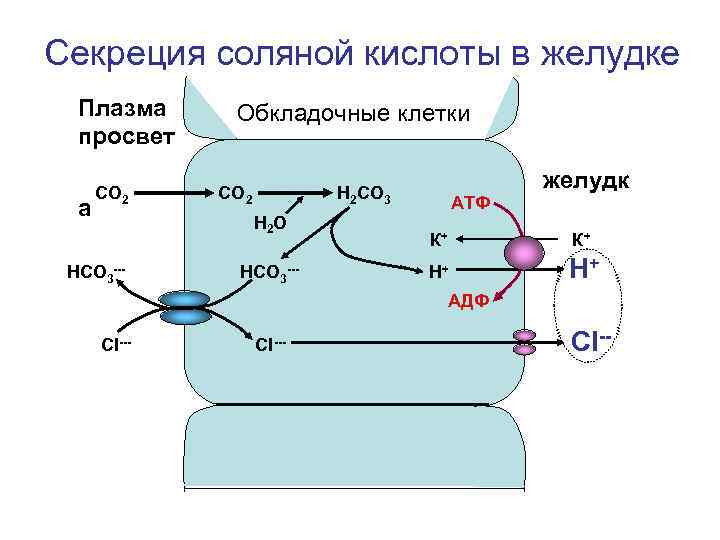
Секреция соляной кислоты в желудке Плазма просвет а СО 2 Обкладочные клетки СО 2 Н 2 О НСО 3 --- желудк Н 2 СО 3 НСО 3 --- АТФ К+ Н+ АДФ СI--- CI--

Медицинские названия нарушений кислотности желудочного сока Повышенная кислотность гиперхлоргидрия Пониженная кислотность гипохлоргидрия Прекращение образования соляной кислоты ахлоргидрия Нарушение секреции НСI и секреции пепсина ахилия
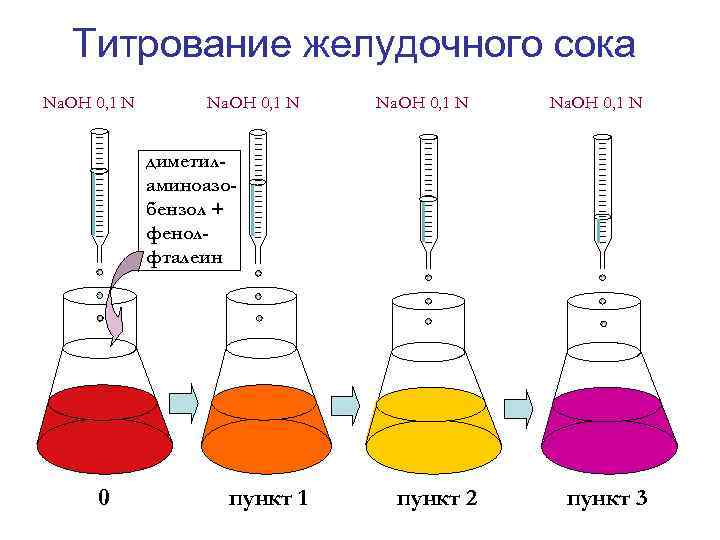
Титрование желудочного сока Na. OH 0, 1 N диметиламиноазобензол + фенолфталеин 0 пункт 1 пункт 2 пункт 3

Расчет результатов титрования 1. Пункт 1. нейтрализация свободной НСI. (мл х 10 = Т. Е. ) 2. Пункт 3. нейтрализация всех кислот желудочного сока. Общая кислотность (мл х 10 = Т. Е. ) 3. Пункт 2 и 3. расчет общей HСI (мл п. 2 + мл. п 3) х 10= Т. E. 2 4. 4. Расчет связанной НСI: Общая HCI свободная НСI = cвязанная HCI

Показатели кислотности желудочного сока в норме (после стимуляции секреции отваром капусты) Общая кислотность - 40 - 60 Т. Е. Общая НСI - 25 - 50 Т. Е. Свободная НСI - 20 - 40 Т. Е. Связанная НСI - 5 - 10 Т. Е.

Показатели кислотности желудочного сока в норме (после стимуляции секреции гистамином) Общая кислотность - 100 - 120 Т. Е. Свободная НСI - 90 - 110 Т. Е.
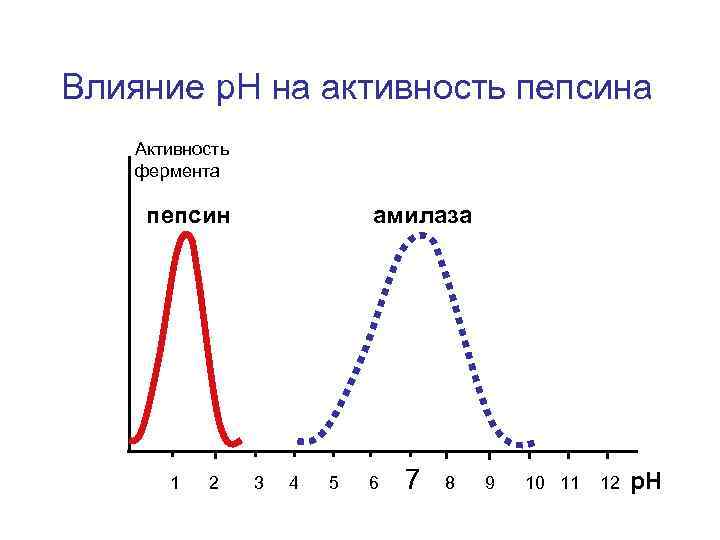
Влияние р. Н на активность пепсина Активность фермента пепсин 1 2 амилаза 3 4 5 6 7 8 9 10 11 12 р. Н
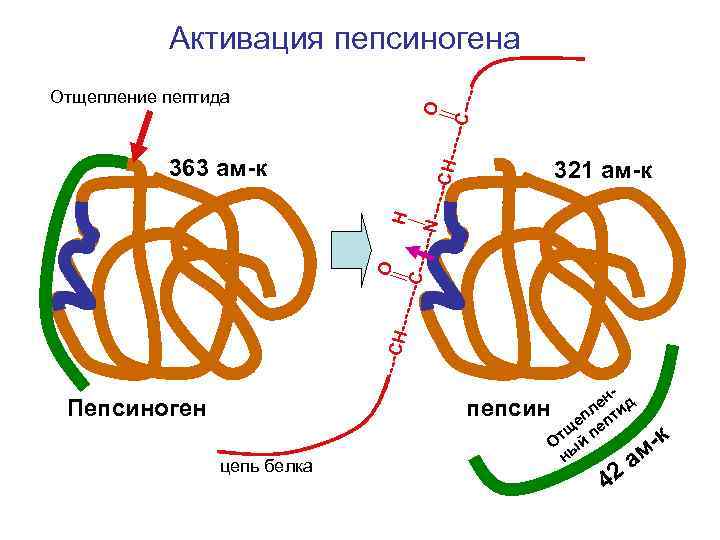
H---- O Отщепление пептида --C-- ---- Активация пепсиногена 321 ам-к ------ CH-- ------ O H С------N-----C 363 ам-к Пепсиноген цепь белка ен ид пепсин епл пт тщ й пе О -к ны ам 42
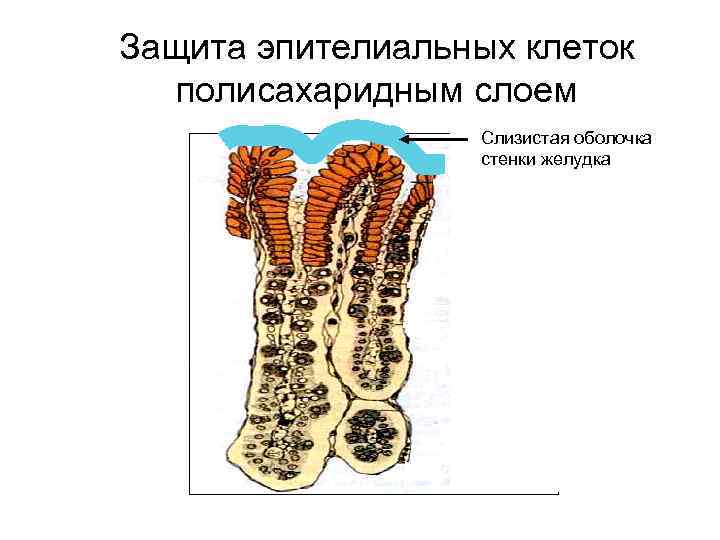
Защита эпителиальных клеток полисахаридным слоем Слизистая оболочка стенки желудка
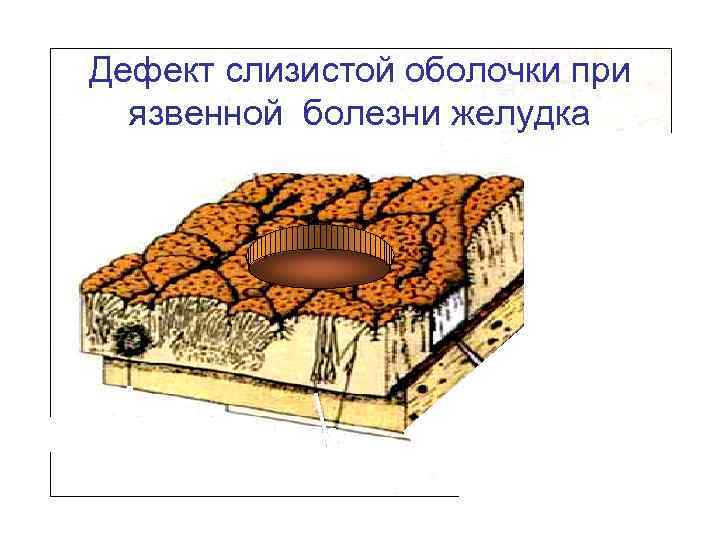
Дефект слизистой оболочки при язвенной болезни желудка

Протеолитические проферменты и ферменты, образующиеся в поджелудочной железе и механизм их активации 229 ам-к трипсиноген 245 ам-к энтерокиназа (кишечная) химотрипсиноген трипсин 223 ам-к трипсин химотрипсин карбоксипептидазы аминопептидазы дипептидазы 230 ам-к
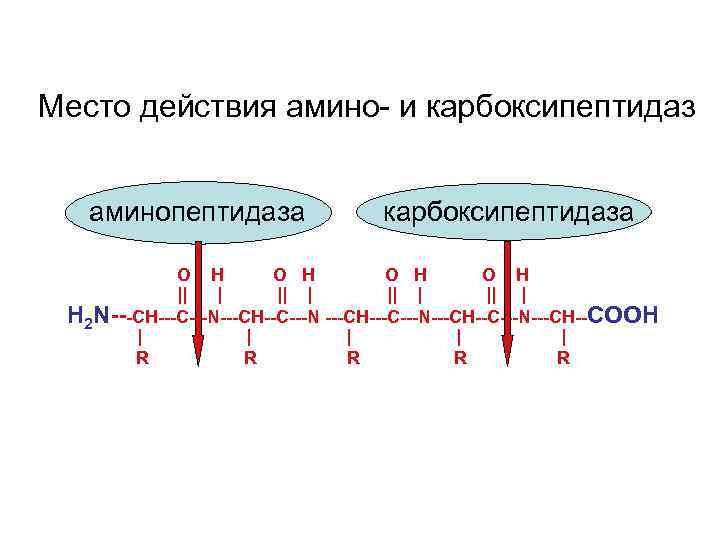
Место действия амино- и карбоксипептидаз аминопептидаза карбоксипептидаза O H O H || | Н 2 N---CH---С---N---CH--C---N ---CH---С---N---CH--COOH | | | R R R
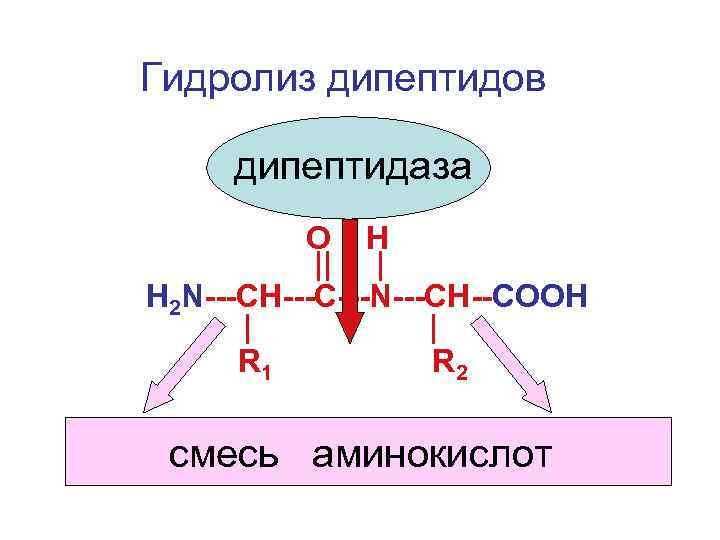
Гидролиз дипептидов дипептидаза O H || | Н 2 N---CH---С---N---CH--COOH | | R 1 R 2 смесь аминокислот
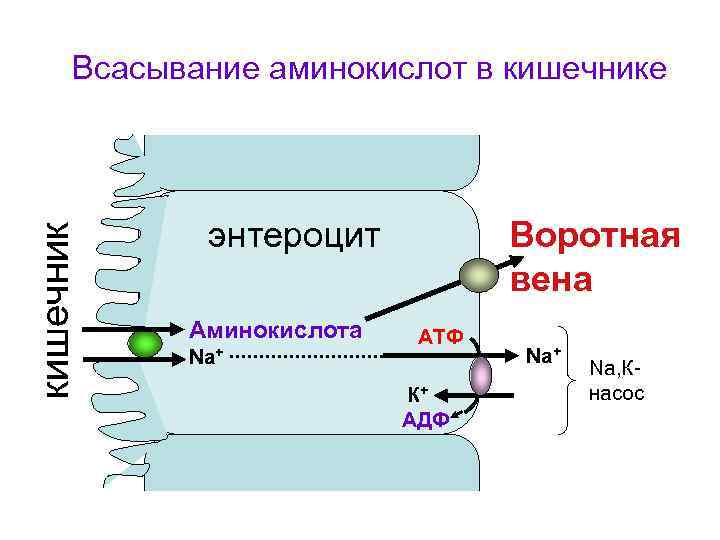
кишечник Всасывание аминокислот в кишечнике энтероцит Аминокислота Na+ Воротная вена АТФ К+ АДФ Nа+ Na, Кнасос

Образование токсичных веществ из аминокислот в кишечнике под влиянием бактерий
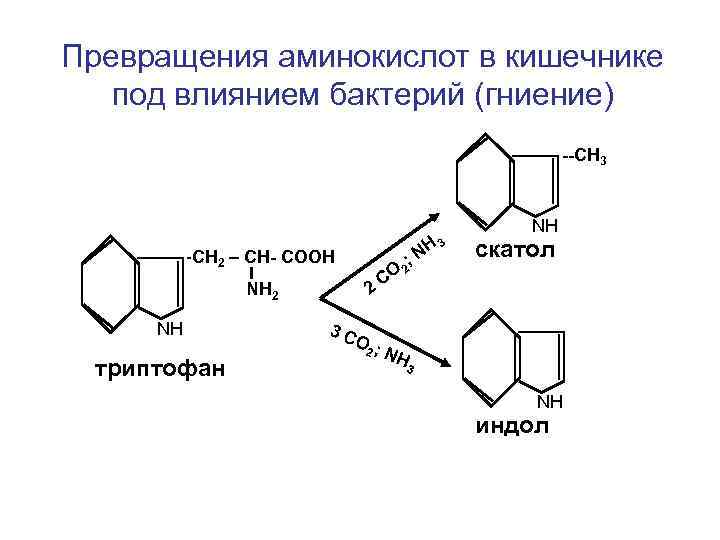
Превращения аминокислот в кишечнике под влиянием бактерий (гниение) --СН 3 -СН 2 – СН- СООН H 3 NН 2 СО 2 NН триптофан ; N 2 NН скатол 3 С О; 2 N H 3 NН индол
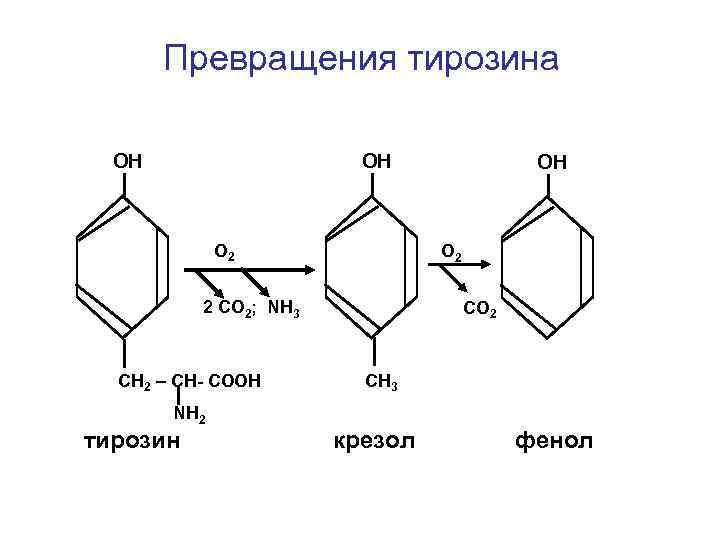
Превращения тирозина ОН ОН O 2 2 СО 2; NH 3 СН 2 – СН- СООН ОН CO 2 СН 3 NН 2 тирозин крезол фенол
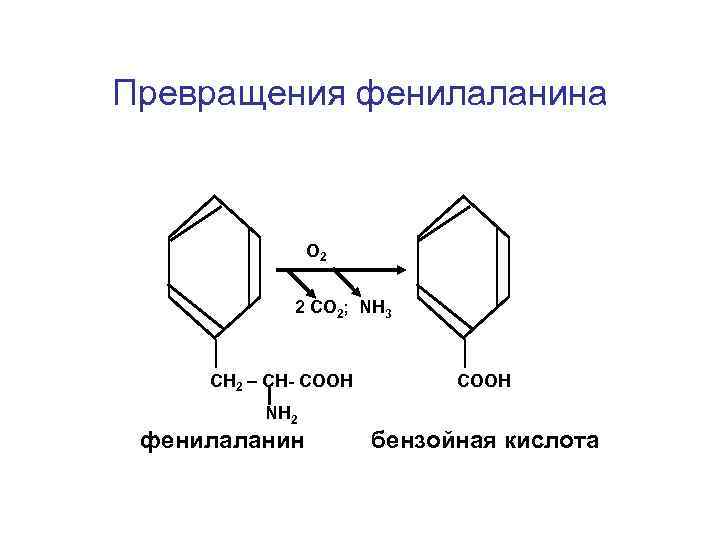
Превращения фенилаланина O 2 2 СО 2; NH 3 СН 2 – СН- СООН NН 2 фенилаланин бензойная кислота
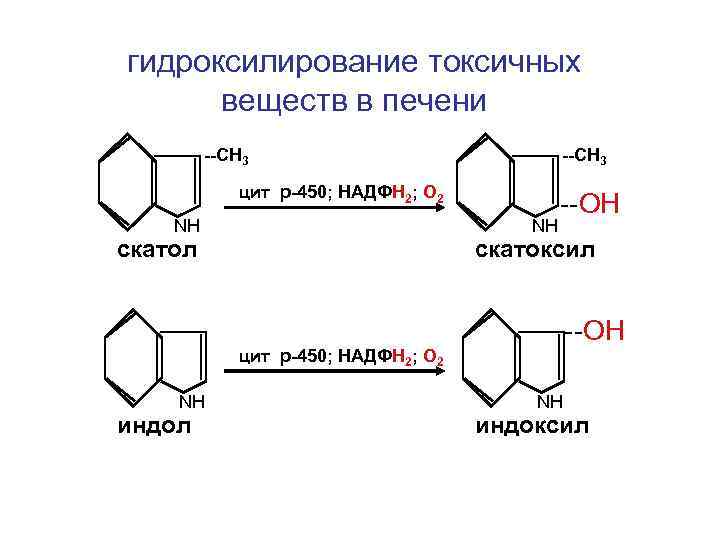
гидроксилирование токсичных веществ в печени --СН 3 цит р-450; НАДФН 2; О 2 NН NН скатол --ОН скатоксил --ОН цит р-450; НАДФН 2; О 2 NН индол NН индоксил
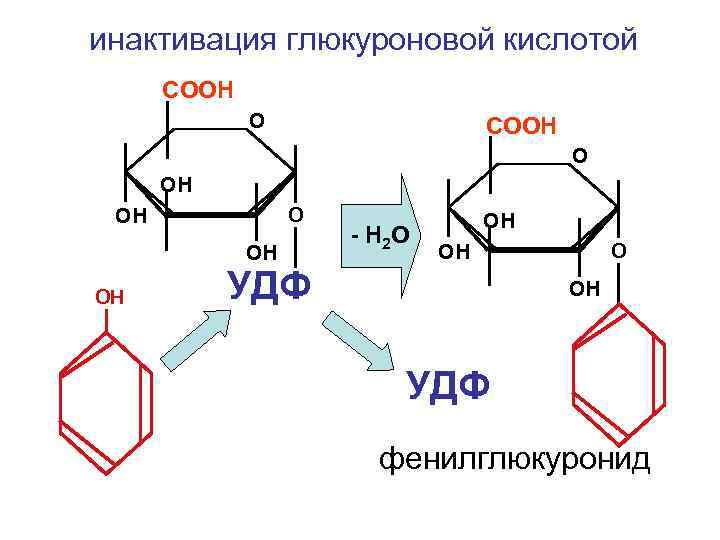
инактивация глюкуроновой кислотой СООН ОН ОН - Н 2 О ОН УДФ фенилглюкуронид
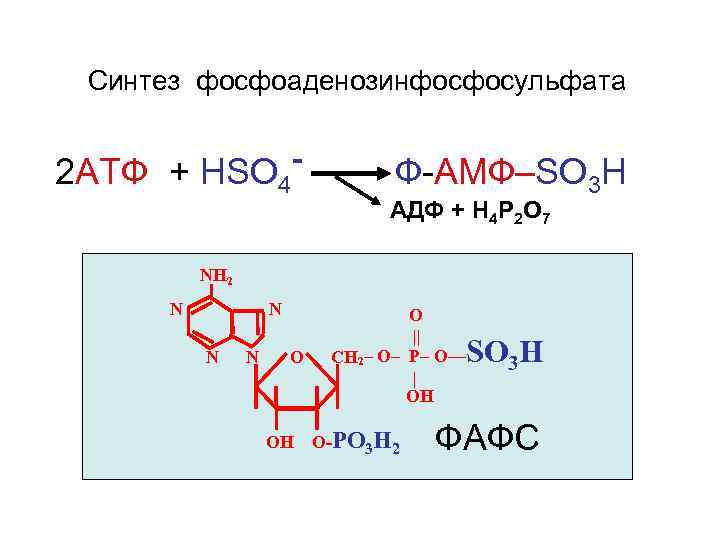
Синтез фосфоаденозинфосфосульфата 2 АТФ + НSO 4 - Ф-АМФ–SO 3 H АДФ + Н 4 Р 2 О 7 NH 2 N N O ОН О || CH 2– O– P– O— | ОН SO 3 H О-PO 3 H 2 ФАФС
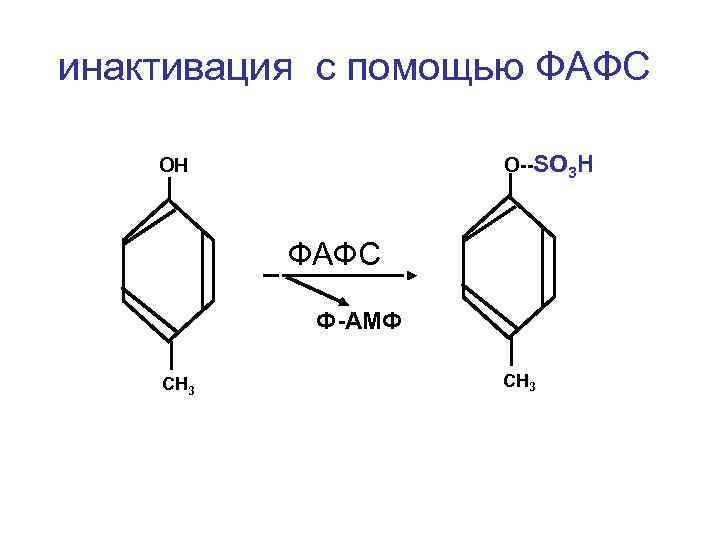
инактивация с помощью ФАФС О--SO 3 H ОН ФАФС Ф-АМФ СН 3

обезвреживание индоксила --ОН ФАФС NН индоксил --О-SO 3 H NН индоксил-гидросульфат --О-SO 3 К NН ИНДИКАН почки
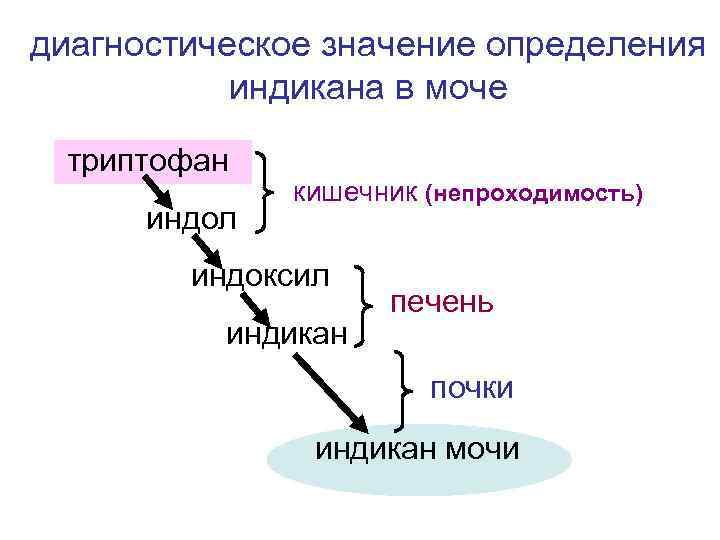
диагностическое значение определения индикана в моче триптофан индол кишечник (непроходимость) индоксил индикан печень почки индикан мочи
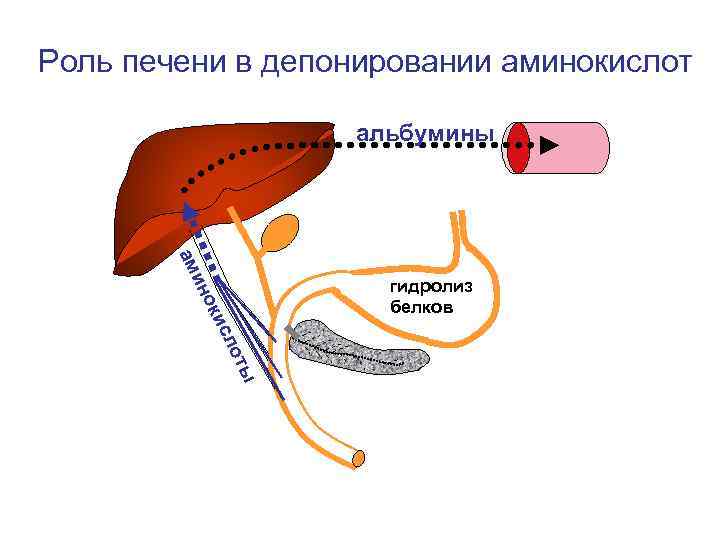
Роль печени в депонировании аминокислот альбумины ам ин гидролиз белков ты ло ис ок

Роль альбумина • Запасной источник аминокислот • • • Компонент буферной системы Осмотически активный белок Переносчик жирных кислот Переносчик жирорастворимых витаминов Переносчик жирорастворимых гормонов Са-связывающий белок в сыворотке крови
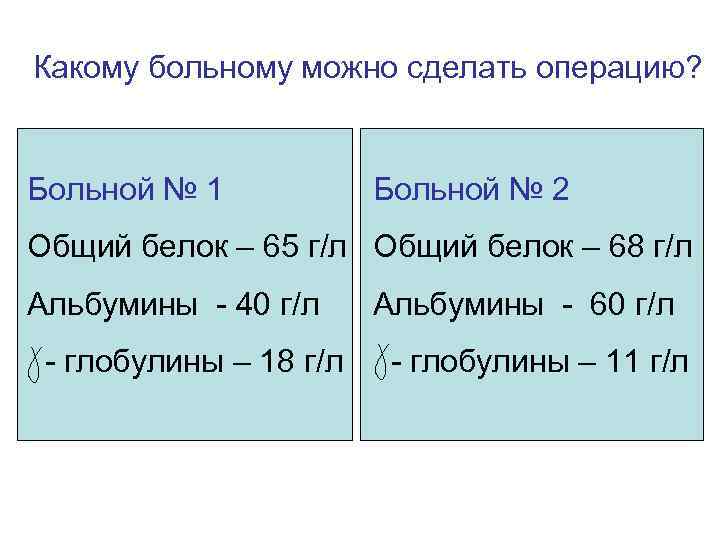
Какому больному можно сделать операцию? Больной № 1 Больной № 2 Общий белок – 65 г/л Общий белок – 68 г/л Альбумины - 40 г/л - глобулины – 18 г/л Альбумины - 60 г/л - глобулины – 11 г/л

Пути превращений аминокислот в клетке 1. Реакции поликонденсации 2. Реакции трансаминирования 3. Реакции декарбоксилирования 4. Реакции окислительного дезаминирования
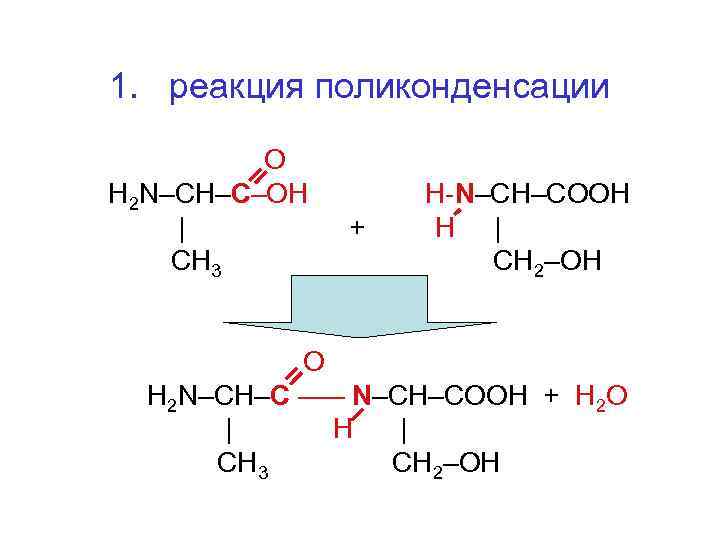
1. реакция поликонденсации О H 2 N–CH–C–OH | СН 3 + H-N–CH–CООH H | СН 2–ОН О H 2 N–CH–C ––– N–CH–CОOH + Н 2 О | H | СН 3 СН 2–ОН
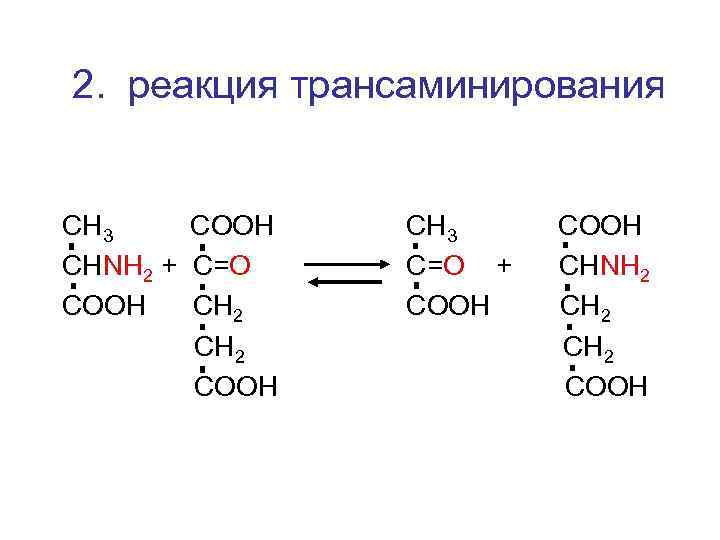
2. реакция трансаминирования СН 3 СООН СНNH 2 + C=О СООН СН 2 СООН СН 3 С=О + СООН СНNH 2 СН 2 СООН
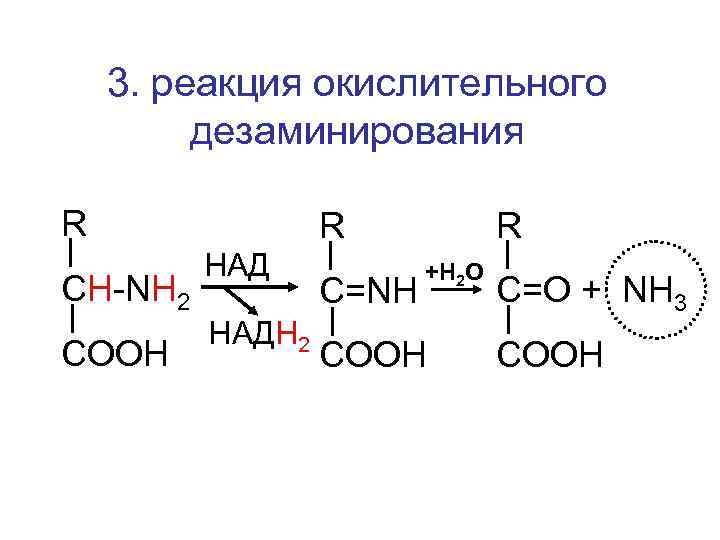
3. реакция окислительного дезаминирования R CH-NH 2 COOH R R HАДН 2 C=NH +Н 2 О COOH C=O + NH 3 COOH
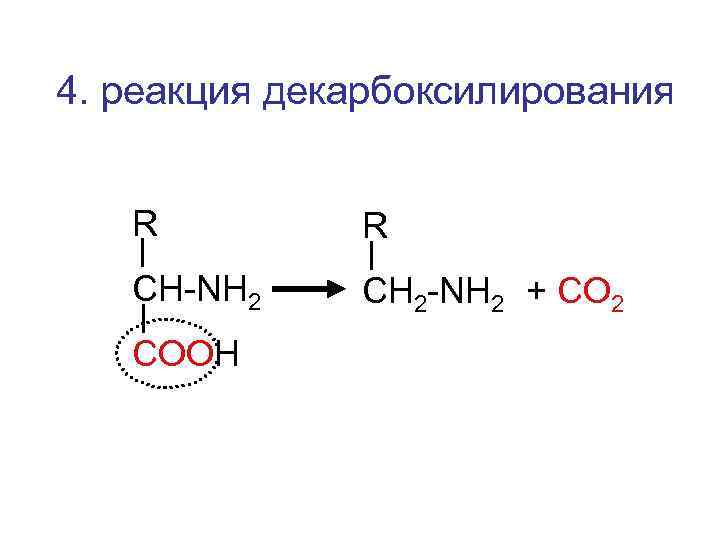
4. реакция декарбоксилирования R R CH-NH 2 CН 2 -NH 2 + СО 2 COOH

Биосинтез белка в клетке

Перечень веществ, необходимых для синтеза белка 1. и-РНК (зрелая) 2. т-РНК ( 61) 3. 20 аминокислот 4. АТФ, ГТФ 5. Ферменты 6. Небелковые компоненты 7. Рибосомы
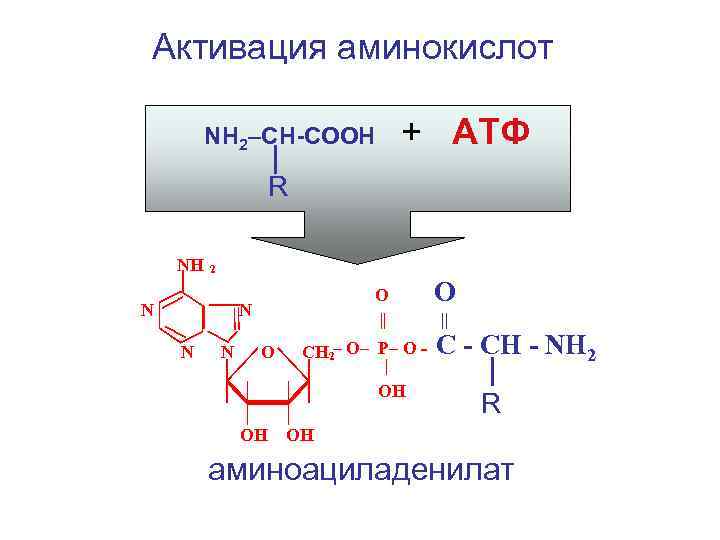
Активация аминокислот NH 2–CH-COOH + АТФ R NH 2 N O || N N N O ОН CH 2– O– P– O | ОН O || C - CH - NH 2 R ОН аминоациладенилат
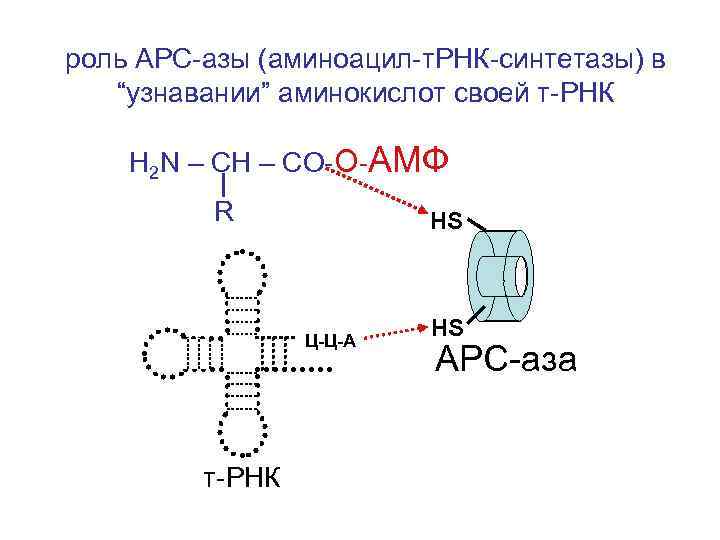
роль АРС-азы (аминоацил-т. РНК-синтетазы) в “узнавании” аминокислот своей т-РНК H 2 N – CH – CO-O-АМФ R НS Ц-Ц-А т-РНК HS АРС-аза
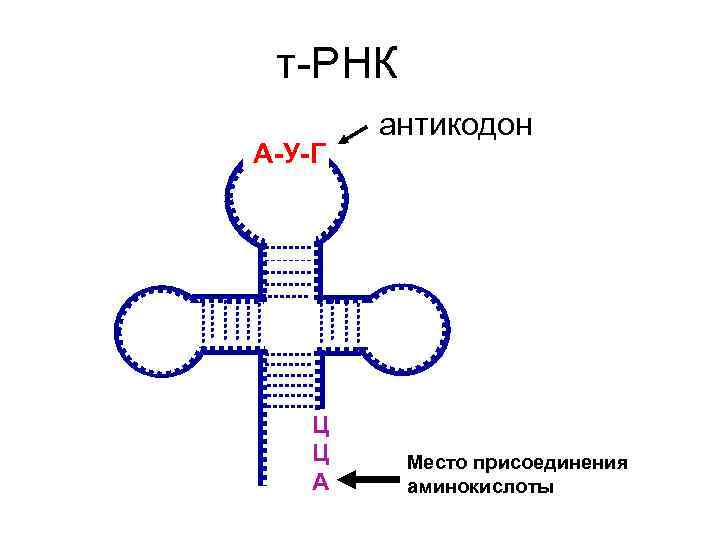
т-РНК А-У-Г Ц Ц А антикодон Место присоединения аминокислоты
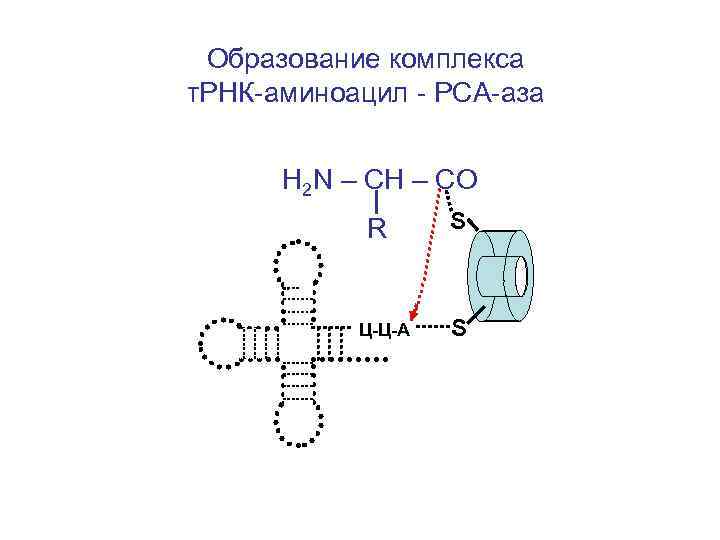
Образование комплекса т. РНК-аминоацил - РСА-аза H 2 N – CH – CO R Ц-Ц-А S S
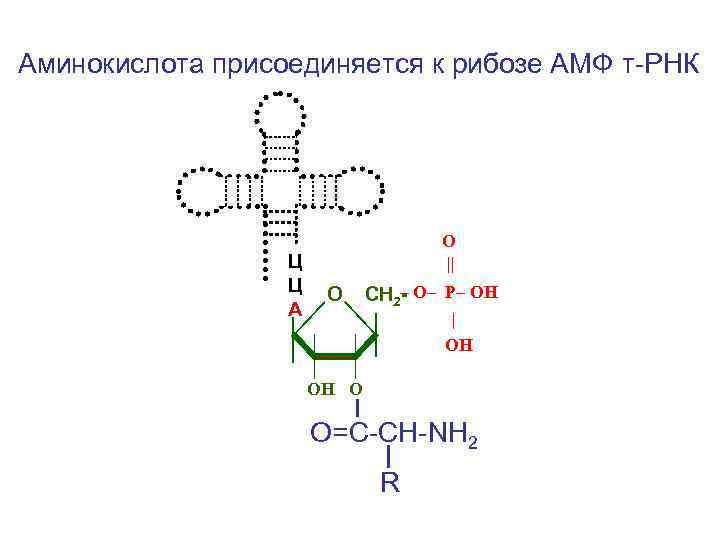
Аминокислота присоединяется к рибозе АМФ т-РНК Ц Ц А O || О СН 2– O– P– OН | ОН ОН О О=С-СН-NH 2 R
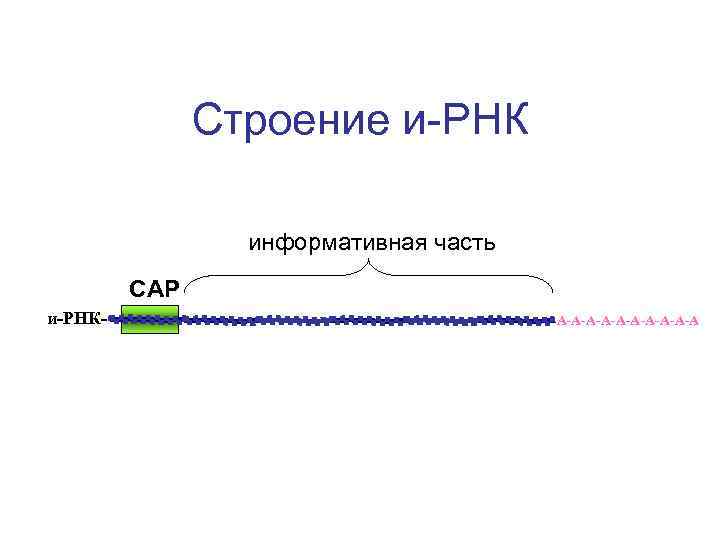
Строение и-РНК информативная часть САР и-РНК- -А-А-А-А-А

Стадии синтеза белка 1. образование инициирующего комплекса; 2. элонгация (удлинение полипептидной цепи); 3. терминация (завершение синтеза); 4. процессинг (окончательное достраивание молекулы белка).
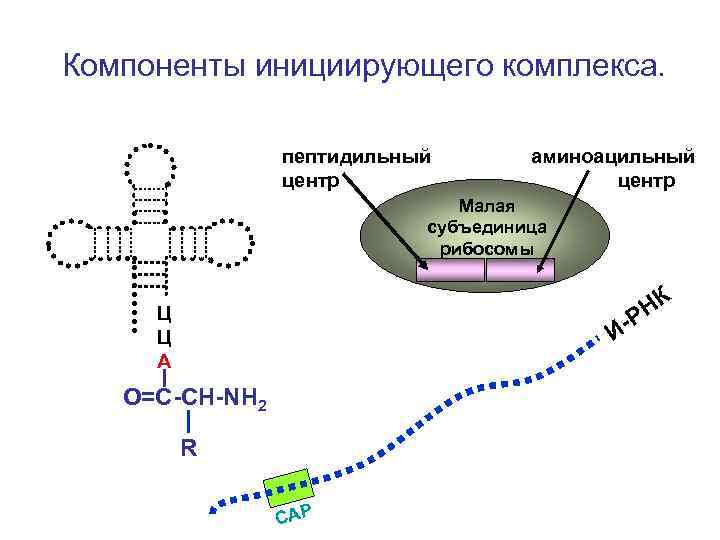
Компоненты инициирующего комплекса. пептидильный центр аминоацильный центр Малая субъединица рибосомы НК Р Ц Ц А И- О=С-СН-NH 2 R С AP
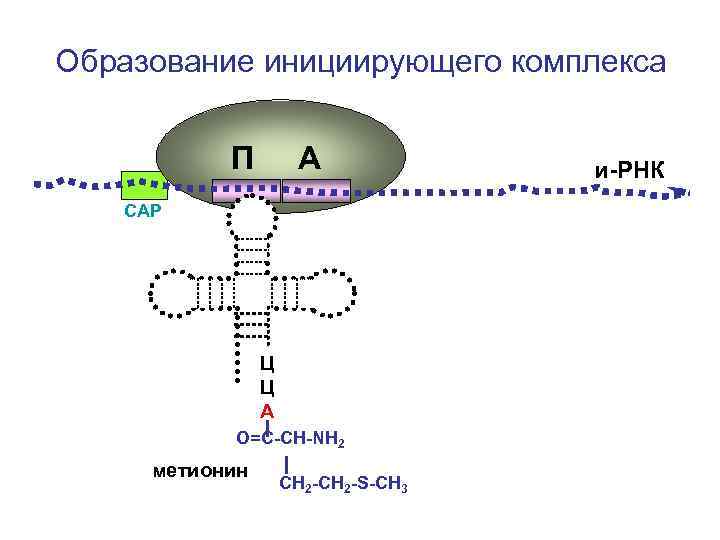
Образование инициирующего комплекса П А СAP Ц Ц А О=С-СН-NH 2 метионин СН 2 -S-CH 3 и-РНК
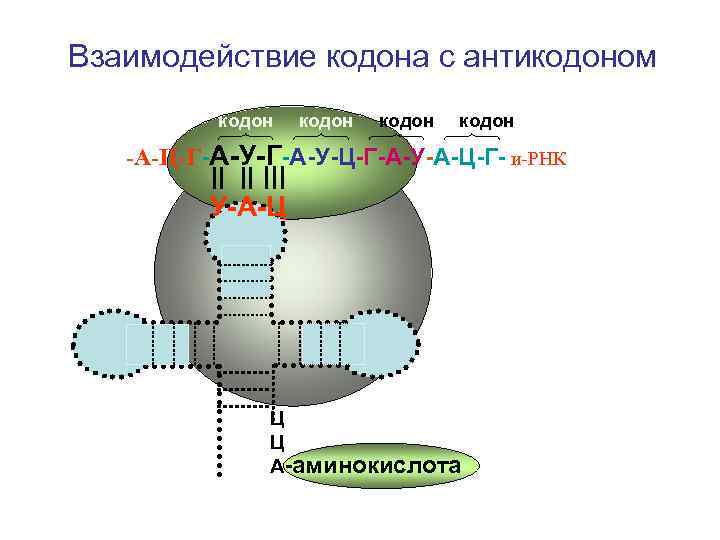
Взаимодействие кодона с антикодоном кодон -А-Ц-Г-А-У-Ц-Г-А-У-А-Ц-Г- и-РНК У-А-Ц Ц Ц А-аминокислота

Биосинтез белка
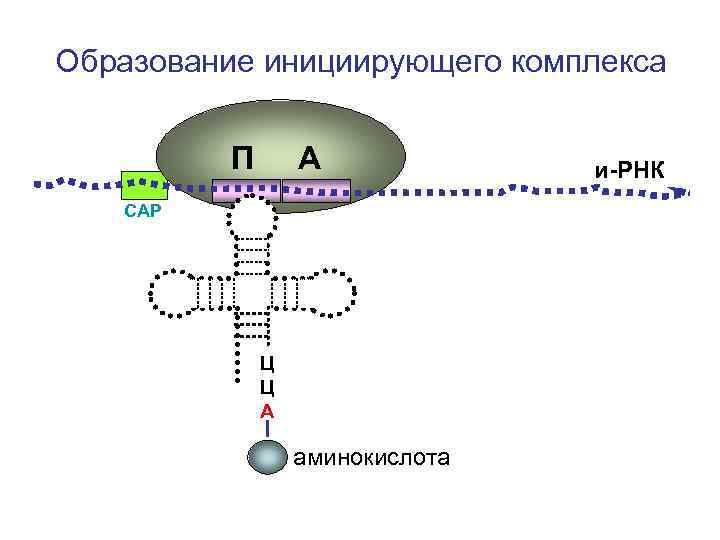
Образование инициирующего комплекса П А СAP Ц Ц А аминокислота и-РНК
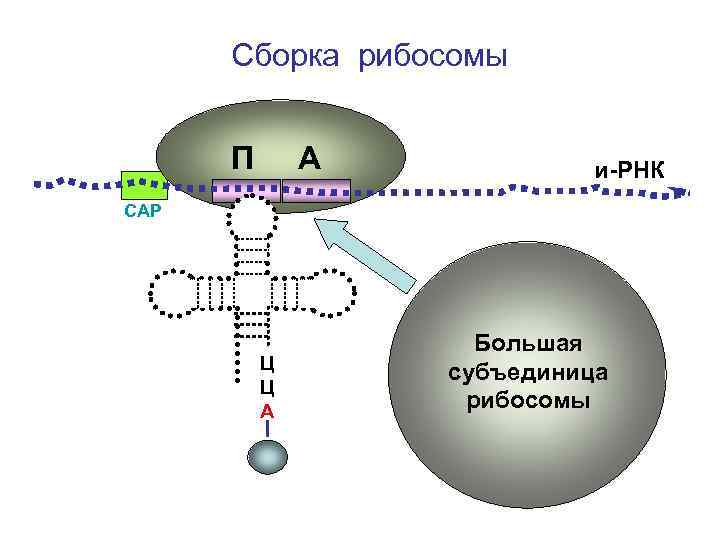
Сборка рибосомы П А и-РНК СAP Ц Ц А Большая субъединица рибосомы
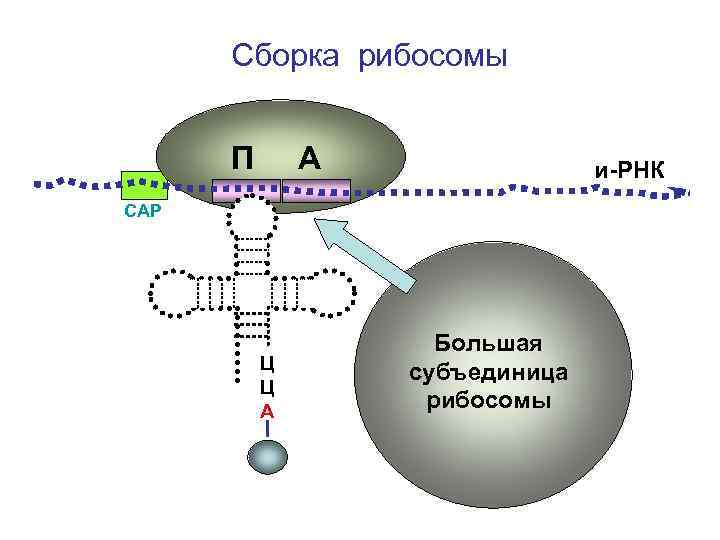
Сборка рибосомы П А и-РНК СAP Ц Ц А Большая субъединица рибосомы
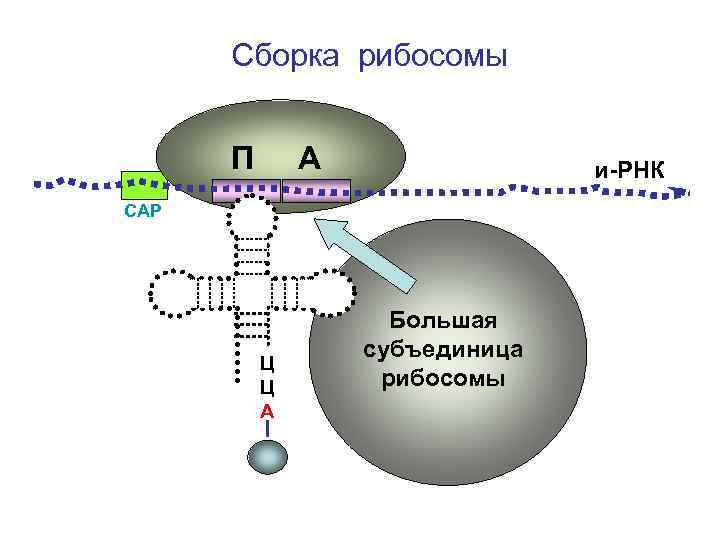
Сборка рибосомы П А и-РНК СAP Ц Ц А Большая субъединица рибосомы
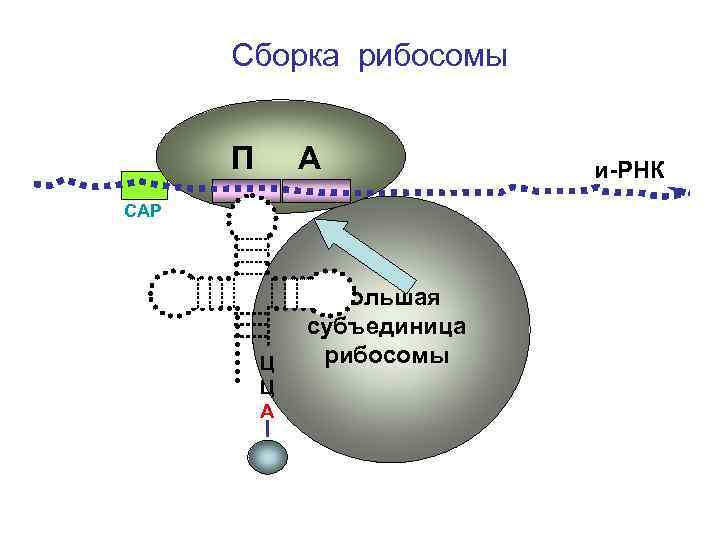
Сборка рибосомы П А СAP Ц Ц А Большая субъединица рибосомы и-РНК
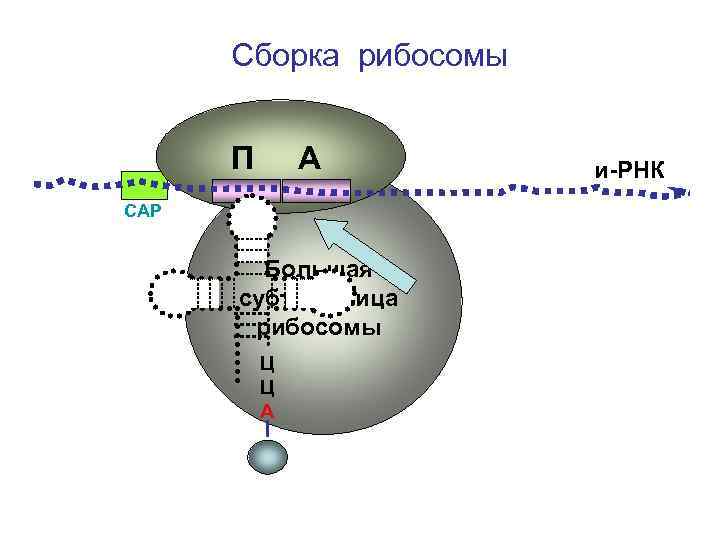
Сборка рибосомы П А СAP Большая субъединица рибосомы Ц Ц А и-РНК
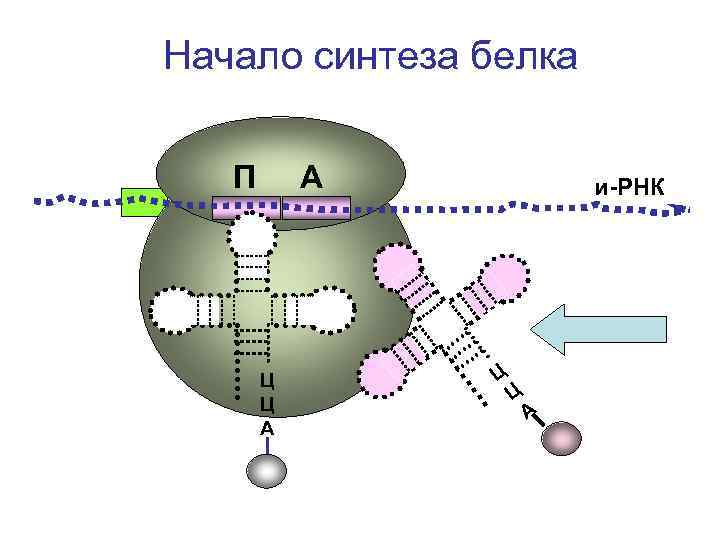
Начало синтеза белка П А Ц Ц А и-РНК Ц Ц А
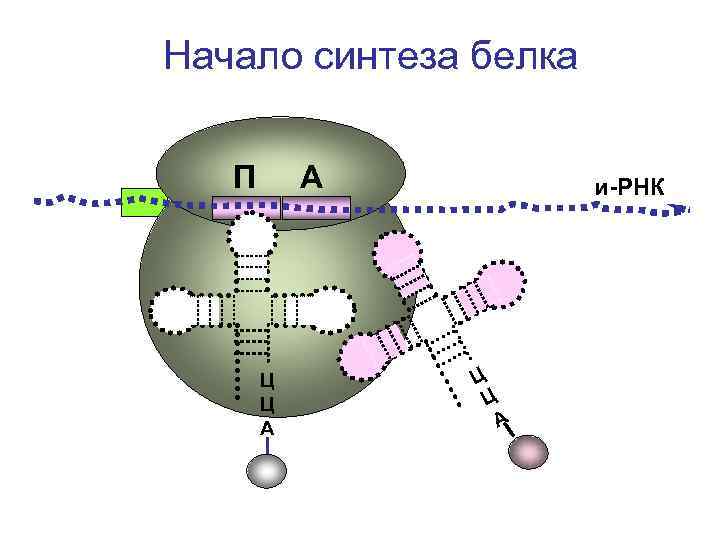
Начало синтеза белка П А Ц Ц А и-РНК Ц Ц А
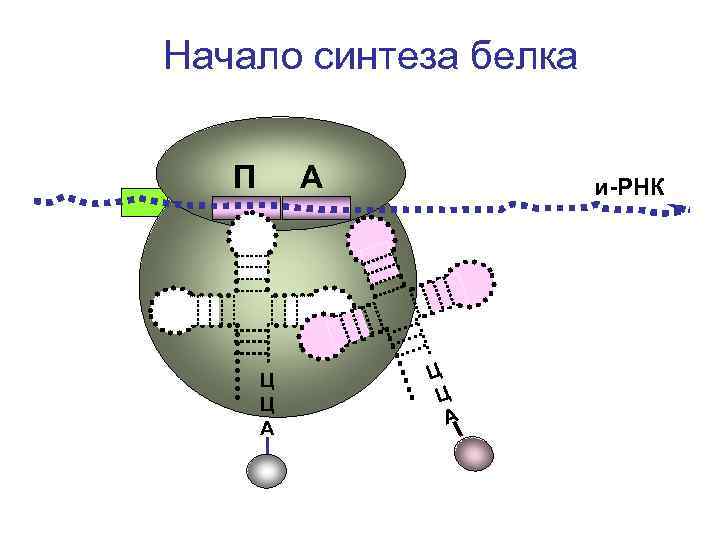
Начало синтеза белка П А Ц Ц А и-РНК Ц Ц А
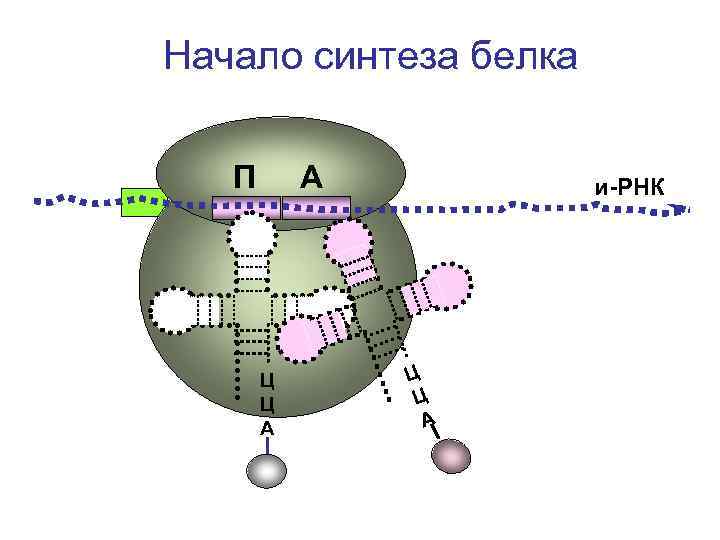
Начало синтеза белка П А Ц Ц А и-РНК Ц Ц А
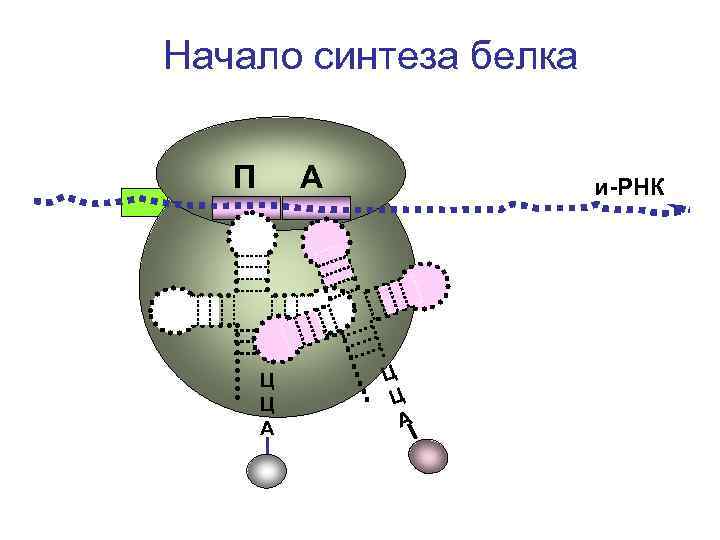
Начало синтеза белка П А Ц Ц А и-РНК Ц Ц А
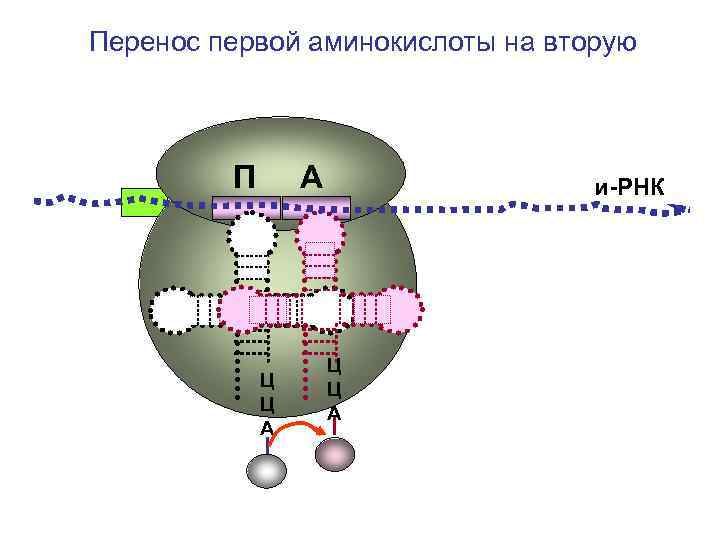
Перенос первой аминокислоты на вторую П А Ц Ц А и-РНК Ц Ц А
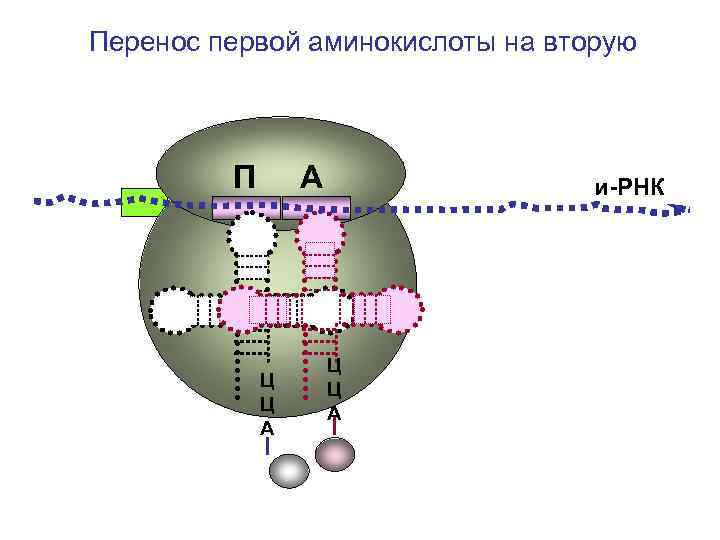
Перенос первой аминокислоты на вторую П А Ц Ц А и-РНК Ц Ц А
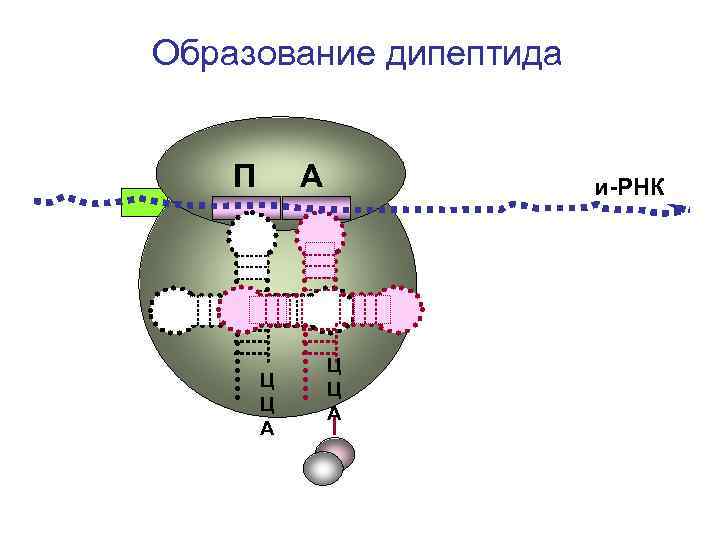
Образование дипептида П А Ц Ц А и-РНК Ц Ц А
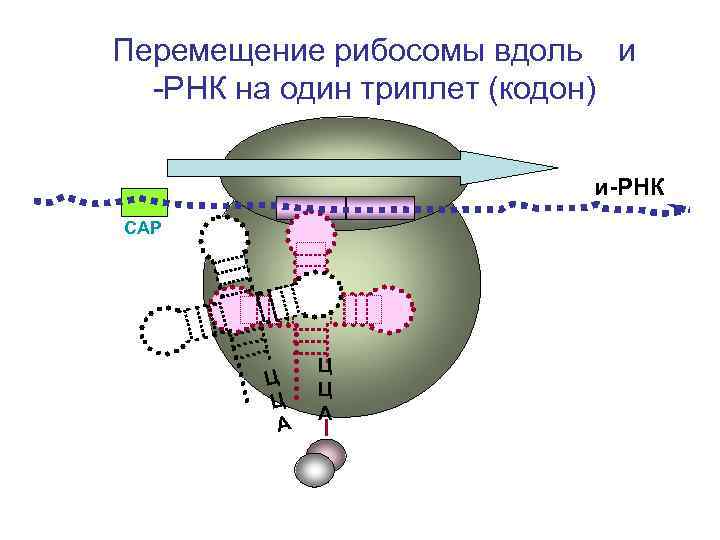
Перемещение рибосомы вдоль и -РНК на один триплет (кодон) и-РНК СAP Ц Ц А
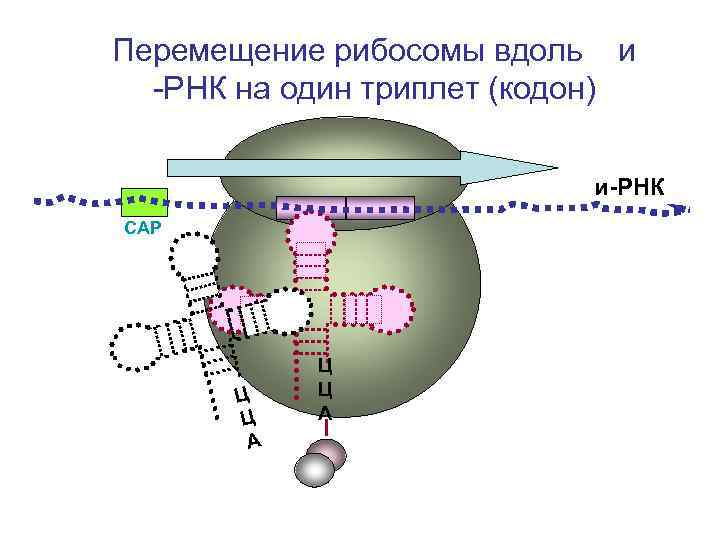
Перемещение рибосомы вдоль и -РНК на один триплет (кодон) и-РНК СAP Ц Ц А
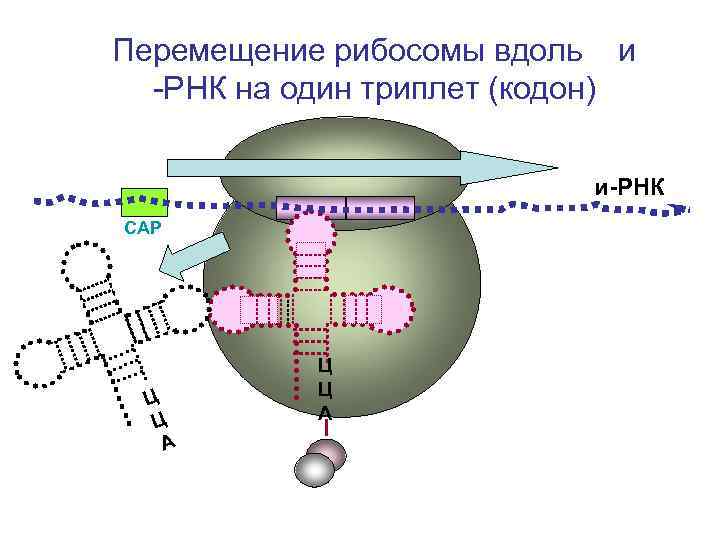
Перемещение рибосомы вдоль и -РНК на один триплет (кодон) и-РНК СAP Ц Ц А
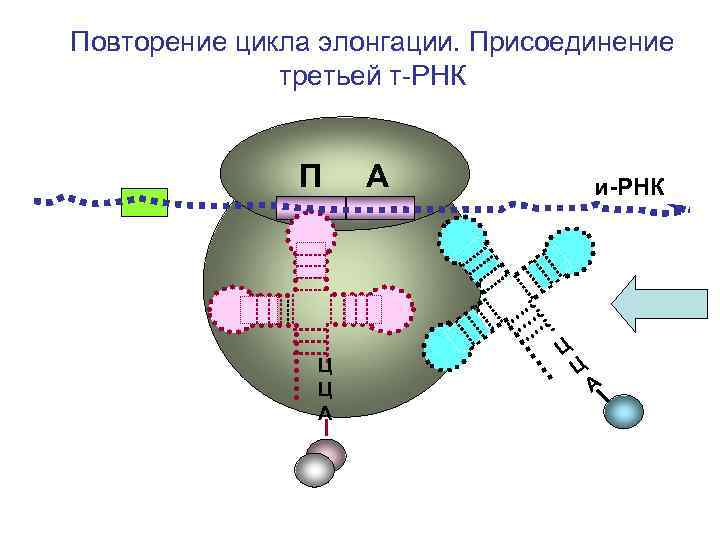
Повторение цикла элонгации. Присоединение третьей т-РНК П Ц Ц А А и-РНК Ц Ц А
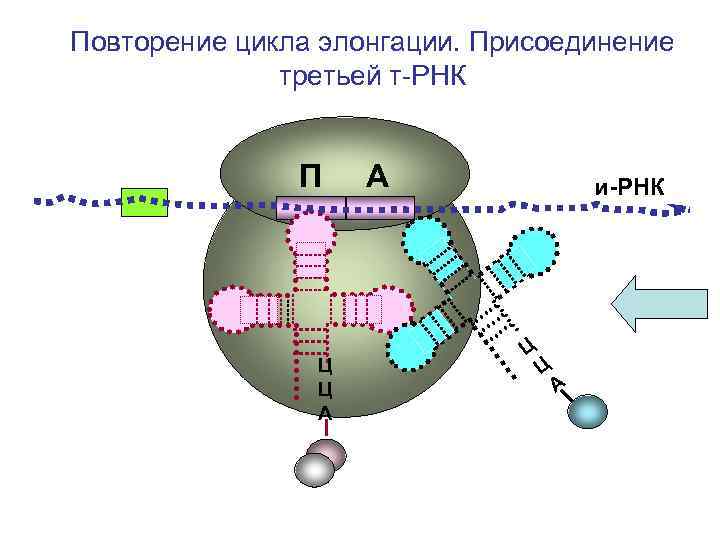
Повторение цикла элонгации. Присоединение третьей т-РНК П Ц Ц А А и-РНК Ц Ц А
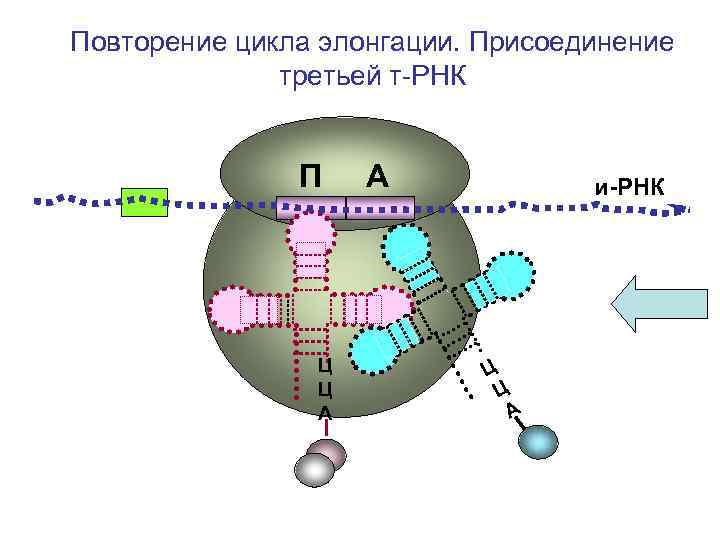
Повторение цикла элонгации. Присоединение третьей т-РНК П Ц Ц А А и-РНК Ц Ц А
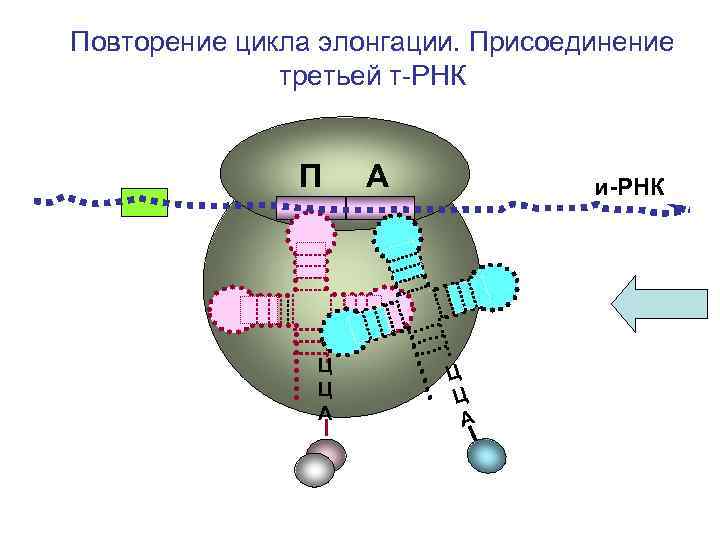
Повторение цикла элонгации. Присоединение третьей т-РНК П Ц Ц А А и-РНК Ц Ц А
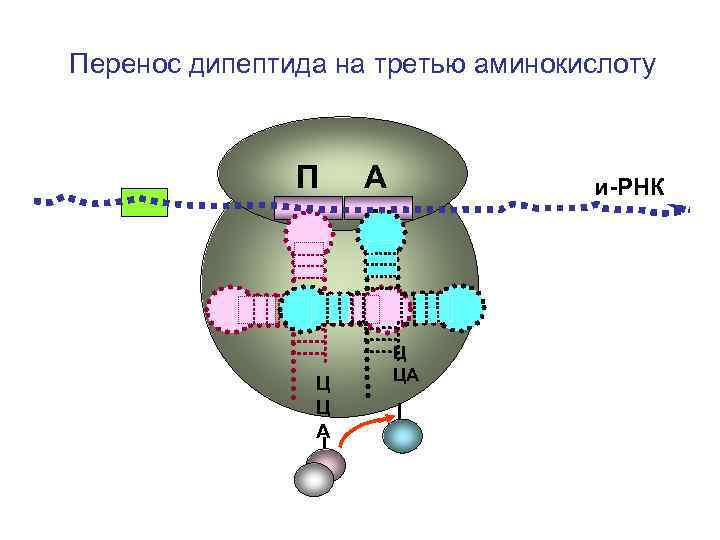
Перенос дипептида на третью аминокислоту П Ц Ц А А и-РНК Ц ЦА
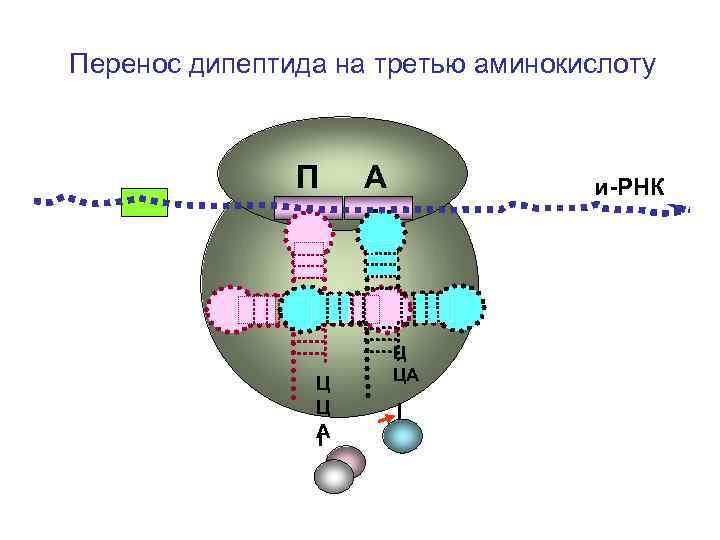
Перенос дипептида на третью аминокислоту П Ц Ц А А и-РНК Ц ЦА
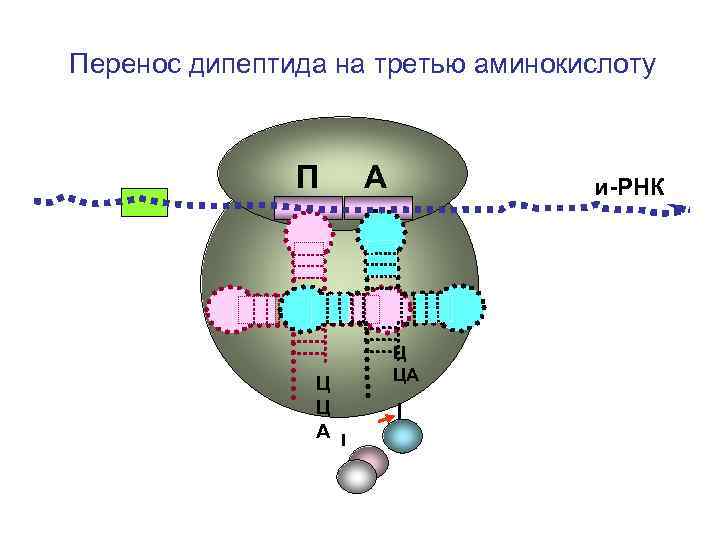
Перенос дипептида на третью аминокислоту П Ц Ц А А и-РНК Ц ЦА
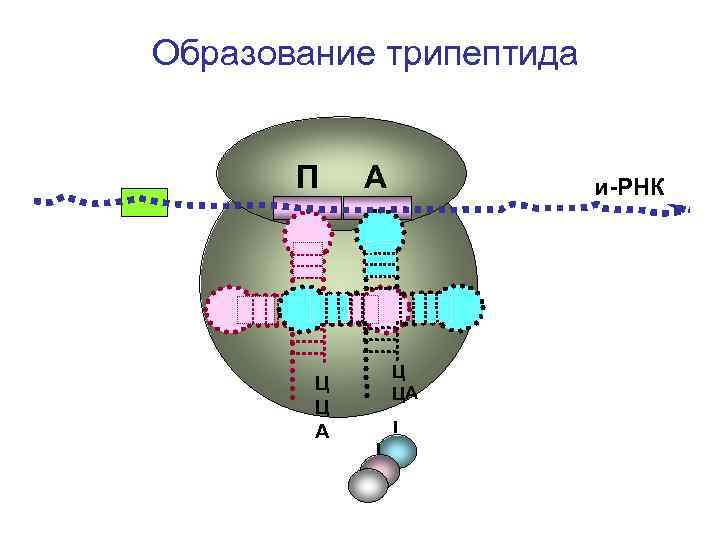
Образование трипептида П Ц Ц А А и-РНК Ц ЦА
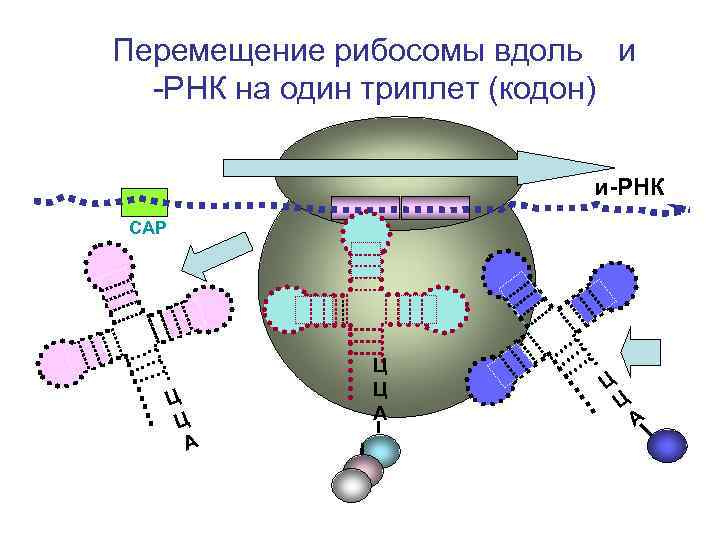
Перемещение рибосомы вдоль и -РНК на один триплет (кодон) и-РНК СAP Ц Ц А

Многократное повторение циклов элонгации, до полного построения белковой молекулы
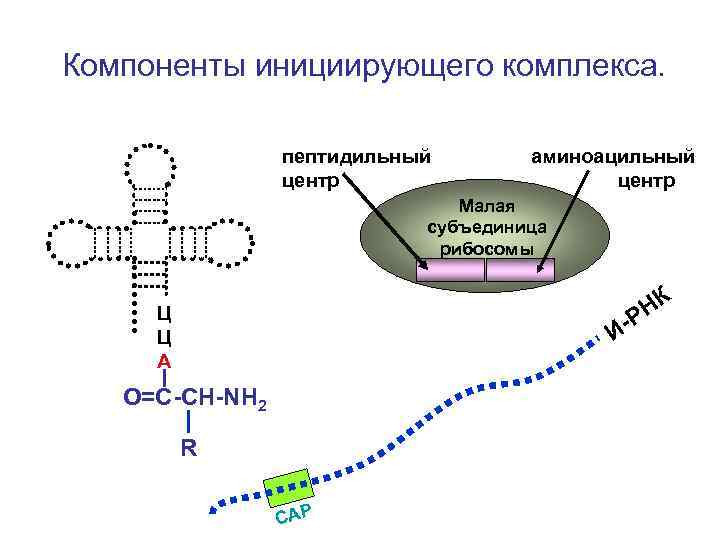
Компоненты инициирующего комплекса. пептидильный центр аминоацильный центр Малая субъединица рибосомы НК Р Ц Ц А И- О=С-СН-NH 2 R С AP
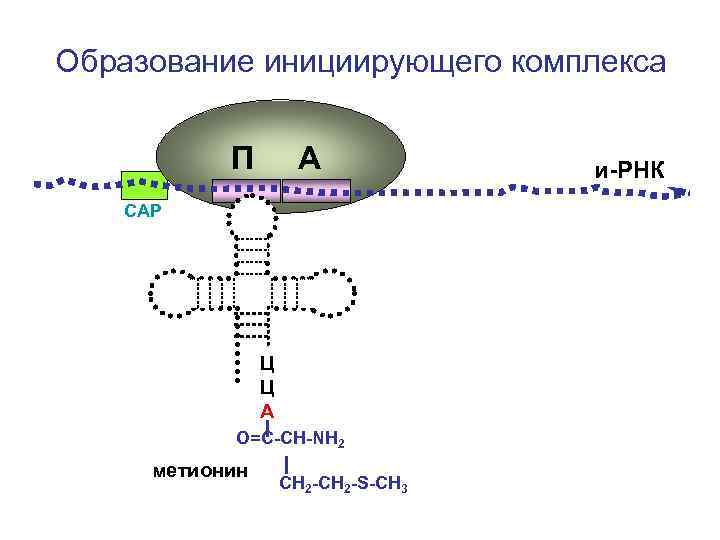
Образование инициирующего комплекса П А СAP Ц Ц А О=С-СН-NH 2 метионин СН 2 -S-CH 3 и-РНК
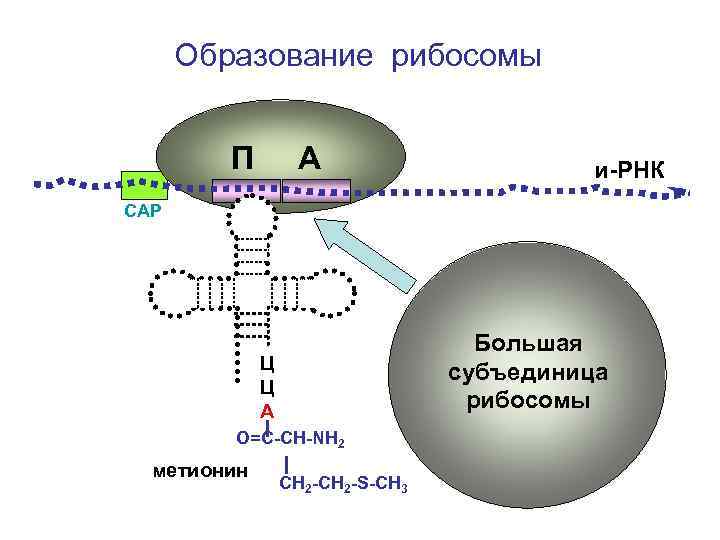
Образование рибосомы П А и-РНК СAP Большая субъединица рибосомы Ц Ц А О=С-СН-NH 2 метионин СН 2 -S-CH 3
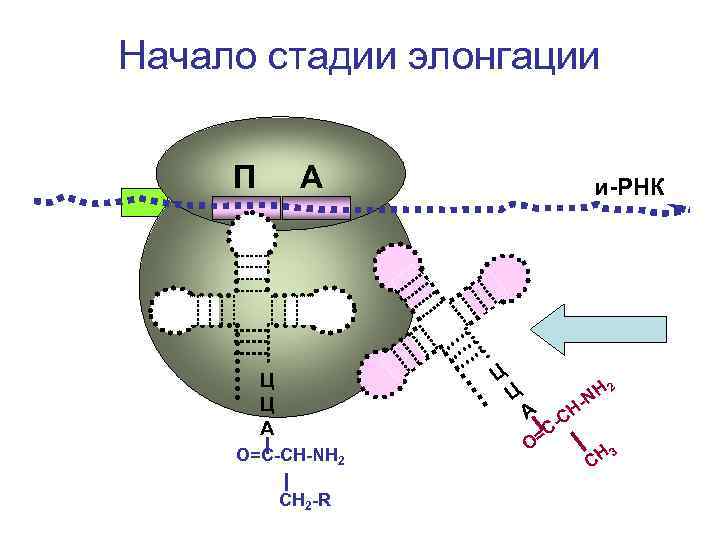
Начало стадии элонгации П А и-РНК Ц Ц Ц А О=С-СН-NH 2 СН 2 -R Ц А H -N 2 CH 3 Н С СО=
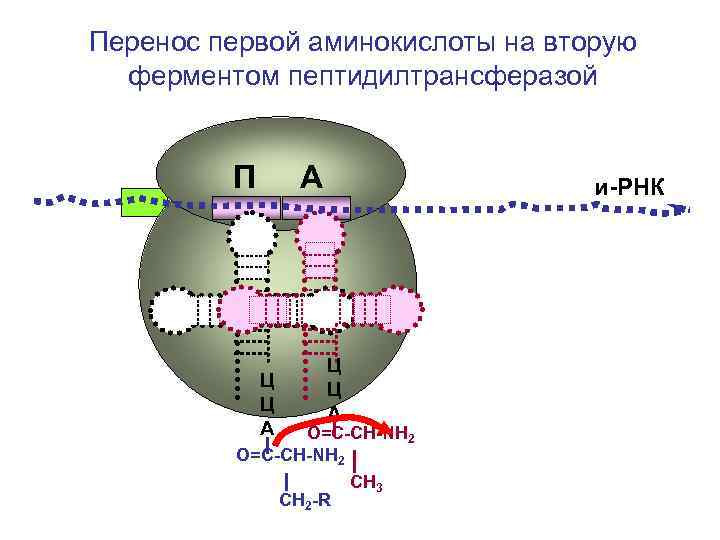
Перенос первой аминокислоты на вторую ферментом пептидилтрансферазой П А Ц Ц А и-РНК Ц Ц А О=С-СН-NH 2 СН 3 СН 2 -R
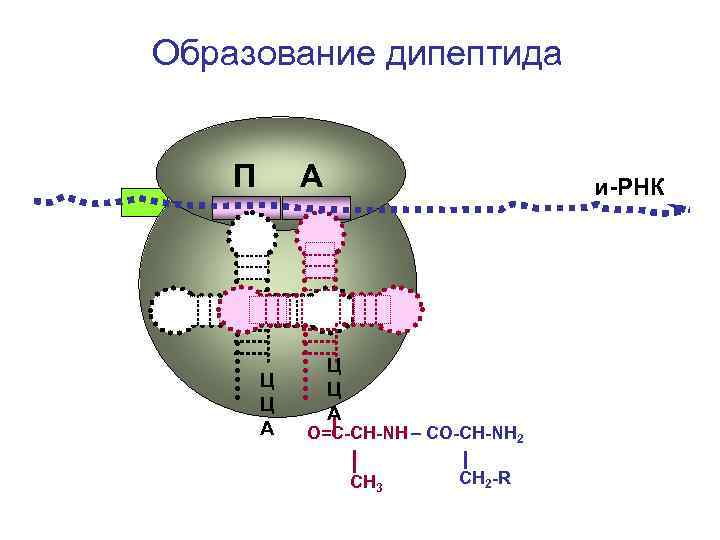
Образование дипептида П А Ц Ц А и-РНК Ц Ц А О=С-СН-NH – CO-CH-NH 2 СН 3 СН 2 -R
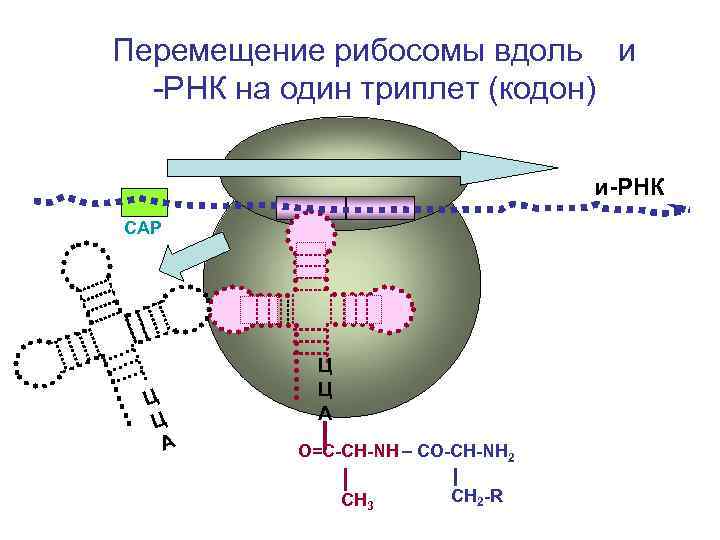
Перемещение рибосомы вдоль и -РНК на один триплет (кодон) и-РНК СAP Ц Ц А О=С-СН-NH – CO-CH-NH 2 СН 3 СН 2 -R
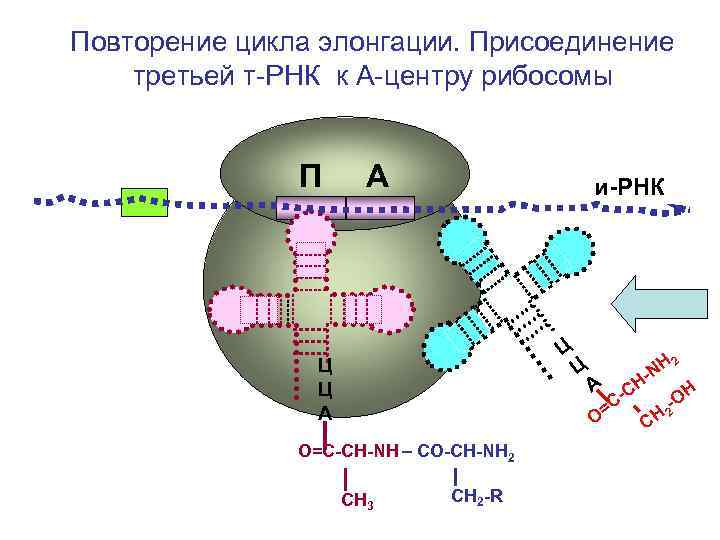
Повторение цикла элонгации. Присоединение третьей т-РНК к А-центру рибосомы П А и-РНК Ц Ц Ц А Н С СО= О=С-СН-NH – CO-CH-NH 2 СН 3 СН 2 -R H -N CH 2 H -O 2
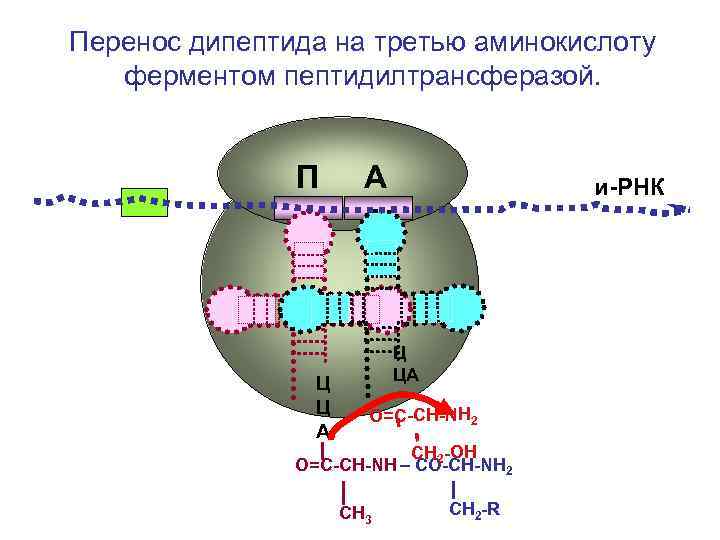
Перенос дипептида на третью аминокислоту ферментом пептидилтрансферазой. П Ц Ц А А и-РНК Ц ЦА О=С-СН-NH 2 CH 2 -OH О=С-СН-NH – CO-CH-NH 2 СН 3 СН 2 -R
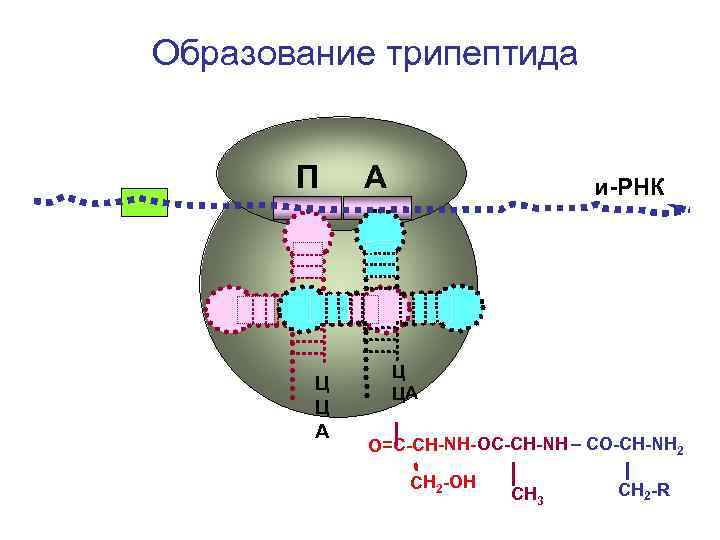
Образование трипептида П Ц Ц А А и-РНК Ц ЦА О=С-СН-NH- ОС-СН-NH – CO-CH-NH 2 CH 2 -OH СН 3 СН 2 -R
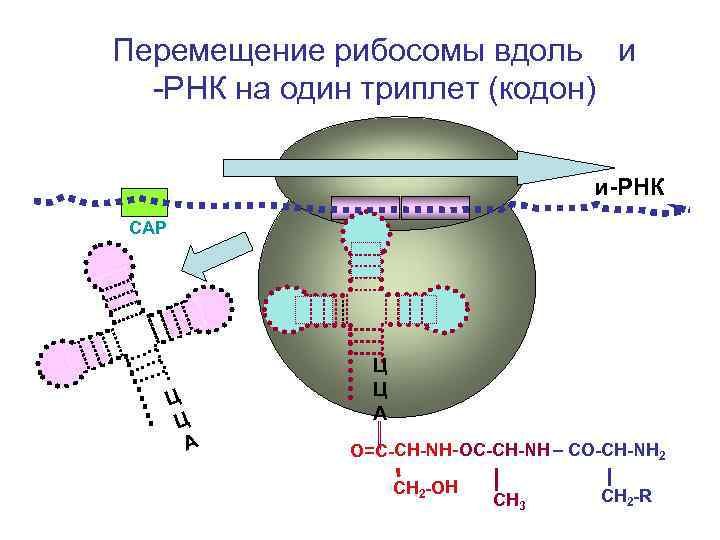
Перемещение рибосомы вдоль и -РНК на один триплет (кодон) и-РНК СAP Ц Ц А О=С-СН-NH- ОС-СН-NH – CO-CH-NH 2 CH 2 -OH СН 3 СН 2 -R

Стадия терминации
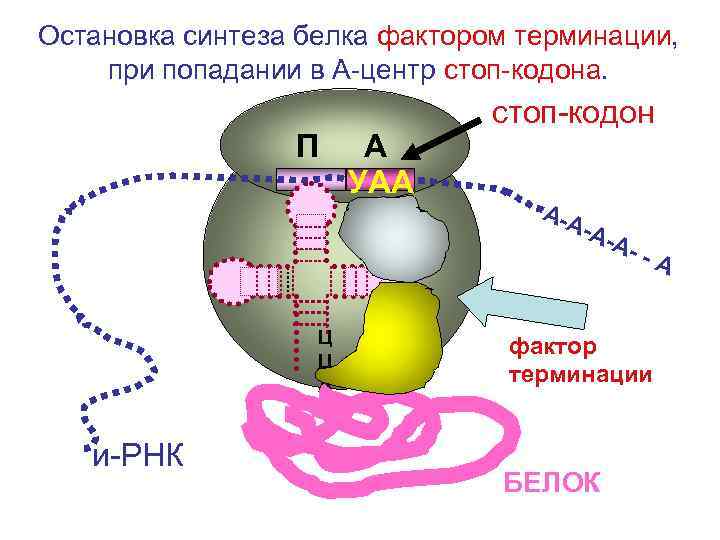
Остановка синтеза белка фактором терминации, при попадании в А-центр стоп-кодона. П А УАА стоп-кодон А-А -А- Ц Ц А и-РНК А- -А фактор терминации БЕЛОК
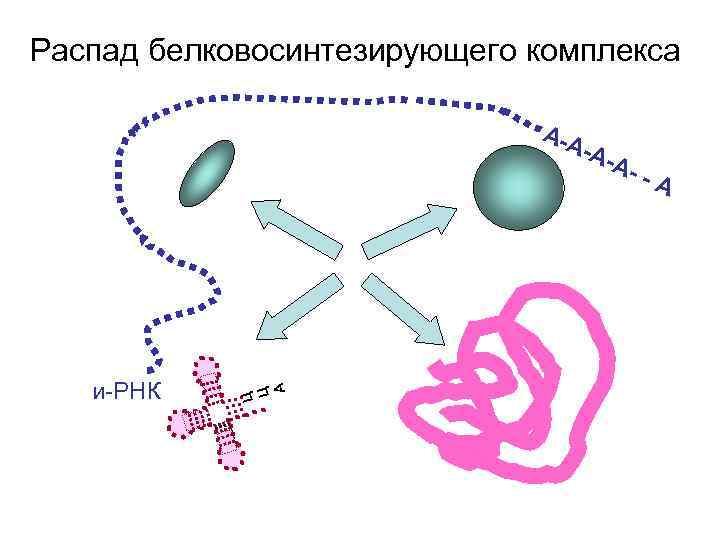
Распад белковосинтезирующего комплекса А-А и-РНК Ц Ц А -А- А- -А
Многие белки требуют достраивания. В аппарат Гольджи
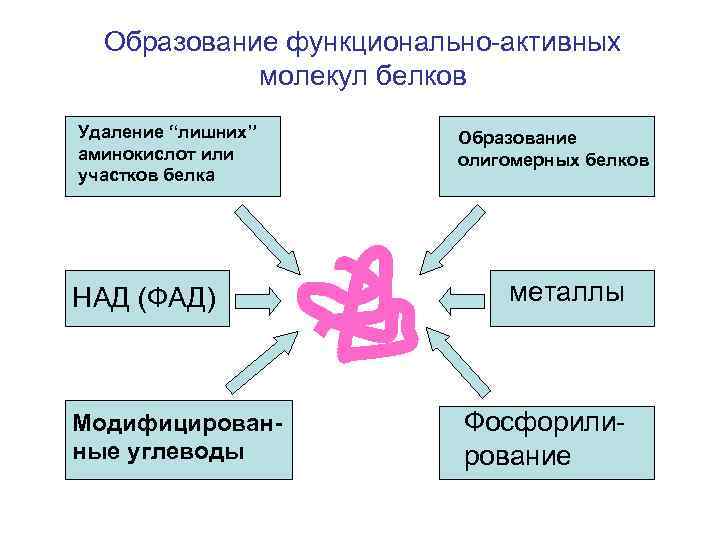
Образование функционально-активных молекул белков Удаление “лишних” аминокислот или участков белка НАД (ФАД) Модифицированные углеводы Образование олигомерных белков металлы Фосфорилирование
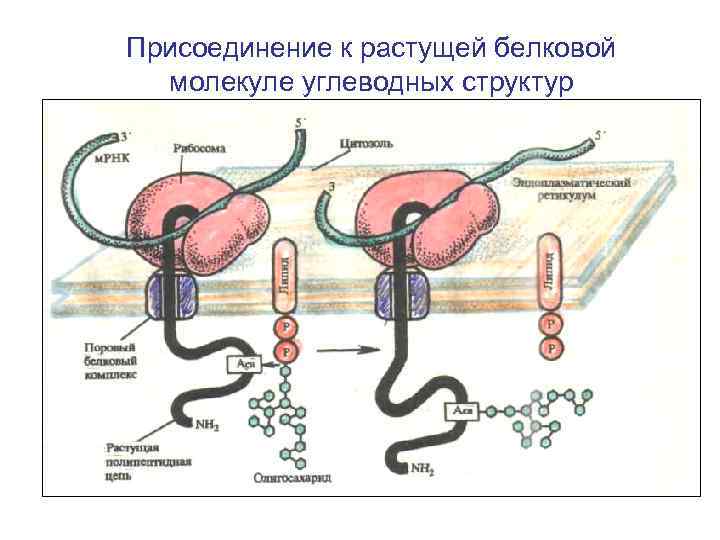
Присоединение к растущей белковой молекуле углеводных структур
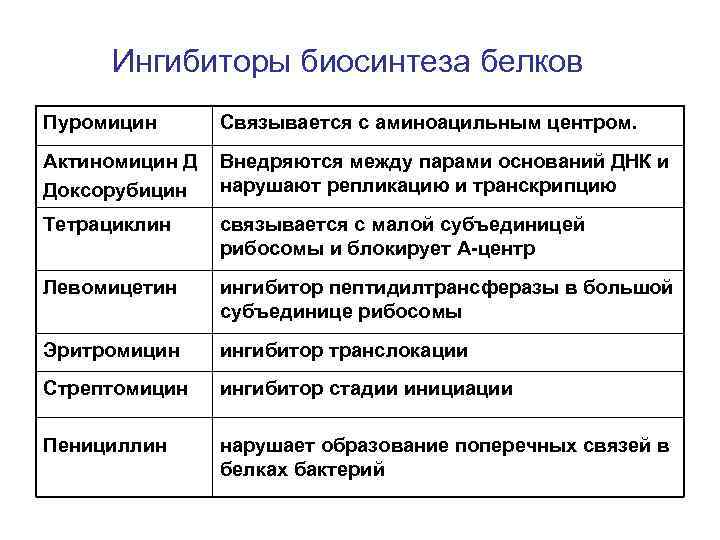
Ингибиторы биосинтеза белков Пуромицин Связывается с аминоацильным центром. Актиномицин Д Доксорубицин Внедряются между парами оснований ДНК и нарушают репликацию и транскрипцию Тетрациклин связывается с малой субъединицей рибосомы и блокирует А-центр Левомицетин ингибитор пептидилтрансферазы в большой субъединице рибосомы Эритромицин ингибитор транслокации Стрептомицин ингибитор стадии инициации Пенициллин нарушает образование поперечных связей в белках бактерий

Трансаминирование аминокислот

Биологическая ценность аминокислот заменимые незаменимые пируват -----------→ аланин треонин глицерин- -----------→ серин метионин серин -------------→ глицин валин аланин------------→ цистеин лейцин щук --------→ аспарагиновая к-та изолейцин оксоглутаровая → глутаминовая к-та лизин глутаминовая к-та -----→ пролин фенилаланин глутаминовая к-та ----→ гистидин триптофан фенилаланин -------→ тирозин аргинин
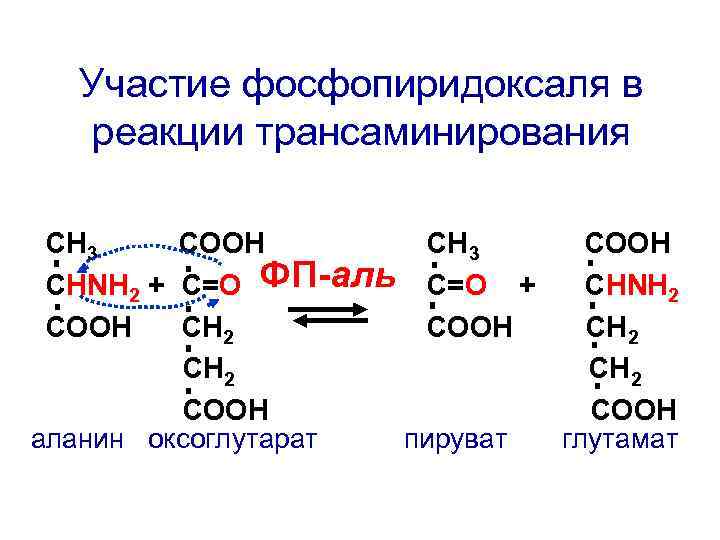
Участие фосфопиридоксаля в реакции трансаминирования СН 3 СООН СНNH 2 + C=О ФП-аль С=О + СНNH 2 СООН СН 2 СООН аланин оксоглутарат пируват глутамат
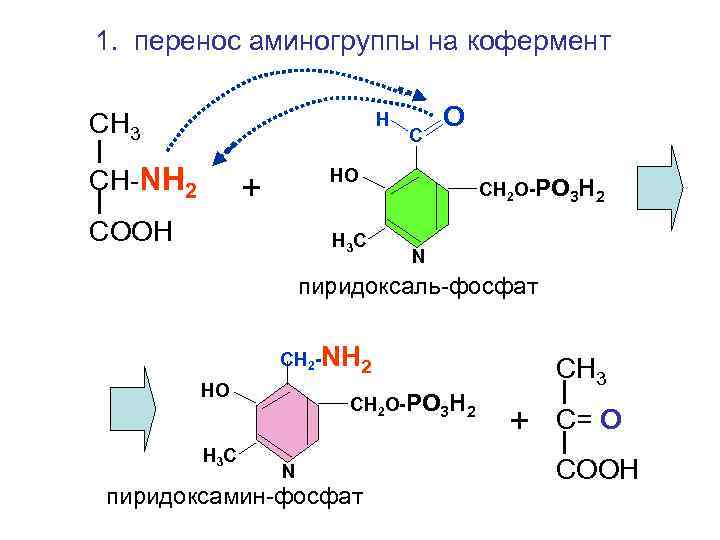
1. перенос аминогруппы на кофермент СН 3 Н СН-NH 2 С О НО + COOH Н 3 С СН 2 О-РО 3 Н 2 N пиридоксаль-фосфат СН 2 -NH 2 НО Н 3 С СН 2 О-РО 3 Н 2 N пиридоксамин-фосфат СН 3 + С= O COOH
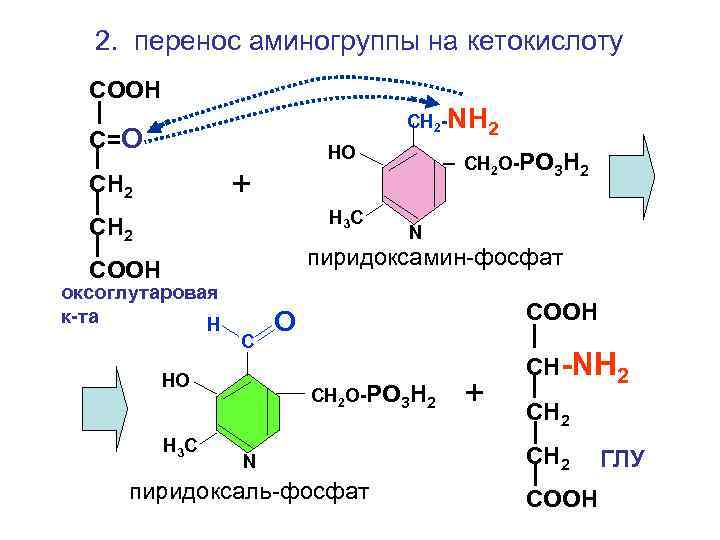
2. перенос аминогруппы на кетокислоту СООН СН 2 -NH 2 С=О НО СН 2 О-РО 3 Н 2 + СН 2 Н 3 С СН 2 N пиридоксамин-фосфат COOH оксоглутаровая к-та Н С НО Н 3 С СООН О СН 2 О-РО 3 Н 2 N пиридоксаль-фосфат + СН-NH 2 СН 2 COOH ГЛУ
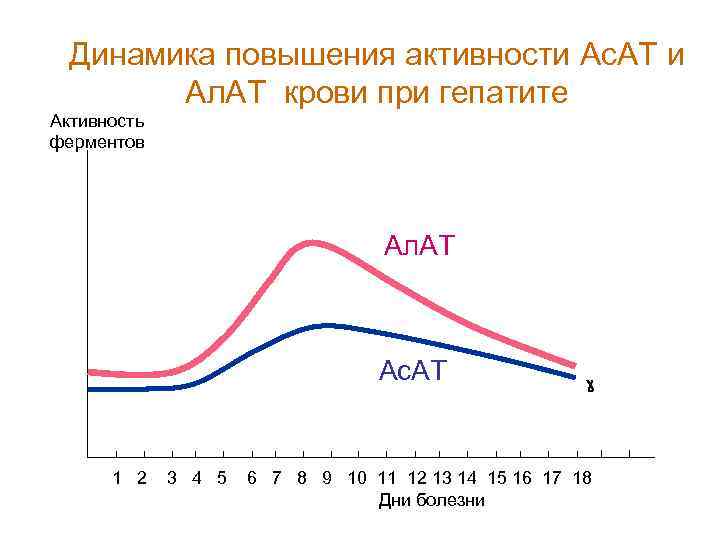
Динамика повышения активности Ас. АТ и Ал. АТ крови при гепатите Активность ферментов Ал. АТ Ас. АТ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 Дни болезни

Декарбоксилирование аминокислот (образование биологическиактивных аминов)
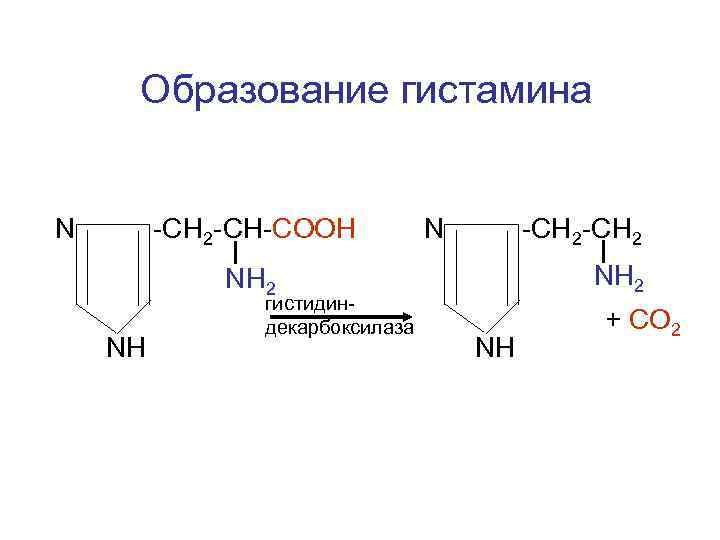
Образование гистамина N -CH 2 -CH-COOH N -CH 2 NH гистидиндекарбоксилаза NH + СО 2
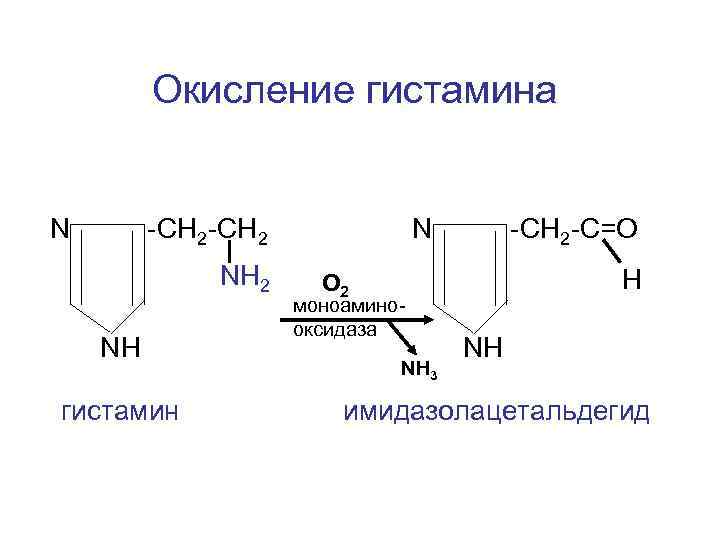
Окисление гистамина N -CH 2 NH гистамин N -CH 2 -C=О Н O 2 моноаминооксидаза NH 3 NH имидазолацетальдегид
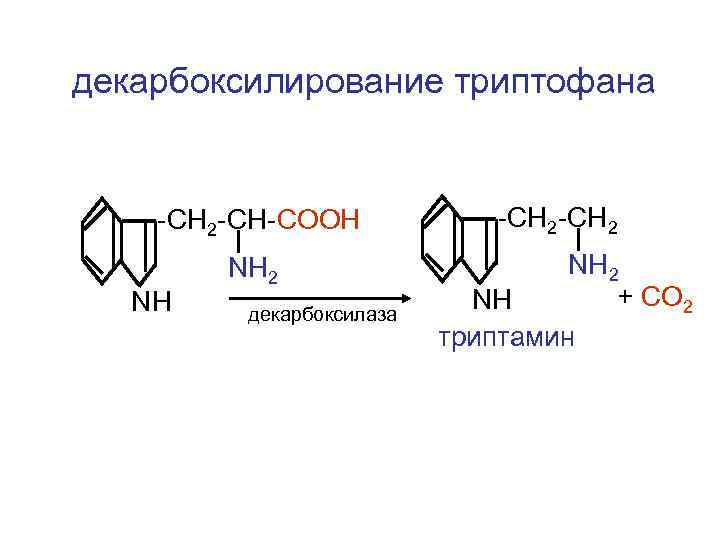
декарбоксилирование триптофана -CH 2 -CH-COOH -CH 2 NH 2 + СО 2 NH триптамин NH декарбоксилаза
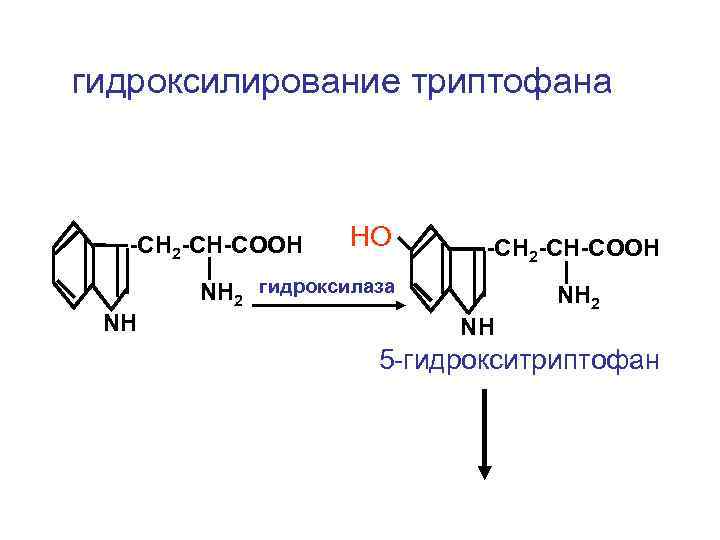
гидроксилирование триптофана -CH 2 -CH-COOH НО -CH 2 -CH-COOH NH 2 гидроксилаза NH NH 2 NH 5 -гидрокситриптофан
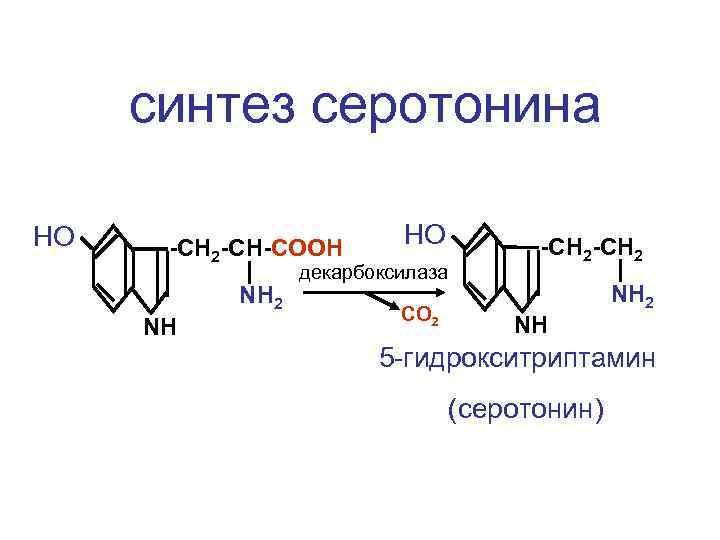
синтез серотонина НО -CH 2 -CH-COOH NH 2 NH НО декарбоксилаза СО 2 -CH 2 NH 5 -гидрокситриптамин (серотонин)
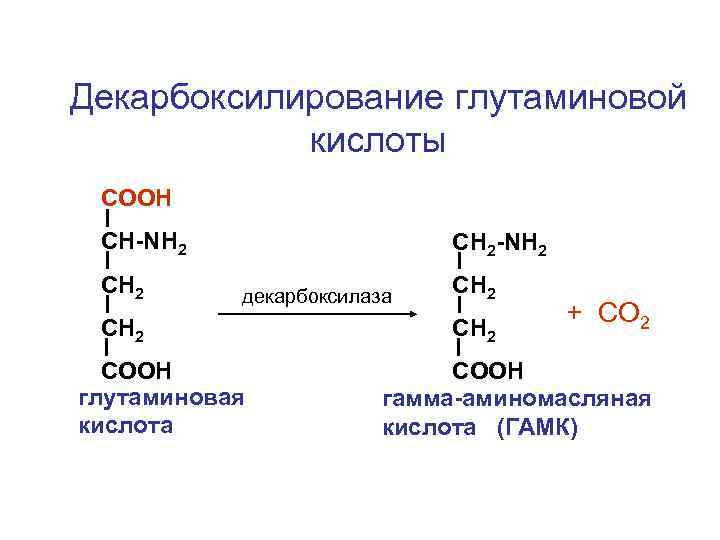
Декарбоксилирование глутаминовой кислоты СOOH CH-NH 2 CH 2 -NH 2 декарбоксилаза CH 2 COOH глутаминовая кислота CH 2 + CO 2 COOH гамма-аминомасляная кислота (ГАМК)
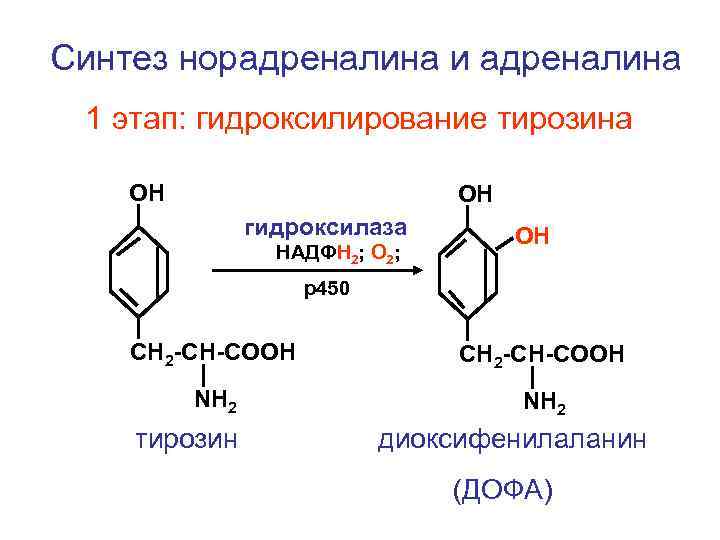
Синтез норадреналина и адреналина 1 этап: гидроксилирование тирозина ОН ОН гидроксилаза НАДФН 2; О 2; ОН р450 CH 2 -CH-COOH NH 2 тирозин диоксифенилаланин (ДОФА)
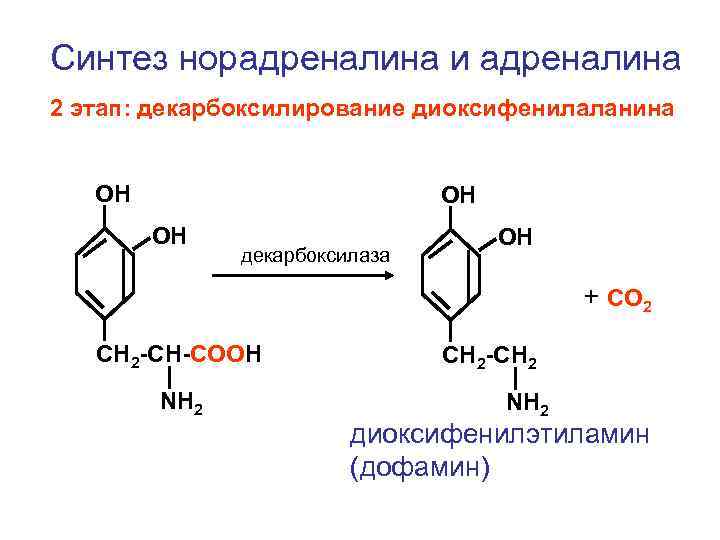
Синтез норадреналина и адреналина 2 этап: декарбоксилирование диоксифенилаланина ОН ОН ОН декарбоксилаза ОН + СО 2 CH 2 -CH-COOH NH 2 CH 2 -CH 2 NH 2 диоксифенилэтиламин (дофамин)
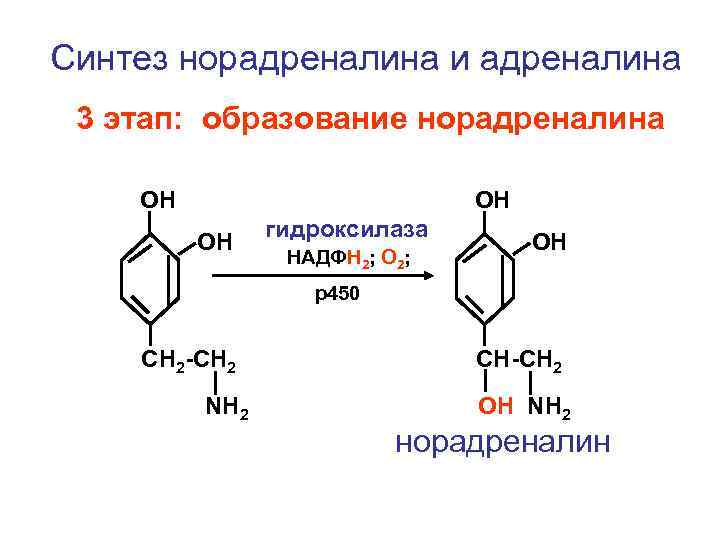
Синтез норадреналина и адреналина 3 этап: образование норадреналина ОН ОН ОН гидроксилаза НАДФН 2; О 2; ОН р450 CH 2 -CH 2 NH 2 CH-CH 2 ОН NH 2 норадреналин
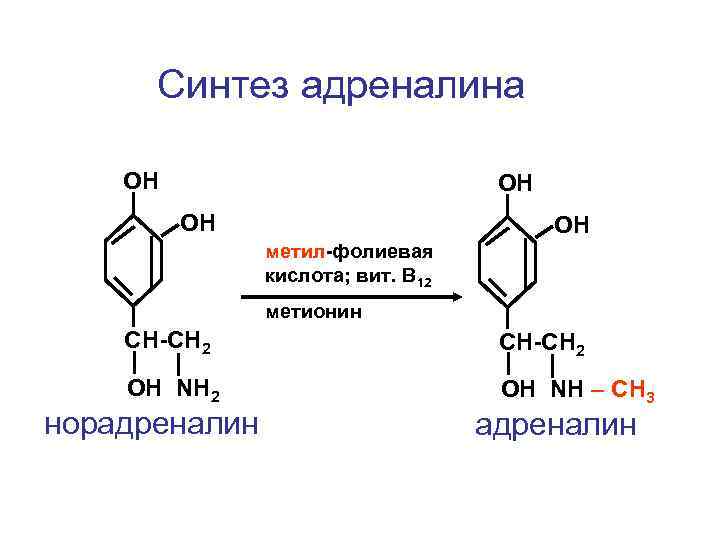
Синтез адреналина ОН ОН метил-фолиевая кислота; вит. В 12 метионин CH-CH 2 ОН NH – СН 3 норадреналин

Окислительное дезаминирование аминокислот
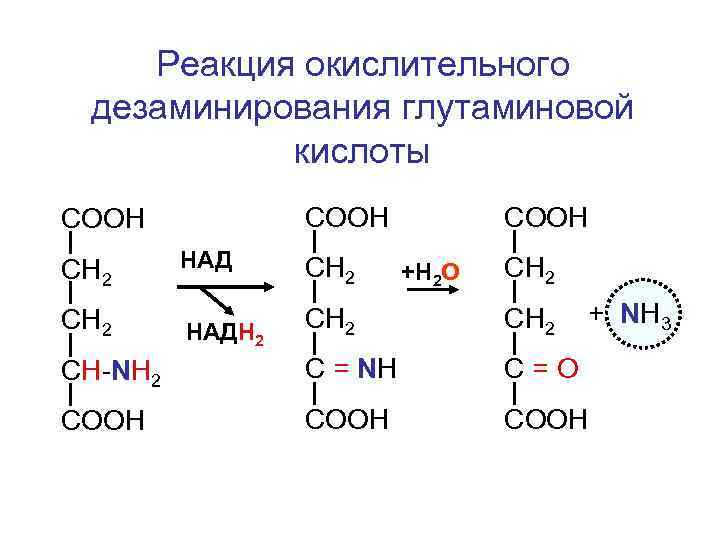
Реакция окислительного дезаминирования глутаминовой кислоты СООН СН 2 HАД СН 2 СООН +Н 2 О СН 2 + NH 3 СН 2 CH-NH 2 C = NH C=О COOH СН 2 HАДН 2
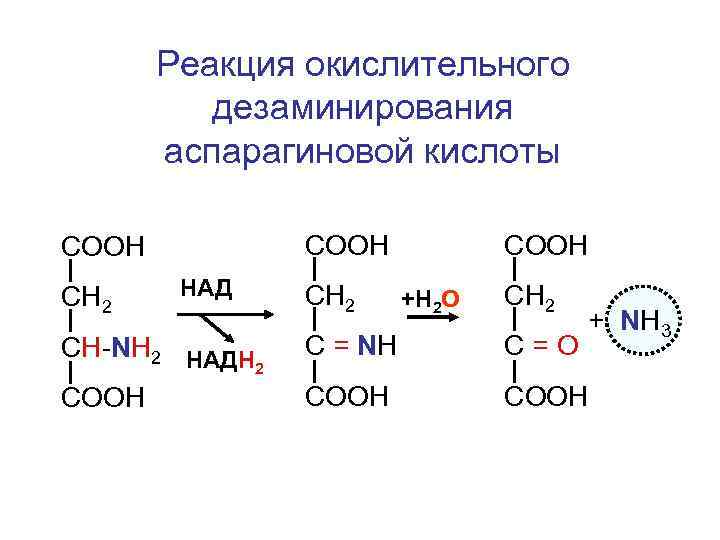
Реакция окислительного дезаминирования аспарагиновой кислоты СООН СН 2 HАД CH-NH 2 HАДН 2 COOH СН 2 СООН +Н 2 О СН 2 + NH 3 C = NH C=О COOH
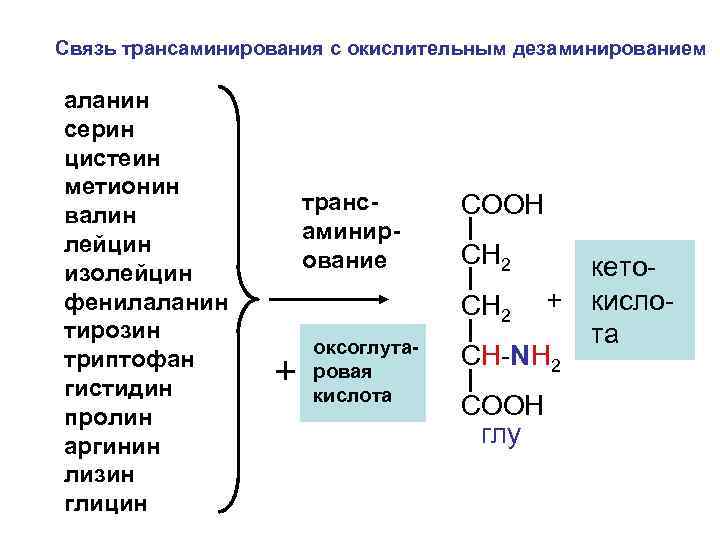
Связь трансаминирования с окислительным дезаминированием аланин серин цистеин метионин валин лейцин изолейцин фенилаланин тирозин триптофан гистидин пролин аргинин лизин глицин трансаминирование СООН СН 2 + оксоглутаровая кислота + CH-NH 2 COOH глу кетокислота
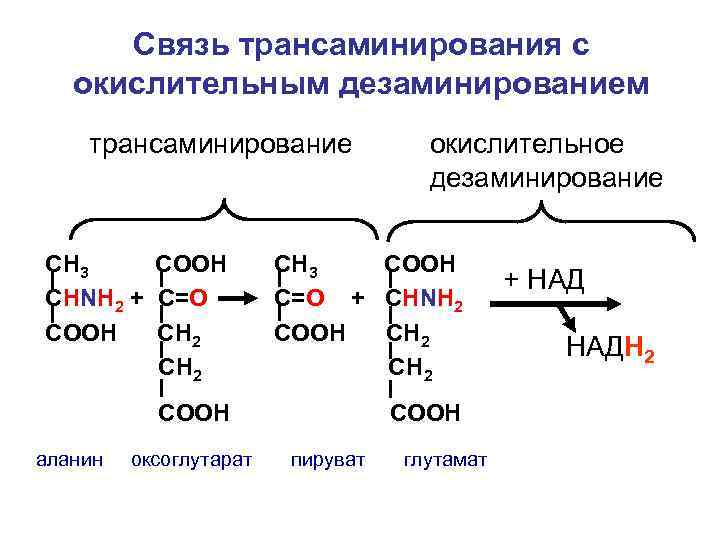
Связь трансаминирования с окислительным дезаминированием трансаминирование окислительное дезаминирование СН 3 СООН СНNH 2 + C=О СООН СН 2 СН 3 СООН С=О + СНNH 2 СООН СН 2 СООН аланин оксоглутарат пируват глутамат + НАДН 2
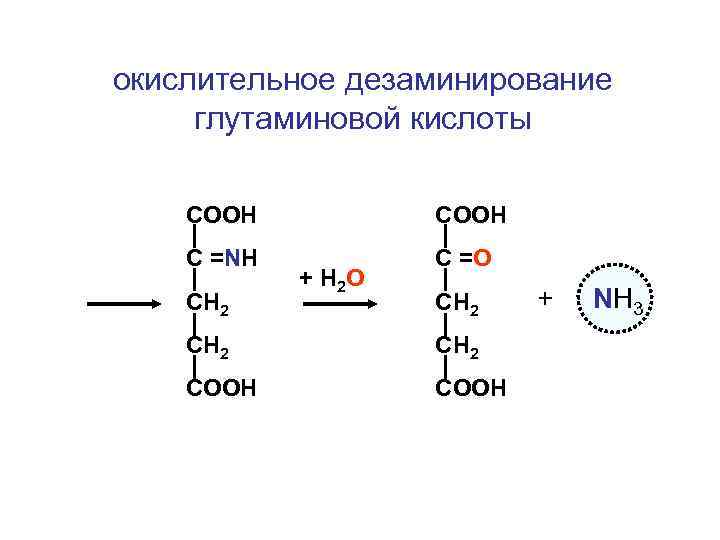
окислительное дезаминирование глутаминовой кислоты СООН С =NH С =O СН 2 + Н 2 О СН 2 CH 2 COOH + NH 3
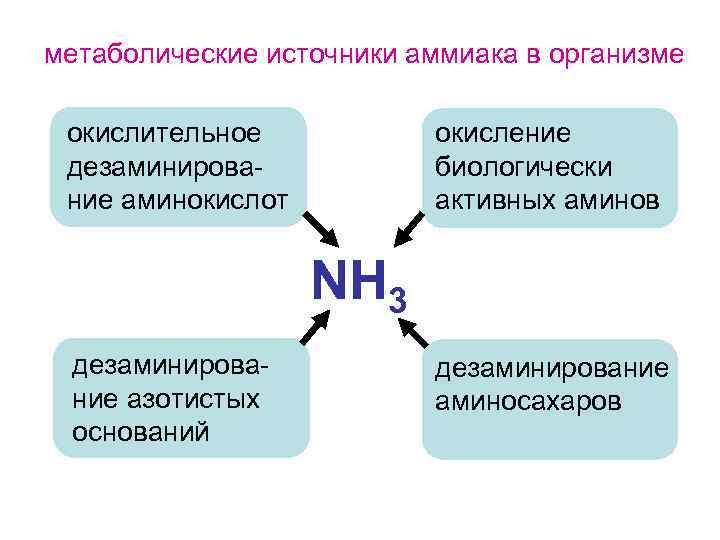
метаболические источники аммиака в организме окислительное дезаминирование аминокислот окисление биологически активных аминов NH 3 дезаминирование азотистых оснований дезаминирование аминосахаров

главный механизм обезвреживания аммиака в организме
Местом обезвреживания аммиака в организме ( 20 г в сутки) является печень • •
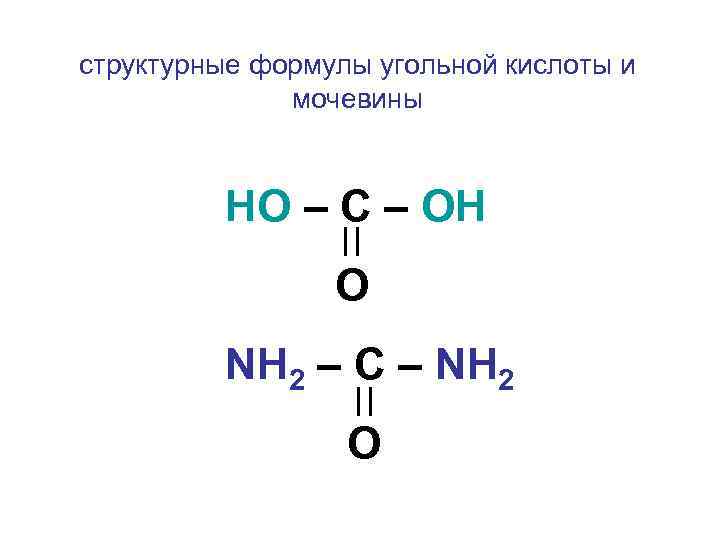
структурные формулы угольной кислоты и мочевины НО – С – ОН О NH 2 – C – NH 2 O

синтез мочевины
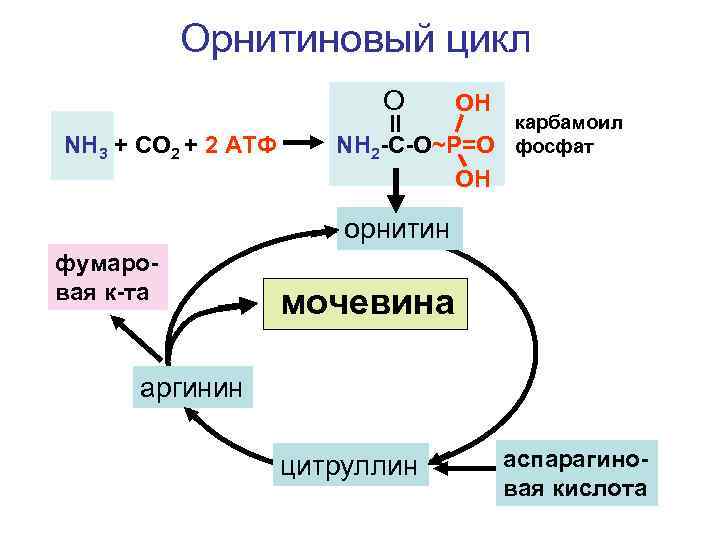
Орнитиновый цикл O NH 3 + CO 2 + 2 АТФ OH NH 2 -C-O~P=O OH карбамоил фосфат орнитин фумаровая к-та мочевина аргинин цитруллин аспарагиновая кислота
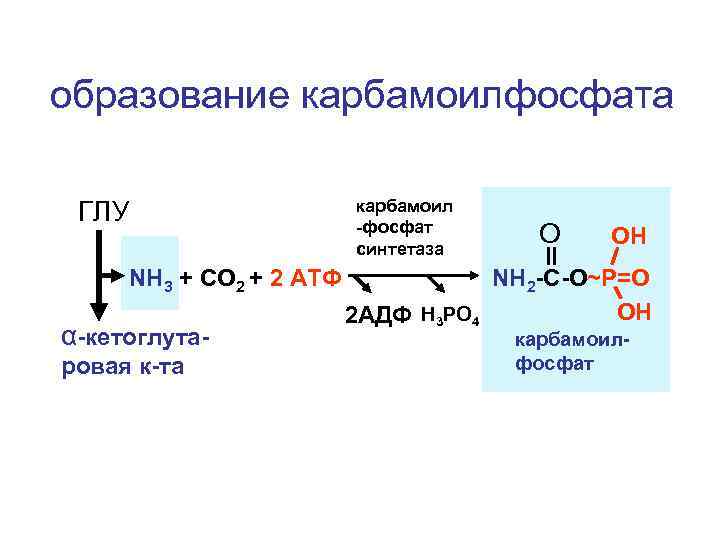
образование карбамоилфосфата ГЛУ NH 3 + CO 2 + 2 АТФ α-кетоглутаровая к-та карбамоил -фосфат синтетаза O OH NH 2 -C-O~P=O OH 2 АДФ H 3 PO 4 карбамоилфосфат
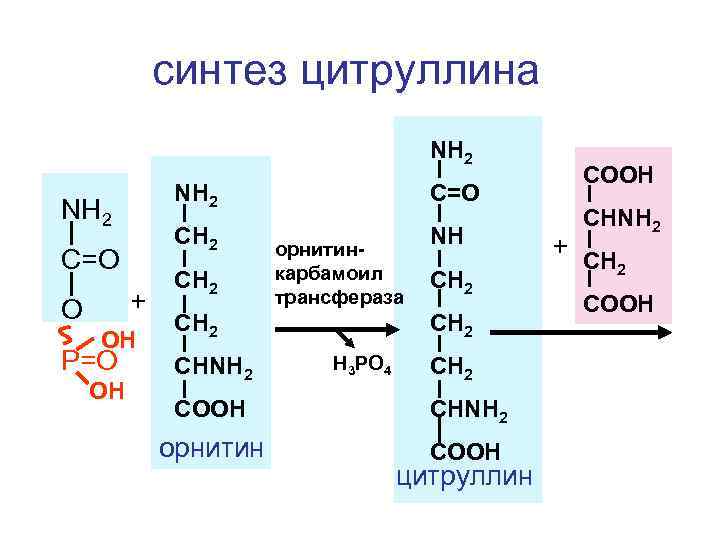
синтез цитруллина NH 2 CH 2 C=O + O OH P=O OH C=O NH 2 CH 2 орнитинкарбамоил трансфераза CH 2 CHNH 2 NH H 3 PO 4 CH 2 COOH CHNH 2 орнитин COOH цитруллин COOH CHNH 2 + CH 2 COOH
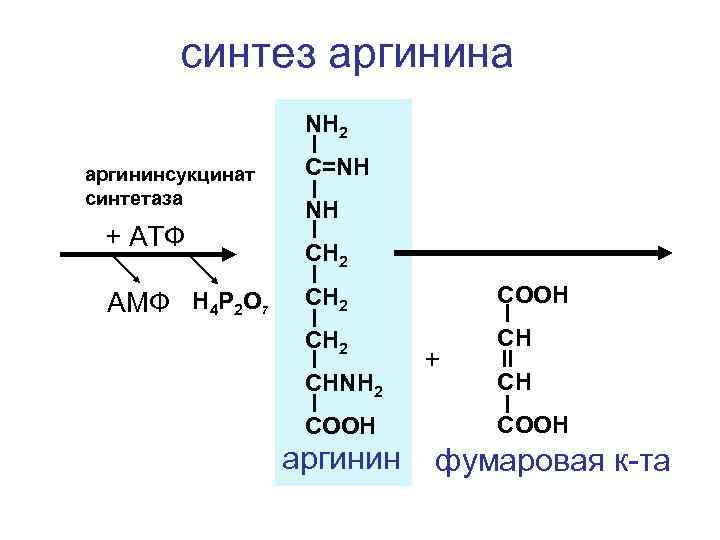
синтез аргинина NH 2 аргининсукцинат синтетаза + АТФ АМФ H 4 P 2 O 7 C=NH NH CH 2 COOH CH 2 CH CHNH 2 COOH аргинин + CH COOH фумаровая к-та
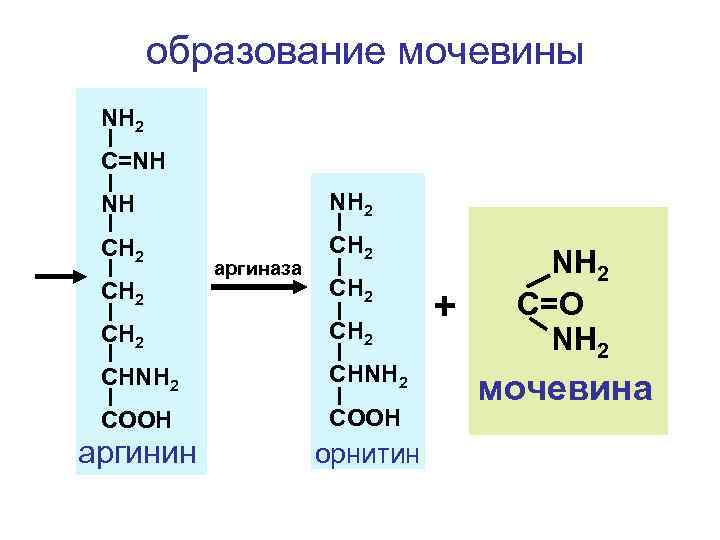
образование мочевины NH 2 C=NH NH NH 2 CH 2 аргиназа CH 2 CHNH 2 COOH аргинин орнитин + NH 2 C=O NH 2 мочевина
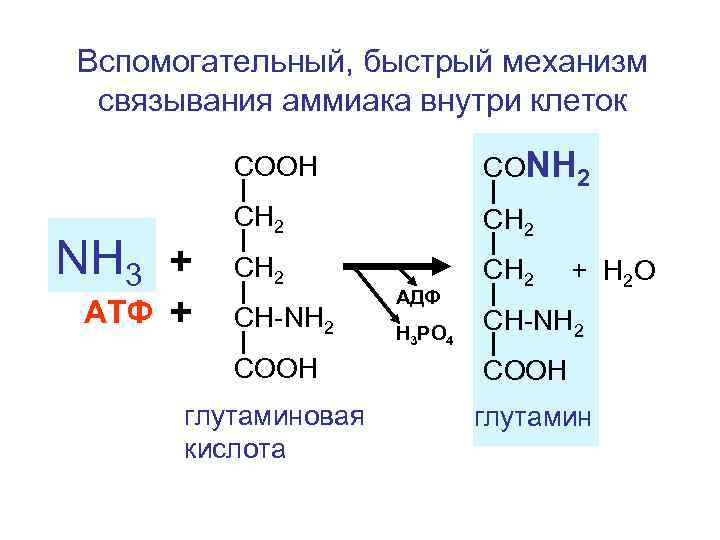
Вспомогательный, быстрый механизм связывания аммиака внутри клеток СООН NH 3 + АТФ + СОNH 2 СН 2 CH-NH 2 АДФ Н 3 РО 4 + H 2 O CH-NH 2 COOH глутаминовая кислота глутамин
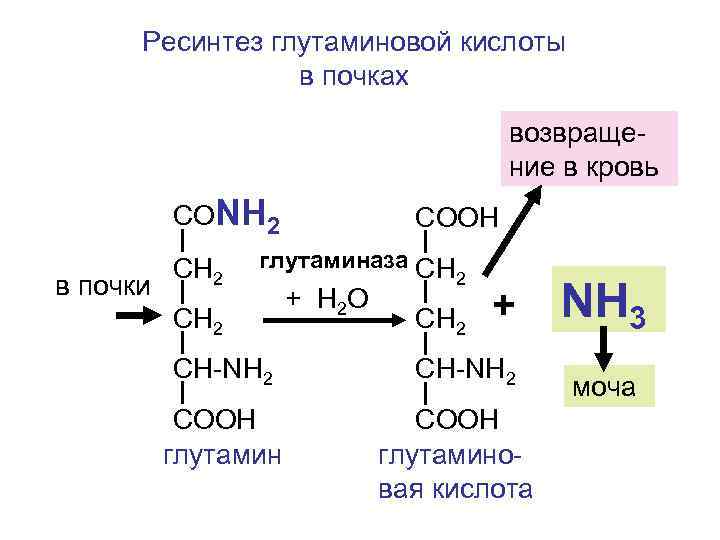
Ресинтез глутаминовой кислоты в почках возвращение в кровь СОNH 2 в почки СН 2 СООН глутаминаза СН СН 2 CH-NH 2 COOH глутамин + H 2 O 2 СН 2 + CH-NH 2 COOH глутаминовая кислота NH 3 моча
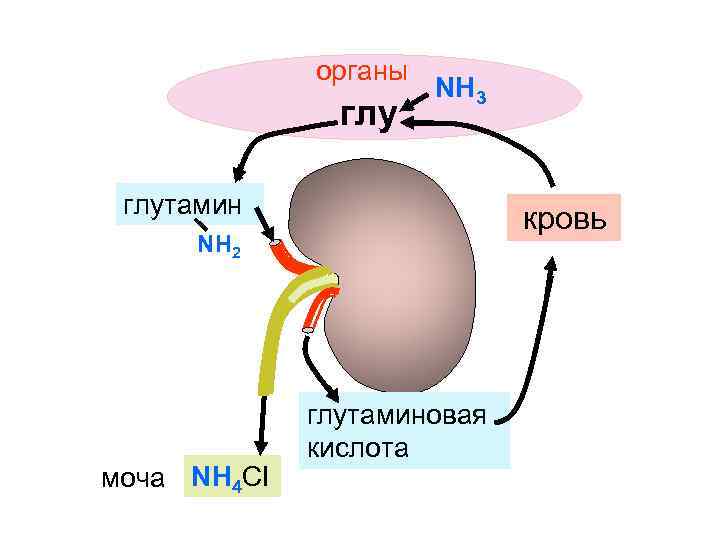
органы глу NH 3 глутамин кровь NH 2 моча NH 4 CI глутаминовая кислота

Содержание мочевины в крови 2, 5 – 8, 3 ммоль/л сыворотки (За сутки с мочой выделяется 20 -35 г)

Регуляция обмена белков
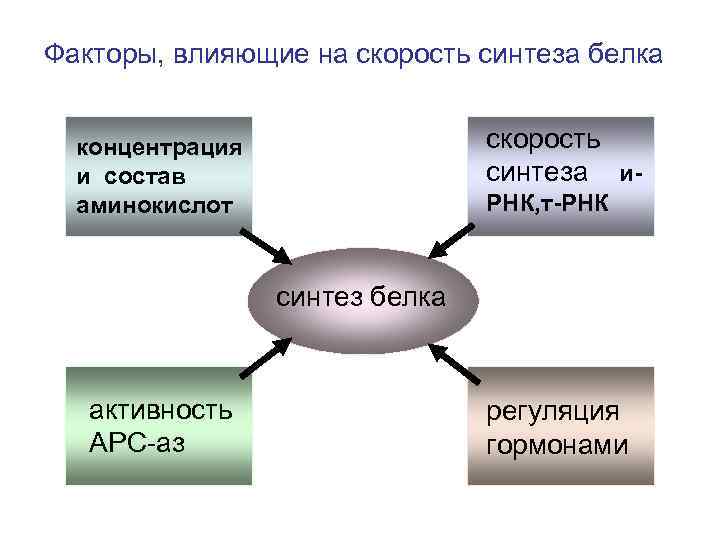
Факторы, влияющие на скорость синтеза белка скорость синтеза и- концентрация и состав аминокислот РНК, т-РНК синтез белка активность АРС-аз регуляция гормонами

Влияние некоторых факторов на концентрацию и состав аминокислот 1. Доступность в белковой диете; 2. 2. Наличие полноценных белков в продуктах; 3. 2. Содержание альбумина в крови; 4. 3. Заболевания органов пищеварения; 5. 4. Нарушения всасывания аминокислот; 6. 5. Заболевания почек, печени, поджелудочной железы; 7. 6. Гиповитаминоз (В 6; фолиевой кислоты,

Влияние некоторых факторов на активность АРС-аз 1. Активность белково-синтезирующей системы; 2. 2. Кислотно-основное состояние в организме; 3. 3. Состояние биоэнергетических процессов.

Факторы, влияющие на скорость синтеза и-РНК и т-РНК 1. Наличие нуклеотидного фонда; 2. Состояние биоэнергетических процессов; 3. 3. Влияние факторов роста на процесс транскрипции (индукция и репрессия генов).

Гормональная регуляция скорости синтеза белка 1. Соматотропин, половые гормоны (индукторы транскрипции и биосинтеза белка); 2. 2. Тироксин (активатор транскрипции ферментов, осуществляющих липолиз и протеолиз); 3. 3. Инсулин (активатор транскрипции ферментов, участвующих в углеводном обмене); 4. 4. Глюкокортикоиды (репрессоры транскрипции генов, контролирующих синтез белков и липидов. Индукторы транскрипции и биосинтеза ферментов глюконеогенеза).

На скорость дезаминирования аминокислот влияют: 1. Соотношение НАДН 2 /НАД. При гипоксии увеличивается концентрация НАДН 2. Недостаток НАД служит причиной замедления скорости дезаминирования аминокислот. 2. 2. Концентрация NH 3. Увеличение концентрации аммиака замедляет процесс дезаминирования. 3. 3. Снижение концентрации глутаминовой кислоты или аспарагиновой кислоты понижает скорость окислительного дезаминирования.

Взаимосвязь между обменом белков, углеводов и липидов.
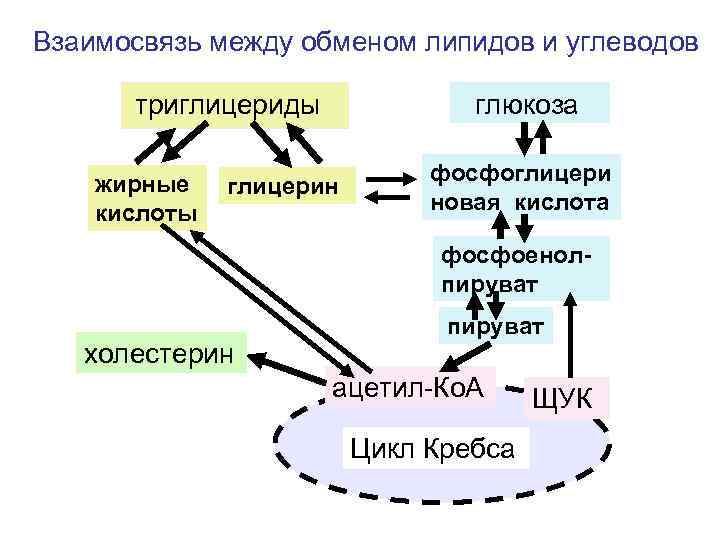
Взаимосвязь между обменом липидов и углеводов триглицериды жирные кислоты глюкоза глицерин фосфоглицери новая кислота фосфоенолпируват холестерин пируват ацетил-Ко. А Цикл Кребса ЩУК
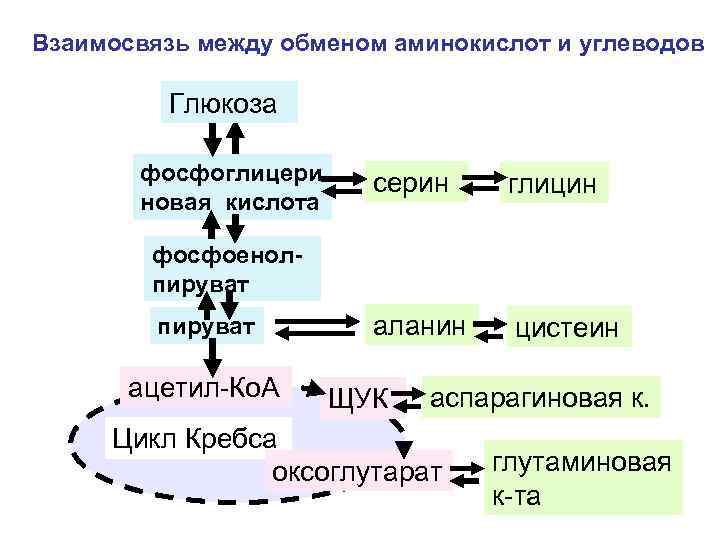
Взаимосвязь между обменом аминокислот и углеводов Глюкоза фосфоглицери новая кислота серин глицин аланин цистеин фосфоенолпируват ацетил-Ко. А ЩУК аспарагиновая к. Цикл Кребса оксоглутарат глутаминовая к-та
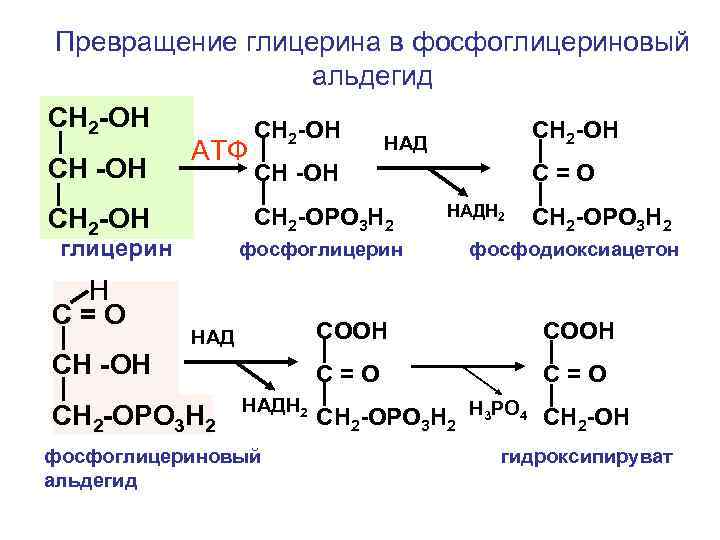
Превращение глицерина в фосфоглицериновый альдегид СН 2 -ОН СН -ОН АТФ глицерин СН -ОН фосфоглицерин С=О НАДН 2 СН 2 -ОРО 3 Н 2 фосфодиоксиацетон СООН СН -ОН НАДН 2 фосфоглицериновый альдегид СООН С=О НАД СН 2 -ОРО 3 Н 2 СН 2 -ОН Н С=О СН 2 -ОРО 3 Н 2 Н 3 РО 4 СН 2 -ОН гидроксипируват
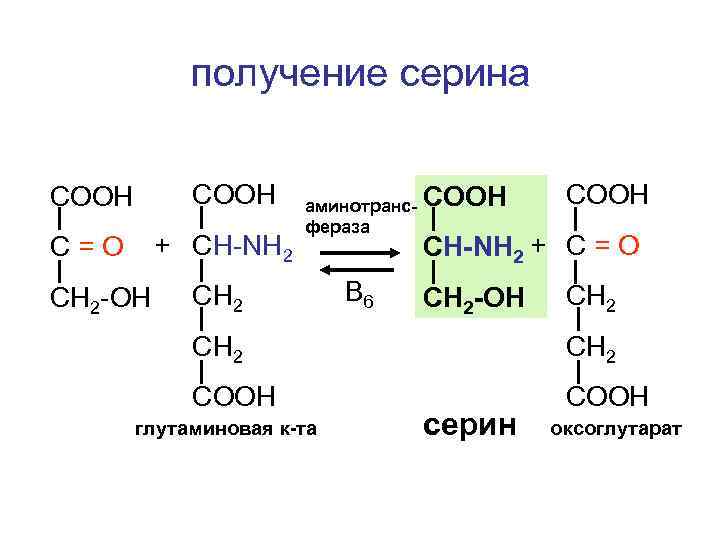
получение серина СООН + СH-NH 2 С=О СН 2 -ОН аминотранс- СООН фераза CH 2 СООН СH-NH 2 + С = O В 6 СН 2 -ОН CH 2 COOH глутаминовая к-та серин оксоглутарат
Обмен белков -5.ppt