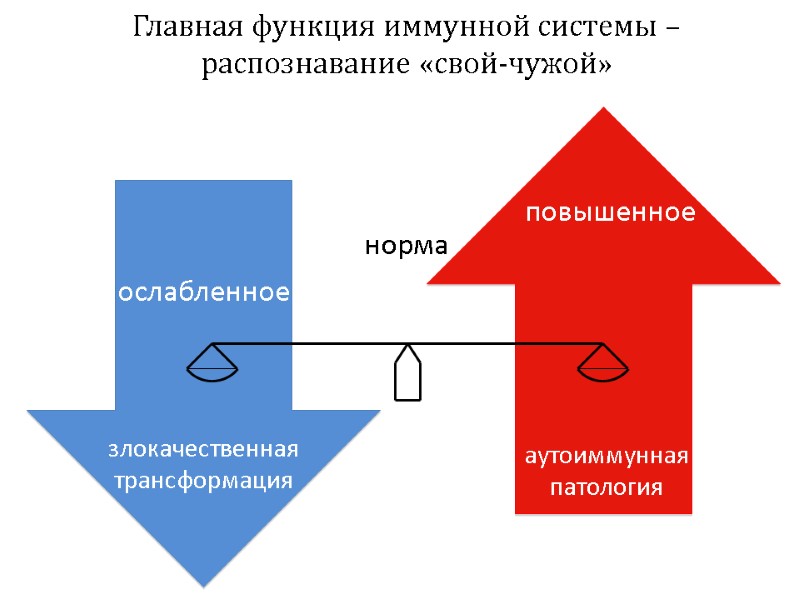
Главная функция иммунной системы – распознавание «свой-чужой» норма












16514-university_3_2012.ppt
- Количество слайдов: 106
 Главная функция иммунной системы – распознавание «свой-чужой» норма ослабленное повышенное злокачественная трансформация аутоиммунная патология
Главная функция иммунной системы – распознавание «свой-чужой» норма ослабленное повышенное злокачественная трансформация аутоиммунная патология
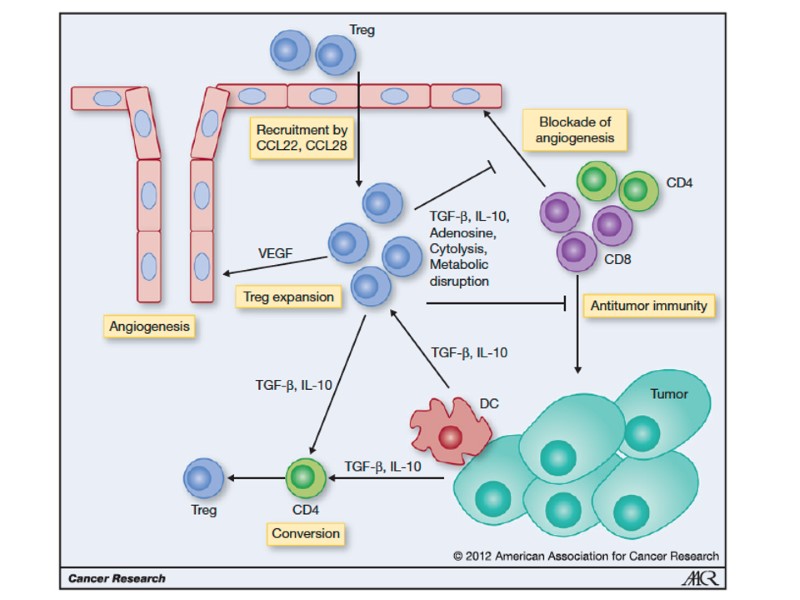
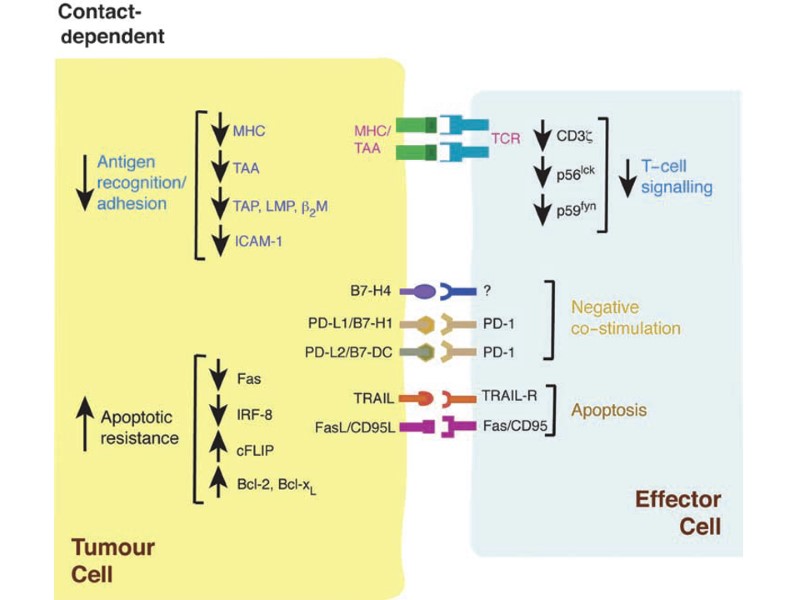
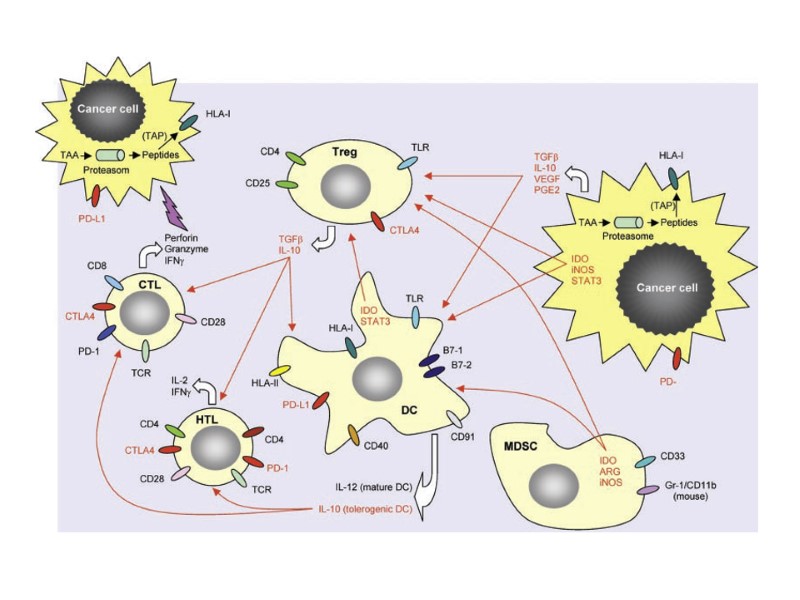
 Несостоятельность противоопухолевого иммунитета: Неполноценность опухолевого АГ Нарушения экспрессии MHC (отсутствуют или изменены) Нарушения костимуляции Феномен усиления опухолевого роста (противоопухолевые АТ защищают опухоль) Синтез супрессорных цитокинов (TGF α,β, IL-10, простагландин E2) Иммунологическая толерантность к опухолевому АГ Активация Т-лимфоцитов супрессоров (Treg) Опухоль индуцирует апоптоз в микроокружении Нарушение сигнальной трансдукции (нет апоптоза в опухоли) Большое количество опухолевой ткани – недостаточно эффекторов
Несостоятельность противоопухолевого иммунитета: Неполноценность опухолевого АГ Нарушения экспрессии MHC (отсутствуют или изменены) Нарушения костимуляции Феномен усиления опухолевого роста (противоопухолевые АТ защищают опухоль) Синтез супрессорных цитокинов (TGF α,β, IL-10, простагландин E2) Иммунологическая толерантность к опухолевому АГ Активация Т-лимфоцитов супрессоров (Treg) Опухоль индуцирует апоптоз в микроокружении Нарушение сигнальной трансдукции (нет апоптоза в опухоли) Большое количество опухолевой ткани – недостаточно эффекторов
 Биотерапия опухолей Биологическая терапия – метод лечения злокачественных опухолей, основанный на использовании модификаторов биологического ответа, непосредственно или косвенно влияющих на уменьшение объема опухолевой массы. Под термином "иммунотерапия" подразумевается раздел биотерапии, ограниченный применением методов, воздействующих на эффекторы иммунной системы.
Биотерапия опухолей Биологическая терапия – метод лечения злокачественных опухолей, основанный на использовании модификаторов биологического ответа, непосредственно или косвенно влияющих на уменьшение объема опухолевой массы. Под термином "иммунотерапия" подразумевается раздел биотерапии, ограниченный применением методов, воздействующих на эффекторы иммунной системы.
 Общие свойства методов БТ: - подавляют ростовые факторы, обуславливающие опухолевую прогрессию, - повышают распознаваемость опухолевых клеток клетками иммунной системы, - повышают цитотоксичность клеток иммунной системы, таких как Т-клетки, NK-клетки, макрофаги, - блокируют процессы трансформации клеток в злокачественные,
Общие свойства методов БТ: - подавляют ростовые факторы, обуславливающие опухолевую прогрессию, - повышают распознаваемость опухолевых клеток клетками иммунной системы, - повышают цитотоксичность клеток иммунной системы, таких как Т-клетки, NK-клетки, макрофаги, - блокируют процессы трансформации клеток в злокачественные,
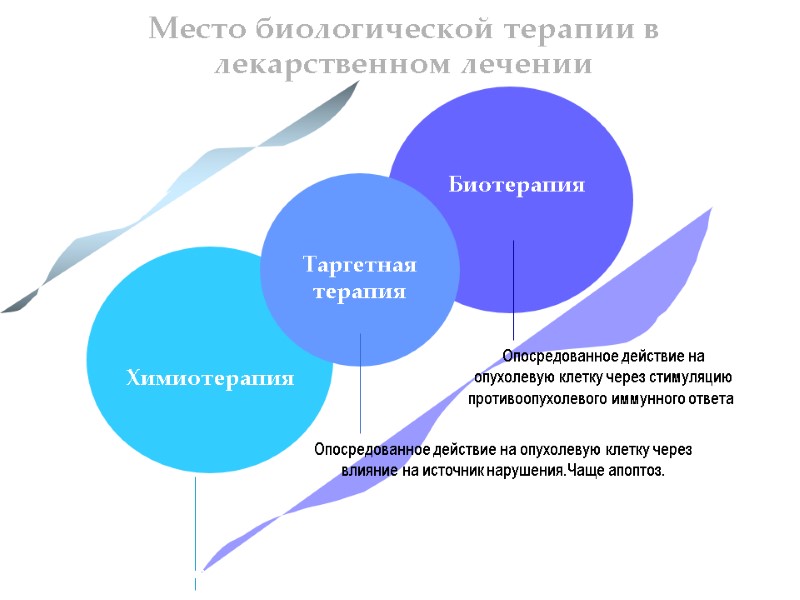
 Место биологической терапии в лекарственном лечении Химиотерапия Таргетная терапия Биотерапия Прямое цитотоксическое действие Опосредованное действие на опухолевую клетку через влияние на источник нарушения.Чаще апоптоз. Опосредованное действие на опухолевую клетку через стимуляцию противоопухолевого иммунного ответа.
Место биологической терапии в лекарственном лечении Химиотерапия Таргетная терапия Биотерапия Прямое цитотоксическое действие Опосредованное действие на опухолевую клетку через влияние на источник нарушения.Чаще апоптоз. Опосредованное действие на опухолевую клетку через стимуляцию противоопухолевого иммунного ответа.
 Общие свойства методов БТ: - регулируют апоптоз, - блокируют неоангиогенез - блокируют некоторые регуляторные системы иммунной системы, ответственные за иммуносупрессию, - снижают риск метастазирования, - повышают восстановление числа иммунокомпетентных клеток после воздействия химио- или лучевой терапии.
Общие свойства методов БТ: - регулируют апоптоз, - блокируют неоангиогенез - блокируют некоторые регуляторные системы иммунной системы, ответственные за иммуносупрессию, - снижают риск метастазирования, - повышают восстановление числа иммунокомпетентных клеток после воздействия химио- или лучевой терапии.










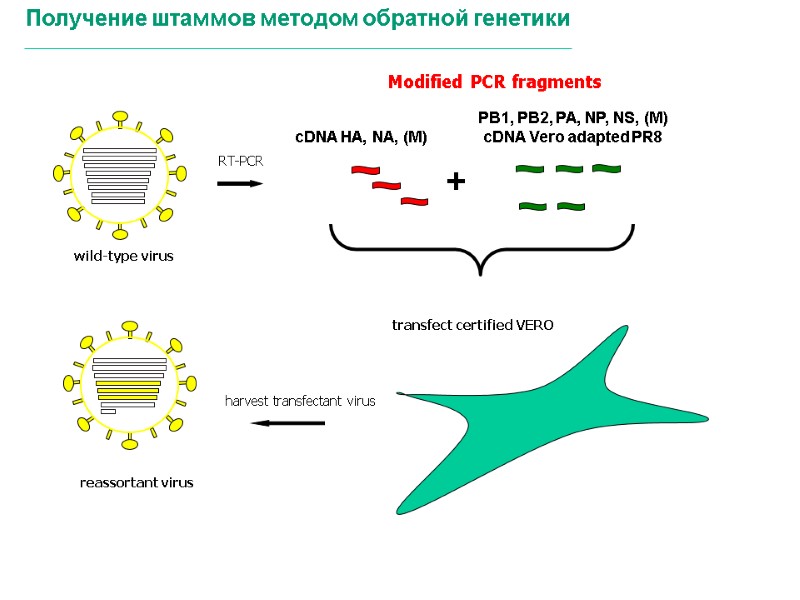
 cDNA HA, NA, (M) + PB1, PB2, PA, NP, NS, (M) cDNA Vero adapted PR8 transfect certified VERO harvest transfectant virus wild-type virus reassortant virus Modified PCR fragments RT-PCR Получение штаммов методом обратной генетики
cDNA HA, NA, (M) + PB1, PB2, PA, NP, NS, (M) cDNA Vero adapted PR8 transfect certified VERO harvest transfectant virus wild-type virus reassortant virus Modified PCR fragments RT-PCR Получение штаммов методом обратной генетики
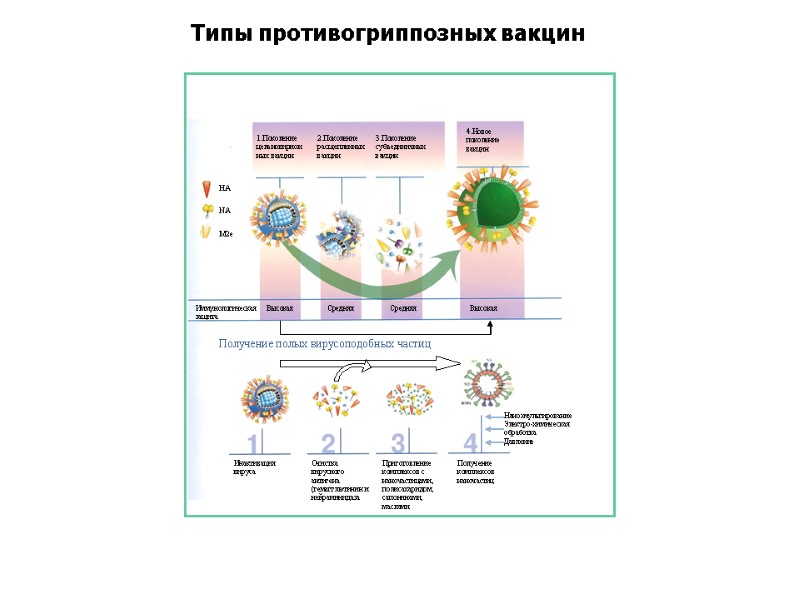
 Типы противогриппозных вакцин
Типы противогриппозных вакцин
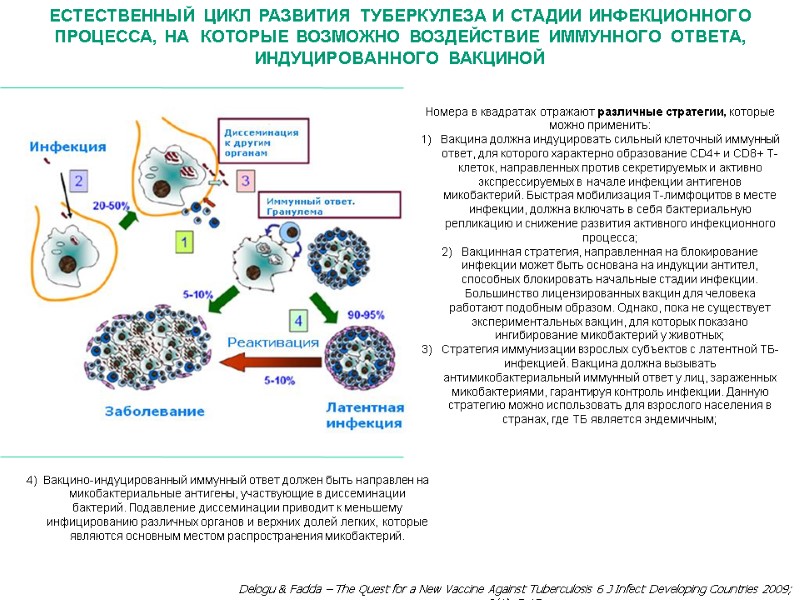
 Delogu & Fadda – The Quest for a New Vaccine Against Tuberculosis 6 J Infect Developing Countries 2009; 3(1): 5-15. Номера в квадратах отражают различные стратегии, которые можно применить: Вакцина должна индуцировать сильный клеточный иммунный ответ, для которого характерно образование CD4+ и CD8+ Т-клеток, направленных против секретируемых и активно экспрессируемых в начале инфекции антигенов микобактерий. Быстрая мобилизация Т-лимфоцитов в месте инфекции, должна включать в себя бактериальную репликацию и снижение развития активного инфекционного процесса; Вакцинная стратегия, направленная на блокирование инфекции может быть основана на индукции антител, способных блокировать начальные стадии инфекции. Большинство лицензированных вакцин для человека работают подобным образом. Однако, пока не существует экспериментальных вакцин, для которых показано ингибирование микобактерий у животных; Стратегия иммунизации взрослых субъектов с латентной ТБ-инфекцией. Вакцина должна вызывать антимикобактериальный иммунный ответ у лиц, зараженных микобактериями, гарантируя контроль инфекции. Данную стратегию можно использовать для взрослого населения в странах, где ТБ является эндемичным; Естественный цикл развития туберкулеза и стадии инфекционного процесса, на которые возможно воздействие иммунного ответа, индуцированного вакциной 4) Вакцино-индуцированный иммунный ответ должен быть направлен на микобактериальные антигены, участвующие в диссеминации бактерий. Подавление диссеминации приводит к меньшему инфицированию различных органов и верхних долей легких, которые являются основным местом распространения микобактерий.
Delogu & Fadda – The Quest for a New Vaccine Against Tuberculosis 6 J Infect Developing Countries 2009; 3(1): 5-15. Номера в квадратах отражают различные стратегии, которые можно применить: Вакцина должна индуцировать сильный клеточный иммунный ответ, для которого характерно образование CD4+ и CD8+ Т-клеток, направленных против секретируемых и активно экспрессируемых в начале инфекции антигенов микобактерий. Быстрая мобилизация Т-лимфоцитов в месте инфекции, должна включать в себя бактериальную репликацию и снижение развития активного инфекционного процесса; Вакцинная стратегия, направленная на блокирование инфекции может быть основана на индукции антител, способных блокировать начальные стадии инфекции. Большинство лицензированных вакцин для человека работают подобным образом. Однако, пока не существует экспериментальных вакцин, для которых показано ингибирование микобактерий у животных; Стратегия иммунизации взрослых субъектов с латентной ТБ-инфекцией. Вакцина должна вызывать антимикобактериальный иммунный ответ у лиц, зараженных микобактериями, гарантируя контроль инфекции. Данную стратегию можно использовать для взрослого населения в странах, где ТБ является эндемичным; Естественный цикл развития туберкулеза и стадии инфекционного процесса, на которые возможно воздействие иммунного ответа, индуцированного вакциной 4) Вакцино-индуцированный иммунный ответ должен быть направлен на микобактериальные антигены, участвующие в диссеминации бактерий. Подавление диссеминации приводит к меньшему инфицированию различных органов и верхних долей легких, которые являются основным местом распространения микобактерий.

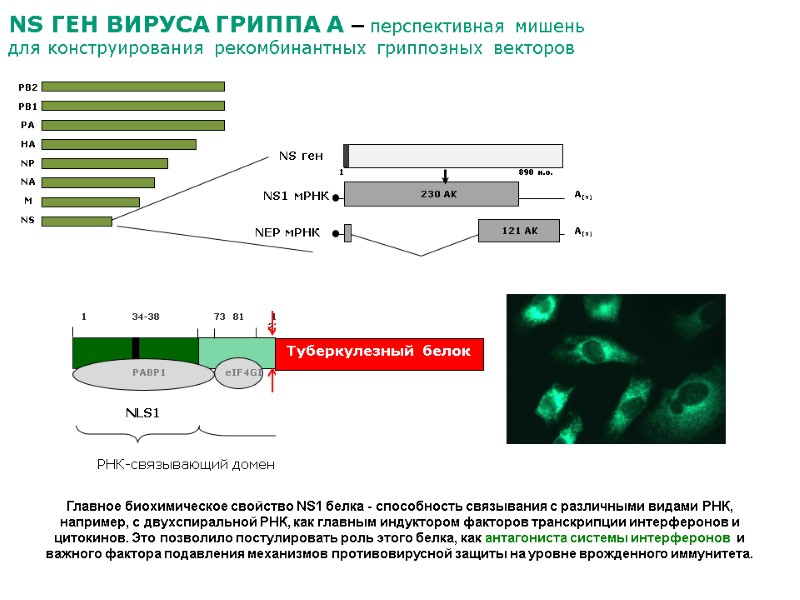
 NS ген вируса гриппа А – перспективная мишень для конструирования рекомбинантных гриппозных векторов Главное биохимическое свойство NS1 белка - способность связывания с различными видами РНК, например, с двухспиральной РНК, как главным индуктором факторов транскрипции интерферонов и цитокинов. Это позволило постулировать роль этого белка, как антагониста системы интерферонов и важного фактора подавления механизмов противовирусной защиты на уровне врожденного иммунитета. Туберкулезный белок
NS ген вируса гриппа А – перспективная мишень для конструирования рекомбинантных гриппозных векторов Главное биохимическое свойство NS1 белка - способность связывания с различными видами РНК, например, с двухспиральной РНК, как главным индуктором факторов транскрипции интерферонов и цитокинов. Это позволило постулировать роль этого белка, как антагониста системы интерферонов и важного фактора подавления механизмов противовирусной защиты на уровне врожденного иммунитета. Туберкулезный белок
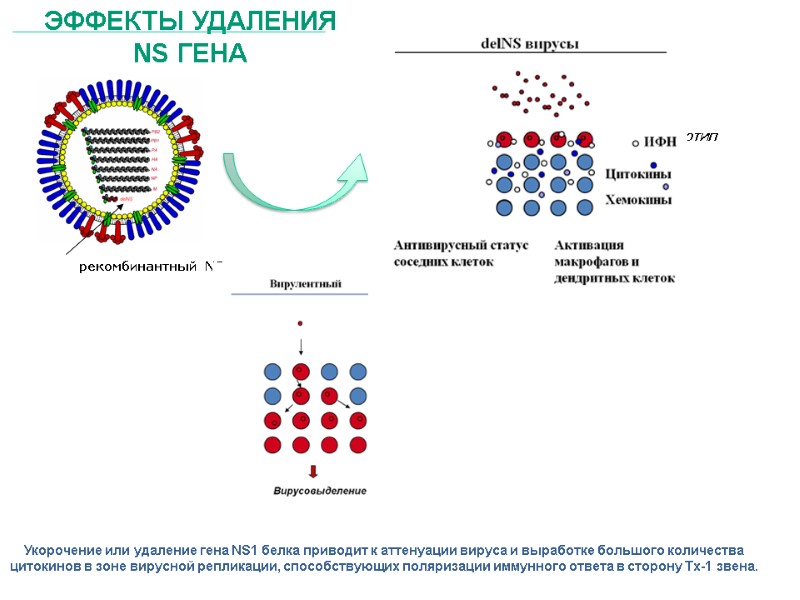
 рекомбинантный NS ген Репликативно-неполноценный фенотип Отсутствие вирусовыделения Адъювантный эффект Эффекты удаления NS гена Укорочение или удаление гена NS1 белка приводит к аттенуации вируса и выработке большого количества цитокинов в зоне вирусной репликации, способствующих поляризации иммунного ответа в сторону Тx-1 звена.
рекомбинантный NS ген Репликативно-неполноценный фенотип Отсутствие вирусовыделения Адъювантный эффект Эффекты удаления NS гена Укорочение или удаление гена NS1 белка приводит к аттенуации вируса и выработке большого количества цитокинов в зоне вирусной репликации, способствующих поляризации иммунного ответа в сторону Тx-1 звена.

 BiaCore T-200 высочайшая чувствительность отсутствие метки количественная характеристика взаимодействия возможность определить механизм взаимодействия
BiaCore T-200 высочайшая чувствительность отсутствие метки количественная характеристика взаимодействия возможность определить механизм взаимодействия
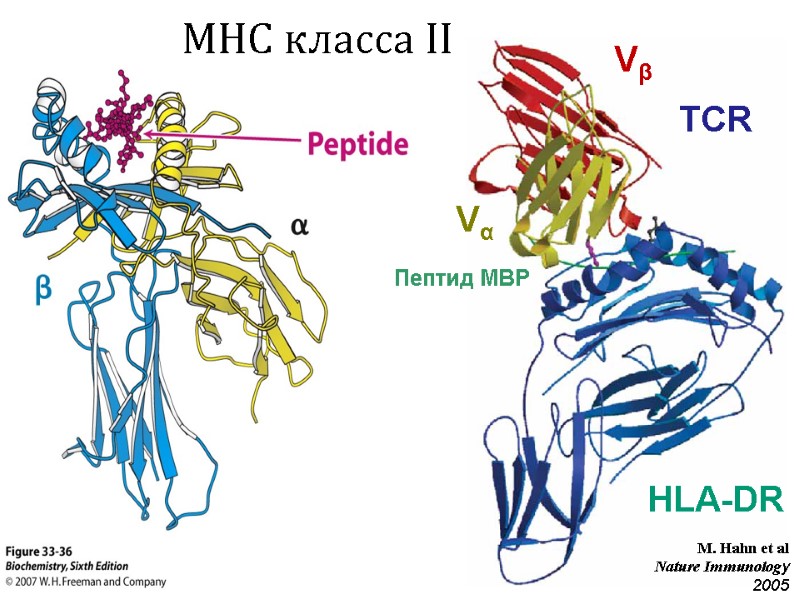
 MHC класса II M. Hahn et al Nature Immunology 2005
MHC класса II M. Hahn et al Nature Immunology 2005
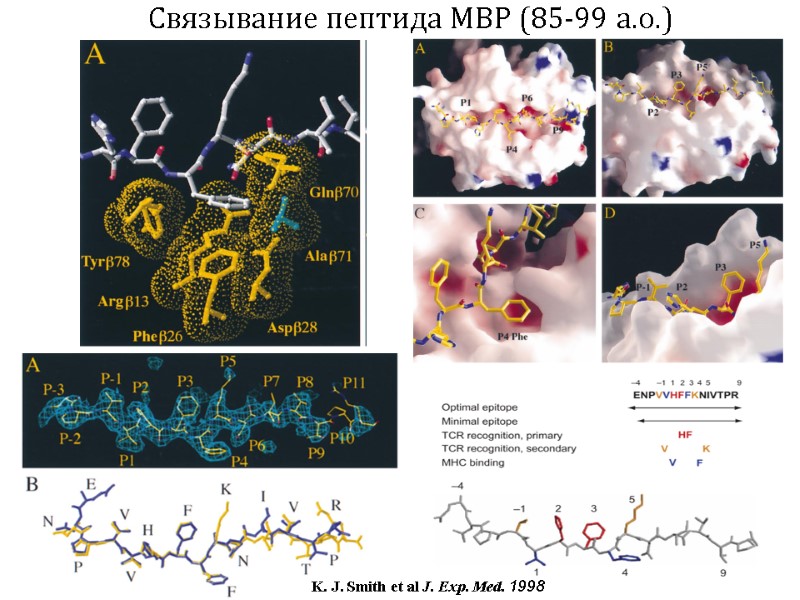
 Связывание пептида MBP (85-99 а.о.) K. J. Smith et al J. Exp. Med. 1998
Связывание пептида MBP (85-99 а.о.) K. J. Smith et al J. Exp. Med. 1998
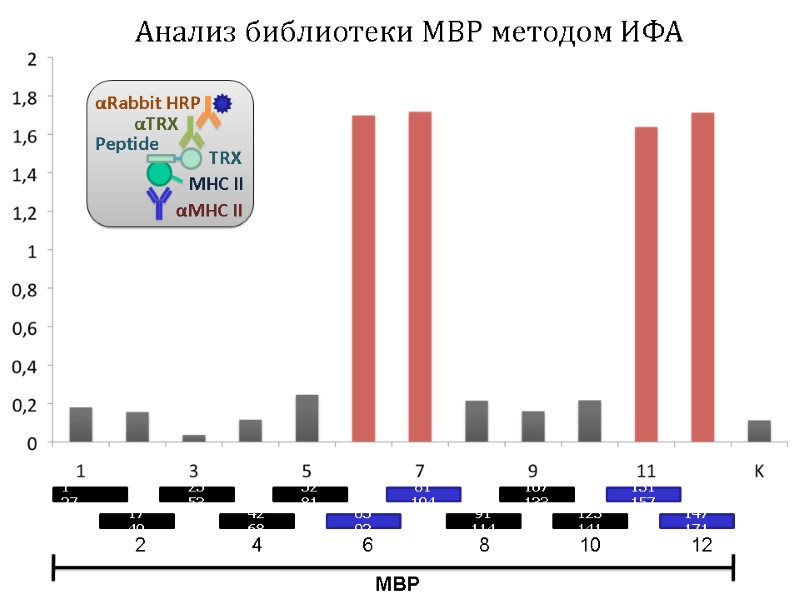
 1 27 17 40 25 53 42 68 52 81 65 92 81 104 91 114 107 133 123 141 131 157 147 171 2 4 6 8 10 12 MBP Анализ библиотеки MBP методом ИФА
1 27 17 40 25 53 42 68 52 81 65 92 81 104 91 114 107 133 123 141 131 157 147 171 2 4 6 8 10 12 MBP Анализ библиотеки MBP методом ИФА
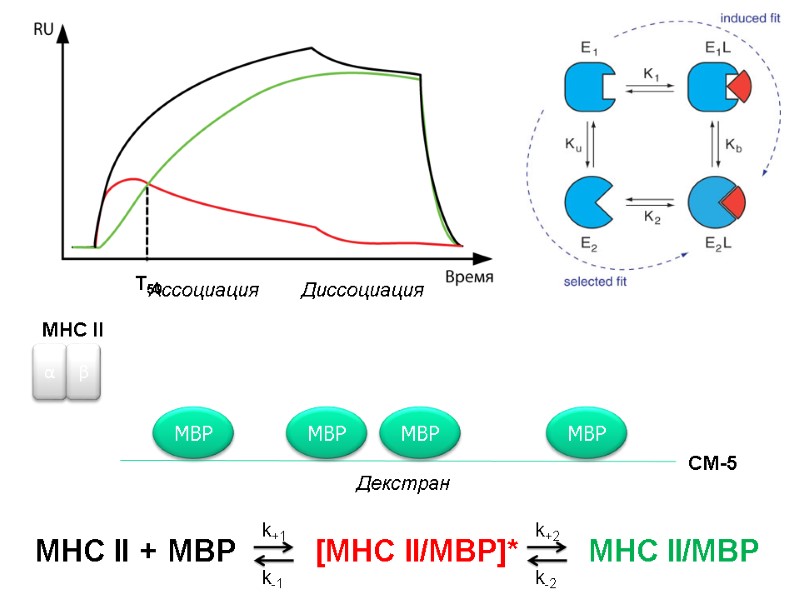
 MBP Декстран CM-5 MBP MBP MBP Ассоциация Диссоциация T50
MBP Декстран CM-5 MBP MBP MBP Ассоциация Диссоциация T50
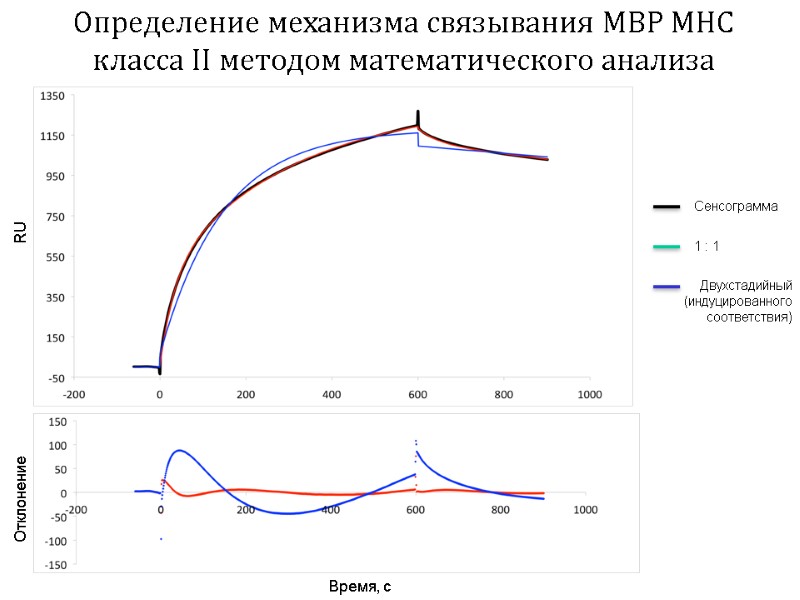
 Определение механизма связывания MBP MHC класса II методом математического анализа Сенсограмма 1 : 1 Двухстадийный (индуцированного соответствия) Время, с RU Отклонение
Определение механизма связывания MBP MHC класса II методом математического анализа Сенсограмма 1 : 1 Двухстадийный (индуцированного соответствия) Время, с RU Отклонение
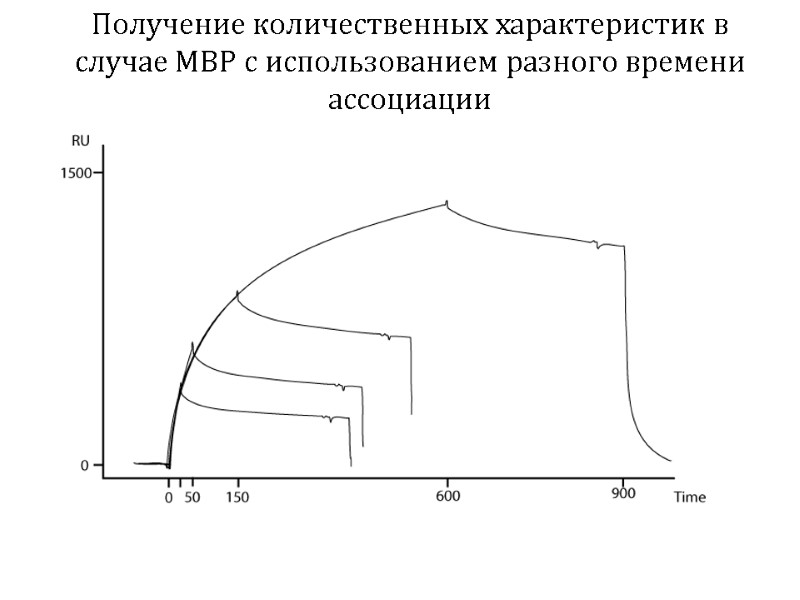
 Получение количественных характеристик в случае MBP с использованием разного времени ассоциации
Получение количественных характеристик в случае MBP с использованием разного времени ассоциации
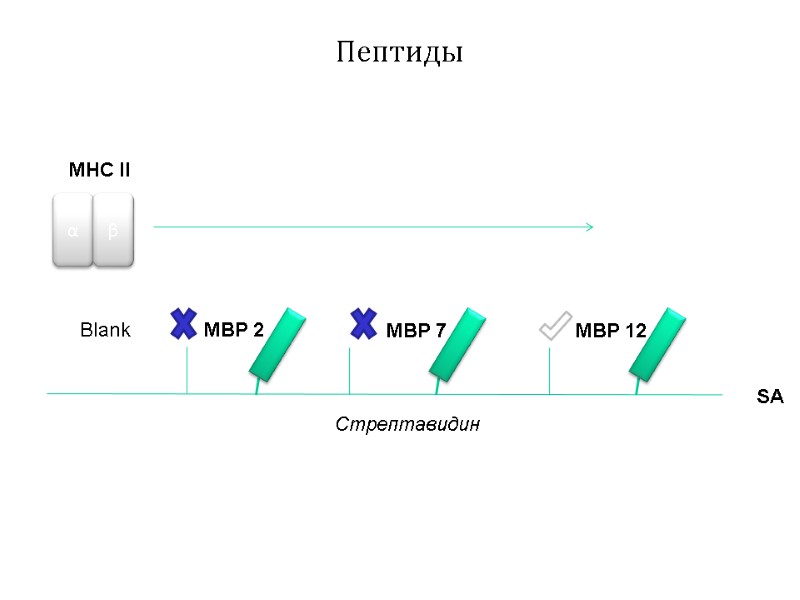
 Пептиды Стрептавидин MBP 2 MBP 7 MBP 12 SA Blank
Пептиды Стрептавидин MBP 2 MBP 7 MBP 12 SA Blank
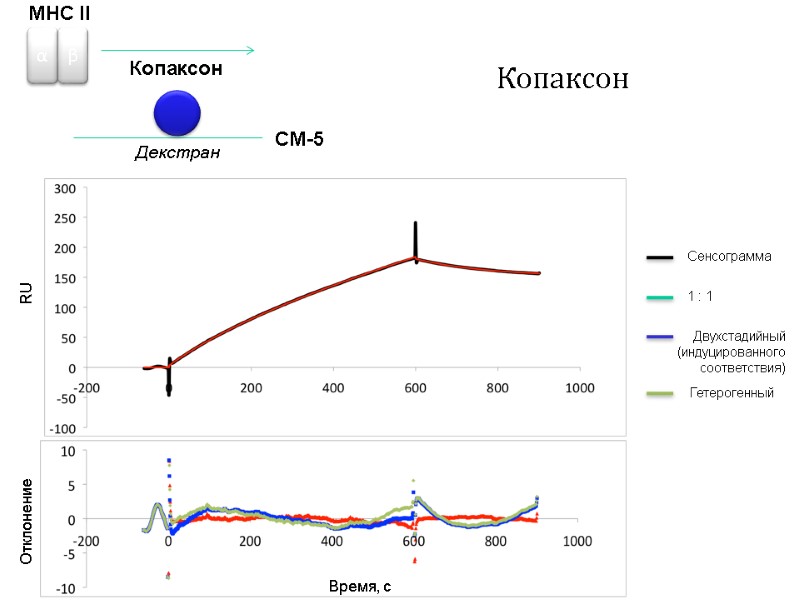
 Копаксон Сенсограмма 1 : 1 Двухстадийный (индуцированного соответствия) Гетерогенный Время, с RU Отклонение
Копаксон Сенсограмма 1 : 1 Двухстадийный (индуцированного соответствия) Гетерогенный Время, с RU Отклонение
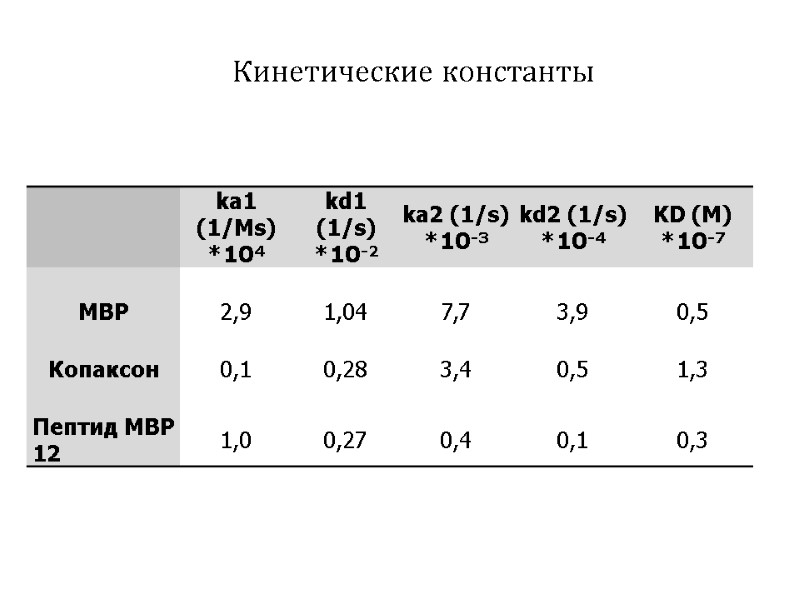
 Кинетические константы
Кинетические константы
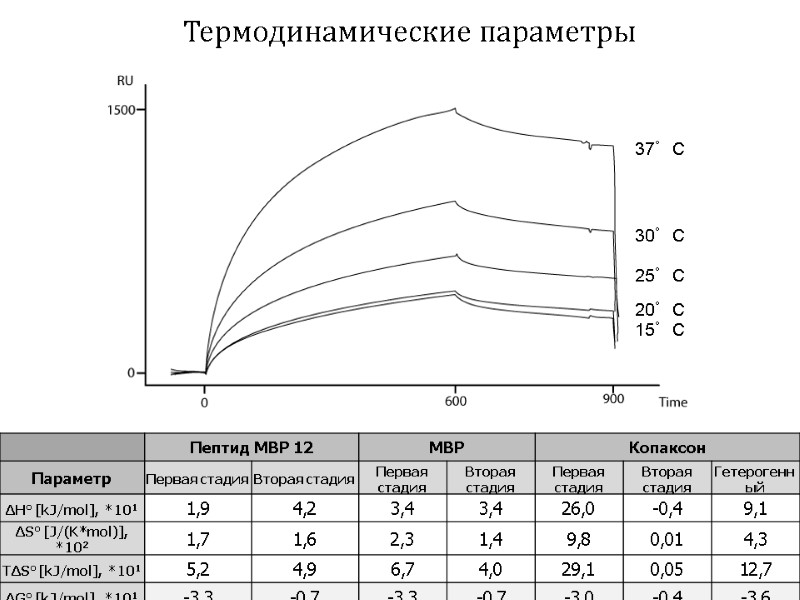
 Термодинамические параметры 37°С 30°С 25°С 20°С 15°С
Термодинамические параметры 37°С 30°С 25°С 20°С 15°С
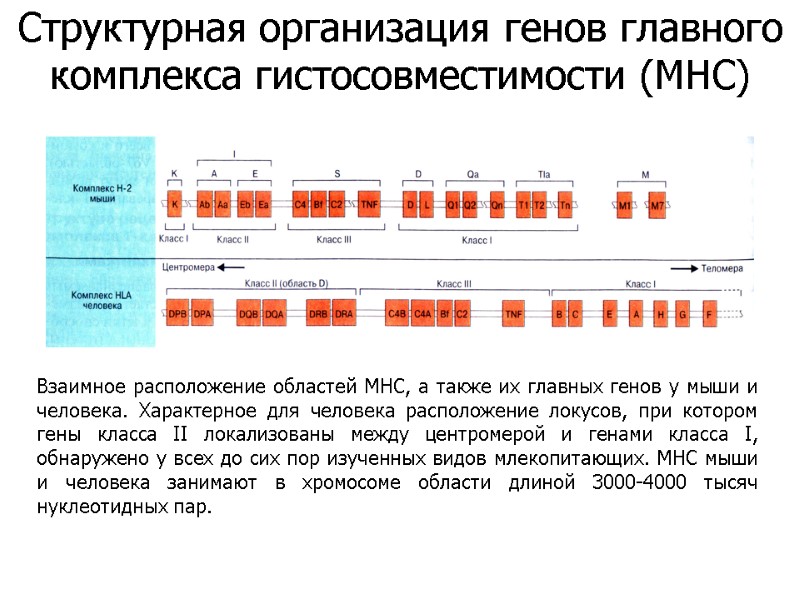
 Взаимное расположение областей МНС, а также их главных генов у мыши и человека. Характерное для человека расположение локусов, при котором гены класса II локализованы между центромерой и генами класса I, обнаружено у всех до сих пор изученных видов млекопитающих. МНС мыши и человека занимают в хромосоме области длиной 3000-4000 тысяч нуклеотидных пар. Структурная организация генов главного комплекса гистосовместимости (MHC)
Взаимное расположение областей МНС, а также их главных генов у мыши и человека. Характерное для человека расположение локусов, при котором гены класса II локализованы между центромерой и генами класса I, обнаружено у всех до сих пор изученных видов млекопитающих. МНС мыши и человека занимают в хромосоме области длиной 3000-4000 тысяч нуклеотидных пар. Структурная организация генов главного комплекса гистосовместимости (MHC)
 В хромосоме человека гены класса I расположены ближе к теломере, чем гены классов II и III. В дополнение к генам классических трансплантационных антигенов (HLA-A, HLA-B и HLA-C) в этом участке идентифицировано несколько «класс l-подобных» генов, вероятно, эквивалентных мышиным генам соответствующих областей. Здесь же содержится ряд других генов, отличных от генов класса I. HLA-гены класса I у человека
В хромосоме человека гены класса I расположены ближе к теломере, чем гены классов II и III. В дополнение к генам классических трансплантационных антигенов (HLA-A, HLA-B и HLA-C) в этом участке идентифицировано несколько «класс l-подобных» генов, вероятно, эквивалентных мышиным генам соответствующих областей. Здесь же содержится ряд других генов, отличных от генов класса I. HLA-гены класса I у человека
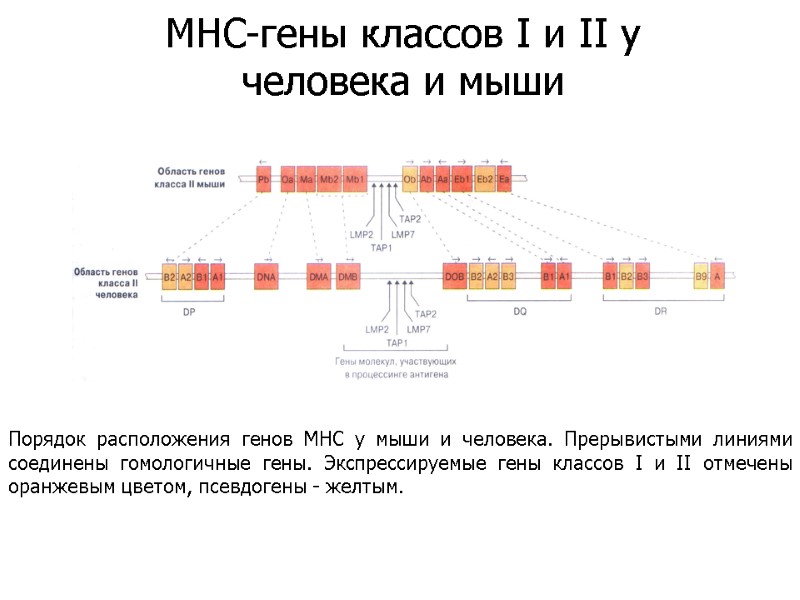
 Порядок расположения генов МНС у мыши и человека. Прерывистыми линиями соединены гомологичные гены. Экспрессируемые гены классов I и II отмечены оранжевым цветом, псевдогены - желтым. MHC-гены классов I и II у человека и мыши
Порядок расположения генов МНС у мыши и человека. Прерывистыми линиями соединены гомологичные гены. Экспрессируемые гены классов I и II отмечены оранжевым цветом, псевдогены - желтым. MHC-гены классов I и II у человека и мыши
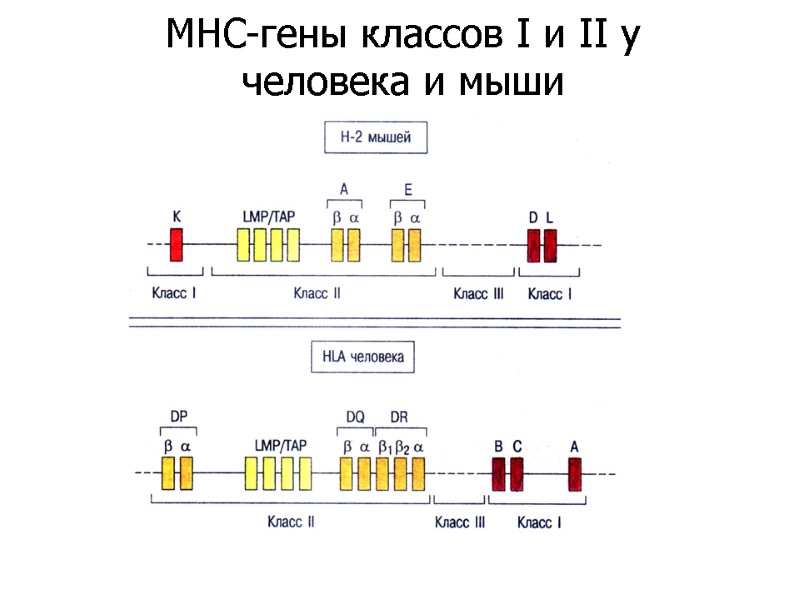
 MHC-гены классов I и II у человека и мыши
MHC-гены классов I и II у человека и мыши
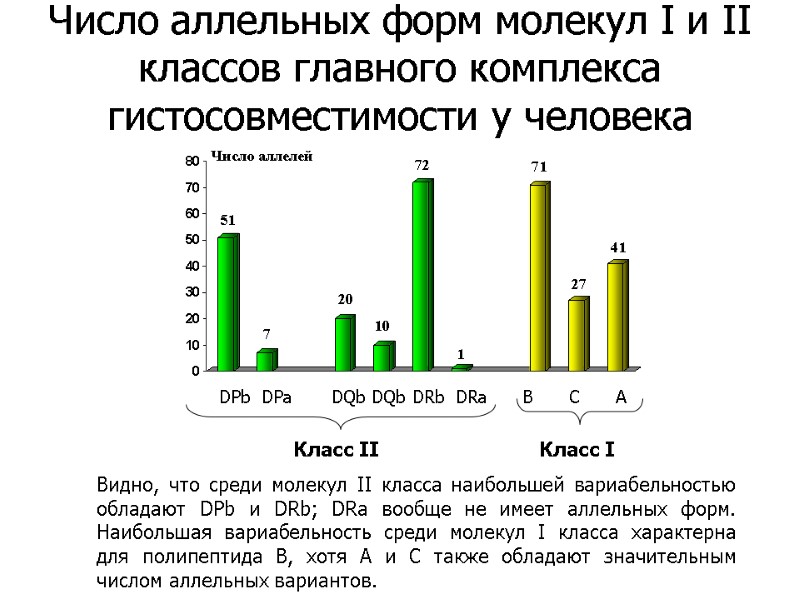
 Видно, что среди молекул II класса наибольшей вариабельностью обладают DPb и DRb; DRa вообще не имеет аллельных форм. Наибольшая вариабельность среди молекул I класса характерна для полипептида В, хотя А и С также обладают значительным числом аллельных вариантов. DPb DPa DQb DQb DRb DRa B С A Класс II Класс I Число аллельных форм молекул I и II классов главного комплекса гистосовместимости у человека
Видно, что среди молекул II класса наибольшей вариабельностью обладают DPb и DRb; DRa вообще не имеет аллельных форм. Наибольшая вариабельность среди молекул I класса характерна для полипептида В, хотя А и С также обладают значительным числом аллельных вариантов. DPb DPa DQb DQb DRb DRa B С A Класс II Класс I Число аллельных форм молекул I и II классов главного комплекса гистосовместимости у человека
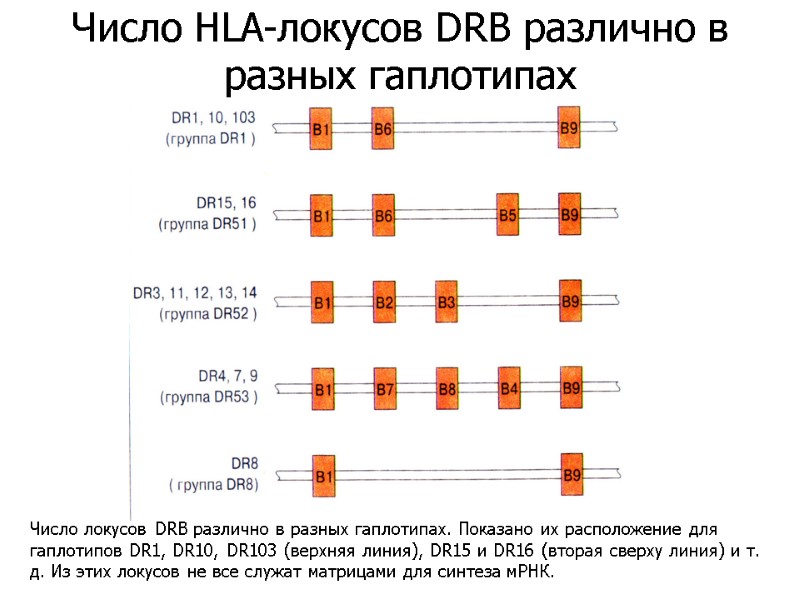
 Число локусов DRB различно в разных гаплотипах. Показано их расположение для гаплотипов DR1, DR10, DR103 (верхняя линия), DR15 и DR16 (вторая сверху линия) и т. д. Из этих локусов не все служат матрицами для синтеза мРНК. Число HLA-локусов DRB различно в разных гаплотипах
Число локусов DRB различно в разных гаплотипах. Показано их расположение для гаплотипов DR1, DR10, DR103 (верхняя линия), DR15 и DR16 (вторая сверху линия) и т. д. Из этих локусов не все служат матрицами для синтеза мРНК. Число HLA-локусов DRB различно в разных гаплотипах
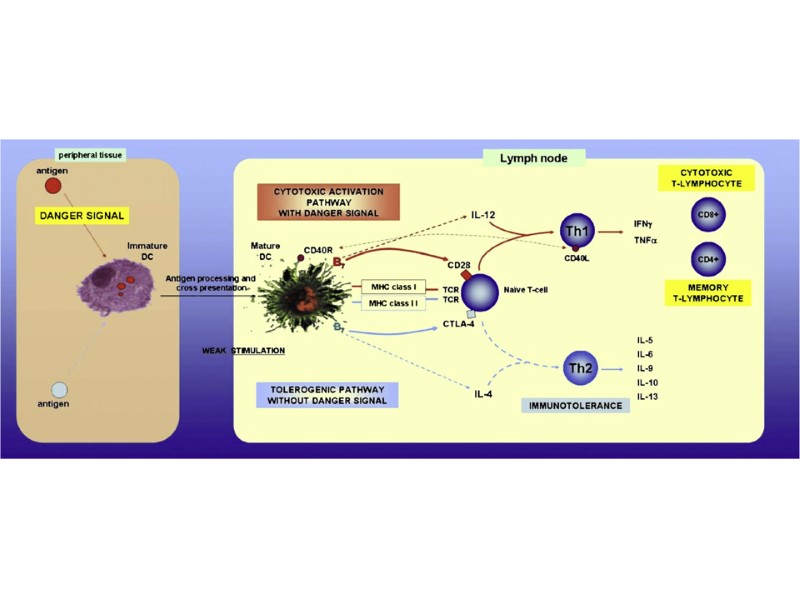
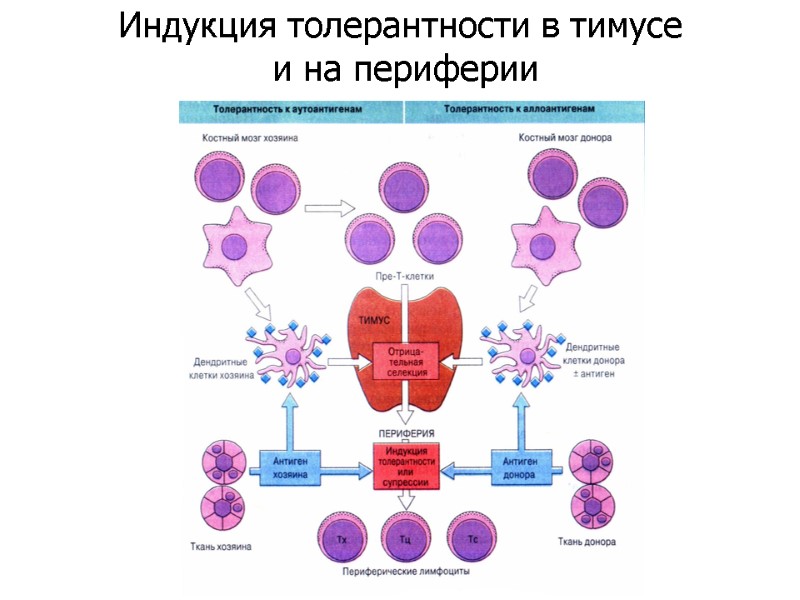
 Индукция толерантности в тимусе и на периферии
Индукция толерантности в тимусе и на периферии
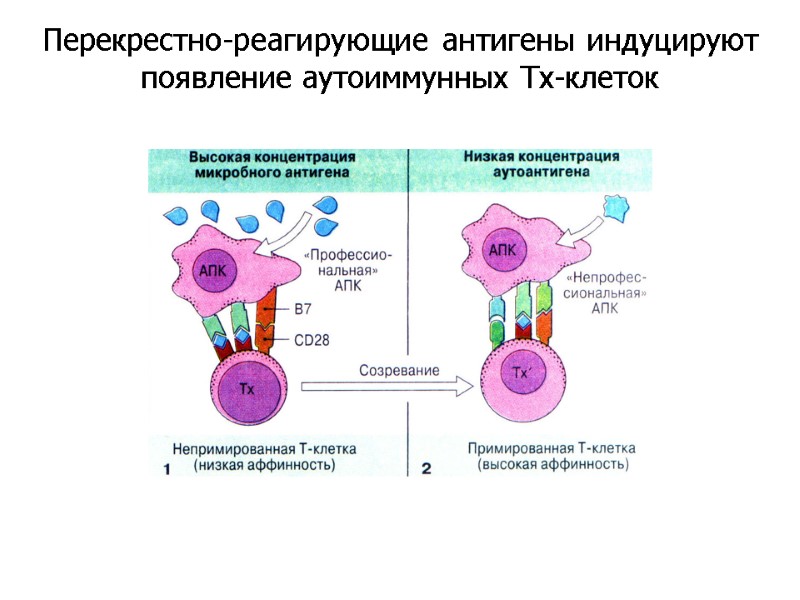
 Перекрестно-реагирующие антигены индуцируют появление аутоиммунных Тх-клеток
Перекрестно-реагирующие антигены индуцируют появление аутоиммунных Тх-клеток
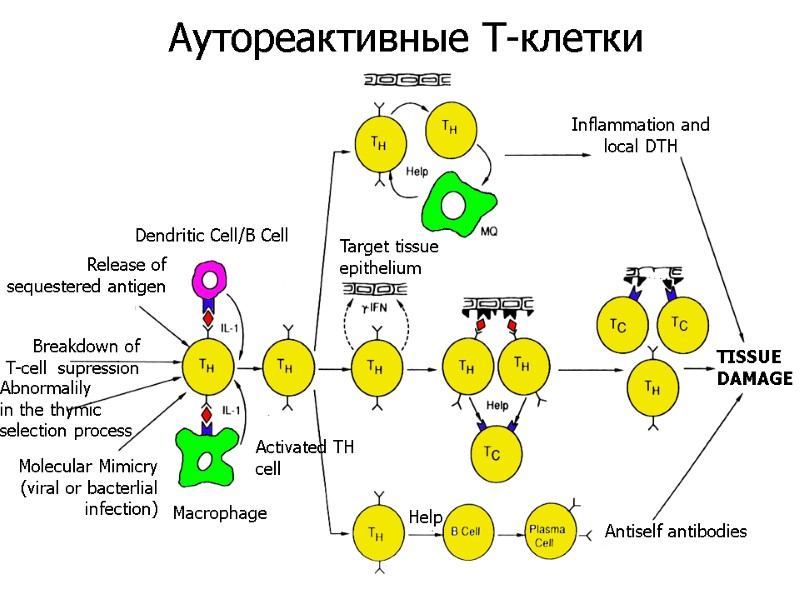
 b Molecular Mimicry (viral or bacterlial infection) Dendritic Cell/B Cell Release of sequestered antigen Breakdown of T-cell supression Abnormalily in the thymic selection process Macrophage Activated TH cell Target tissue epithelium Antiself antibodies Help Inflammation and local DTH TISSUE DAMAGE Аутореактивные Т-клетки
b Molecular Mimicry (viral or bacterlial infection) Dendritic Cell/B Cell Release of sequestered antigen Breakdown of T-cell supression Abnormalily in the thymic selection process Macrophage Activated TH cell Target tissue epithelium Antiself antibodies Help Inflammation and local DTH TISSUE DAMAGE Аутореактивные Т-клетки
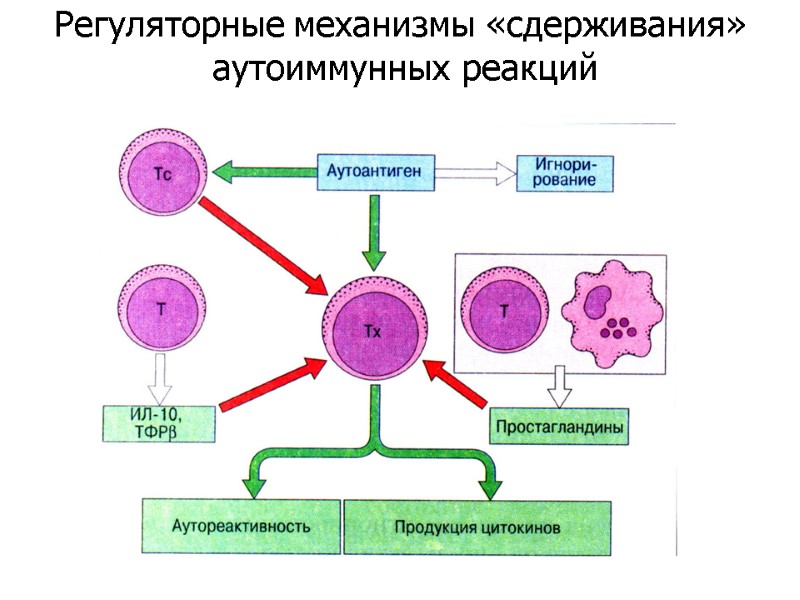
 Регуляторные механизмы «сдерживания» аутоиммунных реакций
Регуляторные механизмы «сдерживания» аутоиммунных реакций
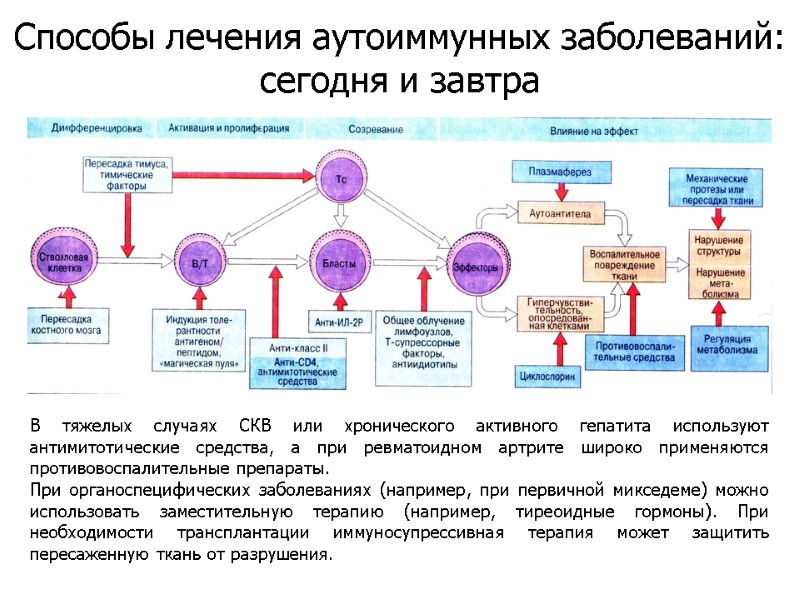
 В тяжелых случаях СКВ или хронического активного гепатита используют антимитотические средства, а при ревматоидном артрите широко применяются противовоспалительные препараты. При органоспецифических заболеваниях (например, при первичной микседеме) можно использовать заместительную терапию (например, тиреоидные гормоны). При необходимости трансплантации иммуносупрессивная терапия может защитить пересаженную ткань от разрушения. Способы лечения аутоиммунных заболеваний: сегодня и завтра
В тяжелых случаях СКВ или хронического активного гепатита используют антимитотические средства, а при ревматоидном артрите широко применяются противовоспалительные препараты. При органоспецифических заболеваниях (например, при первичной микседеме) можно использовать заместительную терапию (например, тиреоидные гормоны). При необходимости трансплантации иммуносупрессивная терапия может защитить пересаженную ткань от разрушения. Способы лечения аутоиммунных заболеваний: сегодня и завтра
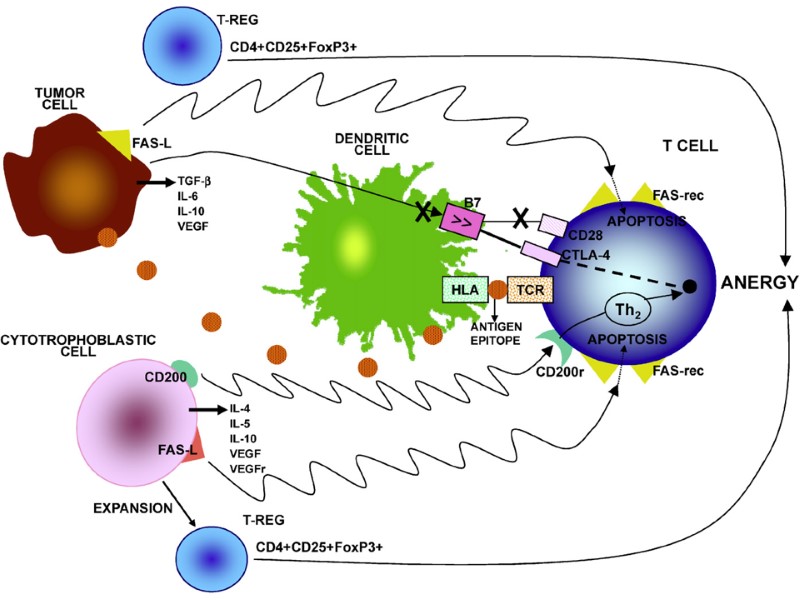
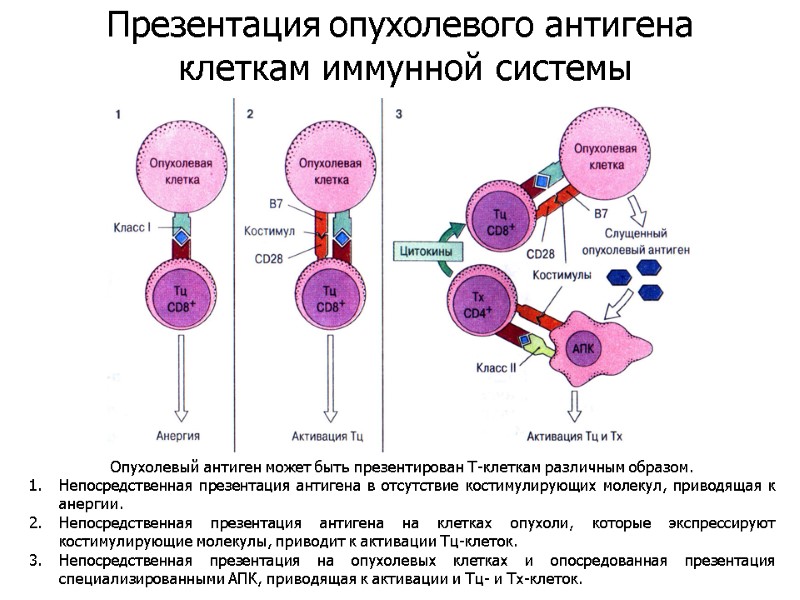
 Опухолевый антиген может быть презентирован Т-клеткам различным образом. Непосредственная презентация антигена в отсутствие костимулирующих молекул, приводящая к анергии. Непосредственная презентация антигена на клетках опухоли, которые экспрессируют костимулирующие молекулы, приводит к активации Тц-клеток. Непосредственная презентация на опухолевых клетках и опосредованная презентация специализированными АПК, приводящая к активации и Тц- и Тх-клеток. Презентация опухолевого антигена клеткам иммунной системы
Опухолевый антиген может быть презентирован Т-клеткам различным образом. Непосредственная презентация антигена в отсутствие костимулирующих молекул, приводящая к анергии. Непосредственная презентация антигена на клетках опухоли, которые экспрессируют костимулирующие молекулы, приводит к активации Тц-клеток. Непосредственная презентация на опухолевых клетках и опосредованная презентация специализированными АПК, приводящая к активации и Тц- и Тх-клеток. Презентация опухолевого антигена клеткам иммунной системы
 В-клеточный иммунный ответ Габибов А.Г. Лекция 4
В-клеточный иммунный ответ Габибов А.Г. Лекция 4
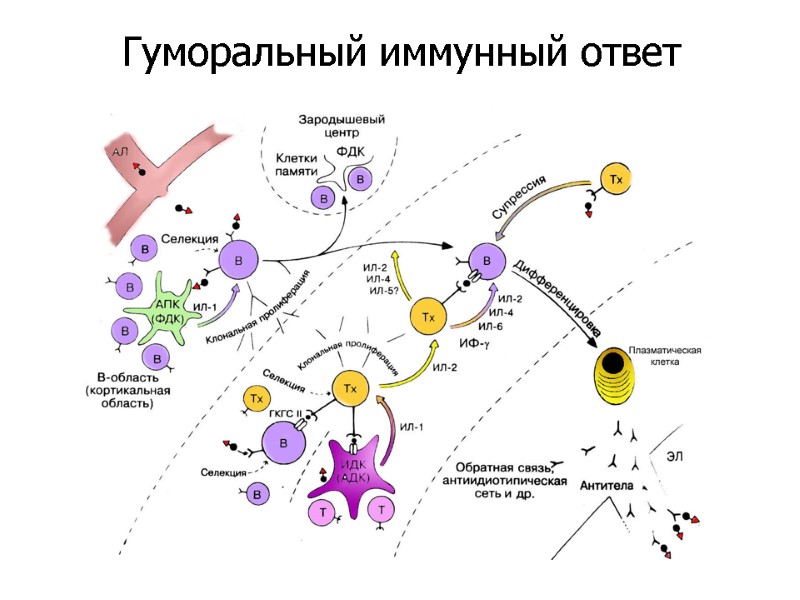
 Гуморальный иммунный ответ
Гуморальный иммунный ответ
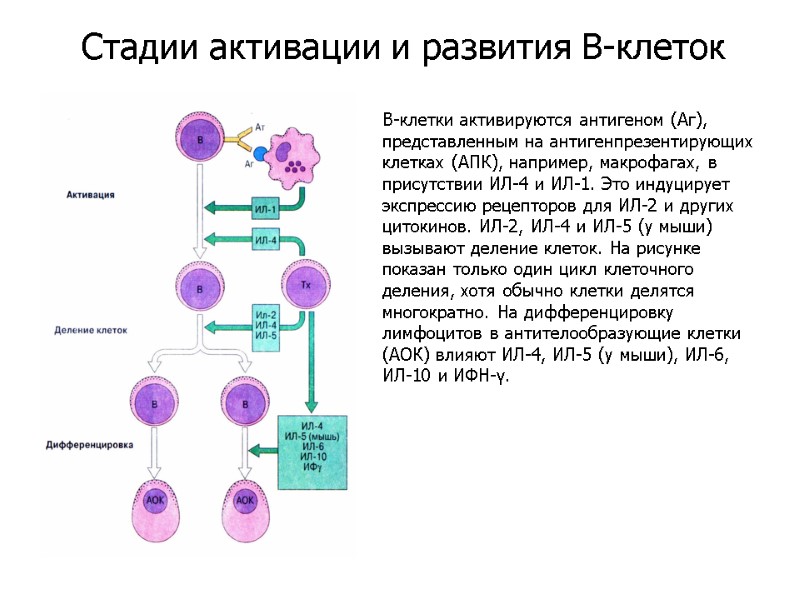
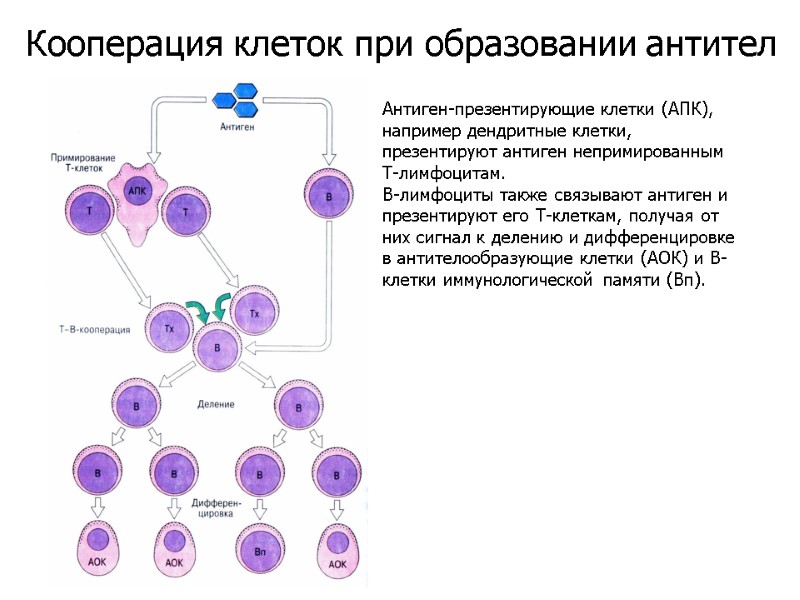
 В-клетки активируются антигеном (Аг), представленным на антигенпрезентирующих клетках (АПК), например, макрофагах, в присутствии ИЛ-4 и ИЛ-1. Это индуцирует экспрессию рецепторов для ИЛ-2 и других цитокинов. ИЛ-2, ИЛ-4 и ИЛ-5 (у мыши) вызывают деление клеток. На рисунке показан только один цикл клеточного деления, хотя обычно клетки делятся многократно. На дифференцировку лимфоцитов в антителообразующие клетки (АОК) влияют ИЛ-4, ИЛ-5 (у мыши), ИЛ-6, ИЛ-10 и ИФН-γ. Стадии активации и развития В-клеток
В-клетки активируются антигеном (Аг), представленным на антигенпрезентирующих клетках (АПК), например, макрофагах, в присутствии ИЛ-4 и ИЛ-1. Это индуцирует экспрессию рецепторов для ИЛ-2 и других цитокинов. ИЛ-2, ИЛ-4 и ИЛ-5 (у мыши) вызывают деление клеток. На рисунке показан только один цикл клеточного деления, хотя обычно клетки делятся многократно. На дифференцировку лимфоцитов в антителообразующие клетки (АОК) влияют ИЛ-4, ИЛ-5 (у мыши), ИЛ-6, ИЛ-10 и ИФН-γ. Стадии активации и развития В-клеток

 Антиген-презентирующие клетки (АПК), например дендритные клетки, презентируют антиген непримированным Т-лимфоцитам. В-лимфоциты также связывают антиген и презентируют его Т-клеткам, получая от них сигнал к делению и дифференцировке в антителообразующие клетки (АОК) и В-клетки иммунологической памяти (Вп). Кооперация клеток при образовании антител
Антиген-презентирующие клетки (АПК), например дендритные клетки, презентируют антиген непримированным Т-лимфоцитам. В-лимфоциты также связывают антиген и презентируют его Т-клеткам, получая от них сигнал к делению и дифференцировке в антителообразующие клетки (АОК) и В-клетки иммунологической памяти (Вп). Кооперация клеток при образовании антител
 Биологическое значение синтеза иммуноглобулинов разных классов IgD Первичное распознавание свободного АГ, участие в активации В-лимфоцитов, участие в презентации АГ Т-лимфоцитам mIgМ Первичное распознавание свободного АГ, участие в регуляции пула зрелых В-клеток, модулирующая роль в активации В-лим- фоцитов, участие в презентации АГ Т-лимфоцитам IgМ Нейтрализация инфекционных свойств патогенов; элиминация антигена в корпускулярной форме из кровотока с участием комплемента; элиминация антигена путем его присоединения к поверхности эритроцитов с последующим фагоцитозом; регу- ляция процессов дифференцировки Т-лимфоцитов и ЕК IgG1-3 Элиминация антигена из кровотока, ЦНС: в молекулярной фор- форме – с участием фагоцитов, в корпускулярной форме - с участием комплемента; нейтрализация инфекционных свойств патогенов, включая вирусы; обеспечение плацентарного имму- нитета; реализация антителозависимой цитотоксичности IgА Формирование барьера на поверхности слизистых оболочек для проникновения антигенов во внутренние среды организма, нейтрализация инфекционных свойств патогенов, в т.ч.вирусов IgE,G4 Формирование тканевого барьера для распространения антиге- нов по организму, нейтрализация инфекционных свойств пато- генов, в т.ч.гельминтов и вирусов; развитие воспаления и шока
Биологическое значение синтеза иммуноглобулинов разных классов IgD Первичное распознавание свободного АГ, участие в активации В-лимфоцитов, участие в презентации АГ Т-лимфоцитам mIgМ Первичное распознавание свободного АГ, участие в регуляции пула зрелых В-клеток, модулирующая роль в активации В-лим- фоцитов, участие в презентации АГ Т-лимфоцитам IgМ Нейтрализация инфекционных свойств патогенов; элиминация антигена в корпускулярной форме из кровотока с участием комплемента; элиминация антигена путем его присоединения к поверхности эритроцитов с последующим фагоцитозом; регу- ляция процессов дифференцировки Т-лимфоцитов и ЕК IgG1-3 Элиминация антигена из кровотока, ЦНС: в молекулярной фор- форме – с участием фагоцитов, в корпускулярной форме - с участием комплемента; нейтрализация инфекционных свойств патогенов, включая вирусы; обеспечение плацентарного имму- нитета; реализация антителозависимой цитотоксичности IgА Формирование барьера на поверхности слизистых оболочек для проникновения антигенов во внутренние среды организма, нейтрализация инфекционных свойств патогенов, в т.ч.вирусов IgE,G4 Формирование тканевого барьера для распространения антиге- нов по организму, нейтрализация инфекционных свойств пато- генов, в т.ч.гельминтов и вирусов; развитие воспаления и шока
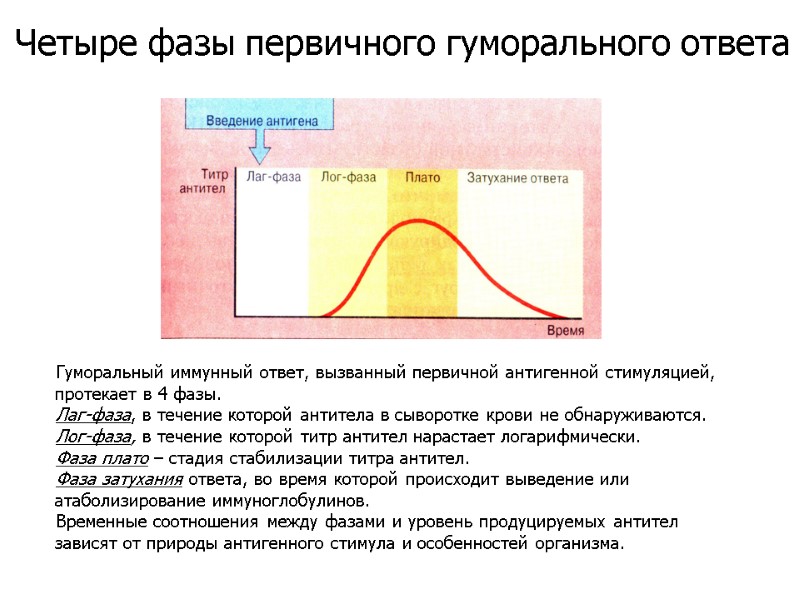
 Гуморальный иммунный ответ, вызванный первичной антигенной стимуляцией, протекает в 4 фазы. Лаг-фаза, в течение которой антитела в сыворотке крови не обнаруживаются. Лог-фаза, в течение которой титр антител нарастает логарифмически. Фаза плато – стадия стабилизации титра антител. Фаза затухания ответа, во время которой происходит выведение или атаболизирование иммуноглобулинов. Временные соотношения между фазами и уровень продуцируемых антител зависят от природы антигенного стимула и особенностей организма. Четыре фазы первичного гуморального ответа
Гуморальный иммунный ответ, вызванный первичной антигенной стимуляцией, протекает в 4 фазы. Лаг-фаза, в течение которой антитела в сыворотке крови не обнаруживаются. Лог-фаза, в течение которой титр антител нарастает логарифмически. Фаза плато – стадия стабилизации титра антител. Фаза затухания ответа, во время которой происходит выведение или атаболизирование иммуноглобулинов. Временные соотношения между фазами и уровень продуцируемых антител зависят от природы антигенного стимула и особенностей организма. Четыре фазы первичного гуморального ответа
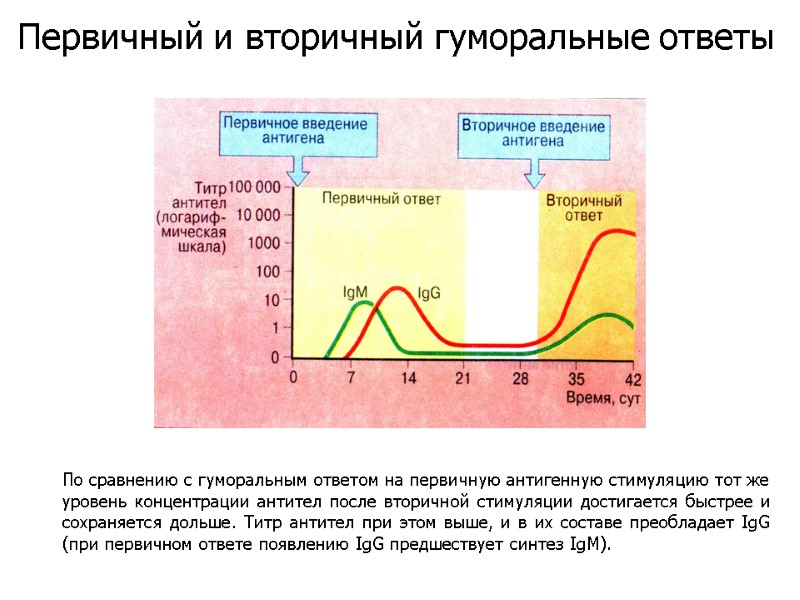
 По сравнению с гуморальным ответом на первичную антигенную стимуляцию тот же уровень концентрации антител после вторичной стимуляции достигается быстрее и сохраняется дольше. Титр антител при этом выше, и в их составе преобладает IgG (при первичном ответе появлению IgG предшествует синтез IgM). Первичный и вторичный гуморальные ответы
По сравнению с гуморальным ответом на первичную антигенную стимуляцию тот же уровень концентрации антител после вторичной стимуляции достигается быстрее и сохраняется дольше. Титр антител при этом выше, и в их составе преобладает IgG (при первичном ответе появлению IgG предшествует синтез IgM). Первичный и вторичный гуморальные ответы
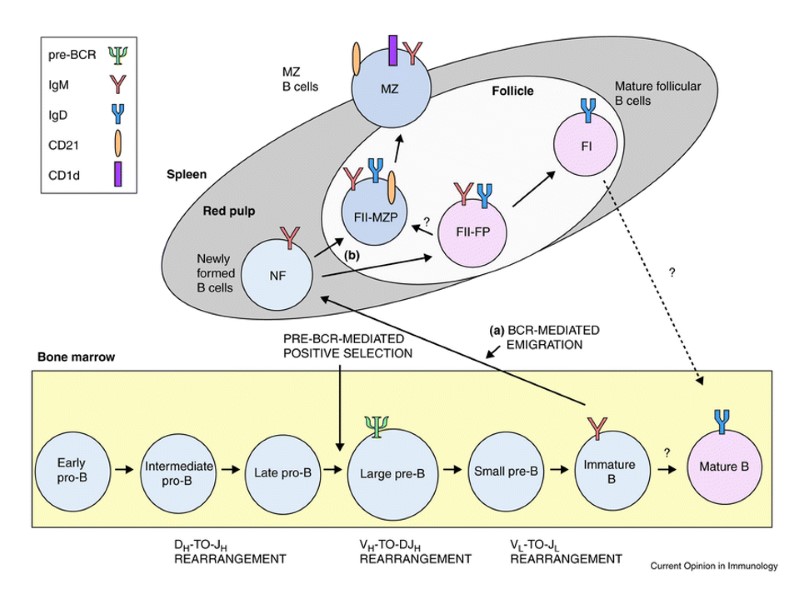
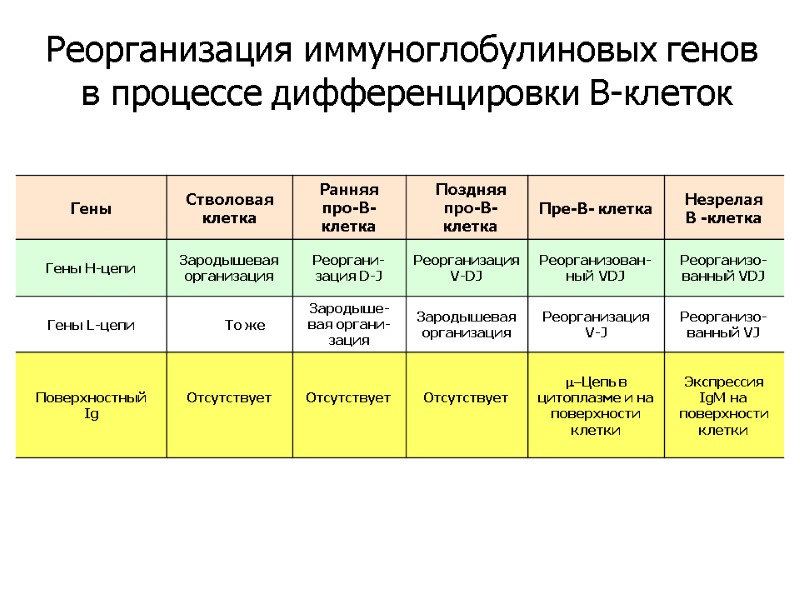
 Реорганизация иммуноглобулиновых генов в процессе дифференцировки В-клеток
Реорганизация иммуноглобулиновых генов в процессе дифференцировки В-клеток
 Первичная иммунизация вызывает образование антител преимущественно IgM- изотипа; повторное введение антигена стимулирует образование антител в основном IgG-изотипа. Механизм переключения (switch-over) изотипа схематично представлен справа. При первичном ответе рекомбинировавший участок V-D-J считывается одновременно с Сμ-сегментом гена. После удаления интронов при процессинге первичного РНК-транскрипта образуется мРНК для секретируемой формы IgM. В процессе «созревания» иммунного ответа происходит переключающая изотип рекомбинация между участком γ3 и расположенным ниже С-геном (в данном случае - Сγ3). Разделяющий их участок ДНК образует петлю, а затем вырезается. В результате происходит утрата генов Сμ и Сδ, а два участка переключения соединяются. «Созревание» (maturation) иммунного ответа и переключение (switch-over) изотипа
Первичная иммунизация вызывает образование антител преимущественно IgM- изотипа; повторное введение антигена стимулирует образование антител в основном IgG-изотипа. Механизм переключения (switch-over) изотипа схематично представлен справа. При первичном ответе рекомбинировавший участок V-D-J считывается одновременно с Сμ-сегментом гена. После удаления интронов при процессинге первичного РНК-транскрипта образуется мРНК для секретируемой формы IgM. В процессе «созревания» иммунного ответа происходит переключающая изотип рекомбинация между участком γ3 и расположенным ниже С-геном (в данном случае - Сγ3). Разделяющий их участок ДНК образует петлю, а затем вырезается. В результате происходит утрата генов Сμ и Сδ, а два участка переключения соединяются. «Созревание» (maturation) иммунного ответа и переключение (switch-over) изотипа
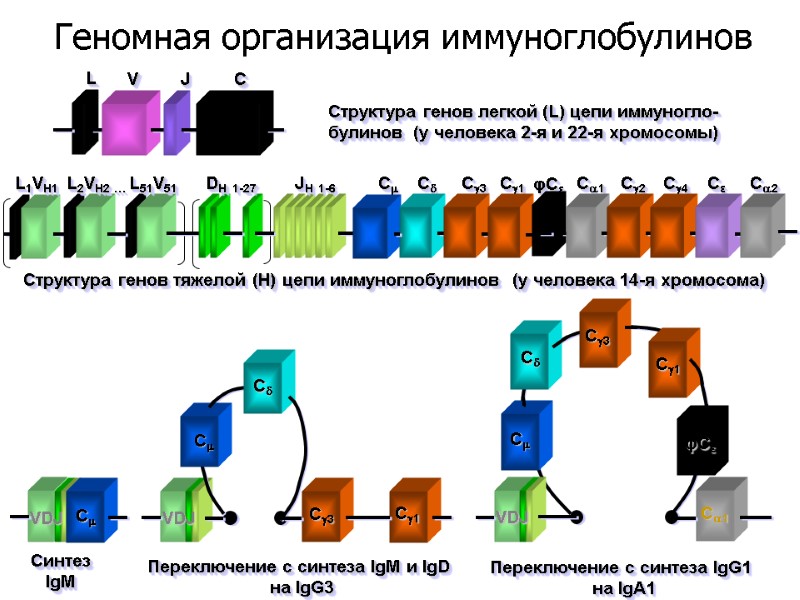
 Структура генов легкой (L) цепи иммуногло- булинов (у человека 2-я и 22-я хромосомы) Структура генов тяжелой (Н) цепи иммуноглобулинов (у человека 14-я хромосома) L JH 1-6 C C C3 C1 φCε C1 C2 C4 Cε C2 C C VDJ C3 C1 VDJ C VDJ C C C3 C1 φCε C1 Cинтез IgM Переключение с синтеза IgM и IgD на IgG3 Переключение с синтеза IgG1 на IgA1 V J C L1VH1 L2VH2 … L51V51 DH 1-27 Геномная организация иммуноглобулинов
Структура генов легкой (L) цепи иммуногло- булинов (у человека 2-я и 22-я хромосомы) Структура генов тяжелой (Н) цепи иммуноглобулинов (у человека 14-я хромосома) L JH 1-6 C C C3 C1 φCε C1 C2 C4 Cε C2 C C VDJ C3 C1 VDJ C VDJ C C C3 C1 φCε C1 Cинтез IgM Переключение с синтеза IgM и IgD на IgG3 Переключение с синтеза IgG1 на IgA1 V J C L1VH1 L2VH2 … L51V51 DH 1-27 Геномная организация иммуноглобулинов
 Рекомбинация генов, кодирующих k-цепи иммуноглобулинов В некоммитированной В-клетке гены, кодирующие k-цепь иммуноглобу-линов, отделены в ДНК значительным расстоянием. Процесс рекомбинации начинается с объединения одного из Vk-генов (Vk2) с одним из J-мини-генов (J4). В результате формируется k-локус, контролирующий незрелую пре-мРНК ядра. При созревании такой РНК происходит слияние (сплайсинг) VJ с Сk-геном за счет делеции некодируемой последовательности нуклеотидов. Зрелая мРНК представляет собой единый информационный участок (LVk2J4Ck), транслирующий первичную к-цепь. При созревании k-цепи лидерная последовательность аминокислотных остатков (L) удаляется, что и приводит, наконец, к формированию полноценной k-цепи
Рекомбинация генов, кодирующих k-цепи иммуноглобулинов В некоммитированной В-клетке гены, кодирующие k-цепь иммуноглобу-линов, отделены в ДНК значительным расстоянием. Процесс рекомбинации начинается с объединения одного из Vk-генов (Vk2) с одним из J-мини-генов (J4). В результате формируется k-локус, контролирующий незрелую пре-мРНК ядра. При созревании такой РНК происходит слияние (сплайсинг) VJ с Сk-геном за счет делеции некодируемой последовательности нуклеотидов. Зрелая мРНК представляет собой единый информационный участок (LVk2J4Ck), транслирующий первичную к-цепь. При созревании k-цепи лидерная последовательность аминокислотных остатков (L) удаляется, что и приводит, наконец, к формированию полноценной k-цепи
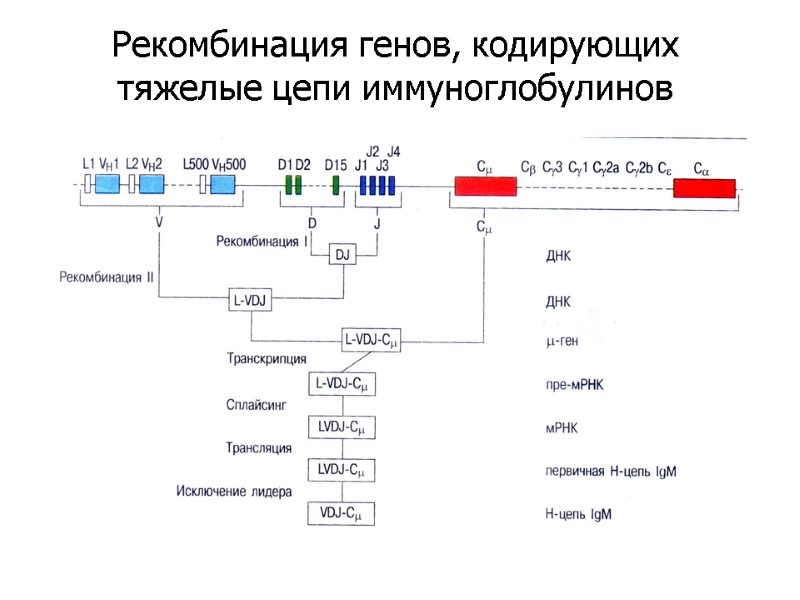
 Рекомбинация генов, кодирующих тяжелые цепи иммуноглобулинов
Рекомбинация генов, кодирующих тяжелые цепи иммуноглобулинов
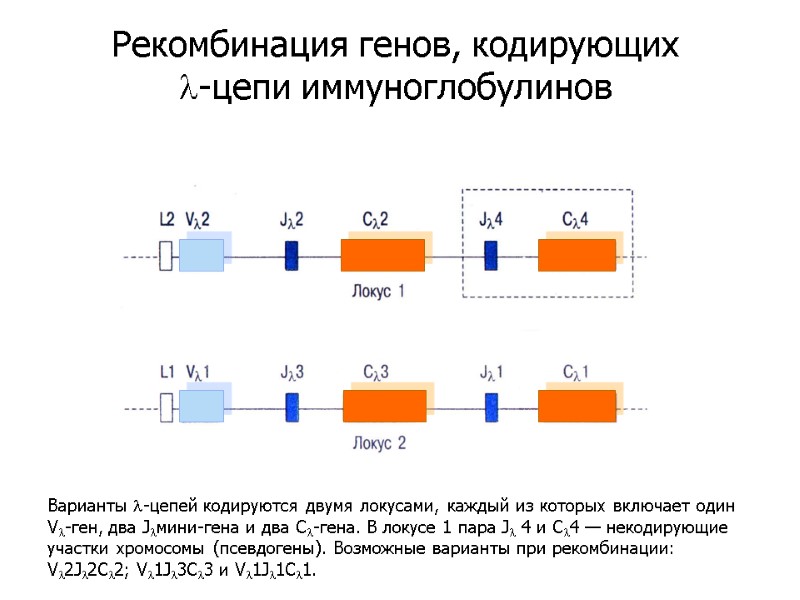
 Варианты l-цепей кодируются двумя локусами, каждый из которых включает один Vl-ген, два Jlмини-гена и два Сl-гена. В локусе 1 пара Jl 4 и Сl4 — некодирующие участки хромосомы (псевдогены). Возможные варианты при рекомбинации: Vl2Jl2Cl2; Vl1Jl3Cl3 и Vl1Jl1Cl1. Рекомбинация генов, кодирующих l-цепи иммуноглобулинов
Варианты l-цепей кодируются двумя локусами, каждый из которых включает один Vl-ген, два Jlмини-гена и два Сl-гена. В локусе 1 пара Jl 4 и Сl4 — некодирующие участки хромосомы (псевдогены). Возможные варианты при рекомбинации: Vl2Jl2Cl2; Vl1Jl3Cl3 и Vl1Jl1Cl1. Рекомбинация генов, кодирующих l-цепи иммуноглобулинов
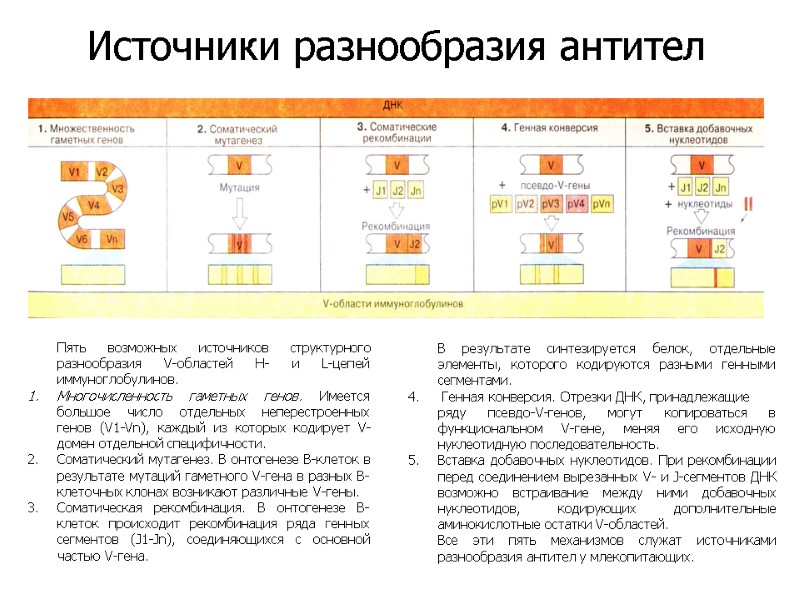
 Пять возможных источников структурного разнообразия V-областей Н- и L-цепей иммуноглобулинов. Многочисленность гаметных генов. Имеется большое число отдельных неперестроенных генов (V1-Vn), каждый из которых кодирует V-домен отдельной специфичности. Соматический мутагенез. В онтогенезе В-клеток в результате мутаций гаметного V-гена в разных В-клеточных клонах возникают различные V-гены. Соматическая рекомбинация. В онтогенезе В-клеток происходит рекомбинация ряда генных сегментов (J1-Jn), соединяющихся с основной частью V-гена. В результате синтезируется белок, отдельные элементы, которого кодируются разными генными сегментами. Генная конверсия. Отрезки ДНК, принадлежащие ряду псевдо-V-генов, могут копироваться в функциональном V-гене, меняя его исходную нуклеотидную последовательность. Вставка добавочных нуклеотидов. При рекомбинации перед соединением вырезанных V- и J-сегментов ДНК возможно встраивание между ними добавочных нуклеотидов, кодирующих дополнительные аминокислотные остатки V-областей. Все эти пять механизмов служат источниками разнообразия антител у млекопитающих. Источники разнообразия антител
Пять возможных источников структурного разнообразия V-областей Н- и L-цепей иммуноглобулинов. Многочисленность гаметных генов. Имеется большое число отдельных неперестроенных генов (V1-Vn), каждый из которых кодирует V-домен отдельной специфичности. Соматический мутагенез. В онтогенезе В-клеток в результате мутаций гаметного V-гена в разных В-клеточных клонах возникают различные V-гены. Соматическая рекомбинация. В онтогенезе В-клеток происходит рекомбинация ряда генных сегментов (J1-Jn), соединяющихся с основной частью V-гена. В результате синтезируется белок, отдельные элементы, которого кодируются разными генными сегментами. Генная конверсия. Отрезки ДНК, принадлежащие ряду псевдо-V-генов, могут копироваться в функциональном V-гене, меняя его исходную нуклеотидную последовательность. Вставка добавочных нуклеотидов. При рекомбинации перед соединением вырезанных V- и J-сегментов ДНК возможно встраивание между ними добавочных нуклеотидов, кодирующих дополнительные аминокислотные остатки V-областей. Все эти пять механизмов служат источниками разнообразия антител у млекопитающих. Источники разнообразия антител
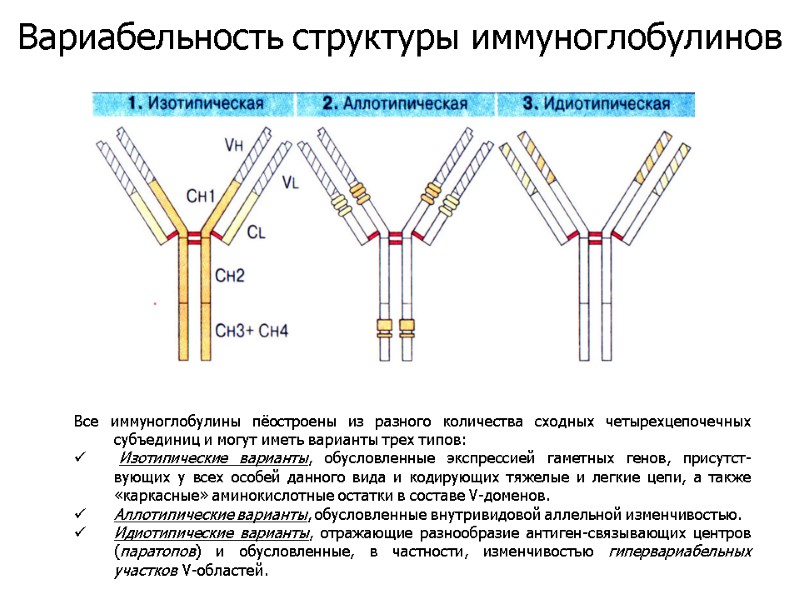
 Все иммуноглобулины пёостроены из разного количества сходных четырехцепочечных субъединиц и могут иметь варианты трех типов: Изотипические варианты, обусловленные экспрессией гаметных генов, присутст-вующих у всех особей данного вида и кодирующих тяжелые и легкие цепи, а также «каркасные» аминокислотные остатки в составе V-доменов. Аллотипические варианты, обусловленные внутривидовой аллельной изменчивостью. Идиотипические варианты, отражающие разнообразие антиген-связывающих центров (паратопов) и обусловленные, в частности, изменчивостью гипервариабельных участков V-областей. Вариабельность структуры иммуноглобулинов
Все иммуноглобулины пёостроены из разного количества сходных четырехцепочечных субъединиц и могут иметь варианты трех типов: Изотипические варианты, обусловленные экспрессией гаметных генов, присутст-вующих у всех особей данного вида и кодирующих тяжелые и легкие цепи, а также «каркасные» аминокислотные остатки в составе V-доменов. Аллотипические варианты, обусловленные внутривидовой аллельной изменчивостью. Идиотипические варианты, отражающие разнообразие антиген-связывающих центров (паратопов) и обусловленные, в частности, изменчивостью гипервариабельных участков V-областей. Вариабельность структуры иммуноглобулинов
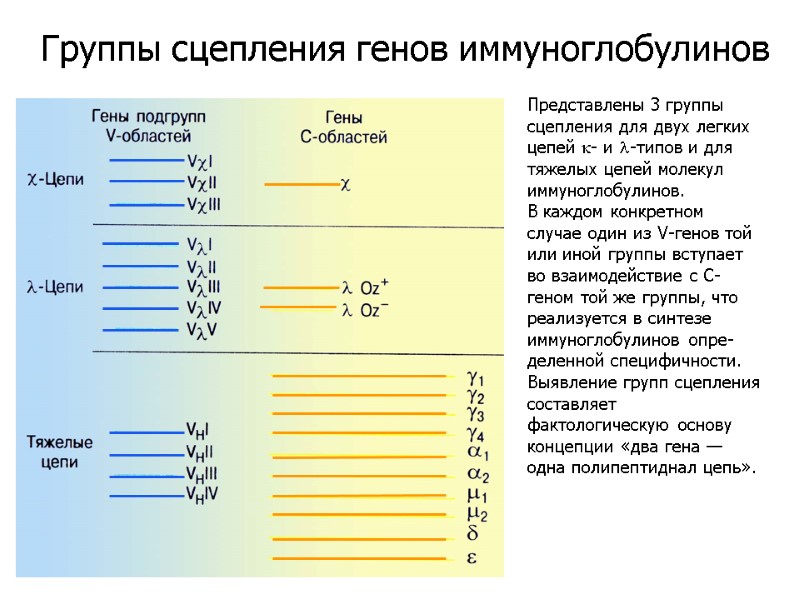
 Представлены 3 группы сцепления для двух легких цепей k- и l-типов и для тяжелых цепей молекул иммуноглобулинов. В каждом конкретном случае один из V-генов той или иной группы вступает во взаимодействие с С-геном той же группы, что реализуется в синтезе иммуноглобулинов опре-деленной специфичности. Выявление групп сцепления составляет фактологическую основу концепции «два гена — одна полипептиднал цепь». Группы сцепления генов иммуноглобулинов
Представлены 3 группы сцепления для двух легких цепей k- и l-типов и для тяжелых цепей молекул иммуноглобулинов. В каждом конкретном случае один из V-генов той или иной группы вступает во взаимодействие с С-геном той же группы, что реализуется в синтезе иммуноглобулинов опре-деленной специфичности. Выявление групп сцепления составляет фактологическую основу концепции «два гена — одна полипептиднал цепь». Группы сцепления генов иммуноглобулинов
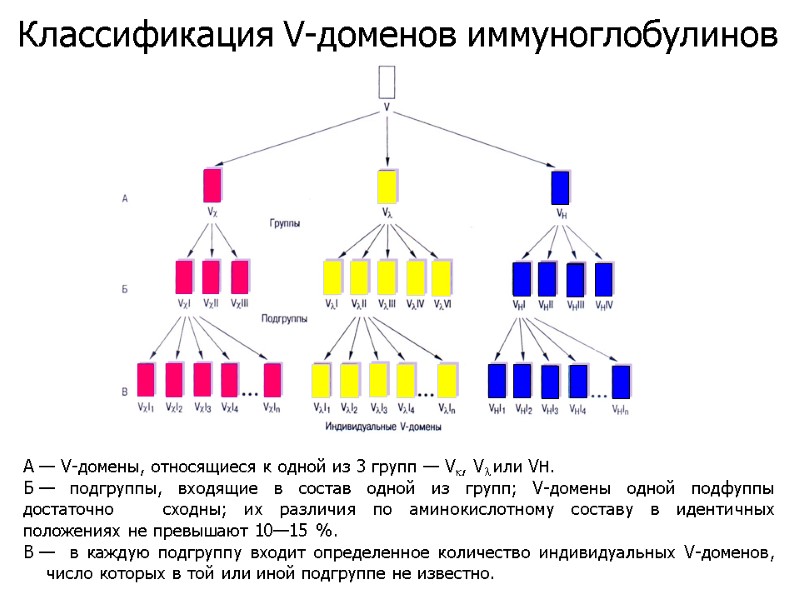
 А — V-домены, относящиеся к одной из 3 групп — Vk, Vl или VH. Б — подгруппы, входящие в состав одной из групп; V-домены одной подфуппы достаточно сходны; их различия по аминокислотному составу в идентичных положениях не превышают 10—15 %. В — в каждую подгруппу входит определенное количество индивидуальных V-доменов, число которых в той или иной подгруппе не известно. Классификация V-доменов иммуноглобулинов
А — V-домены, относящиеся к одной из 3 групп — Vk, Vl или VH. Б — подгруппы, входящие в состав одной из групп; V-домены одной подфуппы достаточно сходны; их различия по аминокислотному составу в идентичных положениях не превышают 10—15 %. В — в каждую подгруппу входит определенное количество индивидуальных V-доменов, число которых в той или иной подгруппе не известно. Классификация V-доменов иммуноглобулинов
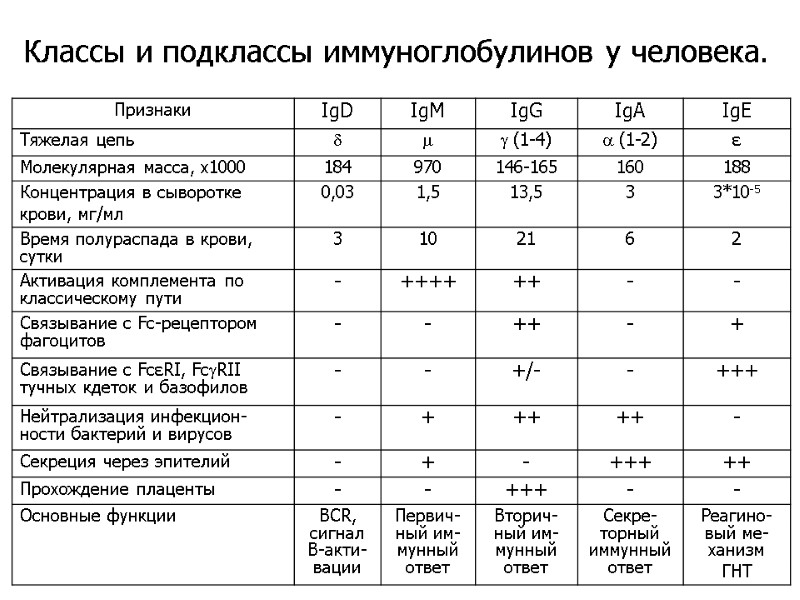
 Классы и подклассы иммуноглобулинов у человека.
Классы и подклассы иммуноглобулинов у человека.
 Классы и подклассы иммуноглобулинов у человека.
Классы и подклассы иммуноглобулинов у человека.
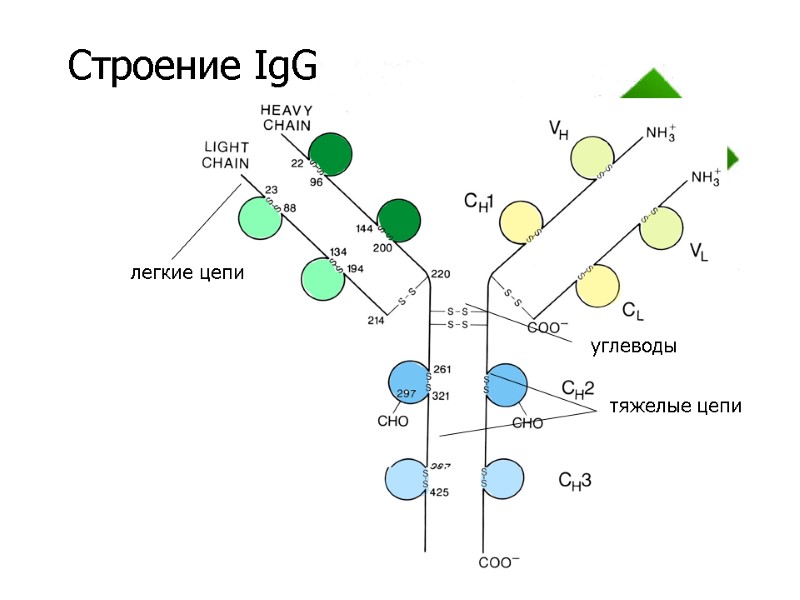
 Строение IgG легкие цепи тяжелые цепи углеводы
Строение IgG легкие цепи тяжелые цепи углеводы
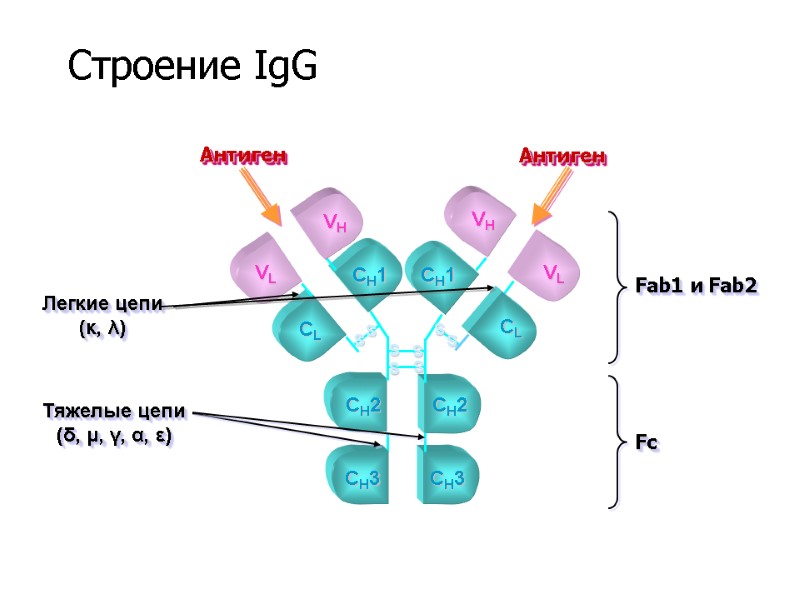
 VL CH3 S S S S CH3 CL S S CH1 CH2 CH2 S S CH1 VL VH VH CL Легкие цепи (κ, λ) Тяжелые цепи (δ, μ, γ, α, ε) Антиген Антиген Fab1 и Fab2 Fc Строение IgG
VL CH3 S S S S CH3 CL S S CH1 CH2 CH2 S S CH1 VL VH VH CL Легкие цепи (κ, λ) Тяжелые цепи (δ, μ, γ, α, ε) Антиген Антиген Fab1 и Fab2 Fc Строение IgG


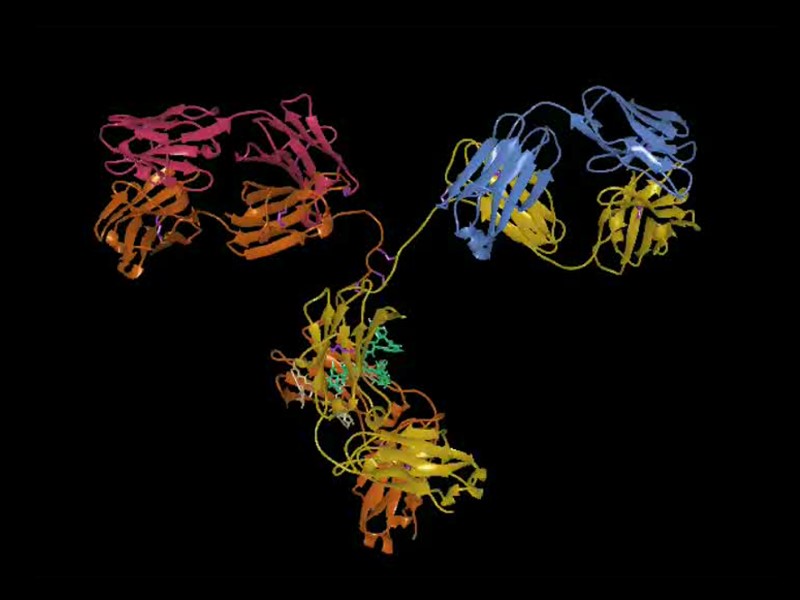
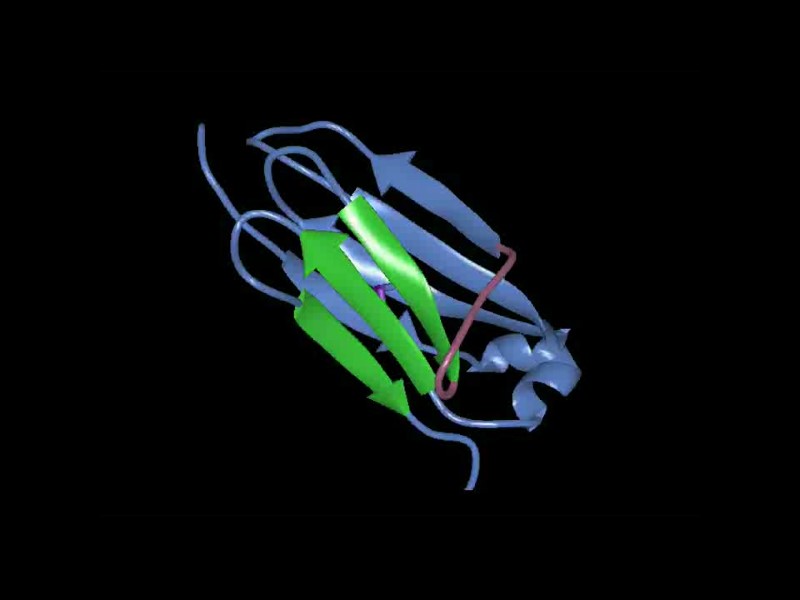
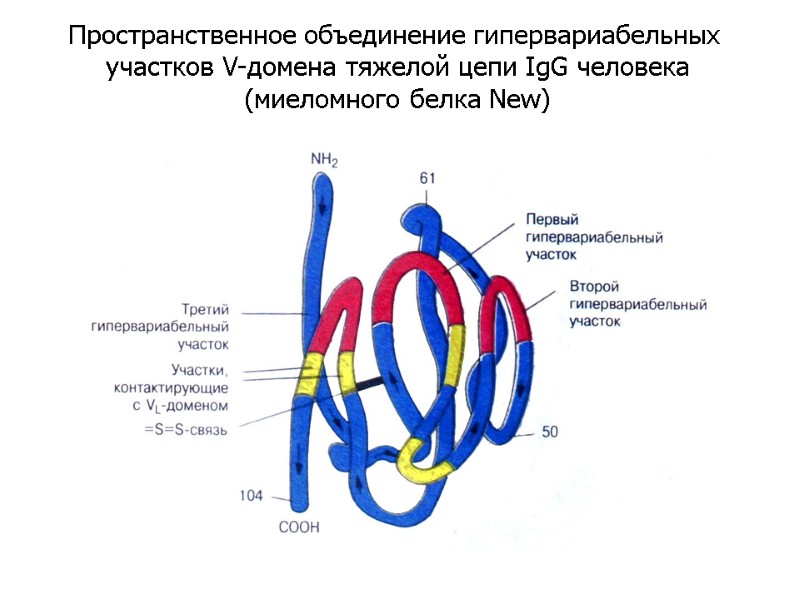
 Пространственное объединение гипервариабельных участков V-домена тяжелой цепи IgG человека (миеломного белка New)
Пространственное объединение гипервариабельных участков V-домена тяжелой цепи IgG человека (миеломного белка New)
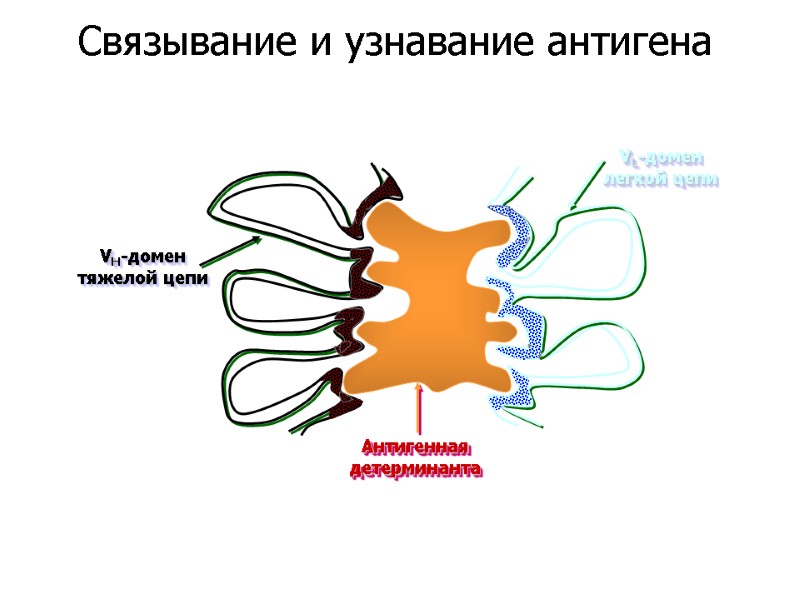
 Антигенная детерминанта VL-домен легкой цепи VH-домен тяжелой цепи Связывание и узнавание антигена
Антигенная детерминанта VL-домен легкой цепи VH-домен тяжелой цепи Связывание и узнавание антигена
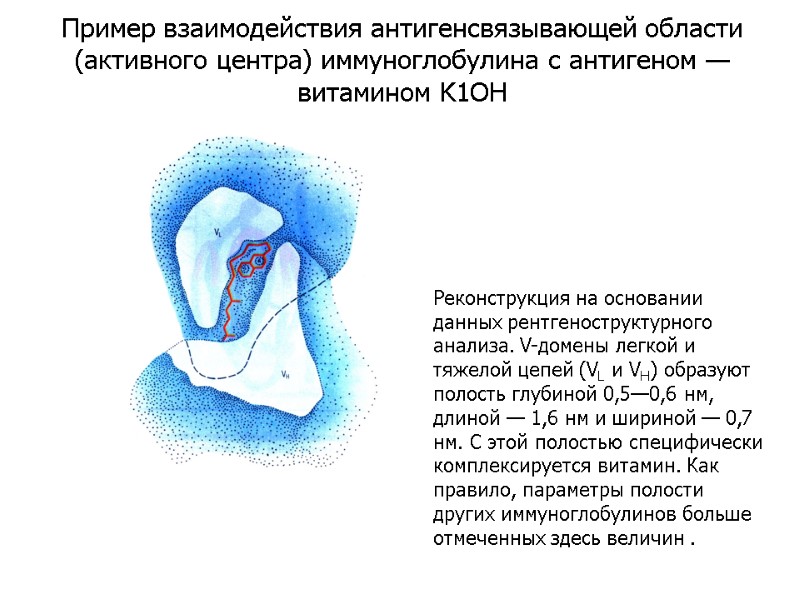
 Реконструкция на основании данных рентгеноструктурного анализа. V-домены легкой и тяжелой цепей (VL и VH) образуют полость глубиной 0,5—0,6 нм, длиной — 1,6 нм и шириной — 0,7 нм. С этой полостью специфически комплексируется витамин. Как правило, параметры полости других иммуноглобулинов больше отмеченных здесь величин . Пример взаимодействия антигенсвязывающей области (активного центра) иммуноглобулина с антигеном — витамином K1OH
Реконструкция на основании данных рентгеноструктурного анализа. V-домены легкой и тяжелой цепей (VL и VH) образуют полость глубиной 0,5—0,6 нм, длиной — 1,6 нм и шириной — 0,7 нм. С этой полостью специфически комплексируется витамин. Как правило, параметры полости других иммуноглобулинов больше отмеченных здесь величин . Пример взаимодействия антигенсвязывающей области (активного центра) иммуноглобулина с антигеном — витамином K1OH
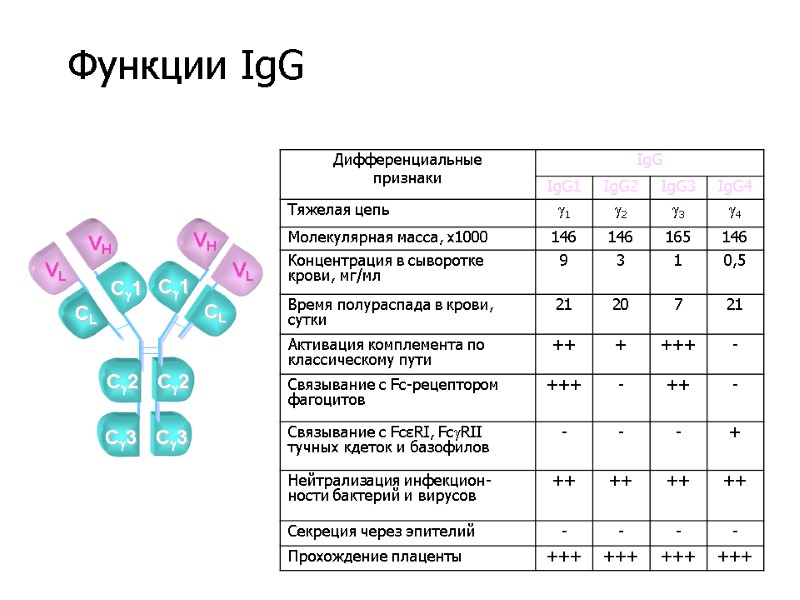
 VL VH VH VL C3 C2 CL C1 CL C1 C2 C3 Функции IgG
VL VH VH VL C3 C2 CL C1 CL C1 C2 C3 Функции IgG
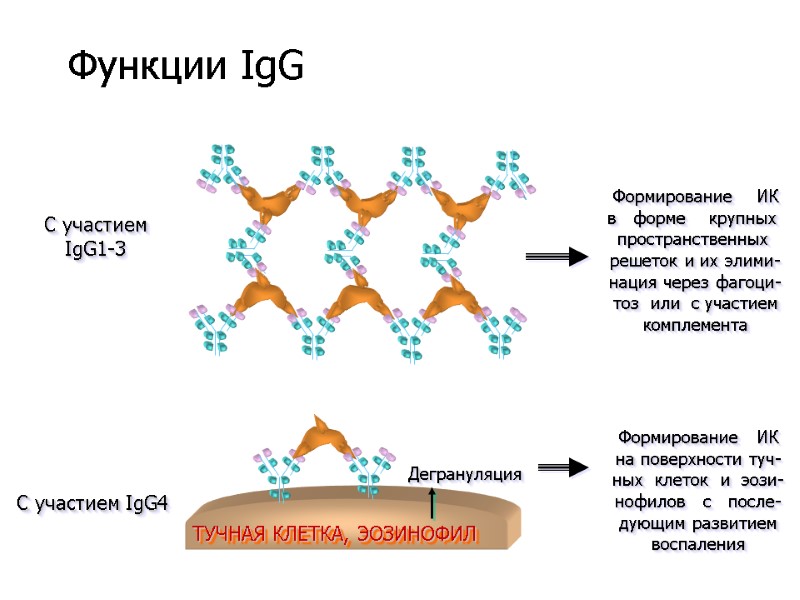
 Формирование ИК в форме крупных пространственных решеток и их элими- нация через фагоци- тоз или с участием комплемента С участием IgG1-3 C участием IgG4 Формирование ИК на поверхности туч- ных клеток и эози- нофилов с после- дующим развитием воспаления ТУЧНАЯ КЛЕТКА, ЭОЗИНОФИЛ Дегрануляция Функции IgG
Формирование ИК в форме крупных пространственных решеток и их элими- нация через фагоци- тоз или с участием комплемента С участием IgG1-3 C участием IgG4 Формирование ИК на поверхности туч- ных клеток и эози- нофилов с после- дующим развитием воспаления ТУЧНАЯ КЛЕТКА, ЭОЗИНОФИЛ Дегрануляция Функции IgG
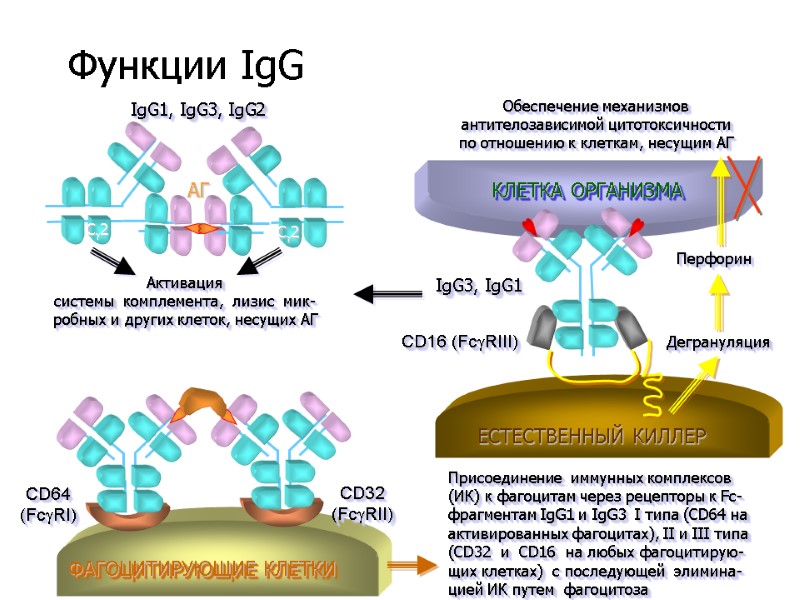
 АГ Активация системы комплемента, лизис мик- робных и других клеток, несущих АГ C2 C2 IgG1, IgG3, IgG2 КЛЕТКА ОРГАНИЗМА IgG3, IgG1 CD16 (FcRIII) ЕСТЕСТВЕННЫЙ КИЛЛЕР Перфорин Обеспечение механизмов антителозависимой цитотоксичности по отношению к клеткам, несущим АГ ФАГОЦИТИРУЮЩИЕ КЛЕТКИ CD64 (FcRI) CD32 (FcRII) Присоединение иммунных комплексов (ИК) к фагоцитам через рецепторы к Fc- фрагментам IgG1 и IgG3 I типа (СD64 на активированных фагоцитах), II и III типа (СD32 и СD16 на любых фагоцитирую- щих клетках) с последующей элимина- цией ИК путем фагоцитоза Дегрануляция Функции IgG
АГ Активация системы комплемента, лизис мик- робных и других клеток, несущих АГ C2 C2 IgG1, IgG3, IgG2 КЛЕТКА ОРГАНИЗМА IgG3, IgG1 CD16 (FcRIII) ЕСТЕСТВЕННЫЙ КИЛЛЕР Перфорин Обеспечение механизмов антителозависимой цитотоксичности по отношению к клеткам, несущим АГ ФАГОЦИТИРУЮЩИЕ КЛЕТКИ CD64 (FcRI) CD32 (FcRII) Присоединение иммунных комплексов (ИК) к фагоцитам через рецепторы к Fc- фрагментам IgG1 и IgG3 I типа (СD64 на активированных фагоцитах), II и III типа (СD32 и СD16 на любых фагоцитирую- щих клетках) с последующей элимина- цией ИК путем фагоцитоза Дегрануляция Функции IgG
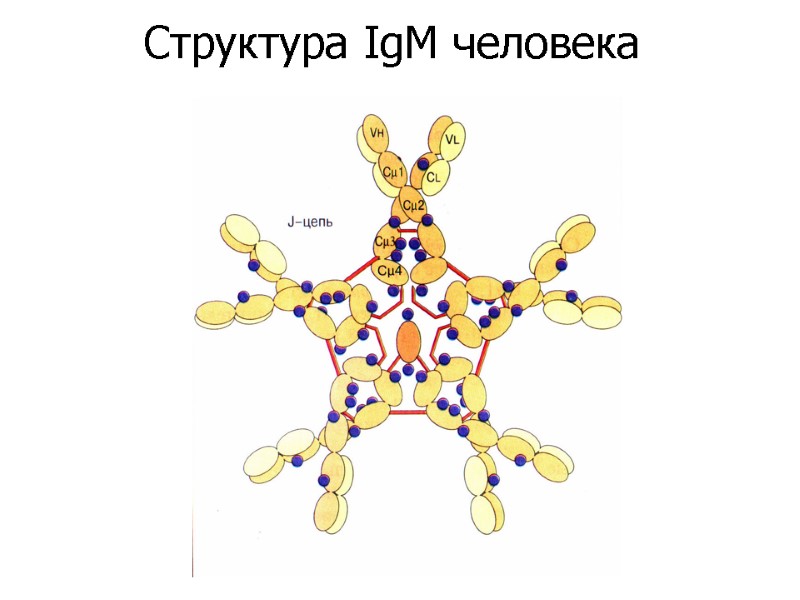
 Структура IgM человека
Структура IgM человека
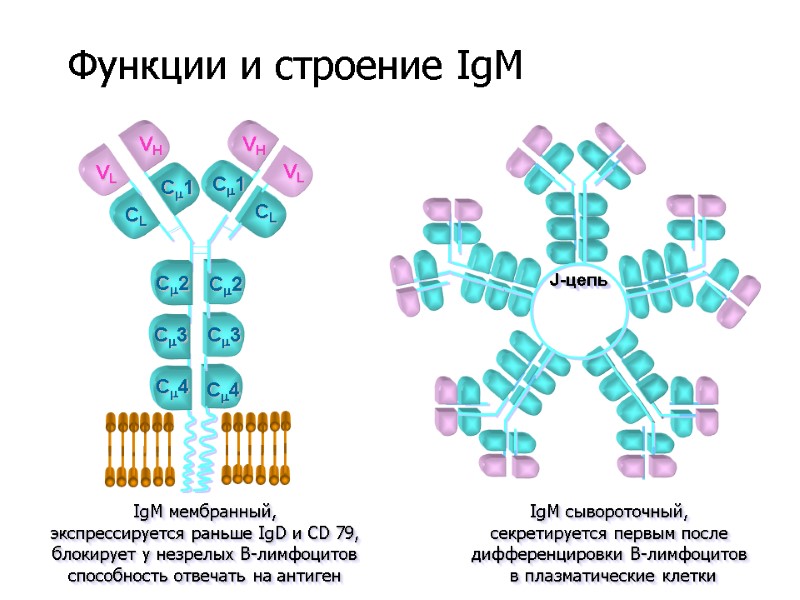
 VL VH VH VL C3 C2 CL C1 IgM мембранный, экспрессируется раньше IgD и CD 79, блокирует у незрелых В-лимфоцитов способность отвечать на антиген IgM сывороточный, секретируется первым после дифференцировки В-лимфоцитов в плазматические клетки CL C1 C2 C3 C4 C4 J-цепь Функции и строение IgM
VL VH VH VL C3 C2 CL C1 IgM мембранный, экспрессируется раньше IgD и CD 79, блокирует у незрелых В-лимфоцитов способность отвечать на антиген IgM сывороточный, секретируется первым после дифференцировки В-лимфоцитов в плазматические клетки CL C1 C2 C3 C4 C4 J-цепь Функции и строение IgM
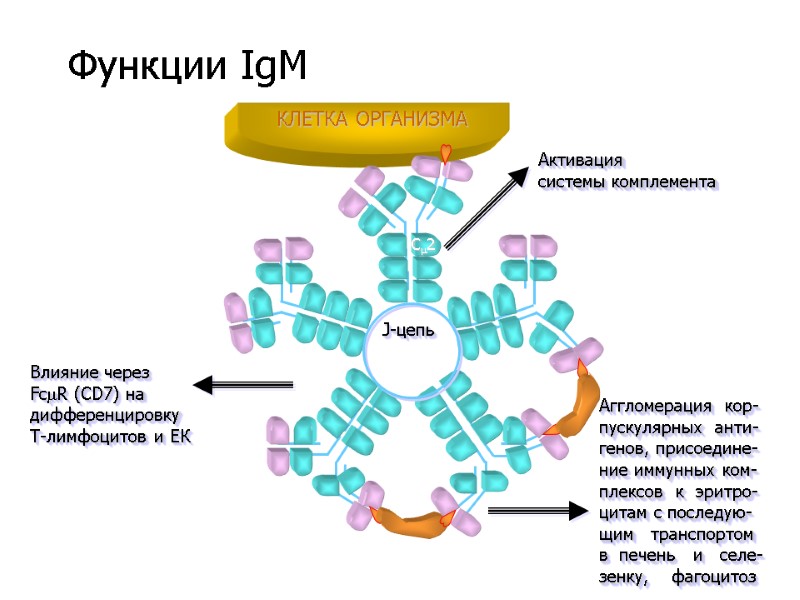
 J-цепь Активация системы комплемента C2 Аггломерация кор- пускулярных анти- генов, присоедине- ние иммунных ком- плексов к эритро- цитам с последую- щим транспортом в печень и селе- зенку, фагоцитоз Влияние через FcR (CD7) на дифференцировку Т-лимфоцитов и ЕК КЛЕТКА ОРГАНИЗМА Функции IgM
J-цепь Активация системы комплемента C2 Аггломерация кор- пускулярных анти- генов, присоедине- ние иммунных ком- плексов к эритро- цитам с последую- щим транспортом в печень и селе- зенку, фагоцитоз Влияние через FcR (CD7) на дифференцировку Т-лимфоцитов и ЕК КЛЕТКА ОРГАНИЗМА Функции IgM
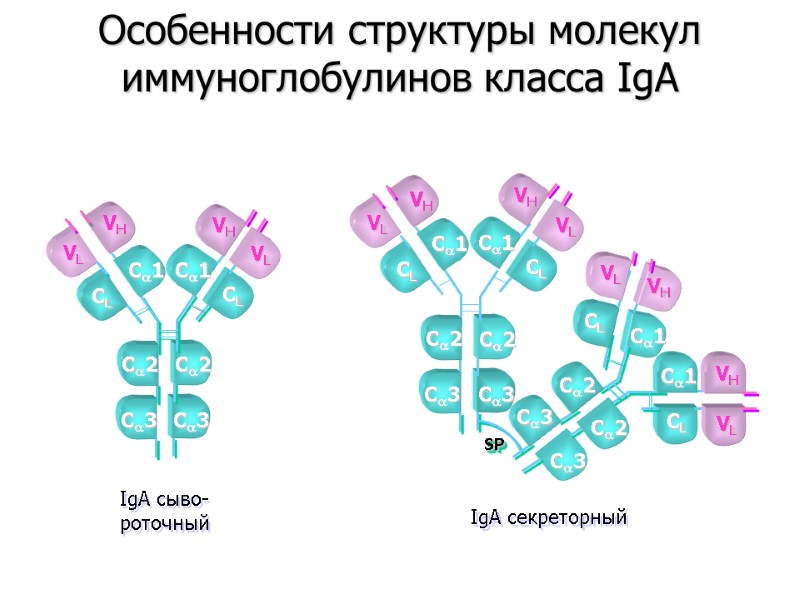
 VL VH VH VL C3 C2 CL C1 CL C1 C2 C3 IgA сыво- роточный VL VH VH VL C3 C2 CL C1 CL C1 C2 C3 C2 C2 VL VH CL C1 C3 C3 SP VH VL CL C1 IgA секреторный Особенности структуры молекул иммуноглобулинов класса IgA
VL VH VH VL C3 C2 CL C1 CL C1 C2 C3 IgA сыво- роточный VL VH VH VL C3 C2 CL C1 CL C1 C2 C3 C2 C2 VL VH CL C1 C3 C3 SP VH VL CL C1 IgA секреторный Особенности структуры молекул иммуноглобулинов класса IgA
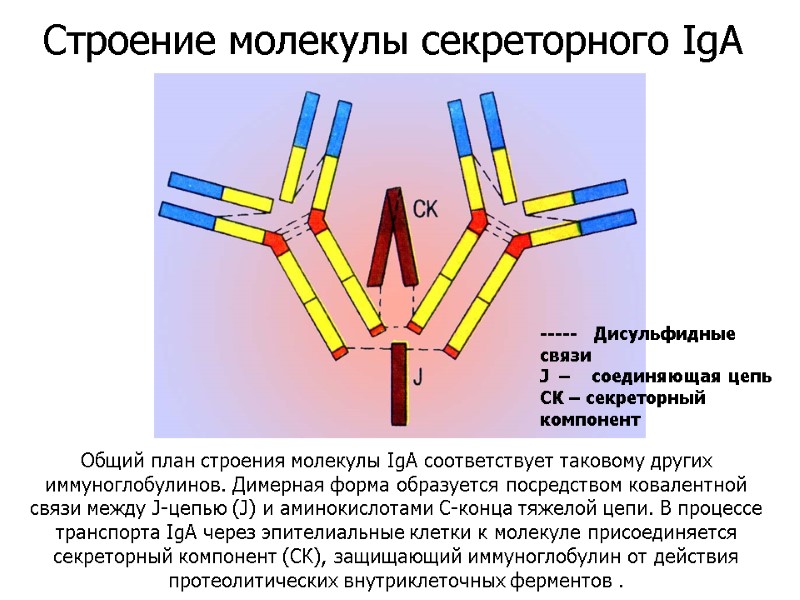
 Общий план строения молекулы IgA соответствует таковому других иммуноглобулинов. Димерная форма образуется посредством ковалентной связи между J-цепью (J) и аминокислотами С-конца тяжелой цепи. В процессе транспорта IgA через эпителиальные клетки к молекуле присоединяется секреторный компонент (СК), защищающий иммуноглобулин от действия протеолитических внутриклеточных ферментов . ----- Дисульфидные связи J – соединяющая цепь СК – секреторный компонент Строение молекулы секреторного IgA
Общий план строения молекулы IgA соответствует таковому других иммуноглобулинов. Димерная форма образуется посредством ковалентной связи между J-цепью (J) и аминокислотами С-конца тяжелой цепи. В процессе транспорта IgA через эпителиальные клетки к молекуле присоединяется секреторный компонент (СК), защищающий иммуноглобулин от действия протеолитических внутриклеточных ферментов . ----- Дисульфидные связи J – соединяющая цепь СК – секреторный компонент Строение молекулы секреторного IgA
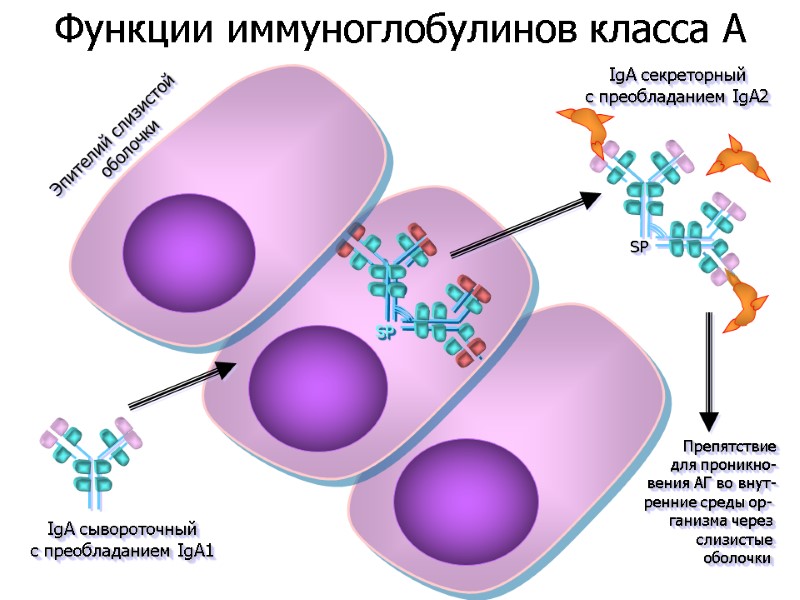
 IgA сывороточный c преобладанием IgA1 SP SP SP IgA секреторный c преобладанием IgA2 Эпителий слизистой оболочки Препятствие для проникно- вения АГ во внут- ренние среды ор- ганизма через слизистые оболочки Функции иммуноглобулинов класса A
IgA сывороточный c преобладанием IgA1 SP SP SP IgA секреторный c преобладанием IgA2 Эпителий слизистой оболочки Препятствие для проникно- вения АГ во внут- ренние среды ор- ганизма через слизистые оболочки Функции иммуноглобулинов класса A
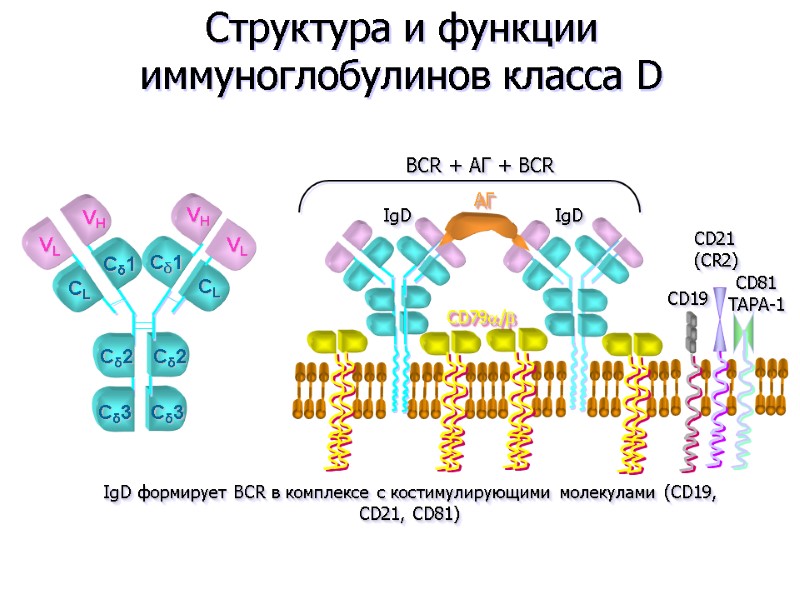
 Структура и функции иммуноглобулинов класса D АГ IgD IgD CD79/ CD19 CD21 (CR2) IgD формирует ВСR в комплексе с костимулирующими молекулами (CD19, CD21, CD81) BCR + АГ + BCR CD81 TAPA-1 VL VH VH VL Cδ3 Cδ2 CL Cδ1 CL Cδ1 Cδ2 Cδ3
Структура и функции иммуноглобулинов класса D АГ IgD IgD CD79/ CD19 CD21 (CR2) IgD формирует ВСR в комплексе с костимулирующими молекулами (CD19, CD21, CD81) BCR + АГ + BCR CD81 TAPA-1 VL VH VH VL Cδ3 Cδ2 CL Cδ1 CL Cδ1 Cδ2 Cδ3
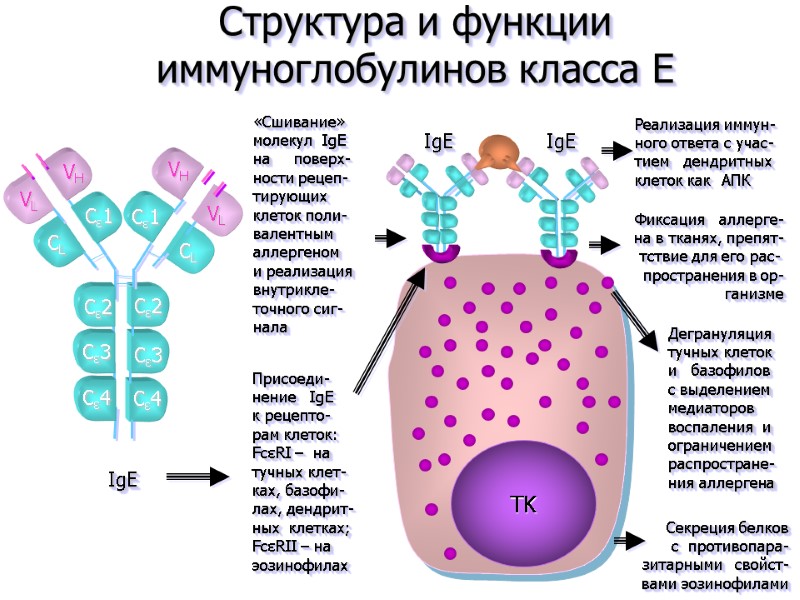
 Секреция белков с противопара- зитарными свойст- вами эозинофилами VL VH VH VL Cε3 Cε2 CL Cε1 CL Cε1 Cε2 Cε3 IgE Cε4 Cε4 Структура и функции иммуноглобулинов класса E TK IgE IgE Реализация иммун- ного ответа с учас- тием дендритных клеток как АПК Фиксация аллерге- на в тканях, препят- тствие для его рас- пространения в ор- ганизме Дегрануляция тучных клеток и базофилов с выделением медиаторов воспаления и ограничением распростране- ния аллергена «Сшивание» молекул IgE на поверх- ности рецеп- тирующих клеток поли- валентным аллергеном и реализация внутрикле- точного сиг- нала Присоеди- нение IgE к рецепто- рам клеток: FcεRI – на тучных клет- ках, базофи- лах, дендрит- ных клетках; FcεRII – на эозинофилах
Секреция белков с противопара- зитарными свойст- вами эозинофилами VL VH VH VL Cε3 Cε2 CL Cε1 CL Cε1 Cε2 Cε3 IgE Cε4 Cε4 Структура и функции иммуноглобулинов класса E TK IgE IgE Реализация иммун- ного ответа с учас- тием дендритных клеток как АПК Фиксация аллерге- на в тканях, препят- тствие для его рас- пространения в ор- ганизме Дегрануляция тучных клеток и базофилов с выделением медиаторов воспаления и ограничением распростране- ния аллергена «Сшивание» молекул IgE на поверх- ности рецеп- тирующих клеток поли- валентным аллергеном и реализация внутрикле- точного сиг- нала Присоеди- нение IgE к рецепто- рам клеток: FcεRI – на тучных клет- ках, базофи- лах, дендрит- ных клетках; FcεRII – на эозинофилах
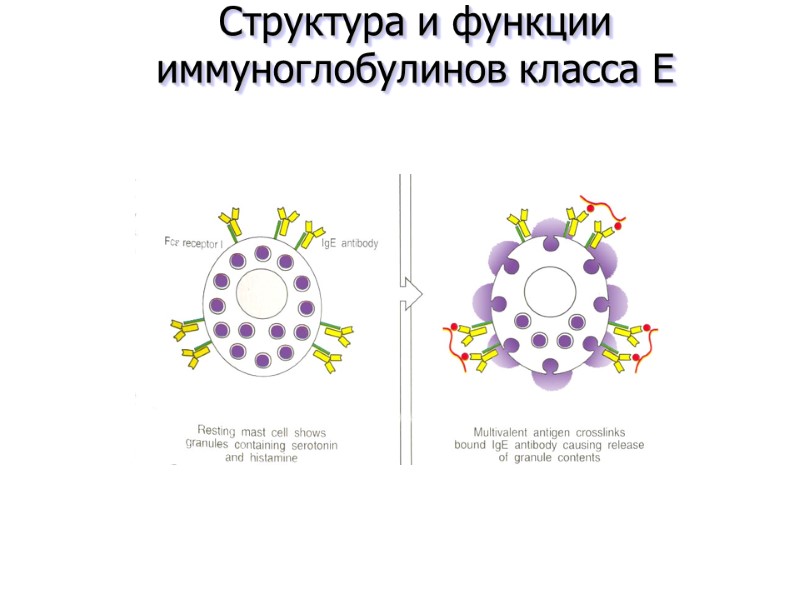
 Структура и функции иммуноглобулинов класса E
Структура и функции иммуноглобулинов класса E
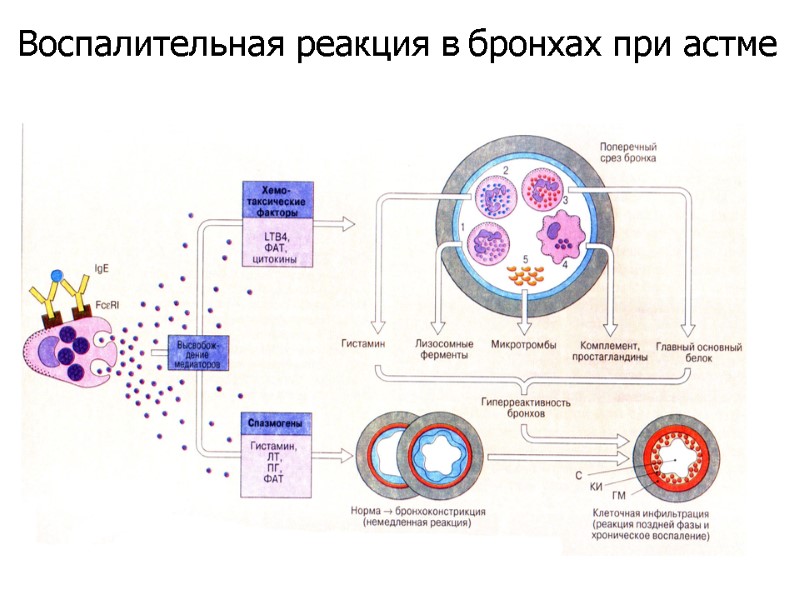
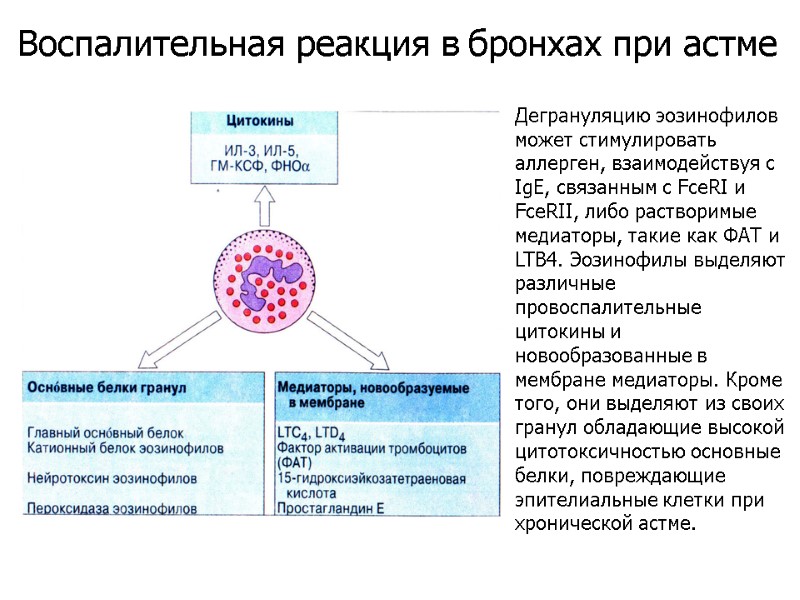
 Воспалительная реакция в бронхах при астме
Воспалительная реакция в бронхах при астме
 Дегрануляцию эозинофилов может стимулировать аллерген, взаимодействуя с IgE, связанным с FceRI и FceRII, либо растворимые медиаторы, такие как ФАТ и LTB4. Эозинофилы выделяют различные провоспалительные цитокины и новообразованные в мембране медиаторы. Кроме того, они выделяют из своих гранул обладающие высокой цитотоксичностью основные белки, повреждающие эпителиальные клетки при хронической астме. Воспалительная реакция в бронхах при астме
Дегрануляцию эозинофилов может стимулировать аллерген, взаимодействуя с IgE, связанным с FceRI и FceRII, либо растворимые медиаторы, такие как ФАТ и LTB4. Эозинофилы выделяют различные провоспалительные цитокины и новообразованные в мембране медиаторы. Кроме того, они выделяют из своих гранул обладающие высокой цитотоксичностью основные белки, повреждающие эпителиальные клетки при хронической астме. Воспалительная реакция в бронхах при астме
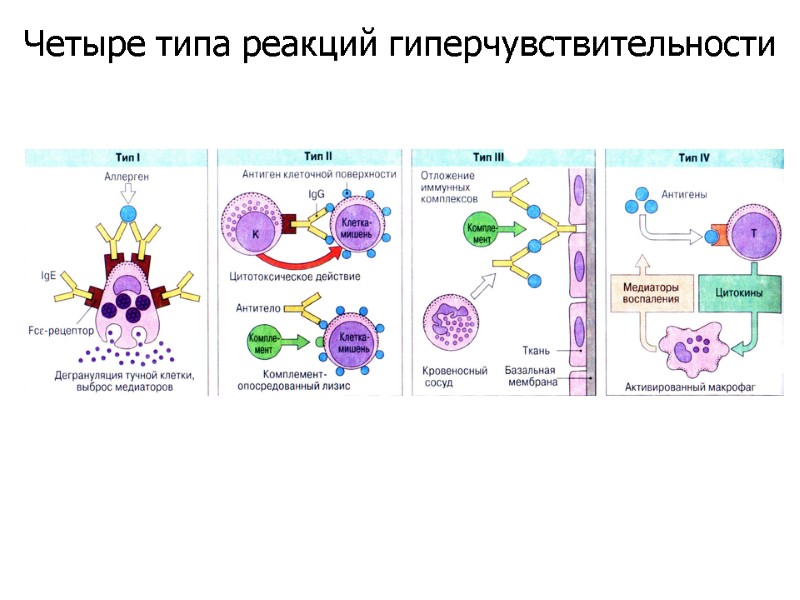
 Четыре типа реакций гиперчувствительности
Четыре типа реакций гиперчувствительности
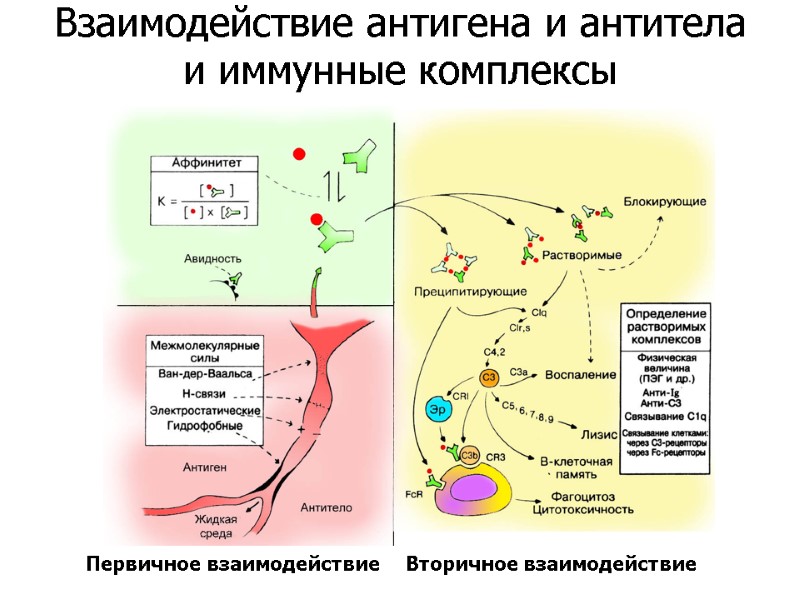
 Первичное взаимодействие Вторичное взаимодействие Взаимодействие антигена и антитела и иммунные комплексы
Первичное взаимодействие Вторичное взаимодействие Взаимодействие антигена и антитела и иммунные комплексы
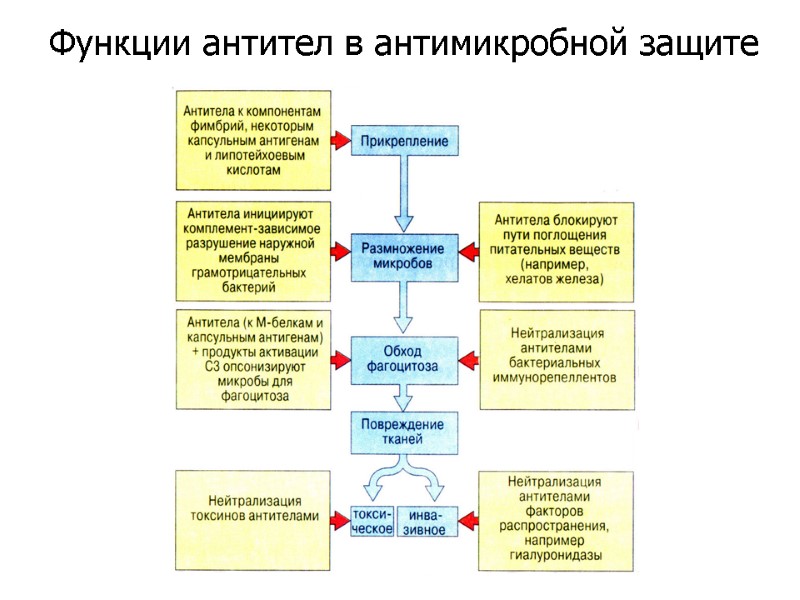
 Функции антител в антимикробной защите
Функции антител в антимикробной защите
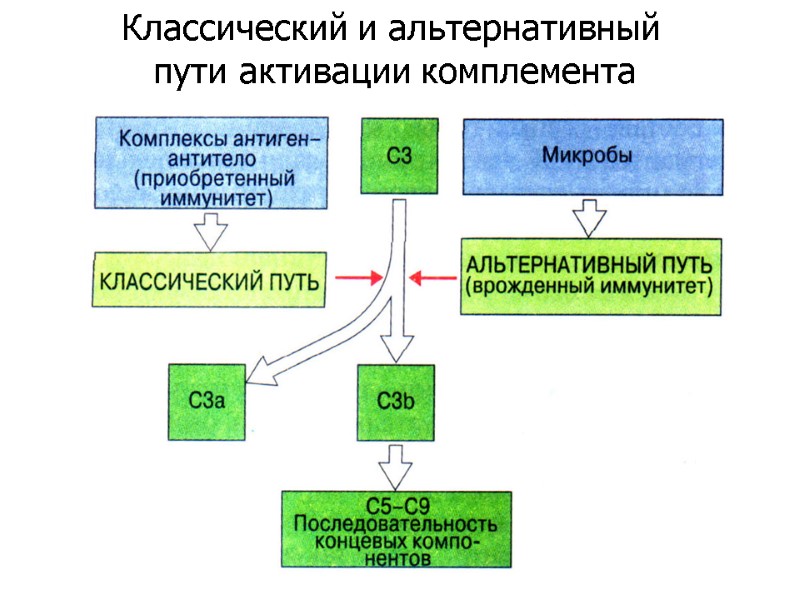
 Классический и альтернативный пути активации комплемента
Классический и альтернативный пути активации комплемента
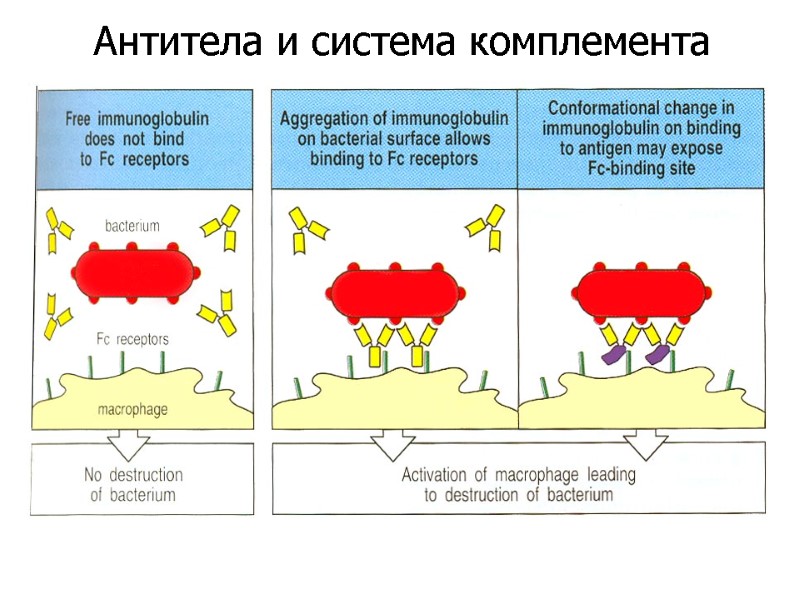
 Антитела и система комплемента
Антитела и система комплемента
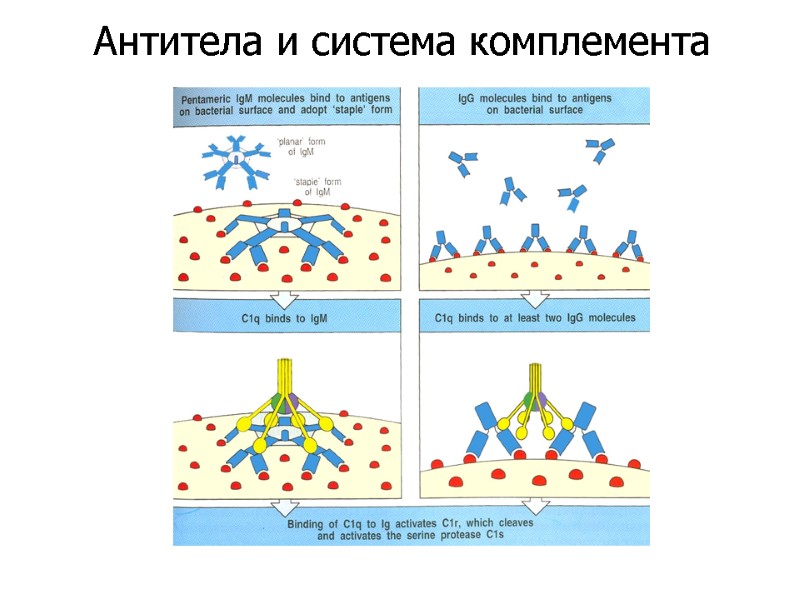
 Антитела и система комплемента
Антитела и система комплемента
 Антитела и НК
Антитела и НК
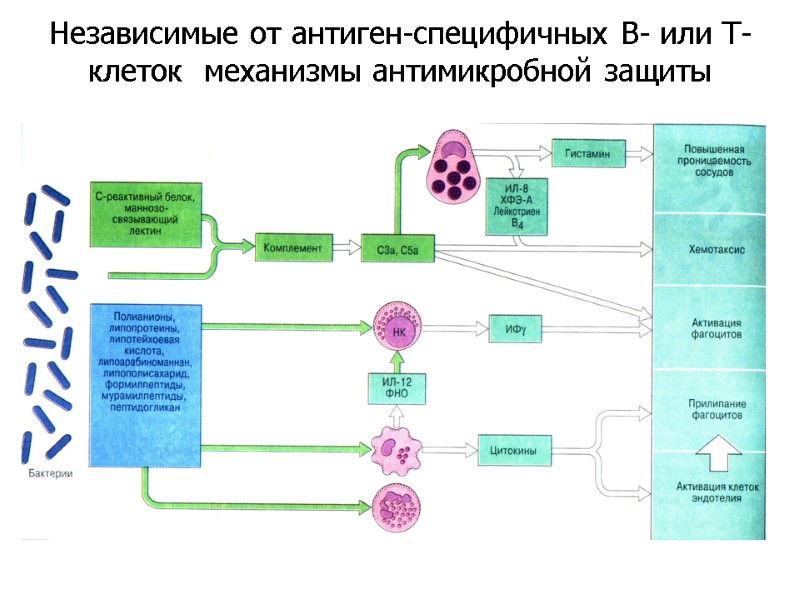
 Независимые от антиген-специфичных В- или Т-клеток механизмы антимикробной защиты
Независимые от антиген-специфичных В- или Т-клеток механизмы антимикробной защиты
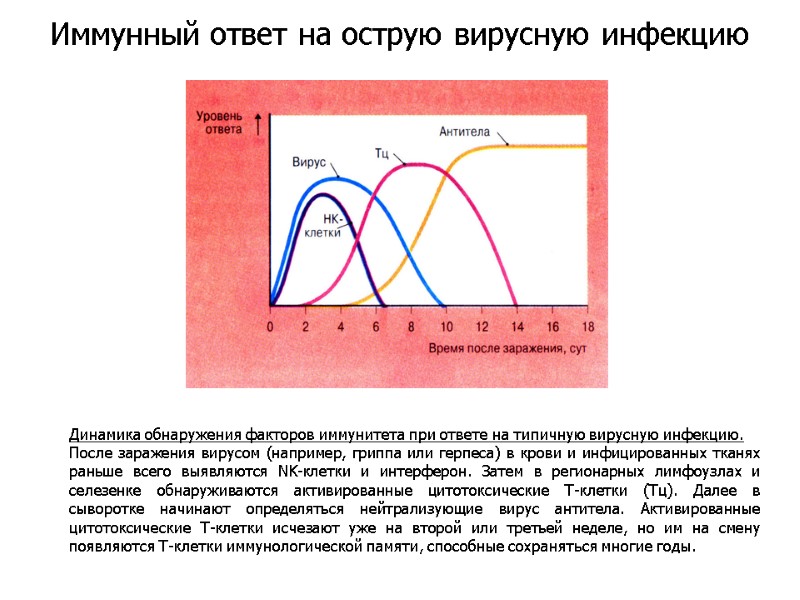
 Динамика обнаружения факторов иммунитета при ответе на типичную вирусную инфекцию. После заражения вирусом (например, гриппа или герпеса) в крови и инфицированных тканях раньше всего выявляются NK-клетки и интерферон. Затем в регионарных лимфоузлах и селезенке обнаруживаются активированные цитотоксические Т-клетки (Тц). Далее в сыворотке начинают определяться нейтрализующие вирус антитела. Активированные цитотоксические Т-клетки исчезают уже на второй или третьей неделе, но им на смену появляются Т-клетки иммунологической памяти, способные сохраняться многие годы. Иммунный ответ на острую вирусную инфекцию
Динамика обнаружения факторов иммунитета при ответе на типичную вирусную инфекцию. После заражения вирусом (например, гриппа или герпеса) в крови и инфицированных тканях раньше всего выявляются NK-клетки и интерферон. Затем в регионарных лимфоузлах и селезенке обнаруживаются активированные цитотоксические Т-клетки (Тц). Далее в сыворотке начинают определяться нейтрализующие вирус антитела. Активированные цитотоксические Т-клетки исчезают уже на второй или третьей неделе, но им на смену появляются Т-клетки иммунологической памяти, способные сохраняться многие годы. Иммунный ответ на острую вирусную инфекцию
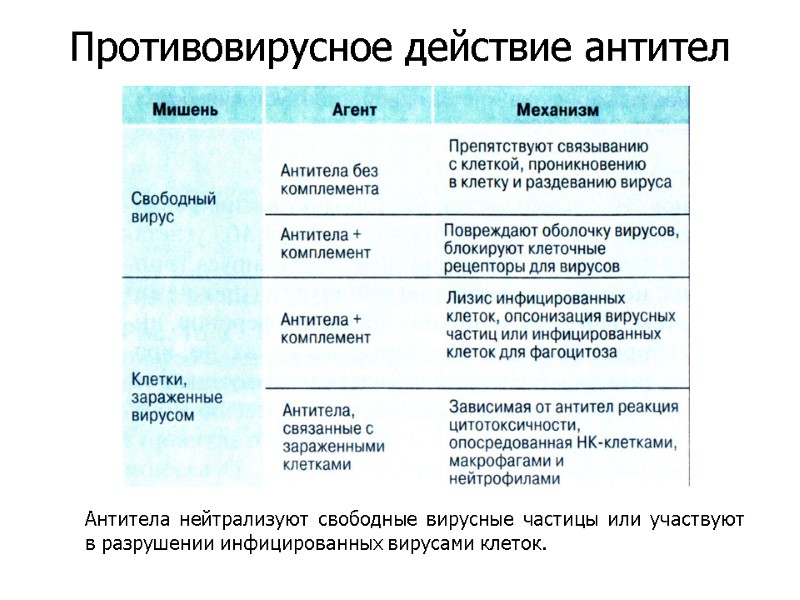
 Антитела нейтрализуют свободные вирусные частицы или участвуют в разрушении инфицированных вирусами клеток. Противовирусное действие антител
Антитела нейтрализуют свободные вирусные частицы или участвуют в разрушении инфицированных вирусами клеток. Противовирусное действие антител
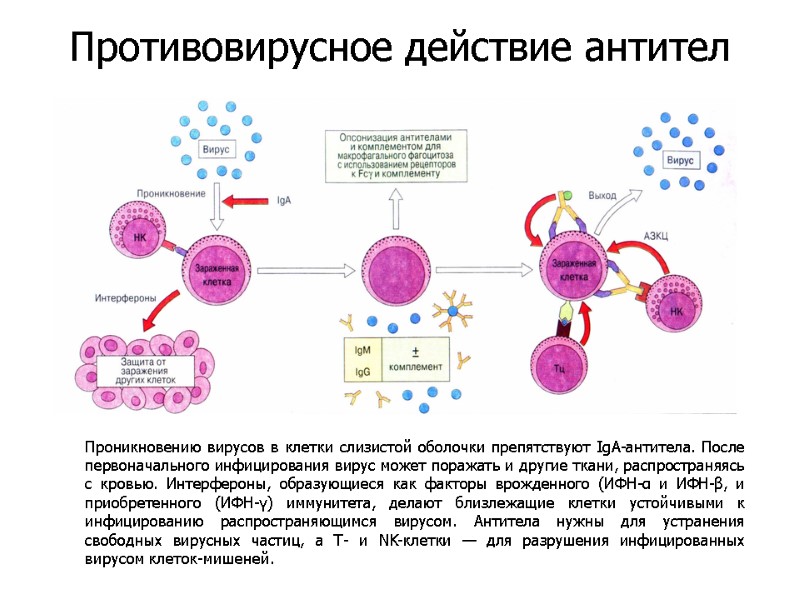
 Проникновению вирусов в клетки слизистой оболочки препятствуют IgA-антитела. После первоначального инфицирования вирус может поражать и другие ткани, распространяясь с кровью. Интерфероны, образующиеся как факторы врожденного (ИФН-α и ИФН-β, и приобретенного (ИФН-γ) иммунитета, делают близлежащие клетки устойчивыми к инфицированию распространяющимся вирусом. Антитела нужны для устранения свободных вирусных частиц, а Т- и NK-клетки — для разрушения инфицированных вирусом клеток-мишеней. Противовирусное действие антител
Проникновению вирусов в клетки слизистой оболочки препятствуют IgA-антитела. После первоначального инфицирования вирус может поражать и другие ткани, распространяясь с кровью. Интерфероны, образующиеся как факторы врожденного (ИФН-α и ИФН-β, и приобретенного (ИФН-γ) иммунитета, делают близлежащие клетки устойчивыми к инфицированию распространяющимся вирусом. Антитела нужны для устранения свободных вирусных частиц, а Т- и NK-клетки — для разрушения инфицированных вирусом клеток-мишеней. Противовирусное действие антител
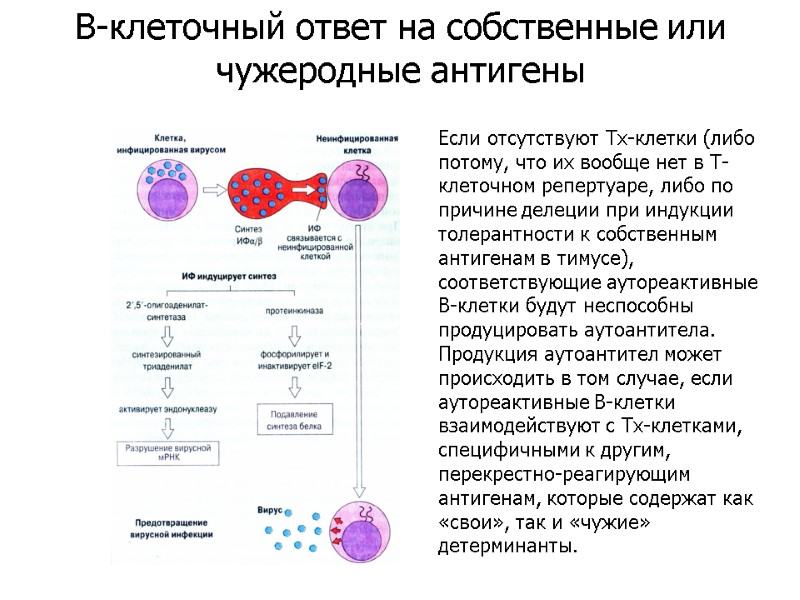
 Если отсутствуют Тх-клетки (либо потому, что их вообще нет в Т-клеточном репертуаре, либо по причине делеции при индукции толерантности к собственным антигенам в тимусе), соответствующие аутореактивные В-клетки будут неспособны продуцировать аутоантитела. Продукция аутоантител может происходить в том случае, если аутореактивные В-клетки взаимодействуют с Тх-клетками, специфичными к другим, перекрестно-реагирующим антигенам, которые содержат как «свои», так и «чужие» детерминанты. В-клеточный ответ на собственные или чужеродные антигены
Если отсутствуют Тх-клетки (либо потому, что их вообще нет в Т-клеточном репертуаре, либо по причине делеции при индукции толерантности к собственным антигенам в тимусе), соответствующие аутореактивные В-клетки будут неспособны продуцировать аутоантитела. Продукция аутоантител может происходить в том случае, если аутореактивные В-клетки взаимодействуют с Тх-клетками, специфичными к другим, перекрестно-реагирующим антигенам, которые содержат как «свои», так и «чужие» детерминанты. В-клеточный ответ на собственные или чужеродные антигены
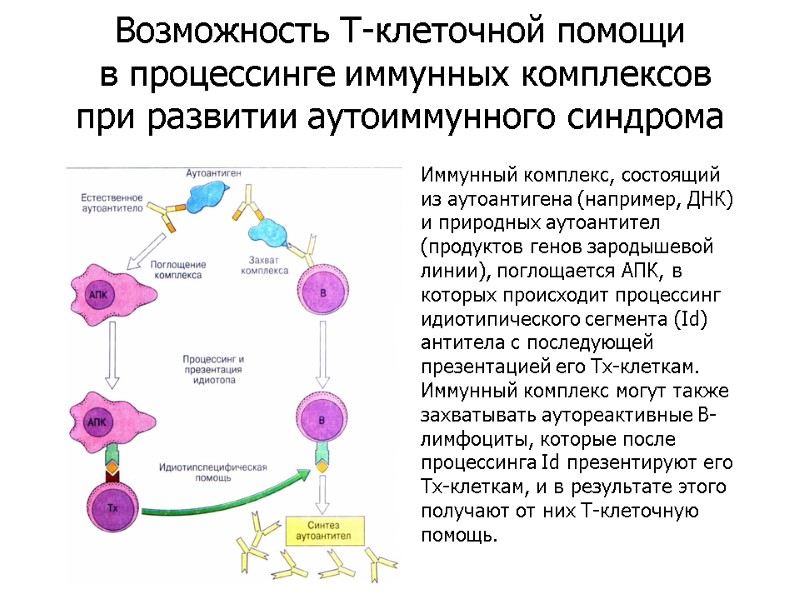
 Иммунный комплекс, состоящий из аутоантигена (например, ДНК) и природных аутоантител (продуктов генов зародышевой линии), поглощается АПК, в которых происходит процессинг идиотипического сегмента (Id) антитела с последующей презентацией его Тх-клеткам. Иммунный комплекс могут также захватывать аутореактивные В-лимфоциты, которые после процессинга Id презентируют его Тх-клеткам, и в результате этого получают от них Т-клеточную помощь. Возможность Т-клеточной помощи в процессинге иммунных комплексов при развитии аутоиммунного синдрома
Иммунный комплекс, состоящий из аутоантигена (например, ДНК) и природных аутоантител (продуктов генов зародышевой линии), поглощается АПК, в которых происходит процессинг идиотипического сегмента (Id) антитела с последующей презентацией его Тх-клеткам. Иммунный комплекс могут также захватывать аутореактивные В-лимфоциты, которые после процессинга Id презентируют его Тх-клеткам, и в результате этого получают от них Т-клеточную помощь. Возможность Т-клеточной помощи в процессинге иммунных комплексов при развитии аутоиммунного синдрома
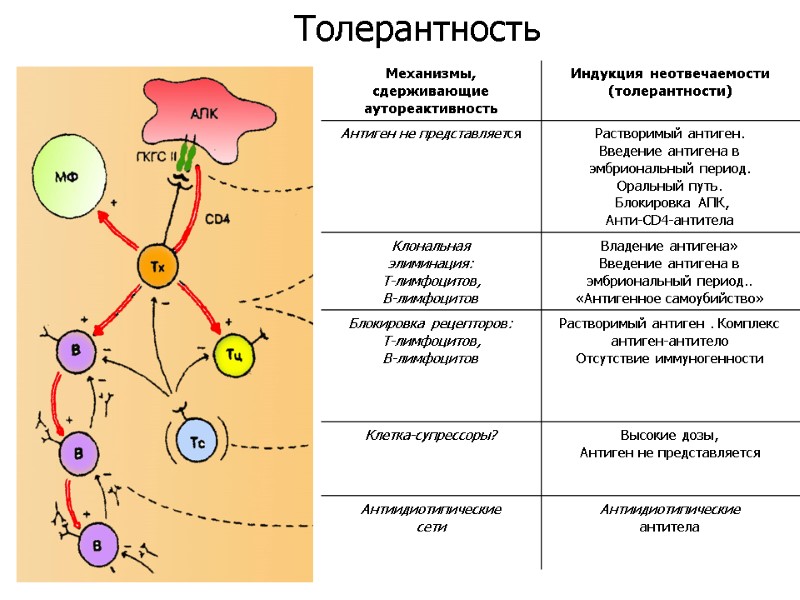
 Толерантность
Толерантность
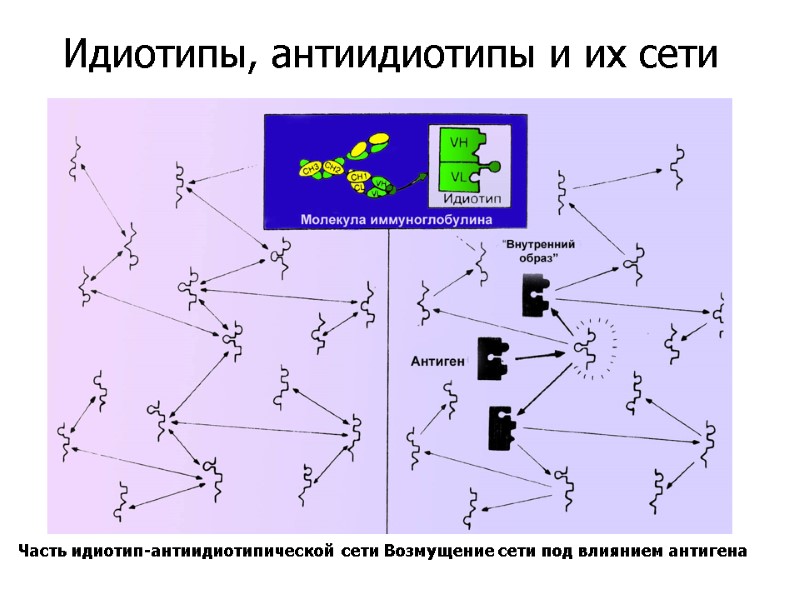
 Часть идиотип-антиидиотипической сети Возмущение сети под влиянием антигена Идиотипы, антиидиотипы и их сети
Часть идиотип-антиидиотипической сети Возмущение сети под влиянием антигена Идиотипы, антиидиотипы и их сети
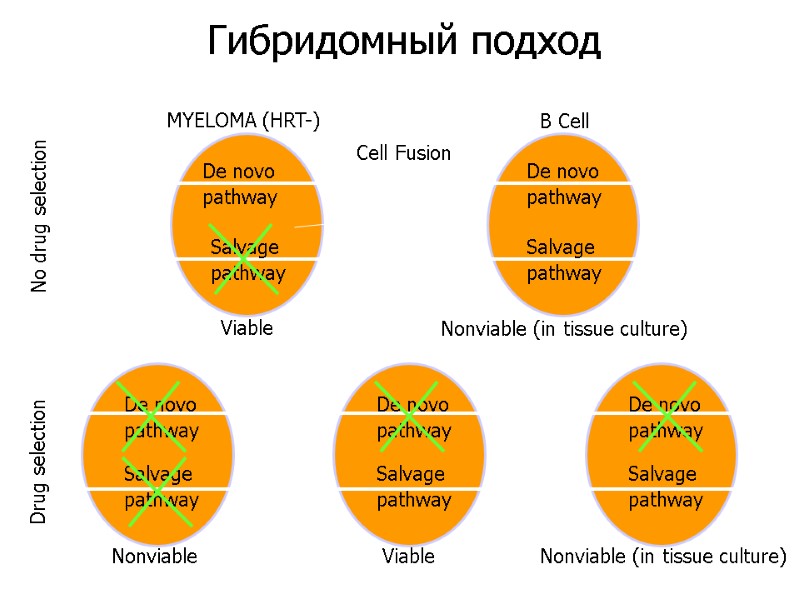
 MYELOMA (HRT-) B Cell No drug selection Drug selection De novo pathway De novo pathway Salvage pathway De novo pathway De novo pathway De novo pathway Salvage pathway Salvage pathway Salvage pathway Salvage pathway Viable Nonviable (in tissue culture) Nonviable (in tissue culture) Nonviable Viable Cell Fusion Гибридомный подход
MYELOMA (HRT-) B Cell No drug selection Drug selection De novo pathway De novo pathway Salvage pathway De novo pathway De novo pathway De novo pathway Salvage pathway Salvage pathway Salvage pathway Salvage pathway Viable Nonviable (in tissue culture) Nonviable (in tissue culture) Nonviable Viable Cell Fusion Гибридомный подход
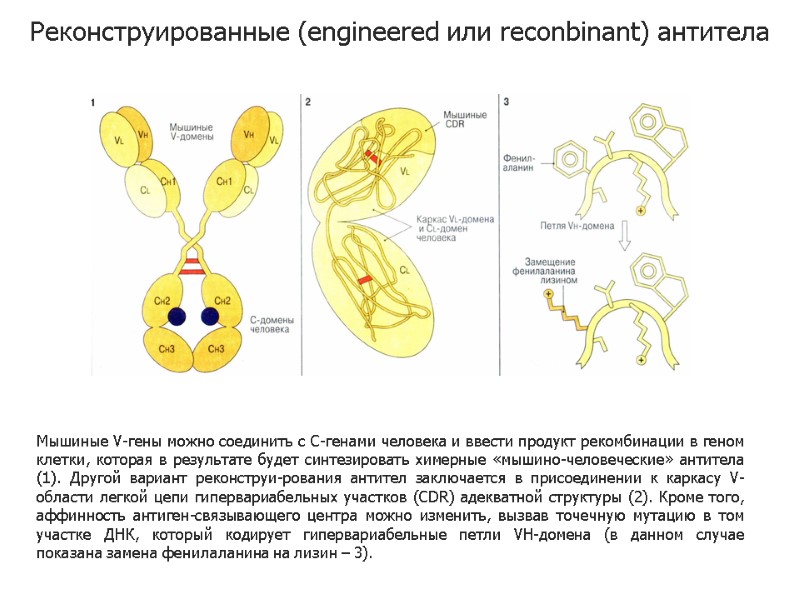
 Мышиные V-гены можно соединить с С-генами человека и ввести продукт рекомбинации в геном клетки, которая в результате будет синтезировать химерные «мышино-человеческие» антитела (1). Другой вариант реконструи-рования антител заключается в присоединении к каркасу V-области легкой цепи гипервариабельных участков (CDR) адекватной структуры (2). Кроме того, аффинность антиген-связывающего центра можно изменить, вызвав точечную мутацию в том участке ДНК, который кодирует гипервариабельные петли VH-домена (в данном случае показана замена фенилаланина на лизин – 3). Реконструированные (engineered или reconbinant) антитела
Мышиные V-гены можно соединить с С-генами человека и ввести продукт рекомбинации в геном клетки, которая в результате будет синтезировать химерные «мышино-человеческие» антитела (1). Другой вариант реконструи-рования антител заключается в присоединении к каркасу V-области легкой цепи гипервариабельных участков (CDR) адекватной структуры (2). Кроме того, аффинность антиген-связывающего центра можно изменить, вызвав точечную мутацию в том участке ДНК, который кодирует гипервариабельные петли VH-домена (в данном случае показана замена фенилаланина на лизин – 3). Реконструированные (engineered или reconbinant) антитела
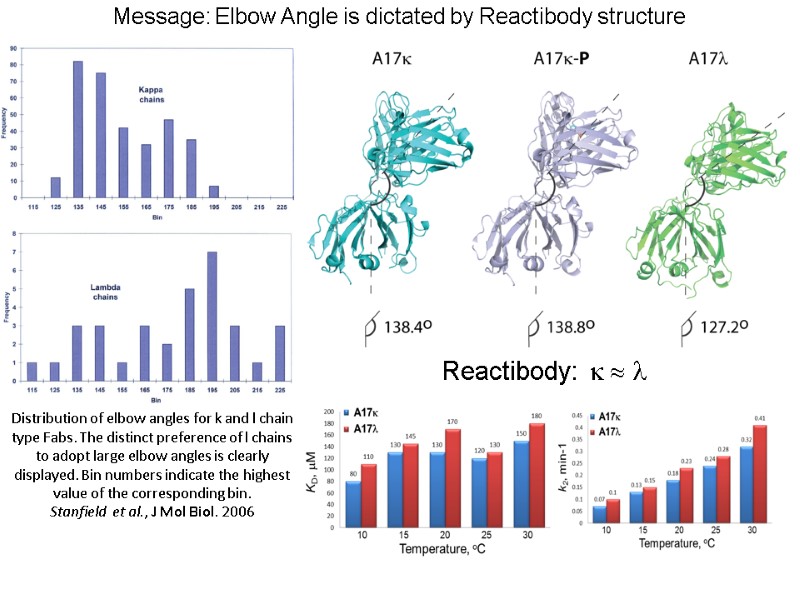
 Distribution of elbow angles for k and l chain type Fabs. The distinct preference of l chains to adopt large elbow angles is clearly displayed. Bin numbers indicate the highest value of the corresponding bin. Stanfield et al., J Mol Biol. 2006 Message: Elbow Angle is dictated by Reactibody structure Reactibody: k l
Distribution of elbow angles for k and l chain type Fabs. The distinct preference of l chains to adopt large elbow angles is clearly displayed. Bin numbers indicate the highest value of the corresponding bin. Stanfield et al., J Mol Biol. 2006 Message: Elbow Angle is dictated by Reactibody structure Reactibody: k l
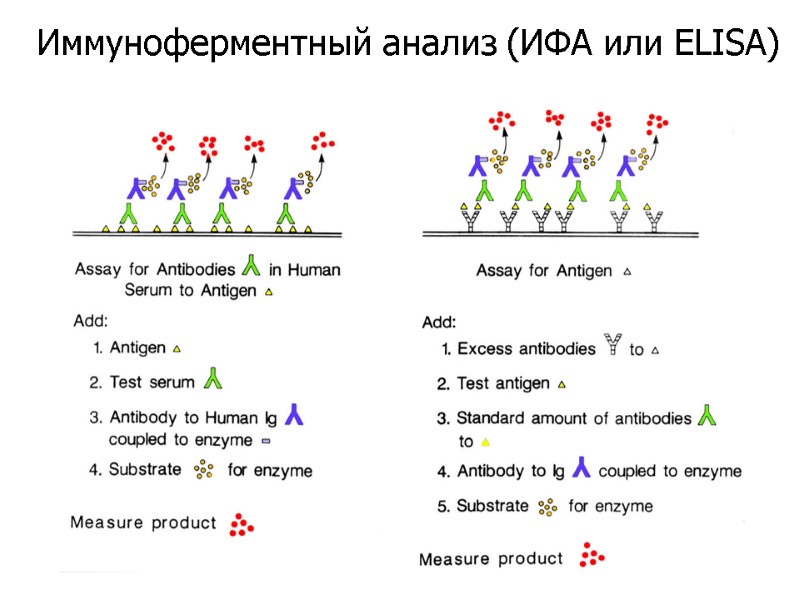
 Иммуноферментный анализ (ИФА или ELISA)
Иммуноферментный анализ (ИФА или ELISA)

