02. Белки, строение.ppt
- Количество слайдов: 28

Глава I. Химический состав клетки Тема: «Строение белков» Задачи: Изучить особенности строения белков, их свойства и функции Пименов А. В.

«Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, причем с прекращением этого обмена веществ прекращается и жизнь, что приводит к разложению белка» . Ф. Энгельс «Живые тела, существующие на Земле, представляют собой открытые, саморегулирующиеся и самовоспроизводящиеся системы, построенными из биополимеров – белков и нуклеиновых кислот» . М. В. Волькенштейн

Общая характеристика белков Из органических веществ клетки по количеству и значению на первом месте стоят белки (10 -20% от массы клетки). В состав белков входят: С, Н, О, N, S. Часть белков образует комплексы с другими молекулами, содержащими фосфор, железо, цинк и медь. Белки обладают огромной молекулярной массой: молекулярная масса альбумина (одного из белков яйца) — 36000, гемоглобина — 152000, миозина (одного из белков мышц) — 500000. Для сравнения: молекулярная масса спирта — 46, уксусной кислоты — 60, бензола — 78. Белки — высокомолекулярные органические вещества, состоящие из остатков α-аминокислот. Белки являются непериодическими полимерами, мономерами которых являются аминокислоты. В клетках и тканях обнаружено свыше 170 различных аминокислот, но в состав белков входит лишь 26.

Общая характеристика белков Причем 6 из 26 аминокислот являются нестандартными. Они образуются в результате модификации стандартных аминокислот уже после их включения в полипептидную цепь. Поэтому обычными компонентами белков считают лишь 20 aльфа -аминокислот. В зависимости от того, могут ли аминокислоты синтезироваться в организме, различают: заменимые аминокислоты — десять аминокислот, синтезируемых в организме; незаменимые аминокислоты, которые в организме не синтезируются. Незаменимые аминокислоты должны поступать в организм вместе с пищей.
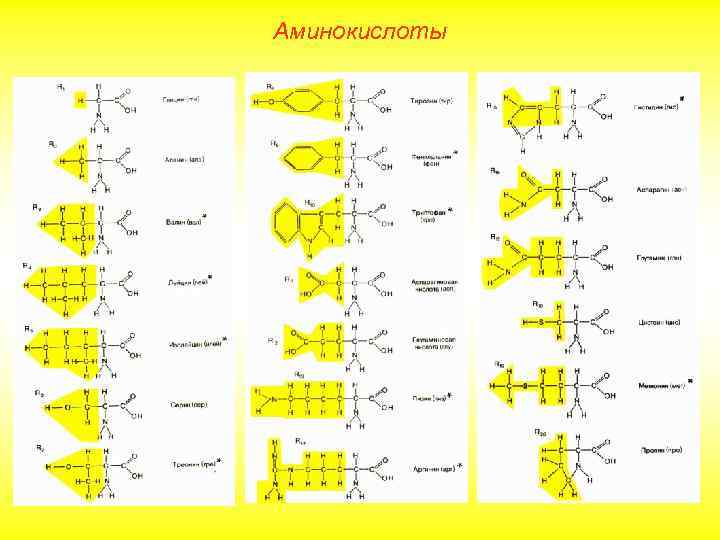
Аминокислоты

Аминокислоты В зависимости от аминокислотного состава, белки бывают: полноценными, если содержат весь набор незаменимых аминокислот; неполноценными, если хотя бы одна незаменимая аминокислота в их составе отсутствует. Различают простые белки — белки, состоящие только из аминокислот (фибрин, трипсин) и сложные — белки, содержащие помимо аминокислот еще и небелковую — простетическую группу. Она может быть представлена ионами металлов (металлопротеины — гемоглобин), углеводами (гликопротеины), липидами (липопротеины), нуклеиновыми кислотами (нуклеопротеины).
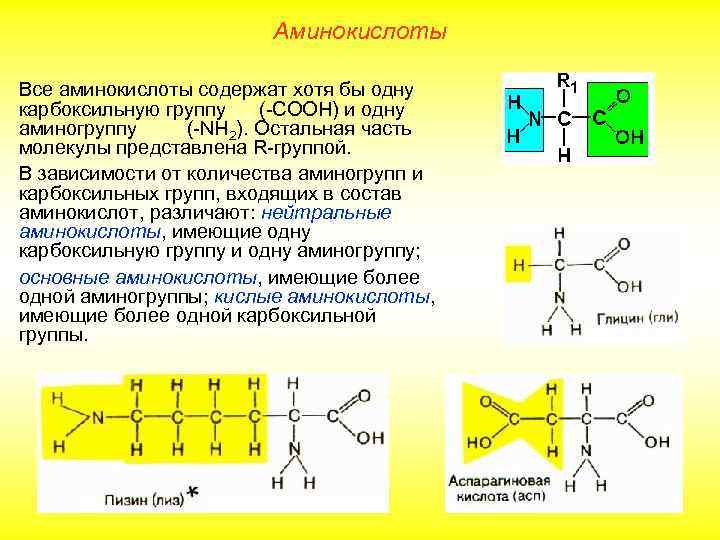
Аминокислоты Все аминокислоты содержат хотя бы одну карбоксильную группу (-СООН) и одну аминогруппу (-NH 2). Остальная часть молекулы представлена R-группой. В зависимости от количества аминогрупп и карбоксильных групп, входящих в состав аминокислот, различают: нейтральные аминокислоты, имеющие одну карбоксильную группу и одну аминогруппу; основные аминокислоты, имеющие более одной аминогруппы; кислые аминокислоты, имеющие более одной карбоксильной группы.
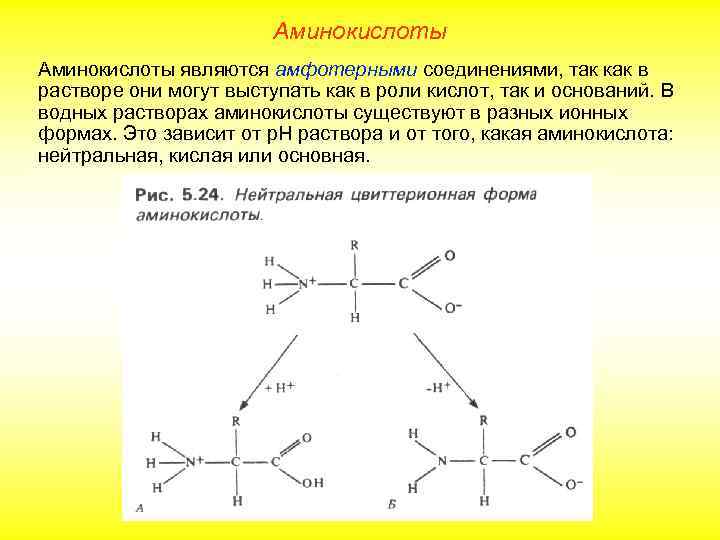
Аминокислоты являются амфотерными соединениями, так как в растворе они могут выступать как в роли кислот, так и оснований. В водных растворах аминокислоты существуют в разных ионных формах. Это зависит от р. Н раствора и от того, какая аминокислота: нейтральная, кислая или основная.

Аминокислоты Нейтральные аминокислоты? Основные аминокислоты? Кислые аминокислоты? Серусодержащие аминокислоты?
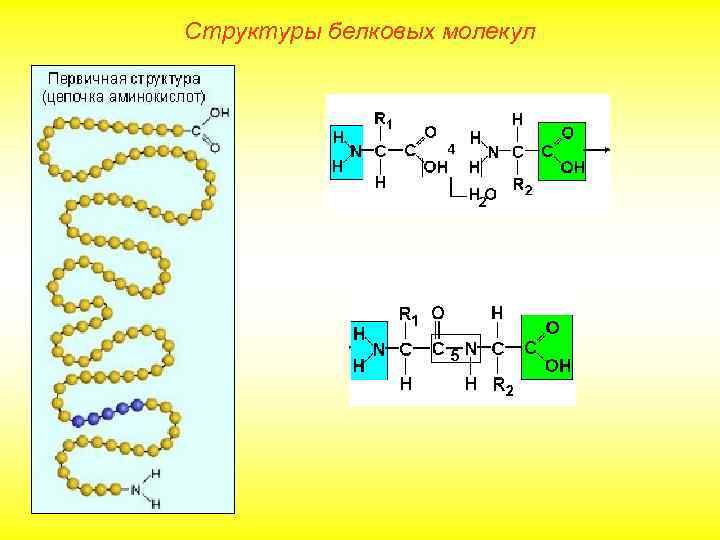
Структуры белковых молекул
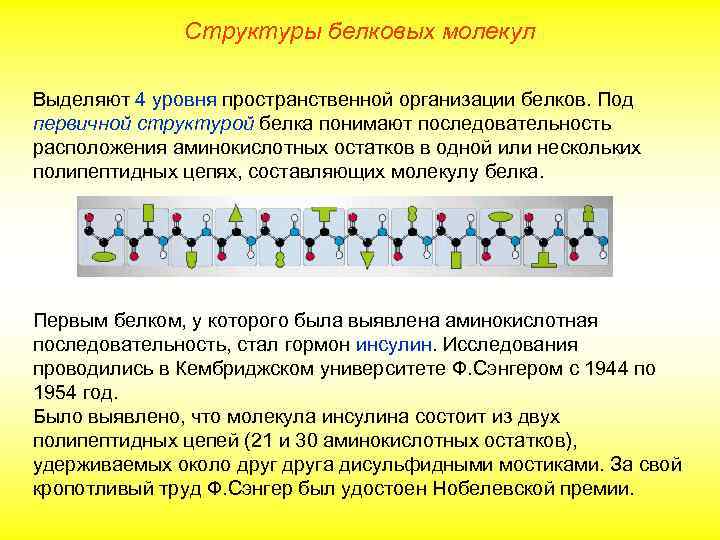
Структуры белковых молекул Выделяют 4 уровня пространственной организации белков. Под первичной структурой белка понимают последовательность расположения аминокислотных остатков в одной или нескольких полипептидных цепях, составляющих молекулу белка. Первым белком, у которого была выявлена аминокислотная последовательность, стал гормон инсулин. Исследования проводились в Кембриджском университете Ф. Сэнгером с 1944 по 1954 год. Было выявлено, что молекула инсулина состоит из двух полипептидных цепей (21 и 30 аминокислотных остатков), удерживаемых около друга дисульфидными мостиками. За свой кропотливый труд Ф. Сэнгер был удостоен Нобелевской премии.

Структуры белковых молекул В организме человека обнаружено порядка 10 тыс. различных белков. Имея всего лишь 20 аминокислот, можно составить из них огромное количество самых разнообразных комбинаций. Так, если молекула белка состоит всего из 10 аминокислотных остатков, то число теоретически возможных вариантов белковых молекул, отличающихся порядком чередования аминокислот, — 2010. Белки же, выделенные из живых организмов, образованы сотнями, а иногда и тысячами аминокислотных остатков. Первичная структура белковой молекулы определяет свойства молекул белка и ее пространственную конфигурацию. Замена всего лишь одной аминокислоты на другую в полипептидной цепочке может привести к изменению свойств и функций белка.

Олимпиадникам Лишь незначительное количество белков имеет строго линейную структуру. Основная масса белков подвергается дальнейшей укладке, фолдингу, сворачиванию пептидной цепи в правильную трехмерную структуру. Если белок состоит из нескольких субъединиц, то фолдинг включает и объединение последних в единую макромолекулу. Вспомогательные белки фолдинга можноо разделить на две группы – фолдазы и молекулярные шапероны (шаперон – пожилая дама, сопровождающая молодую девушку на балах). К ферментам фолдинга относится, например, протеиндисульфидизомераза (ПДИ), которая катализирует образование таких дисульфидных связей, которые соответствуют наиболее оптимальной пространственной структуре.

Олимпиадникам Шапероны отвечают за несколько функций: - обеспечение правильного фолдинга; - обеспечивают рефолдинг (ренатурацию), и устойчивость белков, причем синтез шаперонов значительно возрастает, если клетка долго пребывает в стрессовых условиях. Например, если клетки содержать при температуре 42º, то резко возрастает количество белков теплового шока (HSP, heat shock protein), которые являются шаперонами; - отвечают за транспорт старых белков в лизосомы, в митохондрии переносят новосинтезированные белки в развернутом состоянии, предупреждают преждевременный фолдинг. Митохондриальные шапероны принимают «гостей» и помогают им принять нативную форму.

Олимпиадникам Прионы как антишапероны Существует группа заболеваний, обусловленных неправильным фолдингом определенных белков. Такой белок называется прионом, не способен выполнять свои функции и самое плохое в том, что он вызывает неправильный фолдинг и «правильных» форм. Более того, это процесс автокаталитический, испорченный белок начинает портить очередные порции образовавшегося белка, процесс протекает несколько лет, но заканчивается смертью животного или человека. Прионы отличает устойчивость к протеазам и отдельным молекулам удается проникнуть в неизменном виде из желудочно-кишечного тракта в нервную ткань. Это единственный известный случай, когда инфекционный агент лишен нуклеиновой кислоты.

Олимпиадникам У коров прионы вызывают губчатую энцефалопатию – коровье бешенство. Употребление такого мяса человеком вызывает болезнь Крейнцфельда-Якоба. У туземцев Новой Гвинеи известна болезнь куру, считается, что куру передается при каннибализме. У овец развивается почесуха, что заставляет животных все время чесаться о твердые предметы. Литература: Молекулярная биология Мушкамбарова, Кузнецова

Повторение олимпиадникам: Фолдинг – Формирование нативной структуры белка Фолдаза ПДИ – протеиндисульфидизомераза (ПДИ), катализирует образование таких дисульфидных связей, которые соответствуют наиболее оптимальной пространственной структуре. Шапероны – белки теплового шока – обеспечивают рефолдинг (ренатурацию) и устойчивость белков, причем синтез шаперонов значительно возрастает, если клетка долго пребывает в стрессовых условиях. Прионы – белки с неправильным фолдингом, не способны выполнять свои функции и вызывающие неправильный фолдинг вновь образующихся белков.
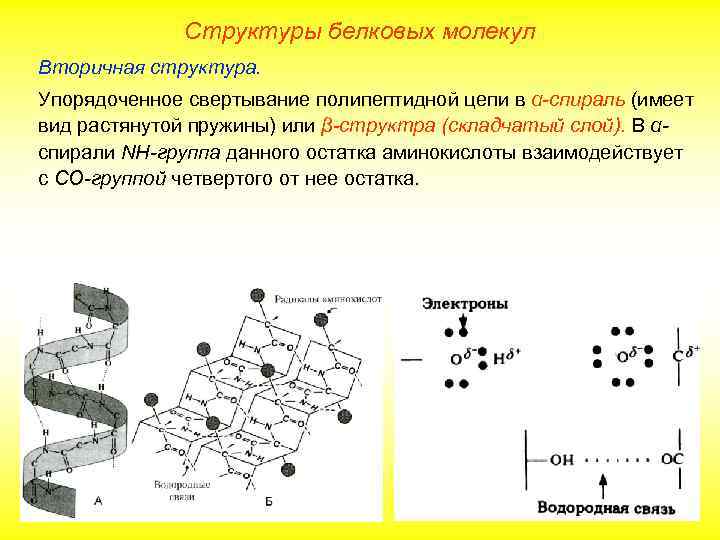
Структуры белковых молекул Вторичная структура. Упорядоченное свертывание полипептидной цепи в α-спираль (имеет вид растянутой пружины) или β-структра (складчатый слой). В αспирали NH-группа данного остатка аминокислоты взаимодействует с СО-группой четвертого от нее остатка.
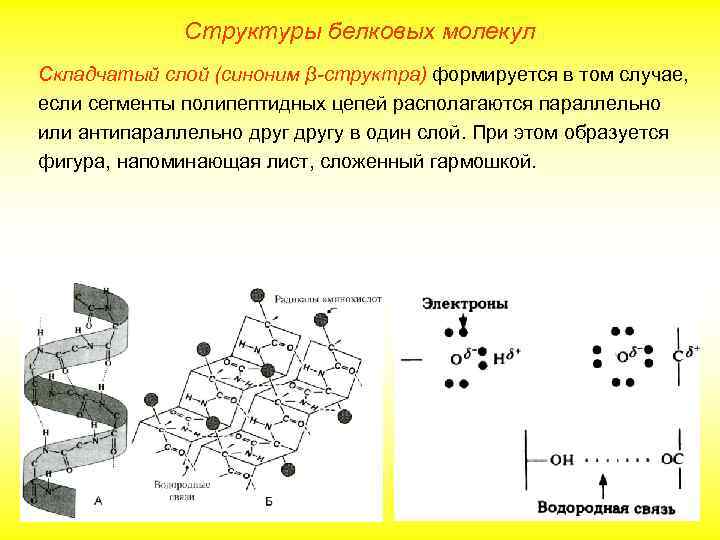
Структуры белковых молекул Cкладчатый слой (синоним β-структра) формируется в том случае, если сегменты полипептидных цепей располагаются параллельно или антипараллельно другу в один слой. При этом образуется фигура, напоминающая лист, сложенный гармошкой.
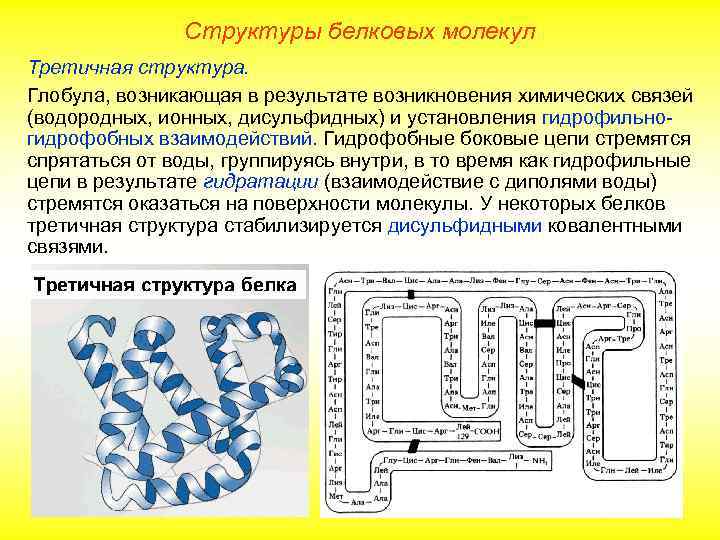
Структуры белковых молекул Третичная структура. Глобула, возникающая в результате возникновения химических связей (водородных, ионных, дисульфидных) и установления гидрофильногидрофобных взаимодействий. Гидрофобные боковые цепи стремятся спрятаться от воды, группируясь внутри, в то время как гидрофильные цепи в результате гидратации (взаимодействие с диполями воды) стремятся оказаться на поверхности молекулы. У некоторых белков третичная структура стабилизируется дисульфидными ковалентными связями.
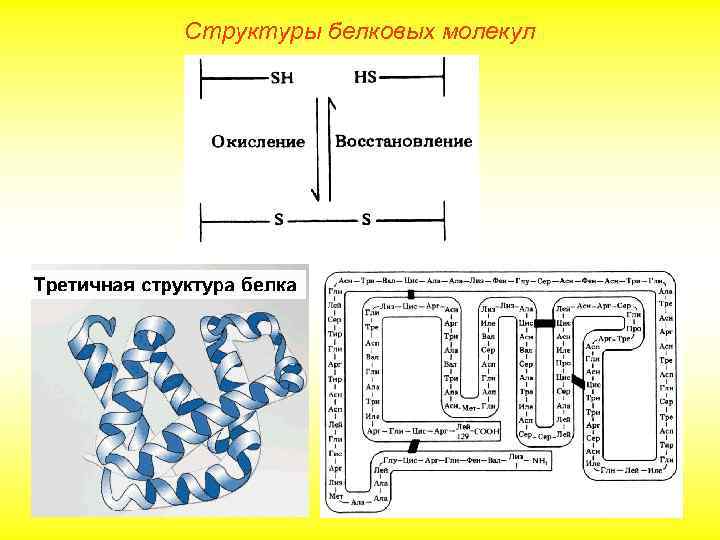
Структуры белковых молекул
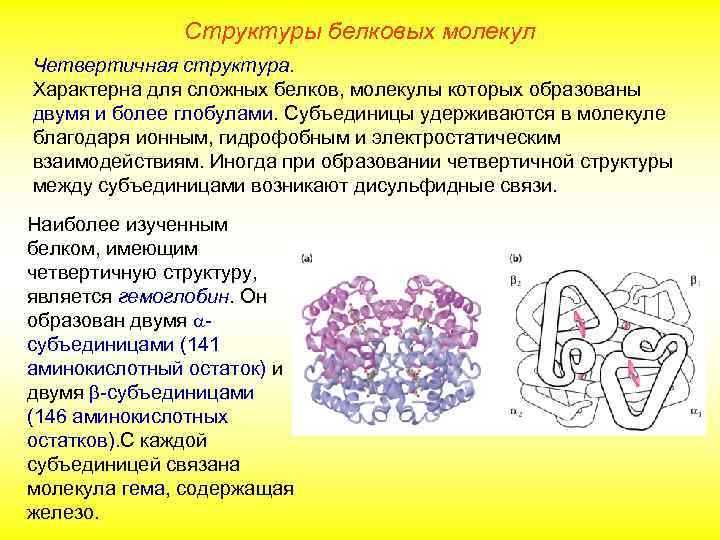
Структуры белковых молекул Четвертичная структура. Характерна для сложных белков, молекулы которых образованы двумя и более глобулами. Субъединицы удерживаются в молекуле благодаря ионным, гидрофобным и электростатическим взаимодействиям. Иногда при образовании четвертичной структуры между субъединицами возникают дисульфидные связи. Наиболее изученным белком, имеющим четвертичную структуру, является гемоглобин. Он образован двумя субъединицами (141 аминокислотный остаток) и двумя -субъединицами (146 аминокислотных остатков). С каждой субъединицей связана молекула гема, содержащая железо.
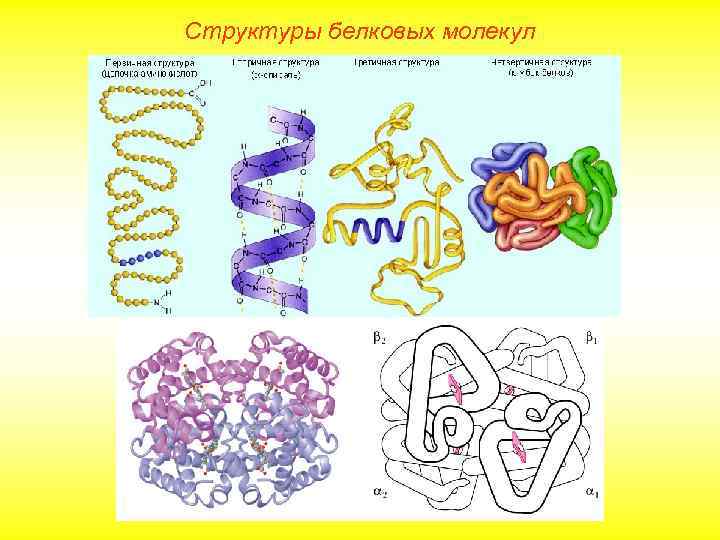
Структуры белковых молекул
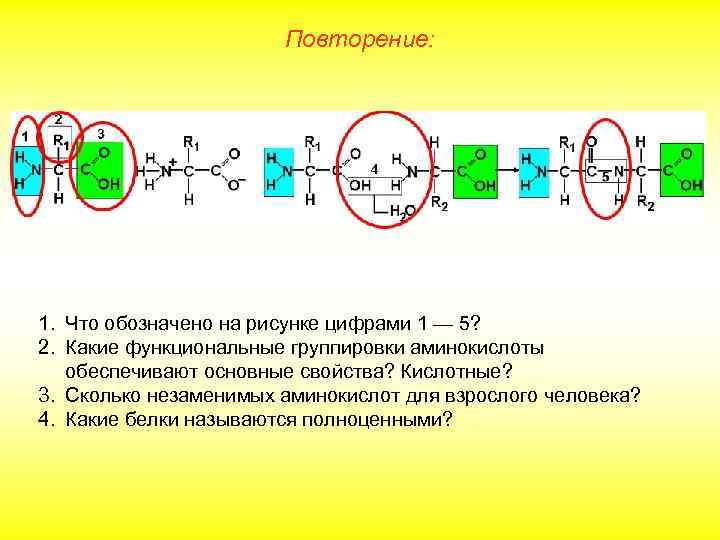
Повторение: 1. Что обозначено на рисунке цифрами 1 — 5? 2. Какие функциональные группировки аминокислоты обеспечивают основные свойства? Кислотные? 3. Сколько незаменимых аминокислот для взрослого человека? 4. Какие белки называются полноценными?

Повторение: Тест 1. На первом месте по массе из органических веществ в клетке находятся: 1. Углеводы. 2. Белки. 3. Липиды. 4. Нуклеиновые кислоты. **Тест 2. В состав простых белков входят следующие элементы: 1. Углерод. 5. Фосфор. 2. Водород. 6. Азот. 3. Кислород. 7. Железо. 4. Сера. 8. Хлор. Тест 3. Количество различных стандартных аминокислот, встречающихся в белках: 1. 170. 2. 26. 3. 20. 4. 10.

Повторение: **Тест 4. Количество незаменимых для человека аминокислот: 1. Таких аминокислот нет. 2. 20. 3. 10. 4. 7. **Тест 5. Неполноценные белки — белки: 1. В которых отсутствуют некоторые аминокислоты. 2. В которых отсутствуют некоторые незаменимые аминокислоты. 3. В которых отсутствуют некоторые заменимые аминокислоты. 4. Все известные белки являются полноценными. Тест 6. Придают аминокислотам свойства: 1. Кислые — радикал, щелочные — аминогруппа. 2. Кислые — аминогруппа, щелочные — радикал. 3. Кислые — карбоксильная группа, — щелочные — радикал. 4. Кислые — карбоксильная группа, щелочные — аминогруппа.

Повторение: Тест 7. Пептидная связь образуется в результате: 1. Реакции гидролиза. 2. Реакции гидратации. 3. Реакции конденсации. 4. Все выше перечисленные реакции могут привести к образованию пептидной связи. Тест 8. Пептидная связь образуется: 1. Между карбоксильными группами соседних аминокислот. 2. Между аминогруппами соседних аминокислот. 3. Между аминогруппой одной аминокислоты и радикалом другой. 4. Между аминогруппой одной аминокислоты и карбоксильной группой другой. **Тест 9. Вторичную структуру белков стабилизируют: 1. Ковалентные. 2. Водородные. 3. Ионные. 4. Такие связи отсутствуют.

Повторение: **Тест 10. Третичную структуру белков стабилизируют: 1. Ковалентные. 2. Водородные. 3. Ионные. 4. Гидрофильно-гидрофобное взаимодействие. 5. Все выше перечисленные виды связей.
02. Белки, строение.ppt