Глава 10. 2009 Биологические наноструктуры.ppt
- Количество слайдов: 68

Глава 10 «Нано» размеры биологических структур. РНК - природный ассемблер. Биологические мембраны. Биомиметики. Липосомы. Везикулы. Мембранный транспорт.

10. 1
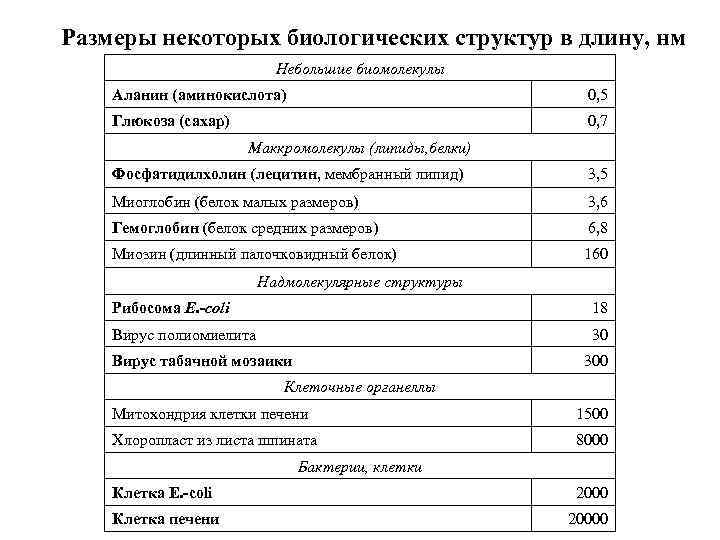
Размеры некоторых биологических структур в длину, нм Небольшие биомолекулы Аланин (аминокислота) 0, 5 Глюкоза (сахар) 0, 7 Маккромолекулы (липиды, белки) Фосфатидилхолин (лецитин, мембранный липид) 3, 5 Миоглобин (белок малых размеров) 3, 6 Гемоглобин (белок средних размеров) 6, 8 Миозин (длинный палочковидный белок) 160 Надмолекулярные структуры Рибосома E. -coli 18 Вирус полиомиелита 30 Вирус табачной мозаики 300 Клеточные органеллы Митохондрия клетки печени 1500 Хлоропласт из листа шпината 8000 Бактерии, клетки Клетка E. -coli 2000 Клетка печени 20000
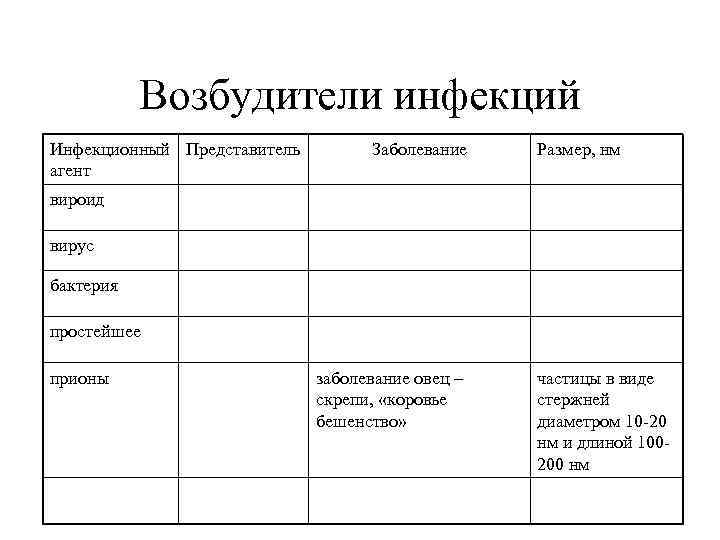
Возбудители инфекций Инфекционный Представитель агент Заболевание Размер, нм вироид вирус бактерия простейшее прионы заболевание овец – скрепи, «коровье бешенство» частицы в виде стержней диаметром 10 -20 нм и длиной 100200 нм

Прионы Американский биохимик С. Прузинер получил в 1997 г. Нобелевскую премию «за открытие прионов - нового биологического принципа инфекций» . Прионы – (от англ. proteinaceous infectious particles) белковоподобная инфекционная частица, белок - Рr. P (от англ. prion protein). По современной классификации, к заболеваниям, вызываемым прионами, относятся четыре болезни человека и шесть – животных. Своеобразие этих медленных болезней проявляется в избирательном поражении центральной нервной системы, что неуклонно приводит к губкообразному состоянию серого и/или белого вещества головного и спинного мозга при отсутствии воспалительной реакции. Напр. , scrapie (англ. ) - название наиболее распространенной в природе прионной инфекции овец и коз. При изучении прионов, выделенных из головного мозга зараженных скрепи животных, были обнаружены частицы в виде стержней диаметром 10 -20 нм и длиной 100 -200 нм. По ультраструктуре они напоминали амилоид (аномальный белок, который обычно образуется при хронических заболеваниях, например туберкулезе легких, костей и т. д. ) и, видимо, представляли собой полимерную форму приона: каждый стержень содержал около тысячи молекул приона.

Общая схема биосинтеза белков в клетке (ДНК - РНК белок) 1. Транскрипция 2. Процессинг и транспорт 4. Трансляция 3. Активация и акцептирование аминокислот 5. Формирование функционального белка

Транскрипция Отдельные участки двутяжевой ДНК, называемые генами, являются матрицами для синтеза на них однотяжевых цепей РНК.
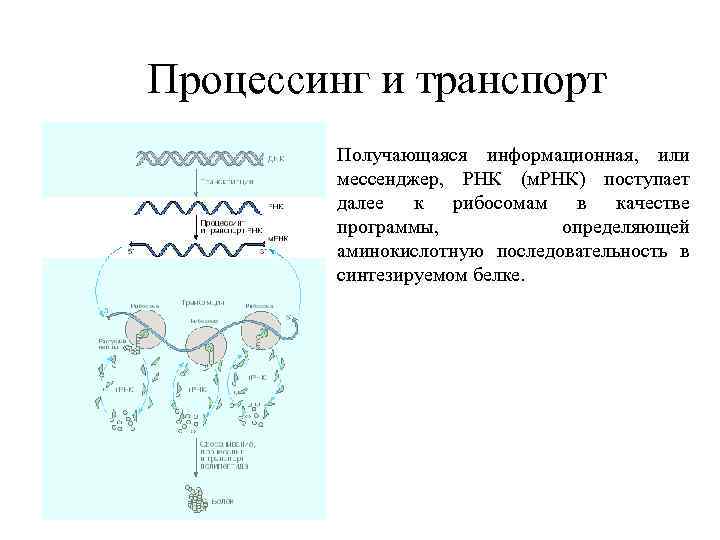
Процессинг и транспорт Получающаяся информационная, или мессенджер, РНК (м. РНК) поступает далее к рибосомам в качестве программы, определяющей аминокислотную последовательность в синтезируемом белке.
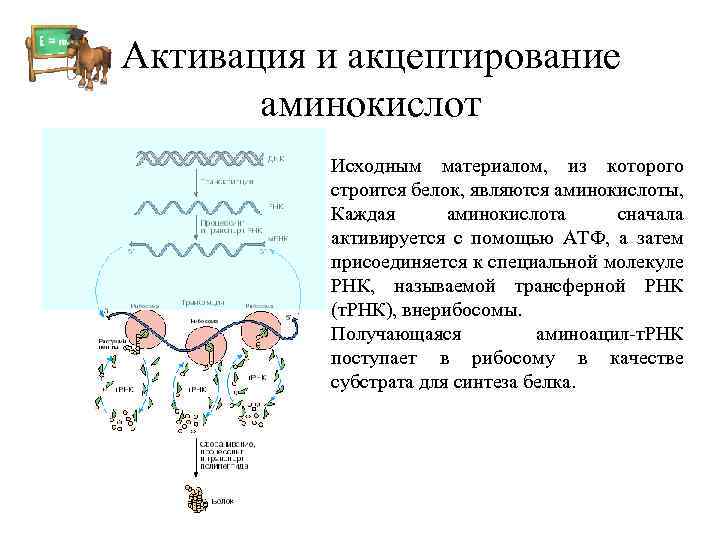
Активация и акцептирование аминокислот Исходным материалом, из которого строится белок, являются аминокислоты, Каждая аминокислота сначала активируется с помощью АТФ, а затем присоединяется к специальной молекуле РНК, называемой трансферной РНК (т. РНК), внерибосомы. Получающаяся аминоацил-т. РНК поступает в рибосому в качестве субстрата для синтеза белка.

Трансляция Каждая рибосома последовательно сканирует цепь м. РНК (движется вдоль нее от одного конца к другому) и соответственно выбирает из среды те аминоацилт. РНК, которые соответствуют (комплементарны) триплетным комбинациям нуклеотидов, находящимся в данный момент в рибосоме. Аминокислотный остаток выбранной аминоацил-т. РНК каждый раз ковалентно присоединяется рибосомой к растущей полипептидной цепи, а деацилированная т. РНК освобождается из рибосомы в раствор. Так последовательно остаток за остатком строится полипептидная цепь.
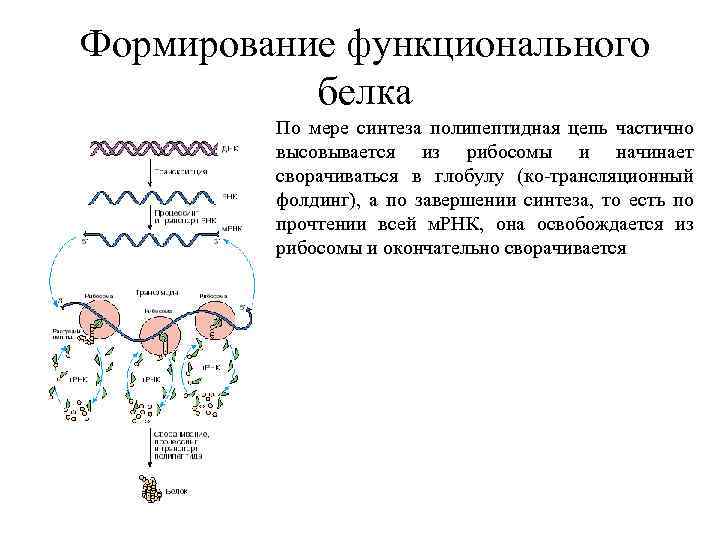
Формирование функционального белка По мере синтеза полипептидная цепь частично высовывается из рибосомы и начинает сворачиваться в глобулу (ко-трансляционный фолдинг), а по завершении синтеза, то есть по прочтении всей м. РНК, она освобождается из рибосомы и окончательно сворачивается

Биомиметики • БИОМИМЕТИКИ - материалы, структурно или химически аналогичные растительным или животным тканям, которые могут служить компонентами человеческих тканей. • Бионика,

Biological Templated Synthesis of Water. Soluble Conductive Polymeric Nanowires Биологические частицы как каркас в химии и материаловедении One-dimensional (1 D) conductive nanowire is one of the most important components for the development of nanosized electronic devices, sensors, and energy storage units. With the rod-like tobacco mosaic virus as the template, 1 D-conducting polyaniline and polypyrrole nanowires can be readily prepared via a hierarchical assembly process. Длинный проводящий нанопровод из полианилина/ВТМ (> 300 нм, больше чем длина начальной частицы ВТМ) может быть сформирован иерархической сборкой. Проводящая наноструна из полианилин/ВТМ может быть приготовлена, нарпимер, выдержкой ВТМ, анилина, полисульфированного стирола и персульфата аммония при комнатной температуре. Zhongwei Niu, Nano Lett. , 2007, 7 (12), pp 3729– 3733

The fabrication of subwavelength antireflective nanostructures using a bio-template СЭМ изображения наноструктур на крыле цикады (а) и готовые ПММА пленки (б) Nanotechnology 19 (2008) 095605 (5 pp)

Biomimetic coating of carbon nanotubes (CNTs) with synthetic glycopolymers Chen, X. ; J. Am. Chem. Soc. 2006, 128, 6292 -3

10. 2

Липидный бислой • ЛИПИДНЫЙ БИСЛОЙ (бимолекулярный липидный слой), термодинамически выгодная форма ассоциации мн. полярных липидов в водной среде, при к-рой молекулы липидов ориентированы таким образом, что их полярные головки обращены в сторону водной фазы и формируют две гидрофильные поверхности, а углеводородные цепи расположены приблизительно под прямым углом к этим пов-стям и образуют между ними гидрофобную область. 1 - полярная головка молекулы; 2 - углеводородная цепь.

Свойства липидного бислоя • Л. б. - основа мол. организации мембран биологических. • Легко формируется липидами, у к-рых невелики различия между площадью поперечного сечения головки и углеводородных цепей. Это свойственно большинству фосфолипидов биол. мембран. • Характерный признак липидов, образующих Л. б. , - низкая величина критич. концентрации мицеллообразования (ок. 10 -10 М). • Толщина Л. б. определяется прежде всего длиной углеводородных цепей и обычно находится в пределах 4 -5 нм. • Присутствие в цепях цис-двойных связей, боковых метильных групп и др. заместителей нарушает плотность упаковки молекул и приводит к уменьшению толщины бислоя. • В зависимости от т-ры Л. б. может находиться в двух состояниях - кристаллическом (гелевом) и жидкокристаллическом

Фазовые переходы в бислое • Переход из одного состояния в другое связан с плавлением углеводородной фазы бислоя и происходит при строго определенной т-ре (Тф. п. ), характерной для каждого липида. • Наиболее высокой Тф. п. обладают липиды с неразветвленными насыщенными углеводородными цепями. Наличие заместителей и особенно цис-двойных связей в углеводородных цепях понижает Тф. п. . • Ниже Тф. п. углеводородные цепи липидных молекул имеют максимально вытянутую трансоидную конформацию, плотно упакованы и обладают ограниченной подвижностью. • Плавление углеводородной фазы сопровождается резким усилением подвижности цепей в результате их транс-, гошизомеризации. Вследствие близкого расположения в бислое соседних цепей, препятствующих свободному вращению вокруг связей С—С, изомеризация происходит в виде сопряженных поворотов в смежных звеньях углеводородных цепей.

Дифузия липидов в бислое • В жидкокристаллич. состоянии липидные молекулы способны легко мигрировать вдоль пов-сти бислоя. Коэф. латеральной диффузии липидов лежит в пределах 10 -7 -10 -9 см 2/с. При переходе бислоя в гелевое состояние скорость такой диффузии резко падает. • Миграция липидных молекул с одной стороны бислоя на другую (т. наз. флип-флоп) происходит медленно. Полупериод флип-флопа составляет неск. часов или даже дней, что обусловлено необходимостью преодоления высокого энергетич. барьера при переносе полярной головки липидной молекулы через гидрофобную область бислоя.

Распределение липидов в бислое • Распределение молекул в плоскости Л. б. может быть неоднородным и зависит от состава липидов, фазового состояния, а также присутствия мембраноактивных вв. • Такое распределение, приводящее к образованию липидных доменов (кластеров) разного состава, происходит, если липиды различаются по структуре полярных головок, углеводородные цепи отличаются по длине более чем на две метиленовые группы и имеют разную степень ненасыщенности. • Распределение липидов между сторонами бислоя также м. б. неодинаковым и зависит от его кривизны, соотношения размеров полярных и неполярных частей липидной молекулы, ее заряда и др.
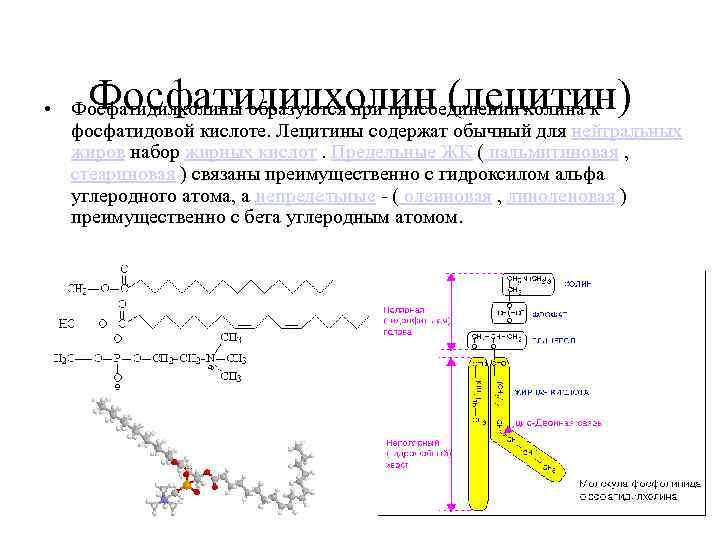
Фосфатидилхолин (лецитин) • Фосфатидилхолины образуются присоединении холина к фосфатидовой кислоте. Лецитины содержат обычный для нейтральных жиров набор жирных кислот. Предельные ЖК ( пальмитиновая , стеариновая ) связаны преимущественно с гидроксилом альфа углеродного атома, а непредельные - ( олеиновая , линоленовая ) преимущественно с бета углеродным атомом.

Липосомы • Липосомы (липо- + греч. soma тело) - искусственно получаемые сферические (полые) частицы диаметром менее 10 мкм. образованные из бимолекулярного слоя липидов • Они относятся к обширному семейству везикулярных (пузырьковых) структур, образуемых амфифильными молекулами. • Липосомы - от греч. липос (жир) и сома (тельце, частица).

Липосомы образуются фосфолипидами (но не только) • Фосфолипиды, являющиеся основными компонентами клеточных мембран, способны самопроизвольно образовывать в воде замкнутые мембранные оболочки, липосомы. • Эти оболочки захватывают в себя часть окружающего водного раствора, а образующая их фосфолипидная мембрана обладает свойствами полупроницаемого барьера, легко пропускающего воду, но препятствующего диффузии растворенных в ней веществ.

История липосом • В середине 60 -х годов 20 столетия английский ученый Алек Бэнгхем, выясняя роль фосфолипидов в свертывании крови, изучал структуру коллоидных дисперсий, образующихся при набухании фосфолипидов в избытке воды. • На электронных микрофотографиях он увидел слоистые частицы, удивительно похожие на мембранные структуры клетки. • Bangham A. D. , Horne R. W. Negative Staining of Phospholipids and their Structured Modification by Surface Agents as Observed in the Electron Microscope // J. Mol. Biol. 1964. Vol. 8. P. 660 -668. • Так впервые было установлено, что фосфолипиды, являющиеся основными компонентами клеточных мембран, способны самопроизвольно образовывать в воде замкнутые мембранные оболочки.

Захват раствора внутрь липосом • Следующее исследование показало, что неорганические ионы, присутствующие в растворе в момент набухания фосфолипидов, включаются внутрь этих частиц и удерживаются там длительное время, обмениваясь с ионами наружного раствора с очень малой скоростью: • Bangham A. D. , Standish M. M. , Watkins J. C. Diffusion of Univalent Ions Across the Lamelae of Swollen Phospholipids // Ibid. 1965. Vol. 13. P. 238 -252. • Липидные оболочки захватывают в себя часть окружающего водного раствора, а образующая их фосфолипидная мембрана обладает свойствами полупроницаемого барьера, легко пропускающего воду, но препятствующего диффузии растворенных в ней веществ.
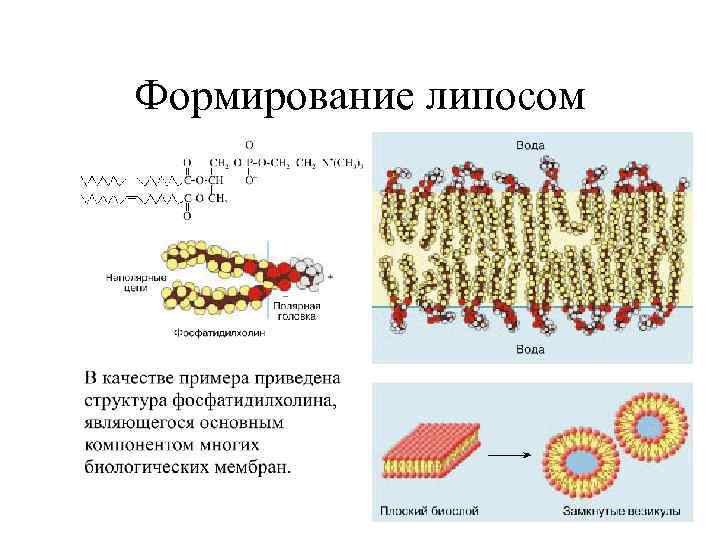
Формирование липосом

Модель биологических мембран • Первая модель строения биологических мембран была предложена в 1902 году. Овертон заметил, что через мембраны лучше всего проникают вещества, хорошо растворимые в липидах, и на основании этого предположил, что биологические мембраны состоят из тонкого слоя фосфолипидов. • На поверхности раздела полярной и неполярной сред (напр. , воды и воздуха) молекулы фосфолипидов образуют мономолекулярный (одномолекулярный) слой. Их полярные "головы" погружены в полярную среду, а неполярные "хвосты" ориентированы в сторону неполярной среды. • Поэтому предполагали, что биологические мембраны построены из монослоя липидов.

Липиды в мембране бимолекулярный слой • В 1925 году Гортер и Грендел показали, что площадь монослоя липидов, экстрагированных из мембран эритроцитов, в два раза больше суммарной площади эритроцитов. • Гортер и Грендел экстрагировали липиды из гемолизированных эритроцитов ацетоном, затем выпаривали раствор на поверхности воды и измеряли площадь образовавшейся мономолекулярной пленки липидов. • На основе результатов этих исследований было сделано предположение, что липиды в мембране располагаются в виде бимолекулярного слоя. • Это предположение подтвердили исследования электрических параметров биологических мембран (Коул и Кёртис, 1935 год): высокое электрическое сопротивление 107 Ом • м 2 и большая электроемкость 0, 5 • 10 -2 Ф/м 2.

• Модель строения биологических мембран Модель - жидкостно-мозаичная. Структурную основу составляет двойной слой фосфолипидов, инкрустированный белками. При этом различают поверхностные (периферические) и интегральные белки. • Липиды находятся при физиологических условиях в жидком агрегатном состоянии. Сравнивают мембрану с фосфолипидным морем, по которому плавают белковые "айсберги". Соотношение между белками и фосфолипидами сильно колеблется: количество белков в миелиновой мембране в 2, 5 раза меньше, чем липидов, а в митохондриях, напротив, белков в 2, 5 раза больше, чем липидов. • В мембранах животных клеток много холестерина (в сравнимом количестве с фосфолипидами и белками). Есть в мембранах другие вещества, напр. , гликолипиды, гликопротеиды. • Белковые "айсберги" не всегда свободно плавают в липидном море, а могут быть "заякорены" на внутренние (цитоплазматические) структуры клетки. К таким структурам относятся микрофиламенты и микротрубочки.

Липосомы и везикулы Часто слова "липосомы" и "липидные везикулы" используют как синонимы. Исторически липосомами впервые были названы частицы, образующиеся при механическом диспергировании взвеси набухших фосфолипидов в воде. Эти частицы являются многослойными, и потому их иногда называют мультиламеллярными везикулами. Они состоят из нескольких десятков, а то и сотен липидных бислоев, разделенных водными промежутками, и имеют довольно крупные размеры (до 50 мкм). На другом полюсе обширного липосомного семейства находятся самые маленькие везикулы (около 20 нм), образованные одним липидным бислоем и называемые малыми моноламеллярными везикулами.
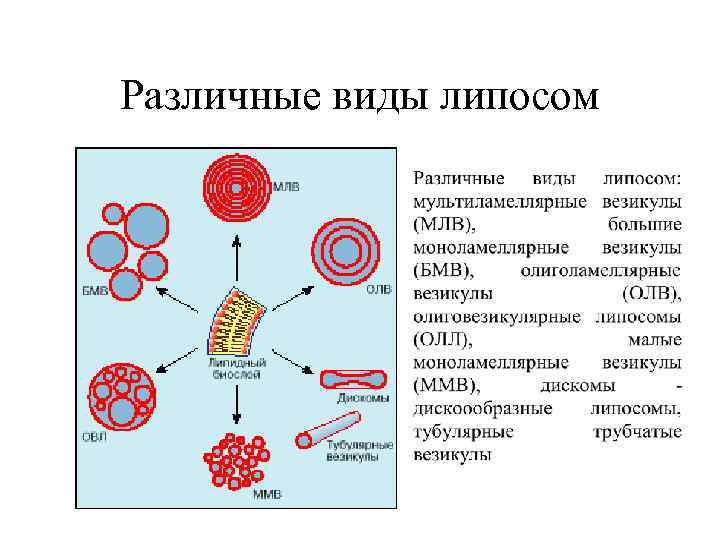
Различные виды липосом

Классификация везикул и липосом Малые моноламеллярные - 20 -50 нм Крупные моноламеллярные - 50 -200 нм и выше. Многослойные (мультиламеллярные) - диаметр до 5000 - 10000 нм, могут быть образованы десятками и даже сотнями липидных бислоев

Получение многослойных липосом • Многослойные Л. легко образуются при встряхивании водной дисперсии набухшего липида. При этом получается взвесь Л. с широким распределением частиц по размерам. • Сравнительно гомог. дисперсию Л. можно получить, пропустив их через поликарбонатные фильтры с заданным размером пор. • Расстояние между соседними липидными бислоями составляет 2 -3 нм, но может возрастать до 20 нм и более в случае заряженных бислоев. На 1 моль липида многослойные Л. содержат 1 -4 л воды. • Они обладают св-вами идеального осмометра, меняя свой объем в ответ на изменение концентрации в-в в окружающей водной среде.

Получение моноламеллярных липосом • Малые моноламеллярные Л. получают из многослойных при обработке их ультразвуком, при впрыскивании спиртового р-ра липидов в водную среду, продавливанисм под большим давлением воднолипидных дисперсий через небольшое отверстие, а также удалением детергента, солюбилизирующего липид, диализом или гель-фильтрацией. Такие Л. содержат 0, 2 -1, 5 л воды на 1 моль липида. Малые моноламеллярные Л. не обладают осмотич. активностью и не коагулируют в течение длит. времени. • Большие моноламеллярные Л. имеют значит. внутр. объем воды (8 -14 л на 1 моль липида) и обладают осмотич. активностью. Обычно их получают удалением солюбилизирующего детергента в условиях контролируемого диализа или впрыскиванием р-ра липида в легколетучем р-рителе (диэтиловый эфир, петролейный эфир, пентан) в подогретую до 60 °С воду.

Крупные однослойные липосомы • Крупные однослойные Л. могут быть также получены из малых липосом путем их слияния под действием Са 2+ или в условиях термотропного фазового перехода. • Получены также Л. , образованные липидами (или подобными молекулами), к-рые способны полимеризоваться (содержат обычно связи С—С или ). Полимеризация может осуществляться как в гидрофобной, так и в гидрофильной области бислоя и приводить к т. наз. полимерным Л. Последние отличаются от обычных Л. большей стабильностью.
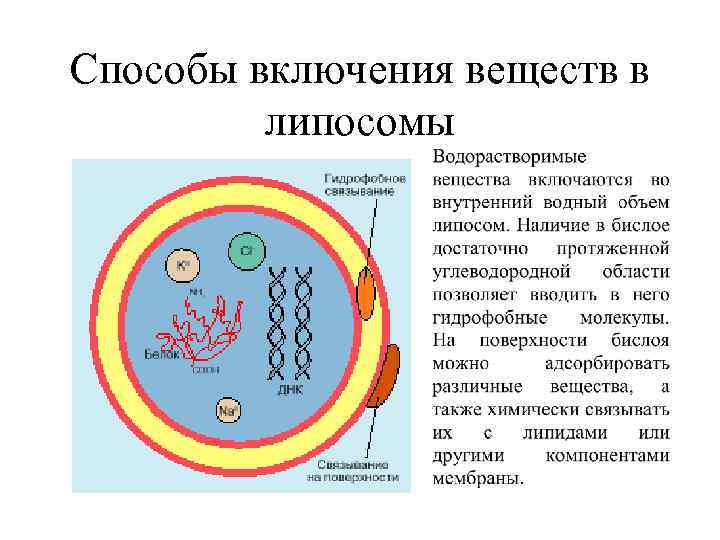
Способы включения веществ в липосомы
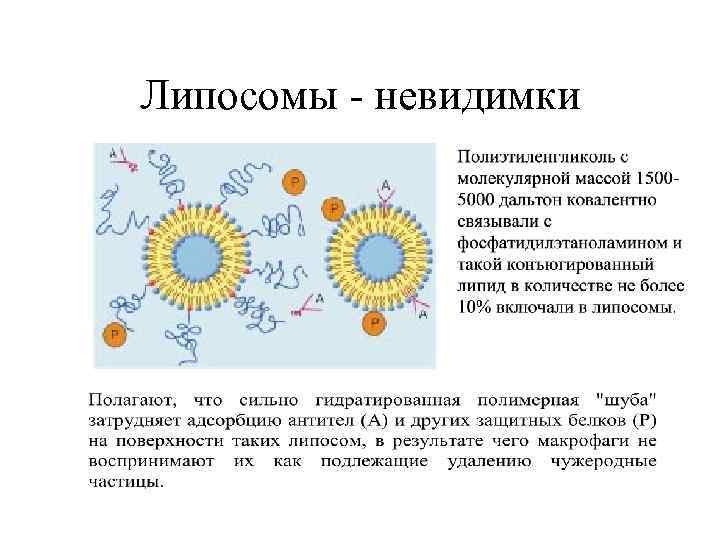
Липосомы - невидимки
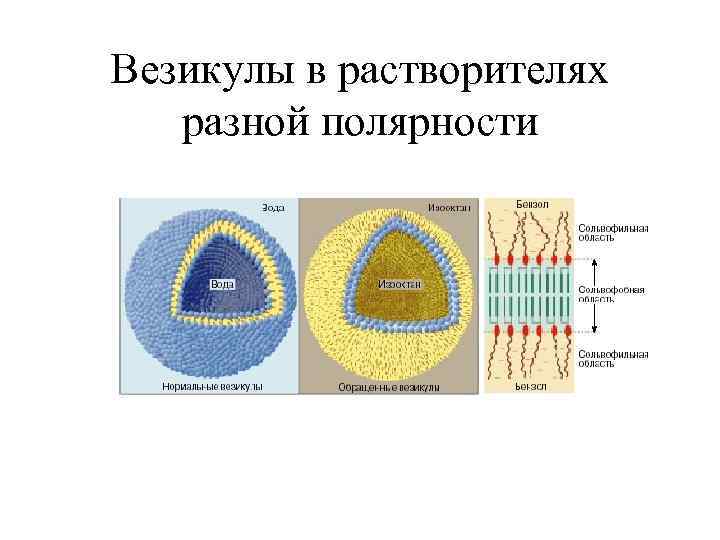
Везикулы в растворителях разной полярности

Свойства липосом и везикул • Несмотря на молекулярную толщину (около 4 нм), липидный бислой отличается исключительной механической прочностью и гибкостью. • В жидкокристаллическом состоянии бислоя его компоненты обладают высокой молекулярной подвижностью, так что в целом мембрана ведет себя как достаточно жидкая, текучая фаза. Благодаря этому липосомы сохраняют целостность при различных повреждающих воздействиях, а их мембрана обладает способностью к самозалечиванию возникающих в ней структурных дефектов. • Вместе с тем гибкость бислоя и его текучесть придают липосомам высокую пластичность. • Липосомы меняют размеры и форму при изменении осмотической концентрации внешнего водного раствора. При сильном осмотическом стрессе целостность бислоя может нарушиться и липосомы могут раздробиться на частицы меньшего размера.

Воздействие детергентов • Хотя липосомы достаточно прочны и стабильны в широком диапазоне условий, их можно легко разрушить до мицеллярного состояния с помощью поверхностно-активных веществ, относящихся к разряду детергентов (моющих средств). • Этот процесс, называемый солюбилизацией, является обратимым, и липосомы вновь формируются, если детергент удалить из мицеллярного раствора. • Самосборку мембран путем удаления солюбилизирующего детергента обычно применяют для встраивания интегральных мембранных белков в липидный бислой, называя этот процесс реконструкцией, а получаемые при этом белоксодержащие липосомы - протеолипосомами.

Липидные поры в мембране

Электрические свойства мембраны


Липосомы в фундаментальных научных исследованиях • • • Моделирование клеточных мембран. Установлены: основные закономерности транспорта веществ через мембрану, важная роль фазовых переходов в функционировании мембран, молекулярные параметры липидного бислоя и его динамические характеристики, изучены процессы слияния мембран и др. Математиков интересуют проблемы топологии двумерных поверхностей в трехмерном пространстве в связи с упругими свойствами липидного бислоя. Физиков липосомы привлекают как фрактальные системы со специфическим поведением при агрегации и богатством морфологических превращений. Для химиков бислойные везикулы интересны как микрореакторы, позволяющие проводить химические реакции в ориентированных средах с возможностью пространственного разделения реагентов и продуктов реакции посредством мембран. Специалистам в области материаловедения липосомы представляются прекрасной основой для создания новых композитных материалов с высокой биосовместимостью.

Липосомы в фармакологии и медицине • • • Многие лекарственные препараты имеют низкий терапевтический индекс. Это означает, что концентрация, в которой они оказывают лечебное действие, мало отличается от концентрации, при которой препарат становится токсичным. В других случаях лекарственный препарат при введении в организм может быстро терять активность под действием инактивирующих агентов. Включение таких препаратов в липосомы может значительно повысить их терапевтическую эффективность, поскольку, с одной стороны, препарат, находящийся в липосоме, защищен ее мембраной от действия неблагоприятных факторов, а с другой - та же мембрана не позволяет токсичному препарату превысить допустимую концентрацию в биологических жидкостях организма. Липосома в данном случае выполняет роль хранилища, из которого препарат высвобождается постепенно, в нужных дозах и в течение требуемого промежутка времени. Липосомы идеальны как переносчики лекарственных препаратов. Они делаются из природных липидов и поэтому нетоксичны, не вызывают нежелательных иммунных реакций и биодеградируемы, то есть должны разрушаться под действием обычных ферментов, присутствующих в организме.

• • • Липосомные носители Липосомы недостаточно стабильны в крови и быстро выводятся из кровотока макрофагами, которые находятся в печени, селезенке и костном мозгу. Липосомные носители обычно не удается направить в нужные органы и ткани. Естественная нацеленность макрофагов на липосомы может быть использована для их активации, что очень полезно для борьбы с вирусными, бактериальными и грибковыми инфекциями. Тот факт, что липосомы не задерживаются такими органами, как сердце, почки, мозг, а также клетками нервной системы, позволяет за счет их использования значительно снизить кардиотоксичность, нефротоксичность и нейротоксичность препаратов противораковой терапии. Прикрепление к поверхности липосом молекул, специфичных к клеткаммишеням (напр. , иммуноглобулинов), эффективно для направленной доставки противораковых, противоинфекционных и противовоспалительных препаратов. Доставка лекарства в нужное место может быть осуществлена путем местного применения липосомных препаратов, напр. , для противоартритных препаратов, а также при лечении дыхательного синдрома новорожденных и астмы.

Липосомы в косметике • В 1987 году две известные косметические компании создали новый продукт, явившийся плодом усилий их исследовательских лабораторий. Это были липосомный гель "Каптюр" фирмы "Кристиан Диор" и крем для кожи под названием "Ниосомы" фирмы "Л'Ореаль". • В ассортименте липосомной косметики имеются кремы для повседневного ухода за кожей, кремы, предотвращающие ее старение, средства для ухода за кожей после бритья, кондиционеры для волос, духи с длительно сохраняющимся запахом, губная помада, солнцезащитные кремы, средства для загара, грим, интимная и декоративная косметика.

Липосомы в косметике – это основа • Основу всех этих препаратов составляет водная дисперсия липосом, как правило многослойных, которые благодаря способности удерживать воду являются прекрасным увлажняющим агентом. • Для усиления полезных эффектов в рецептуру вводят добавки различных биологически активных веществ, таких, как витамины, антибиотики, белковые экстракты, фруктовые кислоты. • Нередко продукция выпускается по принципу "сделай сам", когда покупателю предлагается липосомная основа, в которую он по своему желанию может ввести любые добавки.

Преимущества липосом в косметике • В липосомной форме биологически активные вещества легче проходят через кожу. • Липосомы хороши как инертный, не раздражающий кожу материал, который готовится на водной основе и не содержит в своем составе спиртов, детергентов, масел и других солюбилизаторов (солюбилизантов) неприродного происхождения.

Липосомы в пищевой индустрии • Липиды в виде жиров являются одним из основных компонентов почти любого продукта питания. • Способность липосом солюбилизировать вещества в воде, защищать их от неблагоприятных факторов среды и высвобождать эти вещества в нужное время и предсказуемым образом может быть использована в технологических процессах пищевой промышленности. • В сыроделии использование ферментов в липосомной форме позволило сократить время созревания сыра (для чего иногда требуется около года) на 30 -50%. Кроме того, благодаря более высокой дисперсности липосомных препаратов значительно улучшились вкусовые качества сыра и его консистенция.

Липосомы в хлебобулочных и кондитерских изделиях • Хлебобулочные и кондитерские изделия, содержащие липосомы, которые хорошо удерживают воду, не черствеют и длительное время сохраняют товарный вид. • Добавление липосом в дрожжевое тесто защищает клетки дрожжей от гибели при замораживании, благодаря чему появилась возможность поставлять изделия из этого теста в виде полуфабриката в замороженном виде. • Включение в липосомы вкусовых и ароматизирующих добавок также улучшает потребительские свойства кондитерских изделий.

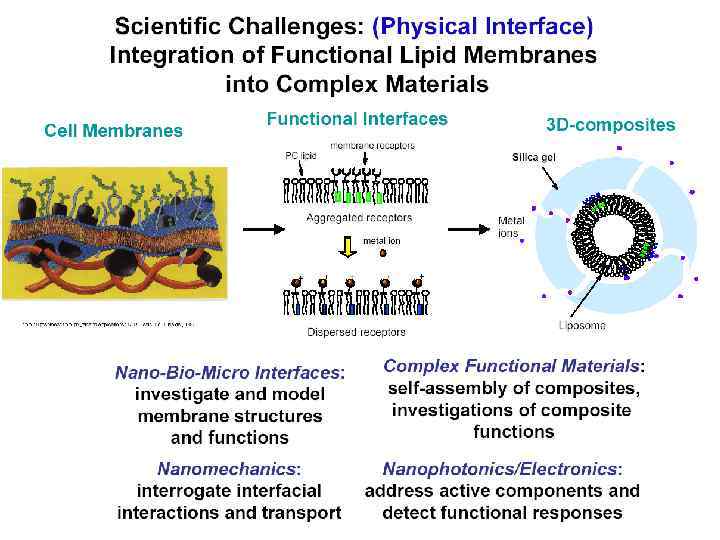
Липосомы, как темплаты для синтеза наноматериалов

Литература • • Марголис Л. Б. , Бергельсон Л. Д. Липосомы и их взаимодействие с клетками. М. : Наука, 1986. Липосомы в биологических системах / Под ред. Г. Грегориадиса, А. Аллисона. М. : Медицина, 1983. Lasic D. D. Liposomes: From Physics to Applications. Amsterdam: Elsevier, 1993. Васьковский В. В. Липиды // Соросовский Образовательный Журнал. 1997. № 3. С. 32 -37

Процессы переноса • Транспорт (перенос) является таким же фундаментальным процессом супрамолекулярной химии, как распознавание и катализ. (Ж. -М. Лен Супрамолекулярная химия: Концепции и перспективы. Пер. с англ. - Новосибирск: Наука, Сиб. Предприятие РАН, 1998. )

10. 3 Пассивный и активный транспорт. Транспорт с переносчиком, симпорт и антипорт.
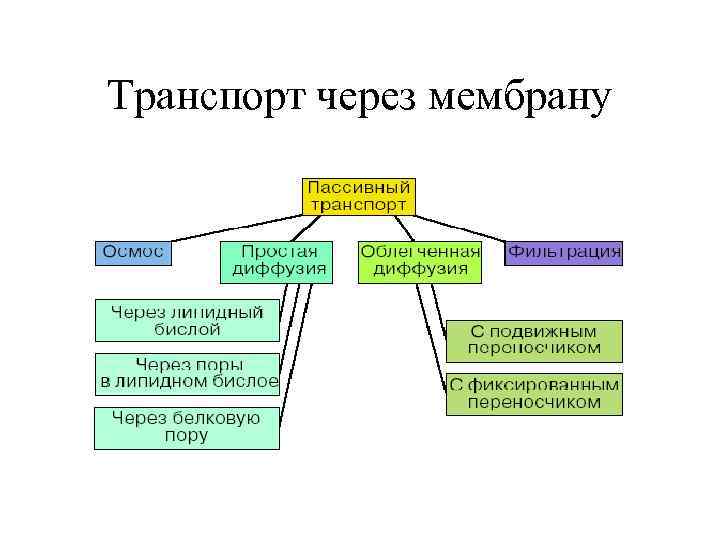
Транспорт через мембрану

Пассивный и активный транспорт • Пассивный транспорт – идет с уменьшением парциальной свободной энергии диффундирующего вещества • Активный транспорт – при изменении парциальных свободных энергий Гиббса нескольких компонентов (при сопряженной диффузии) возможен случай увеличения па парциальной свободной энергии одного из диффундирующих веществ. Иногда в литературе такие системы называют «насосом» .

Активный транспорт
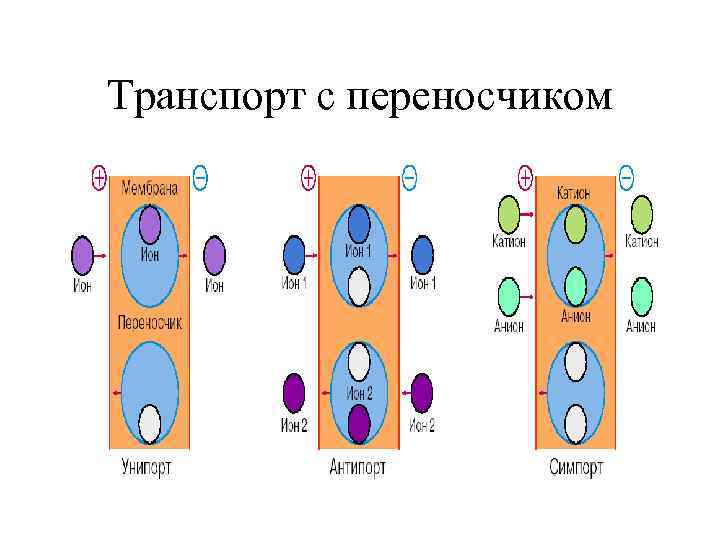
Транспорт с переносчиком
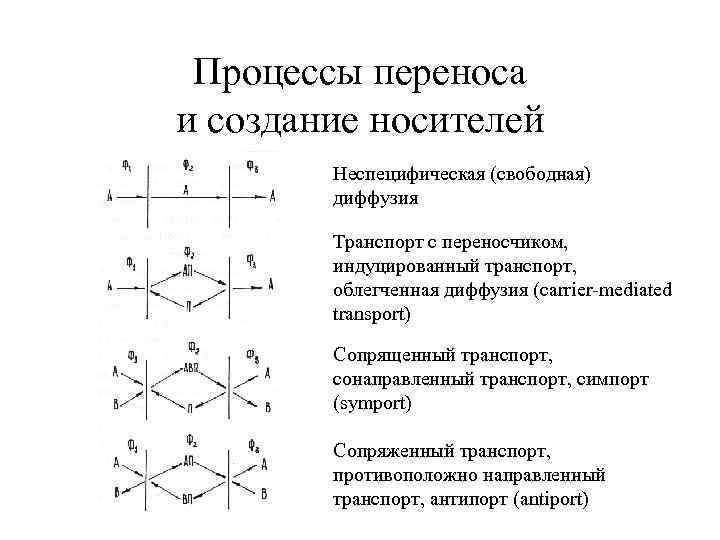
Процессы переноса и создание носителей Неспецифическая (свободная) диффузия Транспорт с переносчиком, индуцированный транспорт, облегченная диффузия (carrier-mediated transport) Сопрященный транспорт, сонаправленный транспорт, симпорт (symport) Сопряженный транспорт, противоположно направленный транспорт, антипорт (antiport)

Краун-эфиры – переносчики
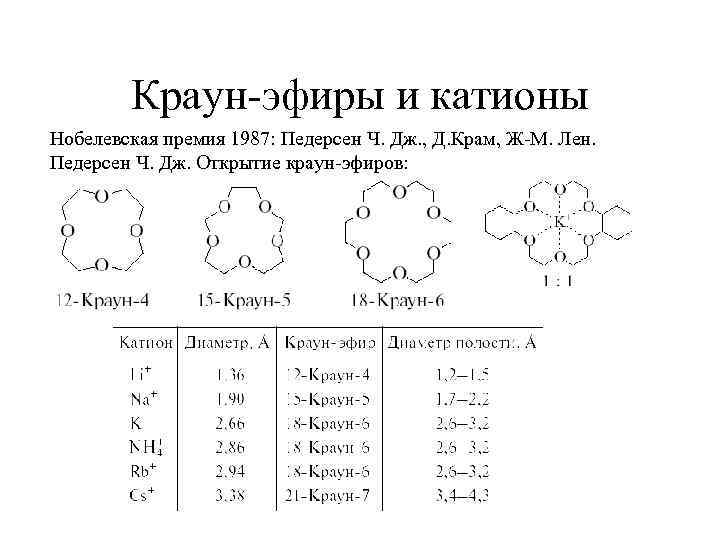
Краун-эфиры и катионы Нобелевская премия 1987: Педерсен Ч. Дж. , Д. Крам, Ж-М. Лен. Педерсен Ч. Дж. Открытие краун-эфиров:
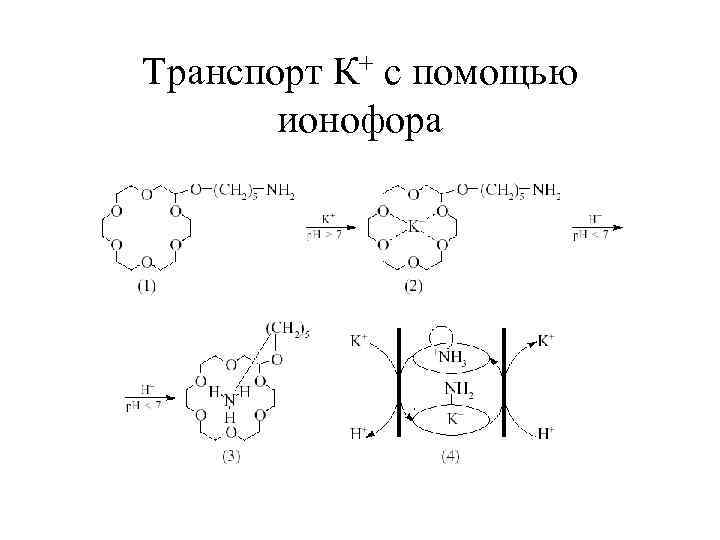
Транспорт К+ с помощью ионофора
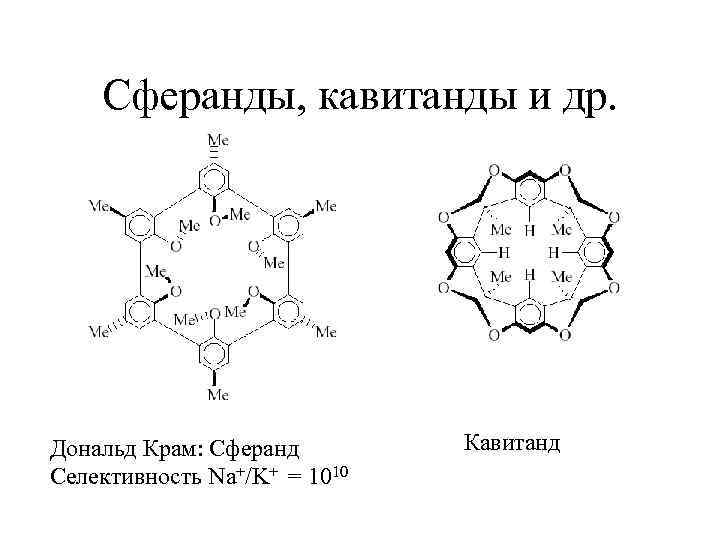
Сферанды, кавитанды и др. Дональд Крам: Сферанд Селективность Na+/K+ = 1010 Кавитанд
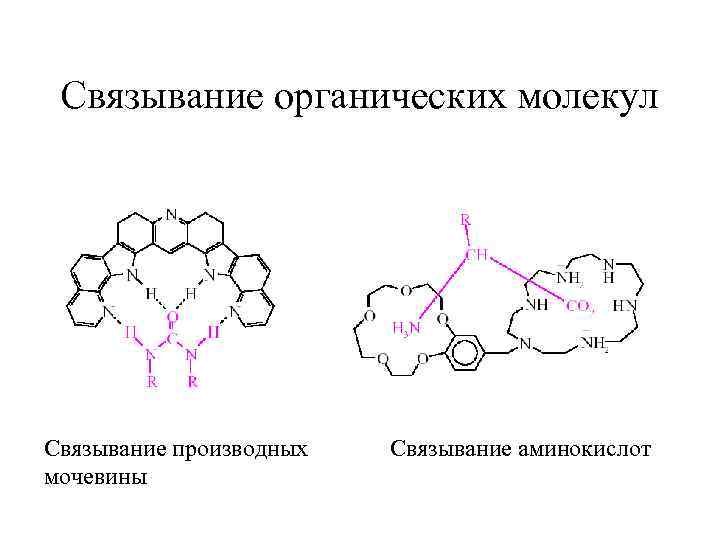
Связывание органических молекул Связывание производных мочевины Связывание аминокислот

Супрамолекулярные ансамбли - полимолекулярные ассоциаты, возникающие в результате спонтанной ассоциации неопределенно большого числа компонентов в специфическую фазу (пленка, слой, мембрана, везикула, мицелла, мезоморфная фаза, микроэмульсия, гель, кристалл и т. д. ). Если снабдить ансамбли фрагментами, способными к распознаванию, и реакционноспособными функциональными группами, можно получить системы, осуществляющие молекулярное распознавание или молекулярный катализ на внешних или внутренних поверхностях органических (молекулярные слои, мембраны, волокна, полимеры и т. д. ) или неорганических (цеолиты, глины, золь-гель-системы и т. д. ) материалов.
Глава 10. 2009 Биологические наноструктуры.ppt