ГИДРОЛИЗ.ppt
- Количество слайдов: 19
 Гидролиз - взаимодействие катионов или анионов соли (или тех и других) с водой, которое приводит к образованию слабого электролита
Гидролиз - взаимодействие катионов или анионов соли (или тех и других) с водой, которое приводит к образованию слабого электролита
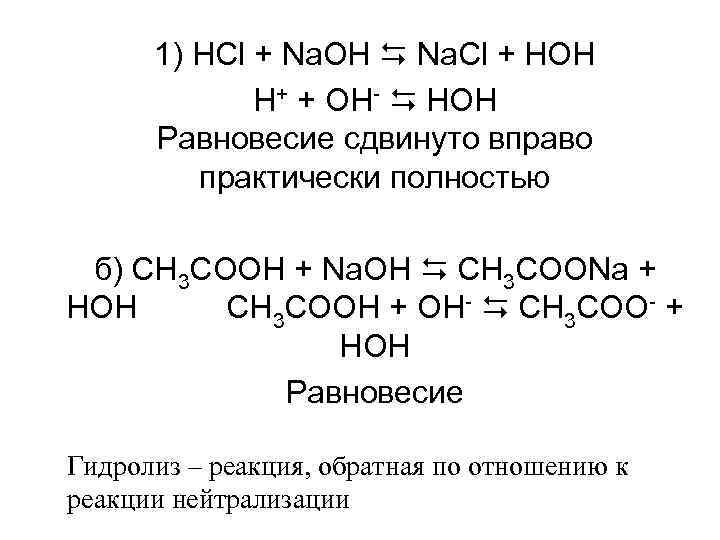 1) HCl + Na. OH Na. Cl + HOH H+ + OH- HOH Равновесие сдвинуто вправо практически полностью б) CH 3 COOH + Na. OH CH 3 COONa + HOH CH 3 COOH + OH- CH 3 COO- + HOH Равновесие Гидролиз – реакция, обратная по отношению к реакции нейтрализации
1) HCl + Na. OH Na. Cl + HOH H+ + OH- HOH Равновесие сдвинуто вправо практически полностью б) CH 3 COOH + Na. OH CH 3 COONa + HOH CH 3 COOH + OH- CH 3 COO- + HOH Равновесие Гидролиз – реакция, обратная по отношению к реакции нейтрализации
 «Правила» гидролиза При гидролизе соли: • на гидролиз одного иона приходится одна молекула воды; • в обычных условиях гидролиз идет практически только по первой ступени, гидролиз может идти до конца только (а) при высокой температуре и (б) при большом разбавлении.
«Правила» гидролиза При гидролизе соли: • на гидролиз одного иона приходится одна молекула воды; • в обычных условиях гидролиз идет практически только по первой ступени, гидролиз может идти до конца только (а) при высокой температуре и (б) при большом разбавлении.
 ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 1. Соль образована сильным основанием и сильной кислотой Na 2 SO 4 + HOH 2 Na+ + SO 42 - + HOH Гидролиз не идет, слабый электролит не образуется. Среда нейтральная, р. Н = 7
ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 1. Соль образована сильным основанием и сильной кислотой Na 2 SO 4 + HOH 2 Na+ + SO 42 - + HOH Гидролиз не идет, слабый электролит не образуется. Среда нейтральная, р. Н = 7
 ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 2. Соль образована слабым основанием и сильной кислотой NH 4 Cl + HOH NH 4 OH + HCl NH 4+ + Cl- + HOH NH 4 OH + H+ + Cl. NH 4+ + HOH NH 4 OH + H+ Гидролиз идет Среда кислая, р. Н < 7
ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 2. Соль образована слабым основанием и сильной кислотой NH 4 Cl + HOH NH 4 OH + HCl NH 4+ + Cl- + HOH NH 4 OH + H+ + Cl. NH 4+ + HOH NH 4 OH + H+ Гидролиз идет Среда кислая, р. Н < 7
 ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 2. Соль образована слабым основанием и сильной кислотой Al 2(SO 4)3 + HOH 2 Al. OHSO 4 + H 2 SO 4 2 Al 3+ + 3 SO 42 - + 2 HOH 2 Al. OH 2+ + 2 H+ + 3 SO 42 Al 3+ + HOH Al. OH 2+ + H+ Гидролиз идет Среда кислая, р. Н < 7
ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 2. Соль образована слабым основанием и сильной кислотой Al 2(SO 4)3 + HOH 2 Al. OHSO 4 + H 2 SO 4 2 Al 3+ + 3 SO 42 - + 2 HOH 2 Al. OH 2+ + 2 H+ + 3 SO 42 Al 3+ + HOH Al. OH 2+ + H+ Гидролиз идет Среда кислая, р. Н < 7
 ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 3. Соль образована сильным основанием и слабой кислотой Na 2 CO 3 + HOH Na. HCO 3 + Na. OH 2 Na+ + CO 32 - + HOH HCO 3 - + 2 Na+ + OHCO 32 - + HOH HCO 3 - + OH- Гидролиз идет Среда щелочная, р. Н > 7
ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 3. Соль образована сильным основанием и слабой кислотой Na 2 CO 3 + HOH Na. HCO 3 + Na. OH 2 Na+ + CO 32 - + HOH HCO 3 - + 2 Na+ + OHCO 32 - + HOH HCO 3 - + OH- Гидролиз идет Среда щелочная, р. Н > 7
 ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 4. Соль образована слабым основанием и слабой кислотой 4. 1 Соль не растворима в воде Cu. S + HOH Гидролиз не идет
ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 4. Соль образована слабым основанием и слабой кислотой 4. 1 Соль не растворима в воде Cu. S + HOH Гидролиз не идет
 ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 4. Соль образована слабым основанием и слабой кислотой 4. 2 Соль в растворе не существует Al 2 S 3 + 6 HOH 2 Al(OH)3 + 3 H 2 S Гидролиз идет полностью, до конца
ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 4. Соль образована слабым основанием и слабой кислотой 4. 2 Соль в растворе не существует Al 2 S 3 + 6 HOH 2 Al(OH)3 + 3 H 2 S Гидролиз идет полностью, до конца
 ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 4. Соль образована слабым основанием и слабой кислотой 4. 3 Соль растворима в воде a) (NH 4)2 CO 3 + HOH NH 4 HCO 3 + NH 4 OH 2 NH 4+ + CO 32 - + HOH HCO 3 - + NH 4 OH + NH 4+ б) NH 4 HCO 3 + HOH H 2 CO 3 + NH 4 OH NH 4+ + HCO 3 - + HOH H 2 CO 3 + NH 4 OH Гидролиз идет по ступеням, полностью, до конца, среда примерно нейтральная, р. Н около 7
ЧЕТЫРЕ СЛУЧАЯ ГИДРОЛИЗА 4. Соль образована слабым основанием и слабой кислотой 4. 3 Соль растворима в воде a) (NH 4)2 CO 3 + HOH NH 4 HCO 3 + NH 4 OH 2 NH 4+ + CO 32 - + HOH HCO 3 - + NH 4 OH + NH 4+ б) NH 4 HCO 3 + HOH H 2 CO 3 + NH 4 OH NH 4+ + HCO 3 - + HOH H 2 CO 3 + NH 4 OH Гидролиз идет по ступеням, полностью, до конца, среда примерно нейтральная, р. Н около 7
 Особые случаи гидролиза 1) Sb. Cl 3 + HOH Sb. OHCl 2 + HCl Sb 3+ + HOH Sb. OH 2+ + H+ 2) Sb. OH 2+ + HOH Sb(OH)2+ + H+ Sb. O+ H 2 O Sb. OHCl 2 + HOH Sb. OCl + H 2 O
Особые случаи гидролиза 1) Sb. Cl 3 + HOH Sb. OHCl 2 + HCl Sb 3+ + HOH Sb. OH 2+ + H+ 2) Sb. OH 2+ + HOH Sb(OH)2+ + H+ Sb. O+ H 2 O Sb. OHCl 2 + HOH Sb. OCl + H 2 O
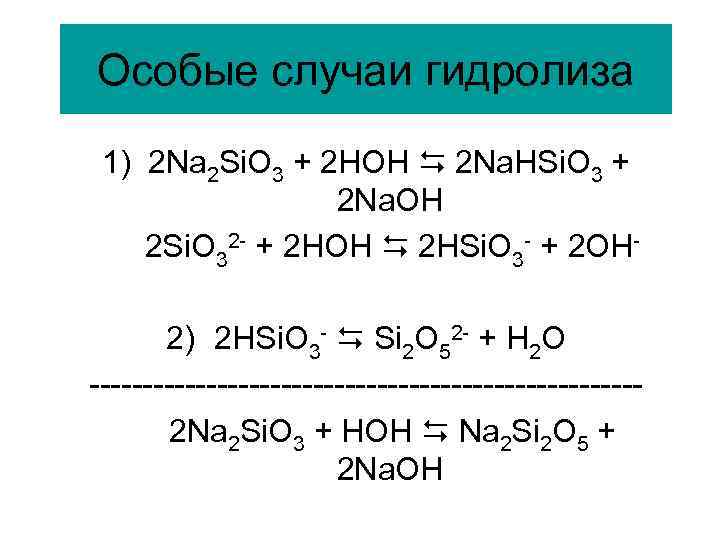 Особые случаи гидролиза 1) 2 Na 2 Si. O 3 + 2 HOH 2 Na. HSi. O 3 + 2 Na. OH 2 Si. O 32 - + 2 HOH 2 HSi. O 3 - + 2 OH 2) 2 HSi. O 3 - Si 2 O 52 - + H 2 O -------------------------- 2 Na 2 Si. O 3 + HOH Na 2 Si 2 O 5 + 2 Na. OH
Особые случаи гидролиза 1) 2 Na 2 Si. O 3 + 2 HOH 2 Na. HSi. O 3 + 2 Na. OH 2 Si. O 32 - + 2 HOH 2 HSi. O 3 - + 2 OH 2) 2 HSi. O 3 - Si 2 O 52 - + H 2 O -------------------------- 2 Na 2 Si. O 3 + HOH Na 2 Si 2 O 5 + 2 Na. OH
 КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ГИДРОЛИЗА Степень гидролиза h =
КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ГИДРОЛИЗА Степень гидролиза h =
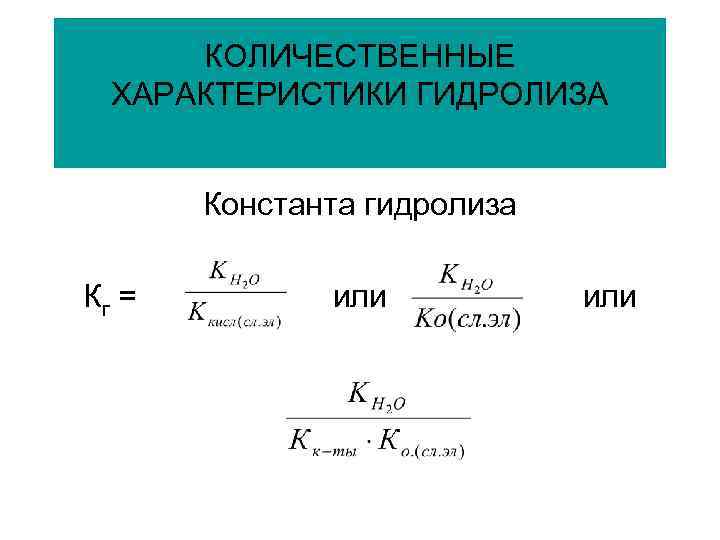 КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ГИДРОЛИЗА Константа гидролиза Кг = или
КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ГИДРОЛИЗА Константа гидролиза Кг = или
 Связь между степенью гидролиза и константой гидролиза Кг = Сh 2 h =
Связь между степенью гидролиза и константой гидролиза Кг = Сh 2 h =
 Kг 1 (К 2 СО 3) = = 2, 1 10 -4 Kг 2 (К 2 СО 3) = = 2, 2 10 -8 Кг 2 « Кг 1
Kг 1 (К 2 СО 3) = = 2, 1 10 -4 Kг 2 (К 2 СО 3) = = 2, 2 10 -8 Кг 2 « Кг 1
 Усиление гидролиза Na 2 CO 3 + HOH Na. HCO 3 + Na. OH 2 Na+ + CO 32 - + HOH HCO 3 - + 2 Na+ + OHCO 32 - + HOH HCO 3 - + OH- - разбавление; - нагревание Опыт. Гидролиз Fe. Cl 3 при нагревании
Усиление гидролиза Na 2 CO 3 + HOH Na. HCO 3 + Na. OH 2 Na+ + CO 32 - + HOH HCO 3 - + 2 Na+ + OHCO 32 - + HOH HCO 3 - + OH- - разбавление; - нагревание Опыт. Гидролиз Fe. Cl 3 при нагревании
 Ослабление гидролиза Na 2 CO 3 + HOH Na. HCO 3 + Na. OH 2 Na+ + CO 32 - + HOH HCO 3 - + 2 Na+ + OHCO 32 - + HOH HCO 3 - + OH- - добавление щелочи (кислоты)
Ослабление гидролиза Na 2 CO 3 + HOH Na. HCO 3 + Na. OH 2 Na+ + CO 32 - + HOH HCO 3 - + 2 Na+ + OHCO 32 - + HOH HCO 3 - + OH- - добавление щелочи (кислоты)
 Взаимное усиление гидролиза 3 Na 2 S + 2 Al. Cl 3 + 6 HOH = 2 Al(OH)3 + 3 H 2 S + 6 Na. Cl
Взаимное усиление гидролиза 3 Na 2 S + 2 Al. Cl 3 + 6 HOH = 2 Al(OH)3 + 3 H 2 S + 6 Na. Cl


