Гидролиз солей.ppt
- Количество слайдов: 16

Гидролиз солей Тесты

Слабая кислота – это: 1) HNO 3 2) H 2 Si. O 3 3) HCl 4) H 3 PO 4

Сильная кислота – это: 1) H 2 SO 3 2) H 2 Si. O 3 3) H 2 SO 4 4) H 2 S

Слабое основание – это: 1) Be(OH)2 2) Ca(OH)2 3) KOH 4) Na. OH

Хлорид меди(II) образован: 1) слабой кислотой и сильным основанием 2) сильной кислотой и слабым основанием 3) слабой кислотой и слабым основанием 4) сильной кислотой и сильным основанием

Причиной щелочной среды является избыток в растворе ионов: 1) Сl– 2) OH– 3) H+ 4) NO 3–

Кислую реакцию среды обуславливают: 1) гидроксид-ионы 2) карбонат-ионы 3) катионы водорода 4) хлорид-ионы

Кислую реакцию среды нельзя обнаружить при помощи: 1) лакмуса 2) фенолфталеина 3) метилоранжа 4) универсального индикатора

Щелочную среду имеет водный раствор: 1) хлорида натрия 2) карбоната калия 3) сульфата бария 4) нитрата магния

Лакмус становится красным в водном растворе: 1) Ca(NO 3)2 2) Na 2 Si. O 3 3) Cr. Cl 3 4) K 2 S

По аниону в водном растворе подвергается гидролизу: 1) Ba. SO 4 2) Cu. Cl 2 3) Cu(NO 3)2 4) K 2 S

По катиону в водном растворе подвергается гидролизу: 1) Cu. SO 4 2) KCl 3) Na. NO 3 4) K 2 S

Среда раствора карбоната калия: 1) щелочная 2) кислая 3) нейтральная 4) слабокислая

Нейтральную среду имеет водный раствор: 1) K 2 Si. O 3 2) Ca. Cl 2 3) Al(NO 3)3 4) Zn. SO 4
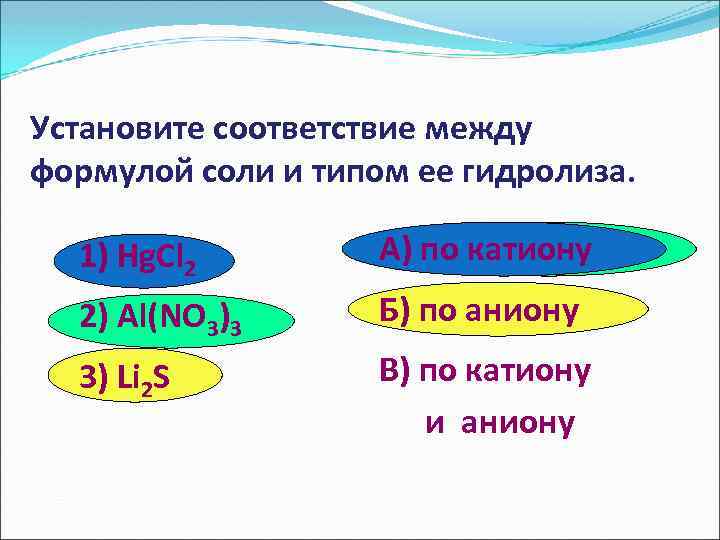
Установите соответствие между формулой соли и типом ее гидролиза. 1) Hg. Cl 2 A) по катиону 2) Al(NO 3)3 Б) по аниону 3) Li 2 S В) по катиону и аниону

Установите соответствие между формулой соли и окраской лакмуса в ее водном растворе. 1) Li. Cl А) фиолетовая 2) K 2 Si. O 3 Б) синяя 3) Al(NO 3)3 B) красная
Гидролиз солей.ppt