 ГИДРОЛИЗ СОЛЕЙ
ГИДРОЛИЗ СОЛЕЙ
 Гидролизом называется взаимодействие составных частей соли с составными частями воды, приводящее к образованию слабого электролита и изменения p. H раствора. Различают четыре случая гидролиза: I. Соли образованные сильным основание и слабой кислотой. II. Гидролиз протекает по аниону.
Гидролизом называется взаимодействие составных частей соли с составными частями воды, приводящее к образованию слабого электролита и изменения p. H раствора. Различают четыре случая гидролиза: I. Соли образованные сильным основание и слабой кислотой. II. Гидролиз протекает по аниону.
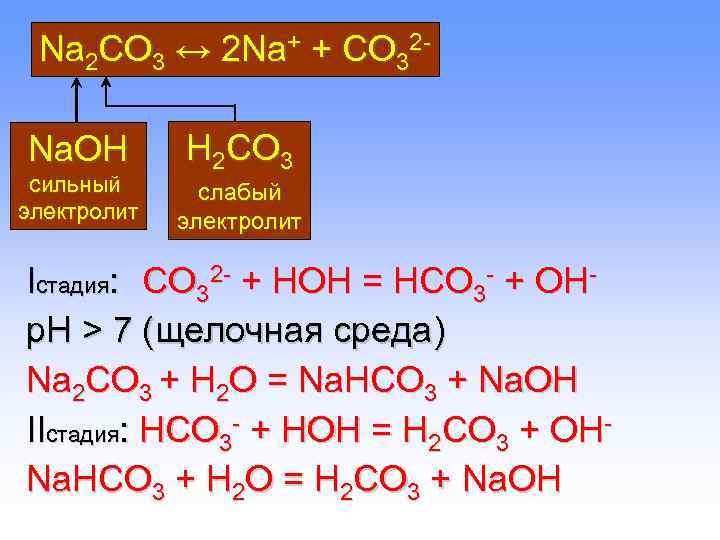 Na 2 CO 3 ↔ 2 Na+ + CO 32 - Na. OH H 2 CO 3 сильный слабый электролит Iстадия: CO 32 - + HOН = HCO 3 - + OH- p. H > 7 (щелочная среда) Na 2 CO 3 + H 2 O = Na. HCO 3 + Na. OH IIстадия: HCO 3 - + HOH = H 2 CO 3 + OH- Na. НCO 3 + H 2 O = H 2 CO 3 + Na. OH
Na 2 CO 3 ↔ 2 Na+ + CO 32 - Na. OH H 2 CO 3 сильный слабый электролит Iстадия: CO 32 - + HOН = HCO 3 - + OH- p. H > 7 (щелочная среда) Na 2 CO 3 + H 2 O = Na. HCO 3 + Na. OH IIстадия: HCO 3 - + HOH = H 2 CO 3 + OH- Na. НCO 3 + H 2 O = H 2 CO 3 + Na. OH
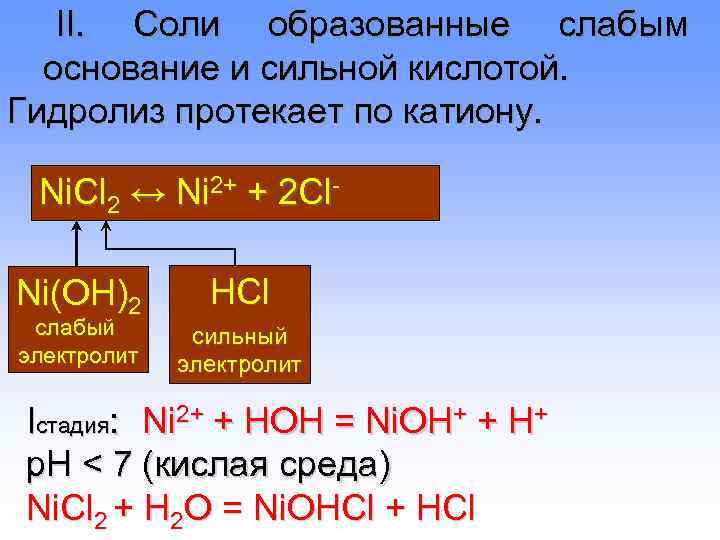 II. Соли образованные слабым основание и сильной кислотой. Гидролиз протекает по катиону. Ni. Cl 2 ↔ Ni 2+ + 2 Cl- Ni(OH)2 HCl слабый сильный электролит Iстадия: Ni 2+ + HOН = Ni. OH+ + H+ p. H < 7 (кислая среда) Ni. Cl 2 + H 2 O = Ni. OHCl + HCl
II. Соли образованные слабым основание и сильной кислотой. Гидролиз протекает по катиону. Ni. Cl 2 ↔ Ni 2+ + 2 Cl- Ni(OH)2 HCl слабый сильный электролит Iстадия: Ni 2+ + HOН = Ni. OH+ + H+ p. H < 7 (кислая среда) Ni. Cl 2 + H 2 O = Ni. OHCl + HCl
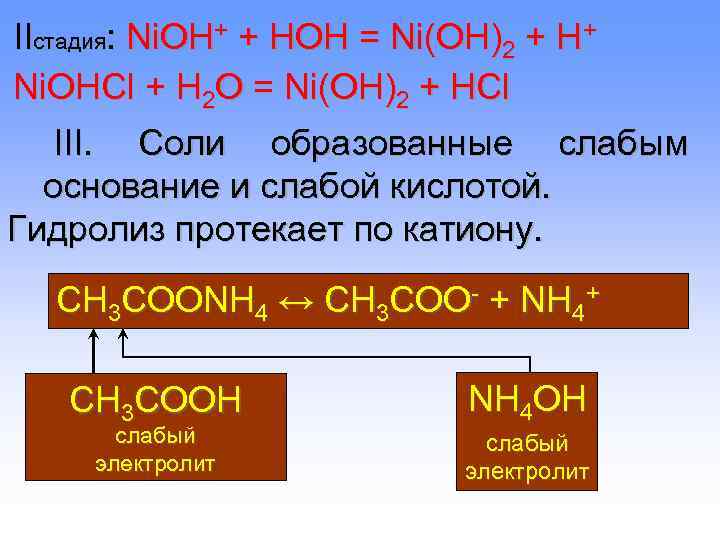 IIстадия: Ni. OH+ + HOH = Ni(OH)2 + H+ Ni. OНCl + H 2 O = Ni(OH)2 + HCl III. Соли образованные слабым основание и слабой кислотой. Гидролиз протекает по катиону. CH 3 COONH 4 ↔ CH 3 COO- + NH 4+ CH 3 COOH NH 4 OH слабый электролит
IIстадия: Ni. OH+ + HOH = Ni(OH)2 + H+ Ni. OНCl + H 2 O = Ni(OH)2 + HCl III. Соли образованные слабым основание и слабой кислотой. Гидролиз протекает по катиону. CH 3 COONH 4 ↔ CH 3 COO- + NH 4+ CH 3 COOH NH 4 OH слабый электролит
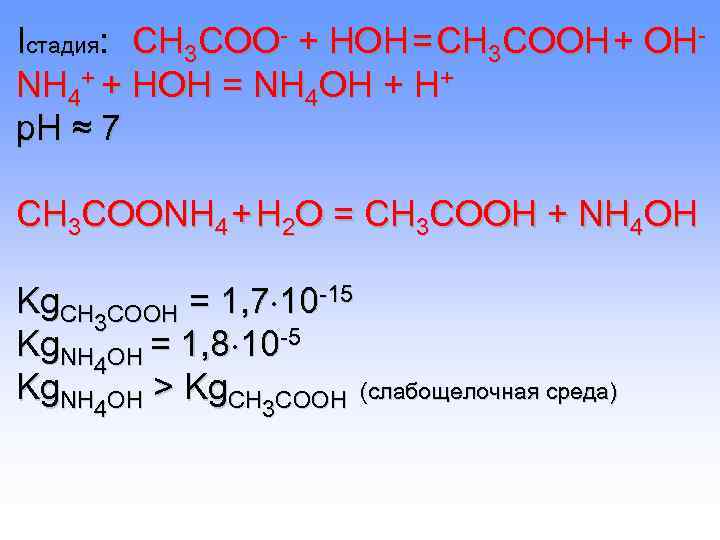 Iстадия: СН 3 COO- + HOН = CH 3 COOH + OH- NH 4+ + НОН = NH 4 OH + H+ p. H ≈ 7 СН 3 COONH 4 + H 2 O = CH 3 COOH + NH 4 OH Kg. CH 3 СООН = 1, 7 10 -15 Kg. NH 4 OH = 1, 8 10 -5 Kg. NH 4 OH > Kg. CH 3 СООН (слабощелочная среда)
Iстадия: СН 3 COO- + HOН = CH 3 COOH + OH- NH 4+ + НОН = NH 4 OH + H+ p. H ≈ 7 СН 3 COONH 4 + H 2 O = CH 3 COOH + NH 4 OH Kg. CH 3 СООН = 1, 7 10 -15 Kg. NH 4 OH = 1, 8 10 -5 Kg. NH 4 OH > Kg. CH 3 СООН (слабощелочная среда)
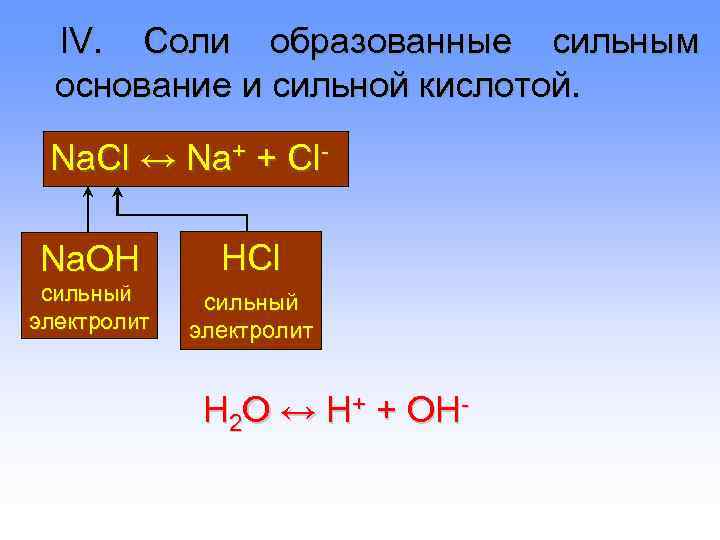 IV. Соли образованные сильным основание и сильной кислотой. Na. Cl ↔ Na+ + Cl- Na. OH HCl сильный электролит H 2 O ↔ H+ + OH-
IV. Соли образованные сильным основание и сильной кислотой. Na. Cl ↔ Na+ + Cl- Na. OH HCl сильный электролит H 2 O ↔ H+ + OH-
 Степень гидролиза Для большинства солей гидролиз обратим. Гидролитическое равновесие количественно характеризуется степенью гидролиза. h или (αг) Растворено 2 моля соли - 0, 01 моль подвергся гидролизу.
Степень гидролиза Для большинства солей гидролиз обратим. Гидролитическое равновесие количественно характеризуется степенью гидролиза. h или (αг) Растворено 2 моля соли - 0, 01 моль подвергся гидролизу.
 На величину h влияют: 1) природа соли 2) температура 3) концентрация соли Чем выше температура и сильнее разбавлен раствор, тем больше h (αг). Чтобы усилить гидролиз надо разбавить раствор и нагреть. Так можно довести гидролиз до конца.
На величину h влияют: 1) природа соли 2) температура 3) концентрация соли Чем выше температура и сильнее разбавлен раствор, тем больше h (αг). Чтобы усилить гидролиз надо разбавить раствор и нагреть. Так можно довести гидролиз до конца.
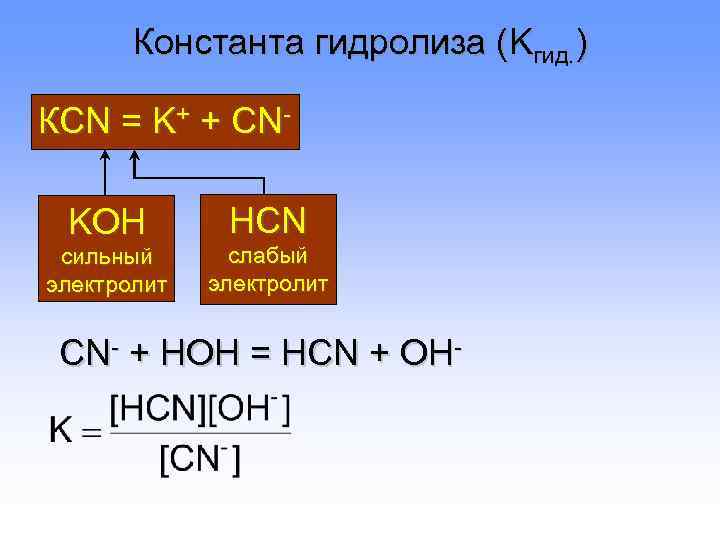 Константа гидролиза (Kгид. ) КCN = K+ + CN- KOH HCN сильный слабый электролит CN- + HOH = HCN + OH-
Константа гидролиза (Kгид. ) КCN = K+ + CN- KOH HCN сильный слабый электролит CN- + HOH = HCN + OH-
 Гидролиз соли протекает по аниону
Гидролиз соли протекает по аниону
 Zn. Cl 2 = Zn 2+ + 2 Cl- Zn(OH)2 HCl слабый сильный электролит Zn 2+ + НОН = [Zn. OH]+ + H+ Гидролиз соли протекает по катиону
Zn. Cl 2 = Zn 2+ + 2 Cl- Zn(OH)2 HCl слабый сильный электролит Zn 2+ + НОН = [Zn. OH]+ + H+ Гидролиз соли протекает по катиону
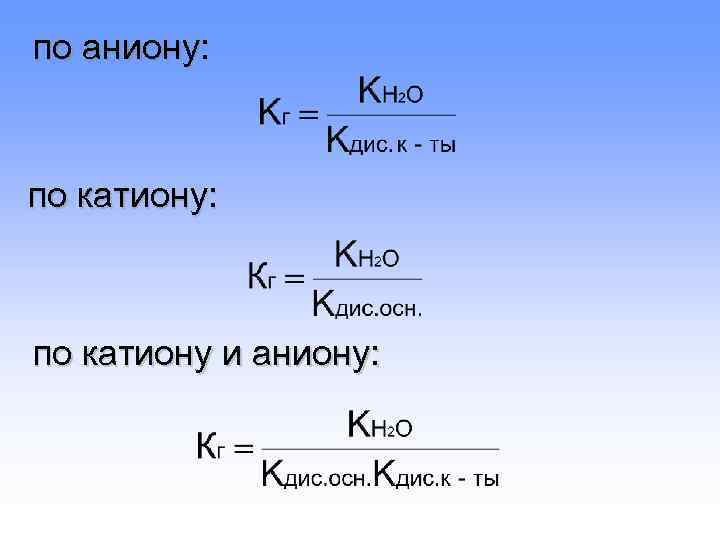 по аниону: по катиону и аниону:
по аниону: по катиону и аниону:
 Необратимый гидролиз Al 2 S 3 + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑ Al(OH)3 H 2 S слабый электролит 2 Al 3+ + 3 S 2 - + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑
Необратимый гидролиз Al 2 S 3 + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑ Al(OH)3 H 2 S слабый электролит 2 Al 3+ + 3 S 2 - + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑
 Совместный гидролиз 2 Al. Cl 3 + 3 Na 2 S + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑ + 6 Na. Cl 2 Al 3+ + 3 S 2 - + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑
Совместный гидролиз 2 Al. Cl 3 + 3 Na 2 S + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑ + 6 Na. Cl 2 Al 3+ + 3 S 2 - + 6 H 2 O = 2 Al(OH)3↓ + 3 H 2 S↑































