d76f5df5c0fa132159be7e28a168c776.ppt
- Количество слайдов: 30
 Гидролиз солей. Единственный путь, Ведущий к знанию, Это деятельность. «Шоу» Составила Громова Ольга Ильинична, учитель химии и биологии «МОУ Лямбирская СОШ № 1»
Гидролиз солей. Единственный путь, Ведущий к знанию, Это деятельность. «Шоу» Составила Громова Ольга Ильинична, учитель химии и биологии «МОУ Лямбирская СОШ № 1»
 Гидроксиды Na. OH, KOH, NH 4 OH, Cu(OH)2, Zn(OH)2, Al(OH)3, H 2 SO 4, HNO 3, HCl. O 4, HCl, HMn. O 4, HI, HBr, H 2 SO 3, H 2 CO 3, H 2 Si. O 3, HF, HNO 2
Гидроксиды Na. OH, KOH, NH 4 OH, Cu(OH)2, Zn(OH)2, Al(OH)3, H 2 SO 4, HNO 3, HCl. O 4, HCl, HMn. O 4, HI, HBr, H 2 SO 3, H 2 CO 3, H 2 Si. O 3, HF, HNO 2
 Электролиты u сильные: Na. OH, KOH, H 2 SO 4, HNO 3, HCl. O 4, HCl, HMn. O 4, HI, HBr; u слабые: , NH 4 OH, Cu(OH)2, Zn(OH)2, Al(OH)3, H 2 SO 3, H 2 CO 3, H 2 Si. O 3, HF, HNO 2, СН 3 СООН 3/19/2018 3 Громова О. И
Электролиты u сильные: Na. OH, KOH, H 2 SO 4, HNO 3, HCl. O 4, HCl, HMn. O 4, HI, HBr; u слабые: , NH 4 OH, Cu(OH)2, Zn(OH)2, Al(OH)3, H 2 SO 3, H 2 CO 3, H 2 Si. O 3, HF, HNO 2, СН 3 СООН 3/19/2018 3 Громова О. И
 Изменение цвета различных индикаторов при действии растворов кислот и щелочей Индикатор Цвет индикатора в среде кислой Лакмус Красный щелочной Синий Фенолфта- Бесцветный Малиновый леин 3/19/2018 4 Громова О. И нейтрально й —— Бесцветный
Изменение цвета различных индикаторов при действии растворов кислот и щелочей Индикатор Цвет индикатора в среде кислой Лакмус Красный щелочной Синий Фенолфта- Бесцветный Малиновый леин 3/19/2018 4 Громова О. И нейтрально й —— Бесцветный
 u Любую соль можно представить как продукт взаимодействия основания с кислотой. u В зависимости от силы основания и кислоты можно выделить 4 типа солей: 3/19/2018 5 Громова О. И
u Любую соль можно представить как продукт взаимодействия основания с кислотой. u В зависимости от силы основания и кислоты можно выделить 4 типа солей: 3/19/2018 5 Громова О. И
 1. Соли, образованные сильной кислотой и слабым основанием (Al. Cl 3, Fe. SO 4, Mn(NO 3)2. ) 2. Соли, образованные сильным основанием и слабой кислотой (Na 2 CO 3, КСN, Na. CH 3 COO). 3. Соли, образованные слабой кислотой и слабым основанием (NH 4 CN, Cu(CH 3 COO)2). 4. Соли, образованные сильной кислотой и сильным основанием (Na. Cl, K 2 SO 4, Ba. I 2). 3/19/2018 6 Громова О. И
1. Соли, образованные сильной кислотой и слабым основанием (Al. Cl 3, Fe. SO 4, Mn(NO 3)2. ) 2. Соли, образованные сильным основанием и слабой кислотой (Na 2 CO 3, КСN, Na. CH 3 COO). 3. Соли, образованные слабой кислотой и слабым основанием (NH 4 CN, Cu(CH 3 COO)2). 4. Соли, образованные сильной кислотой и сильным основанием (Na. Cl, K 2 SO 4, Ba. I 2). 3/19/2018 6 Громова О. И
 Гидролизом называется взаимодействие веществ с водой, при котором составные части вещества соединяются с составными частями воды. u Гидролизу подвержены соединения различных классов. Рассмотрим один случай – гидролиз солей. 3/19/2018 7 Громова О. И
Гидролизом называется взаимодействие веществ с водой, при котором составные части вещества соединяются с составными частями воды. u Гидролизу подвержены соединения различных классов. Рассмотрим один случай – гидролиз солей. 3/19/2018 7 Громова О. И
![Схема гидролиза Na. CN Na. OH HCN сильное основание слабая кислота [OH–] 3/19/2018 8 Схема гидролиза Na. CN Na. OH HCN сильное основание слабая кислота [OH–] 3/19/2018 8](https://present5.com/presentation/d76f5df5c0fa132159be7e28a168c776/image-8.jpg) Схема гидролиза Na. CN Na. OH HCN сильное основание слабая кислота [OH–] 3/19/2018 8 > Громова О. И [H+] Щелчная среда Сила побеждает!
Схема гидролиза Na. CN Na. OH HCN сильное основание слабая кислота [OH–] 3/19/2018 8 > Громова О. И [H+] Щелчная среда Сила побеждает!
 Уравнения гидролиза Na. CN ↔Na+ + CN‾ Н 2 О ↔ H+ + OH ‾ ______________ Полное ионное уравнение гидролиза: Na+ + CN¯ + Н 2 О ↔ Na+ + OH¯ + HCN Сокращённое уравнение гидролиза: CN¯ + Н 2 О ↔ OH¯ + HCN Полное молекулярное уравнение гидролиза: Na. CN + Н 2 О ↔ Na. OH + HCN Ш Избыток гидроксид-ионов дает соли щелочную среду, поэтому лакмус синеет, а фенолфталеин становится малиновым. рн >7, среда щелочная, гидролиз по аниону. 3/19/2018 9 Громова О. И
Уравнения гидролиза Na. CN ↔Na+ + CN‾ Н 2 О ↔ H+ + OH ‾ ______________ Полное ионное уравнение гидролиза: Na+ + CN¯ + Н 2 О ↔ Na+ + OH¯ + HCN Сокращённое уравнение гидролиза: CN¯ + Н 2 О ↔ OH¯ + HCN Полное молекулярное уравнение гидролиза: Na. CN + Н 2 О ↔ Na. OH + HCN Ш Избыток гидроксид-ионов дает соли щелочную среду, поэтому лакмус синеет, а фенолфталеин становится малиновым. рн >7, среда щелочная, гидролиз по аниону. 3/19/2018 9 Громова О. И
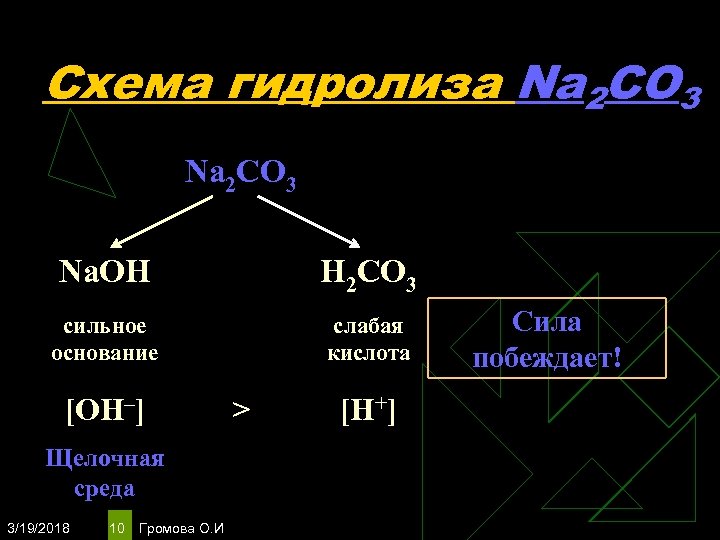 Схема гидролиза Na 2 CO 3 Na. OH H 2 CO 3 сильное основание слабая кислота [OH–] Щелочная среда 3/19/2018 10 Громова О. И > [H+] Сила побеждает!
Схема гидролиза Na 2 CO 3 Na. OH H 2 CO 3 сильное основание слабая кислота [OH–] Щелочная среда 3/19/2018 10 Громова О. И > [H+] Сила побеждает!
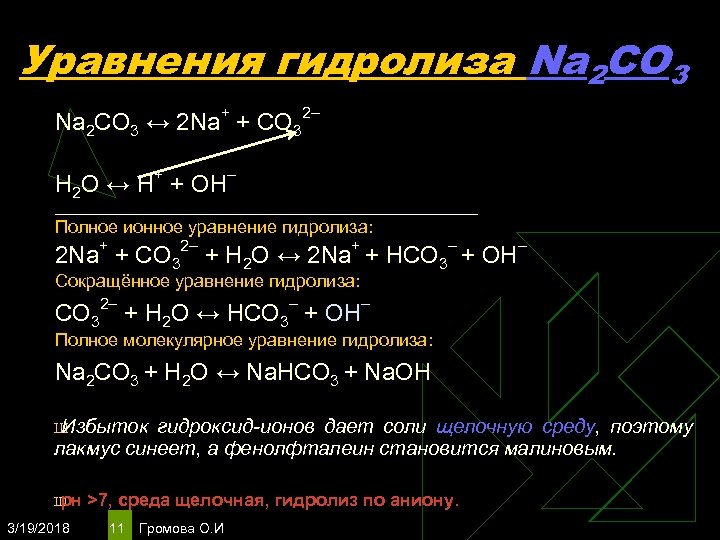 Уравнения гидролиза Na 2 CO 3 + Na 2 CO 3 ↔ 2 Na + СO 3 2– Н 2 O ↔ Н+ + ОН– ______________________________________ Полное ионное уравнение гидролиза: 2 Na+ + СO 32– + Н 2 O ↔ 2 Na+ + HCO 3– + ОН– Сокращённое уравнение гидролиза: СO 32– + Н 2 O ↔ НСO 3– + ОН– Полное молекулярное уравнение гидролиза: Na 2 CO 3 + Н 2 O ↔ Na. HCO 3 + Na. ОН Ш Избыток гидроксид-ионов дает соли щелочную среду, поэтому лакмус синеет, а фенолфталеин становится малиновым. Ш рн 3/19/2018 >7, среда щелочная, гидролиз по аниону. 11 Громова О. И
Уравнения гидролиза Na 2 CO 3 + Na 2 CO 3 ↔ 2 Na + СO 3 2– Н 2 O ↔ Н+ + ОН– ______________________________________ Полное ионное уравнение гидролиза: 2 Na+ + СO 32– + Н 2 O ↔ 2 Na+ + HCO 3– + ОН– Сокращённое уравнение гидролиза: СO 32– + Н 2 O ↔ НСO 3– + ОН– Полное молекулярное уравнение гидролиза: Na 2 CO 3 + Н 2 O ↔ Na. HCO 3 + Na. ОН Ш Избыток гидроксид-ионов дает соли щелочную среду, поэтому лакмус синеет, а фенолфталеин становится малиновым. Ш рн 3/19/2018 >7, среда щелочная, гидролиз по аниону. 11 Громова О. И
![Схема гидролиза NH 4 Cl NH 4 OH HCl слабое основание сильная кислота [OH–] Схема гидролиза NH 4 Cl NH 4 OH HCl слабое основание сильная кислота [OH–]](https://present5.com/presentation/d76f5df5c0fa132159be7e28a168c776/image-12.jpg) Схема гидролиза NH 4 Cl NH 4 OH HCl слабое основание сильная кислота [OH–] < [H+] Кислая среда 3/19/2018 12 Громова О. И Сила побеждает!
Схема гидролиза NH 4 Cl NH 4 OH HCl слабое основание сильная кислота [OH–] < [H+] Кислая среда 3/19/2018 12 Громова О. И Сила побеждает!
 Уравнения гидролиза NH 4 Cl ↔ NH 4+ + Сl– + Н 2 O ↔ Н + ОН – _____________________ Полное ионное уравнение гидролиза + – – : NH 4 + Сl + Н 2 O ↔ NH 3·H 2 О + Сl + Н + Сокращённое уравнение гидролиза: NH 4+ + Н 2 O ↔ NH 3·H 2 О + Н+ Полное молекулярное уравнение гидролиза: NH 4 Cl + Н 2 O ↔ NH 3·H 2 О + НСl Ш Избыток ионов водорода дает соли кислую среду, поэтому лакмус краснеет. Ш рн < 7, среда кислотная, гидролиз по катиону. 3/19/2018 13 Громова О. И
Уравнения гидролиза NH 4 Cl ↔ NH 4+ + Сl– + Н 2 O ↔ Н + ОН – _____________________ Полное ионное уравнение гидролиза + – – : NH 4 + Сl + Н 2 O ↔ NH 3·H 2 О + Сl + Н + Сокращённое уравнение гидролиза: NH 4+ + Н 2 O ↔ NH 3·H 2 О + Н+ Полное молекулярное уравнение гидролиза: NH 4 Cl + Н 2 O ↔ NH 3·H 2 О + НСl Ш Избыток ионов водорода дает соли кислую среду, поэтому лакмус краснеет. Ш рн < 7, среда кислотная, гидролиз по катиону. 3/19/2018 13 Громова О. И
![Схема гидролиза Al. Cl 3 Al(OH)3 HCl слабое основание сильная кислота [OH–] < [H+] Схема гидролиза Al. Cl 3 Al(OH)3 HCl слабое основание сильная кислота [OH–] < [H+]](https://present5.com/presentation/d76f5df5c0fa132159be7e28a168c776/image-14.jpg) Схема гидролиза Al. Cl 3 Al(OH)3 HCl слабое основание сильная кислота [OH–] < [H+] Кислая среда 3/19/2018 14 Громова О. И Сила побеждает!
Схема гидролиза Al. Cl 3 Al(OH)3 HCl слабое основание сильная кислота [OH–] < [H+] Кислая среда 3/19/2018 14 Громова О. И Сила побеждает!
 Уравнения гидролиза Аl. Сl 3 ↔ Аl 3+ + 3 Сl– Н 2 O ↔ Н+ + ОН– ___________________ Полное ионное уравнение гидролиза: Al 3+ + 3 Сl– + Н 2 O ↔ Аl. OН 2+ + 3 Сl– + Н+ Сокращённое уравнение гидролиза: Аl 3+ + Н 2 O ↔ Аl. OН 2+ + Н+ Полное молекулярное уравнение гидролиза: Аl. Сl 3 + Н 2 O ↔ Аl. OНСl 2 + НСl Ш Избыток ионов водорода дает соли кислую среду, поэтому лакмус краснеет. Ш рн 3/19/2018 < 7, среда кислотная, гидролиз по катиону. 15 Громова О. И
Уравнения гидролиза Аl. Сl 3 ↔ Аl 3+ + 3 Сl– Н 2 O ↔ Н+ + ОН– ___________________ Полное ионное уравнение гидролиза: Al 3+ + 3 Сl– + Н 2 O ↔ Аl. OН 2+ + 3 Сl– + Н+ Сокращённое уравнение гидролиза: Аl 3+ + Н 2 O ↔ Аl. OН 2+ + Н+ Полное молекулярное уравнение гидролиза: Аl. Сl 3 + Н 2 O ↔ Аl. OНСl 2 + НСl Ш Избыток ионов водорода дает соли кислую среду, поэтому лакмус краснеет. Ш рн 3/19/2018 < 7, среда кислотная, гидролиз по катиону. 15 Громова О. И
![Схема гидролиза Al 2 S 3 Al(OH)3 H 2 S слабое основание [OH–] Среду Схема гидролиза Al 2 S 3 Al(OH)3 H 2 S слабое основание [OH–] Среду](https://present5.com/presentation/d76f5df5c0fa132159be7e28a168c776/image-16.jpg) Схема гидролиза Al 2 S 3 Al(OH)3 H 2 S слабое основание [OH–] Среду можно определить по Кg 3/19/2018 16 Громова О. И слабая кислота ? [H+] Сила побеждает!
Схема гидролиза Al 2 S 3 Al(OH)3 H 2 S слабое основание [OH–] Среду можно определить по Кg 3/19/2018 16 Громова О. И слабая кислота ? [H+] Сила побеждает!
 Уравнения гидролиза Al 2 S 3 u. Al 2 S 3 + 6 H 2 O-->2 Al(OH)3 + 3 H 2 S Ш Гидролиз 3/19/2018 17 Громова О. И по катиону и аниону.
Уравнения гидролиза Al 2 S 3 u. Al 2 S 3 + 6 H 2 O-->2 Al(OH)3 + 3 H 2 S Ш Гидролиз 3/19/2018 17 Громова О. И по катиону и аниону.
![Схема гидролиза Na. Cl Na. OH HCl сильное основание сильная кислота [OH–] = Нейтральная Схема гидролиза Na. Cl Na. OH HCl сильное основание сильная кислота [OH–] = Нейтральная](https://present5.com/presentation/d76f5df5c0fa132159be7e28a168c776/image-18.jpg) Схема гидролиза Na. Cl Na. OH HCl сильное основание сильная кислота [OH–] = Нейтральная среда 3/19/2018 18 Громова О. И [H+] Сила побеждает!
Схема гидролиза Na. Cl Na. OH HCl сильное основание сильная кислота [OH–] = Нейтральная среда 3/19/2018 18 Громова О. И [H+] Сила побеждает!
 Уравнения гидролиза Na. Cl + Na. Cl ↔ Na + Сl + – Н 2 O ↔ Н + ОН – ______________________________________ Na+ + Сl– + Н 2 O ↔ Na+ + Cl– + H 2 O Ш Одинаковое количество гидроксидионов и ионов водорода дает соли нейтральную среду, поэтому индикаторы не меняют окраску (гидролизу не подвергается). рн =7, среда нейтральная, гидролиз не происходит. 3/19/2018 19 Громова О. И
Уравнения гидролиза Na. Cl + Na. Cl ↔ Na + Сl + – Н 2 O ↔ Н + ОН – ______________________________________ Na+ + Сl– + Н 2 O ↔ Na+ + Cl– + H 2 O Ш Одинаковое количество гидроксидионов и ионов водорода дает соли нейтральную среду, поэтому индикаторы не меняют окраску (гидролизу не подвергается). рн =7, среда нейтральная, гидролиз не происходит. 3/19/2018 19 Громова О. И
 • Выполните следующие задания Какую среду будут иметь водные растворы следующих солей: 1 вариант а) нитрата цинка (II) б) сульфата калия в) сульфида натрия Ш Составьте 2 вариант а) хлорида меди (II) б) сульфита натрия в) нитрата бария ионное уравнение гидролиза этих солей. 3/19/2018 20 Громова О. И
• Выполните следующие задания Какую среду будут иметь водные растворы следующих солей: 1 вариант а) нитрата цинка (II) б) сульфата калия в) сульфида натрия Ш Составьте 2 вариант а) хлорида меди (II) б) сульфита натрия в) нитрата бария ионное уравнение гидролиза этих солей. 3/19/2018 20 Громова О. И
 Ответы 3/19/2018 21 Громова О. И
Ответы 3/19/2018 21 Громова О. И
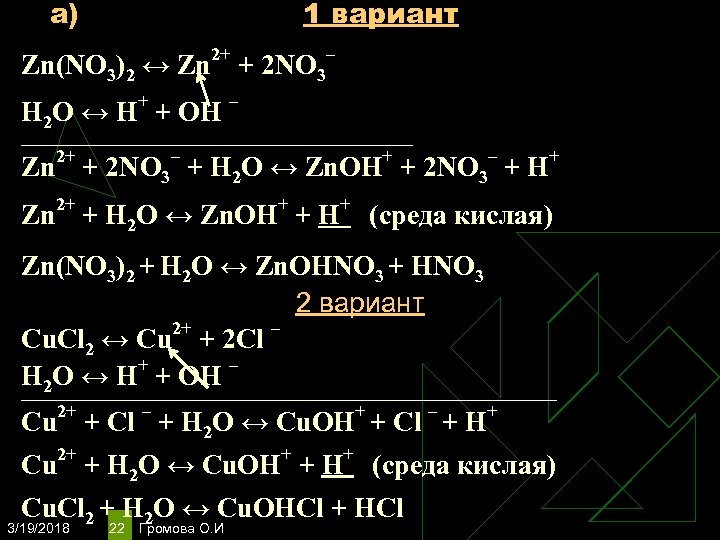 а) 1 вариант 2+ Zn(NO 3)2 ↔ Zn + + Н 2 O ↔ Н + ОН – 2 NO 3 – ____________________________ 2+ – + Zn + 2 NO 3 + Н 2 O ↔ Zn. OН + 2+ + Zn + Н 2 O ↔ Zn. OН + – 2 NO 3 +Н + (среда кислая) Zn(NO 3)2 + Н 2 O ↔ Zn. OНNO 3 + НNO 3 2 вариант Cu. Cl 2 ↔ Cu 2+ + 2 Сl – + – Н 2 O ↔ Н + ОН ____________________________________________________________ Cu 2+ + Сl – + Н 2 O ↔ Cu. OH+ + Cl – + Н+ 2+ + Сu + Н 2 O ↔ Сu. OH + Н + (среда кислая) Cu. Cl 2 + Н 2 O ↔ Cu. OHCl + НCl 3/19/2018 22 Громова О. И
а) 1 вариант 2+ Zn(NO 3)2 ↔ Zn + + Н 2 O ↔ Н + ОН – 2 NO 3 – ____________________________ 2+ – + Zn + 2 NO 3 + Н 2 O ↔ Zn. OН + 2+ + Zn + Н 2 O ↔ Zn. OН + – 2 NO 3 +Н + (среда кислая) Zn(NO 3)2 + Н 2 O ↔ Zn. OНNO 3 + НNO 3 2 вариант Cu. Cl 2 ↔ Cu 2+ + 2 Сl – + – Н 2 O ↔ Н + ОН ____________________________________________________________ Cu 2+ + Сl – + Н 2 O ↔ Cu. OH+ + Cl – + Н+ 2+ + Сu + Н 2 O ↔ Сu. OH + Н + (среда кислая) Cu. Cl 2 + Н 2 O ↔ Cu. OHCl + НCl 3/19/2018 22 Громова О. И
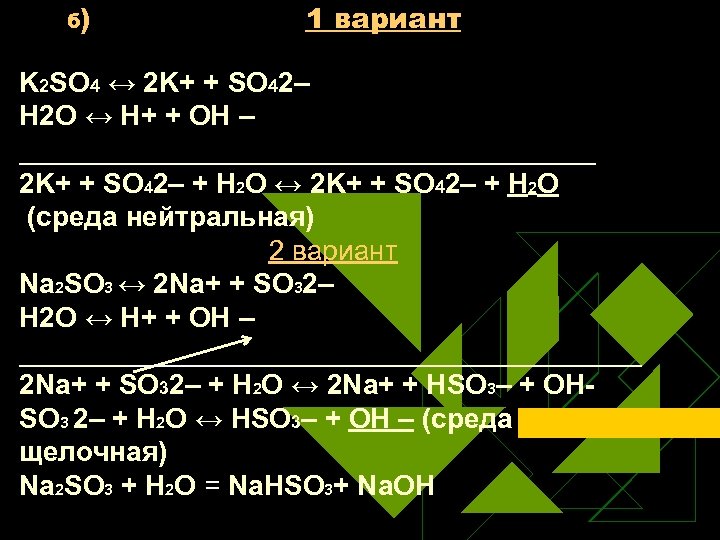 б) 1 вариант K 2 SO 4 ↔ 2 K+ + SO 42– Н 2 O ↔ Н+ + ОН – ___________________ 2 K+ + SO 42– + Н 2 O ↔ 2 K+ + SO 42– + H 2 O (среда нейтральная) 2 вариант Na 2 SO 3 ↔ 2 Na+ + SO 32– Н 2 O ↔ Н+ + ОН – ____________________ 2 Na+ + SO 32– + Н 2 O ↔ 2 Na+ + HSO 3– + ОНSO 3 2– + Н 2 O ↔ НSO 3– + ОН – (среда щелочная) Na 2 SO 3 + Н 2 O = Na. HSO 3+ Na. ОН
б) 1 вариант K 2 SO 4 ↔ 2 K+ + SO 42– Н 2 O ↔ Н+ + ОН – ___________________ 2 K+ + SO 42– + Н 2 O ↔ 2 K+ + SO 42– + H 2 O (среда нейтральная) 2 вариант Na 2 SO 3 ↔ 2 Na+ + SO 32– Н 2 O ↔ Н+ + ОН – ____________________ 2 Na+ + SO 32– + Н 2 O ↔ 2 Na+ + HSO 3– + ОНSO 3 2– + Н 2 O ↔ НSO 3– + ОН – (среда щелочная) Na 2 SO 3 + Н 2 O = Na. HSO 3+ Na. ОН
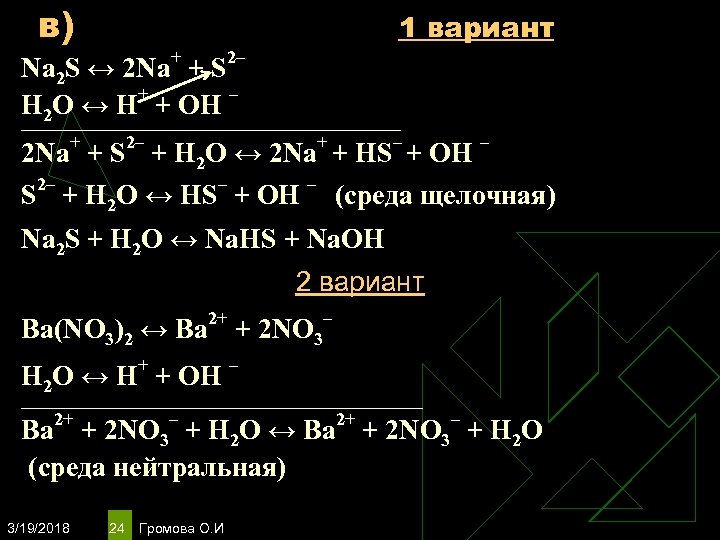 в) 1 вариант + 2– Na 2 S ↔ 2 Na + S + – Н 2 O ↔ Н + ОН ______________________________________ + 2– + – 2 Na + S + Н 2 O ↔ 2 Na + HS + ОН – S 2– + Н 2 O ↔ НS– + ОН – (среда щелочная) Na 2 S + Н 2 O ↔ Na. HS + Na. ОН 2 вариант 2+ Ba(NO 3)2 ↔ Ba + + Н 2 O ↔ Н + ОН – 2 NO 3 – __________________________________ Ba 2+ + 2 NO 3– + Н 2 O ↔ Ba 2+ + 2 NO 3– + Н 2 O (среда нейтральная) 3/19/2018 24 Громова О. И
в) 1 вариант + 2– Na 2 S ↔ 2 Na + S + – Н 2 O ↔ Н + ОН ______________________________________ + 2– + – 2 Na + S + Н 2 O ↔ 2 Na + HS + ОН – S 2– + Н 2 O ↔ НS– + ОН – (среда щелочная) Na 2 S + Н 2 O ↔ Na. HS + Na. ОН 2 вариант 2+ Ba(NO 3)2 ↔ Ba + + Н 2 O ↔ Н + ОН – 2 NO 3 – __________________________________ Ba 2+ + 2 NO 3– + Н 2 O ↔ Ba 2+ + 2 NO 3– + Н 2 O (среда нейтральная) 3/19/2018 24 Громова О. И
 Задания А-26 (ЕГЭ) Задания ЕГЭ 1. Кислую среду имеет водный раствор: 1. Na 3 PO 4 2. KCl 3. Na 2 CO 3 4. Zn. SO 4 2. Кислую среду имеет раствор: 1. Нитрата меди (II) 2. Нитрата бария 3. Ацетата калия 4. Карбоната натрия 3. Кислую реакцию среды имеет каждый из двух растворов: 1. Cu. SO 4 и Ba. Cl 2 2. Fe(NO 3)3 и Fe. Cl 2 3. K 3 PO 4 и Na. Cl 4. Al(NO 3)3 и Ca. Cl 2 4 Кислую реакцию среды имеет каждый из двух растворов: 1. Ba. Cl 2 и Zn. Cl 2 2. Al. Cl 3 и Fe. Cl 2 3. Fe. Cl 3 и Na. Cl 4. KCl и Ca. Cl 2 3/19/2018 25 Громова О. И 5. Щелочную среду имеет водный раствор: 1. Fe. Cl 3 2. K 2 SO 4 3. Na 2 CO 3 4. Ba. Cl 2 6. Фенолфталеин приобретает малиновую окраску в растворе каждой из двух солей: 1. Сульфата меди (II) и сульфида натрия 2. Хлорида калия и хлорида аммония 3. Карбоната натрия и силиката калия 4. Нитрата бария и хлорида железа (II) 7. Одинаковую реакцию среды имеют растворы карбоната натрия и 1. нитрата бария 2. силиката калия 3. сульфата натрия 4. хлорида алюминия 8. Соль, образованная сильным основанием и сильной кислотой, 1. Гидролизуется по катиону 2. Гидролизуется по аниону 3. Не подвергается гидролизу 4. Полностью разлагается водой
Задания А-26 (ЕГЭ) Задания ЕГЭ 1. Кислую среду имеет водный раствор: 1. Na 3 PO 4 2. KCl 3. Na 2 CO 3 4. Zn. SO 4 2. Кислую среду имеет раствор: 1. Нитрата меди (II) 2. Нитрата бария 3. Ацетата калия 4. Карбоната натрия 3. Кислую реакцию среды имеет каждый из двух растворов: 1. Cu. SO 4 и Ba. Cl 2 2. Fe(NO 3)3 и Fe. Cl 2 3. K 3 PO 4 и Na. Cl 4. Al(NO 3)3 и Ca. Cl 2 4 Кислую реакцию среды имеет каждый из двух растворов: 1. Ba. Cl 2 и Zn. Cl 2 2. Al. Cl 3 и Fe. Cl 2 3. Fe. Cl 3 и Na. Cl 4. KCl и Ca. Cl 2 3/19/2018 25 Громова О. И 5. Щелочную среду имеет водный раствор: 1. Fe. Cl 3 2. K 2 SO 4 3. Na 2 CO 3 4. Ba. Cl 2 6. Фенолфталеин приобретает малиновую окраску в растворе каждой из двух солей: 1. Сульфата меди (II) и сульфида натрия 2. Хлорида калия и хлорида аммония 3. Карбоната натрия и силиката калия 4. Нитрата бария и хлорида железа (II) 7. Одинаковую реакцию среды имеют растворы карбоната натрия и 1. нитрата бария 2. силиката калия 3. сульфата натрия 4. хлорида алюминия 8. Соль, образованная сильным основанием и сильной кислотой, 1. Гидролизуется по катиону 2. Гидролизуется по аниону 3. Не подвергается гидролизу 4. Полностью разлагается водой
 Задания В-4 (ЕГЭ) 1. Установите соответствие между составом соли и реакцией среды её водного раствора. Состав соли Реакция среды А) Na. NO 2 Б) Al 2(SO 4)3 В) Na. NO 3 Г) KCN 1. 3/19/2018 26 Громова О. И 2. 3. кислая щелочная нейтральная
Задания В-4 (ЕГЭ) 1. Установите соответствие между составом соли и реакцией среды её водного раствора. Состав соли Реакция среды А) Na. NO 2 Б) Al 2(SO 4)3 В) Na. NO 3 Г) KCN 1. 3/19/2018 26 Громова О. И 2. 3. кислая щелочная нейтральная
 2. Установите соответствие между составомсоли и реакцией среды её водного раствора ФОРМУЛА СОЛИ СРЕДА РАСТВОРА А) K 2 SO 4 Б) Cr. Cl 3 В) Li 2 CO 3 Г) NH 4 Br нейтральная щелочная кислая 3/19/2018 27 Громова О. И .
2. Установите соответствие между составомсоли и реакцией среды её водного раствора ФОРМУЛА СОЛИ СРЕДА РАСТВОРА А) K 2 SO 4 Б) Cr. Cl 3 В) Li 2 CO 3 Г) NH 4 Br нейтральная щелочная кислая 3/19/2018 27 Громова О. И .
 3. Установите соответствие между названием соли и средой её водного раствора. Название соли Среда раствора А) нитрат свинца (Pb(NO 3)2) Б) карбонат калия (K 2 CO 3) В) нитрат натрия (Na. NO 3) Г) сульфид лития (Li 2 S) 1. 3/19/2018 28 Громова О. И 2. 3. кислая щелочная нейтральная
3. Установите соответствие между названием соли и средой её водного раствора. Название соли Среда раствора А) нитрат свинца (Pb(NO 3)2) Б) карбонат калия (K 2 CO 3) В) нитрат натрия (Na. NO 3) Г) сульфид лития (Li 2 S) 1. 3/19/2018 28 Громова О. И 2. 3. кислая щелочная нейтральная
 Задние на дом: Параграф 18, № 1 -11. В контакте. Ru, в заметках, материал ЕГЭ выполнить. 3/19/2018 29 Громова О. И
Задние на дом: Параграф 18, № 1 -11. В контакте. Ru, в заметках, материал ЕГЭ выполнить. 3/19/2018 29 Громова О. И
 Источники материалов u u 3/19/2018 Кузьменко Н. Е. , Еремин В. В. , Попков В. А. Начала химии. — М. : Экзамен, 2001. Хомченко Г. П. , Хомченко И. Г. Сборник задач по химии. — М. , 2000. http: //hydorlysis. narod. ru/pages/teoria. ht m http: //www. xumuk. ru/encyklopedia/1047. html 30 Громова О. И
Источники материалов u u 3/19/2018 Кузьменко Н. Е. , Еремин В. В. , Попков В. А. Начала химии. — М. : Экзамен, 2001. Хомченко Г. П. , Хомченко И. Г. Сборник задач по химии. — М. , 2000. http: //hydorlysis. narod. ru/pages/teoria. ht m http: //www. xumuk. ru/encyklopedia/1047. html 30 Громова О. И


