13. Гидролиз солей.pptx
- Количество слайдов: 21
 Гидролиз солей. Единственный путь, Ведущий к знанию, Это деятельность. «Шоу»
Гидролиз солей. Единственный путь, Ведущий к знанию, Это деятельность. «Шоу»
 Электролиты u сильные: Na. OH, KOH, H 2 SO 4, HNO 3, HCl. O 4, HCl, HMn. O 4, HI, HBr; u слабые: , NH 4 OH, Cu(OH)2, Zn(OH)2, Al(OH)3, H 2 SO 3, H 2 CO 3, H 2 Si. O 3, HF, HNO 2, СН 3 СООН
Электролиты u сильные: Na. OH, KOH, H 2 SO 4, HNO 3, HCl. O 4, HCl, HMn. O 4, HI, HBr; u слабые: , NH 4 OH, Cu(OH)2, Zn(OH)2, Al(OH)3, H 2 SO 3, H 2 CO 3, H 2 Si. O 3, HF, HNO 2, СН 3 СООН
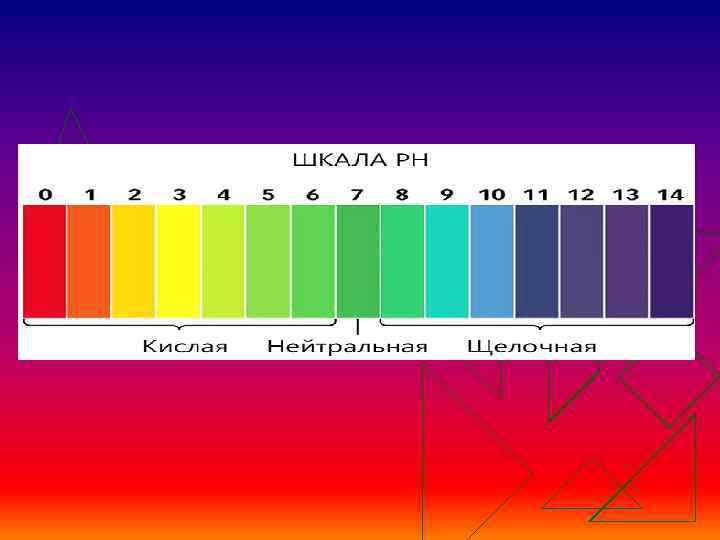
 Изменение цвета различных индикаторов при действии растворов кислот и щелочей Индикатор Цвет индикатора в среде кислой Лакмус Красный щелочной Синий Фенолфта- Бесцветный Малиновый леин нейтрально й —— Бесцветный
Изменение цвета различных индикаторов при действии растворов кислот и щелочей Индикатор Цвет индикатора в среде кислой Лакмус Красный щелочной Синий Фенолфта- Бесцветный Малиновый леин нейтрально й —— Бесцветный
 СОЛЬ (КBr) кислота HBr + основание KOH
СОЛЬ (КBr) кислота HBr + основание KOH
 u Любую соль можно представить как продукт взаимодействия основания с кислотой. u В зависимости от силы основания и кислоты можно выделить 4 типа солей:
u Любую соль можно представить как продукт взаимодействия основания с кислотой. u В зависимости от силы основания и кислоты можно выделить 4 типа солей:
 1. Соли, образованные сильной кислотой и слабым основанием (Al. Cl 3, Fe. SO 4, Mn(NO 3)2. ) 2. Соли, образованные сильным основанием и слабой кислотой (Na 2 CO 3, КСN, Na. CH 3 COO). 3. Соли, образованные слабой кислотой и слабым основанием (NH 4 CN, Cu(CH 3 COO)2). 4. Соли, образованные сильной кислотой и сильным основанием (Na. Cl, K 2 SO 4, Ba. I 2).
1. Соли, образованные сильной кислотой и слабым основанием (Al. Cl 3, Fe. SO 4, Mn(NO 3)2. ) 2. Соли, образованные сильным основанием и слабой кислотой (Na 2 CO 3, КСN, Na. CH 3 COO). 3. Соли, образованные слабой кислотой и слабым основанием (NH 4 CN, Cu(CH 3 COO)2). 4. Соли, образованные сильной кислотой и сильным основанием (Na. Cl, K 2 SO 4, Ba. I 2).
 Гидролизом называется взаимодействие веществ с водой, при котором составные части вещества соединяются с составными частями воды. u Гидролизу подвержены соединения различных классов. Рассмотрим один случай – гидролиз солей.
Гидролизом называется взаимодействие веществ с водой, при котором составные части вещества соединяются с составными частями воды. u Гидролизу подвержены соединения различных классов. Рассмотрим один случай – гидролиз солей.
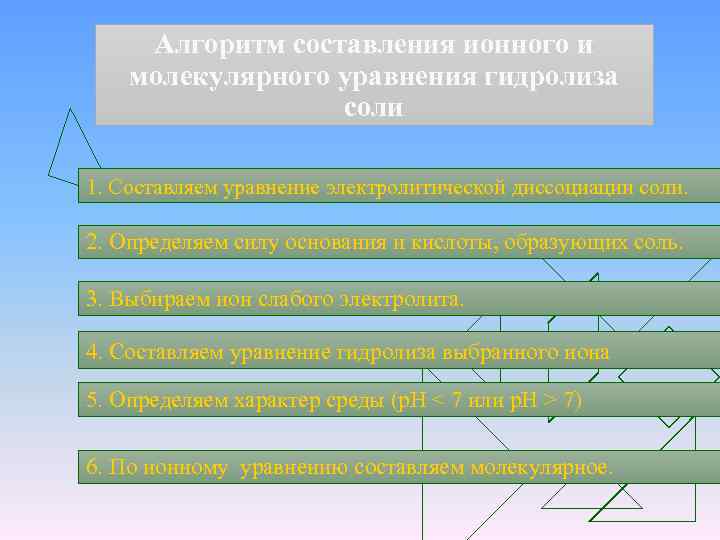 Алгоритм составления ионного и молекулярного уравнения гидролиза соли 1. Составляем уравнение электролитической диссоциации соли. 2. Определяем силу основания и кислоты, образующих соль. 3. Выбираем ион слабого электролита. 4. Составляем уравнение гидролиза выбранного иона 5. Определяем характер среды (р. Н < 7 или р. Н > 7) 6. По ионному уравнению составляем молекулярное.
Алгоритм составления ионного и молекулярного уравнения гидролиза соли 1. Составляем уравнение электролитической диссоциации соли. 2. Определяем силу основания и кислоты, образующих соль. 3. Выбираем ион слабого электролита. 4. Составляем уравнение гидролиза выбранного иона 5. Определяем характер среды (р. Н < 7 или р. Н > 7) 6. По ионному уравнению составляем молекулярное.
![Схема гидролиза Na. CN Na. OH HCN сильное основание слабая кислота [OH–] > [H+] Схема гидролиза Na. CN Na. OH HCN сильное основание слабая кислота [OH–] > [H+]](https://present5.com/presentation/234515828_453785228/image-10.jpg) Схема гидролиза Na. CN Na. OH HCN сильное основание слабая кислота [OH–] > [H+] Щелочная среда Сила побеждает!
Схема гидролиза Na. CN Na. OH HCN сильное основание слабая кислота [OH–] > [H+] Щелочная среда Сила побеждает!
 Уравнения гидролиза Na. CN ↔Na+ + CN‾ Н 2 О ↔ OH ‾ + H+ ______________ Полное ионное уравнение гидролиза: Na+ + CN¯ + Н 2 О ↔ Na+ + OH¯ + HCN Сокращённое уравнение гидролиза: CN¯ + Н 2 О ↔ OH¯ + HCN Полное молекулярное уравнение гидролиза: Na. CN + Н 2 О ↔ Na. OH + HCN Ш Избыток гидроксид-ионов дает соли щелочную среду, поэтому лакмус синеет, а фенолфталеин становится малиновым. рн >7, среда щелочная, гидролиз по аниону.
Уравнения гидролиза Na. CN ↔Na+ + CN‾ Н 2 О ↔ OH ‾ + H+ ______________ Полное ионное уравнение гидролиза: Na+ + CN¯ + Н 2 О ↔ Na+ + OH¯ + HCN Сокращённое уравнение гидролиза: CN¯ + Н 2 О ↔ OH¯ + HCN Полное молекулярное уравнение гидролиза: Na. CN + Н 2 О ↔ Na. OH + HCN Ш Избыток гидроксид-ионов дает соли щелочную среду, поэтому лакмус синеет, а фенолфталеин становится малиновым. рн >7, среда щелочная, гидролиз по аниону.
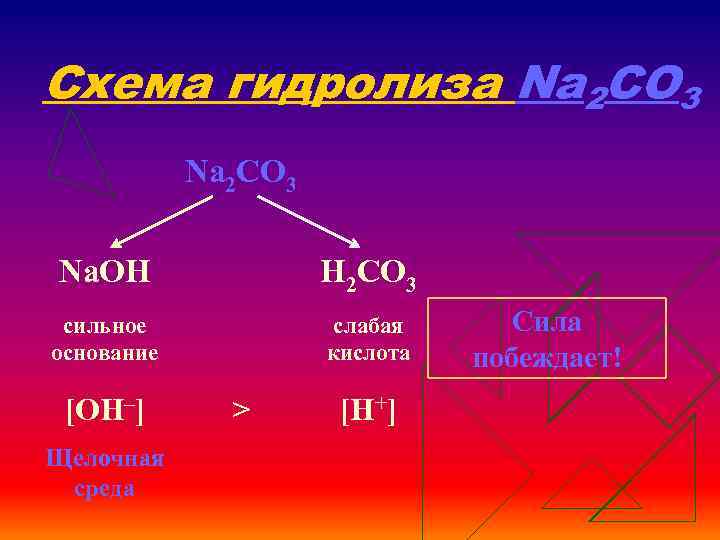 Схема гидролиза Na 2 CO 3 Na. OH H 2 CO 3 сильное основание слабая кислота [OH–] Щелочная среда > [H+] Сила побеждает!
Схема гидролиза Na 2 CO 3 Na. OH H 2 CO 3 сильное основание слабая кислота [OH–] Щелочная среда > [H+] Сила побеждает!
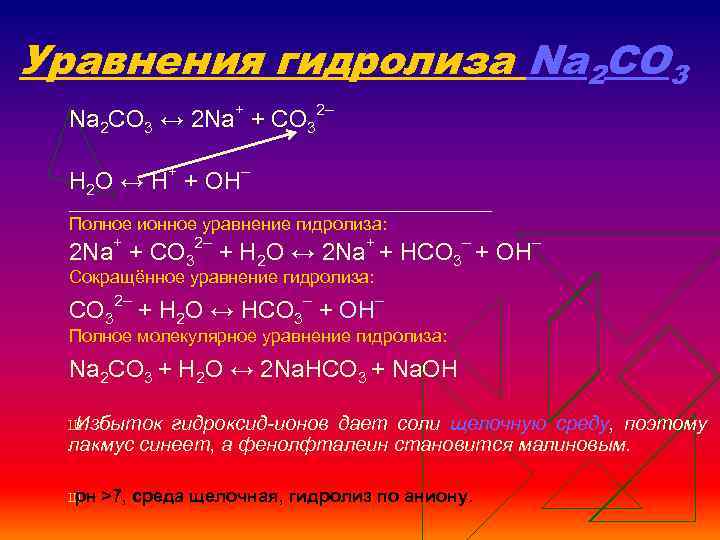 Уравнения гидролиза Na 2 CO 3 ↔ 2 Na+ + СO 32– Н 2 O ↔ Н+ + ОН– ______________________________________ Полное ионное уравнение гидролиза: 2 Na+ + СO 32– + Н 2 O ↔ 2 Na+ + HCO 3– + ОН– Сокращённое уравнение гидролиза: СO 32– + Н 2 O ↔ НСO 3– + ОН– Полное молекулярное уравнение гидролиза: Na 2 CO 3 + Н 2 O ↔ 2 Na. HCO 3 + Na. ОН Ш Избыток гидроксид-ионов дает соли щелочную среду, поэтому лакмус синеет, а фенолфталеин становится малиновым. Ш рн >7, среда щелочная, гидролиз по аниону.
Уравнения гидролиза Na 2 CO 3 ↔ 2 Na+ + СO 32– Н 2 O ↔ Н+ + ОН– ______________________________________ Полное ионное уравнение гидролиза: 2 Na+ + СO 32– + Н 2 O ↔ 2 Na+ + HCO 3– + ОН– Сокращённое уравнение гидролиза: СO 32– + Н 2 O ↔ НСO 3– + ОН– Полное молекулярное уравнение гидролиза: Na 2 CO 3 + Н 2 O ↔ 2 Na. HCO 3 + Na. ОН Ш Избыток гидроксид-ионов дает соли щелочную среду, поэтому лакмус синеет, а фенолфталеин становится малиновым. Ш рн >7, среда щелочная, гидролиз по аниону.
![Схема гидролиза NH 4 Cl NH 4 OH HCl слабое основание сильная кислота [OH–] Схема гидролиза NH 4 Cl NH 4 OH HCl слабое основание сильная кислота [OH–]](https://present5.com/presentation/234515828_453785228/image-14.jpg) Схема гидролиза NH 4 Cl NH 4 OH HCl слабое основание сильная кислота [OH–] < [H+] Кислая среда Сила побеждает!
Схема гидролиза NH 4 Cl NH 4 OH HCl слабое основание сильная кислота [OH–] < [H+] Кислая среда Сила побеждает!
 Уравнения гидролиза NH 4 Cl ↔ NH 4+ + Сl– + Н 2 O ↔ Н + ОН – _____________________ Полное ионное уравнение гидролиза + – – : NH 4 + Сl + Н 2 O ↔ NH 3·H 2 О + Сl + Н + Сокращённое уравнение гидролиза: NH 4+ + Н 2 O ↔ NH 3·H 2 О + Н+ Полное молекулярное уравнение гидролиза: NH 4 Cl + Н 2 O ↔ NH 3·H 2 О + НСl Ш Избыток ионов водорода дает соли кислую среду, поэтому лакмус краснеет. Ш рн < 7, среда кислотная, гидролиз по катиону.
Уравнения гидролиза NH 4 Cl ↔ NH 4+ + Сl– + Н 2 O ↔ Н + ОН – _____________________ Полное ионное уравнение гидролиза + – – : NH 4 + Сl + Н 2 O ↔ NH 3·H 2 О + Сl + Н + Сокращённое уравнение гидролиза: NH 4+ + Н 2 O ↔ NH 3·H 2 О + Н+ Полное молекулярное уравнение гидролиза: NH 4 Cl + Н 2 O ↔ NH 3·H 2 О + НСl Ш Избыток ионов водорода дает соли кислую среду, поэтому лакмус краснеет. Ш рн < 7, среда кислотная, гидролиз по катиону.
![Схема гидролиза Al. Cl 3 Al(OH)3 HCl слабое основание сильная кислота [OH–] < [H+] Схема гидролиза Al. Cl 3 Al(OH)3 HCl слабое основание сильная кислота [OH–] < [H+]](https://present5.com/presentation/234515828_453785228/image-16.jpg) Схема гидролиза Al. Cl 3 Al(OH)3 HCl слабое основание сильная кислота [OH–] < [H+] Кислая среда Сила побеждает!
Схема гидролиза Al. Cl 3 Al(OH)3 HCl слабое основание сильная кислота [OH–] < [H+] Кислая среда Сила побеждает!
 Уравнения гидролиза Аl. Сl 3 ↔ Аl 3+ + 3 Сl– Н 2 O ↔ Н+ + ОН– ___________________ Полное ионное уравнение гидролиза: Al 3+ + 3 Сl– + Н 2 O ↔ Аl. OН 2+ + 3 Сl– + Н+ Сокращённое уравнение гидролиза: Аl 3+ + Н 2 O ↔ Аl. OН 2+ + Н+ Полное молекулярное уравнение гидролиза: Аl. Сl 3 + Н 2 O ↔ Аl. OНСl + НСl Ш Избыток ионов водорода дает соли кислую среду, поэтому лакмус краснеет. Ш рн < 7, среда кислотная, гидролиз по катиону.
Уравнения гидролиза Аl. Сl 3 ↔ Аl 3+ + 3 Сl– Н 2 O ↔ Н+ + ОН– ___________________ Полное ионное уравнение гидролиза: Al 3+ + 3 Сl– + Н 2 O ↔ Аl. OН 2+ + 3 Сl– + Н+ Сокращённое уравнение гидролиза: Аl 3+ + Н 2 O ↔ Аl. OН 2+ + Н+ Полное молекулярное уравнение гидролиза: Аl. Сl 3 + Н 2 O ↔ Аl. OНСl + НСl Ш Избыток ионов водорода дает соли кислую среду, поэтому лакмус краснеет. Ш рн < 7, среда кислотная, гидролиз по катиону.
![Схема гидролиза Al 2 S 3 Al(OH)3 H 2 S слабое основание [OH–] Среду Схема гидролиза Al 2 S 3 Al(OH)3 H 2 S слабое основание [OH–] Среду](https://present5.com/presentation/234515828_453785228/image-18.jpg) Схема гидролиза Al 2 S 3 Al(OH)3 H 2 S слабое основание [OH–] Среду можно определить по Кg слабая кислота ? [H+] Сила побеждает!
Схема гидролиза Al 2 S 3 Al(OH)3 H 2 S слабое основание [OH–] Среду можно определить по Кg слабая кислота ? [H+] Сила побеждает!
 Уравнения гидролиза Al 2 S 3 u. Al 2 S 3 + 6 H 2 O-->2 Al(OH)3 + 3 H 2 S Ш Гидролиз по катиону и аниону.
Уравнения гидролиза Al 2 S 3 u. Al 2 S 3 + 6 H 2 O-->2 Al(OH)3 + 3 H 2 S Ш Гидролиз по катиону и аниону.
![Схема гидролиза Na. Cl Na. OH HCl сильное основание сильная кислота [OH–] = Нейтральная Схема гидролиза Na. Cl Na. OH HCl сильное основание сильная кислота [OH–] = Нейтральная](https://present5.com/presentation/234515828_453785228/image-20.jpg) Схема гидролиза Na. Cl Na. OH HCl сильное основание сильная кислота [OH–] = Нейтральная среда [H+] Сила побеждает!
Схема гидролиза Na. Cl Na. OH HCl сильное основание сильная кислота [OH–] = Нейтральная среда [H+] Сила побеждает!
 Уравнения гидролиза Na. Cl ↔ Na+ + Сl– + – Н 2 O ↔ Н + ОН ______________________________________ Na+ + Сl– + Н 2 O ↔ Na+ + Cl– + H 2 O Ш Одинаковое количество гидроксидионов и ионов водорода дает соли нейтральную среду, поэтому индикаторы не меняют окраску (гидролизу не подвергается). рн =7, среда нейтральная, гидролиз не происходит.
Уравнения гидролиза Na. Cl ↔ Na+ + Сl– + – Н 2 O ↔ Н + ОН ______________________________________ Na+ + Сl– + Н 2 O ↔ Na+ + Cl– + H 2 O Ш Одинаковое количество гидроксидионов и ионов водорода дает соли нейтральную среду, поэтому индикаторы не меняют окраску (гидролизу не подвергается). рн =7, среда нейтральная, гидролиз не происходит.


